Similar presentations:
Производство серной кислоты
1.
Производствосерной кислоты
2.
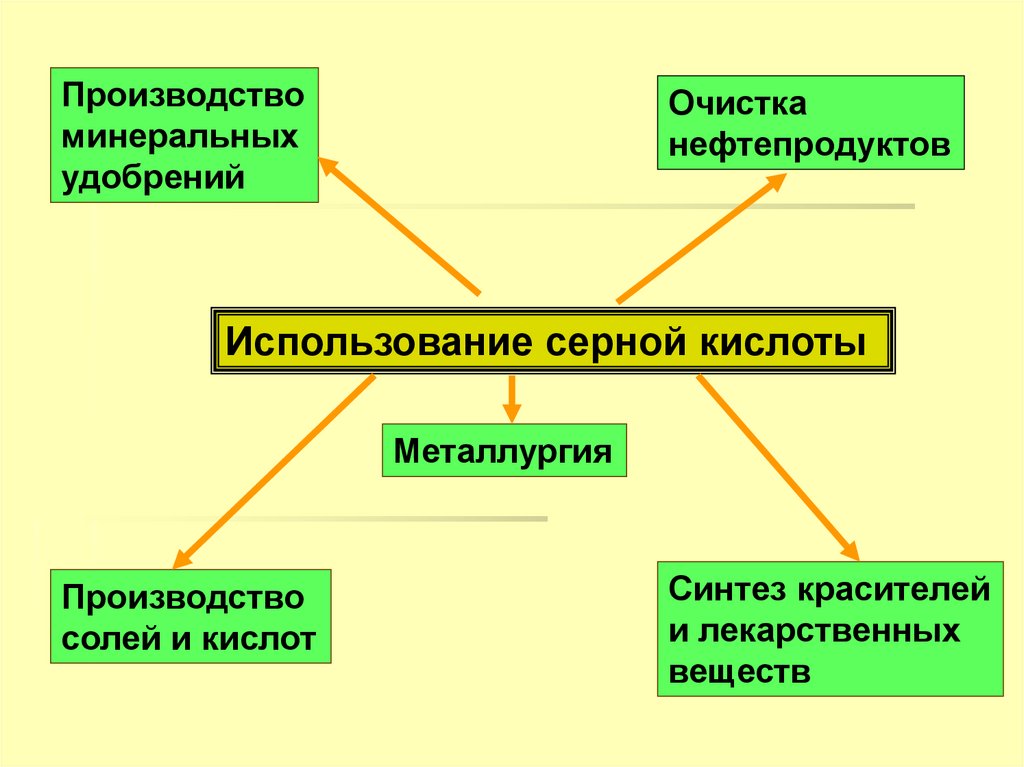
Производствоминеральных
удобрений
Очистка
нефтепродуктов
Использование серной кислоты
Металлургия
Производство
солей и кислот
Синтез красителей
и лекарственных
веществ
3.
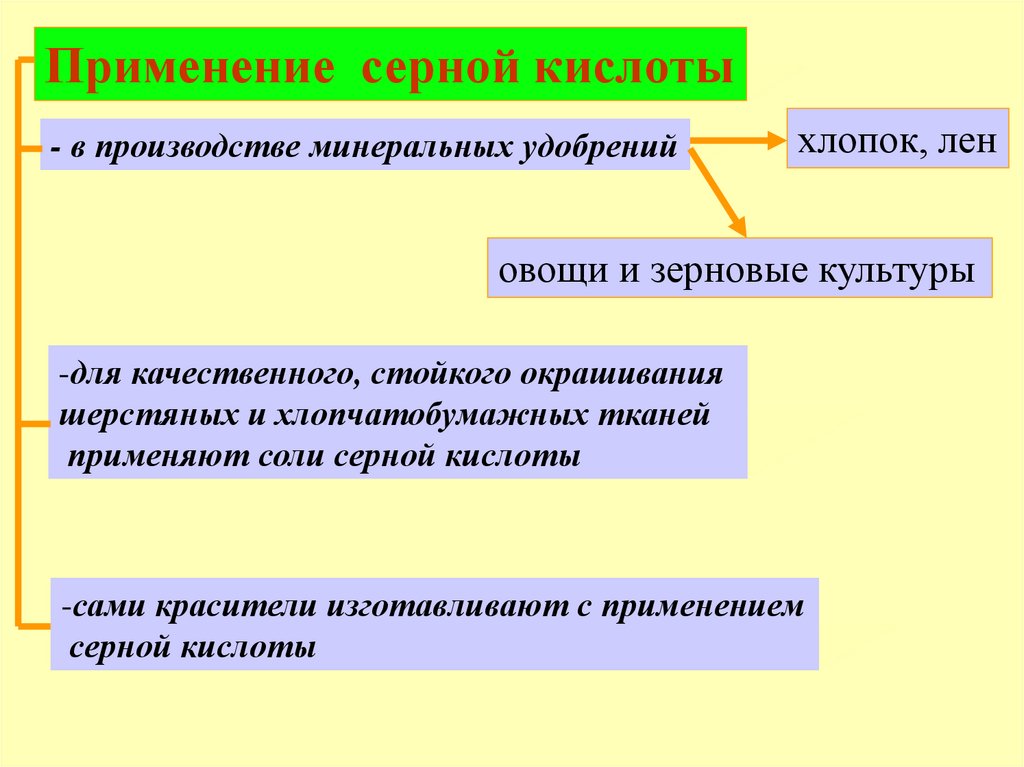
Применение серной кислоты- в производстве минеральных удобрений
хлопок, лен
овощи и зерновые культуры
-для качественного, стойкого окрашивания
шерстяных и хлопчатобумажных тканей
применяют соли серной кислоты
-сами красители изготавливают с применением
серной кислоты
4.
5.
6.
Применение серной кислоты-для обработки кожи, применяемой на обувных
фабриках
- в производстве мыла
- для отбеливания бумаги
для изготовления чернил
- в производстве смазочных масел и керосина
7.
8.
9.
Применение серной кислоты- в фармацевтической промышленности
- для производства искусственного волокна
- в производстве взрывчатых веществ
10.
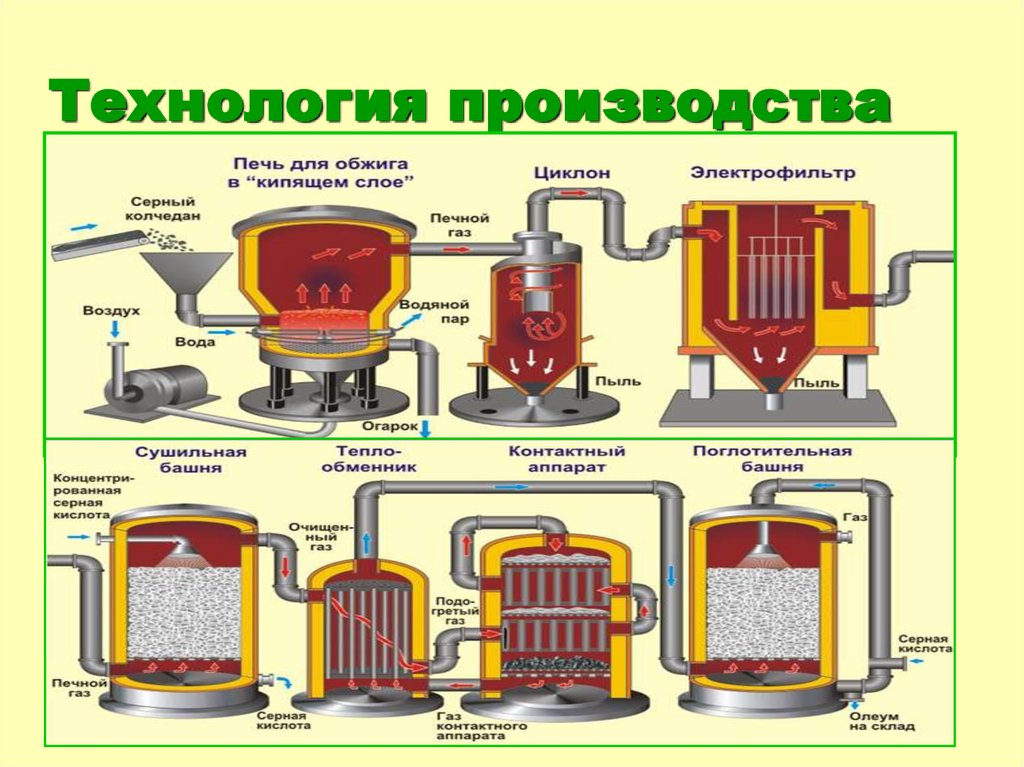
11. Технология производства
12. Сырьё
FeS2 - пирит, серный колчедан, железныйколчедан
S8 самородная ромбическая сера
H2S – сероводород
Сu2S; ZnS; PbS – сульфиды цветных
металлов
CaSO4*2H2O – гипс
13.
14.
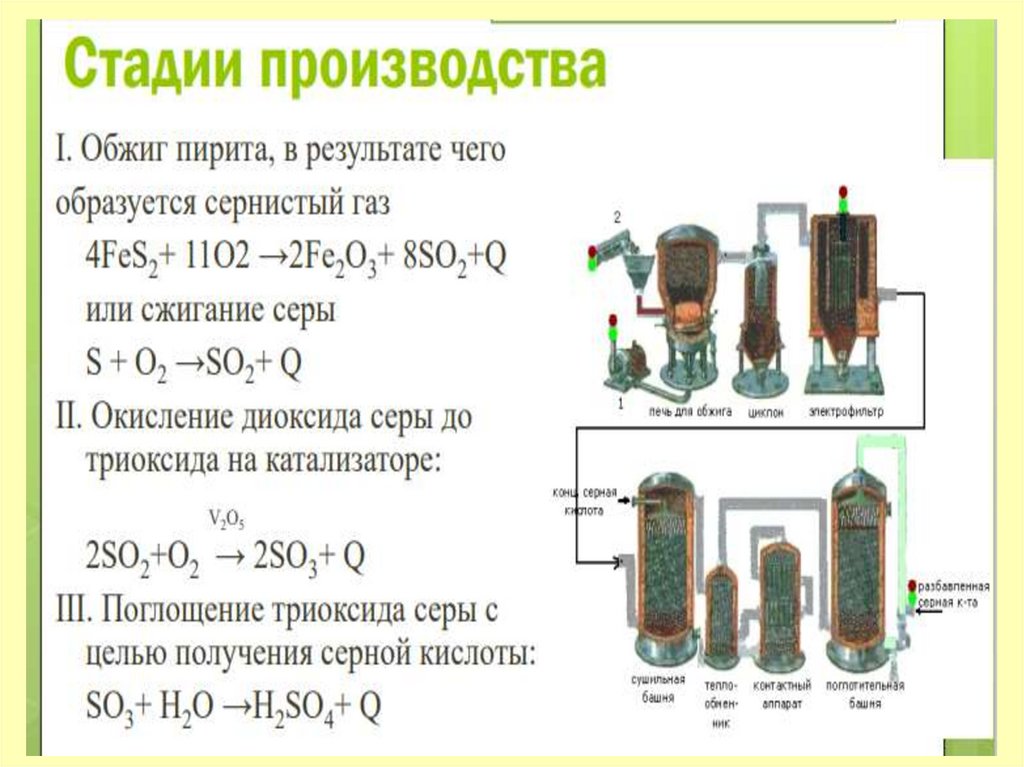
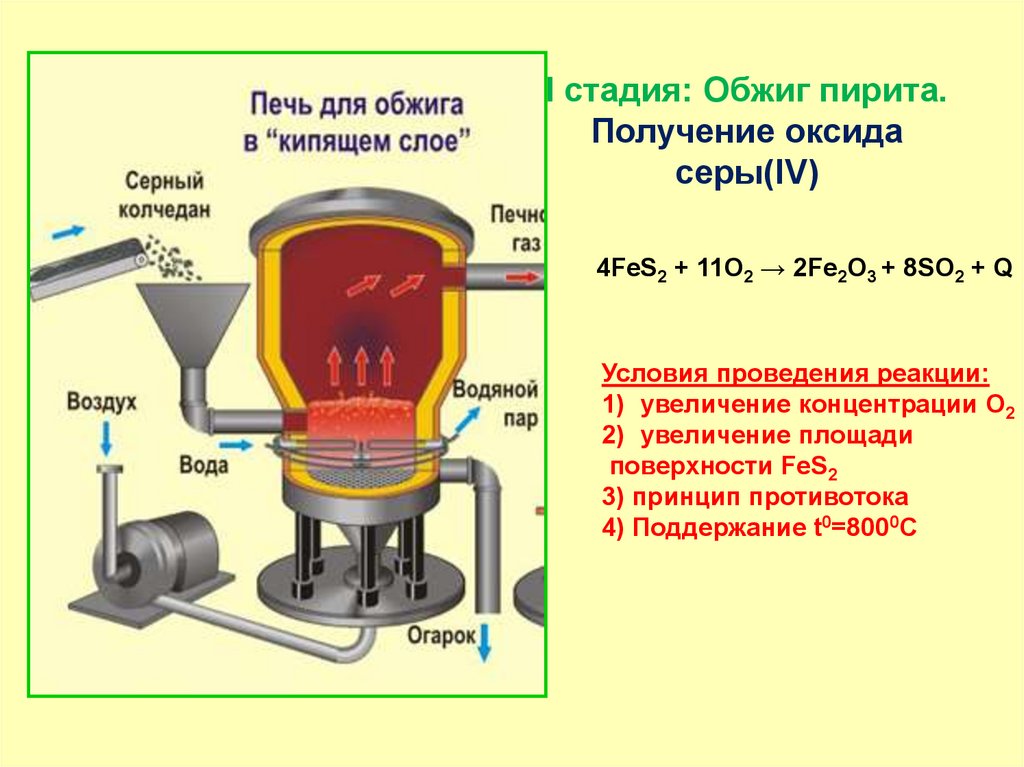
I стадия: Обжиг пирита.Получение оксида
серы(IV)
4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q
Условия проведения реакции:
1) увеличение концентрации О2
2) увеличение площади
поверхности FeS2
3) принцип противотока
4) Поддержание t0=8000C
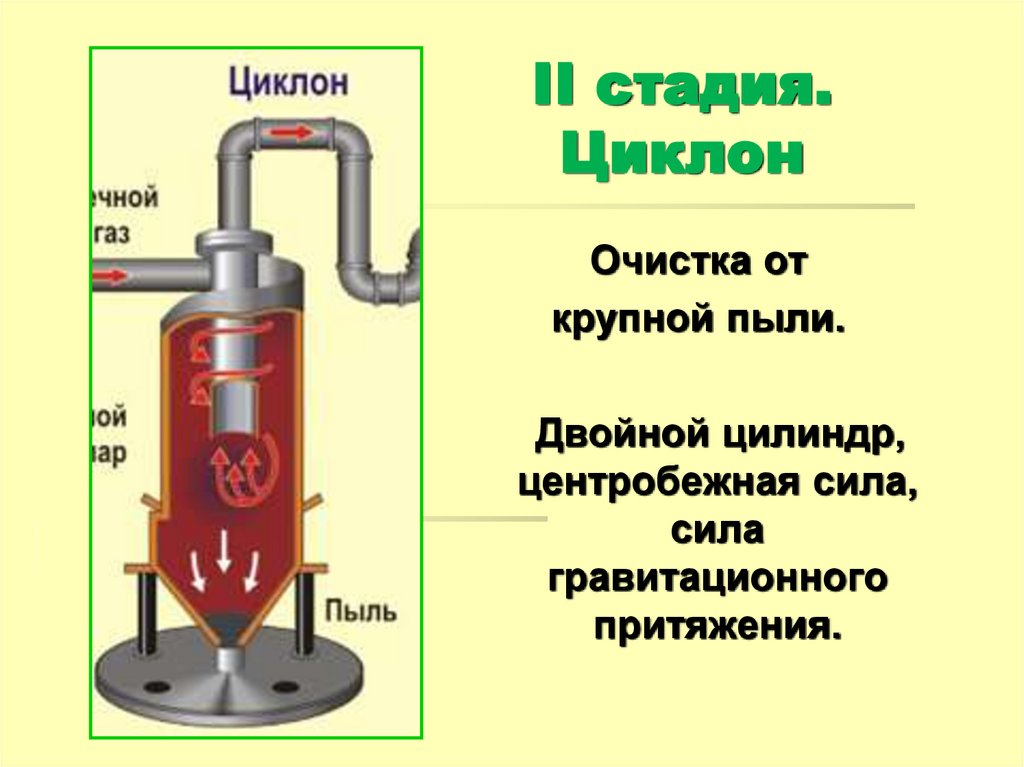
15. II стадия. Циклон
Очистка открупной пыли.
Двойной цилиндр,
центробежная сила,
сила
гравитационного
притяжения.
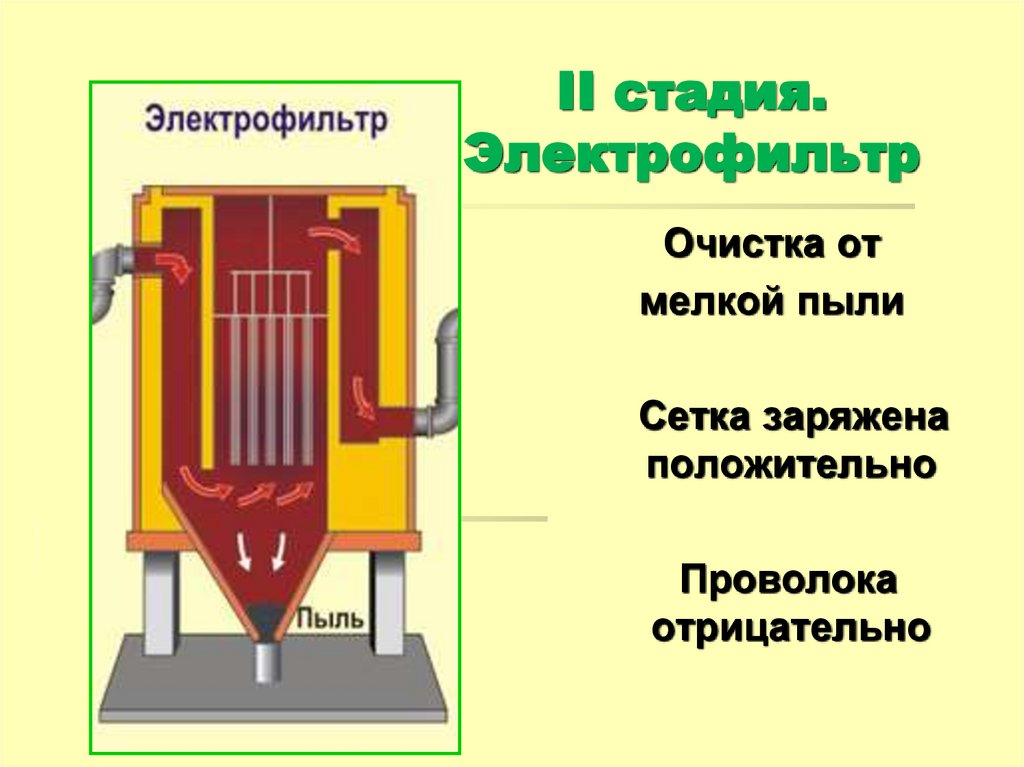
16. II стадия. Электрофильтр
Очистка отмелкой пыли
Сетка заряжена
положительно
Проволока
отрицательно
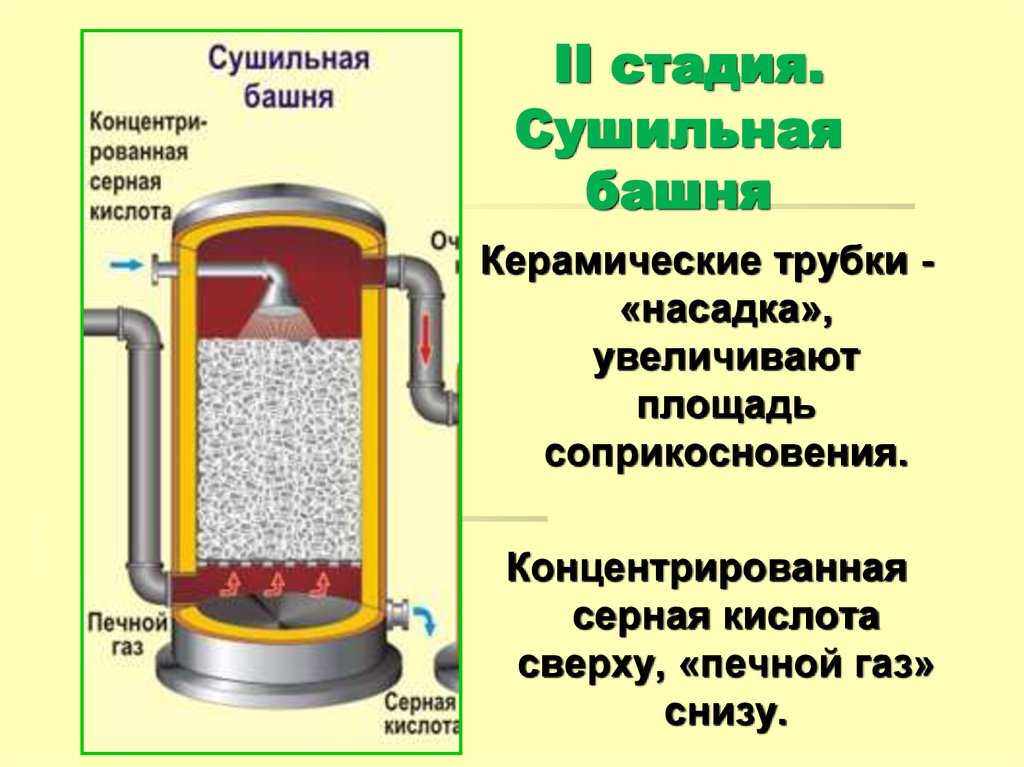
17. II стадия. Сушильная башня
Керамические трубки «насадка»,увеличивают
площадь
соприкосновения.
Концентрированная
серная кислота
сверху, «печной газ»
снизу.
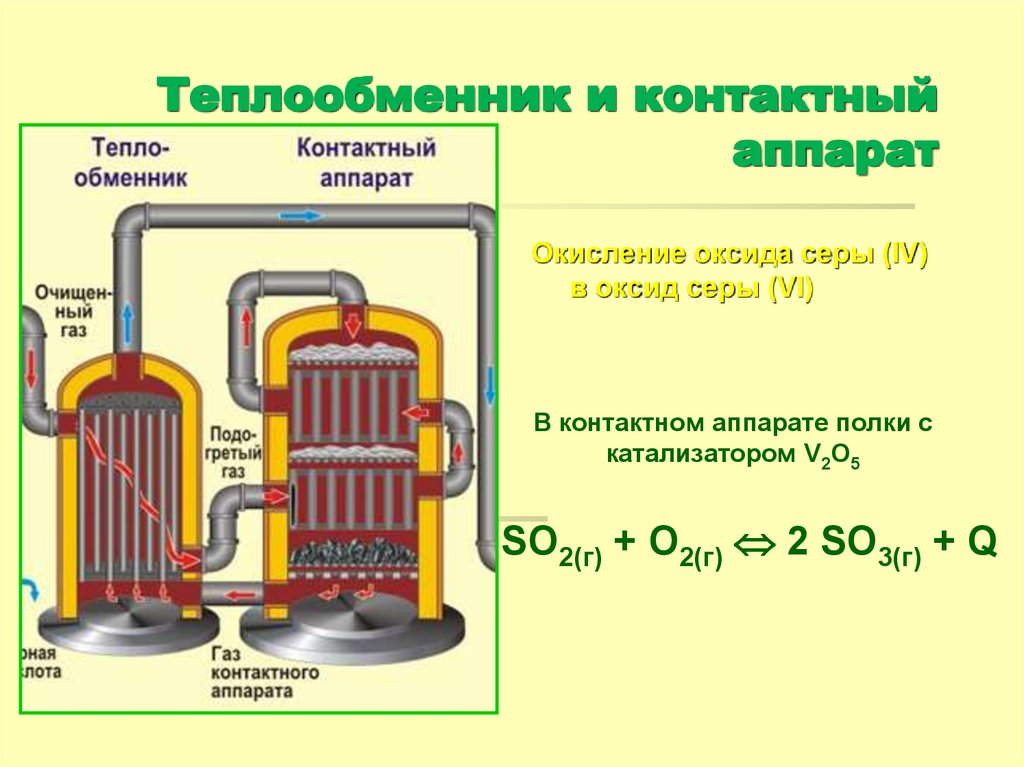
18. Теплообменник и контактный аппарат
Окисление оксида серы (IV)в оксид серы (VI)
В контактном аппарате полки с
катализатором V2O5
2 SO2(г) + O2(г) 2 SO3(г) + Q
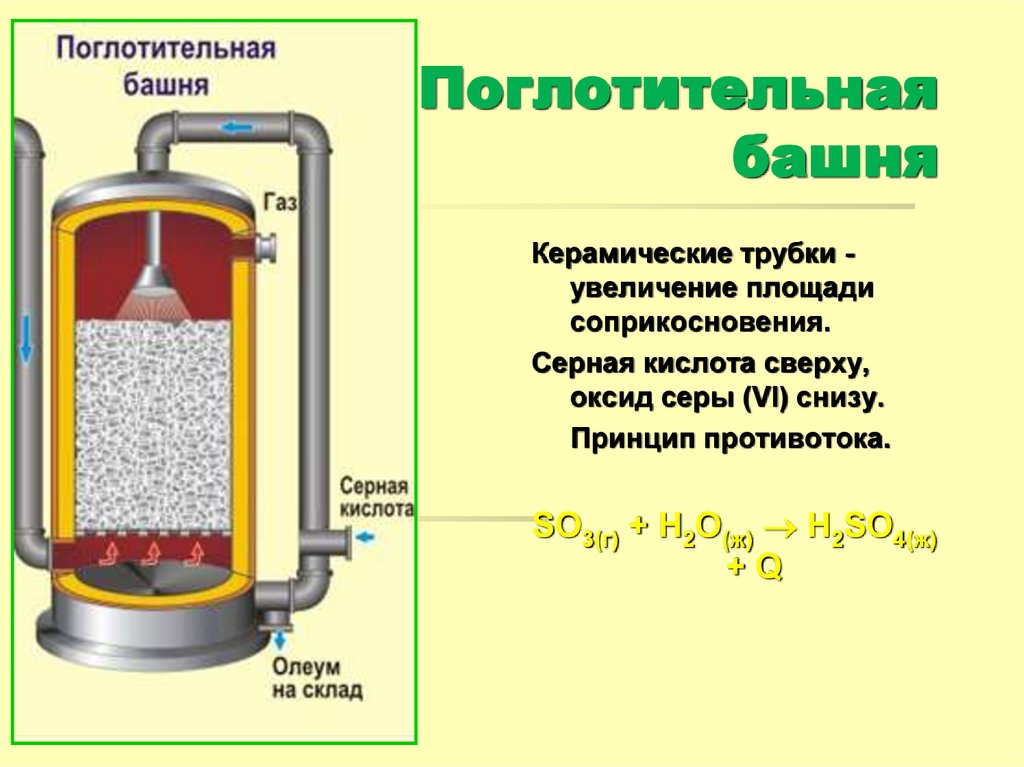
19. Поглотительная башня
Керамические трубки увеличение площадисоприкосновения.
Серная кислота сверху,
оксид серы (VI) снизу.
Принцип противотока.
SO3(г) + Н2О(ж) Н2SO4(ж)
+Q
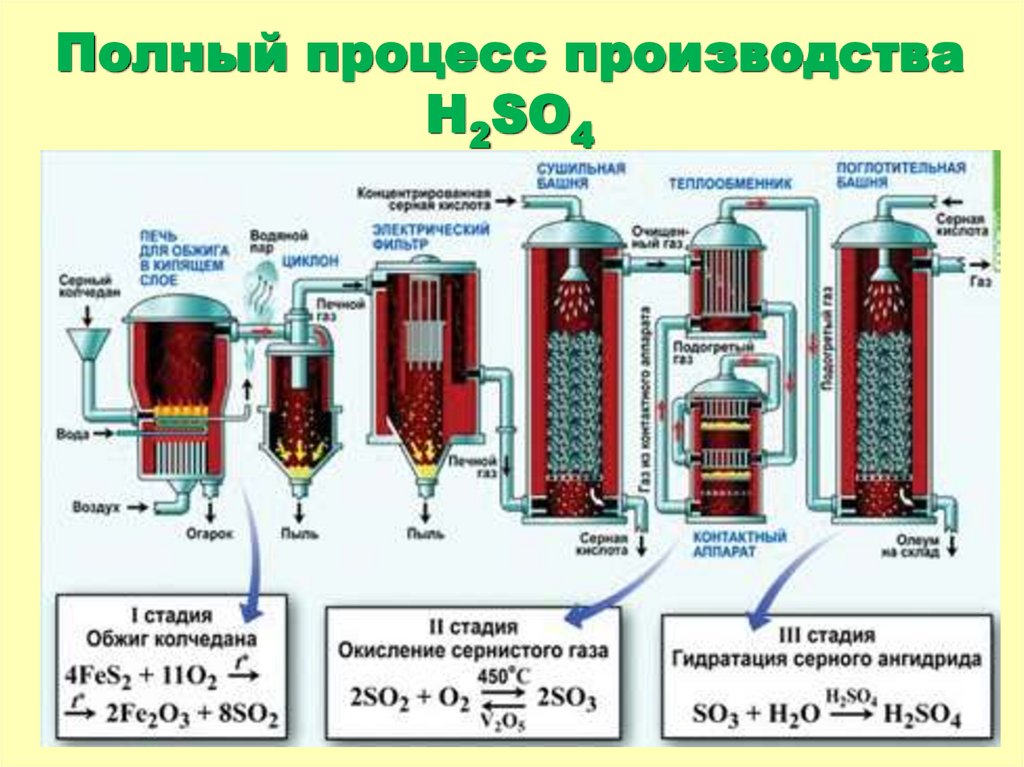
20. Полный процесс производства H2SO4
21. Принципы производства
1. Механизация процесса;2. Автоматизация процесса;
3. Оптимальные условия реакций (8000C,
давление, «кипящий слой», катализатор);
4. Использование теплоты;
5. Противоток;
6. Обогащение кислородом воздуха;
7. Герметизация аппаратуры.
22. Профессии работников сернокислотного производства:
1. Инженер – технолог.2. Аппаратчик.
3. Лаборант – аналитик.
23. Транспортировка и хранение серной кислоты
Транспортируют в железнодорожных и автоцистернах изкислотостойкой стали
Хранят в герметически закрытых емкостях из полимера или
нержавеющей стали, покрытой кислотоупорной плёнкой
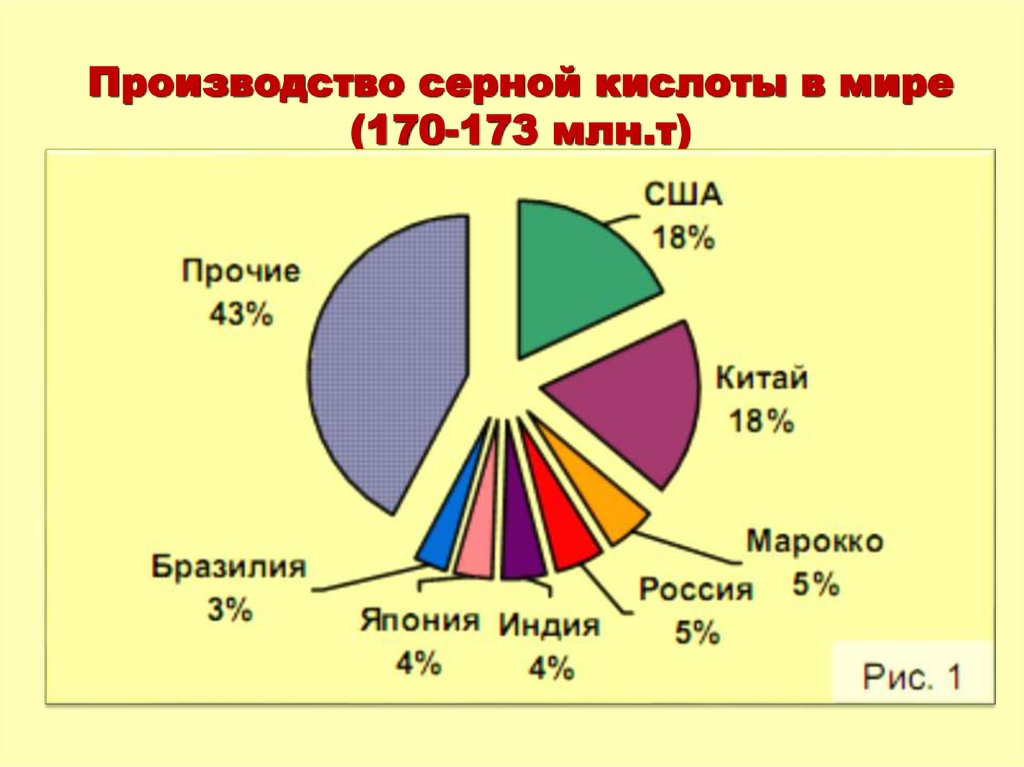
24. Производство серной кислоты в мире (170-173 млн.т)
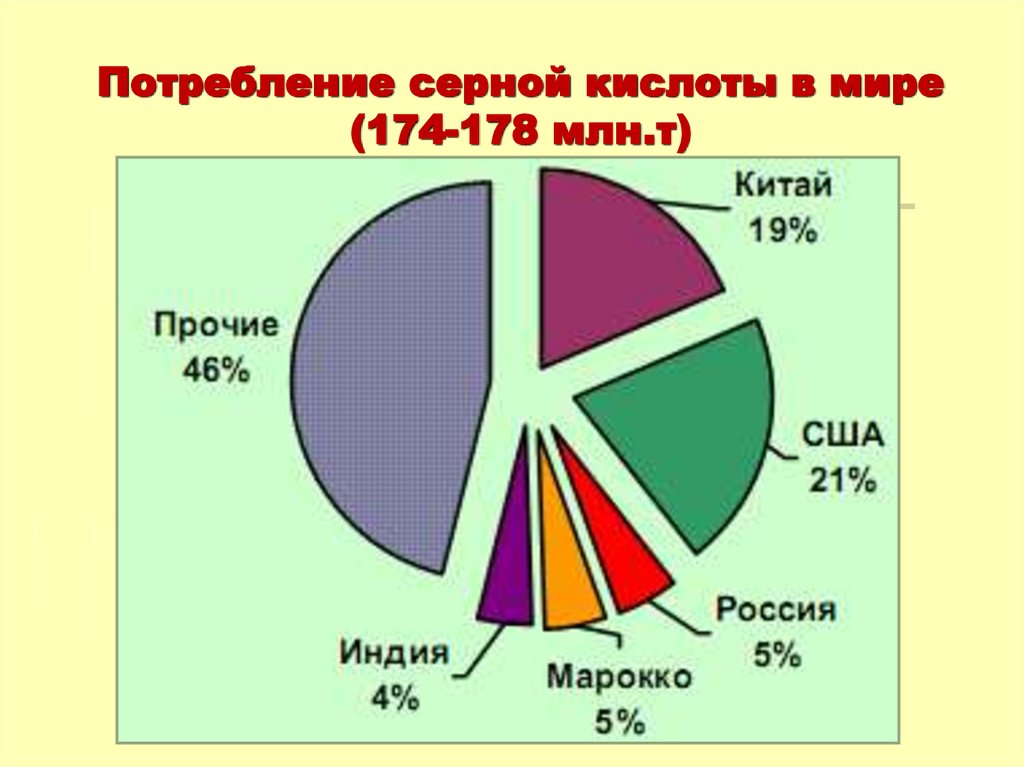
25. Потребление серной кислоты в мире (174-178 млн.т)
26. Потребление серной кислоты
1. Производство минеральных удобрений.2. Производство сульфатов (солей серной кислоты).
3. Производство синтетических волокон.
4. Черная и цветная металлургия.
5. Производство органических красителей.
6. Спирты, кислоты, эфиры(орг. вещества).
7. Пищевая промышленность(патока, глюкоза),
эмульгатор (загуститель) Е513.
8. Нефтехимия(минеральные масла).
9. Производство взрывчатых веществ.
27. Экологический ущерб производства
При аварийных выбросах в атмосферупопадают соединения серы:
SO2;SO3; H2S; H2SO4; Fe2O3(пыль)
Последствия: «закисление» почв и водоёмов,
«металлизация» атмосферы
РЕШЕНИЕ ЭКОЛОГИЧЕСКИХ ПРОБЛЕМ:
Непрерывность технологического процесса;
Комплексное использование сырья;
Совершенствование технологического оборудования.

















 chemistry
chemistry








