Similar presentations:
Бинарная сополимеризация винильных мономеров
1. Бинарная сополимеризация винильных мономеров
2. Типы сополимеров по составу сополимера и способу распределения звеньев в цепи
Состав сополимера можновыражать:
- соотношением звеньев
сомономеров в % или долях; - количеством звеньев одного
сомономера, приходящихся
на 1 звено второго и т.д.
3. Значение СоПМ
• Информация о реакционной способности радикалов,карбанионов и ионов карбония и о влиянии
химической структуры на реакционную способность
• Увеличение возможности получения продуктов с
заданными свойствами путем изменения природы и
относительных количеств звеньев сомономеров в
сополимере.
• - Свойства стат. сополимеров усредняются - ABS –
пластики
• - Блок- и привитые к сополимеры - аддитивность
физико-механичских свойств
4. Важной задачей при синтезе сополимеров с заданными свойствами является установление связи между составом сополимера и составом
исходной смесимономеров.
• Процесс сополимеризации включает те же стадии, что и
гомополимеризация: инициирование, рост цепи, обрыв и
передача цепи.
• Наиболее важной с точки зрения строения и свойств
сополимеров является стадия роста цепи. Она полностью
определяет как состав сополимера, так и распределение
мономерных звеньев в его макромолекулах.
• Модель Майо – Льюиса – модель концевого звена: реакционная
способность активного центра на конце растущей цепи
определяется только природой концевого звена
5.
Допущения, позволяющие значительно упростить выводколичественных соотношений при цепной соПМ
1. Все стадии соПМ необратимы.
2. СоПМ происходит в условиях псевдостационарного
состояния.
3. Реакционная способность растущих активных центров не
зависит от
длины цепи (принцип Флори).
4. Мономеры расходуются только на стадии роста цепи,
поэтому расходом мономеров в реакциях инициирования и
передачи цепи можно пренебречь.
5. Скорость инициирования
мономерной смеси.
не
зависит
от
состава
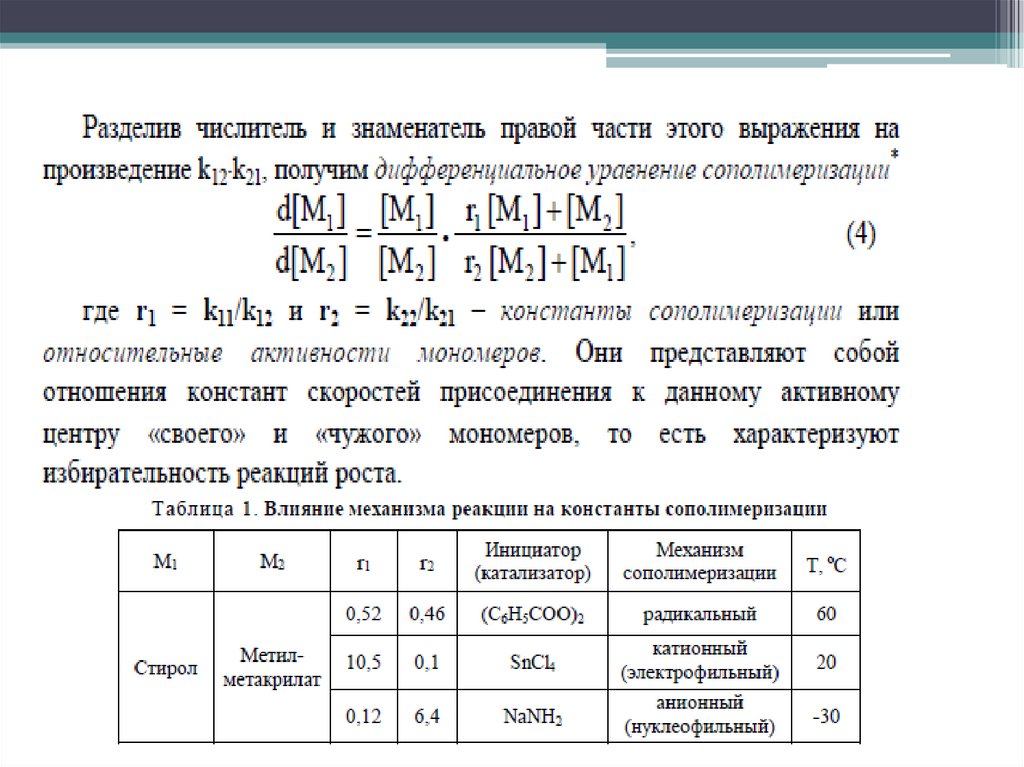
6. Уравнение дифференциального состава сополимера Майо-Льюиса
1- 4элементарные
реакции роста
цепи (гоморост
и перекрестный
рост)
7.
8.
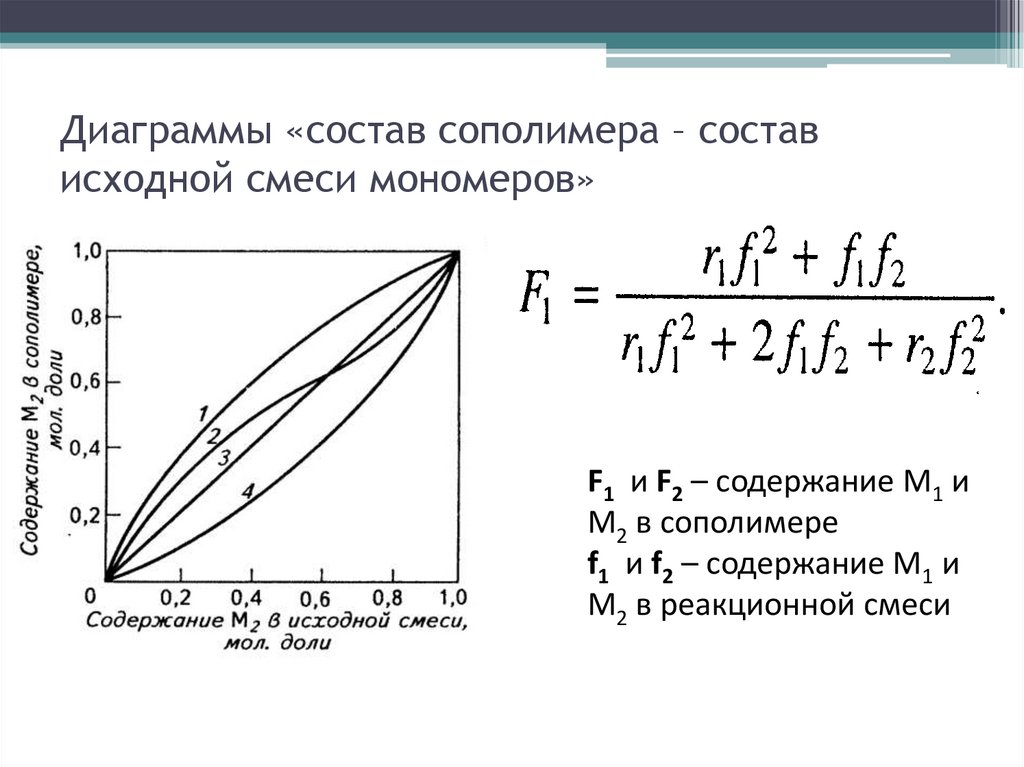
9. Диаграммы «состав сополимера – состав исходной смеси мономеров»
F1 и F2 – содержание М1 иМ2 в сополимере
f1 и f2 – содержание М1 и
М2 в реакционной смеси
10. Пределы применимости уравнения СоПМ
• Уравнение СоПМ отражает мгновенный составсополимера
• Уравнение СоПМ применимо для рад., кат., ан. процессов;
ионная СоПМ всегда более селективна
• Для всех типов инициирования константы СоПМ и,
следовательно, состав сополимера не зависят от:
- от температуры в рамках одного типа инициирования;
- констант скоростей инициирования и обрыва цепи;
- отсутствия или наличия агентов передачи цепи и
ингибиторов;
- от степени полимеризации;
- в рамках одного типа инициирования не зависит от
конкретного выбора инициатора.
11. Типы процессов СоПМ в зависимости от величины констант СоПМ Идеальная СоПМ, r1 . r2=1 - обе растущие частицы обладают
одинаковой способностьюприсоединять оба мономера, распределение
звеньев - статистическое
r1 = r2=1 (прямая 1)
Частные случаи:
r1 >1 r2<1 (кривая 2)
r1 <1 r2>1 (кривая 4)
12. Регулярно чередующаяся СоПМ, r1 . r2=0, эквимольный состав, чередующееся распределение звеньев
r1 = r2=0, кривая 5Частные случаи:
r1 =0 r2<1 кривая 6
r1 =0 r2>1 кривая 7
13.
• Блочная СоПМ r1 >1 r2>1- одновременная гомополимеризация r1 >>1 r2>>1
• Особые случаи СоПМ:
- азеотропная СоПМ (r1<1 и r2<1) кривая 3
- последовательная гомополимеризация (r1 >>1
r2<<1)
14. Специфические особенности радикальной СоПМ
• Константы СоПМ почти не зависят отприроды реакционной среды и метода
проведения процесса, от температуры
процесса.
• Реакционная способность радикалов и
мономеров зависит от сопряжения
(резонансного эффекта); стерических
затруднений; полярности.
15. Схема Q –e Алфрея и Прайса
- полуэмпирический подход к определениюконстант сополимеризации, предложенный
для радикальной сополимеризации. В этом
методе реакционная способность мономеров
по отношению к радикалам характеризуется
двумя параметрами: резонансной
стабилизацией и полярным фактором.
16. Схема Q –e Алфрея и Прайса
.Схема Q –e Алфрея и Прайса
Схема Q –e Алфрея и Прайса: P1 – мера общей активности
радикала, Q2 – мера общей активности мономера, а е1 и е2 –
меры полярности радикала и мономера соответственно.
Величины P и Q определяют резонансные эффекты в радикале и
мономере. Одно и то же значение е относится и к мономеру, и к
его радикалу (допущение).
kij = PiQj exp(-eiej)
17.
Схема Q –e Алфрея и ПрайсаДля стирола принято Q = 1.0 и е = -0.8. Относительные
величины Q и е для других мономеров определяют из
экспериментальных значений r1 и r2 по уравнениям:
.
1. Если мономеры не проявляют полярный эффект (е1=е2=0), то
r1=Q1/Q2, r2=Q2/Q1 и r1r2=1. Это случай "идеальной"
сополимеризации, при которой активность мономеров определяется
только фактором сопряжения, а распределение звеньев в
макромолекуле носит статистический характер.
2. Если мономеры содержат противоположные по направлению
поляризации заместители (например, е1<0<е2), полярный эффект
оказывает существенное влияние и на скорость реакции, и на
строение сополимера. Тогда r1r2=exp{-(e1-e2)}2 стремится к нулю,
наблюдается тенденция к чередованию мономерных звеньев за счет
преобладания реакций перекрестного роста.
















 chemistry
chemistry








