Similar presentations:
Полиэлектролиты
1. ПОЛИЭЛЕКТРОЛИТЫ
2.
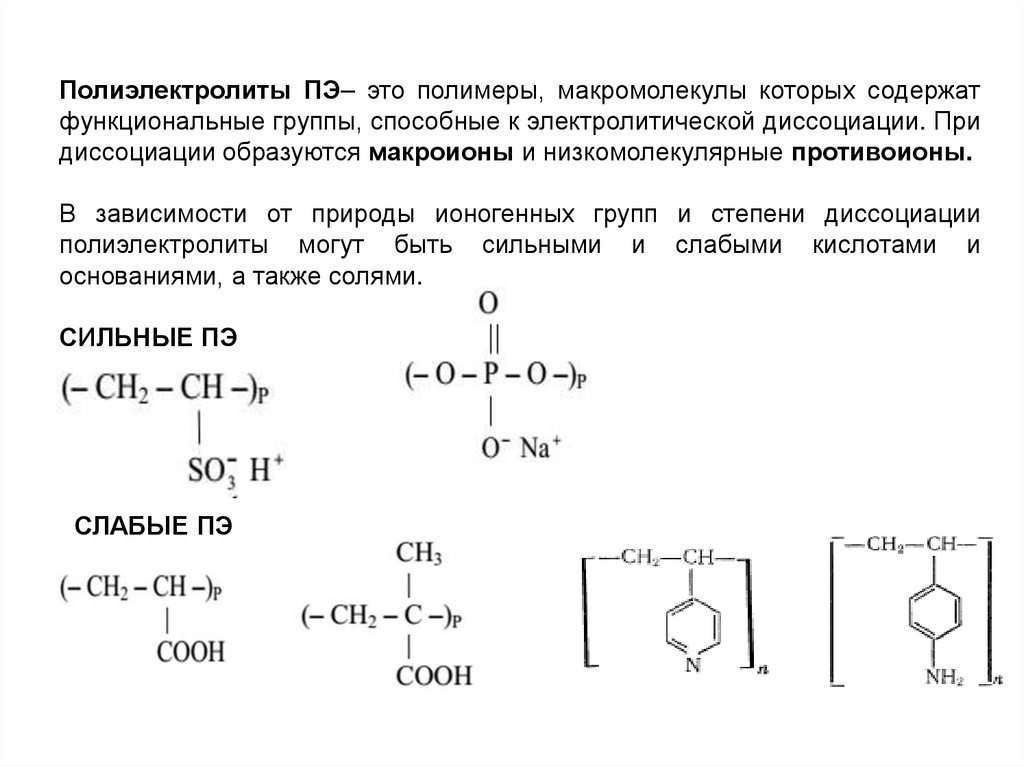
Полиэлектролиты ПЭ– это полимеры, макромолекулы которых содержатфункциональные группы, способные к электролитической диссоциации. При
диссоциации образуются макроионы и низкомолекулярные противоионы.
В зависимости от природы ионогенных групп и степени диссоциации
полиэлектролиты могут быть сильными и слабыми кислотами и
основаниями, а также солями.
СИЛЬНЫЕ ПЭ
Полиэлектролиты: классификация, применение.
СЛАБЫЕ ПЭ
3.
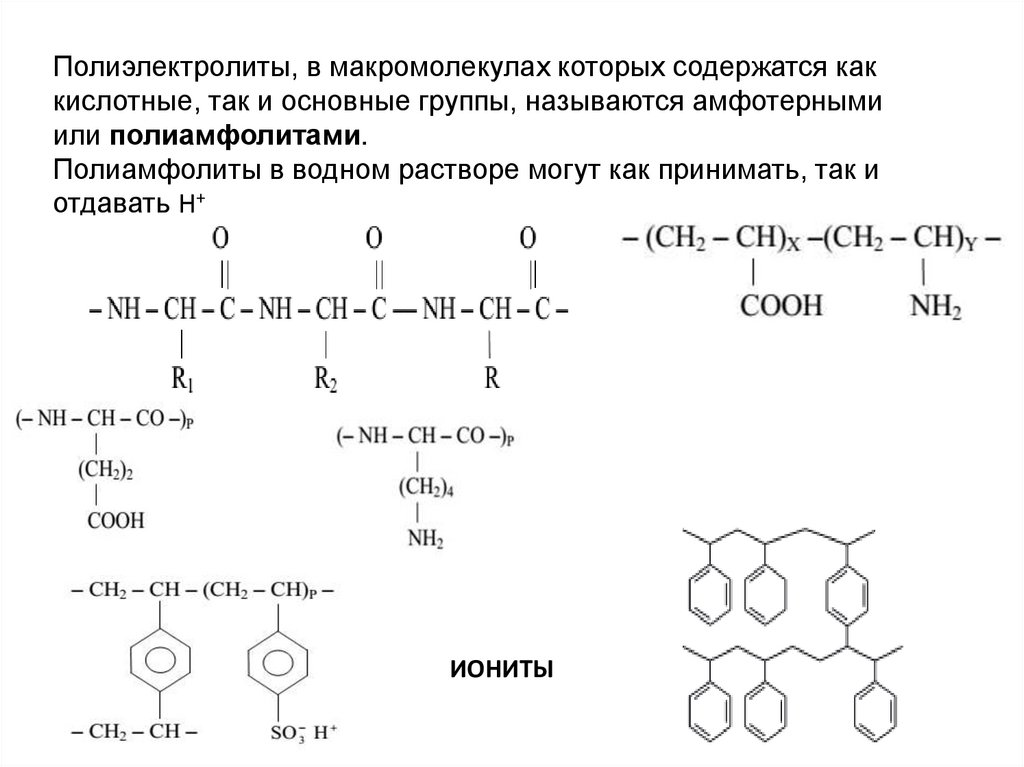
Полиэлектролиты, в макромолекулах которых содержатся каккислотные, так и основные группы, называются амфотерными
или полиамфолитами.
Полиамфолиты в водном растворе могут как принимать, так и
отдавать Н+
ИОНИТЫ
4.
ПЭ сочетают свойства неионогенных полимеров инизкомолекулярных электролитов - растворы
полиэлектролитов, как и растворы неионогенных полимеров,
обладают высокой вязкостью и, как растворы
низкомолекулярных электролитов, хорошо проводят
электрический ток.
Все специфические свойства ПЭ проявляются лишь
в условиях, когда их макромолекулы несут
локально нескомпенсированные заряды.
Эти свойства определяются взаимодействием заряженных
групп полиионов между собой и с окружающими их
низкомолекулярными противоионами.
5.
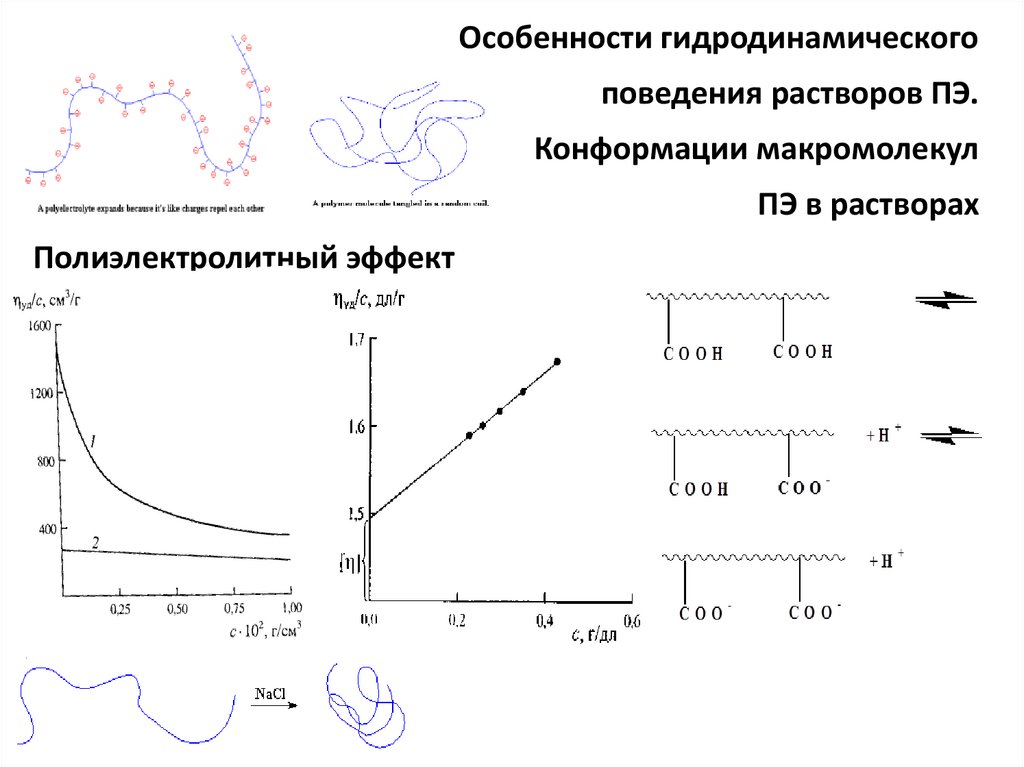
Особенности гидродинамическогоповедения растворов ПЭ.
Конформации макромолекул
ПЭ в растворах
Полиэлектролитный эффект
6.
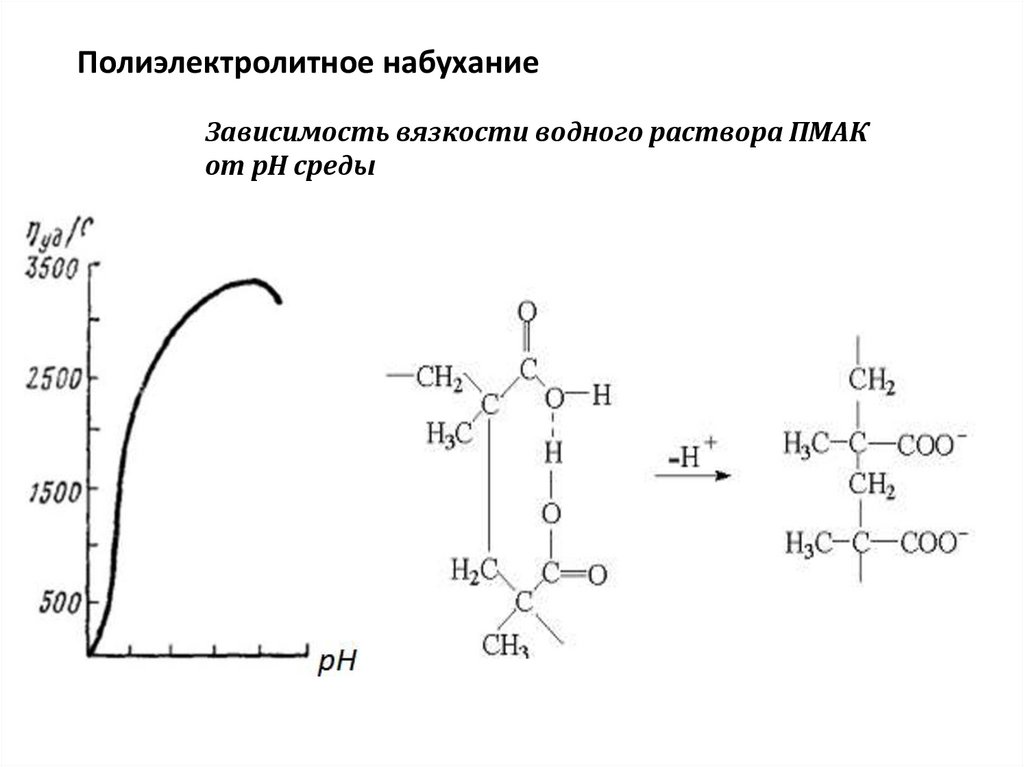
Полиэлектролитное набуханиеЗависимость вязкости водного раствора ПМАК
от рН среды
7.
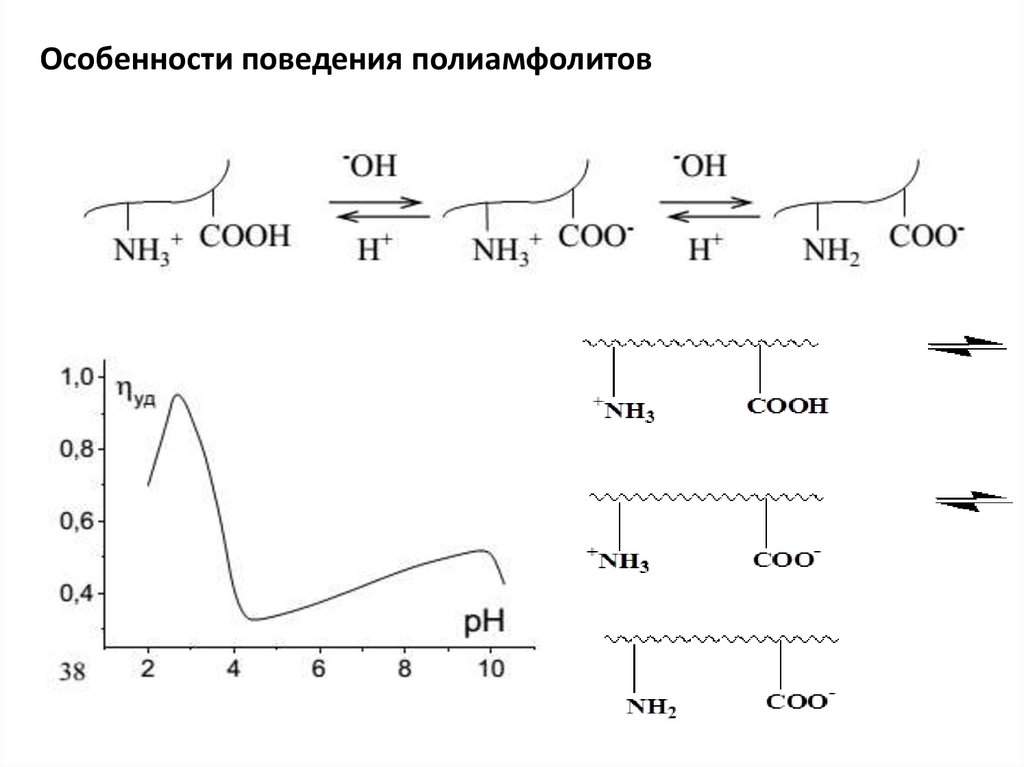
Особенности поведения полиамфолитов8.
Характеристики полиамфолитовИЭТ – значение рН раствора, при кот. суммарный заряд
на цепи равен 0. Степень набухания, растворимость
полиамфолитов, осмотическое давление и вязкость их
растворов в ИЭТ проходят через минимум. ИЭТ не
зависит от концентрации полиамфолита и является его
характеристикой.
ИИТ – величина рН водного раствора полиамфолита в
отсутствие посторонних ионов, определяемая только
диссоциацией собственных ионогенных групп и
зависящая от природы и соотношения ионогенных групп.
Зависит от концентрации раствора.
9.
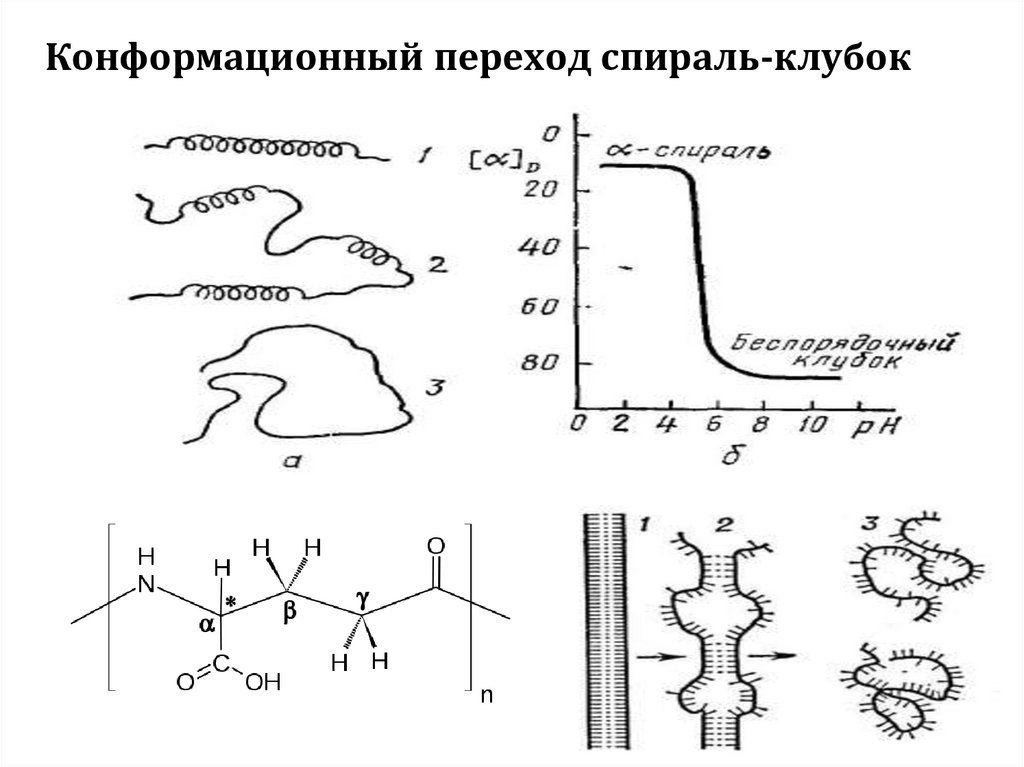
Конформационный переход спираль-клубок10.
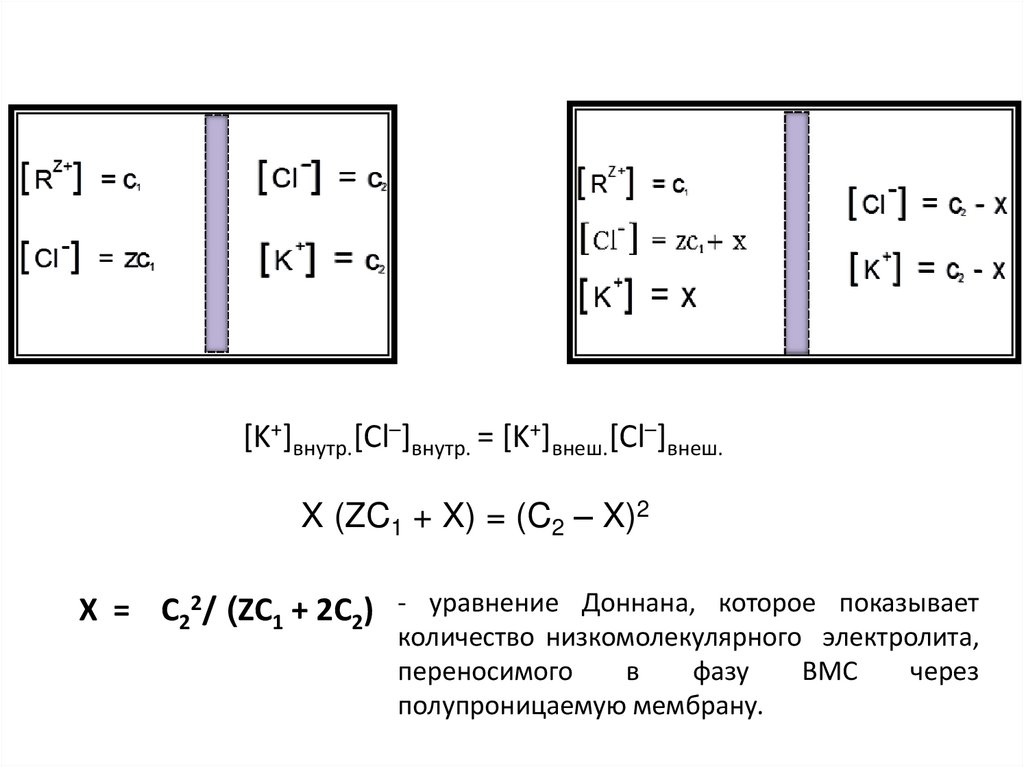
Мембранное равновесие Ф. ДоннанаМембранное равновесие играет большую роль при
распределении ионов между клетками и окружающей их
средой, при возникновении биопотенциалов, при
набухании живых тканей и др.
Мембранное равновесие Доннана связано с переносом
некоторого количества вещества низкомолекулярного
электролита
внутрь
пространства,
содержащего
полимер, и, вследствие этого, неравномерного
распределения концентраций этого электролита по обе
стороны полупроницаемой мембраны.
11.
[K+]внутр.[Cl–]внутр. = [K+]внеш.[Cl–]внеш.X (ZC1 + X) = (C2 – X)2
X = C22/ (ZC1 + 2C2) - уравнение Доннана, которое показывает
количество низкомолекулярного электролита,
переносимого
в
фазу
ВМС
через
полупроницаемую мембрану.
12.
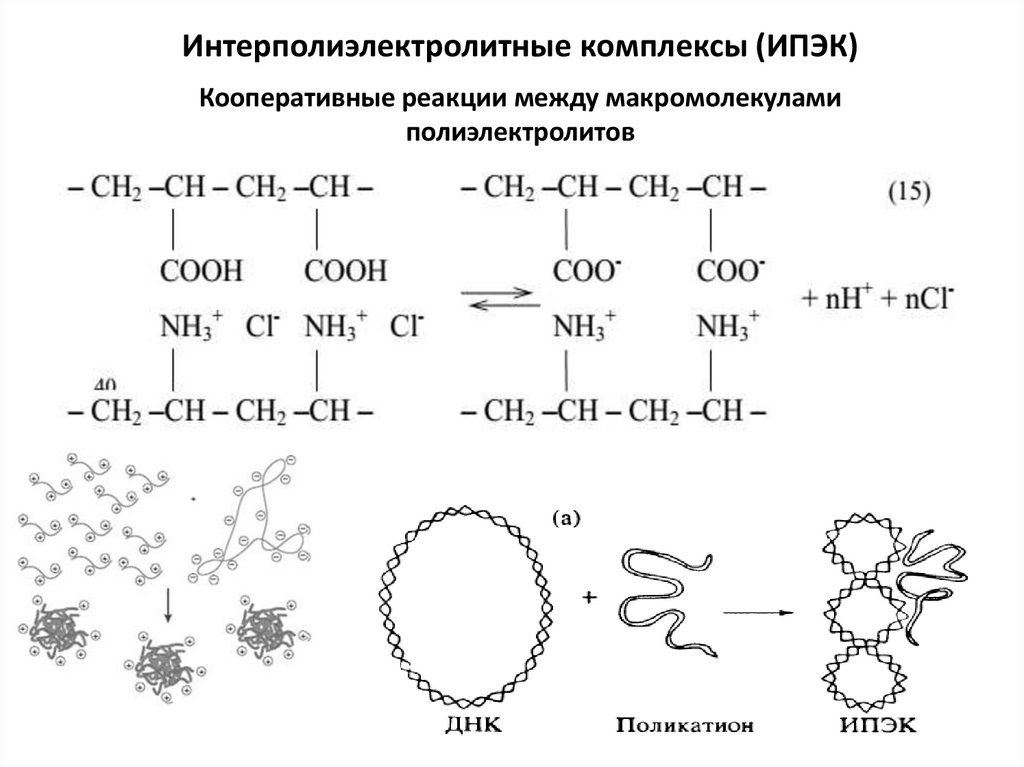
Интерполиэлектролитные комплексы (ИПЭК)Кооперативные реакции между макромолекулами
полиэлектролитов
13.
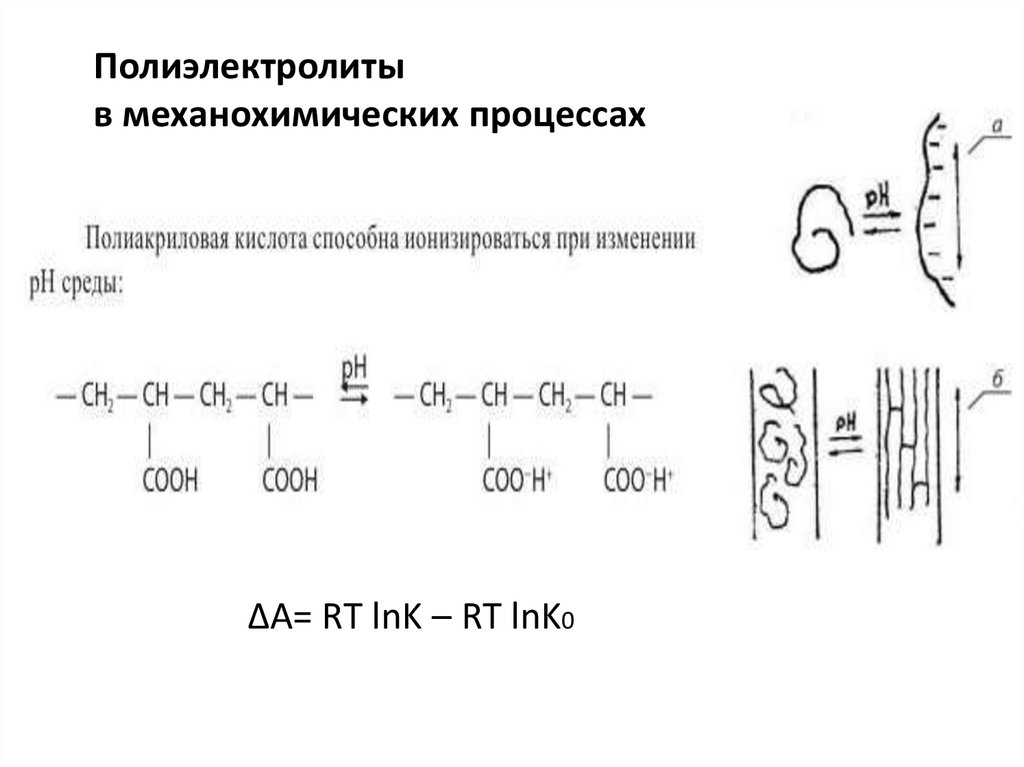
Полиэлектролитыв механохимических процессах
ΔA= RT lnK – RT lnK0




 chemistry
chemistry