Similar presentations:
Гидродинамические свойства полимеров. Полиэлектролиты
1. Гидродинамические свойства полимеров. Полиэлектролиты.
2.
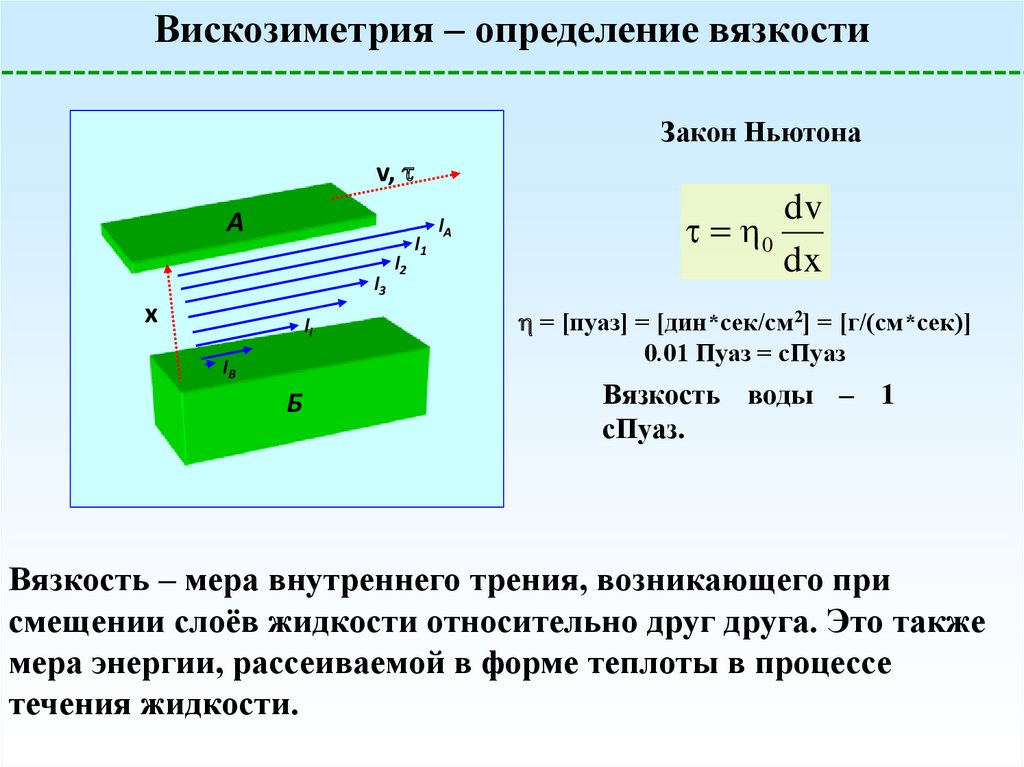
Вискозиметрия – определение вязкостиЗакон Ньютона
v,
A
l3
x
li
lB
Б
l2
l1
lA
dv
0
dx
= [пуаз] = [дин*сек/см2] = [г/(см*сек)]
0.01 Пуаз = сПуаз
Вязкость воды – 1
сПуаз.
Вязкость – мера внутреннего трения, возникающего при
смещении слоёв жидкости относительно друг друга. Это также
мера энергии, рассеиваемой в форме теплоты в процессе
течения жидкости.
3.
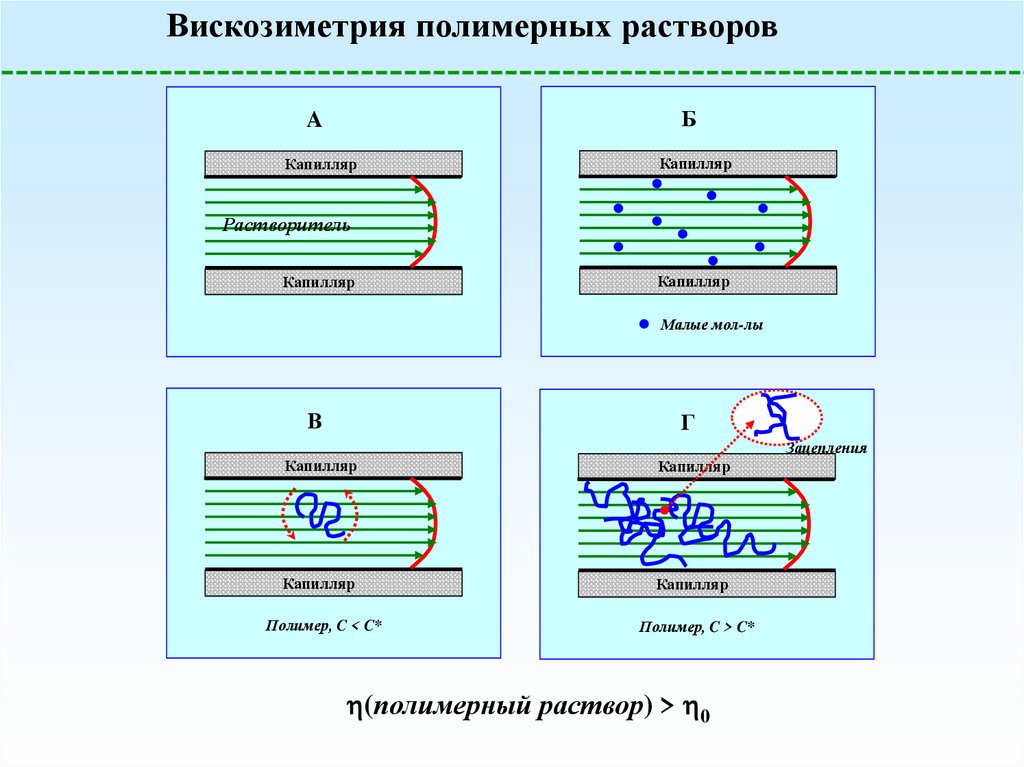
Вискозиметрия полимерных растворовБ
A
Капилляр
Капилляр
Растворитель
Капилляр
Капилляр
Малые мол-лы
В
Г
Зацепления
Капилляр
Капилляр
Капилляр
Капилляр
Полимер, C < C*
Полимер, C > C*
(полимерный раствор) > 0
4.
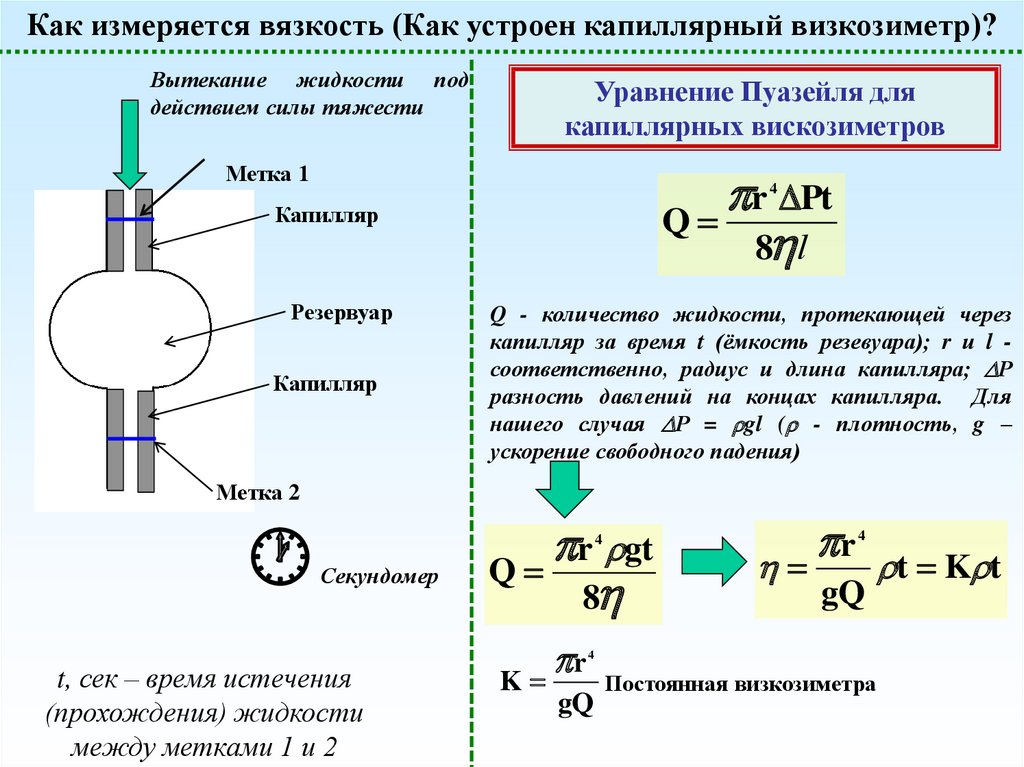
Как измеряется вязкость (Как устроен капиллярный визкозиметр)?Вытекание жидкости под
действием силы тяжести
Уравнение Пуазейля для
капиллярных вискозиметров
r Pt
Q
8 l
Метка 1
4
Капилляр
Резервуар
Капилляр
Q - количество жидкости, протекающей через
капилляр за время t (ёмкость резевуара); r и l соответственно, радиус и длина капилляра; Р
разность давлений на концах капилляра. Для
нашего случая Р = gl ( - плотность, g –
ускорение свободного падения)
Метка 2
r gt
Q
8
4
Секундомер
t, сек – время истечения
(прохождения) жидкости
между метками 1 и 2
r
K
r
4
gQ
4
gQ
Постоянная визкозиметра
t K t
5.
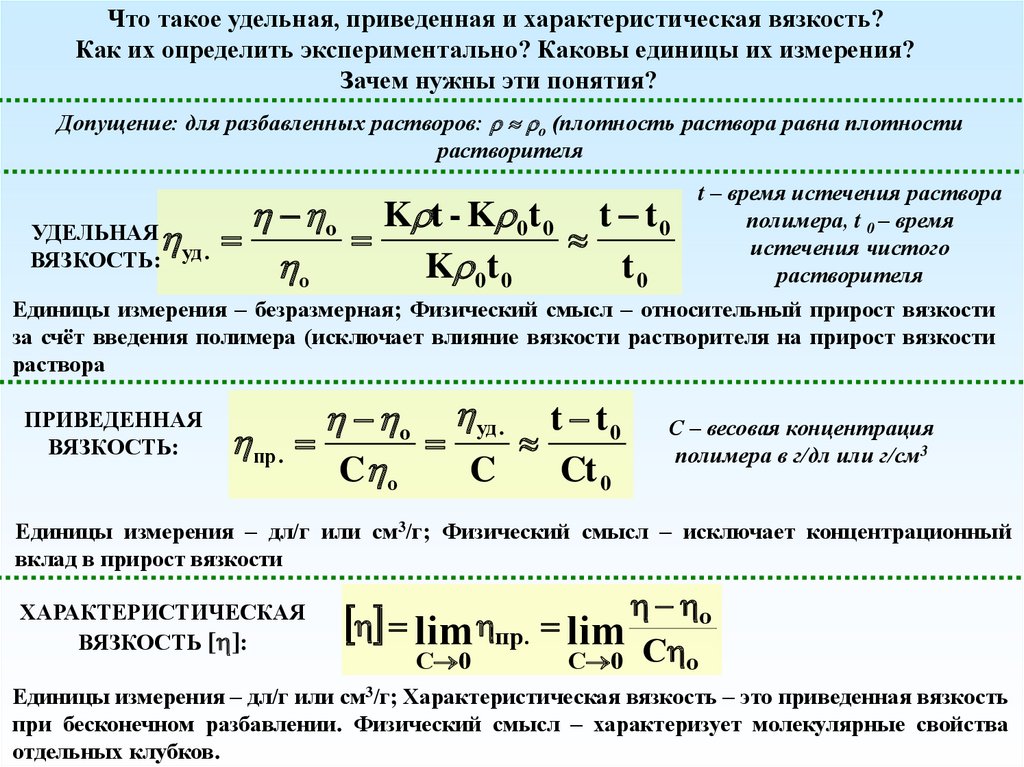
Что такое удельная, приведенная и характеристическая вязкость?Как их определить экспериментально? Каковы единицы их измерения?
Зачем нужны эти понятия?
Допущение: для разбавленных растворов: o (плотность раствора равна плотности
растворителя
t – время истечения раствора
o K t - K 0t 0 t t 0
полимера, t 0 – время
УДЕЛЬНАЯ
истечения чистого
ВЯЗКОСТЬ: уд .
K
t
t
растворителя
о
0 0
0
Единицы измерения – безразмерная; Физический смысл – относительный прирост вязкости
за счёт введения полимера (исключает влияние вязкости растворителя на прирост вязкости
раствора
ПРИВЕДЕННАЯ
ВЯЗКОСТЬ:
пр .
o уд . t t 0
C о
C
Ct 0
С – весовая концентрация
полимера в г/дл или г/см3
Единицы измерения – дл/г или см3/г; Физический смысл – исключает концентрационный
вклад в прирост вязкости
ХАРАКТЕРИСТИЧЕСКАЯ
ВЯЗКОСТЬ [ ]:
lim пр. lim o
C 0
C 0
С о
Единицы измерения – дл/г или см3/г; Характеристическая вязкость – это приведенная вязкость
при бесконечном разбавлении. Физический смысл – характеризует молекулярные свойства
отдельных клубков.
6.
Как экспериментально определить характеристическуювязкость?
Уравнение Хаггинса (эмпирическое) для разбавленных растворов
незаряженных полимеров:
пр.
пр . 2 K hC
tg =[ ]2Kh
[ ]
С, г/дл
Kh - Константа Хаггинса - для гибкоцепных полимеров качественно характеризует
термодинамическое качество растворителя:
Kh = 0.2 0.3 - термодинамически хорошие растворители;
Kh > 0.5 - термодинамически плохие растворители;
7.
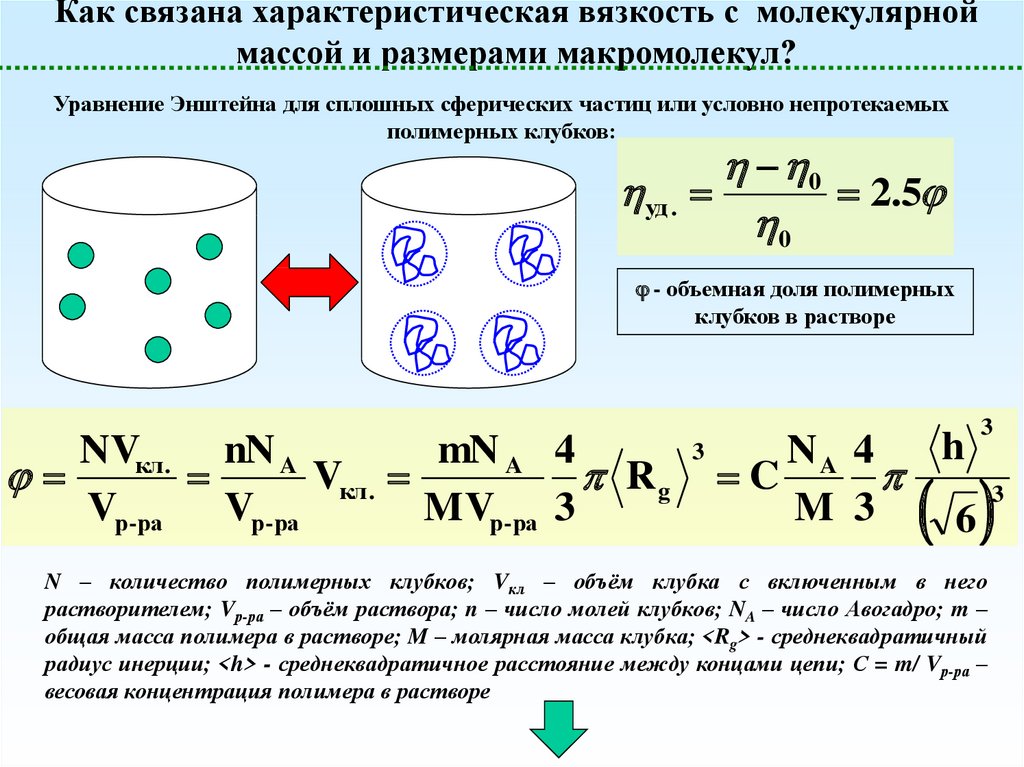
Как связана характеристическая вязкость с молекулярноймассой и размерами макромолекул?
Уравнение Энштейна для сплошных сферических частиц или условно непротекаемых
полимерных клубков:
уд .
0
2.5
0
- объемная доля полимерных
клубков в растворе
NVкл . nN A
mN A 4
Vкл .
Rg
Vр-ра
Vр-ра
MVр-ра 3
3
h
NA 4
C
M 3
6
3
N – количество полимерных клубков; Vкл – объём клубка с включенным в него
растворителем; Vр-ра – объём раствора; n – число молей клубков; NA – число Авогадро; m –
общая масса полимера в растворе; M – молярная масса клубка; <Rg> - среднеквадратичный
радиус инерции; <h> - среднеквадратичное расстояние между концами цепи; С = m/ Vр-ра –
весовая концентрация полимера в растворе
3
8.
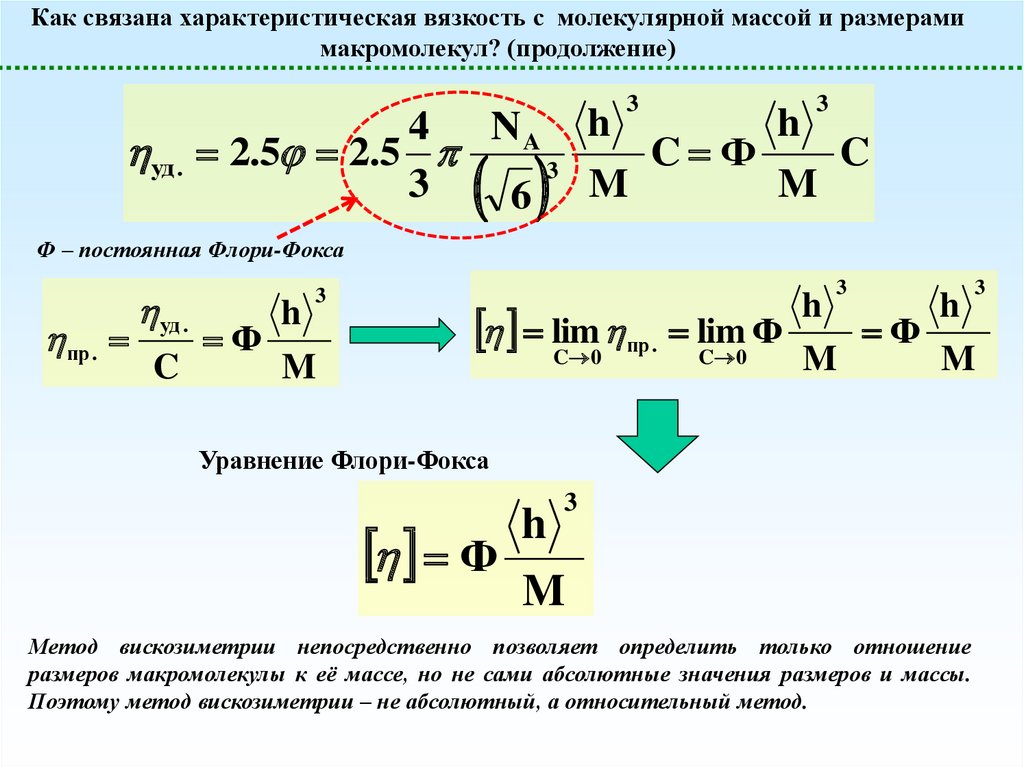
Как связана характеристическая вязкость с молекулярной массой и размерамимакромолекул? (продолжение)
3
уд .
3
h
4
NA h
2.5 2.5
C Ф
C
3
3
M
6 M
Ф – постоянная Флори-Фокса
пр .
уд .
3
h
Ф
C
M
lim
пр .
C 0
3
3
h
h
lim Ф
Ф
C 0
M
M
Уравнение Флори-Фокса
3
h
Ф
M
Метод вискозиметрии непосредственно позволяет определить только отношение
размеров макромолекулы к её массе, но не сами абсолютные значения размеров и массы.
Поэтому метод вискозиметрии – не абсолютный, а относительный метод.
9.
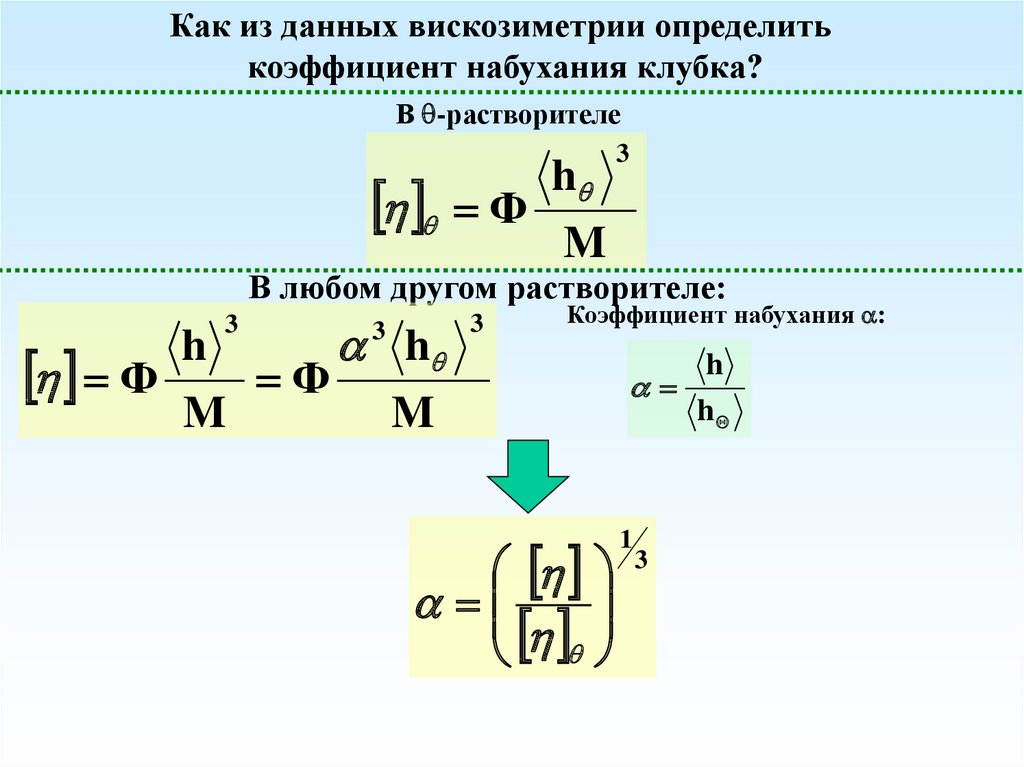
Как из данных вискозиметрии определитькоэффициент набухания клубка?
В -растворителе
Ф
3
h
M
В любом другом растворителе:
h
h
Ф
Ф
M
M
3
3
3
Коэффициент набухания :
h
h
1
3
10.
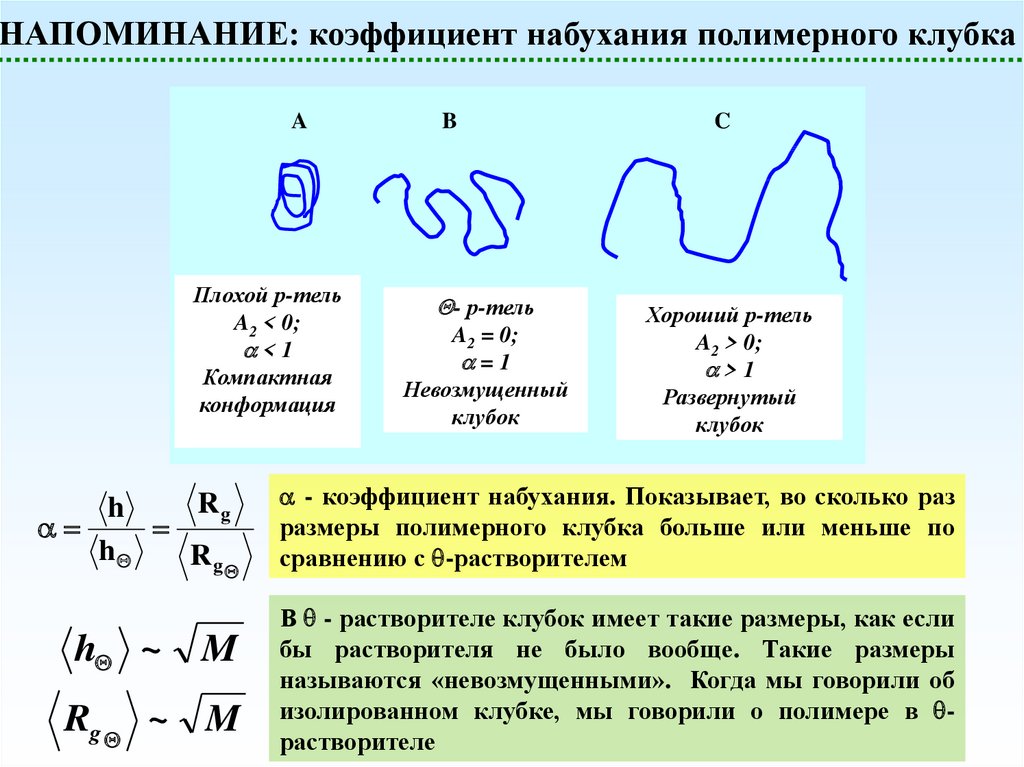
НАПОМИНАНИЕ: коэффициент набухания полимерного клубкаA
Плохой р-тель
A2 < 0;
<1
Компактная
конформация
Rg
h
h
Rg
h ~
M
Rg ~ M
B
- р-тель
A2 = 0;
=1
Невозмущенный
клубок
C
Хороший р-тель
A2 > 0;
>1
Развернутый
клубок
- коэффициент набухания. Показывает, во сколько раз
размеры полимерного клубка больше или меньше по
сравнению с -растворителем
В - растворителе клубок имеет такие размеры, как если
бы растворителя не было вообще. Такие размеры
называются «невозмущенными». Когда мы говорили об
изолированном клубке, мы говорили о полимере в растворителе
11.
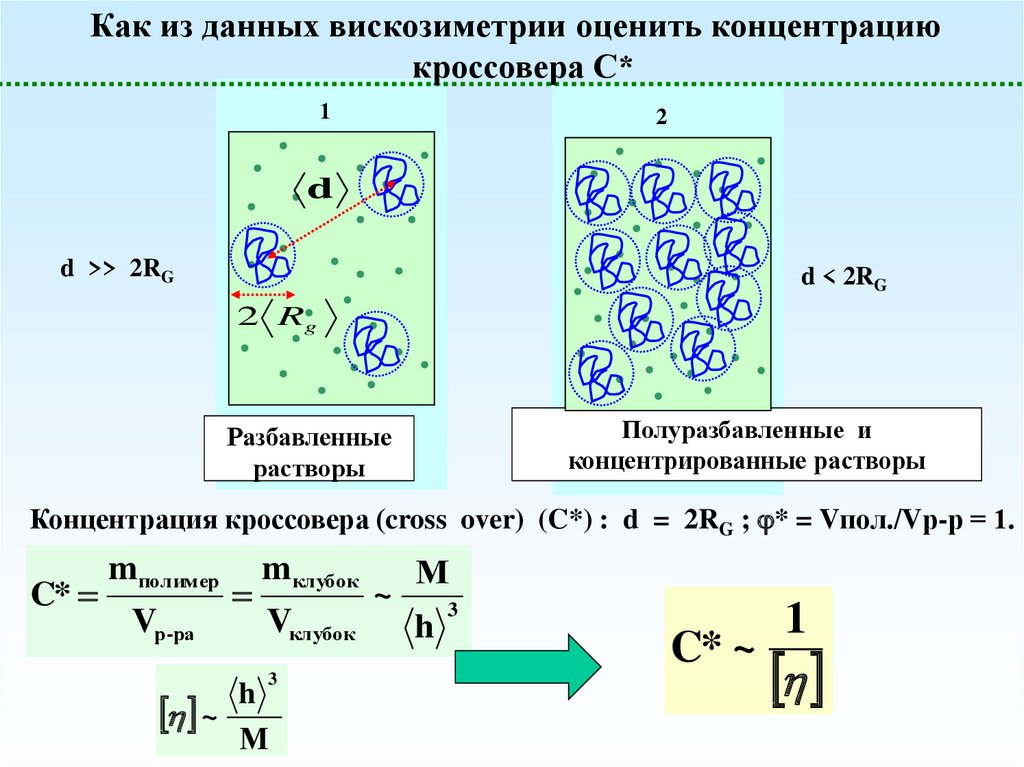
Как из данных вискозиметрии оценить концентрациюкроссовера С*
1
2
d
d >> 2RG
d < 2RG
2 Rg
Полуразбавленные и
концентрированные растворы
Разбавленные
растворы
Концентрация кроссовера (cross over) (C*) : d = 2RG ; * = Vпол./Vр-р = 1.
C*
mполимер
Vр-ра
m клубок
Vклубок
3
h
~
М
~
М
h
3
C* ~
1
12.
~Можно ли из данных вискозиметрии определить
молекулярную массу полимера?
3
Можно исключить <h> и
h
характеристическую вязкость
сделать
функцией
одной переменной – молекулярной массы М.
h ~M
М
Уравнение Марка-Куна-Хаувинка
KM
a
К и а – постоянные для данной
системы полимер-растворитель при
постоянной температуре
Как получить значения К и а? Они берутся из калибровки: для серии полимерных образцов
разных молекулярных масс (определенных другими методами) экспериментально
определяются значения [ ]. Строится зависимость lg[ ] от lgM. Полученные значения К и а
заносятся в справочники и используются для определения молекулярной массы полимерных
образцов данной химической структуры.
lg[ ]
lg[ ] lg K a lg M
lg K
lg M
tg = a
Mn M M w
M - Средневязкостная молекулярная масса
13.
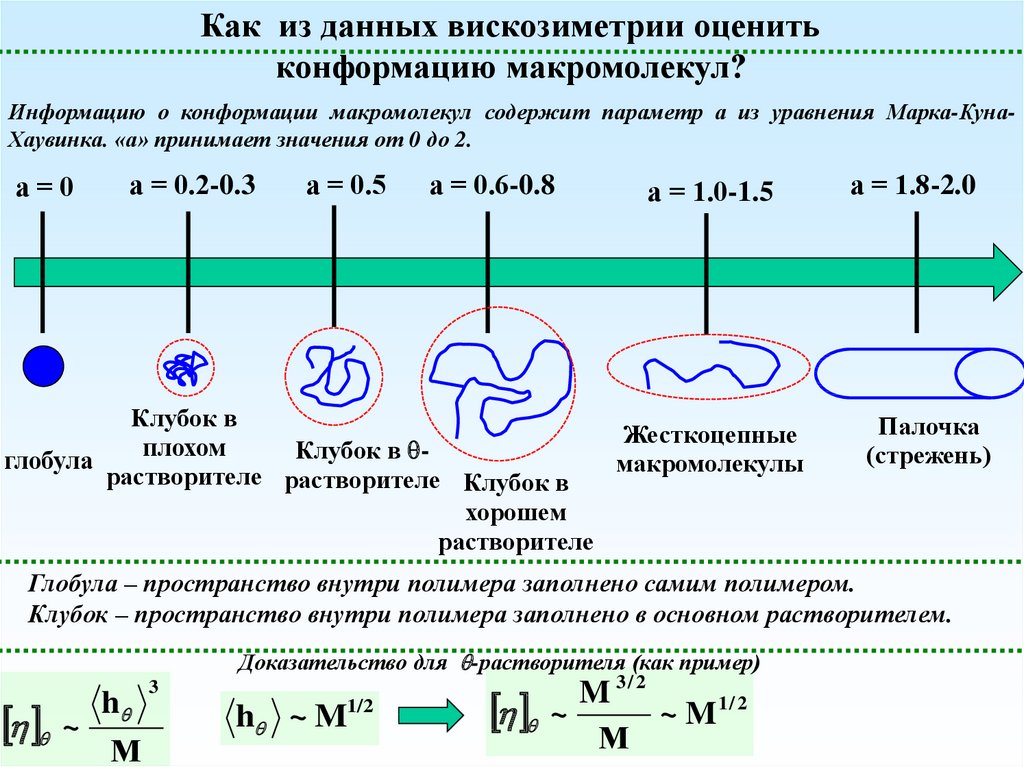
Как из данных вискозиметрии оценитьконформацию макромолекул?
Информацию о конформации макромолекул содержит параметр а из уравнения Марка-КунаХаувинка. «а» принимает значения от 0 до 2.
а=0
а = 0.2-0.3
а = 0.5
а = 0.6-0.8
а = 1.0-1.5
Клубок в
Жесткоцепные
плохом
Клубок
в
глобула
макромолекулы
растворителе растворителе Клубок в
хорошем
растворителе
а = 1.8-2.0
Палочка
(стрежень)
Глобула – пространство внутри полимера заполнено самим полимером.
Клубок – пространство внутри полимера заполнено в основном растворителем.
Доказательство для -растворителя (как пример)
~
h
М
3
h ~ M1/2
M 3/ 2
~
~ M1 / 2
М
14.
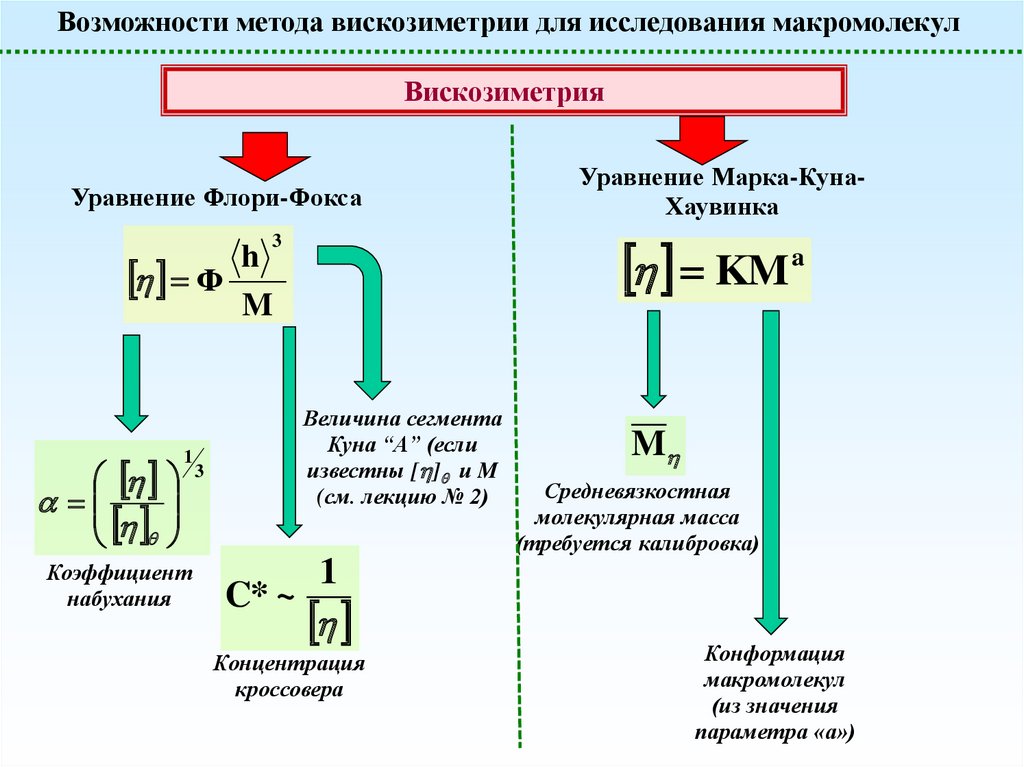
Возможности метода вискозиметрии для исследования макромолекулВискозиметрия
Уравнение Флори-Фокса
KM
3
h
Ф
M
1
Коэффициент
набухания
Величина сегмента
Куна “A” (если
известны [ ] и M
(см. лекцию № 2)
3
C* ~
Уравнение Марка-КунаХаувинка
a
M
Средневязкостная
молекулярная масса
(требуется калибровка)
1
Концентрация
кроссовера
Конформация
макромолекул
(из значения
параметра «а»)
15.
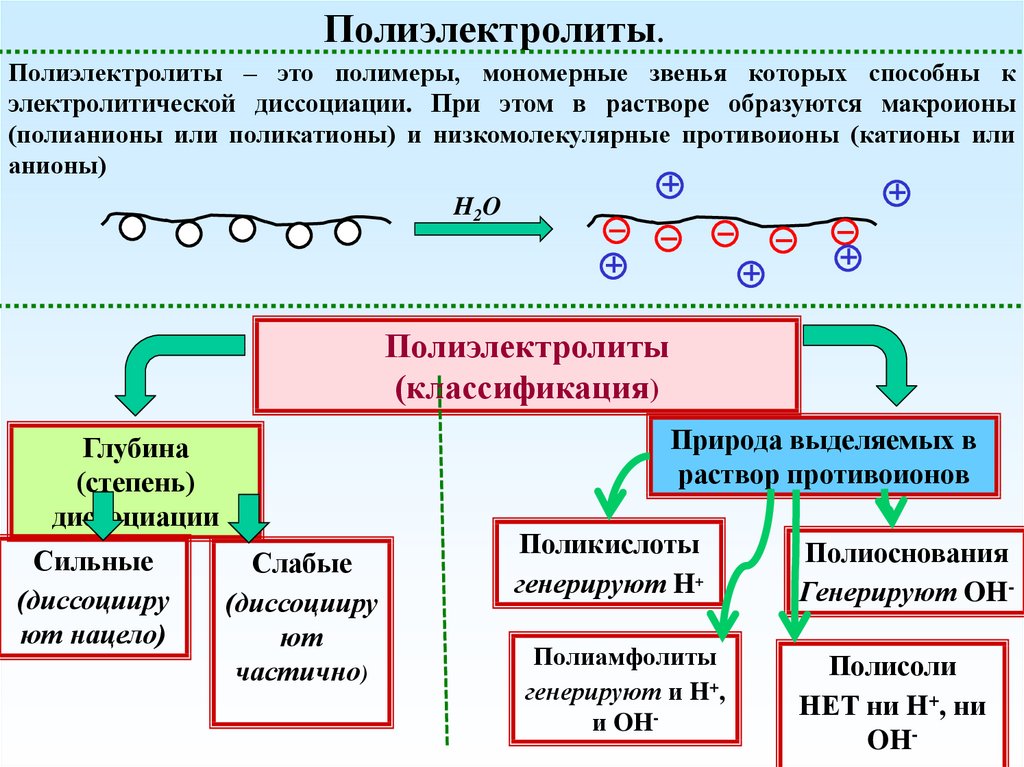
Полиэлектролиты.Полиэлектролиты – это полимеры, мономерные звенья которых способны к
электролитической диссоциации. При этом в растворе образуются макроионы
(полианионы или поликатионы) и низкомолекулярные противоионы (катионы или
анионы)
H2O
Полиэлектролиты
(классификация)
Природа выделяемых в
раствор противоионов
Глубина
(степень)
диссоциации
Сильные
(диссоцииру
ют нацело)
Слабые
(диссоцииру
ют
частично)
Поликислоты
генерируют H+
Полиамфолиты
генерируют и H+,
и OH-
Полиоснования
Генерируют OHПолисоли
НЕТ ни H+, ни
OH-
16.
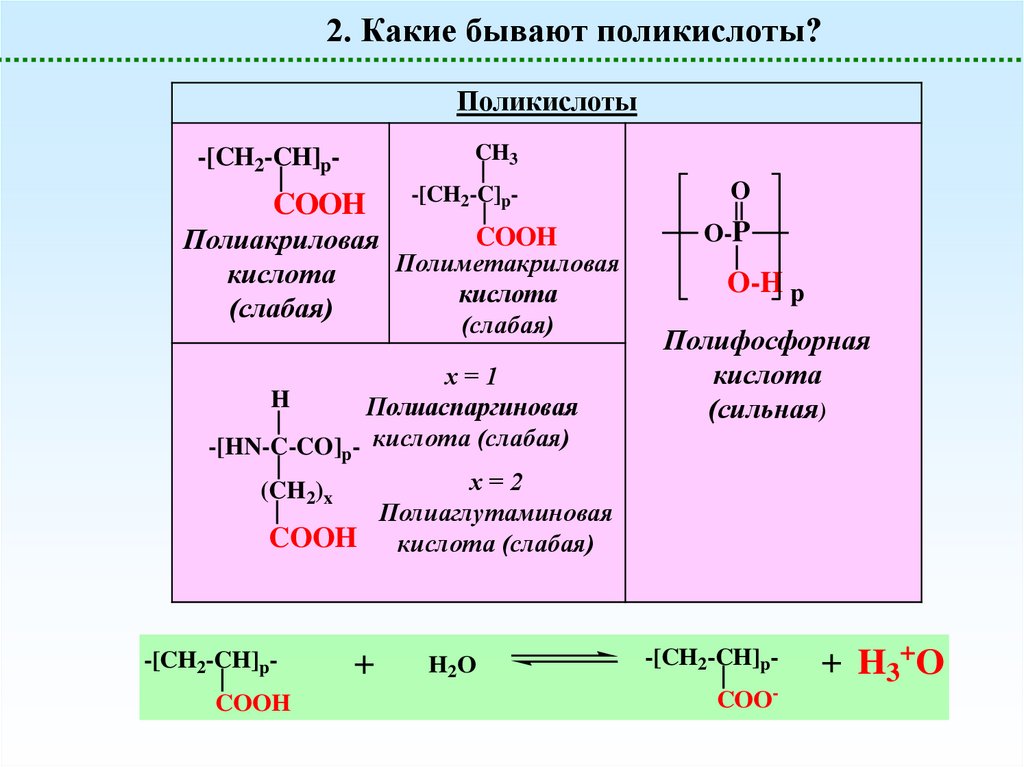
2. Какие бывают поликислоты?Поликислоты
CH3
-[CH2-CH]p-
COOH
-[CH2-C]p-
COOH
Полиакриловая
Полиметакриловая
кислота
кислота
(слабая)
(слабая)
х=1
H
Полиаспаргиновая
-[HN-C-CO]p- кислота (слабая)
х=2
(CH2)x
Полиаглутаминовая
COOH кислота (слабая)
-[CH2-CH]pCOOH
+
H2O
O
O-P
O-H p
Полифосфорная
кислота
(сильная)
-[CH2-CH]pCOO-
+ H3+O
17.
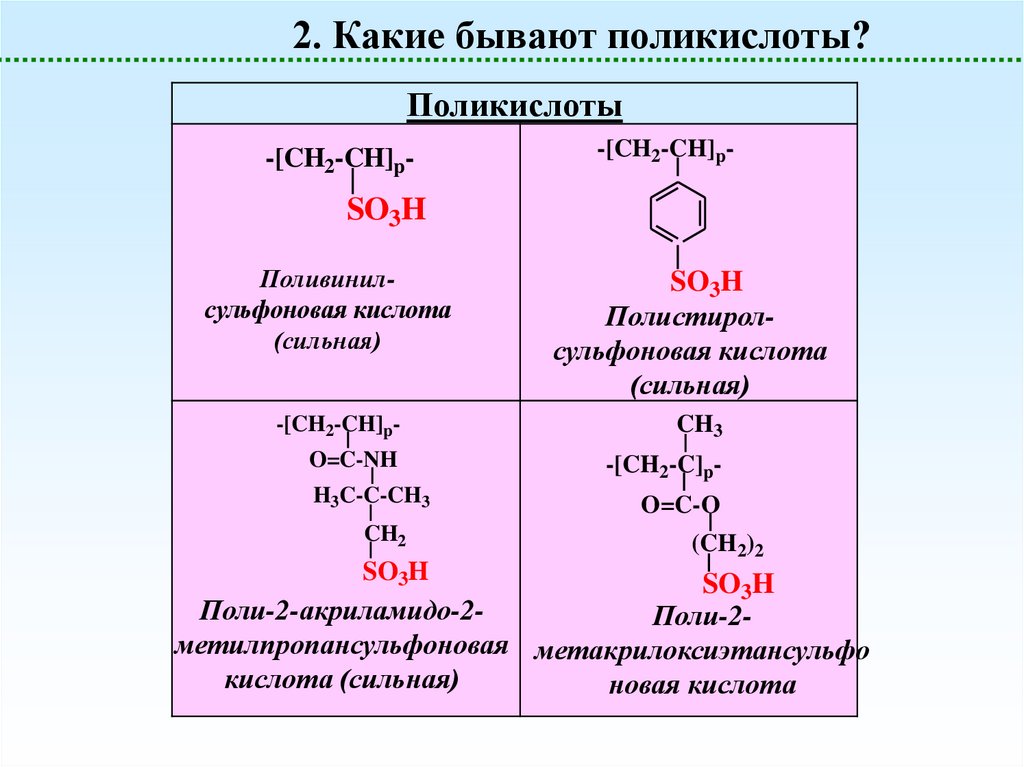
2. Какие бывают поликислоты?Поликислоты
-[CH2-CH]p-
-[CH2-CH]p-
SO3H
Поливинилсульфоновая кислота
(сильная)
SO3H
Полистиролсульфоновая кислота
(сильная)
-[CH2-CH]p-
CH3
O=C-NH
-[CH2-C]p-
H3C-C-CH3
CH2
SO3H
O=C-O
(CH2)2
SO3H
Поли-2-акриламидо-2Поли-2метилпропансульфоновая метакрилоксиэтансульфо
кислота (сильная)
новая кислота
18.
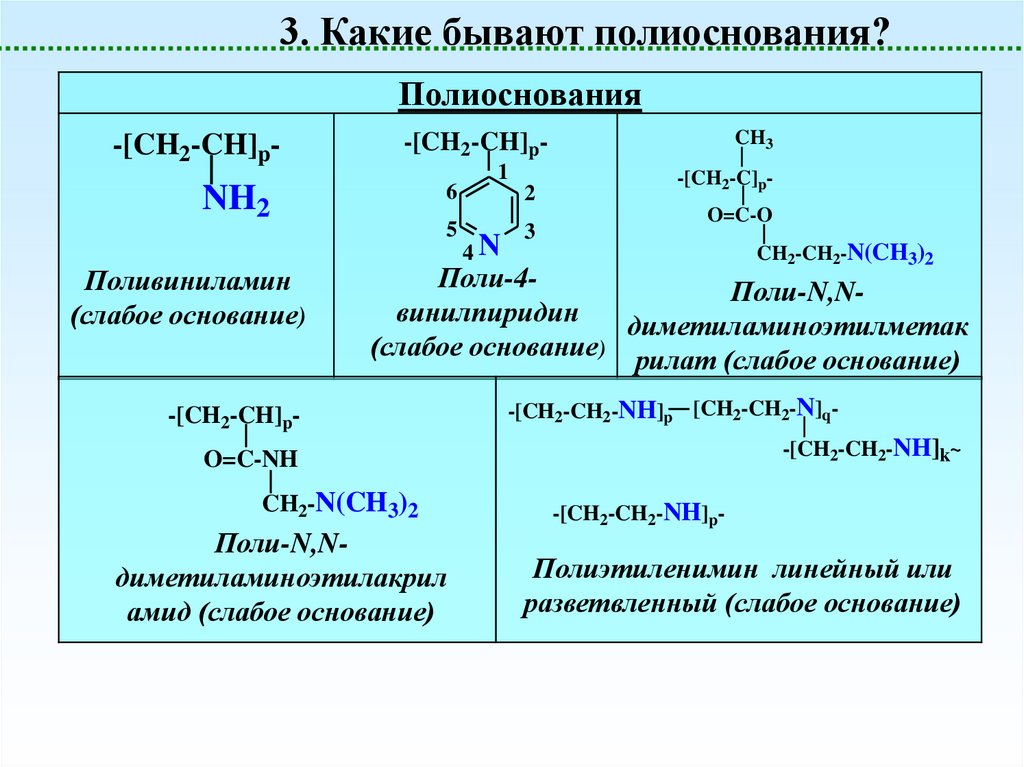
3. Какие бывают полиоснования?Полиоснования
-[CH2-CH]p-
6
NH2
Поливиниламин
(слабое основание)
CH3
-[CH2-CH]p5
1
2
4N
3
-[CH2-C]pO=C-O
CH2-CH2-N(CH3)2
Поли-4Поли-N,Nвинилпиридин
диметиламиноэтилметак
(слабое основание) рилат (слабое основание)
-[CH2-CH]p-
-[CH2-CH2-NH]p [CH2-CH2-N]q-[CH2-CH2-NH]k~
O=C-NH
CH2-N(CH3)2
Поли-N,Nдиметиламиноэтилакрил
амид (слабое основание)
-[CH2-CH2-NH]p-
Полиэтиленимин линейный или
разветвленный (слабое основание)
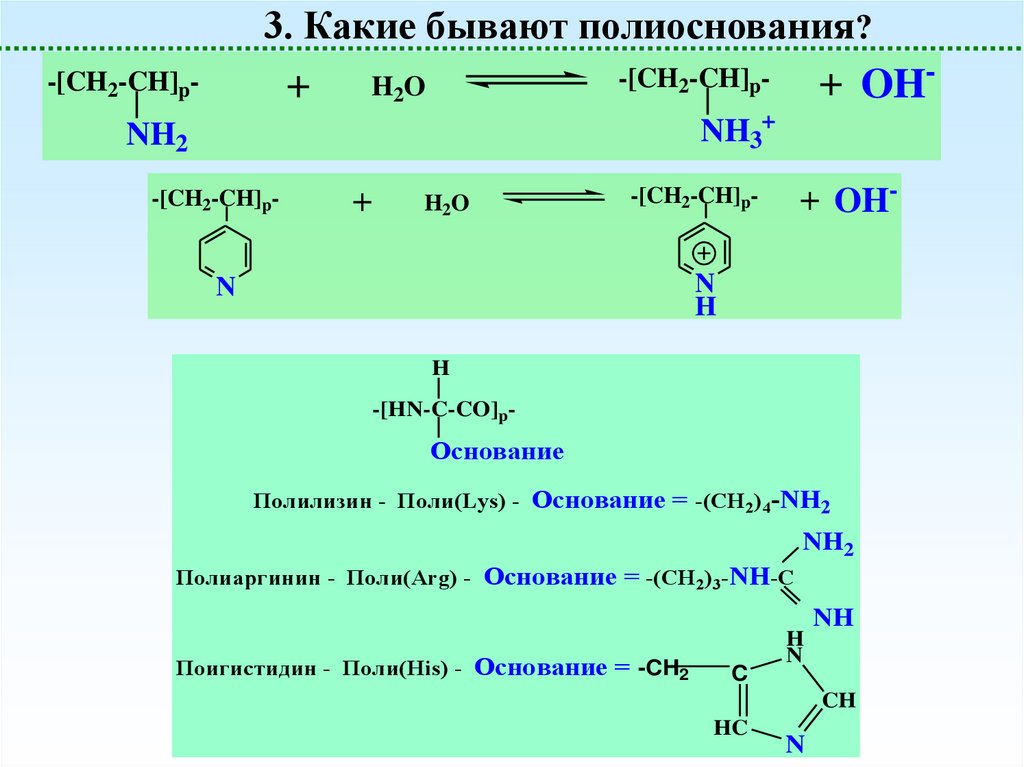
19.
3. Какие бывают полиоснования?-[CH2-CH]p+ OH+ H2O
-[CH2-CH]p-
NH3+
NH2
-[CH2-CH]p-
+
H2O
+ OH-
-[CH2-CH]p-
N
H
N
H
-[HN-C-CO]p-
Основание
Полилизин - Поли(Lys) - Основание = -(CH2)4-NH2
NH2
Полиаргинин - Поли(Arg) - Основание = -(CH2)3-NH-C
NH
Поигистидин - Поли(His) - Основание = -CH2
C
H
N
CH
HC
N
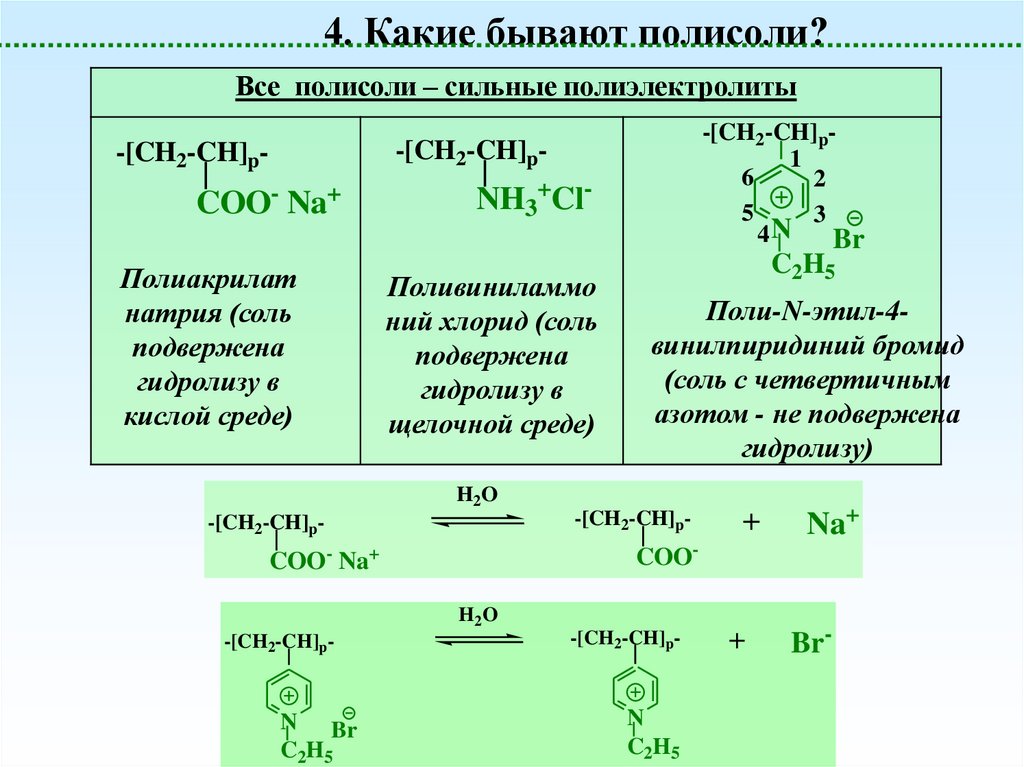
20.
4. Какие бывают полисоли?Все полисоли – сильные полиэлектролиты
-[CH2-CH]p1
6
2
5
3
4N
Br
-[CH2-CH]p-
-[CH2-CH]p-
COO- Na+
Полиакрилат
натрия (соль
подвержена
гидролизу в
кислой среде)
NH3+ClПоливиниламмо
ний хлорид (соль
подвержена
гидролизу в
щелочной среде)
C2H5
Поли-N-этил-4винилпиридиний бромид
(соль с четвертичным
азотом - не подвержена
гидролизу)
H2O
-[CH2-CH]p-
-[CH2-CH]p-
H2 O
N Br
C2H5
Na+
COO-
COO- Na+
-[CH2-CH]p-
+
-[CH2-CH]p-
N
C2H5
+
Br-
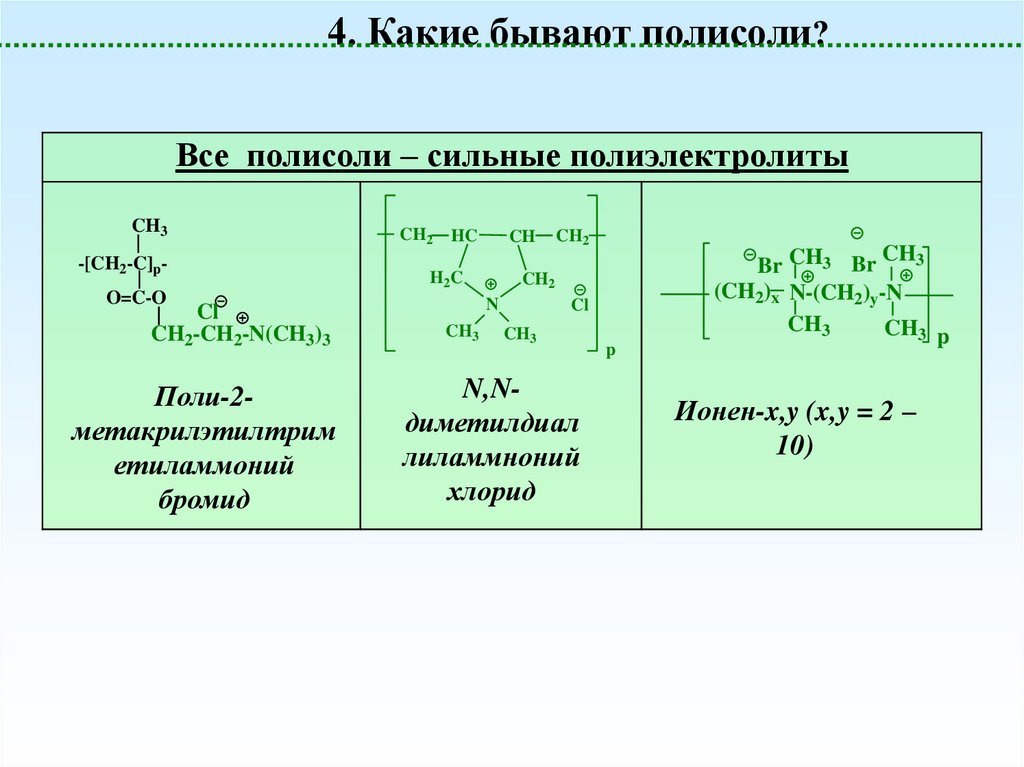
21.
4. Какие бывают полисоли?Все полисоли – сильные полиэлектролиты
CH3
-[CH2-C]p-
CH2
HC
H2C
O=C-O
Cl
CH2-CH2-N(CH3)3
Поли-2метакрилэтилтрим
етиламмоний
бромид
CH
CH2
N
CH3
CH2
Cl
CH3
N,Nдиметилдиал
лиламмноний
хлорид
p
CH3
Br CH3 Br
(CH2)x N-(CH2)y-N
CH3
CH3
Ионен-x,y (x,y = 2 –
10)
p
22.
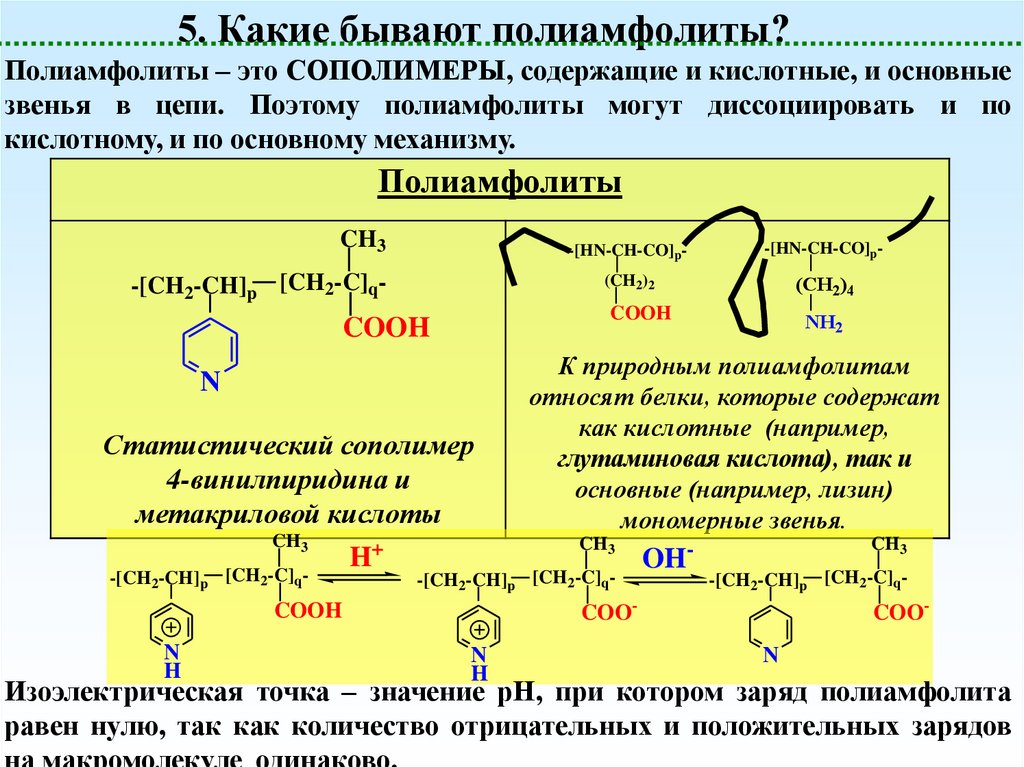
5. Какие бывают полиамфолиты?Полиамфолиты – это СОПОЛИМЕРЫ, содержащие и кислотные, и основные
звенья в цепи. Поэтому полиамфолиты могут диссоциировать и по
кислотному, и по основному механизму.
Полиамфолиты
CH3
-[CH2-CH]p [CH2-C]q-
N
Статистический сополимер
4-винилпиридина и
метакриловой кислоты
CH3
H+
(CH2)2
(CH2)4
NH2
К природным полиамфолитам
относят белки, которые содержат
как кислотные (например,
глутаминовая кислота), так и
основные (например, лизин)
мономерные звенья.
CH3
-[CH2-CH]p [CH2-C]q-
OH-
CH3
-[CH2-CH]p [CH2-C]q-
COO-
COOH
N
H
-[HN-CH-CO]p-
COOH
COOH
-[CH2-CH]p [CH2-C]q-
-[HN-CH-CO]p-
N
H
COON
Изоэлектрическая точка – значение рН, при котором заряд полиамфолита
равен нулю, так как количество отрицательных и положительных зарядов
на макромолекуле одинаково.
23.
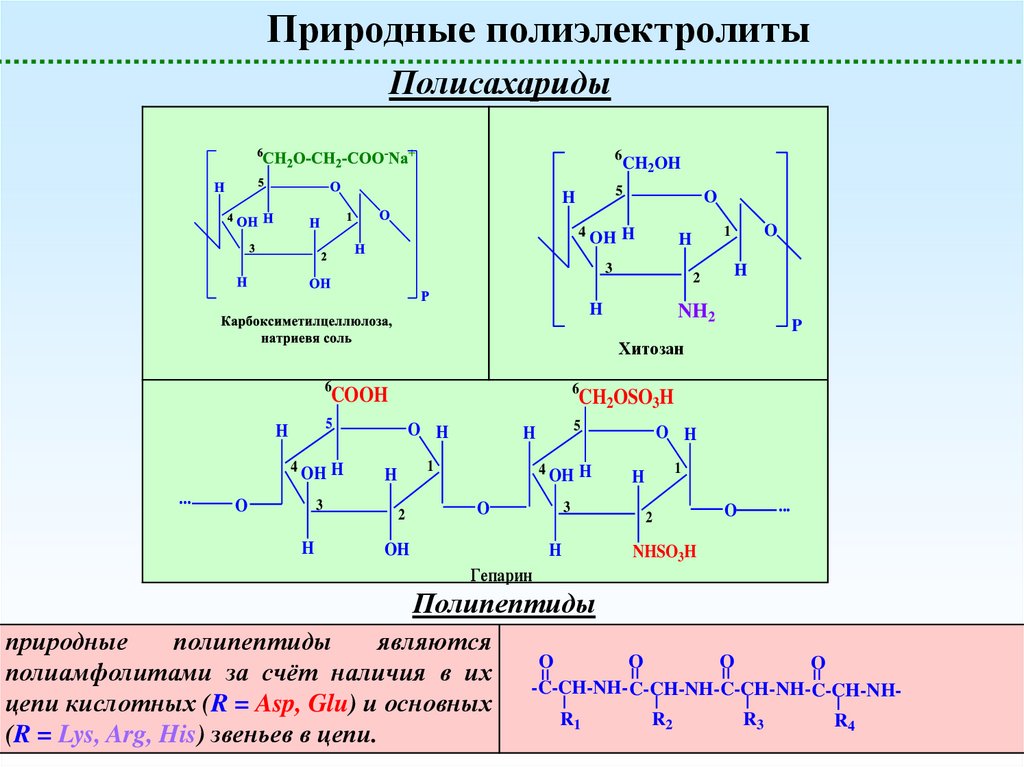
Природные полиэлектролитыПолисахариды
6
CH2OH
5
H
O
4 OH H
3
2
H
O
1
H
H
NH2
P
Хитозан
6
6
COOH
5
H
4 OH H
...
CH2OSO3H
O
3
H
O H
1
H
2
5
H
4 OH H
O
3
OH
H
O H
1
H
2
...
O
NHSO3H
Гепарин
Полипептиды
природные
полипептиды
являются
полиамфолитами за счёт наличия в их
цепи кислотных (R = Asp, Glu) и основных
(R = Lys, Arg, His) звеньев в цепи.
O
O
O
O
-C-CH-NH- C-CH-NH-C-CH-NH-C-CH-NHR1
R2
R3
R4
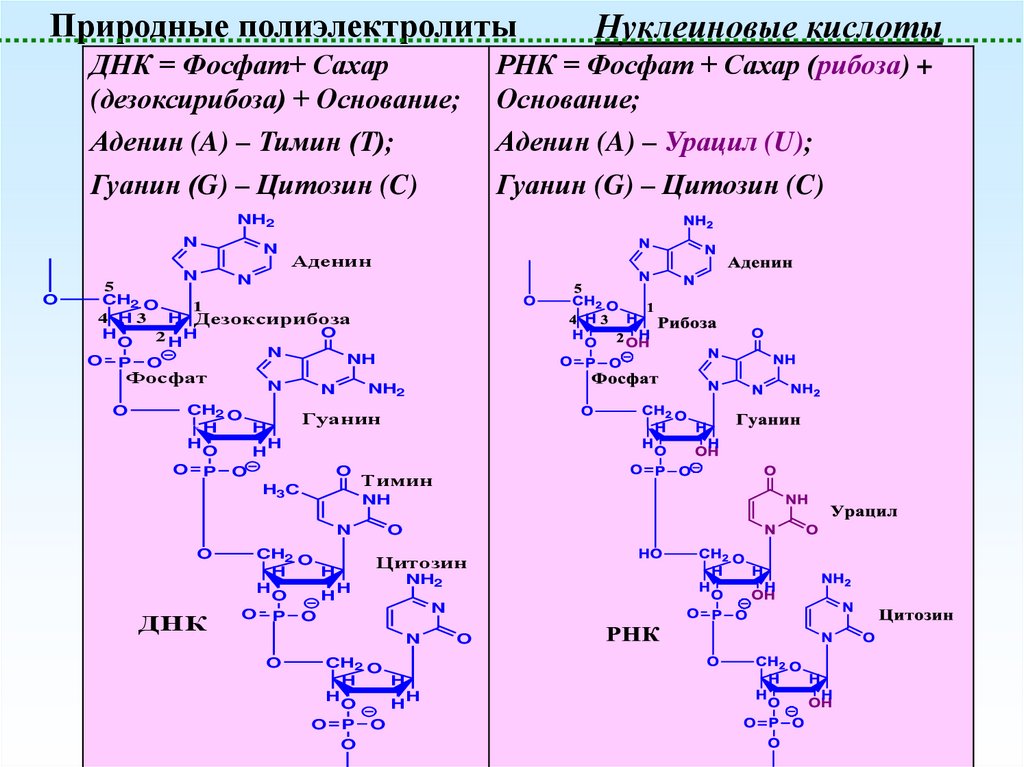
24.
Природные полиэлектролитыДНК = Фосфат+ Сахар
(дезоксирибоза) + Основание;
Аденин (A) – Тимин (T);
Гуанин (G) – Цитозин (C)
NH2
N
N
Аденин
N
O
N
5
CH2 O
1
H Дезоксирибоза
4 H3
O
H
2 HH
O
N
NH
O P O
Фосфат
O
N
NH2
N
CH2 O
Гуанин
H
H
H
H
O
H
O P O
O
Тимин
H3C
NH
N
O
ДНК
CH2 O
H
H
H
H
O
H
O P O
O
Цитозин
NH2
N
N
O
CH2 O
H
H
H
H
O
H
O P O
O
O
Нуклеиновые кислоты
РНК = Фосфат + Сахар (рибоза) +
Основание;
Аденин (A) – Урацил (U);
Гуанин (G) – Цитозин (C)
25.
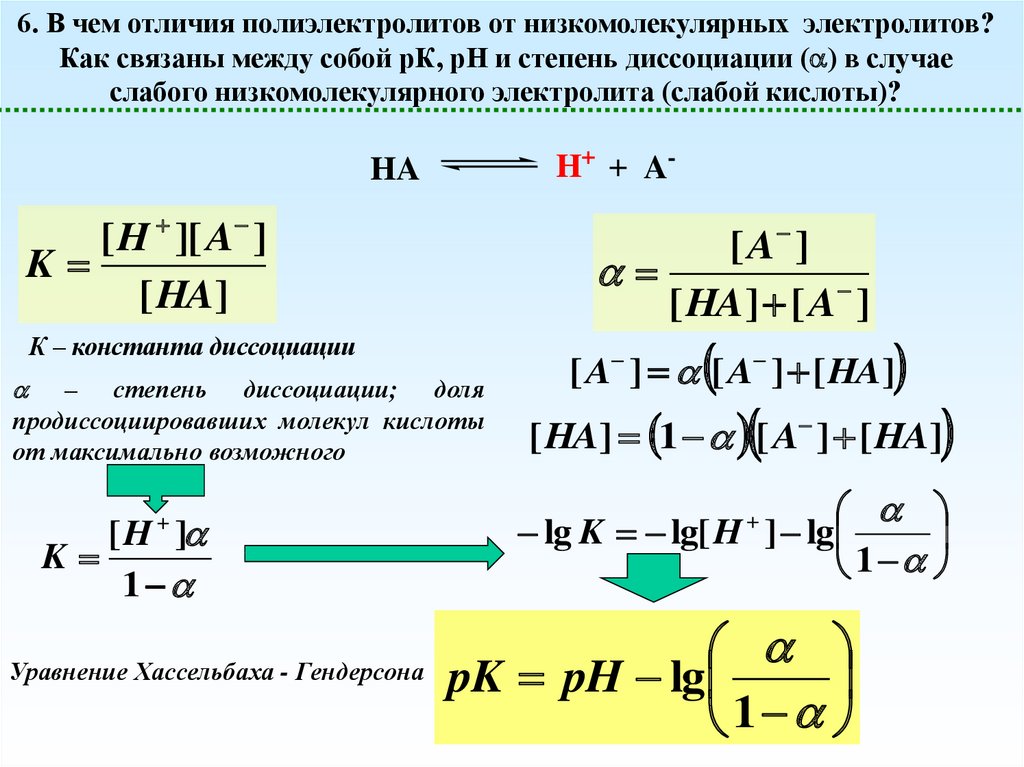
6. В чем отличия полиэлектролитов от низкомолекулярных электролитов?Как связаны между собой рК, рН и степень диссоциации ( ) в случае
слабого низкомолекулярного электролита (слабой кислоты)?
H+ + A-
HA
[ A ]
[ HA] [ A ]
[ H ][ A ]
K
[ HA]
К – константа диссоциации
– степень диссоциации; доля
продиссоциировавших молекул кислоты
от максимально возможного
[H ]
K
1
Уравнение Хассельбаха - Гендерсона
[ A ] [ A ] [ HA]
[ HA] 1 [ A ] [ HA]
lg K lg[ H ] lg
1
pK pH lg
1
26.
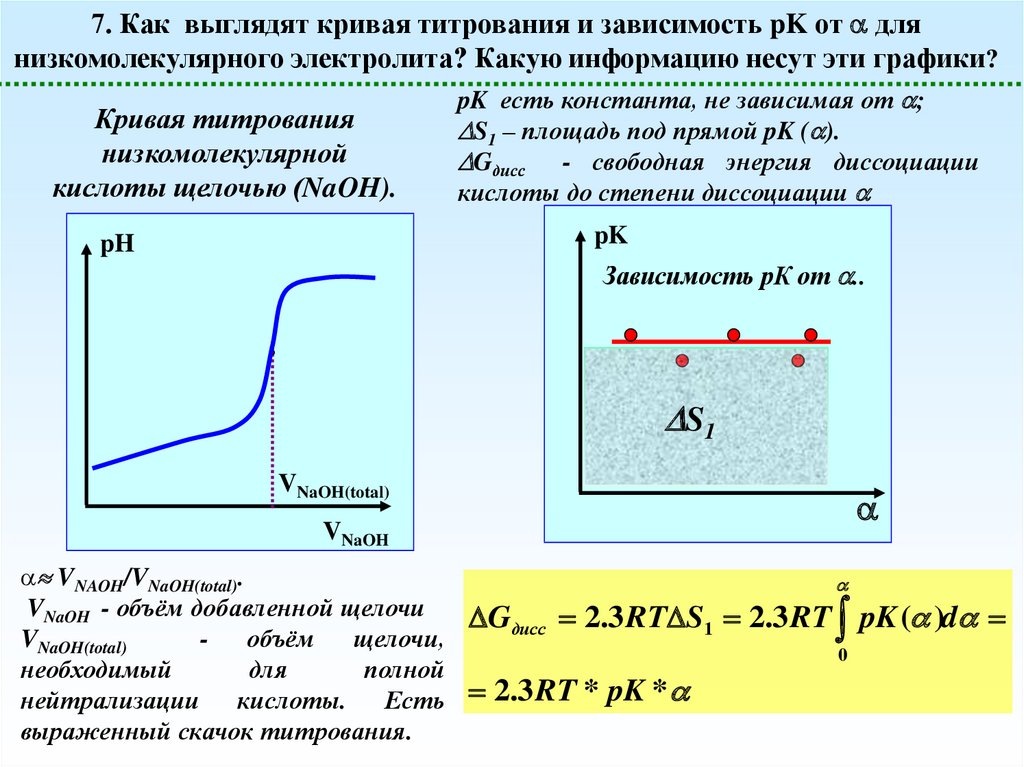
7. Как выглядят кривая титрования и зависимость pK от длянизкомолекулярного электролита? Какую информацию несут эти графики?
Кривая титрования
низкомолекулярной
кислоты щелочью (NaOH).
pK есть константа, не зависимая от ;
S1 – площадь под прямой pK ( ).
Gдисс - свободная энергия диссоциации
кислоты до степени диссоциации
pK
pH
Зависимость рК от ..
S1
VNaOH(total)
VNaOH
VNAOH/VNaOH(total).
VNaOH - объём добавленной щелочи
VNaOH(total)
объём щелочи,
необходимый
для
полной
нейтрализации кислоты. Есть
выраженный скачок титрования.
Gдисс 2.3 RT S1 2.3 RT pK ( )d
0
2.3 RT * pK *
27.
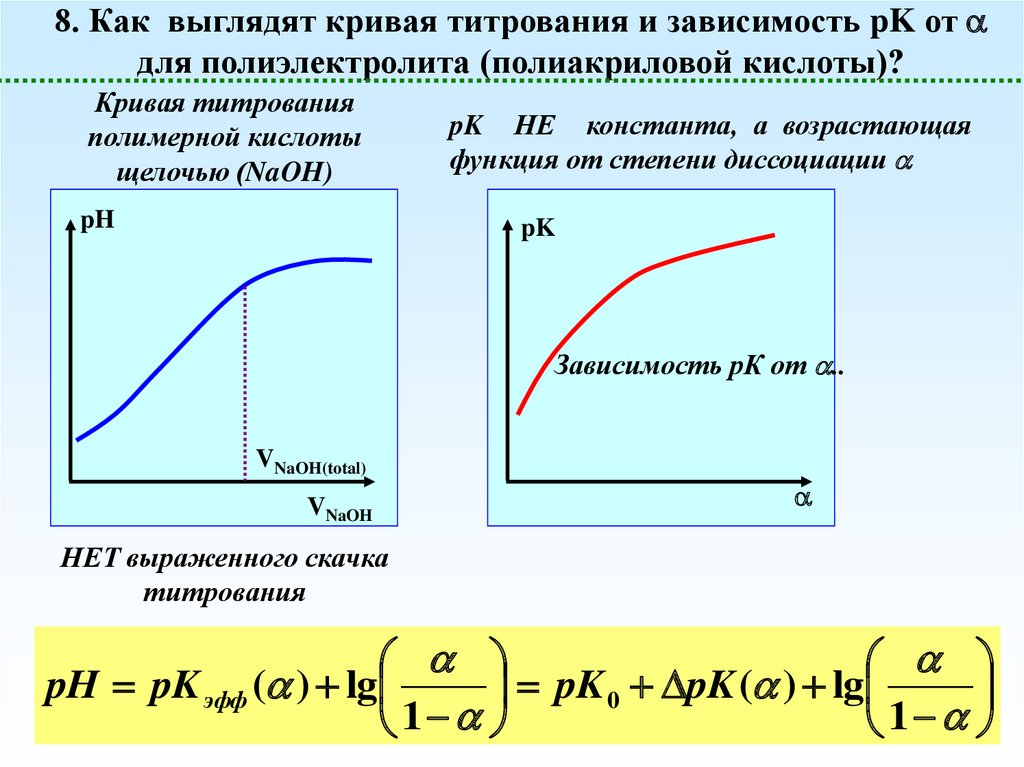
8. Как выглядят кривая титрования и зависимость pK отдля полиэлектролита (полиакриловой кислоты)?
Кривая титрования
полимерной кислоты
щелочью (NaOH)
pH
pK НЕ константа, а возрастающая
функция от степени диссоциации
pK
Зависимость рК от ..
VNaOH(total)
VNaOH
НЕТ выраженного скачка
титрования
pH pK эфф ( ) lg
pK 0 pK ( ) lg
1
1
28.
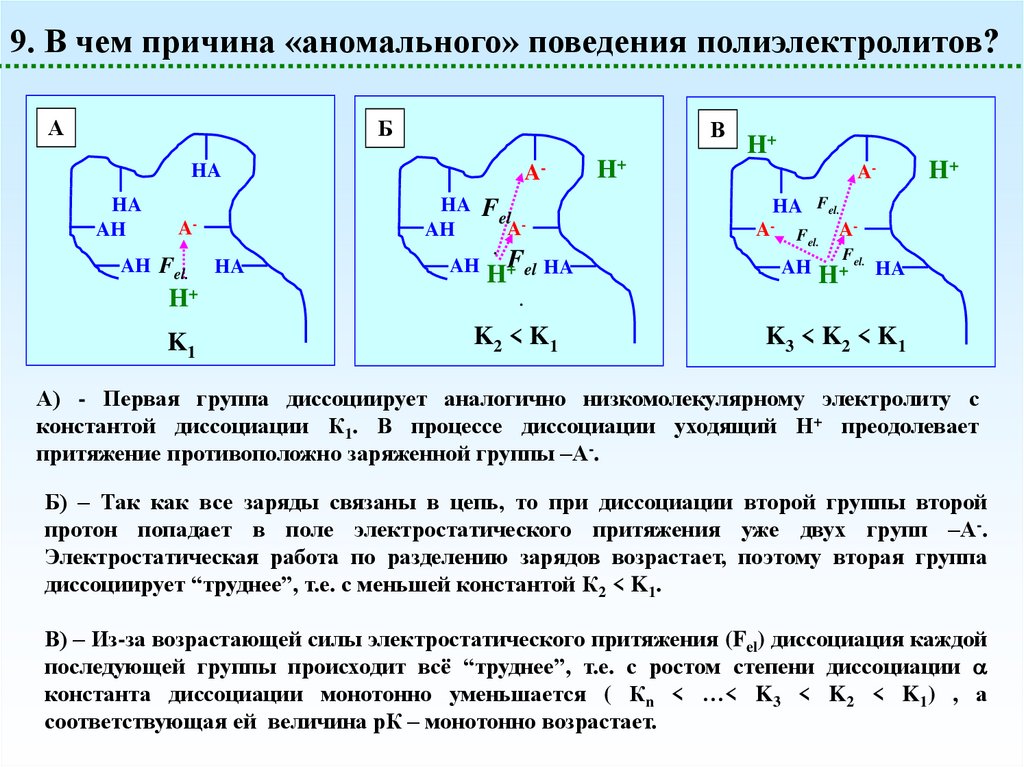
9. В чем причина «аномального» поведения полиэлектролитов?А
Б
В
A-
HA
HA
AH
HA
AH
A-
AH Fel.
H+
K1
Fel
A-
.
HA
AH
F
H+ el HA
H+
H+
A-
H+
HA Fel.
A- Fel. AAH
Fel.
+
H HA
.
K2 < K 1
K3 < K 2 < K 1
А) - Первая группа диссоциирует аналогично низкомолекулярному электролиту с
константой диссоциации К1. В процессе диссоциации уходящий Н+ преодолевает
притяжение противоположно заряженной группы –А-.
Б) – Так как все заряды связаны в цепь, то при диссоциации второй группы второй
протон попадает в поле электростатического притяжения уже двух групп –А-.
Электростатическая работа по разделению зарядов возрастает, поэтому вторая группа
диссоциирует “труднее”, т.е. с меньшей константой К2 < K1.
В) – Из-за возрастающей силы электростатического притяжения (Fel) диссоциация каждой
последующей группы происходит всё “труднее”, т.е. с ростом степени диссоциации
константа диссоциации монотонно уменьшается ( Кn < …< K3 < K2 < K1) , а
соответствующая ей величина рК – монотонно возрастает.
29.
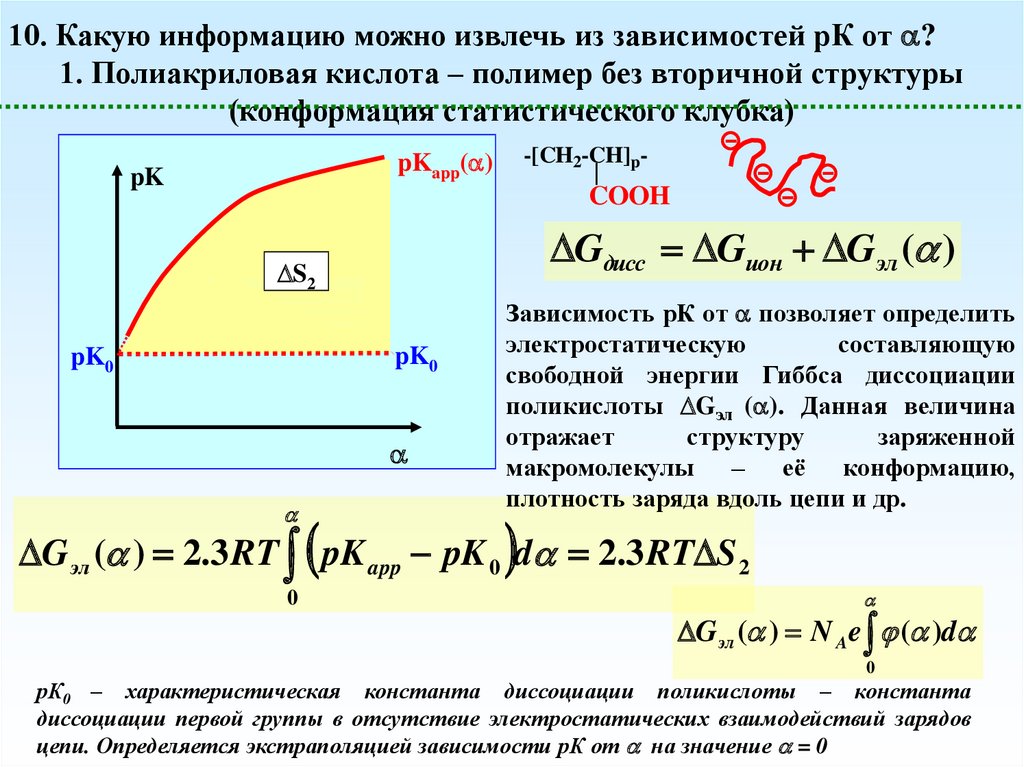
10. Какую информацию можно извлечь из зависимостей рК от ?1. Полиакриловая кислота – полимер без вторичной структуры
(конформация статистического клубка)
-[CH2-CH]p-
pKapp( )
pK
COOH
Gдисс Gион Gэл ( )
S2
pK0
pK0
Зависимость рК от позволяет определить
электростатическую
составляющую
свободной энергии Гиббса диссоциации
поликислоты Gэл ( ). Данная величина
отражает
структуру
заряженной
макромолекулы – её конформацию,
плотность заряда вдоль цепи и др.
G эл ( ) 2.3 RT pK app pK 0 d 2.3 RT S 2
0
G эл ( ) N Ae ( )d
0
рК0 – характеристическая константа диссоциации поликислоты – константа
диссоциации первой группы в отсутствие электростатических взаимодействий зарядов
цепи. Определяется экстраполяцией зависимости рК от на значение = 0
30.
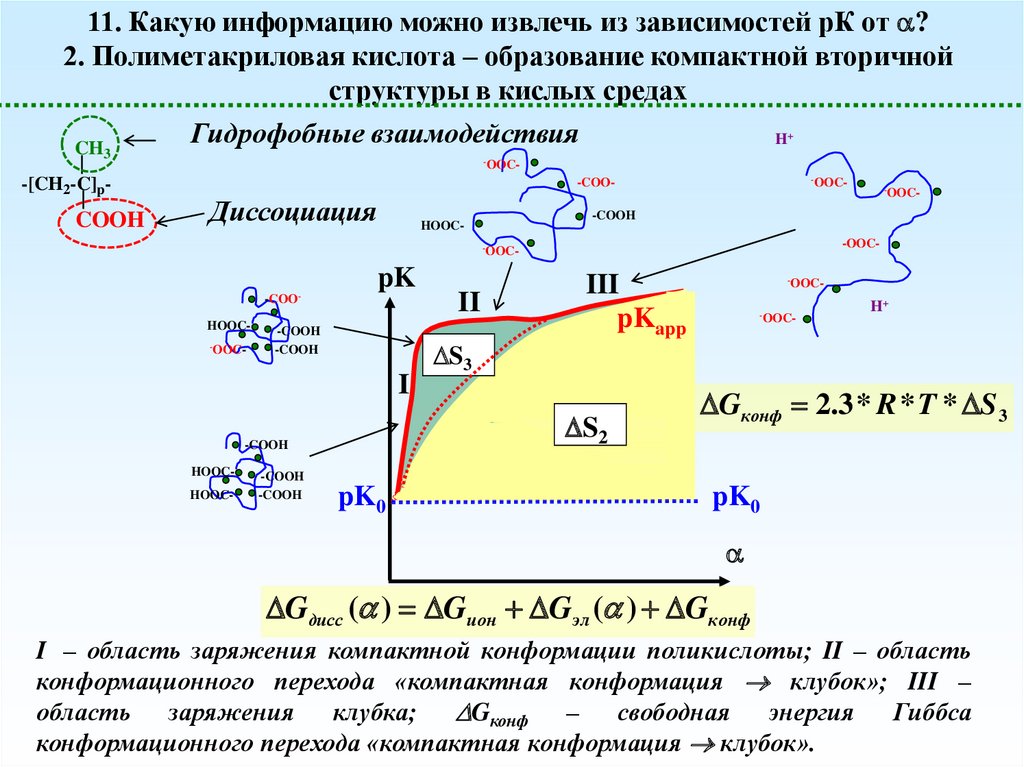
11. Какую информацию можно извлечь из зависимостей рК от ?2. Полиметакриловая кислота – образование компактной вторичной
структуры в кислых средах
CH3
-[CH2-C]p-
COOH
Гидрофобные взаимодействия
H+
-OOC-OOC-
-COO-
Диссоциация
-COOH
HOOC-
-OOC-
-OOC-
pK
-COOHOOC-OOC-
-COOH
-COOH
I
HOOC-
-COOH
-COOH
S3
III
pKapp
S2
-COOH
HOOC-
II
pK0
-OOC-
-OOC-
-OOC-
H+
Gконф 2.3 * R * T * S 3
pK0
Gдисс ( ) Gион Gэл ( ) Gконф
I – область заряжения компактной конформации поликислоты; II – область
конформационного перехода «компактная конформация клубок»; III –
область заряжения клубка; Gконф – свободная энергия Гиббса
конформационного перехода «компактная конформация клубок».
31.
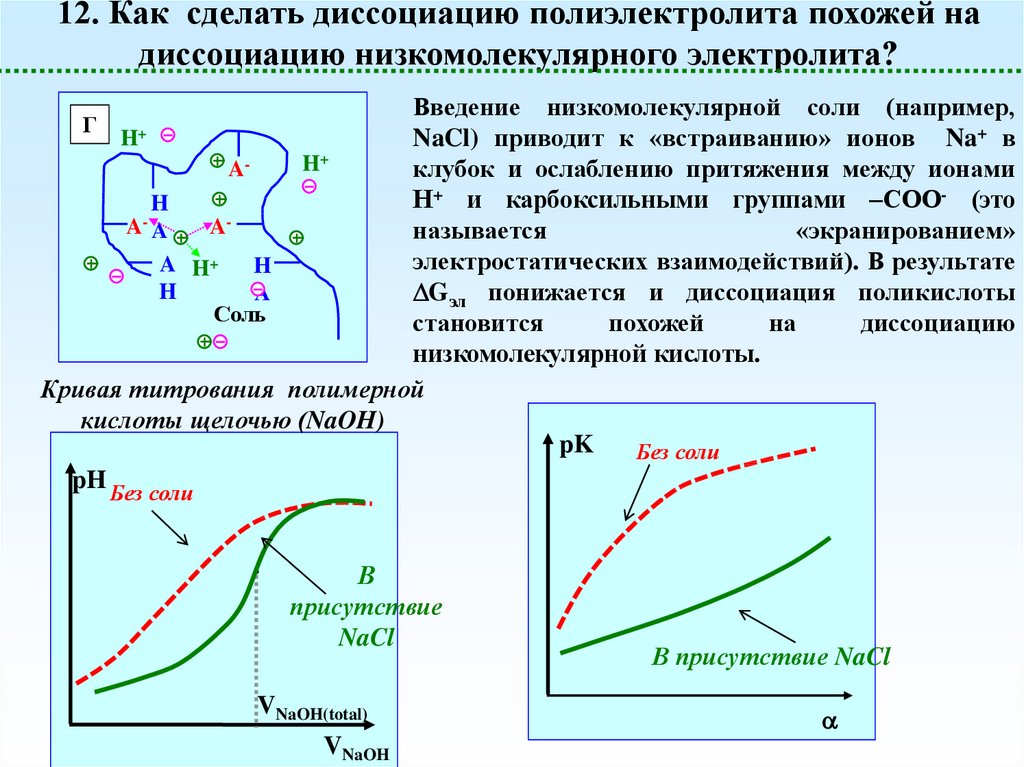
12. Как сделать диссоциацию полиэлектролита похожей надиссоциацию низкомолекулярного электролита?
Введение низкомолекулярной соли (например,
H+
NaCl) приводит к «встраиванию» ионов Na+ в
H+
Aклубок и ослаблению притяжения между ионами
Н+ и карбоксильными группами –СОО- (это
H
A- A
Aназывается
«экранированием»
электростатических взаимодействий). В результате
A H+
H
H
A
Gэл понижается и диссоциация поликислоты
Соль
становится
похожей
на
диссоциацию
низкомолекулярной кислоты.
Кривая титрования полимерной
кислоты щелочью (NaOH)
pK
Без соли
pH Без соли
Г
В
присутствие
NaCl
VNaOH(total)
VNaOH
В присутствие NaCl
32.
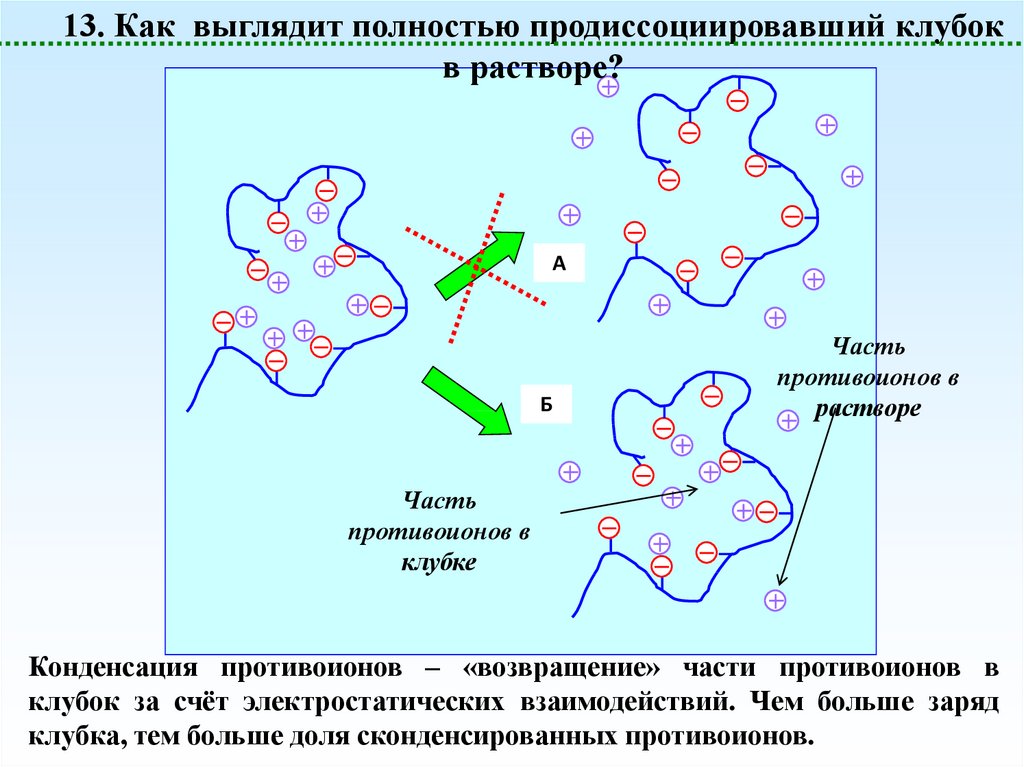
13. Как выглядит полностью продиссоциировавший клубокв растворе?
A
Б
Часть
противоионов в
растворе
Часть
противоионов в
клубке
Конденсация противоионов – «возвращение» части противоионов в
клубок за счёт электростатических взаимодействий. Чем больше заряд
клубка, тем больше доля сконденсированных противоионов.
33.
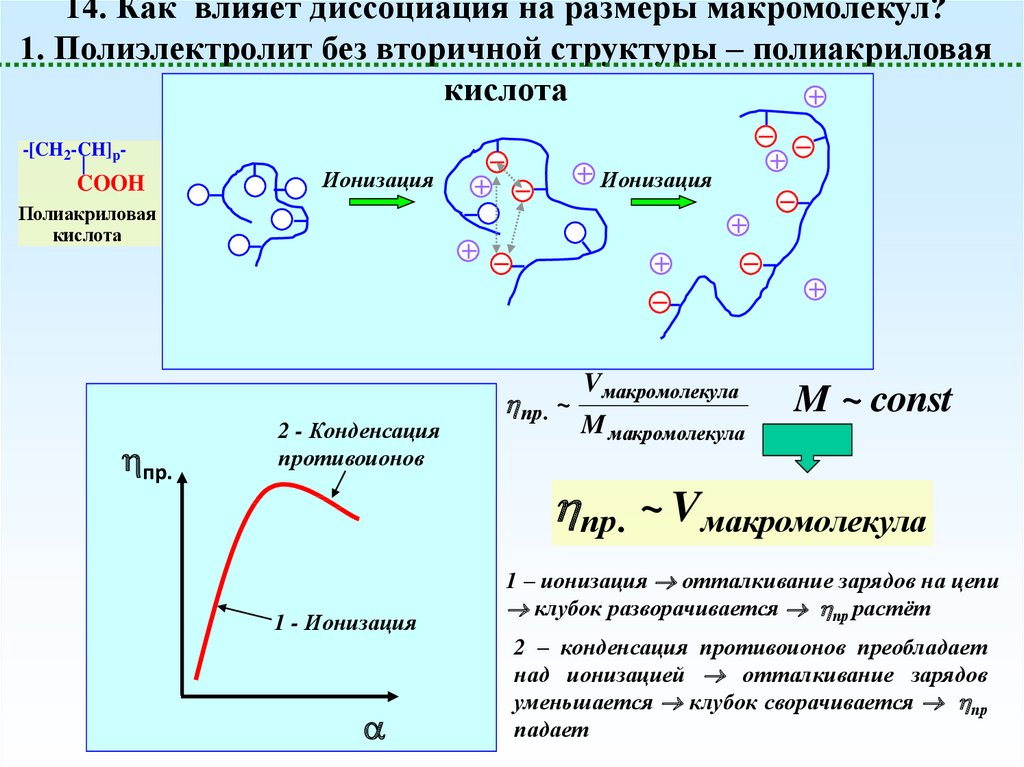
14. Как влияет диссоциация на размеры макромолекул?1. Полиэлектролит без вторичной структуры – полиакриловая
кислота
-[CH2-CH]p-
COOH
Ионизация
Ионизация
Полиакриловая
кислота
пр.
2 - Конденсация
противоионов
пр. ~
Vмакромолекула
M макромолекула
M ~ const
пр. ~ Vмакромолекула
1 - Ионизация
1 – ионизация отталкивание зарядов на цепи
клубок разворачивается пр растёт
2 – конденсация противоионов преобладает
над ионизацией отталкивание зарядов
уменьшается клубок сворачивается пр
падает
34.
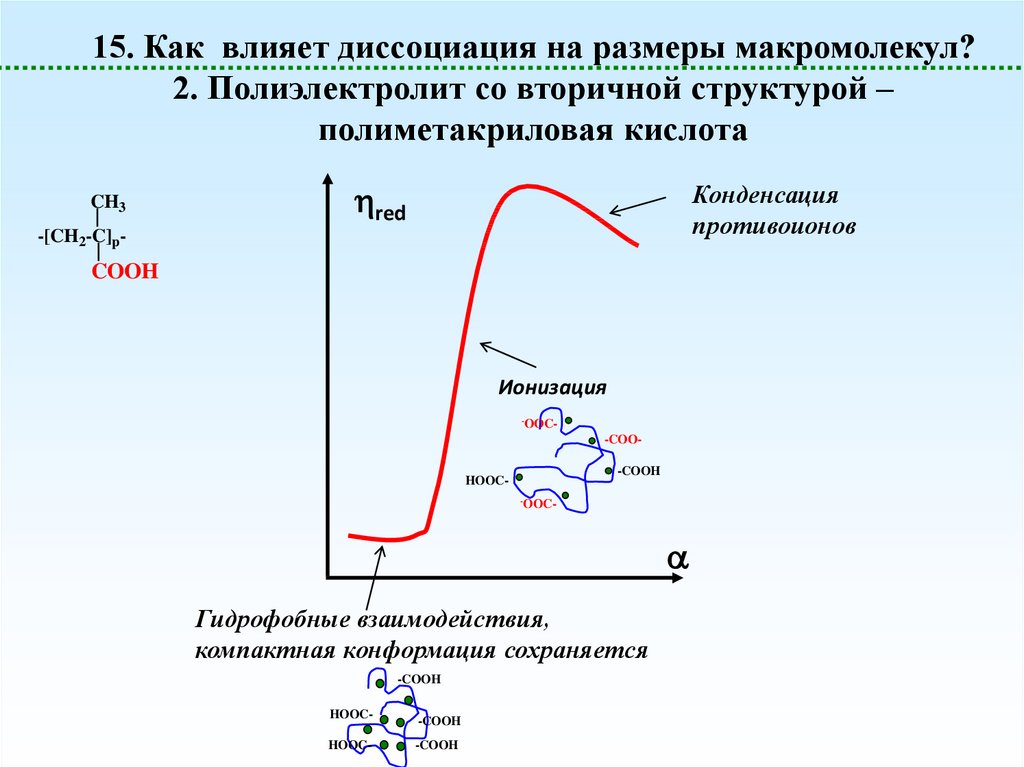
15. Как влияет диссоциация на размеры макромолекул?2. Полиэлектролит со вторичной структурой –
полиметакриловая кислота
CH3
red
Конденсация
противоионов
-[CH2-C]p-
COOH
Ионизация
-OOC-
-COO-COOH
HOOC-OOC-
Гидрофобные взаимодействия,
компактная конформация сохраняется
-COOH
HOOCHOOC-
-COOH
-COOH
35.
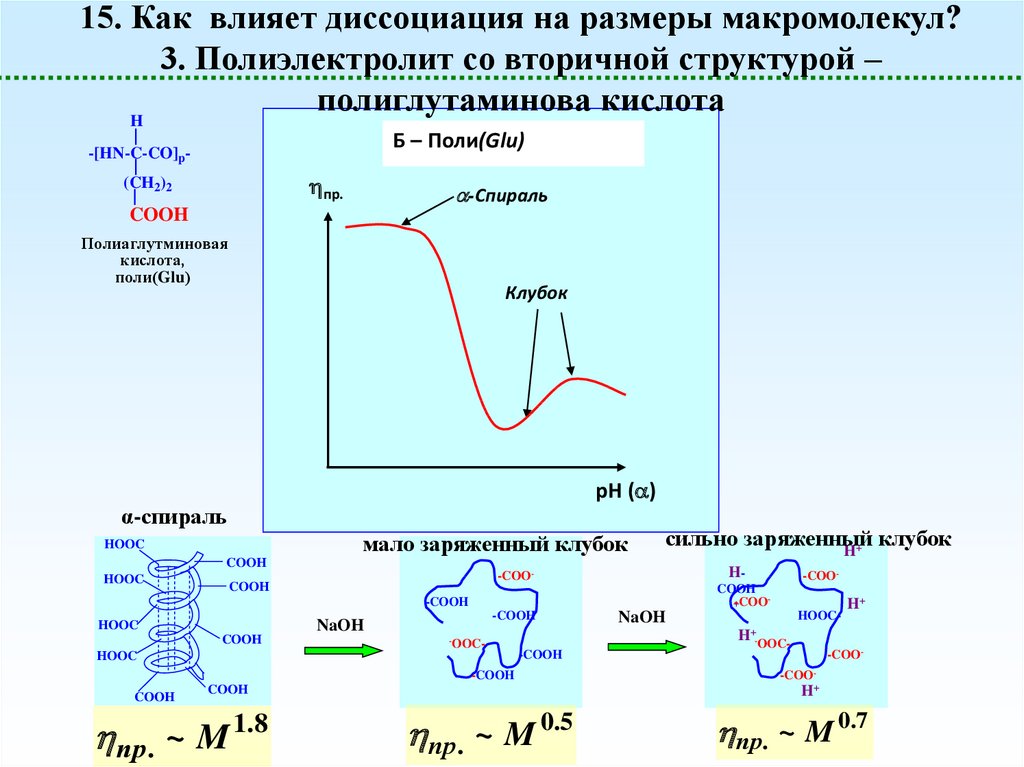
15. Как влияет диссоциация на размеры макромолекул?3. Полиэлектролит со вторичной структурой –
полиглутаминова кислота
H
Б – Поли(Glu)
-[HN-C-CO]p-
пр.
(CH2)2
-Спираль
COOH
Полиаглутминовая
кислота,
поли(Glu)
Клубок
рН ( )
α-спираль
мало заряженный клубок
HOOC
COOH
HOOC
сильно заряженный
клубок
H+
HCOOH
-COO+
-COO-
COOH
-COOH
-COOH
NaOH
HOOC
COOH
-OOC-
HOOC
-COOH
-COOH
COOH
пр . ~ M
NaOH
HOOC-
H+-OOC-
H+
-COO-
-COO-
H+
COOH
1 .8
-COO-
пр. ~ M 0.5
пр. ~ M 0.7
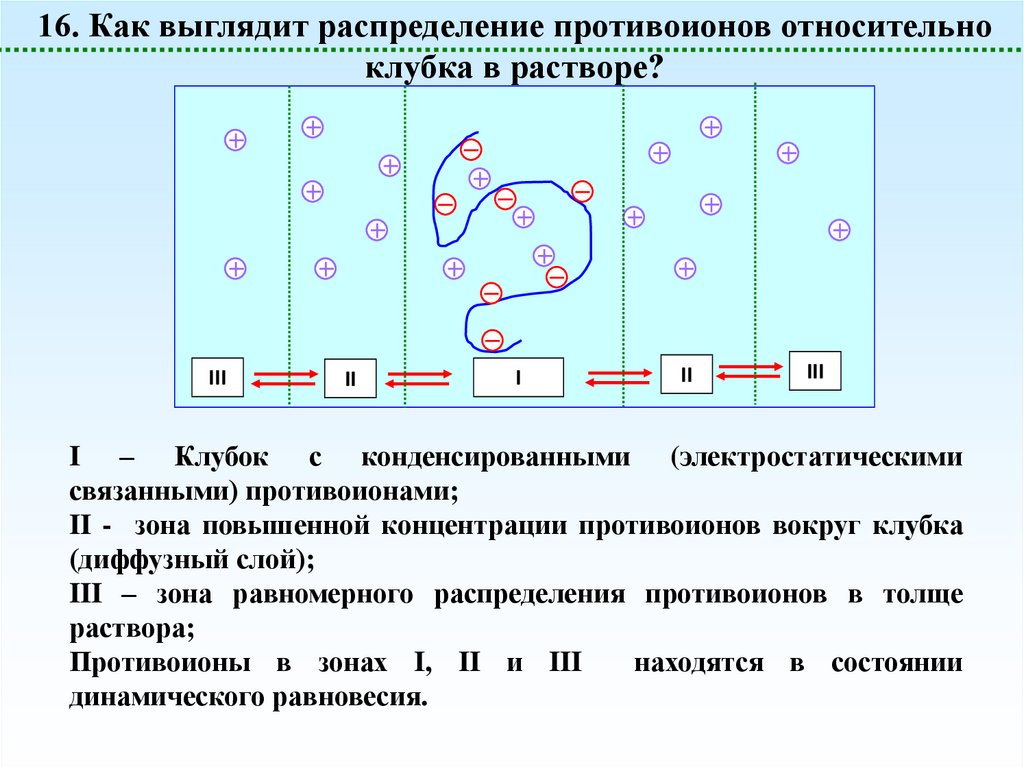
36.
16. Как выглядит распределение противоионов относительноклубка в растворе?
III
II
I
II
III
I – Клубок с конденсированными (электростатическими
связанными) противоионами;
II - зона повышенной концентрации противоионов вокруг клубка
(диффузный слой);
III – зона равномерного распределения противоионов в толще
раствора;
Противоионы в зонах I, II и III
находятся в состоянии
динамического равновесия.
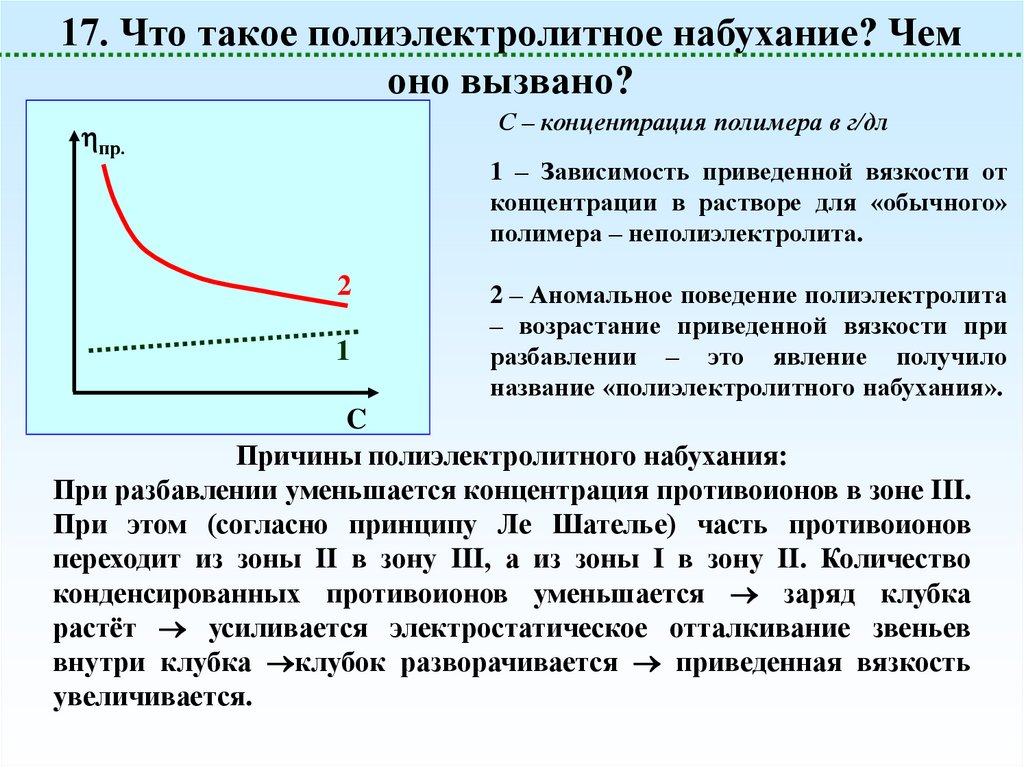
37.
17. Что такое полиэлектролитное набухание? Чемоно вызвано?
С – концентрация полимера в г/дл
пр.
1 – Зависимость приведенной вязкости от
концентрации в растворе для «обычного»
полимера – неполиэлектролита.
2
1
2 – Аномальное поведение полиэлектролита
– возрастание приведенной вязкости при
разбавлении – это явление получило
название «полиэлектролитного набухания».
C
Причины полиэлектролитного набухания:
При разбавлении уменьшается концентрация противоионов в зоне III.
При этом (согласно принципу Ле Шателье) часть противоионов
переходит из зоны II в зону III, а из зоны I в зону II. Количество
конденсированных противоионов уменьшается заряд клубка
растёт усиливается электростатическое отталкивание звеньев
внутри клубка клубок разворачивается приведенная вязкость
увеличивается.
38.
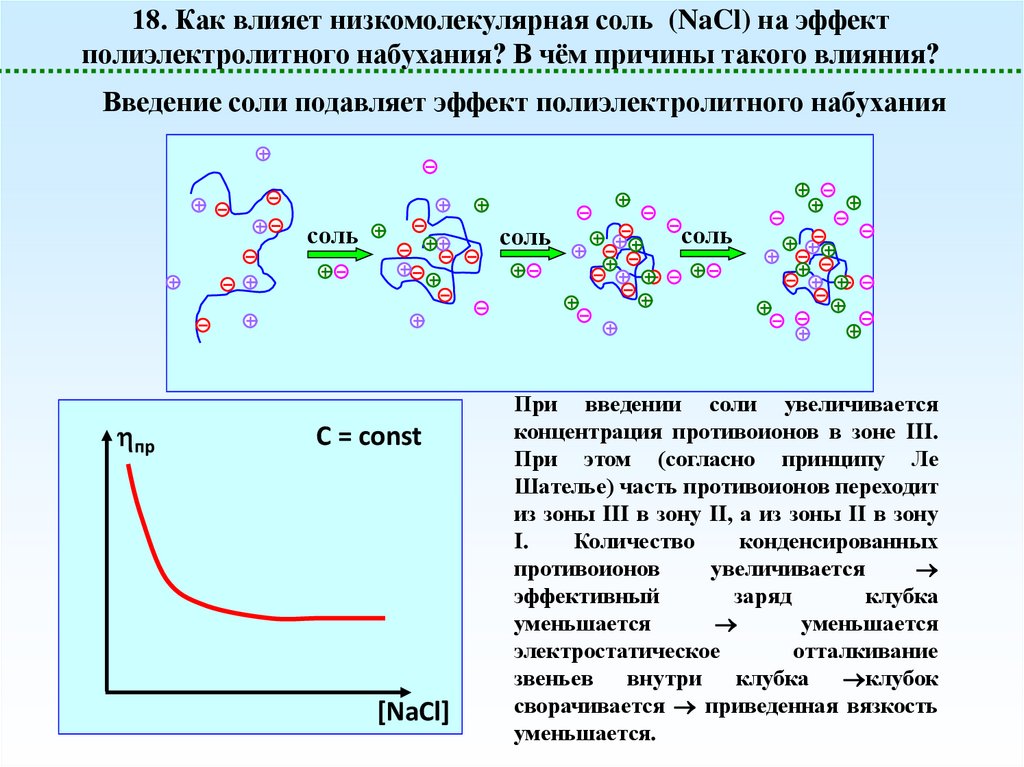
18. Как влияет низкомолекулярная соль (NaCl) на эффектполиэлектролитного набухания? В чём причины такого влияния?
Введение соли подавляет эффект полиэлектролитного набухания
соль
пр
соль
C = const
[NaCl]
соль
При введении соли увеличивается
концентрация противоионов в зоне III.
При этом (согласно принципу Ле
Шателье) часть противоионов переходит
из зоны III в зону II, а из зоны II в зону
I.
Количество
конденсированных
противоионов
увеличивается
эффективный
заряд
клубка
уменьшается
уменьшается
электростатическое
отталкивание
звеньев внутри
клубка
клубок
сворачивается приведенная вязкость
уменьшается.
39.
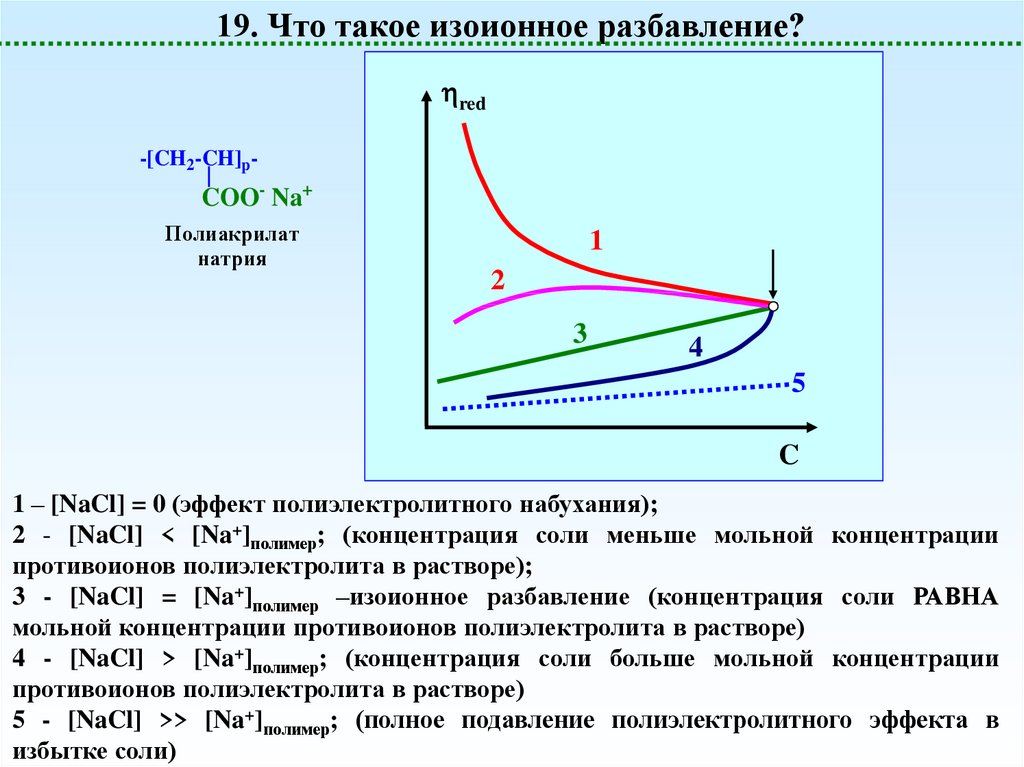
19. Что такое изоионное разбавление?red
-[CH2-CH]p-
COO- Na+
Полиакрилат
натрия
1
2
3
4
5
C
1 – [NaCl] = 0 (эффект полиэлектролитного набухания);
2 - [NaCl] < [Na+]полимер; (концентрация соли меньше мольной концентрации
противоионов полиэлектролита в растворе);
3 - [NaCl] = [Na+]полимер –изоионное разбавление (концентрация соли РАВНА
мольной концентрации противоионов полиэлектролита в растворе)
4 - [NaCl] > [Na+]полимер; (концентрация соли больше мольной концентрации
противоионов полиэлектролита в растворе)
5 - [NaCl] >> [Na+]полимер; (полное подавление полиэлектролитного эффекта в
избытке соли)
40.
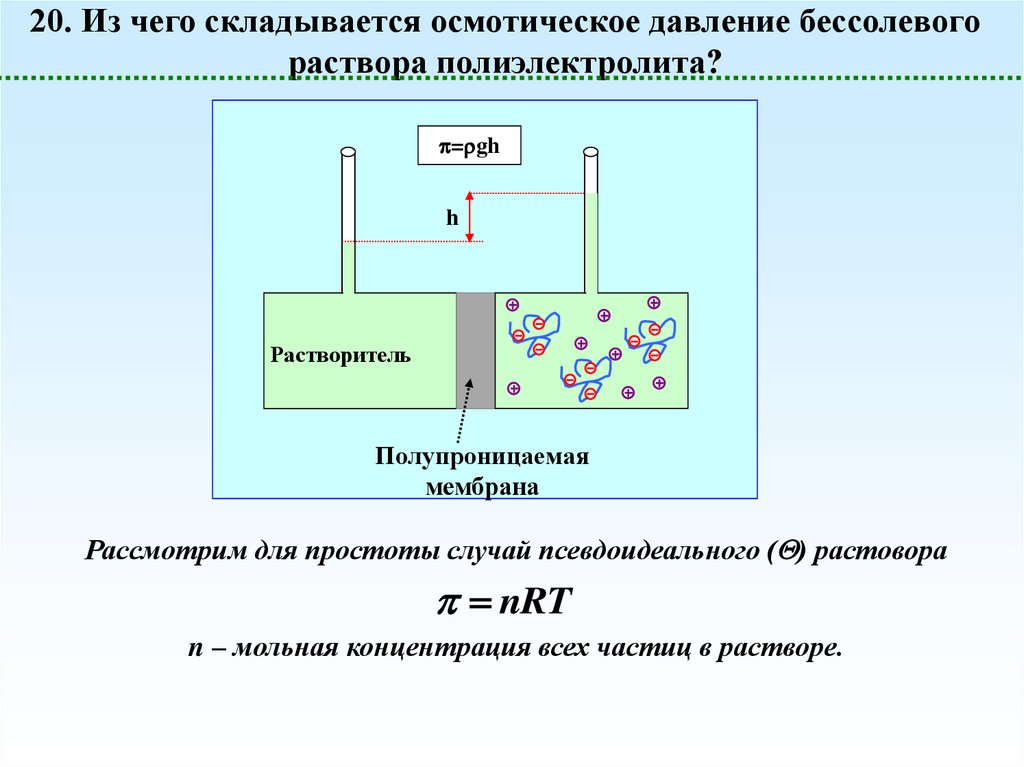
20. Из чего складывается осмотическое давление бессолевогораствора полиэлектролита?
= gh
h
Растворитель
Полупроницаемая
мембрана
Рассмотрим для простоты случай псевдоидеального ( ) растовора
nRT
n – мольная концентрация всех частиц в растворе.
41.
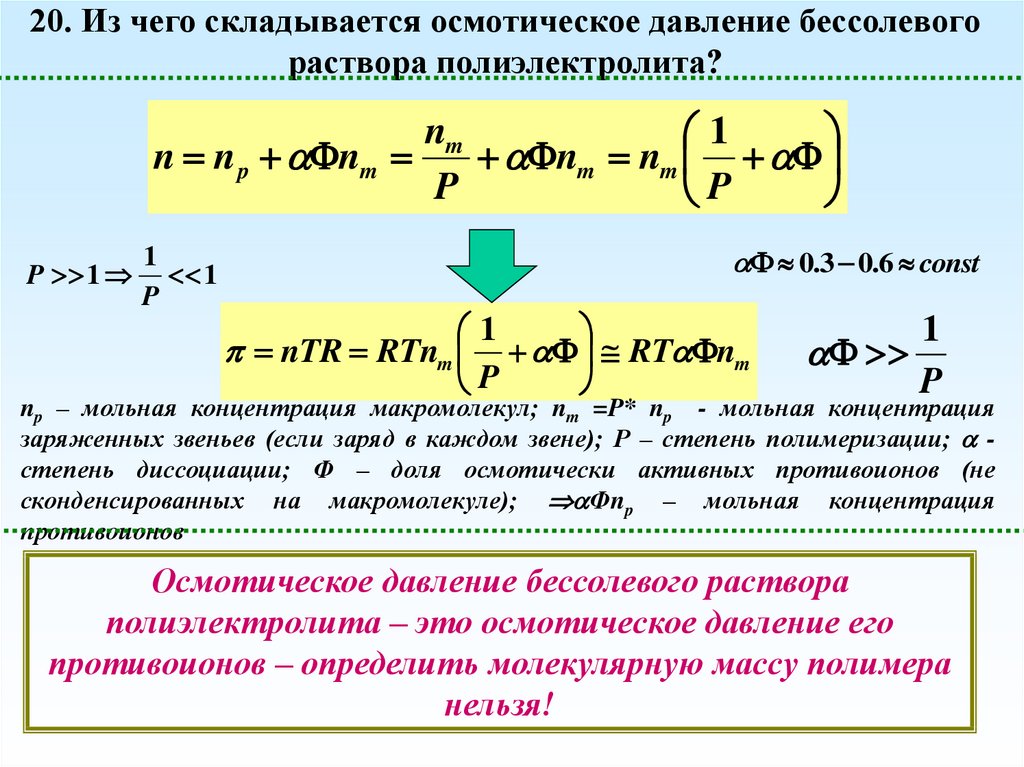
20. Из чего складывается осмотическое давление бессолевогораствора полиэлектролита?
nm
1
n n p nm
nm nm
P
P
P 1
1
1
P
0.3 0.6 const
1
nTR RTnm RT nm
P
1
P
np – мольная концентрация макромолекул; nm =P* np - мольная концентрация
заряженных звеньев (если заряд в каждом звене); Р – степень полимеризации; степень диссоциации; Ф – доля осмотически активных противоионов (не
сконденсированных на макромолекуле); Фnp – мольная концентрация
противоионов
Осмотическое давление бессолевого раствора
полиэлектролита – это осмотическое давление его
противоионов – определить молекулярную массу полимера
нельзя!
42.
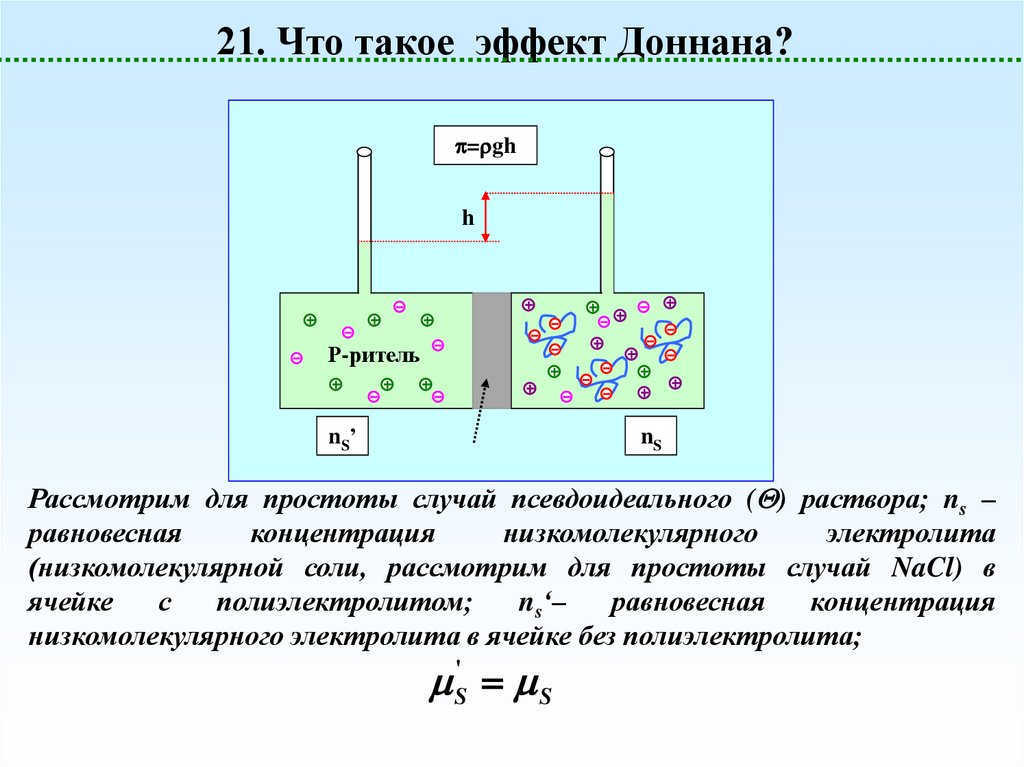
21. Что такое эффект Доннана?= gh
h
Р-ритель
nS’
nS
Рассмотрим для простоты случай псевдоидеального ( ) раствора; ns –
равновесная
концентрация
низкомолекулярного
электролита
(низкомолекулярной соли, рассмотрим для простоты случай NaCl) в
ячейке
с
полиэлектролитом;
ns‘–
равновесная
концентрация
низкомолекулярного электролита в ячейке без полиэлектролита;
S' S
43.
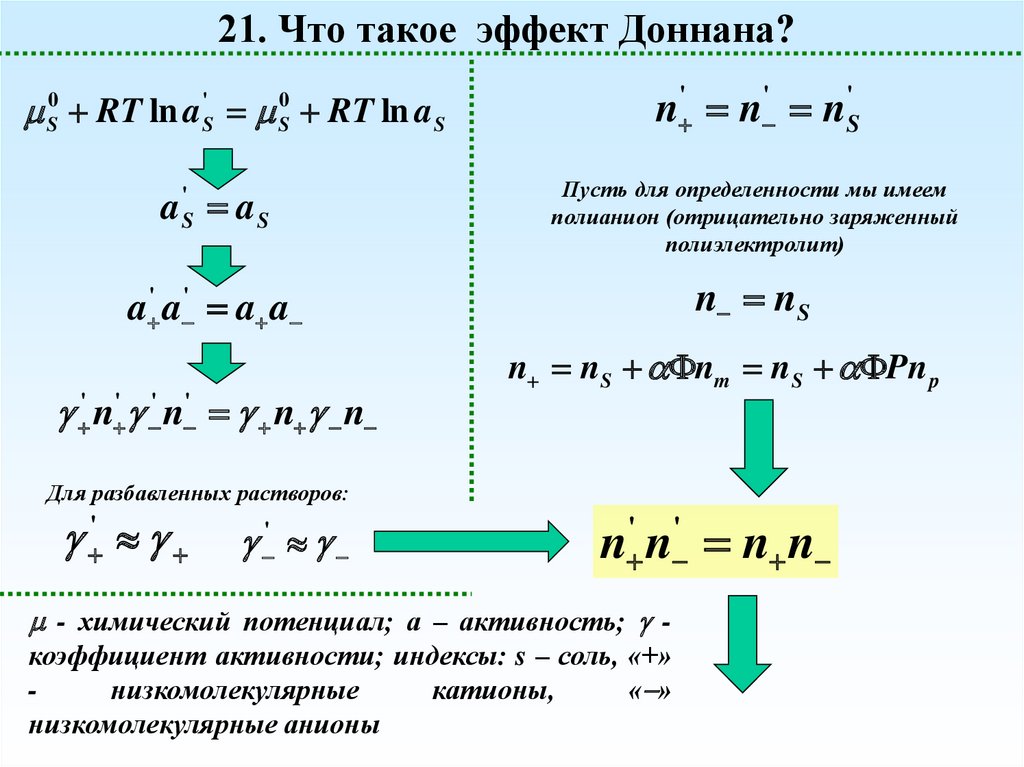
21. Что такое эффект Доннана?S0 RT ln a 'S S0 RT ln a S
n ' n ' n'S
a aS
Пусть для определенности мы имеем
полианион (отрицательно заряженный
полиэлектролит)
a ' a ' a a
n nS
'
S
' n ' ' n ' n n
n nS nm nS Pn p
Для разбавленных растворов:
'
'
n ' n ' n n
- химический потенциал; а – активность; коэффициент активности; индексы: s – соль, «+»
низкомолекулярные
катионы,
« »
низкомолекулярные анионы
44.
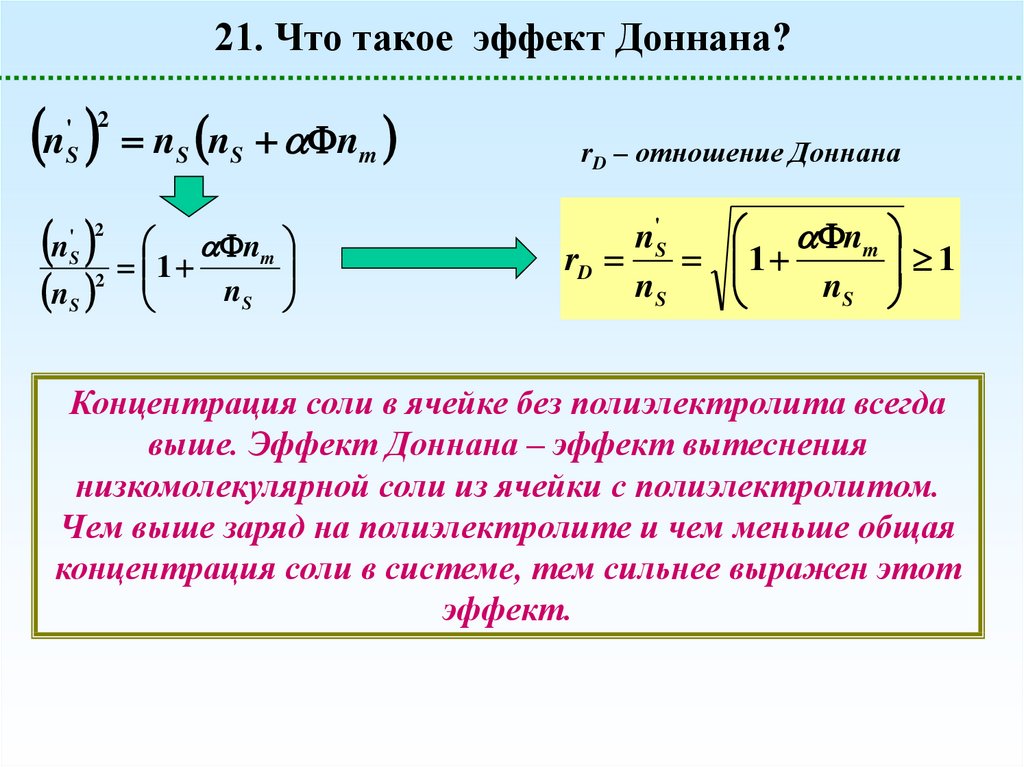
21. Что такое эффект Доннана?n
' 2
S
n
' 2
S
2
S
n
nS nS nm
nm
1
nS
rD – отношение Доннана
nm
n'S
1
rD
1
nS
nS
Концентрация соли в ячейке без полиэлектролита всегда
выше. Эффект Доннана – эффект вытеснения
низкомолекулярной соли из ячейки с полиэлектролитом.
Чем выше заряд на полиэлектролите и чем меньше общая
концентрация соли в системе, тем сильнее выражен этот
эффект.
45.
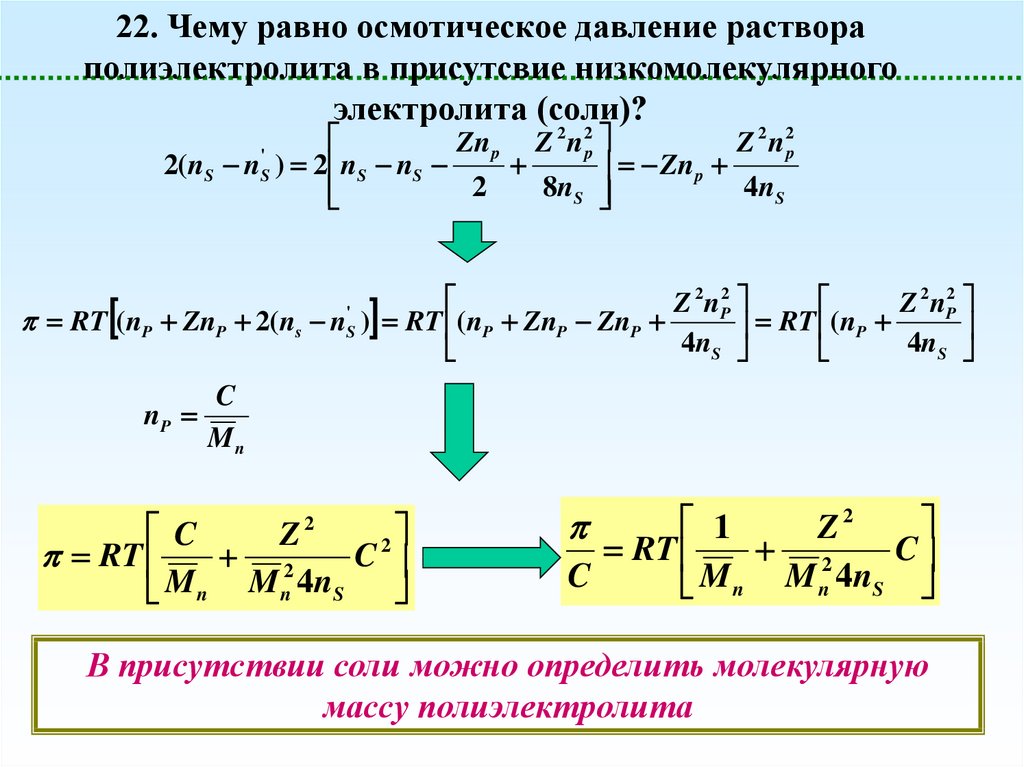
22. Чему равно осмотическое давление раствора полиэлектролита вприсутсвие низкомолекулярного электролита (соли)?
Для простоты опять примем, что в отсутствие диссоциации раствор был бы псевдоидеальным
RT ( nP nm 2( ns n'S )
nm Pn p Zn p
Z = РФ – заряд макромолекулы
RT ( nP ZnP 2( ns n'S )
1
2
Zn p
Zn p Z n
n
1
1
nS
nS
2 ns
8nS2
'
S
n nS
'
S
2
Zn p
2
Z 2 n2p
8n S
2
p
1 x
1
2
x x2
1
2 8
Zn p
nS
x 1
1
Считаем, что добавили избыток соли
46.
22. Чему равно осмотическое давление раствораполиэлектролита в присутсвие низкомолекулярного
электролита (соли)?
2 2
2 2
Zn
Z
n
Z
np
p
p
'
2( nS nS ) 2 nS nS
Zn p
2
8nS
4n S
Z 2 nP2
Z 2 nP2
RT (nP ZnP 2(ns n ) RT (nP ZnP ZnP
RT ( nP
4
n
4
n
S
S
'
S
nP
C
Mn
C
Z
2
RT
2
C
M n M n 4nS
2
1
Z2
RT
2
C
C
M n M n 4nS
В присутствии соли можно определить молекулярную
массу полиэлектролита
47.
23. Чему равен второй вириальный коэффициентполиэлектролита?
2
2
1 Z
A2
0
2
4nS M n 4nS
Z
плотность заряда макромолек улы
Mn
Для полиэлектролитов А2 > 0; Чем больше плотность
заряда на макромолекуле и чем ниже концентрация
низкомолекулярного электролита, тем выше значение
второго вириального коэффициента
48.
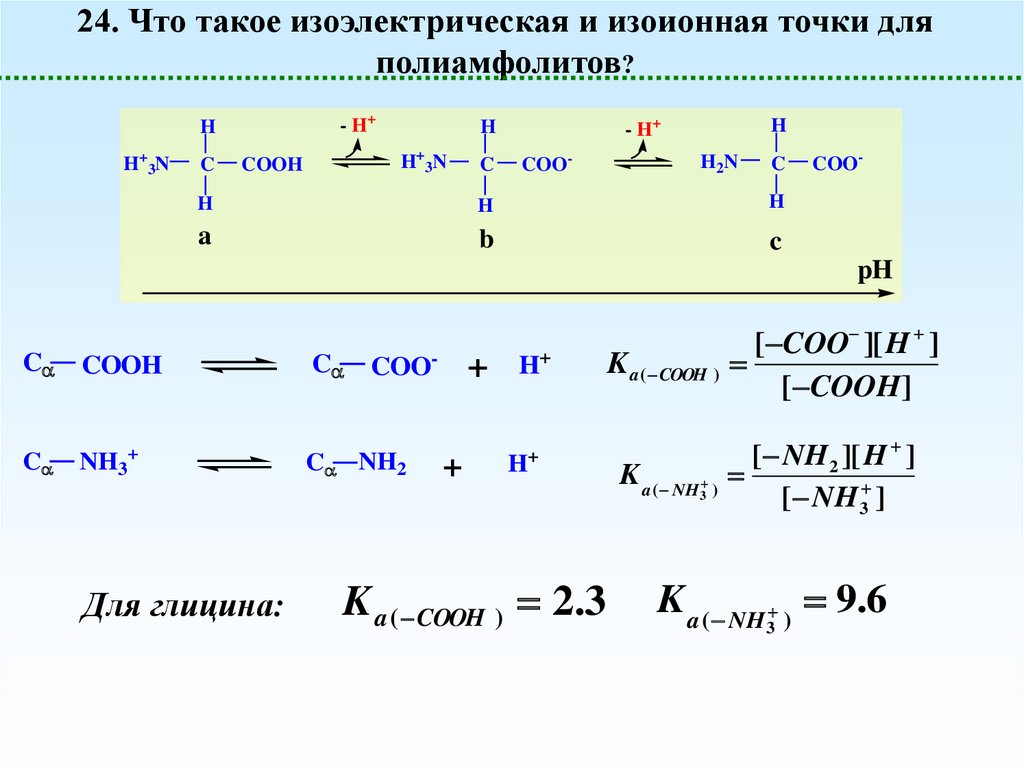
24. Что такое изоэлектрическая и изоионная точки дляполиамфолитов?
- H+
H
H+3N
C
H+3N
COOH
- H+
H
C
COO-
H
H2N
C
H
H
H
a
b
c
COO-
pH
COO-
C
COOH
C
C
NH3+
C NH2
+
+
H+
H+
K a ( COOH )
K a ( NH )
3
Для глицина:
K a ( COOH ) 2.3
[ COO ][ H ]
[ COOH]
[ NH 2 ][ H ]
[ NH 3 ]
K a ( NH ) 9.6
3
49.
24. Что такое изоэлектрическая и изоионная точки дляполиамфолитов?
Изоэлектрическая точка (pI, ИЭТ) – значение рН раствора,
при котором суммарный заряд амфолита равен нулю.
Для простого амфолита с двумя диссоциирующими группами:
pI
pK a ( COOH ) pK a ( NH )
3
2
Для глицина: pI 2.3 9.6 5.95
2
H
H
H + 3N
C
H
COO-
H2 N
C
COOH
H
ИЭТ – константа для данного полиамфолита,
определяемая значениями констант диссоциации
индивидуальных групп
50.
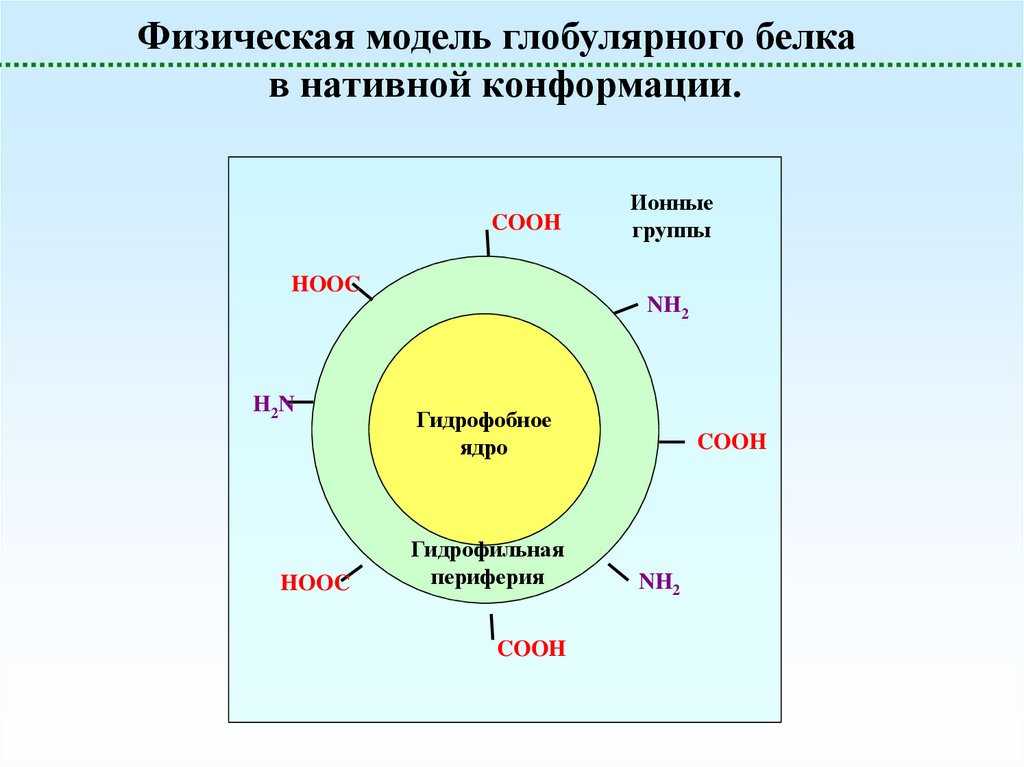
Физическая модель глобулярного белкав нативной конформации.
COOH
Ионные
группы
HOOC
NH2
H2N
HOOC
Гидрофобное
ядро
Гидрофильная
периферия
COOH
COOH
NH2
51.
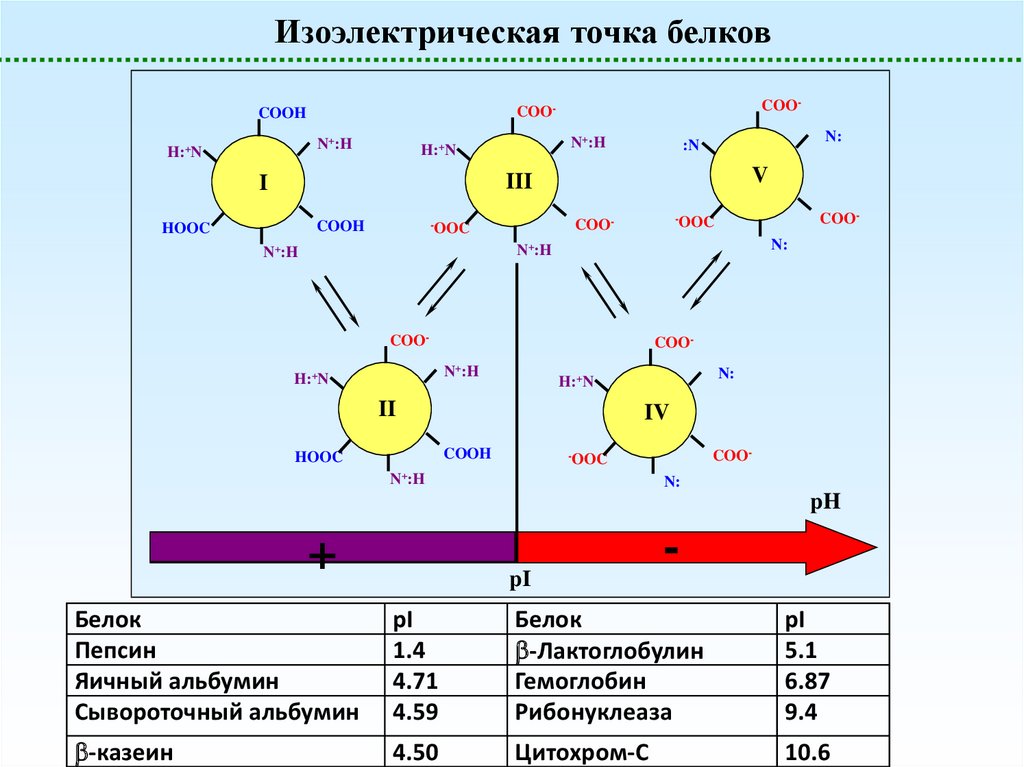
Изоэлектрическая точка белковN+:H
H:+N
COO-
COO-
COOH
N+:H
H:+N
N:
:N
V
III
I
COOH
HOOC
COO-
-OOC
COO-
-OOC
N:
N+:H
N+:H
COO-
COON+:H
H:+N
II
IV
COOH
HOOC
N:
H:+N
COO-
-OOC
N+:H
N:
pH
+
pI
-
Белок
Пепсин
Яичный альбумин
Сывороточный альбумин
pI
1.4
4.71
4.59
Белок
-Лактоглобулин
Гемоглобин
Рибонуклеаза
pI
5.1
6.87
9.4
-казеин
4.50
Цитохром-C
10.6
52.
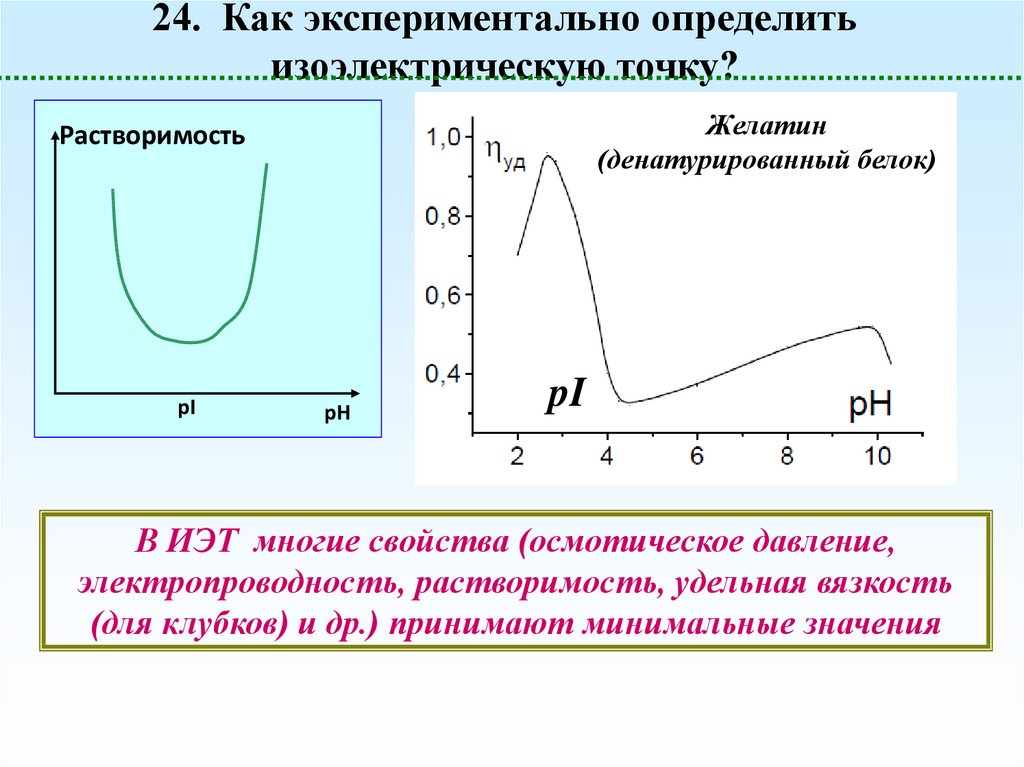
24. Как экспериментально определитьизоэлектрическую точку?
Желатин
(денатурированный белок)
Растворимость
pI
pH
pI
В ИЭТ многие свойства (осмотическое давление,
электропроводность, растворимость, удельная вязкость
(для клубков) и др.) принимают минимальные значения
53.
24. Что такое изоионная точка? Как она связана сизоэлектрической точкой?
Изоионная точка (pS, ИИТ) – собственное значение рН
раствора полиамфолита.
Для бессолевого раствора полиамфолита справедливо
уравнение электронейтральности:
Znp [ H ] [OH ] 0
[OH ] [ H ]
Z
np
1. Если ИИТ лежит в щелочной области, то ИЭТ лежит
правее, если ИИТ лежит в кислой области, то ИЭТ лежит
левее на шкале рН. Если ИИТ = 7, то и ИЭТ = 7.
2. Если концентрация полиамфолита не очень мала и ИИТ
лежит не в очень кислой или щелочной области, то ИИТ ИЭТ
54.
24. Как влияет избирательное связывание малыхионов с полиамфолитом на положение ИИТ и ИЭТ?
a) –
нет избирательности
Na+, K+, Cl- , HPO42- и др.
pS pI
б)
– избирательное связывание
pI
катионов pS
в) – избирательное связывание
анионов pI
pS
pH
Mg2+, Ca2+, Fe3+ и др.
pH
I-, SO42-, PO43- и др.
pH
55.
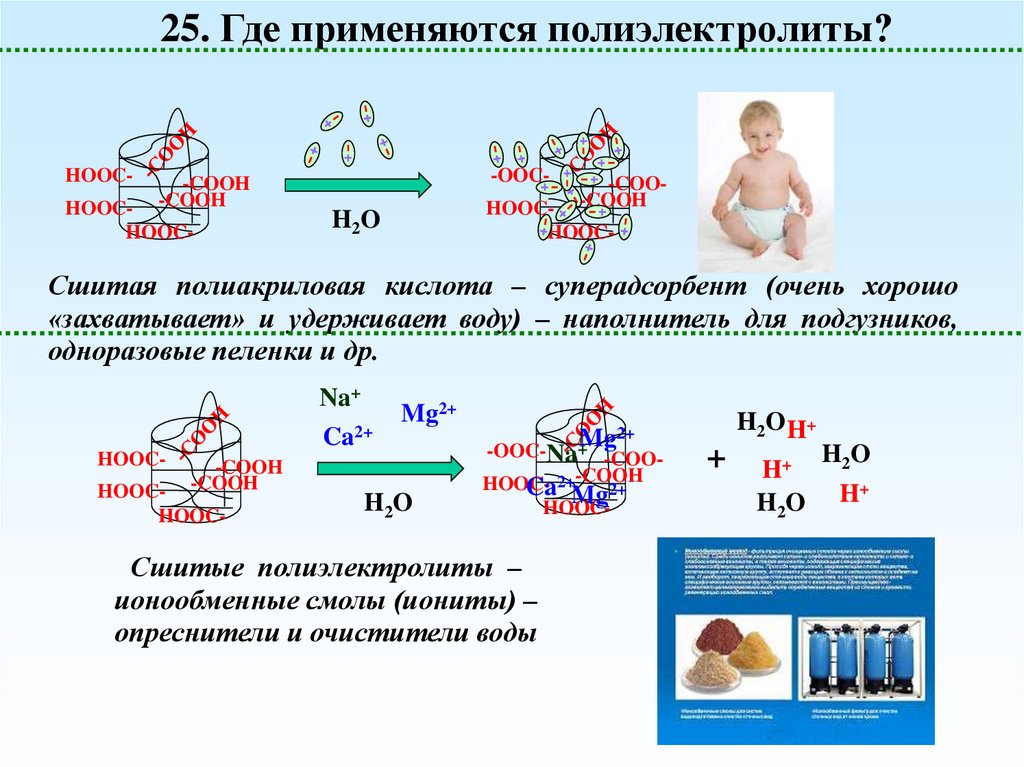
25. Где применяются полиэлектролиты?HOOC-
-COOH
-COOH
HOOCHOOC-
-OOC-
-COO-COOH
HOOCHOOC-
H2O
Сшитая полиакриловая кислота – суперадсорбент (очень хорошо
«захватывает» и удерживает воду) – наполнитель для подгузников,
одноразовые пеленки и др.
Na+
Ca2+
HOOC-
-COOH
-COOH
HOOCHOOC-
Mg2+
H2O
2+
+Mg
-OOC-Na -COOHOOC- 2+-COOH
Ca Mg2+
HOOC-
Сшитые полиэлектролиты –
ионообменные смолы (иониты) –
опреснители и очистители воды
H2O H+
+
H+
H2O
H2O
H+
56.
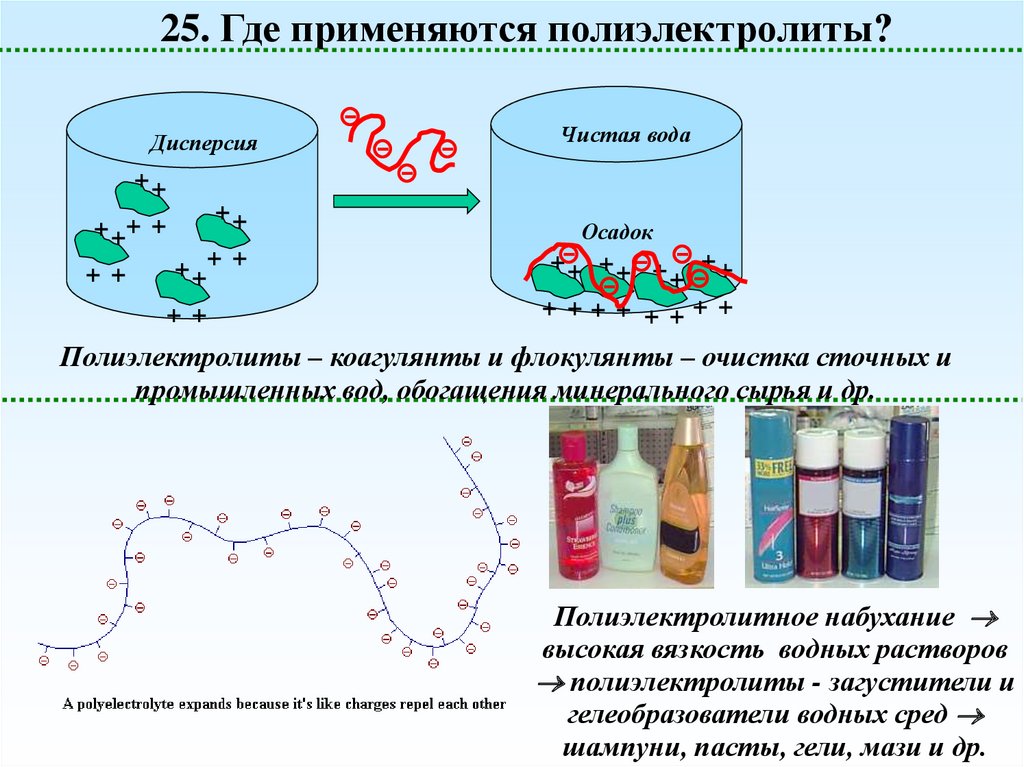
25. Где применяются полиэлектролиты?Дисперсия
Чистая вода
++
+ ++ +
+ +
++
+ ++ +
+ +
Осадок
++ ++ + ++
+
+ ++ + + ++ +
Полиэлектролиты – коагулянты и флокулянты – очистка сточных и
промышленных вод, обогащения минерального сырья и др.
Полиэлектролитное набухание
высокая вязкость водных растворов
полиэлектролиты - загустители и
гелеобразователи водных сред
шампуни, пасты, гели, мази и др.








 chemistry
chemistry