Similar presentations:
рН уровень в исследовании кислотно-щелочных свойств бытовых веществ
1.
«рН уровень в исследованиикислотно-щелочных свойств
бытовых веществ»
ИИП по предмету- химия
Мишарина Мария 8г класс *СОШ Усть-Кулом*
Руководитель: Карманова В.И.
2025г.
2.
Введение:• Химия-это наука, с которой человек ближе всего взаимодействует
в быту. Кислоты и щёлочи окружают нас в повседневной жизни: в
пище, средствах гигиены, бытовой химии. Кроме того,
ежедневно, сам того не подозревая, каждый человек
осуществляет элементарные химические реакции: мытьё рук
мылом, стирка вещей средствами для стирки, добавление
овощей и зажарки в суп для насыщенности цвета и вкуса и т.п.
Знание свойств кислот и щелочей помогает их правильно
использовать.
3.
Актуальность:• Изучение кислотности важно в быту, науке и экологии.
• Натуральные индикаторы-безопасная и доступная альтернатива
химическим аналогам при изучении химических реакций в
домашней и школьной практике.
4.
Цель:• Определить кислотность или щёлочность различных бытовых
веществ с помощью самодельного индикатора: в нашем случае
индикатором будет настой из листьев чая Каркадэ.
5.
Задачи:• Изготовить индикатор из природного сырья( листья чая Каркадэ).
• Провести эксперименты с образцами: мыло, лимонный сок, сода,
молоко.
• Сравнить результаты с эталонной шкалой рН.
• Сделать соответствующие выводы .
6.
Немного истории появления шкалы рН:• История рН шкалы началась в начале
ХХ века благодаря работе датского химика
Сёрена Сёрнсена (1868-1939),который
в 1909 году ввел понятие рН во время
исследований в Карлсбергской лаборато рии пивоваренного завода,
где Сёрнсен изучал влияние кислотности
на ферменты и процессы брожения- ключевые для производства пива. Он предложил логарифмическую шкалу для упрощения
расчётов- шкалу рН.
7.
Теоретическая часть:• Две латинские буквы рН означают pondus Hidrogenii- водородный
показатель (дословно-вес водорода) среды или показатель
кислотности.
• Водородный показатель зависит от концентрации ионов
водорода в растворе. Раствор с повышенной концентрацией
ионов называется кислотным, а раствор с пониженной
концентрацией этих ионов- щелочным.
• Значение рН изменяются от 1 до 14.Чем меньше число, тем более
кислотным является данный раствор.
• Известно, что выделяют три типа среды раствора: кислая,
нейтральная и щелочная.
8.
Вспомним, что такое кислота и щёлочь:• Кислота- это химическое соединение обычно кислого вкуса,
содержащее водород и кислотный остаток, способный
замещаться металлом при образовании соли.
Кислоты в быту: щавелевая, борная, соляная, уксусная и
лимонная, серная.
• Щёлочь- это растворимые в воде сильные основания, имеющие
горький вкус. Они нейтрализуют кислоту с получением воды и
соли.
Щёлочь в быту: аммиак( нашатырный спирт), каустическая сода,
известь, силикат калия.
9.
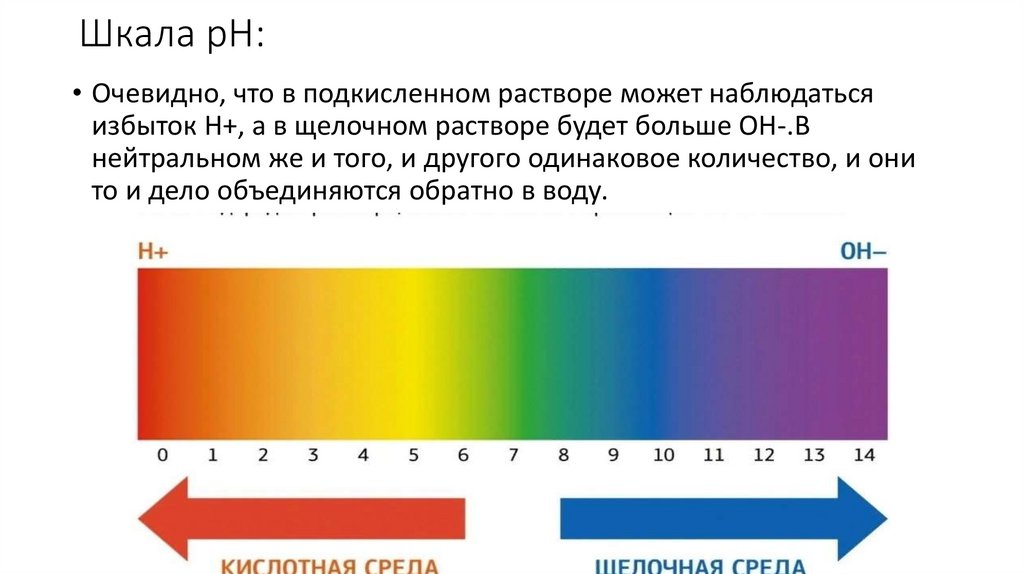
Шкала рН:• Очевидно, что в подкисленном растворе может наблюдаться
избыток Н+, а в щелочном растворе будет больше ОН-.В
нейтральном же и того, и другого одинаковое количество, и они
то и дело объединяются обратно в воду.
10.
Практическая часть:• Настой каркадэ содержит антоцианы,
которые меняют цвет в зависимости
от рН среды.
• МАТЕРИАЛЫ И ОБОРУДОВАНИЕ:
- Сухой каркадэ ,вода.
- Прозрачные стаканы, пипетки.
- Бытовые средства: уксус, сода,
мыльный раствор, лимонный сок,
стиральный порошок(раствор).
- Перчатки и очки.
11.
Экспериментальная часть:1.Приготовление индикатора
• Заварить 2-3 пакетика каркадэ
• в 100 мл . кипятка.
* Остудить и процедить настой.
2.Тестирование на бытовых средствах
• В прозрачные стаканы налить по 50 мл.
раствора каждого средства.
• Добавить 5-10 капель настоя каркадэ.
• Наблюдать и записать изменение цвета.
12.
Раствор № 1:• Раствор лимонной кислоты. Цвет после добавления индикатора
розовый. Предполагаемый рН -2,кислый.
13.
Раствор №2:Раствор соды. Цвет после добавления каркадэ – фиолетовый.
Предполагаемый рН 9-10,щелочной.
14.
Раствор №3• Мыльный раствор . Цвет после добавления индикатора
фиолетовый. Предполагаемый рН 11-12,щелочной.
15.
Раствор №4• Уксусный раствор. Цвет после добавления каркадэ ярко-розовый.
Предполагаемый рН 1,кислый.
16.
Результаты и анализ:• Мы измерили рН бытовых веществ.
• Результаты исследования показали, что мои средства прошли
проверку. Эксперимент показал, что натуральный индикатор
эффективен для определения рН. Однако, точность ниже, чем у
химических аналогов.
• Таким образом знание о кислотно-щелочном балансе помогает
понимать, как различные индикаторы влияют на среду и
процессы в бытовых веществах.
17.
Практическое значение:Кислотно-щелочной баланс имеет широкое применение в жизни.
1.В быту:
*Проверка кислотности почвы для растений.
*Определение рН косметических средств( например, мыла).
2.В кулинарии:
*Создание цветных эффектов в блюдах( например, красный борщ
со свекольным индикатором).
3.В науке:
*Демонстрация кислотно-основных реакций на уроках химии.
18.
Выводы:Каркадэ *Доступный природный индикатор.
*Позволяет определить рН бытовых средств в домашних условиях.
*Безопасен и прост в использовании.
*Объясняет наглядно основы кислотно-щелочного баланса.
19.
Пояснительная записка:• Использована тема, которую изучают на уроке химии в 8 классе и
,которая соответствует программе, но при этом достаточно интересная
для проекта.
• Информация составлена так, чтобы она была понятна
восьмикласснику. Использован простой язык без сложной
терминологии, но при этом сохранена научная точность.
• Все примеры и объяснения соответствуют реальным химическим
процессам.
• Меры безопасности при опытах соблюдены, материалы доступны.
• Ошибки проверены и исправлены
20.
Список литературы:• Учебник химии 8 класс. Автор: Н.Е. Кузнецова, И.М Титова
• Интернет-ресурсы : научные статьи о природных индикаторах.
• Видео-эксперименты по данной теме.



















 chemistry
chemistry








