Similar presentations:
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
1.
2. Периодическая система химических элементов Д.И.Менделеева
II
1
H
II
2
Li
III
3
Na
4
K
IV
5
6
V
7
8
VI
9
VII
II
Группы элементов
IV
V
VI
III
VII
VIII
He
Щелочные металлы
1
1.00797
Водород
6,939
11 Mg
22,988
65.37
Цинк
37 Sr
85.47
Рубидий
38 Y
87.62
Стронций
112.41
Кадмий
55 Ba
132.905
Индий
Барий
79 Au
80 Hg Tl
Золото
Ртуть
196.966
10 Франций
200.59
87 Ra
[223]
Радий
Лантан
91.224
Цирконий
178.49
Гафний
Свинец
Ac 104 Rf
227.028
Актиний
[261]
Резерфордий
92.906
51.996
Хром
Селен
Хлор
10
20,18
Неон
17 Ar
35,453
54.938
Марганец
34 Br
78.96
95.94
Молибден
51 Te
121.75
Сурьма
Ta
180.9479
Тантал
82 Bi
207.2
Сера
32,064
9 Ne
18.9984
18
Аргон
39,948
Бром
55.847
35 Kr
79.904
58.933
Железо
Кобальт
58.71
Никель
36
83,8
Криптон
Nb 42 Mo 43 Tс 44 Ru 45 Rh 46 Pd
Ниобий
73
фтор
16 Cl
33 Se
74.9216
Мышьяк
41
F
V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni
50.942
Ванадий
50 Sb
118.71
Олово
81 Pb
204.383
Таллий
88 89
[226]
Zr
La 72 Hf
138.81
Фосфор
8
15.996
Кислород
15 S
30,9738
32 As
72.59
Германий
49 Sn
114.82
7 O
14.0067
Ti 23
47.90
Титан
39 40
88.9059
Иттрий
56 57
137.34
22
Азот
14 P
28,086
Кремний
31 Ge
69.72
Галлий
Цезий
Fr
44.956
Скандий
Ag 48 Cd In
107.868
Серебро
Cs
Кальций
Sс
6 N
12,011
Углерод
13 Si
26,9815
Алюминий
20 21
40,08
5 C
10 .811
Cu 30 Zn Ga
63.546
Медь
47
Бор
12 Al
24,312
Магний
19 Ca
39.102
Калий
Rb
4 В
9,012
Вериллий
Натрий
29
Гелий
3 Be
Литий
2
4,003
Теллур
74
Висмут
Дубний
101.07
53 Xe
Иод
126.904
102.905
Рутений
Родий
106.4
Палладий
54
Ксенон
131,3
W 75 Re 76 Os 77 Ir 78 Pt
183.85
186.2
Рений
84 At
208.982
Полоний
105 Db 106
[262]
52 I
127.60
Вольфрам
83 Po
208.98
99
Технеций
Sg
[263]
Сиборгий
Астат
190.2
85 Rn
210
192.2
Осмий
Иридий
86
Радон
[222]
107 Bh 108 Hs 109 Mt
[262]
Борий
[265 ]
Хассий
[266 ]
Мейтнерий
195.09
Платина
3.
Общая характеристика элементов Iгруппы главной подгруппы
4.
История открытия литияАрфведсон
Юхан Август
(12 .01.1792 г. –
28 .10.1841 г.)
А.Арфведсон, изучая минерал Петалит в 1817
году, открыл элемент литий в форме соединения
в минерале петалит. Он установил, что в
петалите содержится "огнепостоянная щелочь
до сих пор неизвестной природы".
• Берцелиус предложил назвать ее литионом
(Lithion), поскольку эта щелочь в отличие от
кали и натра впервые была найдена в "царстве
минералов" (камней); название зто произведено
от греч.- камень.
Металлический Литий впервые получен в 1818 г. Г.
Дэви путем злектролиза щелочи.
В 1855 г. Бунзен и Маттессен разработали
промышленный
способ
получения
металлического лития злектролизом хлорида
лития.
5.
История открытия натрияГемфри Дэви
(17.12.1778 г –
29.05.1829 г)
Натрий (Natrium, от англ. и франц. Sodium,
нем. Natrium от древнеевр. neter —
бурлящее вещество. В 1807 г. Г.Дэви путем
электролиза слегка увлажненных твердых
щелочей получил свободный металл натрий, назвав его содий (Sodium).
В следующем году Гильберт предложил
именовать новый металл
натронием
(Natronium); Берцелиус сократил последнее
название до "натрий" (Natrium).
6.
История открытия калияКалий (англ. Potassium, франц. Potassium, нем.
Kalium) открыл в 1807 г. Г.Дэви, производивший
электролиз твердого, слегка увлажненного
едкого кали. Дэви именовал новый металл
потассием (Potassium), но это название не
прижилось. Крестным отцом металла оказался
Гильберт, известный издатель
журнала
"Annalen deг Physik", предложивший название
"калий"; оно было принято в Германии и
России.
Гемфри Дэви
(17.12.1778 г –
29.05.1829 г)
7.
История открытия рубидияРоберт Вильгельм Бунзен
(31.03.1811 - 16.08.1899)
Густав Роберт Кирхгоф
(12.03.1824 – 17.10.1887)
При
спектроскопическом
анализе
минерала лепидолит (фторсиликат лития
и алюминия) и
обнаружились две
новые красные линии в красной части
спектра. Эти линии Р. Бунзен и
Г.Кирхгофф правильно отнесли к новому
металлу, который назвали рубидием
(лат. rubidus - красный) из-за цвета его
спектральных линий. Получить рубидий
в виде металла Бунзену удалось в 1863
году.
8.
История открытия францияПЕРЕ (Perey)
Маргарита
(19.10.1909 13.05.1975)
Этот
элемент
был
предсказан
Д.И.Менделеевым (как Эка-цезий), и был
открыт (по его радиоактивности) в 1939 г.
Маргаритой Пере, сотрудницей Института
радия в Париже с порядковым номером
Z = 87 и периодом полураспада 21 мин.
Она же дала ему в 1964 г. название в честь
своей
родины
–
франций.
.
Микроскопические количества франция223 и франция-224 могут быть химически
выделены из минералов урана и тория.
Другие изотопы франция получают
искусственным путём с помощью ядерных
реакций.
9.
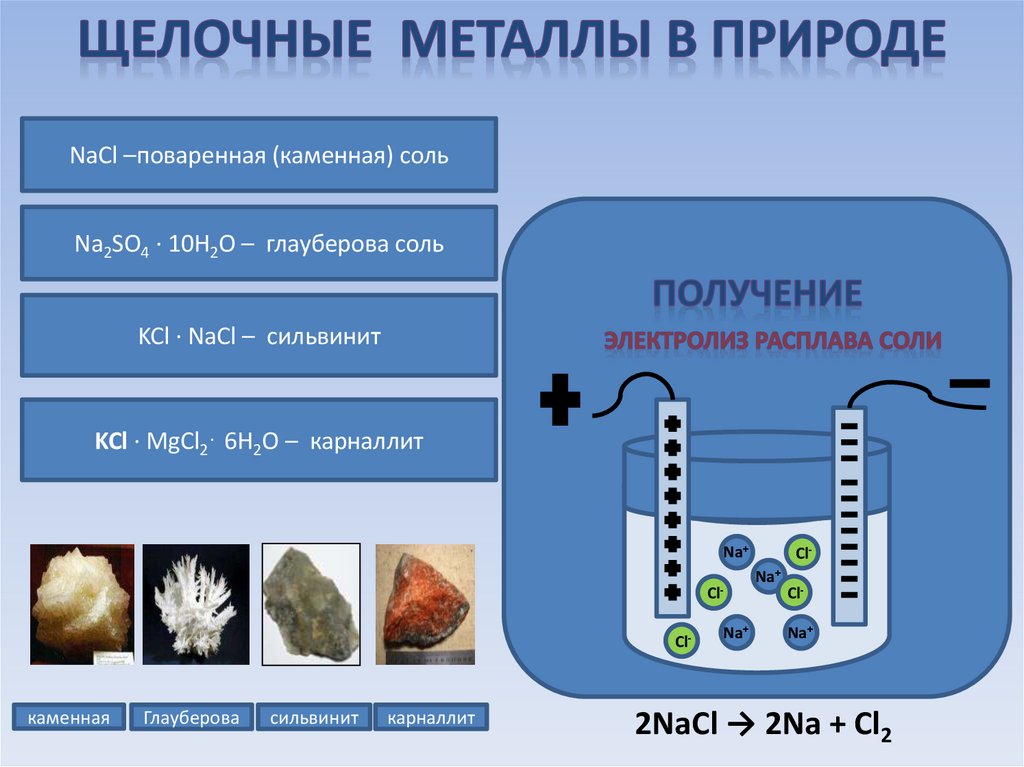
NaCl –поваренная (каменная) сольNa2SO4 ∙ 10H2O – глауберова соль
KCl ∙ NaCl – сильвинит
KCl ∙ MgCl2· 6H2O – карналлит
Na+
ClCl-
каменная
Глауберова
сильвинит
карналлит
Na+
ClNa+
ClNa+
2NaCl → 2Na + Cl2
10.
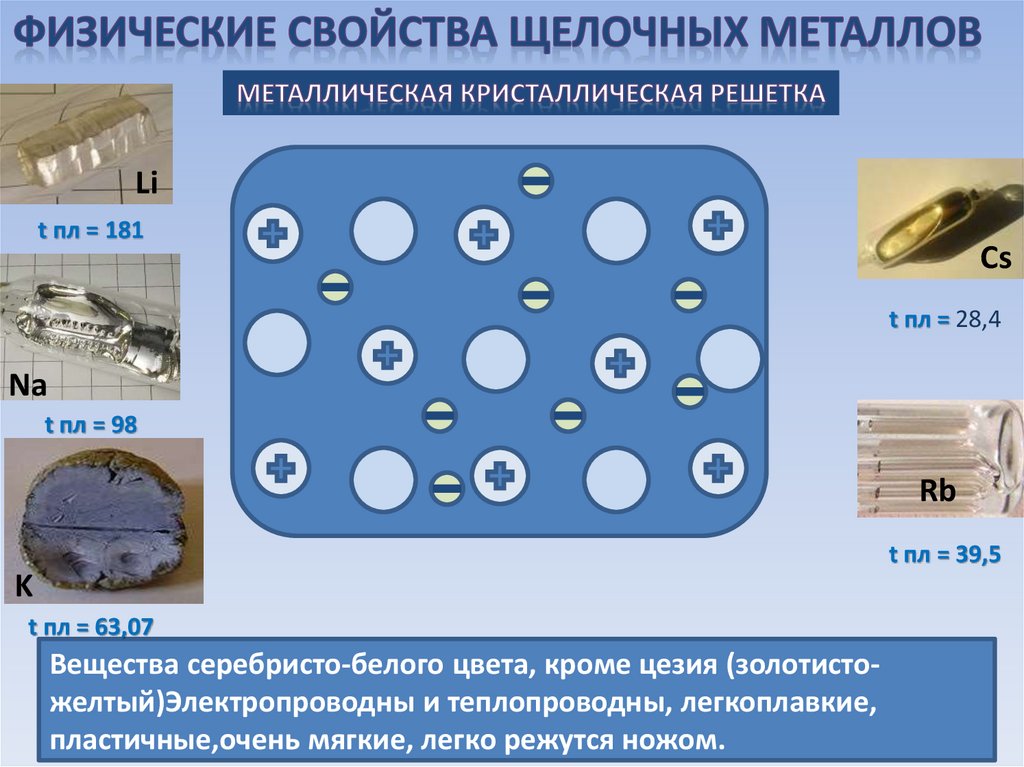
Lit пл = 181
Сs
t пл = 28,4
Na
t пл = 98
Rb
t пл = 39,5
K
t пл = 63,07
Вещества серебристо-белого цвета, кроме цезия (золотистожелтый)Электропроводны и теплопроводны, легкоплавкие,
пластичные,очень мягкие, легко режутся ножом.
11.
Химические свойства1) 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются)
2) 4Li + O2 = 2Li2O
2Na + O2 = Na2O2
3) 2Na + Н2 = 2NaН
(при нагревании 200-400oC)
оксид Li
пероксид Na
2K + 2O2 = KO2
надпероксид K
4) 6Li + N2 = 2Li3N (Li - при комнатной T, остальные щелочные Me -при нагревании)
5) 2Na + 2Н2О = 2NaОН + Н2
(Li - спокойно, Na - энергично,
остальные – со взрывом –
воспламеняется выделяющийся Н2
Rb и Cs реагируют не только
с жидкой Н2О, но и со льдом. .
6) 2C2H5OH + 2Na = 2C2H5ONa + Н2
12.
Качественное определение щелочных металловДля распознавания соединений щелочных металлов по окраске пламени
исследуемое вещество вносится в пламя горелки на кончике железной
проволоки.
Li+ - карминово-красный K+ - фиолетовый Cs+ - фиолетово-синий
Na+ - желтый
Rb + - розово-фиолетовый
13.
Применение щелочных металловДля
получения
трития
Литий
Получение
сплавов для
подшипников
Химические
источники
тока
Восстановитель
в органическом
синтезе
Пиротехника
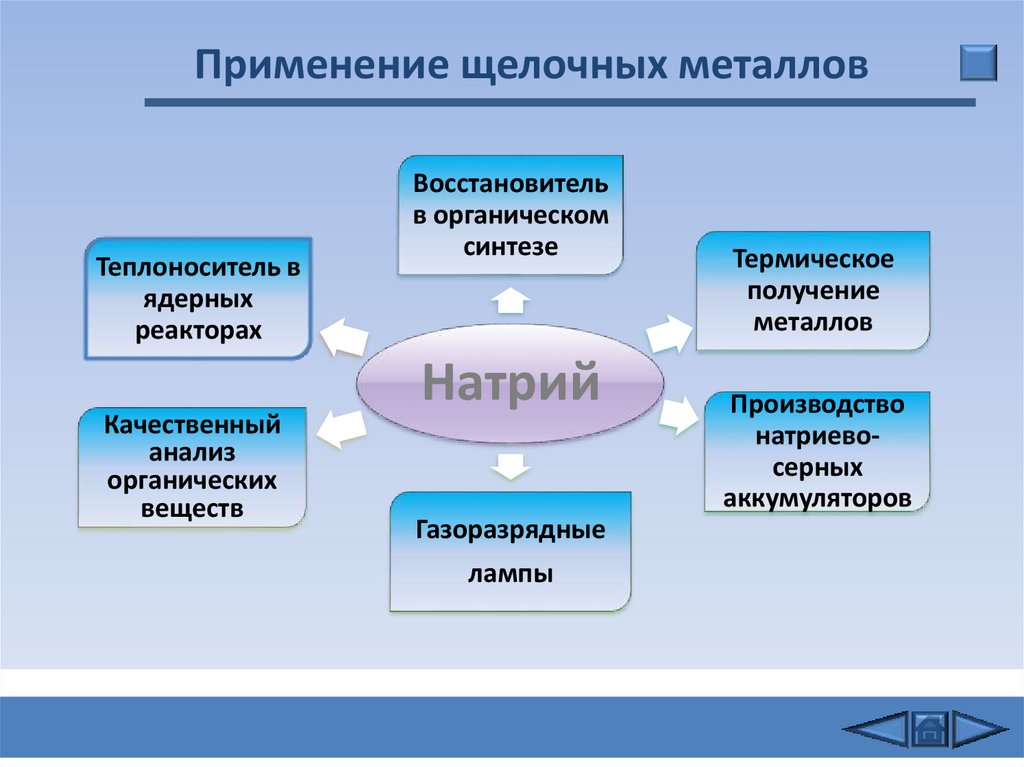
14.
Применение щелочных металловТеплоноситель в
ядерных
реакторах
Качественный
анализ
органических
веществ
Восстановитель
в органическом
синтезе
Натрий
Газоразрядные
лампы
Термическое
получение
металлов
Производство
натриевосерных
аккумуляторов
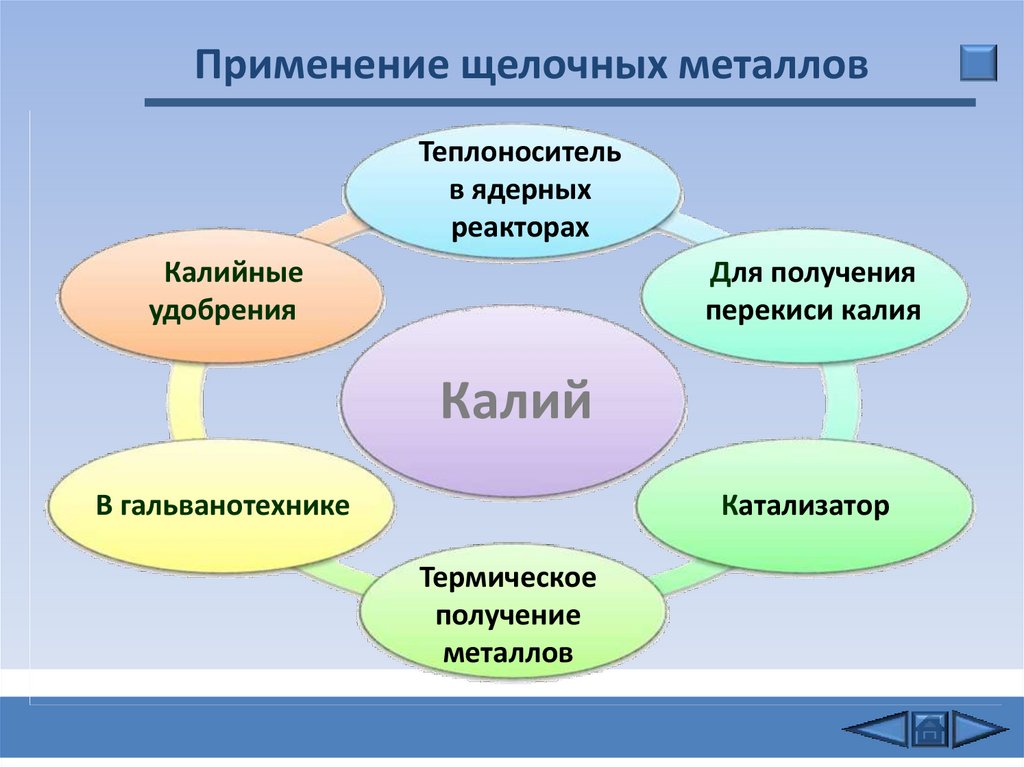
15.
Применение щелочных металловТеплоноситель
в ядерных
реакторах
Калийные
удобрения
Для получения
перекиси калия
Калий
В гальванотехнике
Катализатор
Термическое
получение
металлов
16.
Применение щелочных металлов17.
Применение щелочных металлов18.
Проверь себя:Выберите неверные суждения о щелочных металлах:
1. Число электронов на внешнем энергетическом уровне
щелочных металлов равно 1.
2. При переходе от лития к калию уменьшается радиус атома
3.В реакциях щелочные металлы являются восстановителями.
4. При взаимодействии калия с кислородом образуется оксид
калия
5. Щелочные металлы – это металлы IA группы Периодической
системы химических элементов.
6. Щелочные металлы получают электролизом расплавов их
солей.
7. Щелочные металлы не взаимодействуют с водой.
8. Встречаются в природе в свободном виде
19.
Интернет-ресурсыhttp://school-collection.edu.ru/
http://ru.wikipedia.org/
images.yandex.ru
Химия.9 класс. О.С.Габриелян.-М.:Дрофа,2013













 chemistry
chemistry








