Similar presentations:
Энергия алмасуы туралы түсінік
1.
ТАҚЫРЫБЫ:ЭНЕРГИЯ АЛМАСУЫ.
2.
Жоспары:1.Энергия алмасуы туралы түсінік.
2.Көмірсулар, липидтердің және
нәруыздардың арнайы жолдармен
ыдырауы.
3.Үш карбон қышқылдарының циклі (ҮКЦ).
4.Биологиялық тотығу (БТ).
5.Тотығудан фосфорлану (ТФ).
3.
Энергия алмасуы туралы түсінікЭнергия алмасуы – бұл энергетикалық
материалдардың ағзада ыдырап, энергия бөлу
немесе белгілі бір қосылыс түрінде синтезделіп,
энергияны сақтау процесі.
Күннің көзінде сутектің 4 атомы жоғары
температура мен жоғары қысым астында өзара
бірігіп, гелийдің бір атомын түзгенде бөлініп
шыққан энергия Күннің бетінде жиналады.
Энергияның артық мөлшері әртүрлі электромагнит
толқындар түрінде (сәуле, радио толқындар,
рентген, инфрақызыл сәуле, т.б.) кеңістікте
таралады.
4.
Жер бетіндегі аутотрофтар (өсімдіктер) күнэнергиясын хлорофилл молекуласы арқылы
сіңіріп алып, су мен СО2-ден глюкозаны
синтездейді.
Бұл процесті фотосинтез деп атайды. Бұл
процесте Күн энергиясы химиялық энергияға
айналады.
Фотосинтезді келесі реакция түрінде көрсетуге
болады:
2847кДж
6Н2О+6СО2
С6Н12О6+6О2
глюкоза
5.
Жануарлар (гетеротрофтар) энергия қорынөсімдіктермен қоректену арқылы толықтырып
отырады. Жануарлар ағзасында қарама-қарсы
реакция жүреді:
С6Н12О6+6О2
Н2О+6СО2+2847 кДж
Бірақ бұл энергия біртіндеп, энергия алмасуының
әрбір сатысында бөлінеді.
Бөлінген энергияның бір бөлігі АТФ түзілуіне
жұмсалады, ал қалған бөлігі жылу түрінде тарап
кетеді.
АТФ ағзада екі процесте түзіледі:
1) тотығудан фосфорлану;
2) субстраттан фосфорлану.
6.
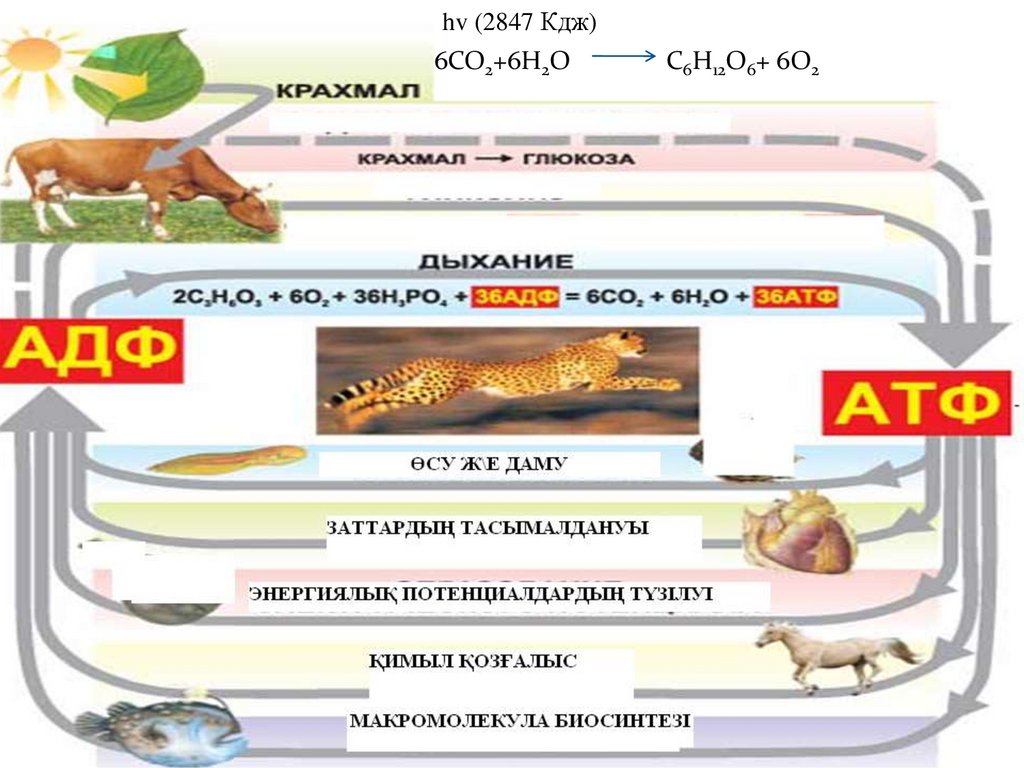
hv (2847 Кдж)6СО2+6Н2О
С6Н12О6+ 6О2
7.
Энергия алмасуы 4 сатыдантұрады:
І. Негізгі қоректік заттардың арнайы
жолдармен ыдырап, ортақ өнім
активті сірке қышқылын (АСҚ) түзуі.
ІІ. Үшкарбон қышқылдарының циклі
(ҮҚЦ).
ІІІ. Биологиялық тотығу (БТ).
ІV.Тотығудан фосфорлану (ТФ).
8.
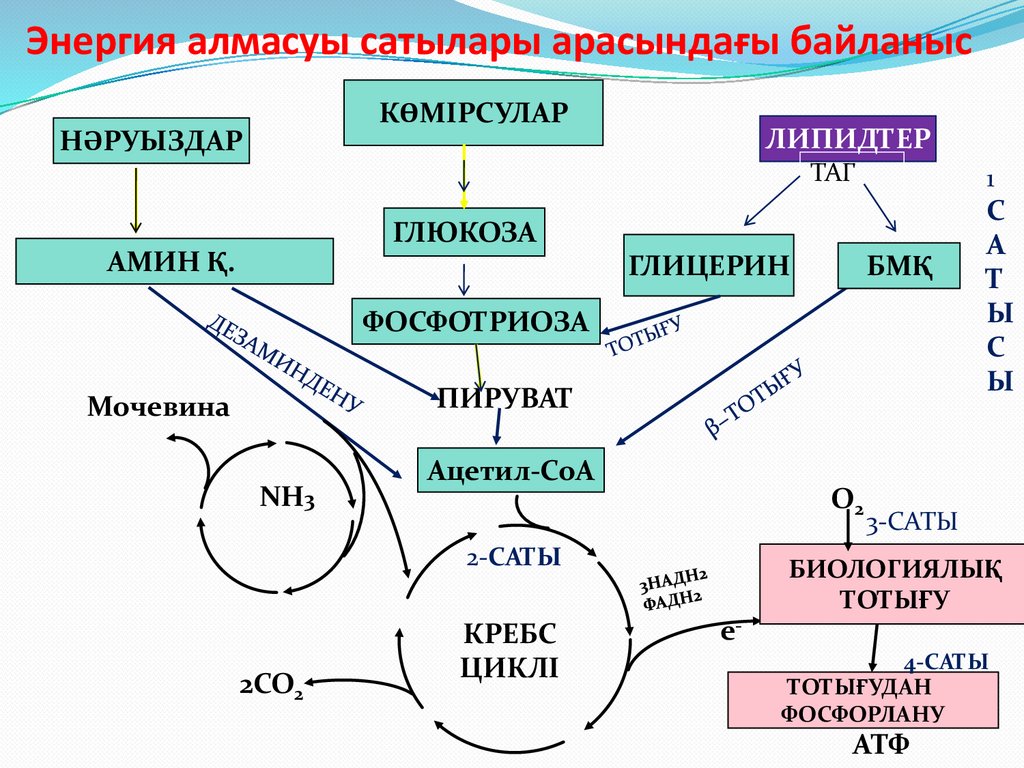
Энергия алмасуы сатылары арасындағы байланысКӨМІРСУЛАР
НӘРУЫЗДАР
ЛИПИДТЕР
ТАГ
1
ГЛЮКОЗА
АМИН Қ.
ГЛИЦЕРИН
БМҚ
ФОСФОТРИОЗА
ПИРУВАТ
Мочевина
ΝΗ3
Ацетил-CoA
O2
2-САТЫ
2CO2
КРЕБС
ЦИКЛІ
С
А
Т
Ы
С
Ы
3-САТЫ
БИОЛОГИЯЛЫҚ
ТОТЫҒУ
e4-САТЫ
ТОТЫҒУДАН
ФОСФОРЛАНУ
ATФ
9.
І сатысыІ сатысы ас қорыту жолдарында
оттек қатысуынсыз жүреді және
субстраттардағы барлық энергияның
шамамен 1%-ы бөлінеді. Нәруыздар,
көмірсулар
және
липидтердің
әрқайсысы сәйкес ферменттердің
қатысуымен ыдырайды.
10.
КөмірсуларАҚЖ-да
моносахаридтерге дейін ыдырайды,
қанға негізінен глюкоза шығады.
Глюкоза фосфотриозаларға, әрі қарай
пирожүзім қышқылына (ПЖҚ) дейін
тотығады.
11.
Липидтер (ТАГ) асқорытужолдарында глицерин мен бос май
қышқылдарына (БМҚ) дейін ыдырайды,
глицерин ПЖҚ-ға дейін, БМҚ бетатотығу арқылы АСҚ-на дейін
ыдырайды.
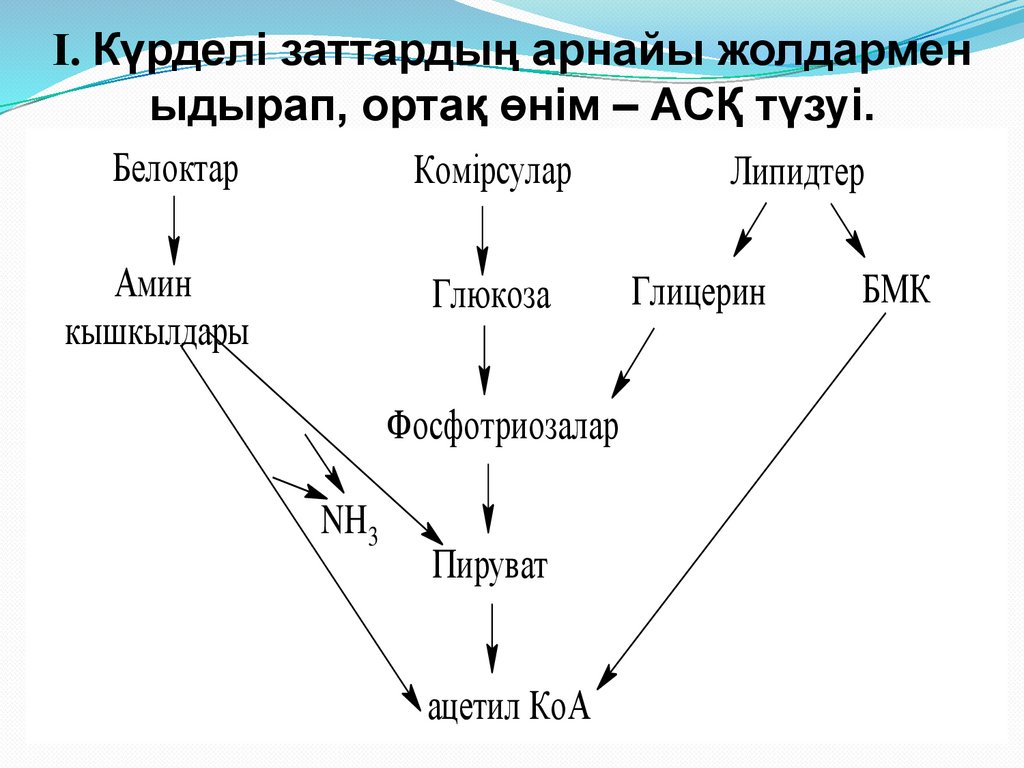
Нәруыздар ас қорыту жолдарында
амин қышқылдарына дейін ыдырайды,
АҚ тіндерде дезаминденіп, ПЖҚ немесе
АСҚ түзеді.
12.
І. Күрделі заттардың арнайы жолдарменыдырап, ортақ өнім – АСҚ түзуі.
Белоктар
Комірсулар
Амин
кышкылдары
Глюкоза
Фосфотриозалар
NH3
Пируват
ацетил КоА
Липидтер
Глицерин
БМК
13.
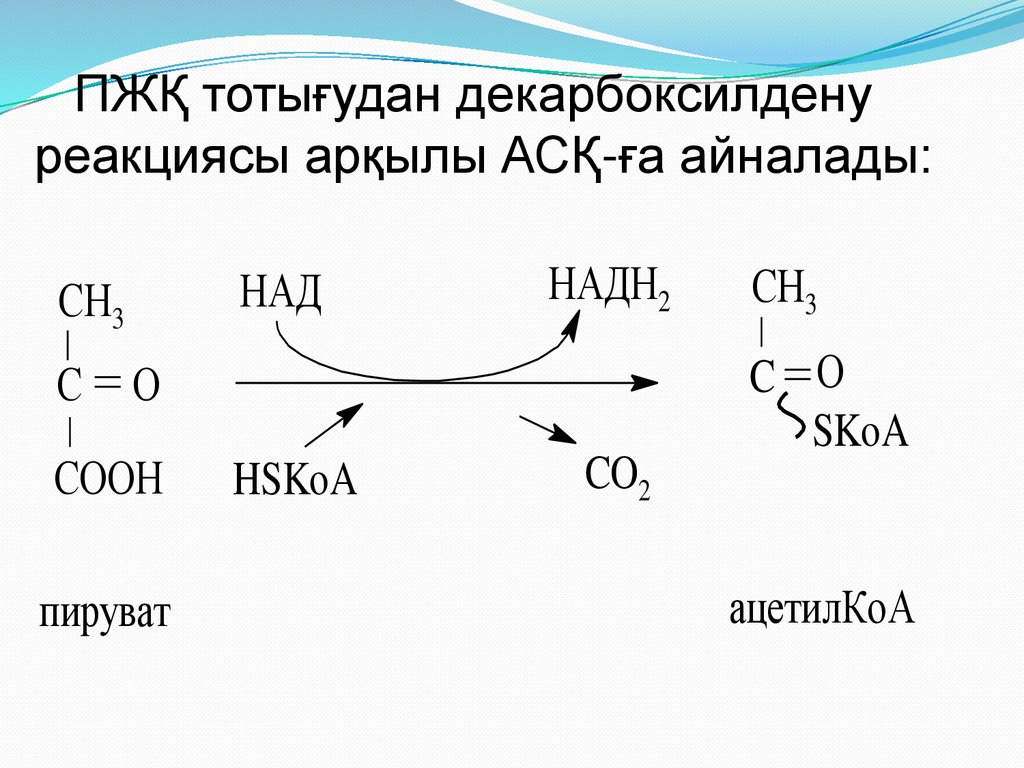
ПЖҚ тотығудан декарбоксилденуреакциясы арқылы АСҚ-ға айналады:
НАД
СН3
С
НАДН2
О
СOOН
пируват
HSKoA
CO2
СН3
C О
SKoA
ацетилКоА
14.
ІІ. Үшкарбон қышқылдарыныңциклі (ҮҚЦ).
Бұл циклді лимон қышқылының
циклі немесе Кребс циклі деп те
атайды, оны алғаш рет 1937
жылы Ганс Кребс ашқан. 1953
жылы Нобель сыйлығын алды.
ҮКЦ-ның жалпы теңдеуі:
АцетилКоА
2СО2+3НАДН2 +ФПН2+АТФ
15.
ҮКЦ-ң ролі:1.АСҚ СО2-ге дейін тотығады;
2.Пластикалық қызмет атқарады. ҮҚЦде түзілген аралық өнімдер басқа
метаболизм
үдерістеріне
субстрат
ретінде пайдаланылады.
Мысалы:
❖α-кетоглутарат,
қымыздық
сірке
қышқылы алмастырылатын АҚ синтезіне;
❖ҚСҚ глюконеогенезге, т.б. жұмсалады.
16.
3.Заттар
алмасуын
өзара
байланыстырады.
4. Энергия активті сутектер түрінде
(НАДН2, ФПН2) сақтайды.
5. Тотықсызданған дегидрогеназалар
(НАДН2, ФПН2) биологиялық тотығуға
субстрат болады.
17.
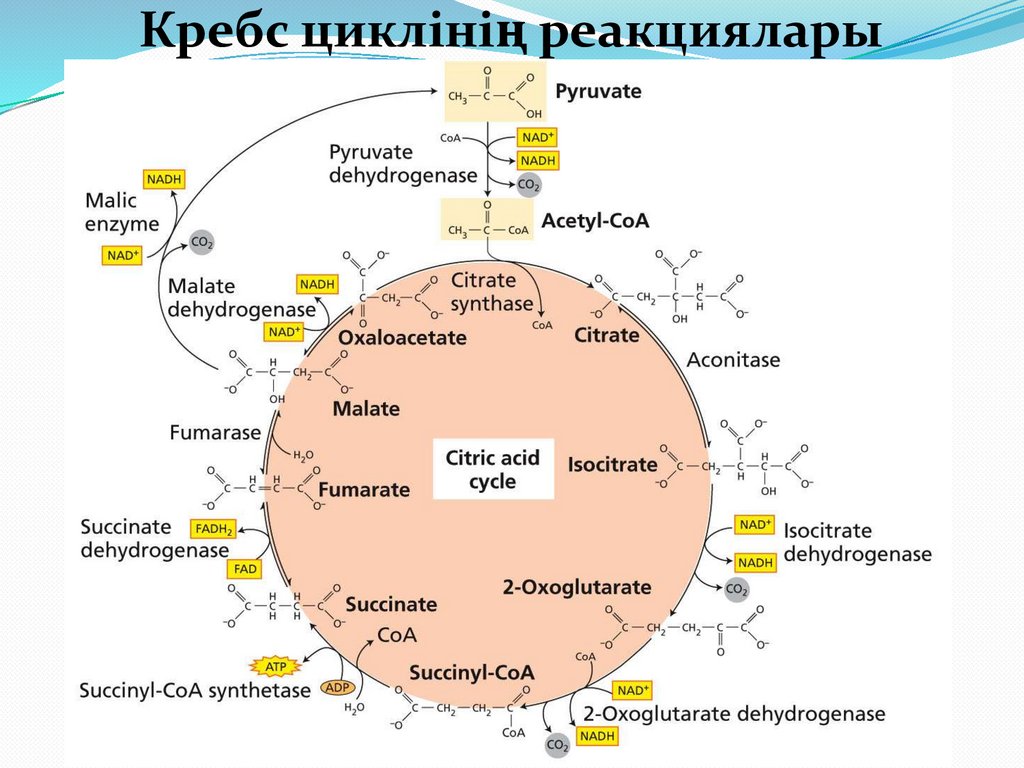
Кребс циклінің реакциялары18.
ҮКЦ-ң реакциялары1-реакция.
Ацетил-КоА
(АСҚ)
цитратсинтетазаның
әсерінен
қымыздық сірке қышқылымен (ҚСҚоксалоацетат)
конденсацияланып,
лимон қышқылы (цитрат) түзіледі.
Реакция судың қатысуымен өтеді,
НSКоА бөлініп кетеді.
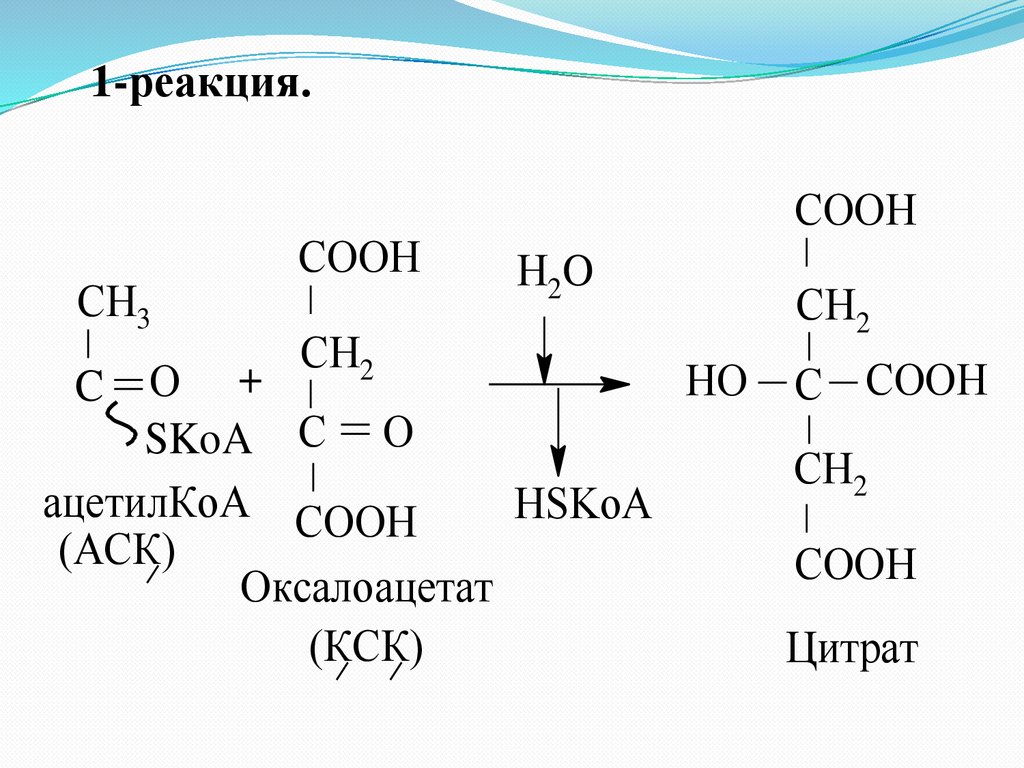
19.
1-реакция.СН3
СOOН
СН2
СOOН
Н2O
СН2
НO С СOOН
О +
SKoA С О
СН2
ацетилКоА СOOН
НSKoA
(АСК)
СOOН
Оксалоацетат
(КСК)
Цитрат
C
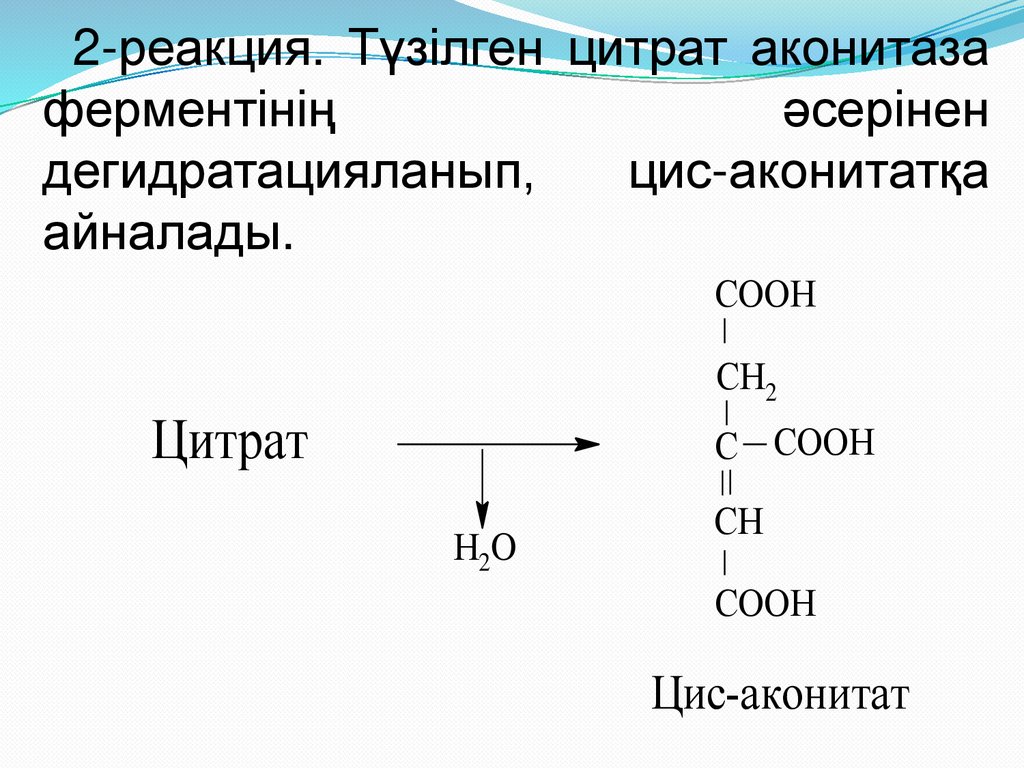
20.
2-реакция. Түзілген цитрат аконитазаферментінің
әсерінен
дегидратацияланып,
цис-аконитатқа
айналады.
СOOН
СН2
Цитрат
С СOOН
Н2O
СН
СOOН
Цис-аконитат
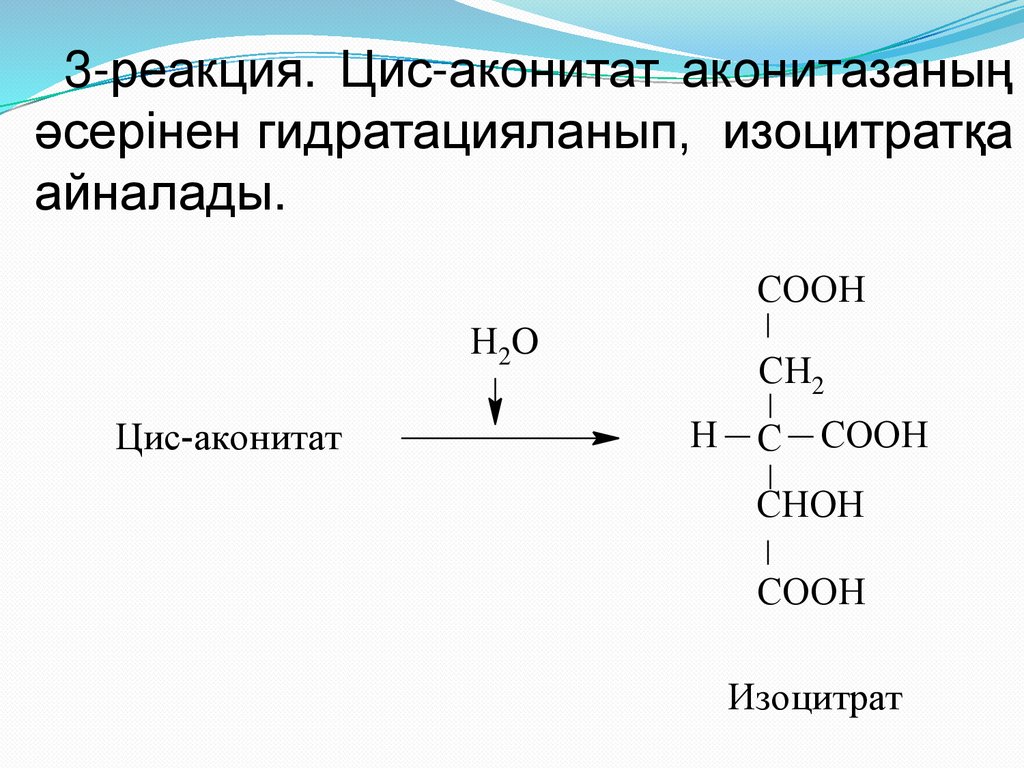
21.
3-реакция. Цис-аконитат аконитазаныңәсерінен гидратацияланып, изоцитратқа
айналады.
СOOН
Н2 O
Цис-аконитат
СН2
Н
С СOOН
СНOН
СOOН
Изоцитрат
22.
4-реакция.Изоцитрат
тотығып
(дегидрленіп),
қымыздық
янтарь
қышқылын (оксалосукцинат) түзеді. Бұл
реакцияны
изоцитратдегидрогеназа
(ИДГ) ферменті катализдейді, Ко НАД
НАДН2-ге тотықсызданады.
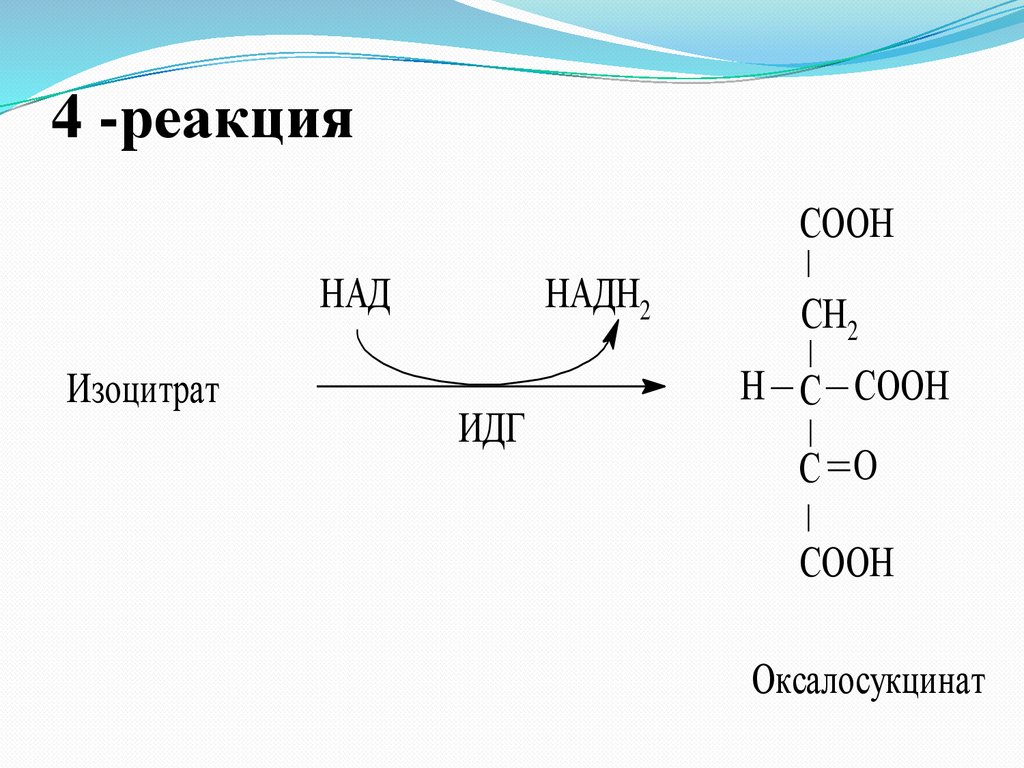
23.
4 -реакцияСOOН
НАД
Изоцитрат
НАДН2
ИДГ
СН2
Н С СOOН
С O
СOOН
Оксалосукцинат
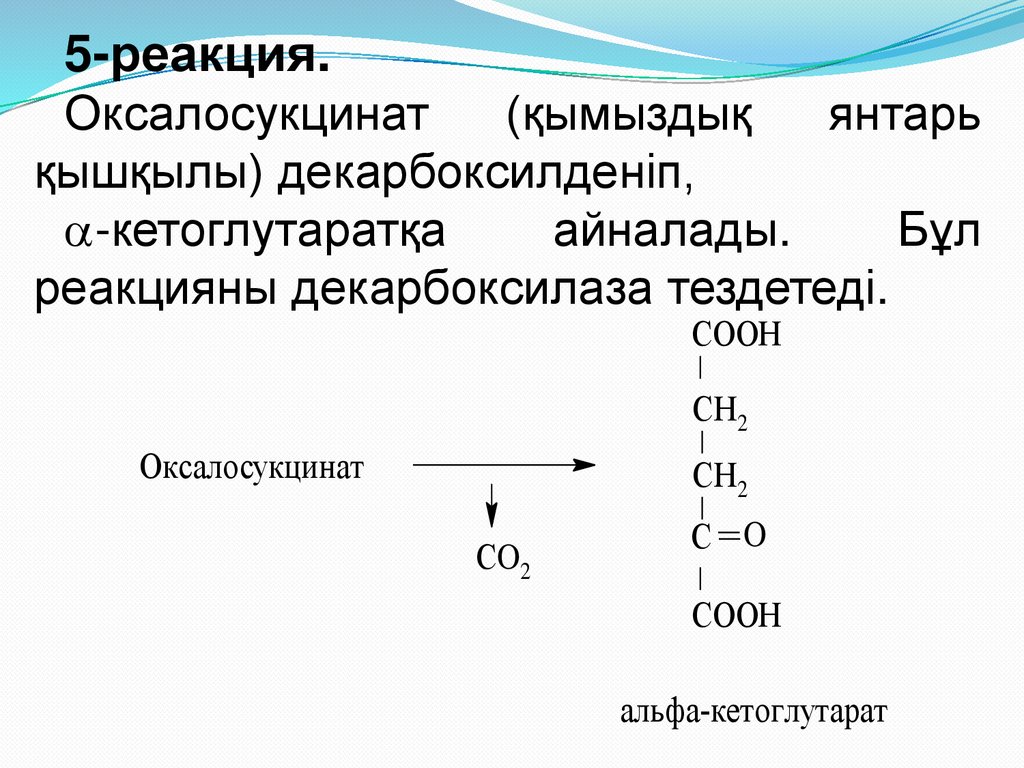
24.
5-реакция.Оксалосукцинат
(қымыздық
янтарь
қышқылы) декарбоксилденіп,
-кетоглутаратқа
айналады.
Бұл
реакцияны декарбоксилаза тездетеді.
СOOН
СН2
Оксалосукцинат
СН2
СO2
С O
СOOН
альфа-кетоглутарат
25.
6-реакция.Тотығудан декарбоксилдену реакциясы
нәтижесінде
-кетоглутараттан
СО2
бөлінеді,
Ко
НАД
НАДН2-ге
тотықсызданады.
Реакция -кетоглутаратдегидрогеназды
мультиферменттік
комплекстің
қатысуымен
жүреді.
Түзілген
өнім
мароэргиялық байланыс
~ арқылы
~SКоА-мен байланысқандықтан, оны
активті янтарь қышқылы (сукцинил-КоА)
деп атайды.
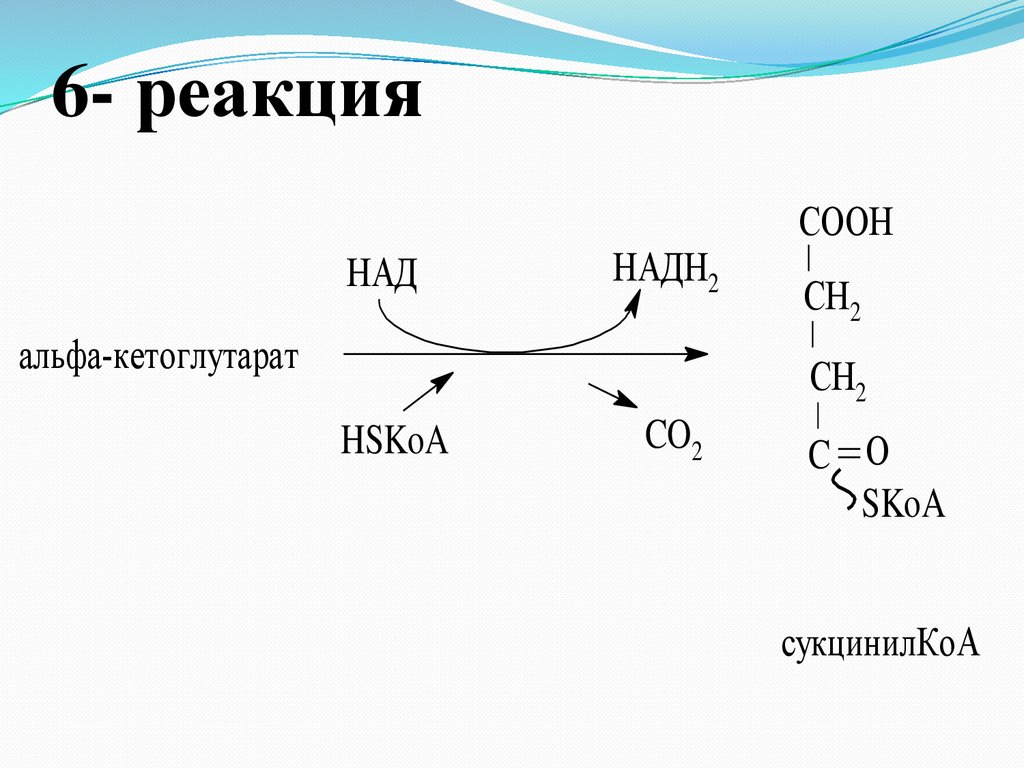
26.
6- реакцияНАД
НАДН2
альфа-кетоглутарат
СOOН
СН2
СН2
HSKoA
CO2
C О
SKoA
сукцинилКоА
27.
7-реакция.Сукцинаттиокиназа ферментінің
әсерінен сукцинил-КоА-дағы
макроэргиялық байланыс үзіліп,
энергия бөлінеді. Бұл энергия ГДФ пен
Н3РО4-н ГТФ түзілуіне жұмсалады, ал
ГТФ АТФ-ке айналады, яғни
субстраттан фосфорлану реакциясы
жүреді. Сукцинат (янтарь қышқылы)
және НSКоА түзіледі.
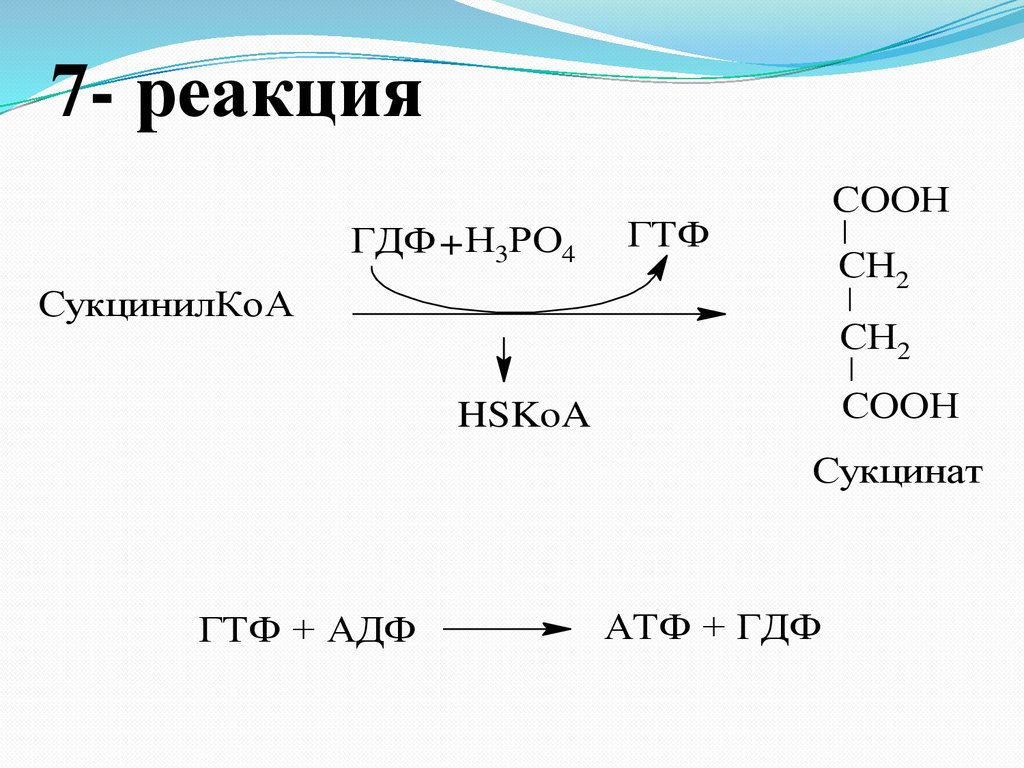
28.
7- реакцияГДФ + Н3РО4
СOOН
ГТФ
СН2
СукцинилКоА
СН2
СOOН
HSKoA
Сукцинат
ГТФ + АДФ
АТФ + ГДФ
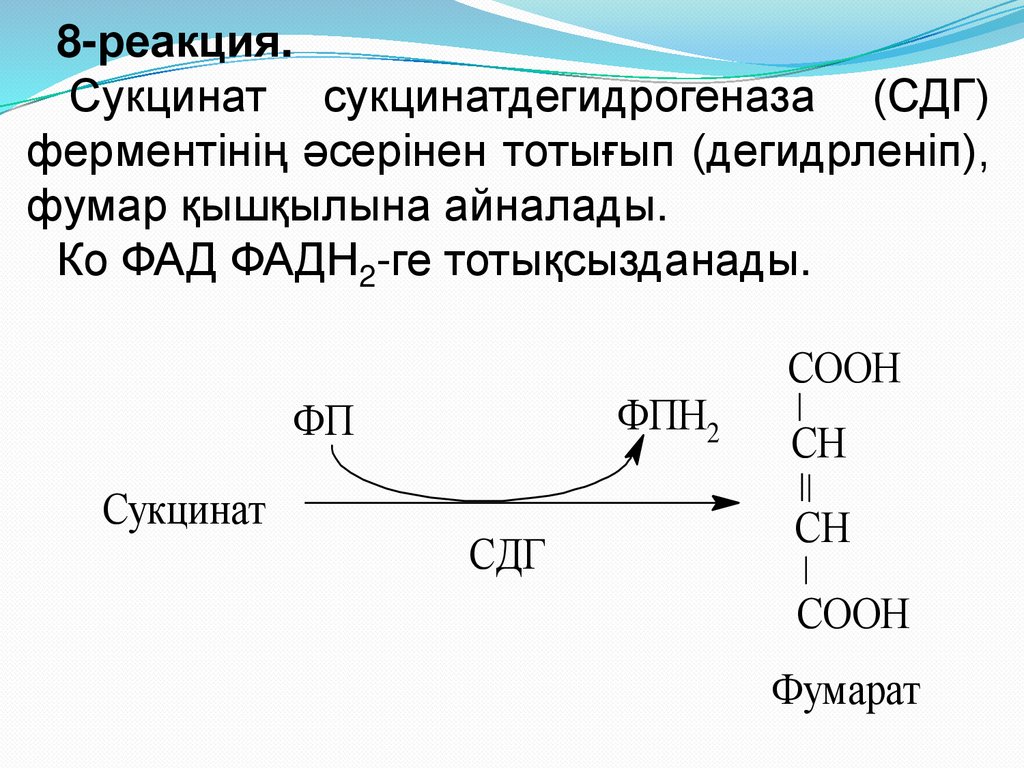
29.
8-реакция.Сукцинат сукцинатдегидрогеназа (СДГ)
ферментінің әсерінен тотығып (дегидрленіп),
фумар қышқылына айналады.
Ко ФАД ФАДН2-ге тотықсызданады.
ФПН2
ФП
Сукцинат
СДГ
СOOН
СН
СН
СOOН
Фумарат
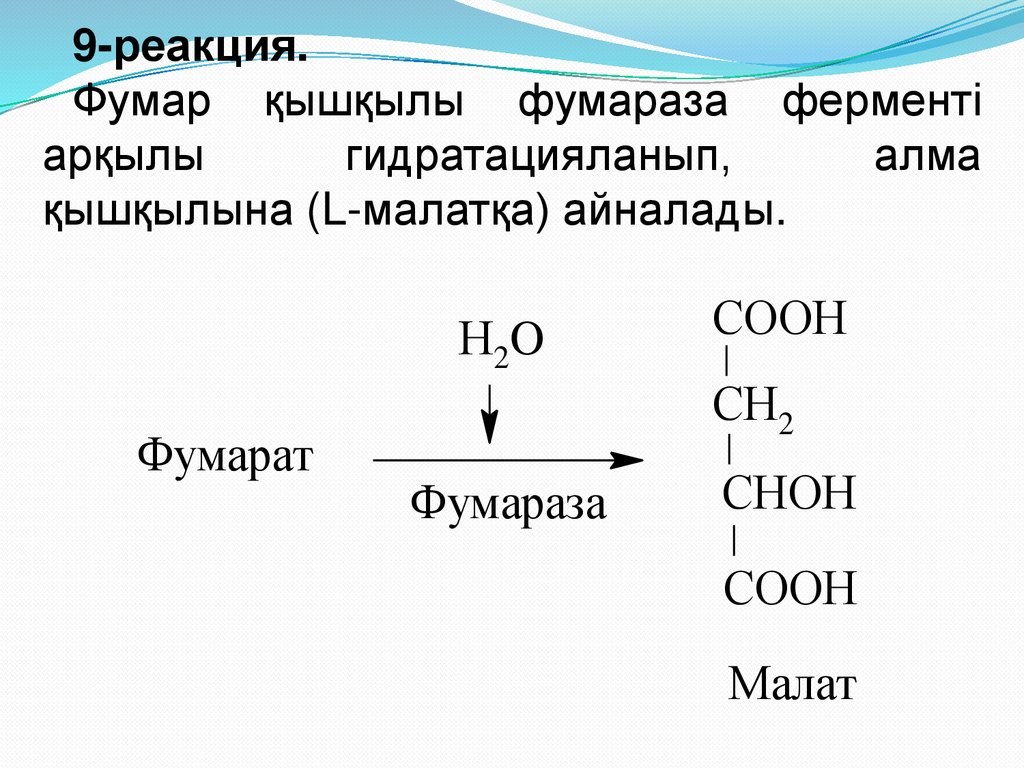
30.
9-реакция.Фумар қышқылы фумараза ферменті
арқылы
гидратацияланып,
алма
қышқылына (L-малатқа) айналады.
Н2O
Фумарат
СOOН
СН2
Фумараза
СНOН
СOOН
Малат
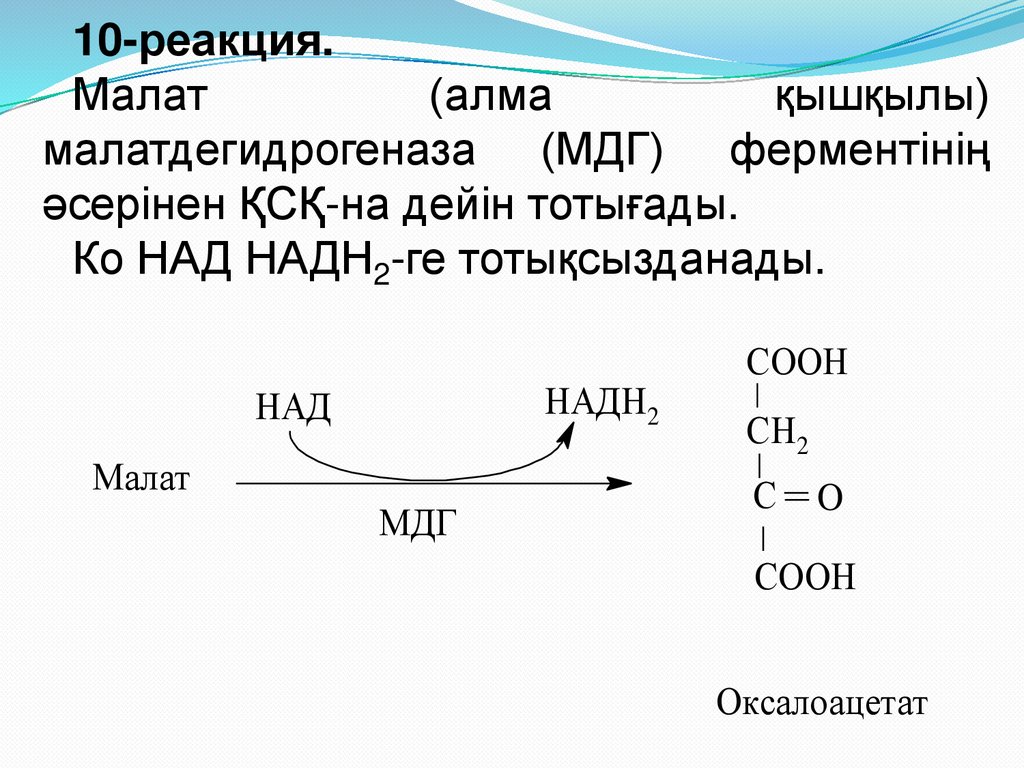
31.
10-реакция.Малат
(алма
қышқылы)
малатдегидрогеназа (МДГ) ферментінің
әсерінен ҚСҚ-на дейін тотығады.
Ко НАД НАДН2-ге тотықсызданады.
НАДН2
НАД
Малат
МДГ
СOOН
СН2
С
O
СOOН
Оксалоацетат
32.
ІІІ сатысы. Биологиялық тотығу(БТ) немесе тіндік тыныс алу
Биологиялық тотығу (БТ) немесе
тіндік тыныс алу – тотықсызданған
дегидрогеназалардың
оттегінің
қатысуымен тотығуы.
33.
БТ–
тотығу-тотықсыздану
реакцияларының
тізбегі,
бұл
реакциялардың нәтижесінде активті
сутектер (НАДН2, ФПН2) протондар мен
электрондарға дейін ыдырайды.
Тыныс алудың мәнін ең алғаш рет
А.-Л.Лавуазье (1743-1794ж.) түсіндірген.
34.
БТ-ның жалпы теңдеуі:2Н+ + О2- → Н2О + энергия
БТ-ның ролі:
1) энергия біртіндеп бөлінеді,
бөлінген энергия пайдаланылады:
✓АТФ түзілуіне (40-48 %)
✓ жылу (52-60%).
2) эндогенді су түзіледі.
35.
БТ жасуша митохондриясында өтеді.БТ тізбегінде барлық ферменттер
алдымен тотығуы, одан тотықсыздануы
кейін керек, яғни тіндік тыныс алуға
қатысатын оксидоредуктазалар
ауыспалы күйде: бірде тотыққан, бірде
тотықсызданған күйде болуы мүмкін.
36.
Оксидоредуктазалар БТ тізбегінде тотығутотықсыздану потенциалының (ТТП) өсуретіне байланысты орналасады:
ПФ(НАД) < ФП(ФМН) < КоQ < Цх b <
< Цхс1 < Цхс < Цха < Цха3.
ТТП ең төмен НАД/ НАДН2
(-0,32 В)
тізбектің бас жағында, ал ТТП ең
жоғары 1/2 О2 / Н2О (+0,82 В) тізбектің
соңында орналасқан.
37.
БТ сатыларыБТ 11 реакциядан тұрады.
І. Субстрат өзіндегі сутегін жоғалтып,
Пиридин ферменттері (ПФ) арқылы
тотығады, ал НАД тотықсызданады.
ПФ-нің тотықтыратын субстраттары:
➢ изолимон қышқылы,
➢ сүт қышқылы,
➢ алма қышқылы.
ФП-ның субстраттары:
❖ янтар қышқылы,
❖ -кетоглутар қышқылы.
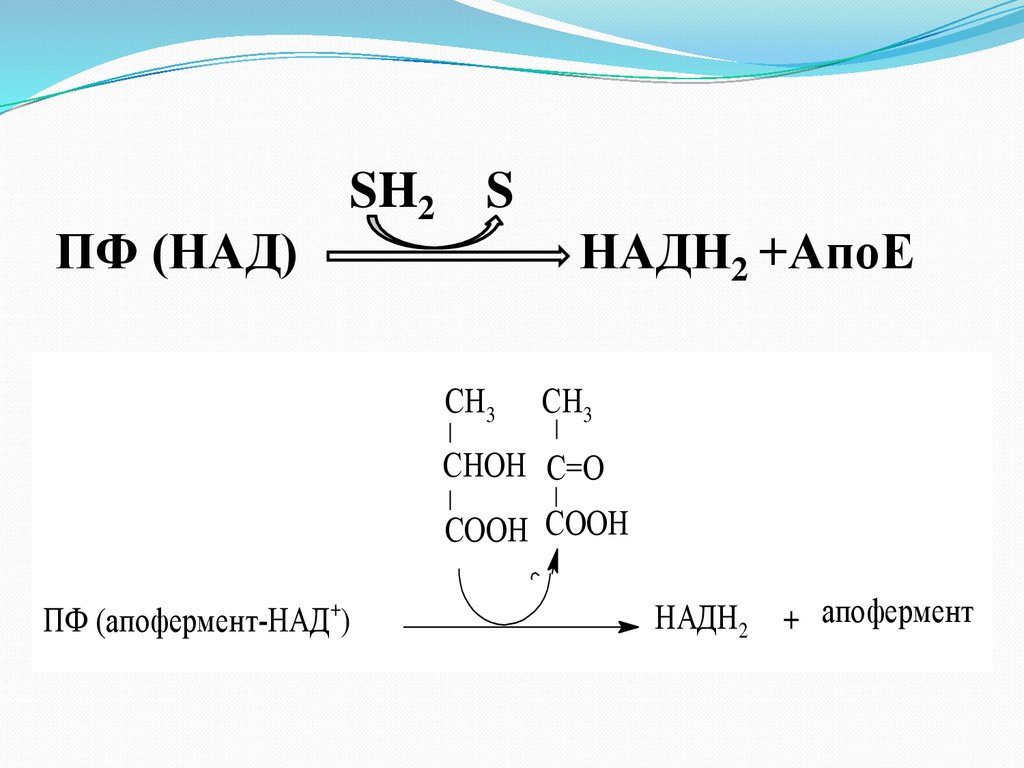
38.
ПФ (НАД)SH2
S
НАДН2 +АпоЕ
СН3
СН3
СНОН С=О
СООН СООН
ПФ (апофермент-НАД+)
НАДН2
+ апофермент
39.
ІІ.КоферментіФМН
болатын
флавопротеиндер тотықсызданған НАДН2-н
сутегін
бөліп
алып,
тотықсызданады
(ФМНН2-ге), ал НАДН2 НАД-қа тотығады:
+
НАД
НАДН2
ФП (апофермент-ФМН)
+46 кДж
ФПН2 (апофермент-ФМНН2)
Бұл сатыда 46 кДж энергия бөлінеді, оның
33 кДж 1 молекула АТФ-тің түзілуіне
жұмсалады, қалған бөлігі жылу түрінде
бөлінеді.
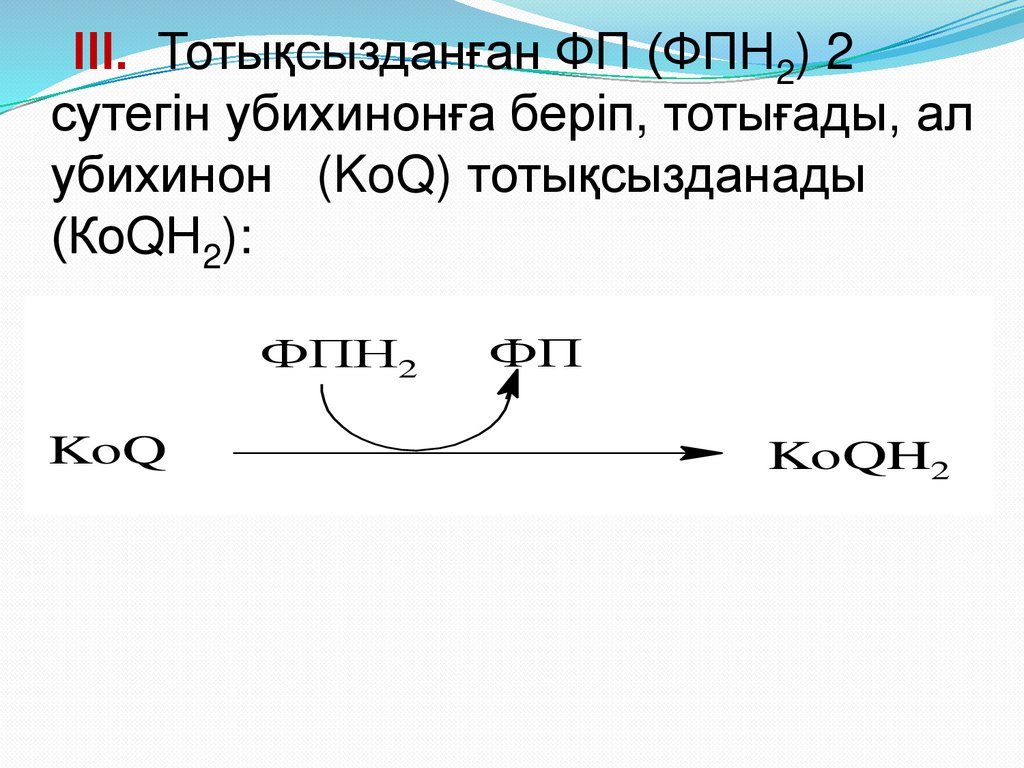
40.
ІІІ. Тотықсызданған ФП (ФПН2) 2сутегін убихинонға беріп, тотығады, ал
убихинон (KoQ) тотықсызданады
(КоQН2):
ФПН2
KoQ
ФП
KoQH2
41.
ІV. Сутегі субстраттан қашықтағансайын сутек атомындағы протон
мен
электрон
арасындағы
байланыс әлсіреп, ол 2 протон мен
2 электронға ыдырайды:
2Н0 → 2Н+ + 2ē
ерітіндіде цитохром
Протондар ерітіндіде қалады да,
электрондар
цитохром
жүйесі
арқылы оттекке тасымалданады.
42.
V. Бөлініп шыққан электрондар 2феррицитохром b-ға (Цхb(Ғе3+)) беріліп,
ферроцитохром
b-ға
(Цхb(Ғе2+))
тотықсызданады:
2e2Ц х b(Fe+ 3)
ІІІ, ІV, V сатыларында
бөлінген энергияның мөлшері аз
болғандықтан,
АТФ
синтезіне
жұмсалмай, жылу түрінде бөлінеді.
БТ-дың
І,
2Ц х b(Fe+ 2)
43.
VІ. 2 ферроЦхb электрондарды 2ферриЦхс1-ге беріп, өзі тотығады, ал 2
ферриЦхс1
тотықсызданып,
ферроформаға айналады:
2Цхb(Fe ) 2Цхb(Fe )
2+
2Цх c1(Fe+ 3)
3+
2Цхc1(Fe ) +43 кДж
+2
ФерроЦхb тотыққанда 43 кДж энергия
бөлініп,
тағы
бір
АТФ
түзіледі,
энергияның қалған бөлігі жылу түрінде
таралады.
44.
VІІ. 2 ферроЦхс1 электрондарды 2ферриЦхс-ға беріп, өзі тотығады, ал 2
ферриЦхс тотықсызданып, ферроформаға айналады:
2Ц хc1(Fe ) 2Ц х c1(Fe )
+2
2Ц х c(Fe )
+3
+3
2Цхc(Fe )
2+
45.
VІІІ. 2 ферроЦхс электрондарды 2ферриЦха-ға беріп, өзі тотығады, ал 2
ферриЦха тотықсызданады да, ферроформаға айналады:
2Цхc(Fe ) 2Цх c(Fe )
2+
2Цх a(Fe )
+3
+3
2Цхa(Fe+ 2)
VІІ, VІІІ сатыда бөлінген энергияның
мөлшері аз, АТФ синтезіне жұмсалмай,
жылу түрінде бөлінеді.
46.
ІХ. 2 ферроЦха электрондарды 2ферриЦха3-ке беріп, өзі тотығады, ал 2
ферриЦха3 тотықсызданады да, ферроформаға айналады:
2Ц хa(Fe ) 2Ц х a(Fe )
+2
2Ц х a3(Fe )
+3
+3
2Цхa3(Fe )
2+
Цха мен Цха3 цитохромоксидаза (ЦХО)
комплексін түзіп, электрондарды Цхс-дан
оттек молекуласына тасымалдайды.
47.
Х. 4 Ферроцха3 молекулалық оттекпенәрекеттесіп,
оны
оттек
ионына
айналдырады. Оттек молекуласының
тотықсыздануы үшін 4 электрон қажет
болғандықтан, оттекпен 4 ферроцха3
әрекеттесуі тиіс:
4Цх а3 (Fe2+)+О2→4Цх а3 (Fe3+)+202ІХ, Х сатыда 102 кДж энергия бөлінеді,
оның 33 кДж 1 АТФ түзуге жұмсалады,
қалғаны жылу түрінде таралады.
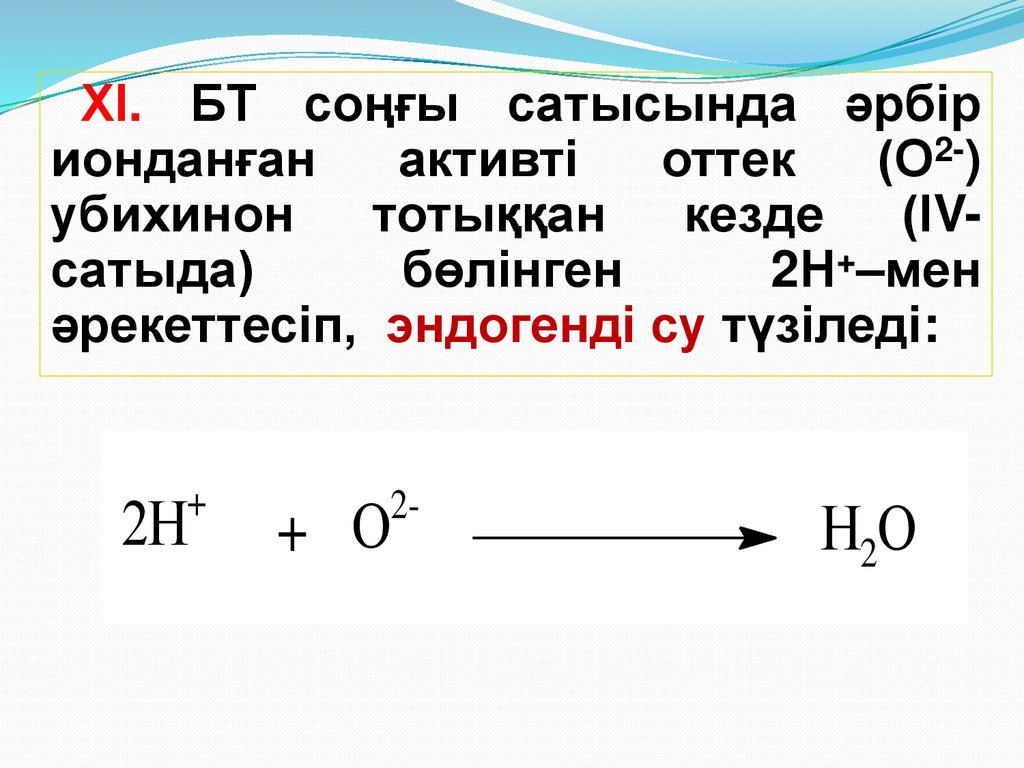
48.
ХІ. БТ соңғы сатысында әрбірионданған
активті
оттек
(О2-)
убихинон
тотыққан
кезде
(ІVсатыда)
бөлінген
2Н+–мен
әрекеттесіп, эндогенді су түзіледі:
2Н
+
+ О
2-
Н2О
49.
Биологиялық тотығу кезінде бөлінгенэнергия тотығу энергиясы
болып
табылады.
Сонымен,
БТ үш сатысында
– НАДН2,
ферроЦхb, ферроЦха мен ферроЦха3
тотыққан кезде АТФ түзуге жеткілікті
энергия бөлінеді. БТ-ң бұл сатыларын
БТ мен ТФ қабысу нүктелері деп
атайды.
50.
4 сатысы. Тотығуданфосфорлану (ТФ )
ТФ – АДФ пен бейорганикалық
фосфаттан БТ энергиясы есебінен
АТФ-ң түзілуі, АТФ-синтетазамен
катализденеді:
АДФ + Н3РО4 + WБТ → АТФ + Н2О
51.
Р/О коэффициенті – тотығуданфосфорлану коэффициентi.
Сіңірілген оттектің әрбір атомына
сәйкес
келетін
бейорганикалық
фосфаттың моль санын (АТФ–тің
түзілуіне
кеткен)
тотығудан
фосфорлану коэффициенті немесе
Р/О коэффициенті деп атайды.
52.
Қалыпты жағдайда:❖Егер субстрат ПФ арқылы тотықса,
Р/О=3.
❖субстрат ФАД тәуелді ФП-мен
тотықса, Р/О=2
53.
БТмен
ТФ
өзара
тығыз
байланысты.
ТФ
БТ-ң
жылдамдығын
бақылайды, мұны тыныс алуды
бақылау деп атайды.
Егер АДФ аз, ал АТФ көп болса,
БТ жылдамдығы төмендейді.
АДФ мөлшері көп, АТФ мөлшері
аз болса, БТ жылдамдығы артады.
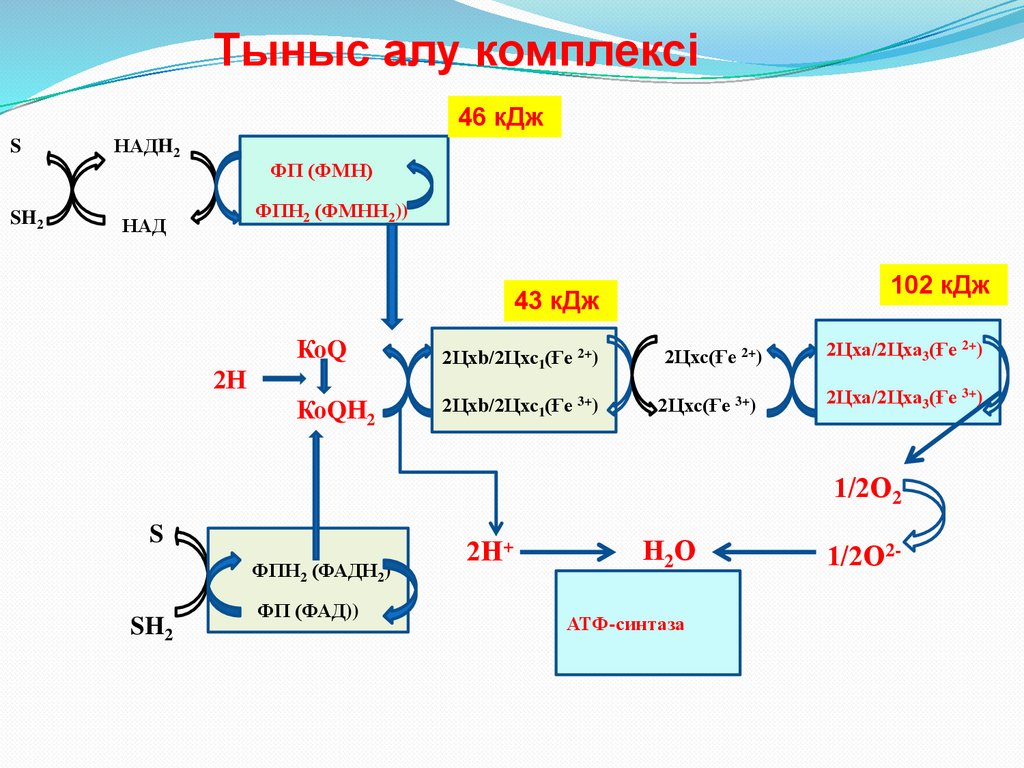
54.
Тыныс алу комплексіБТ-ға қатысатын мембранамен
байланысқан ферменттер митохондрияда
сызықты түрде орналаспайды, олар 5
комплекске біріккен:
І комплекс ФП (ФМН);
ІІ комплекс ФП (ФАД);
ІІІ комплекс – Цхb және Цхс1;
ІV комплекс – Цха және Цха3;
V комплекс – АТФ-синтаза
55.
Тыныс алу комплексінің ферменттеріІ-НАДН-дегидрогеназа (құрамында FеS-
протеин мен ФМН бар)
ІІ-сукцинатдегидрогеназа немесе ацилКоАдегидрогеназа (құрамында FеS-протеин
мен ФАД бар)
ІІІ-КоQ –цитохром с -оксидоредуктаза
(құрамында FеS-протеин бар)
IV-цитохромоксидаза (құрамында 2 мыс
ионы бар)
V-АТФ-синтаза
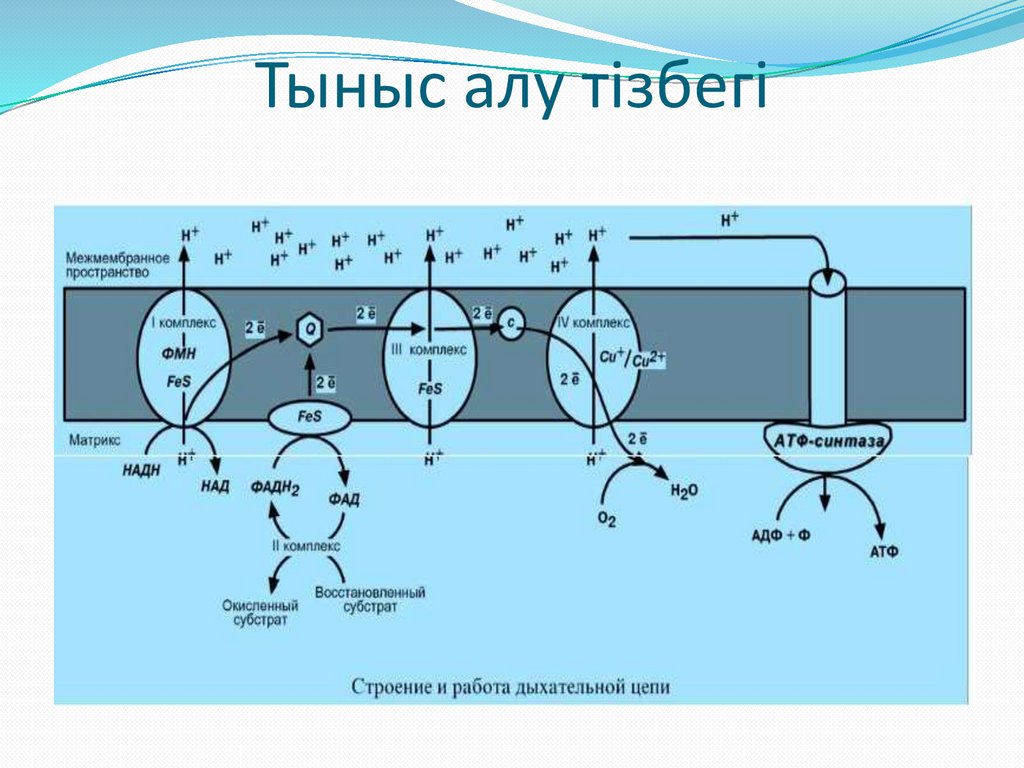
56.
Тыныс алу тізбегі57.
КоQмен
Цхс
еритіндіктен,
фосфолипидтерімен
еркін жылжи алады.
майда
жақсы
мембрана
байланысып,
КоQ І және ІІ комплексті ІІІ
комплекспен, ал
Цхс ІІІ және ІV
комплексті байланыстырады.
58.
Тыныс алу комплексі46 кДж
S
SH2
НАДH2
ФП (ФМН)
ФПН2 (ФМНН2))
НАД
102 кДж
43 кДж
КоQ
2Цхb/2Цхс1(Ғе 2+)
/2Цхс(Ғе 2+)
2Цха/2Цха3(Ғе 2+)
КоQН2
2Цхb/2Цхс1(Ғе 3+)
2Цхс(Ғе 3+)
2Цха/2Цха3(Ғе 3+)
2Н
1/2О2
S
ФПН2 (ФАДН2)
SH2
ФП (ФАД))
2Н+
Н2 О
АТФ-синтаза
1/2О2-
59.
БТ мен ТФ-ңқабысуын
бұзатын
заттарды БТ мен ТФ-ң ажыратқыштары
деп атайды.
Олар:
❖динитрофенол;
❖тироксин;
❖антимицин;
❖билирубин, т.б.
БТ мен ТФ ажырағанда, БТ жүре береді,
бірақ бөлінген энергия АТФ түзілуіне
жұмсалмай, тек жылу түрінде таралады.
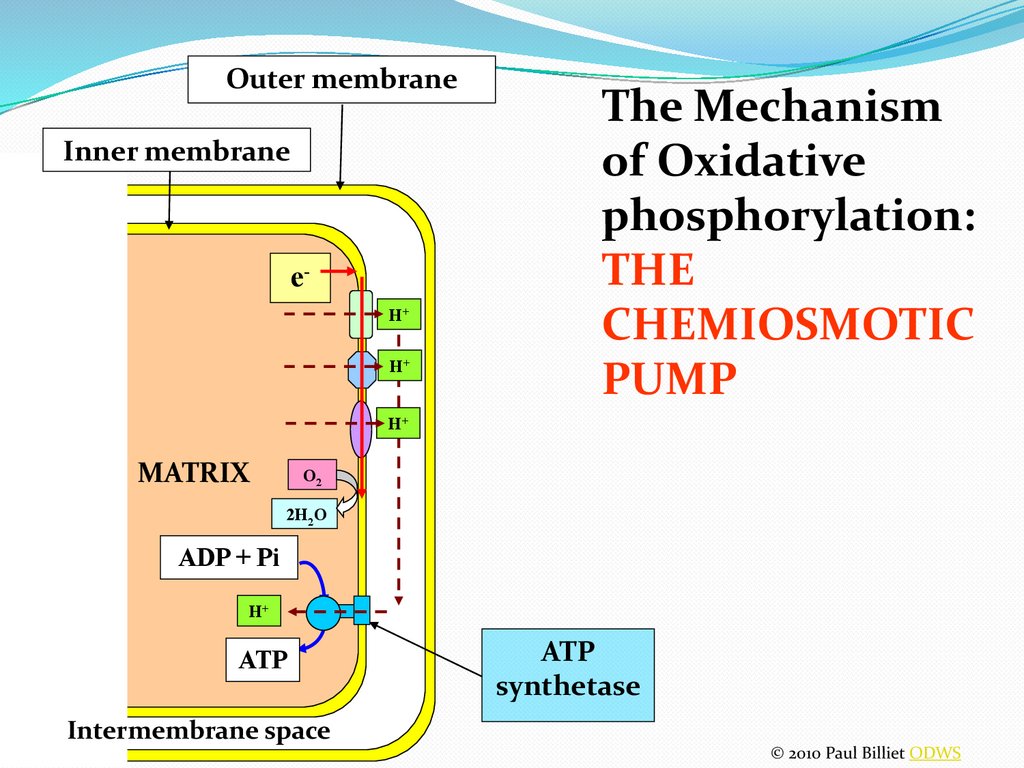
60.
БТ мен ТФ-ң қабысуы қалай жүзегеасады?
1961 жылы Митчелл хемиосмостық
теорияны
ұсынды.
Бұл
теория
бойынша
митохондрияның
ішкі
мембранасындағы протондық насос
арқылы митохондрия матриксінен
протондар ішкі мембрана аралық
кеңістікке тасымалданады.
61.
БТ тізбегінде 2 электрон тасымалданғандаматрикстен мембрана аралық кеңістікке
шамамен 10 протон шығарылады. Ішкі
мембрананың сыртқы жағы – оң, ал ішкі
жағы теріс зарядталады. Ішкі мембранада
пайда болған протондардың
электрохимиялық потенциалының
айырымы АТФ-синтазаның әсер етуіне
әкеледі, яғни АТФ түзіледі.
62.
Outer membraneInner membrane
eH+
H+
The Mechanism
of Oxidative
phosphorylation:
THE
CHEMIOSMOTIC
PUMP
H+
MATRIX
O2
2H2O
ADP + Pi
H+
ATP
ATP
synthetase
Intermembrane space
© 2010 Paul Billiet ODWS
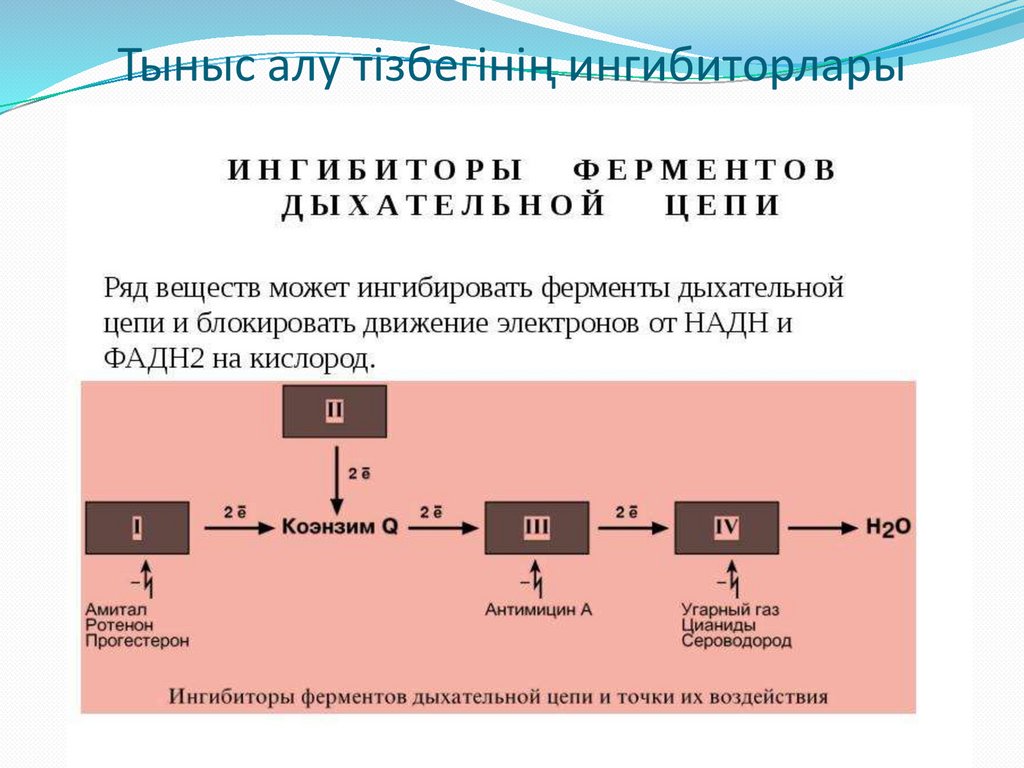
63.
БТ тізбегінің ингибиторларыБарбитураттар (амобарбитал),
пиерицидинА мен ротенон І-ші комплекстен
электрондардың тасымалдануын тежейді.
ІІ-сукцинатдегидрогеназа мен КоQ аралығында
БТ тізбегінің ингибиторлары карбоксин мен
ТТҒА (теноилтрифторацетон)
Малонат – сукцинатдегидрогеназаның
бәсекелес ингибиторы
64.
БТ тізбегінің (БТТ) ингибиторларыДимеркапрол мен антимицин А цитохром b
мен цитохром с арасында БТТ ингибирлейді
H2S, көмір тотығы (СО), цианидтер
цитохромоксидазаның ингибиторлары.
Антибиотик олигомицин тотығудан
фосфорлануды тежейді.
65.
Тыныс алу тізбегінің ингибиторлары66.
БТ мен ТФ ажыратушы заттарАТФ түзілу үшін:
1- митохондрия мембранасының өткізгіштігі
қалыпты болуы керек;
2- мембранада потенциалдың айырымы болуы керек.
БТ мен ТФ ажыратушы заттар: 2,4-динитрофенол
және тироксин (көп мөлшерде болғанда).
2,4-динитрофенол (протонофор) протондарды
мембрана арқылы тасымалдайды, сондықтан
мембранада потенциалдың айырымы пайда
болмайды, АТФ түзілмейді.
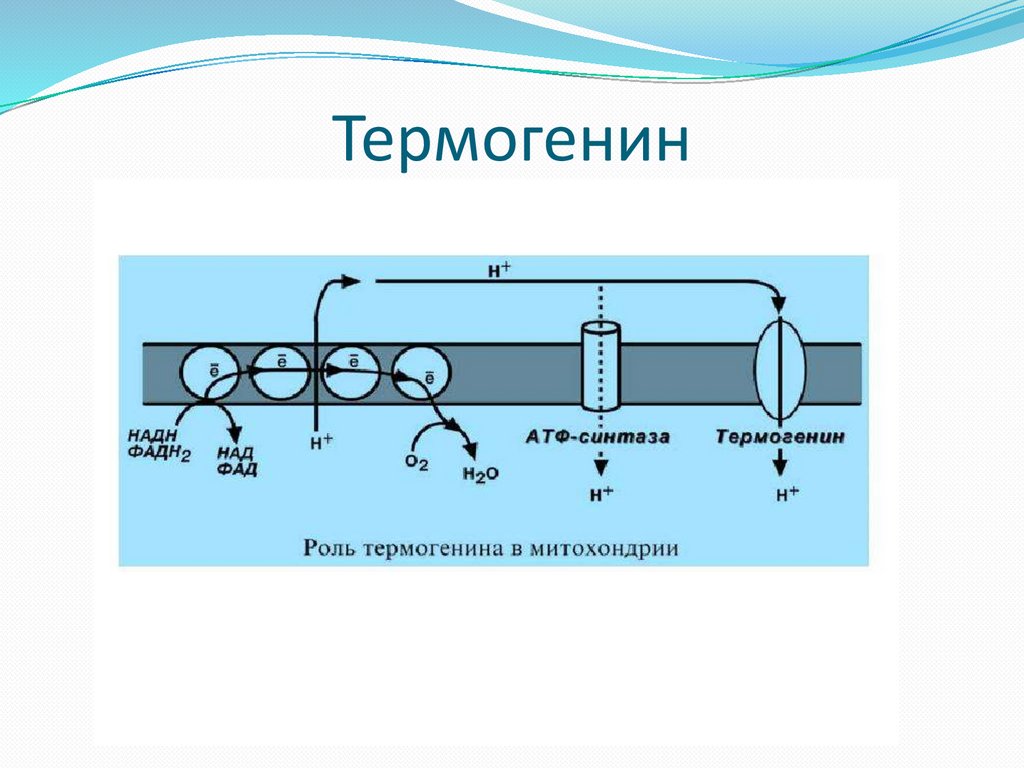
67.
Физиологиялық протонофор “термогенин” дегеннәруыз. Ол қоңыр май тінінде көп болады. Қоңыр
май тінінде митохондриялар көп.
Ағза салқындағанда симпатикалық жүйке жүйесі
арқылы қоңыр май тінінде липолиз артады. БТТ
жұмысы күшейеді, митохондрия мембранасында
потенциалдың айырымы түзіледі.
Митохондрия мембранасында АТФ-синтаза аз,
бірақ термогенин көп болады. Сондықтан АТФ аз
түзіледі, энергия жылу түрінде тарайды.
68.
Термогенин69.
БТ мен ТФ ажыратушы заттарПротонофорға салицилаттар, май қышқылдары,
билирубин, тиреоидты гормондар да жатады.
70.
Сұрақтар1.ҮКЦ-де қанша пиридин ферменттері
тотықсызданады?
2-Қандай фермент тотыққанда сутек атомы протон мен
электронға ыдырайды?
3-Қандай фермент феррицхс1-ді тотықсыздандырады?
4-БТ мен ТФ қабысу нүктелерінде не түзіледі?
5-Тотықсызданған пиридин ферменті тотыққанда қанша
АТФ түзіледі?
71.
ӘДЕБИЕТТЕР:Қазақ тілінде:
1.Северин Е.С. (қазақ тіліне аударған және жауапты
редакторы А.Ж.Сейтембетова) «Биохимия», Мәскеу, 2014.
2. Сеитов З.С. Биологиялық химия, Алматы, 2012 ж.
3. Сейтембетов Т.С., Төлеуов Б.И., Сейтембетова А.Ж..
Биологиялық химия.-Қарағанды, 2007.
4. Тапбергенов С.О. Медициналық биохимия.-Павлодар.2008.
5. Плешкова С.М. және басқалары Биохимияны
студенттердің өздігінен оқып-білуіне арналған оқу құралы
1Бөлім. Белоктар, ферменттер, энергия алмасуы,
витаминдер.
2Бөлім. Заттар алмасуы және оның реттелуі.
3Бөлім. Адам ағзасындағы сұйықтықтар мен тіндер
биохимиясы.– Алматы, 2009 ж.
72.
ӘДЕБИЕТТЕР:Орыс және ағылшын тілдерінде:
1. Северин Е,С. «Биохимия», М.: ГЭОТАР-МЕДИА, 2013г.
2. Сеитов З.С. «Биохимия», Алматы, 2012 г.
3. Harvey, A.Richard Biochemistry [Текст] / Lippincott’s
illustrated Reviews.- Sixth edition.- New Delhi, Philadelphia,
Wolters Kluwer Health, 2014.
4. Harper's Illustrated Biochemistry, 29e, 2012 y.
5. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия
человека. 2003 г.
6. Кольман Я., Рем К-Г. Наглядная биохимия.- М.: Мир, 2004
г.
7. Шарманов Т.Ш., Плешкова С.М. «Метаболические
основы питания с курсом общей биохимии», г. Алматы,
1998г.

















































 biology
biology








