Similar presentations:
Ранняя интенсификация сахароснижающей терапии
1.
Название и вид мероприятияУсиливать нельзя откладывать
Ранняя интенсификация сахароснижающей
терапии
ФИО лектора
Дата мероприятия
Место проведения с указанием точного адреса
Мероприятие организовано при поддержке Представительства ЗАК «АстраЗенека Ю-Кей Лимитед» в РК
Представлена информация в рамках зарегистрированных в РК показаний
Мнение спикера не всегда может совпадать с точкой зрения компании АстраЗенека
Номер одобрения KZ- 3823 дата одобрения: 26.08.2024
дата истечения срока действия:26.08.2025
Лекция предназначена для врачей эндокринологов, терапевтов, ВОП
Т О Л Ь К О Д Л Я В Н У Т Р Е Н Н Е ГО И С П О Л Ь З О В А Н И Я
2.
Раскрытие информации о потенциальном конфликте интересовФ.И.О. Лектора
Должность, ученая степень, место работы
Научные гранты/клинические исследования
Член научного (консультативного) совета,
консультант
Лектор
Сотрудник (в том числе частичная занятость)
3.
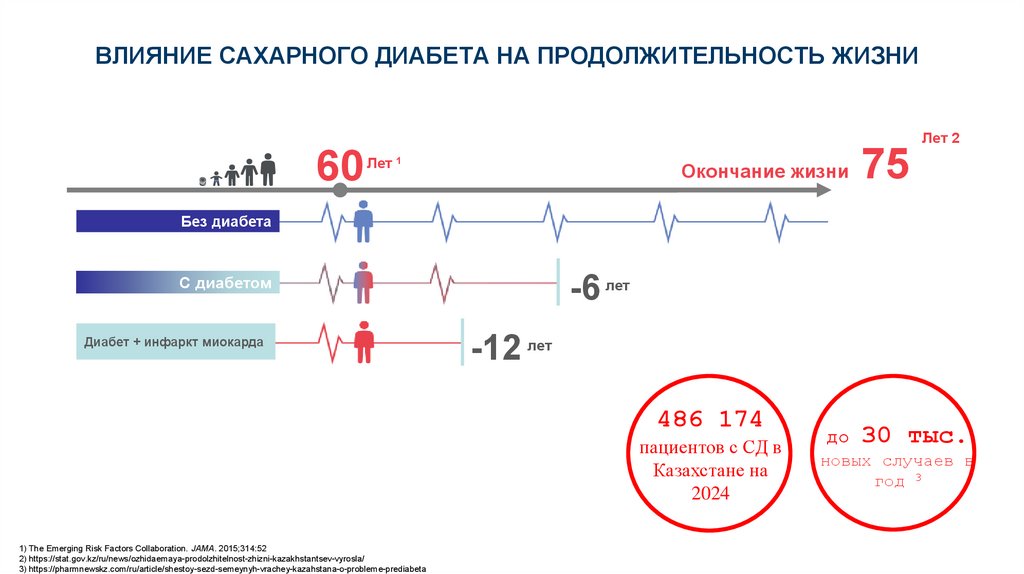
ВЛИЯНИЕ САХАРНОГО ДИАБЕТА НА ПРОДОЛЖИТЕЛЬНОСТЬ ЖИЗНИЛет 2
60
Лет 1
Окончание жизни
75
Без диабета
С диабетом
Диабет + инфаркт миокарда
-6 лет
-12 лет
486 174
пациентов с СД в
Казахстане на
2024
1) The Emerging Risk Factors Collaboration. JAMA. 2015;314:52
2) https://stat.gov.kz/ru/news/ozhidaemaya-prodolzhitelnost-zhizni-kazakhstantsev-vyrosla/
3) https://pharmnewskz.com/ru/article/shestoy-sezd-semeynyh-vrachey-kazahstana-o-probleme-prediabeta
до 30
тыс.
новых случаев в
год 3
4.
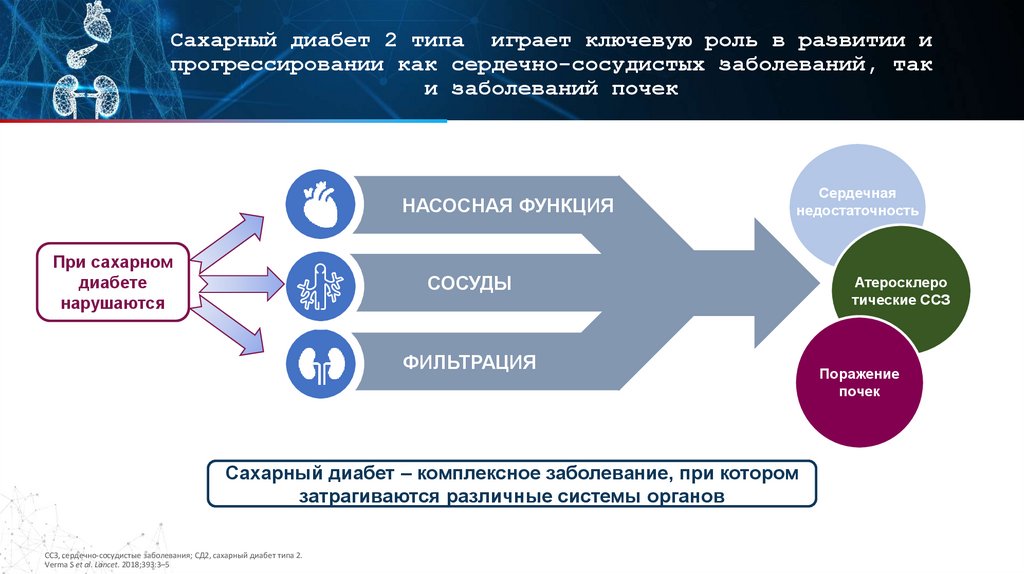
Сахарный диабет 2 типа играет ключевую роль в развитии ипрогрессировании как сердечно-сосудистых заболеваний, так
и заболеваний почек
НАСОСНАЯ ФУНКЦИЯ
При сахарном
диабете
нарушаются
Сердечная
недостаточность
СОСУДЫ
ФИЛЬТРАЦИЯ
Сахарный диабет – комплексное заболевание, при котором
затрагиваются различные системы органов
ССЗ, сердечно-сосудистые заболевания; СД2, сахарный диабет типа 2.
Verma S et al. Lancet. 2018;393:3–5
Атеросклеро
тические ССЗ
Поражение
почек
5.
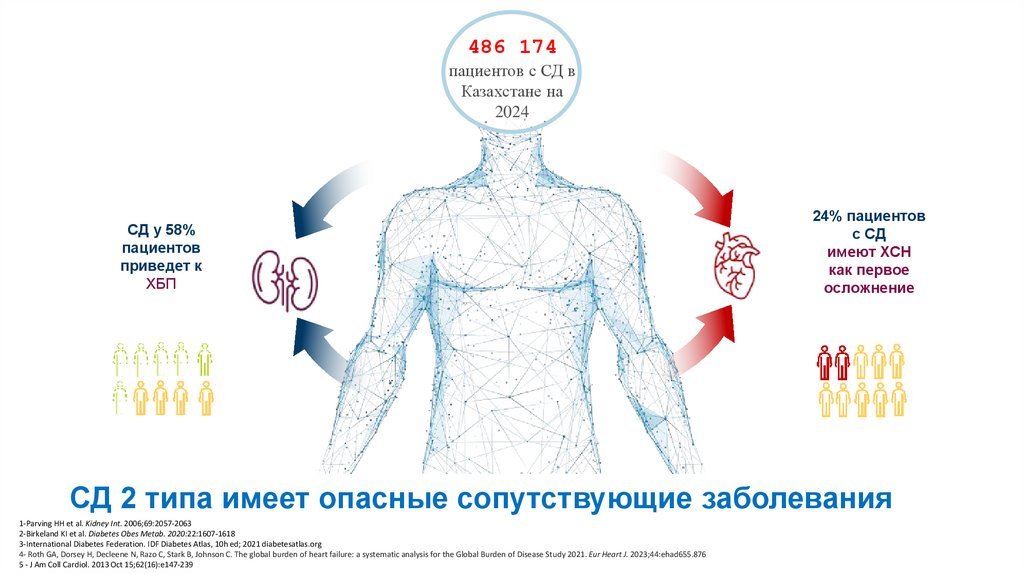
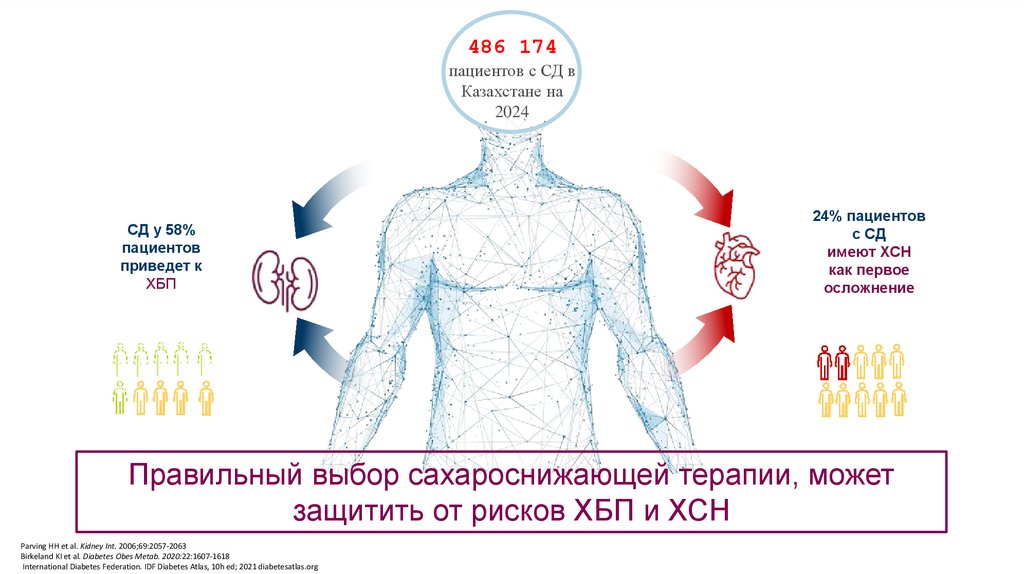
486 174пациентов с СД в
Казахстане на
2024
СД у 58%
пациентов
приведет к
ХБП
24% пациентов
с СД
имеют ХСН
как первое
осложнение
СД 2 типа имеет опасные сопутствующие заболевания
1-Parving HH et al. Kidney Int. 2006;69:2057-2063
2-Birkeland KI et al. Diabetes Obes Metab. 2020:22:1607-1618
3-International Diabetes Federation. IDF Diabetes Atlas, 10h ed; 2021 diabetesatlas.org
4- Roth GA, Dorsey H, Decleene N, Razo C, Stark B, Johnson C. The global burden of heart failure: a systematic analysis for the Global Burden of Disease Study 2021. Eur Heart J. 2023;44:ehad655.876
5 - J Am Coll Cardiol. 2013 Oct 15;62(16):e147-239
6.
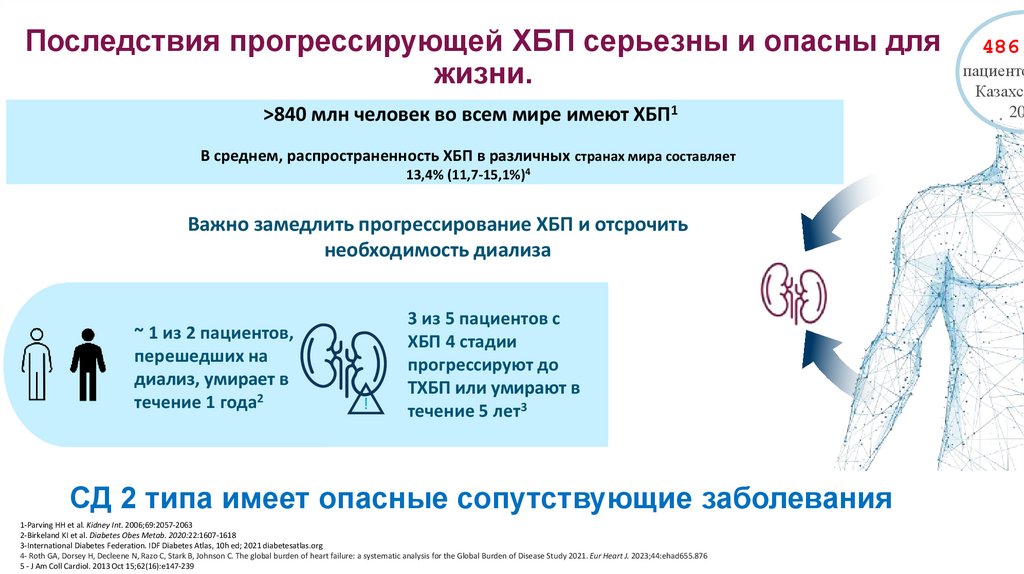
Последствия прогрессирующей ХБП серьезны и опасны дляжизни.
>840 млн человек во всем мире имеют ХБП1
В среднем, распространенность ХБП в различных странах мира составляет
13,4% (11,7-15,1%)4
Важно замедлить прогрессирование ХБП и отсрочить
необходимость диализа
~ 1 из 2 пациентов,
перешедших на
диализ, умирает в
течение 1 года2
!
3 из 5 пациентов с
ХБП 4 стадии
прогрессируют до
ТХБП или умирают в
течение 5 лет3
СД 2 типа имеет опасные сопутствующие заболевания
1-Parving HH et al. Kidney Int. 2006;69:2057-2063
2-Birkeland KI et al. Diabetes Obes Metab. 2020:22:1607-1618
3-International Diabetes Federation. IDF Diabetes Atlas, 10h ed; 2021 diabetesatlas.org
4- Roth GA, Dorsey H, Decleene N, Razo C, Stark B, Johnson C. The global burden of heart failure: a systematic analysis for the Global Burden of Disease Study 2021. Eur Heart J. 2023;44:ehad655.876
5 - J Am Coll Cardiol. 2013 Oct 15;62(16):e147-239
486
пациенто
Казахст
20
7.
174Смертность от сердечной недостаточности только растет
тов с СД в
стане на
024
Более 56.5 млн случаев СН по миру
В среднем распространенность - 96,9 на 100,000 населения 4
После первой госпитализации по поводу СН погибает 5
Каждый
Каждый
Каждый
10
5
2
пациент
пациент
пациент
в течение 30 дней
в течение 1 года
в течение 5 лет
СД 2 типа имеет опасные сопутствующие заболевания
1-Parving HH et al. Kidney Int. 2006;69:2057-2063
2-Birkeland KI et al. Diabetes Obes Metab. 2020:22:1607-1618
3-International Diabetes Federation. IDF Diabetes Atlas, 10h ed; 2021 diabetesatlas.org
4- Roth GA, Dorsey H, Decleene N, Razo C, Stark B, Johnson C. The global burden of heart failure: a systematic analysis for the Global Burden of Disease Study 2021. Eur Heart J. 2023;44:ehad655.876
5 - J Am Coll Cardiol. 2013 Oct 15;62(16):e147-239
8.
486 174пациентов с СД в
Казахстане на
2024
СД у 58%
пациентов
приведет к
ХБП
24% пациентов
с СД
имеют ХСН
как первое
осложнение
Правильный выбор сахароснижающей терапии, может
защитить от рисков ХБП и ХСН
Parving HH et al. Kidney Int. 2006;69:2057-2063
Birkeland KI et al. Diabetes Obes Metab. 2020:22:1607-1618
International Diabetes Federation. IDF Diabetes Atlas, 10h ed; 2021 diabetesatlas.org
9.
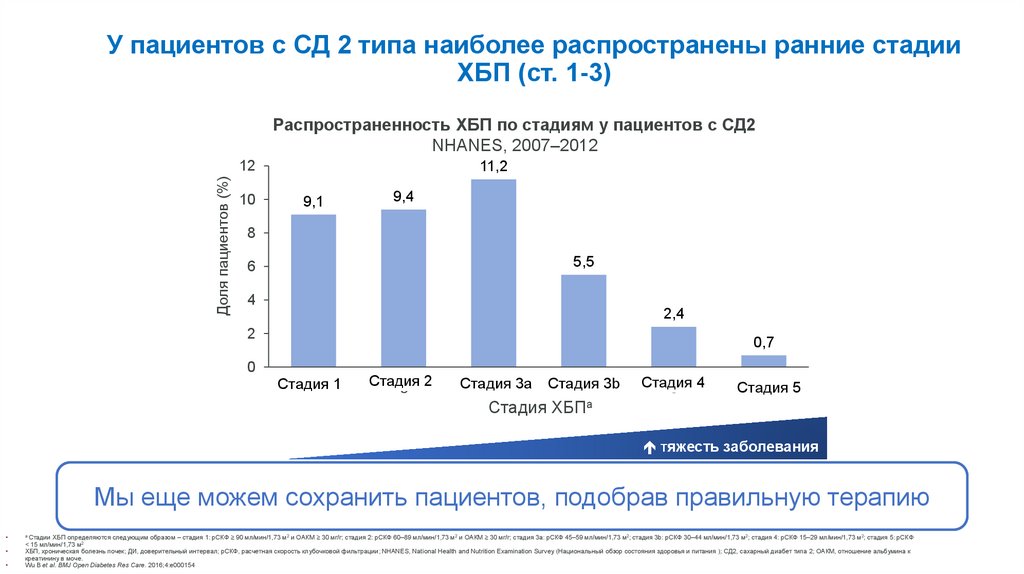
У пациентов с СД 2 типа наиболее распространены ранние стадииХБП (ст. 1-3)
Распространенность ХБП по стадиям у пациентов с СД2
NHANES, 2007–2012
Доля пациентов (%)
12
10
11,2
9,1
9,4
8
5,5
6
4
2,4
2
0,7
0
Стадия
Stage 11
Стадия
Stage 22
Стадия
3а
Stage 3a
Стадия
3b
Stage 3b
Стадия
Stage 44
Stage 5 5
Стадия
Стадия ХБПa
тяжесть заболевания
Мы еще можем сохранить пациентов, подобрав правильную терапию
a Стадии ХБП определяются следующим образом – стадия 1: рСКФ ≥ 90 мл/мин/1,73 м2 и ОАКМ ≥ 30 мг/г; стадия 2: рСКФ 60–89 мл/мин/1,73 м2 и ОАКМ ≥ 30 мг/г; стадия 3a: рСКФ 45–59 мл/мин/1,73 м2; стадия 3b: рСКФ 30–44 мл/мин/1,73 м2; стадия 4: рСКФ 15–29 мл/мин/1,73 м2; стадия 5: рСКФ
< 15 мл/мин/1,73 м2
ХБП, хроническая болезнь почек; ДИ, доверительный интервал; рСКФ, расчетная скорость клубочковой фильтрации; NHANES, National Health and Nutrition Examination Survey (Национальный обзор состояния здоровья и питания ); СД2, сахарный диабет типа 2; ОАКМ, отношение альбумина к
креатинину в моче.
Wu B et al. BMJ Open Diabetes Res Care. 2016;4:e000154
10.
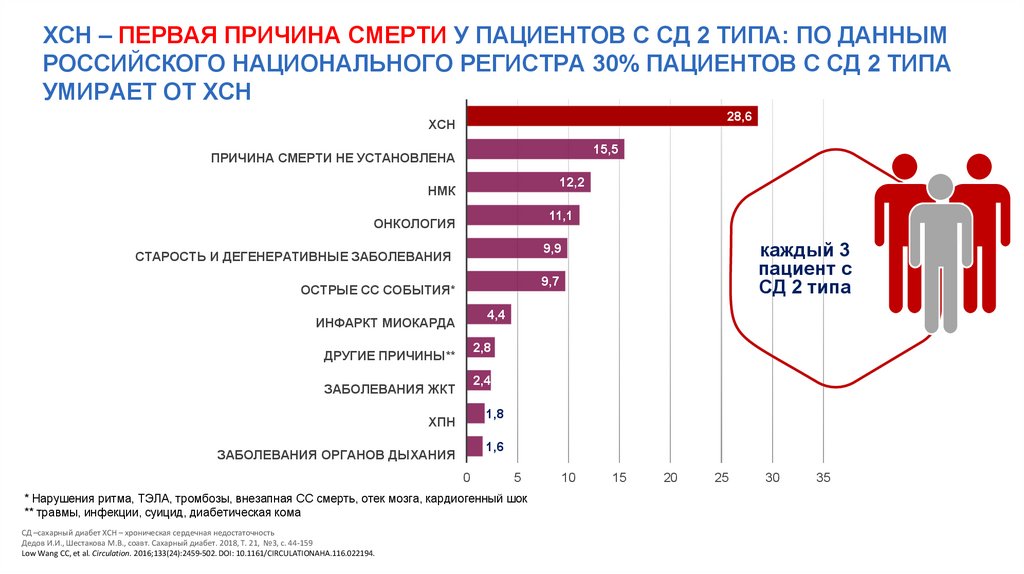
ХСН – ПЕРВАЯ ПРИЧИНА СМЕРТИ У ПАЦИЕНТОВ С СД 2 ТИПА: ПО ДАННЫМРОССИЙСКОГО НАЦИОНАЛЬНОГО РЕГИСТРА 30% ПАЦИЕНТОВ С СД 2 ТИПА
УМИРАЕТ ОТ ХСН
28,6
ХСН
15,5
ПРИЧИНА СМЕРТИ НЕ УСТАНОВЛЕНА
12,2
НМК
11,1
ОНКОЛОГИЯ
СТАРОСТЬ И ДЕГЕНЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ
9,9
ОСТРЫЕ СС СОБЫТИЯ*
9,7
4,4
ИНФАРКТ МИОКАРДА
ДРУГИЕ ПРИЧИНЫ**
2,8
ЗАБОЛЕВАНИЯ ЖКТ
2,4
ХПН
1,8
ЗАБОЛЕВАНИЯ ОРГАНОВ ДЫХАНИЯ
1,6
0
5
* Нарушения ритма, ТЭЛА, тромбозы, внезапная СС смерть, отек мозга, кардиогенный шок
** травмы, инфекции, суицид, диабетическая кома
СД –сахарный диабет ХСН – хроническая сердечная недостаточность
Дедов И.И., Шестакова М.В., соавт. Сахарный диабет. 2018, Т. 21, №3, с. 44-159
Low Wang CC, et al. Circulation. 2016;133(24):2459-502. DOI: 10.1161/CIRCULATIONAHA.116.022194.
каждый 3
пациент с
СД 2 типа
10
15
20
25
30
35
11.
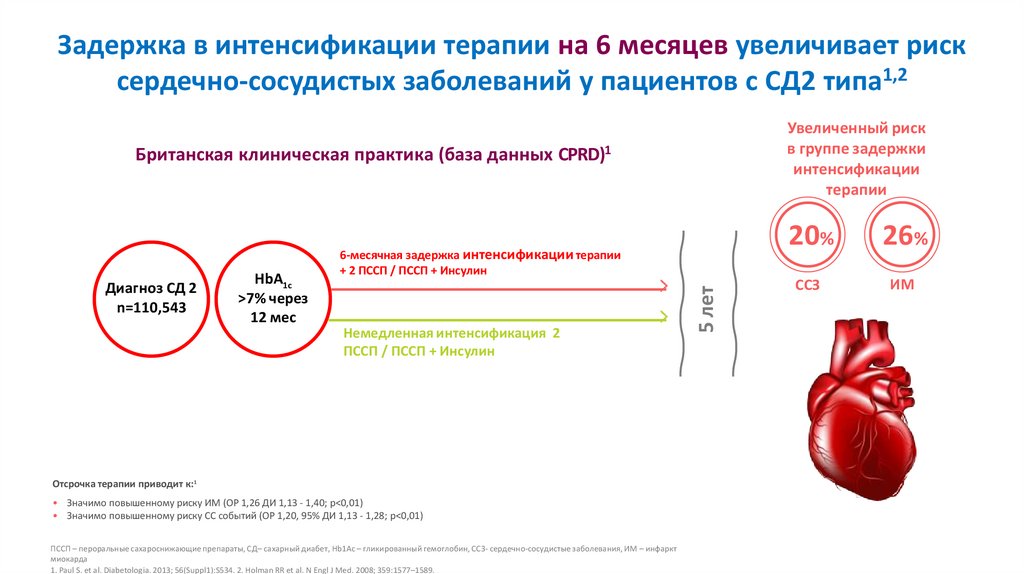
Задержка в интенсификации терапии на 6 месяцев увеличивает рисксердечно-сосудистых заболеваний у пациентов с СД2 типа1,2
Увеличенный риск
в группе задержки
интенсификации
терапии
Британская клиническая практика (база данных CPRD)1
HbA1c
>7% через
12 мес
Немедленная интенсификация 2
ПССП / ПССП + Инсулин
Отсрочка терапии приводит к:1
• Значимо повышенному риску ИМ (ОР 1,26 ДИ 1,13 - 1,40; p<0,01)
• Значимо повышенному риску СС событий (ОР 1,20, 95% ДИ 1,13 - 1,28; p<0,01)
ПССП – пероральные сахароснижающие препараты, СД– сахарный диабет, Hb1Ac – гликированный гемоглобин, ССЗ- сердечно-сосудистые заболевания, ИМ – инфаркт
миокарда
1. Paul S. et al. Diabetologia. 2013; 56(Suppl1):S534. 2. Holman RR et al. N Engl J Med. 2008; 359:1577–1589.
5 лет
Диагноз СД 2
n=110,543
6-месячная задержка интенсификации терапии
+ 2 ПССП / ПССП + Инсулин
20%
26%
ССЗ
ИМ
12.
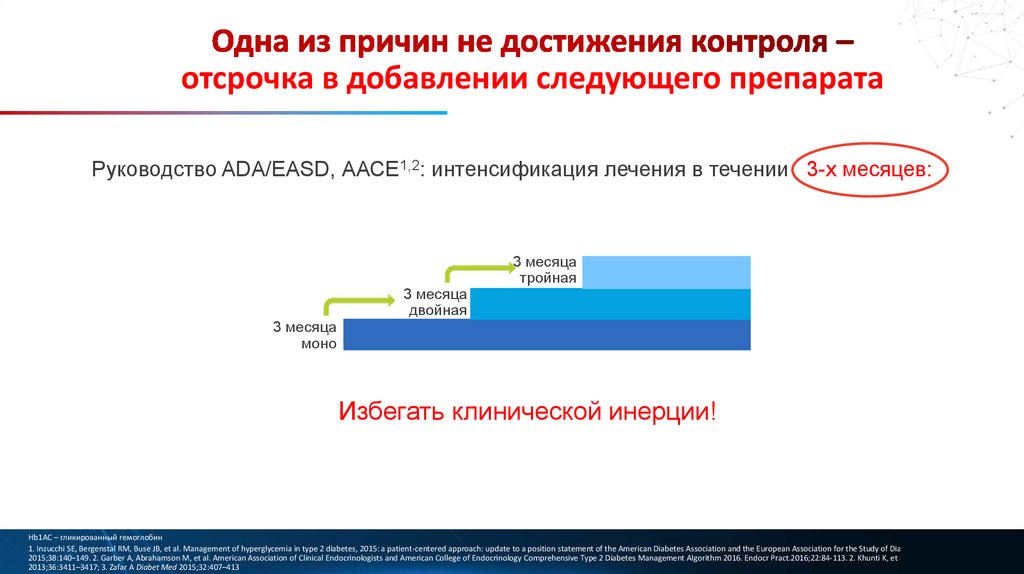
отсрочка в добавлении следующего препаратаРуководство ADA/EASD, ААСЕ1,2: интенсификация лечения в течении 3-x месяцев:
3 месяца
двойная
3 месяца
тройная
3 месяца
моно
Избегать клинической инерции!
Hb1AC – гликированный гемоглобин
1. Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of hyperglycemia in type 2 diabetes, 2015: a patient-centered approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care
2015;38:140–149. 2. Garber A, Abrahamson M, et al. American Association of Clinical Endocrinologists and American College of Endocrinology Comprehensive Type 2 Diabetes Management Algorithm 2016. Endocr Pract.2016;22:84-113. 2. Khunti K, et al. Diabetes Care
2013;36:3411–3417; 3. Zafar A Diabet Med 2015;32:407–413
13.
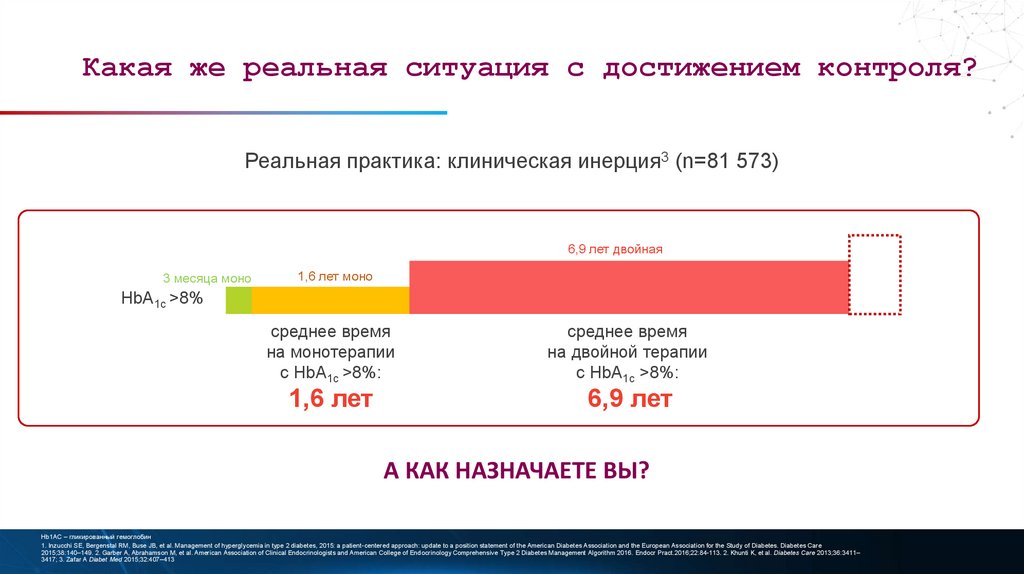
Какая же реальная ситуация с достижением контроля?Реальная практика: клиническая инерция3 (n=81 573)
6,9 лет двойная
3 месяца моно
1,6 лет моно
HbA1c >8%
среднее время
на монотерапии
с HbA1c >8%:
1,6 лет
среднее время
на двойной терапии
с HbA1c >8%:
6,9 лет
А КАК НАЗНАЧАЕТЕ ВЫ?
Hb1AC – гликированный гемоглобин
1. Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of hyperglycemia in type 2 diabetes, 2015: a patient-centered approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care
2015;38:140–149. 2. Garber A, Abrahamson M, et al. American Association of Clinical Endocrinologists and American College of Endocrinology Comprehensive Type 2 Diabetes Management Algorithm 2016. Endocr Pract.2016;22:84-113. 2. Khunti K, et al. Diabetes Care 2013;36:3411–
3417; 3. Zafar A Diabet Med 2015;32:407–413
14.
У вас есть такие пациенты?Хочу увидеть
свадьбу дочери
Отпраздновать
юбилей
Поддержать
внука на
первом звонке
HbA1c 7,5%
61 год
ХБП 3а, А2.
АД 150/90 мм рт. ст.
ИМТ 30 кг/м2
Получает МЕТ 0,5 года
HbA1c 7,8%
57 лет
СКФ 93 мл/мин
ИМТ 31 кг/м2
АД 140/90 мм рт.ст.
Недавно выявленный
пациент
HbA1c 7,9%
63 лет
ИБС: стенокардия напряжения 2 ФК
АД 150/90 мм рт ст
ИМТ 35 кг/м2
Получает МЕТ 1 год
*Гипотетические профили пациентов
HbA1c – гликированный гемоглобин, МЕТ – метформин, ХБП – хроническая болезнь почек, АД – артериальная гипертензия, ИМТ –индекс массы тела, МЕТ –метформин, СКФ – скорость клубочковой фильтрации, СД- сахарный диабет, ИБС – ишемическая болезнь сердца
15.
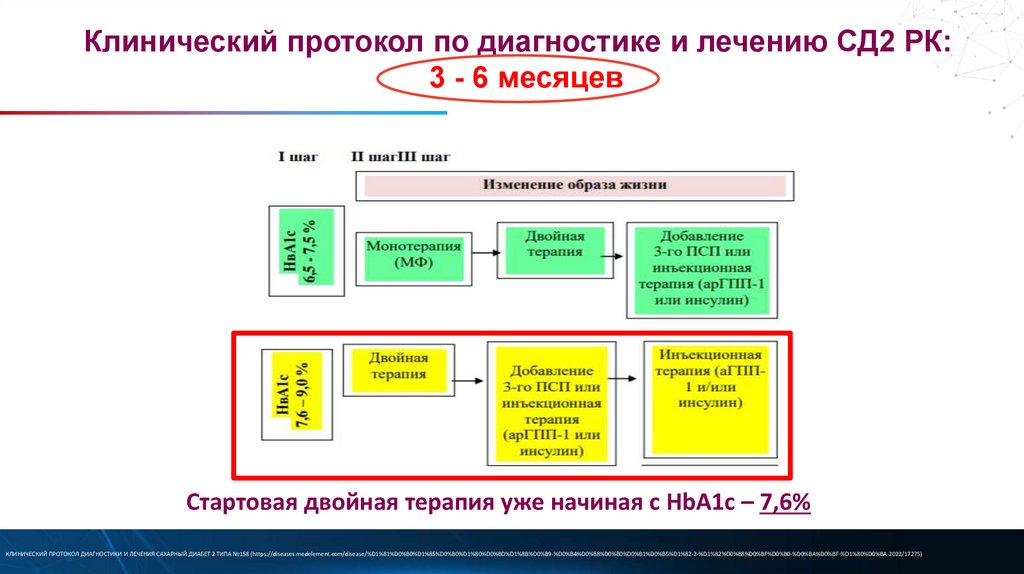
Клинический протокол по диагностике и лечению СД2 РК:3 - 6 месяцев
Стартовая двойная терапия уже начиная с HbA1c – 7,6%
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ САХАРНЫЙ ДИАБЕТ 2 ТИПА №158 (https://diseases.medelement.com/disease/%D1%81%D0%B0%D1%85%D0%B0%D1%80%D0%BD%D1%8B%D0%B9-%D0%B4%D0%B8%D0%B0%D0%B1%D0%B5%D1%82-2-%D1%82%D0%B8%D0%BF%D0%B0-%D0%BA%D0%BF-%D1%80%D0%BA-2022/17275)
16.
Какой класс ПССП выбрать для интенсификации?иНГЛТ-2
СМ
иДПП-4
Эффективность
Не вызывает
гипогликемию
Не повышает
массу тела
Риск гСН
- положительное влияние
Влияние на почки
- нейтральное влияние
- отрицательное влияние
иНГЛТ-2 – единственный класс ПССП, обеспечивающий защиту от рисков ССЗ и ХБП,
не вызывая гипогликемию*
* - среди ПССП путем сравнения ОХЛП (http://register.ndda.kz/category/search_prep)
ПССП –пероральные сахаропонижающие препараты, пСМ – производные сульфонил мочевины, иДПП-4 – ингибиторы дипептидил пептидазы -4, гСН – госпитализация по сердечной недостаточности, иНГЛТ-2 – ингибитор натрий-глюкозного транспортера-2, ССЗ –сердечно-сосудистые заболевания, ХБП – хроническая болезнь почек,
ХСН – хроническая сердечная недостаточность
Inzucchi S, et al. Diabetologia 2015;58:429–442
17.
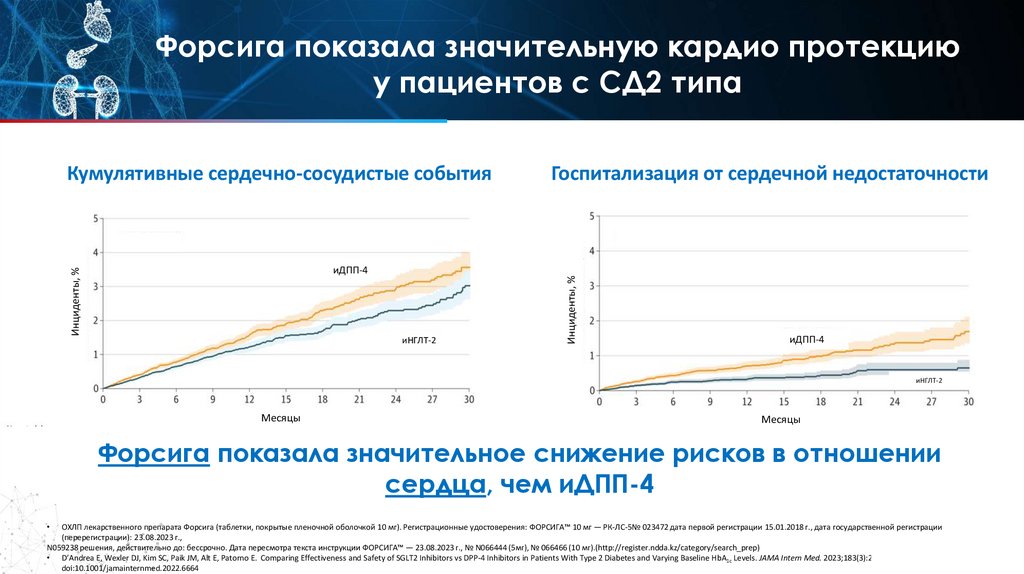
Форсига показала значительную кардио протекциюу пациентов с СД2 типа
Инциденты, %
иДПП-4
иНГЛТ-2
Госпитализация от сердечной недостаточности
Инциденты, %
Кумулятивные сердечно-сосудистые события
иДПП-4
иНГЛТ-2
Месяцы
Месяцы
Форсига показала значительное снижение рисков в отношении
сердца, чем иДПП-4
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации
(перерегистрации): 23.08.2023 г.,
N059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
• D’Andrea E, Wexler DJ, Kim SC, Paik JM, Alt E, Patorno E. Comparing Effectiveness and Safety of SGLT2 Inhibitors vs DPP-4 Inhibitors in Patients With Type 2 Diabetes and Varying Baseline HbA1c Levels. JAMA Intern Med. 2023;183(3):242–254.
doi:10.1001/jamainternmed.2022.6664
18.
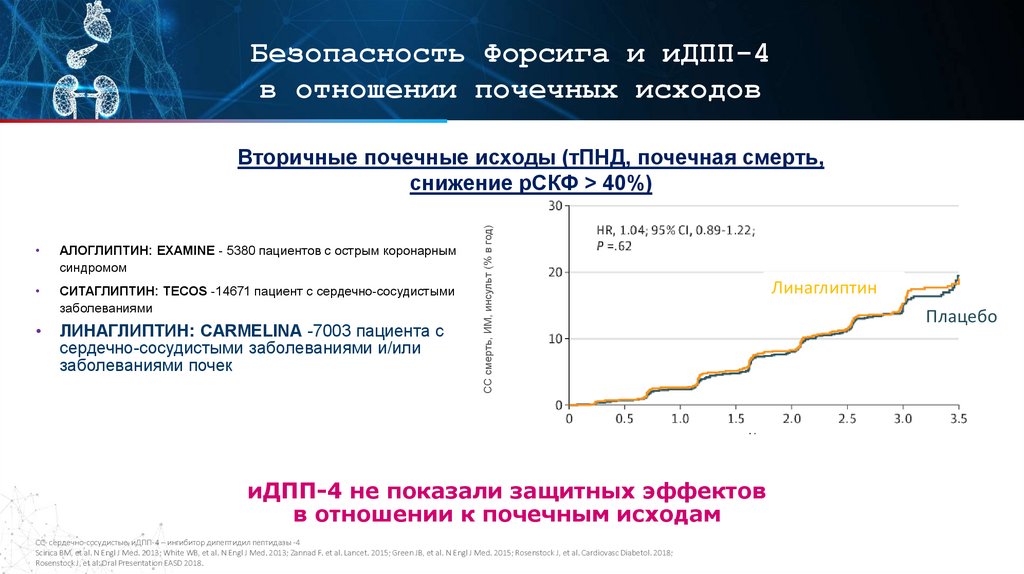
Безопасность Форсига и иДПП-4в отношении почечных исходов
АЛОГЛИПТИН: EXAMINE - 5380 пациентов с острым коронарным
синдромом
СИТАГЛИПТИН: TECOS -14671 пациент с сердечно-сосудистыми
заболеваниями
ЛИНАГЛИПТИН: CARMELINA -7003 пациента с
сердечно-сосудистыми заболеваниями и/или
заболеваниями почек
СС смерть, ИМ, инсульт (% в год)
Вторичные почечные исходы (тПНД, почечная смерть,
снижение рСКФ > 40%)
иДПП-4 не показали защитных эффектов
в отношении к почечным исходам
СС- сердечно-сосудистые, иДПП-4 – ингибитор дипептидил пептидазы -4
Scirica BM, et al. N Engl J Med. 2013; White WB, et al. N Engl J Med. 2013; Zannad F. et al. Lancet. 2015; Green JB, et al. N Engl J Med. 2015; Rosenstock J, et al. Cardiovasc Diabetol. 2018;
Rosenstock J, et al. Oral Presentation EASD 2018.
Линаглиптин
Плацебо
19.
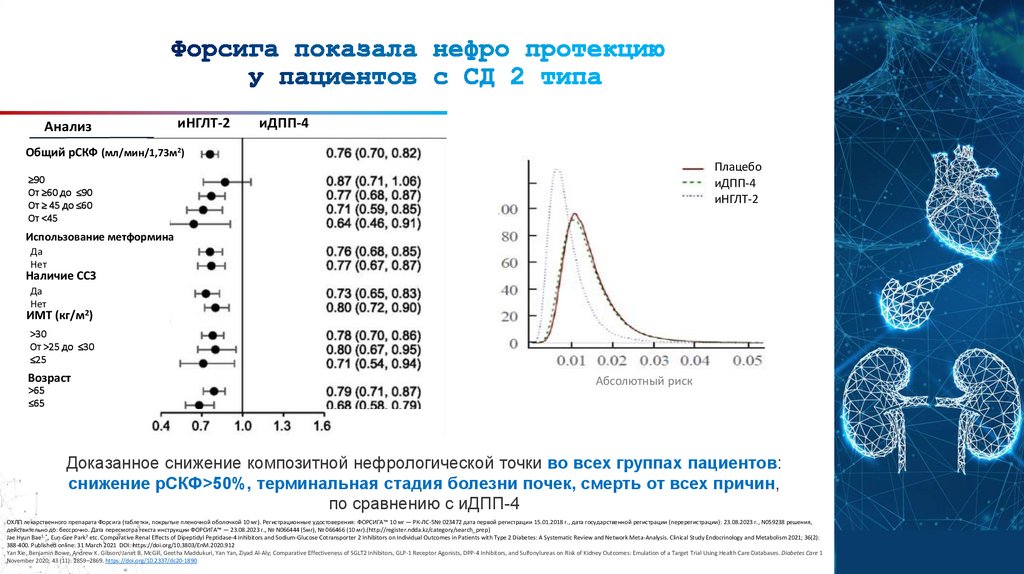
АнализиНГЛТ-2
иДПП-4
Общий рСКФ (мл/мин/1,73м2)
Плацебо
иДПП-4
иНГЛТ-2
≥90
От ≥60 до ≤90
От ≥ 45 до ≤60
От <45
Использование метформина
Да
Нет
Наличие ССЗ
Да
Нет
ИМТ (кг/м2)
>30
От >25 до ≤30
≤25
Возраст
>65
≤65
Абсолютный риск
Доказанное снижение композитной нефрологической точки во всех группах пациентов:
снижение рСКФ>50%, терминальная стадия болезни почек, смерть от всех причин,
по сравнению с иДПП-4
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023 г., N059238 решения,
действительно до: бессрочно. Дата пересмотра текста инструкции ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
Jae Hyun Bae1, *, Eun-Gee Park2 etc. Comparative Renal Effects of Dipeptidyl Peptidase-4 Inhibitors and Sodium-Glucose Cotransporter 2 Inhibitors on Individual Outcomes in Patients with Type 2 Diabetes: A Systematic Review and Network Meta-Analysis. Clinical Study Endocrinology and Metabolism 2021; 36(2):
388-400. Published online: 31 March 2021 DOI: https://doi.org/10.3803/EnM.2020.912
Yan Xie, Benjamin Bowe, Andrew K. Gibson, Janet B. McGill, Geetha Maddukuri, Yan Yan, Ziyad Al-Aly; Comparative Effectiveness of SGLT2 Inhibitors, GLP-1 Receptor Agonists, DPP-4 Inhibitors, and Sulfonylureas on Risk of Kidney Outcomes: Emulation of a Target Trial Using Health Care Databases. Diabetes Care 1
November 2020; 43 (11): 2859–2869. https://doi.org/10.2337/dc20-1890
20.
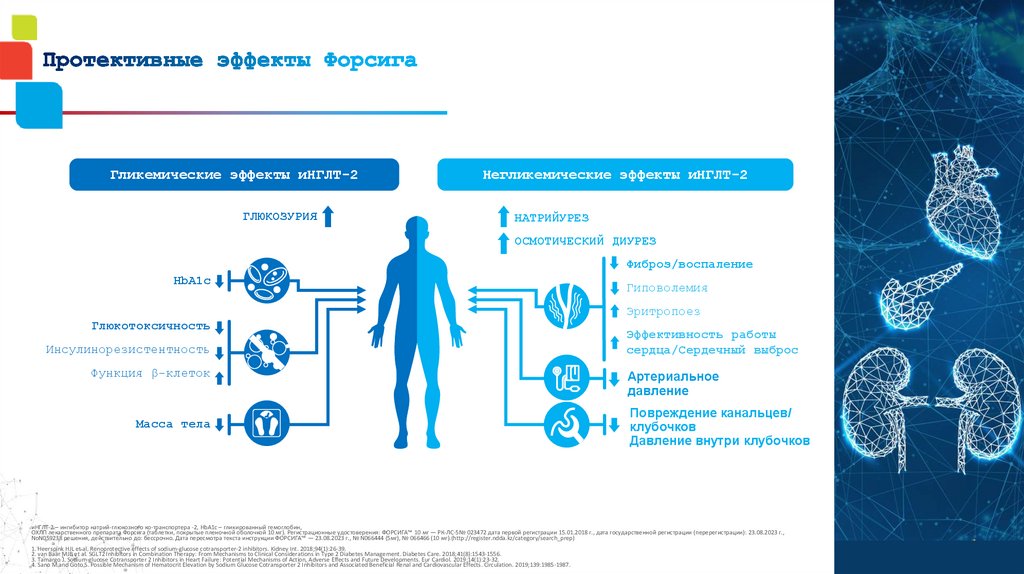
Гликемические эффекты иНГЛТ-2ГЛЮКОЗУРИЯ
Негликемические эффекты иНГЛТ-2
НАТРИЙУРЕЗ
ОСМОТИЧЕСКИЙ ДИУРЕЗ
Фиброз/воспаление
HbA1c
Гиповолемия
Эритропоез
Глюкотоксичность
Инсулинорезистентность
Функция β-клеток
Масса тела
Эффективность работы
сердца/Сердечный выброс
Артериальное
давление
Повреждение канальцев/
клубочков
Давление внутри клубочков
иНГЛТ-2 – ингибитор натрий-глюкозного ко-транспортера -2, HbA1c – гликированный гемоглобин,
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023 г.,
NoN059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
1. Heerspink HJL et al. Renoprotective effects of sodium-glucose cotransporter-2 inhibitors. Kidney Int. 2018;94(1):26-39.
2. van Baar MJB et al. SGLT2 Inhibitors in Combination Therapy: From Mechanisms to Clinical Considerations in Type 2 Diabetes Management. Diabetes Care. 2018;41(8):1543-1556.
3. Tamargo J. Sodium-glucose Cotransporter 2 Inhibitors in Heart Failure: Potential Mechanisms of Action, Adverse Effects and Future Developments. Eur Cardiol. 2019;14(1):23-32.
4. Sano M and Goto S. Possible Mechanism of Hematocrit Elevation by Sodium Glucose Cotransporter 2 Inhibitors and Associated Beneficial Renal and Cardiovascular Effects. Circulation. 2019;139:1985-1987.
21.
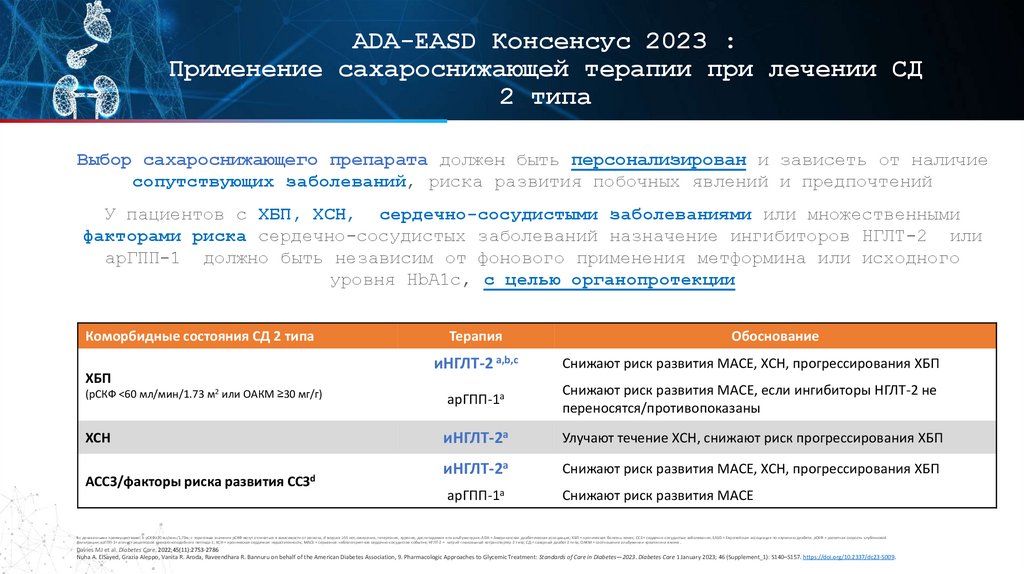
ADA-EASD Консенсус 2023 :Применение сахароснижающей терапии при лечении СД
2 типа
Выбор сахароснижающего препарата должен быть персонализирован и зависеть от наличие
сопутствующих заболеваний, риска развития побочных явлений и предпочтений
У пациентов с ХБП, ХСН, сердечно-сосудистыми заболеваниями или множественными
факторами риска сердечно-сосудистых заболеваний назначение ингибиторов НГЛТ-2 или
арГПП-1 должно быть независим от фонового применения метформина или исходного
уровня HbA1c, с целью органопротекции
Коморбидные состояния СД 2 типа
Терапия
Обоснование
иНГЛТ-2 a,b,c
Снижают риск развития МАСЕ, ХСН, прогрессирования ХБП
(рСКФ <60 мл/мин/1.73 м2 или ОАКМ ≥30 мг/г)
арГПП-1a
Снижают риск развития MACE, если ингибиторы НГЛТ-2 не
переносятся/противопоказаны
ХСН
иНГЛТ-2a
Улучают течение ХСН, снижают риск прогрессирования ХБП
иНГЛТ-2a
Снижают риск развития МАСЕ, ХСН, прогрессирования ХБП
арГПП-1a
Снижают риск развития МАСЕ
ХБП
АССЗ/факторы риска развития ССЗd
а с доказанными преимуществами; b рСКФ≥20 мл/мин/1,73м; с пороговые значения рСКФ могут отличаться в зависимости от региона, d возраст ≥55 лет, ожирение, гипертония, курение, дислипидемия или альбуминурия. ADA = Американская диабетическая ассоциация; ХБП = хроническая болезнь почек; ССЗ = сердечно-сосудистые заболевания; EASD = Европейская ассоциация по изучению диабета; рСКФ = расчетная скорость клубочковой
фильтрации; арГПП-1= агонист рецепторов глюкагоноподобного пептида-1; ХСН = хроническая сердечная недостаточность; MACE = серьезное неблагоприятное сердечно-сосудистое событие; НГЛТ-2 = натрий-глюкозыный котранспортер 2 типа; СД = сахарный диабет 2 типа; ОАКМ = соотношение альбумина и креатинина в моче .
Davies MJ et al. Diabetes Care. 2022;45(11):2753-2786
Nuha A. ElSayed, Grazia Aleppo, Vanita R. Aroda, Raveendhara R. Bannuru on behalf of the American Diabetes Association, 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes—2023. Diabetes Care 1 January 2023; 46 (Supplement_1): S140–S157. https://doi.org/10.2337/dc23-S009.
22.
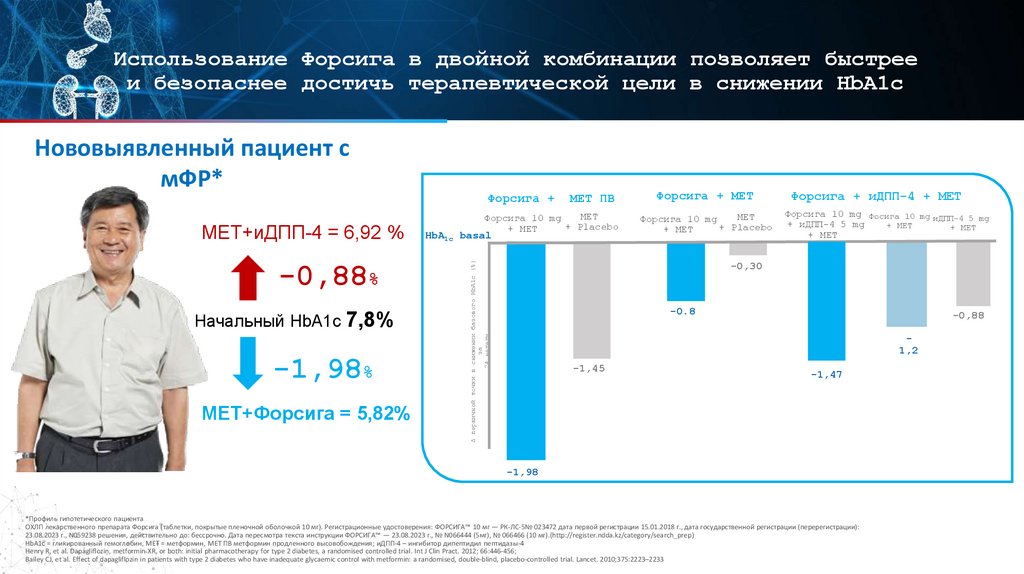
Использование Форсига в двойной комбинации позволяет быстрееи безопаснее достичь терапевтической цели в снижении HbA1c
МЕТ+иДПП-4 = 6,92 %
-0,88%
Начальный HbA1c 7,8%
-1,98%
МЕТ+Форсига = 5,82%
Форсига +
MET ПВ
MET
Форсига 10 mg
+ Placebo
+ MET
HbA1c basal
Δ первичной точки в снижении базового HbA1c (%)
за
24 недели
Нововыявленный пациент с
мФР*
Форсига + МЕТ
MET
Форсига 10 mg
+ Placebo
+ MET
Форсига + иДПП-4 + MET
Форсига 10 mg Фосига 10 mg иДПП-4 5 mg
+ иДПП-4 5 mg
+ МЕТ
+ МЕТ
+ МЕТ
-0,30
-0.8
-0,88
1,2
-1,45
-1,47
-1,98
*Профиль гипотетического пациента
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации):
23.08.2023 г., N059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
HbA1c = гликированный гемоглобин, MET = метформин, MET ПВ метформин продленного высовобождения; иДПП-4 – ингибитор дипептидил пептидазы-4
Henry R, et al. Dapagliflozin, metformin XR, or both: initial pharmacotherapy for type 2 diabetes, a randomised controlled trial. Int J Clin Pract. 2012; 66:446-456;
Bailey CJ, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with metformin: a randomised, double-blind, placebo-controlled trial. Lancet. 2010;375:2223–2233
23.
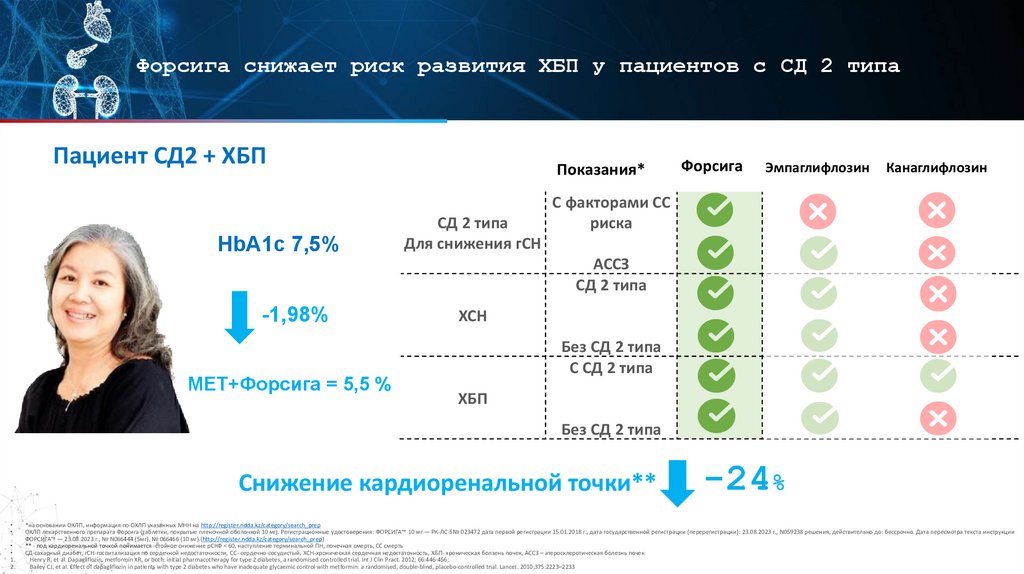
Форсига снижает риск развития ХБП у пациентов с СД 2 типаПациент СД2 + ХБП
HbA1c 7,5%
Показания*
СД 2 типа
Для снижения гСН
Форсига
Эмпаглифлозин
Канаглифлозин
С факторами СС
риска
АССЗ
СД 2 типа
2,6%
*HbA1c
basal> 9%
-1,98%
МЕТ+Форсига = 5,5 %
ХСН
Без СД 2 типа
С СД 2 типа
ХБП
Без СД 2 типа
Снижение кардиоренальной точки**
1.
2.
-24%
*на основании ОХЛП, информация по ОХЛП указанных МНН на http://register.ndda.kz/category/search_prep
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023 г., N059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции
ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
** - под кардиоренальной точкой понимается -стойкое снижение рСКФ < 60, наступление терминальной ПН, почечная смерть, СС смерть
СД-сахарный диабет, гСН-госпитализация по сердечной недостаточности, СС- сердечно-сосудистый, ХСН-хроническая сердечная недостаточность, ХБП- хроническая болзень почек, АССЗ – атеросклеротическая болезнь почек
Henry R, et al. Dapagliflozin, metformin XR, or both: initial pharmacotherapy for type 2 diabetes, a randomised controlled trial. Int J Clin Pract. 2012; 66:446-456;
Bailey CJ, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with metformin: a randomised, double-blind, placebo-controlled trial. Lancet. 2010;375:2223–2233
24.
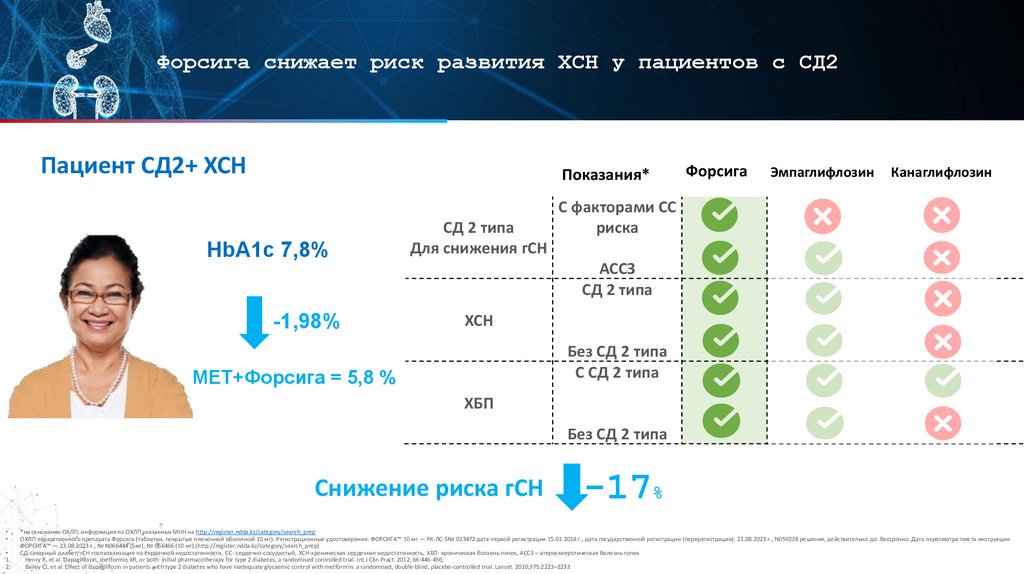
Форсига снижает риск развития ХСН у пациентов с СД2Пациент СД2+ ХСН
Показания*
HbA1c 7,8%
2,6%
*HbA1c
basal> 9%
-1,98%
СД 2 типа
Для снижения гСН
Форсига
Эмпаглифлозин
Канаглифлозин
С факторами СС
риска
АССЗ
СД 2 типа
ХСН
Без СД 2 типа
С СД 2 типа
МЕТ+Форсига = 5,8 %
ХБП
Без СД 2 типа
Снижение риска гСН
1.
2.
-17%
*на основании ОХЛП, информация по ОХЛП указанных МНН на http://register.ndda.kz/category/search_prep
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023 г., N059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции
ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
СД-сахарный диабет, гСН-госпитализация по сердечной недостаточности, СС- сердечно-сосудистый, ХСН-хроническая сердечная недостаточность, ХБП- хроническая болзень почек, АССЗ – атеросклеротическая болезнь почек
Henry R, et al. Dapagliflozin, metformin XR, or both: initial pharmacotherapy for type 2 diabetes, a randomised controlled trial. Int J Clin Pract. 2012; 66:446-456;
Bailey CJ, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with metformin: a randomised, double-blind, placebo-controlled trial. Lancet. 2010;375:2223–2233
25.
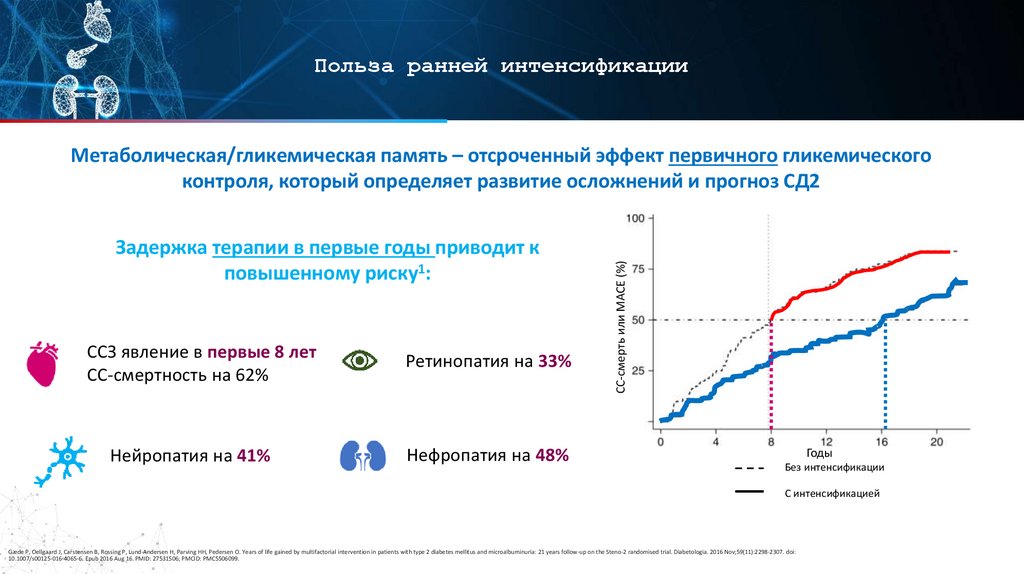
Польза ранней интенсификацииЗадержка терапии в первые годы приводит к
повышенному риску1:
ССЗ явление в первые 8 лет
СС-смертность на 62%
Ретинопатия на 33%
Нейропатия на 41%
Нефропатия на 48%
СС-смерть или МАСЕ (%)
Метаболическая/гликемическая память – отсроченный эффект первичного гликемического
контроля, который определяет развитие осложнений и прогноз СД2
Годы
Без интенсификации
С интенсификацией
Gæde P, Oellgaard J, Carstensen B, Rossing P, Lund-Andersen H, Parving HH, Pedersen O. Years of life gained by multifactorial intervention in patients with type 2 diabetes mellitus and microalbuminuria: 21 years follow-up on the Steno-2 randomised trial. Diabetologia. 2016 Nov;59(11):2298-2307. doi:
10.1007/s00125-016-4065-6. Epub 2016 Aug 16. PMID: 27531506; PMCID: PMC5506099.
26.
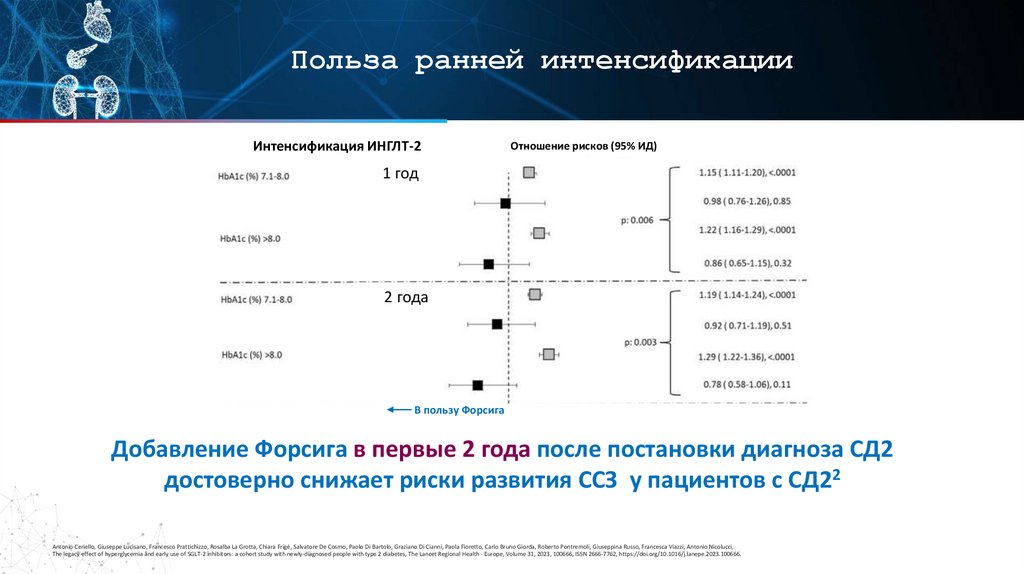
Польза ранней интенсификацииИнтенсификация ИНГЛТ-2
Отношение рисков (95% ИД)
1 год
2 года
В пользу Форсига
Добавление Форсига в первые 2 года после постановки диагноза СД2
достоверно снижает риски развития ССЗ у пациентов с СД22
Antonio Ceriello, Giuseppe Lucisano, Francesco Prattichizzo, Rosalba La Grotta, Chiara Frigé, Salvatore De Cosmo, Paolo Di Bartolo, Graziano Di Cianni, Paola Fioretto, Carlo Bruno Giorda, Roberto Pontremoli, Giuseppina Russo, Francesca Viazzi, Antonio Nicolucci,
The legacy effect of hyperglycemia and early use of SGLT-2 inhibitors: a cohort study with newly-diagnosed people with type 2 diabetes, The Lancet Regional Health - Europe, Volume 31, 2023, 100666, ISSN 2666-7762, https://doi.org/10.1016/j.lanepe.2023.100666.
27.
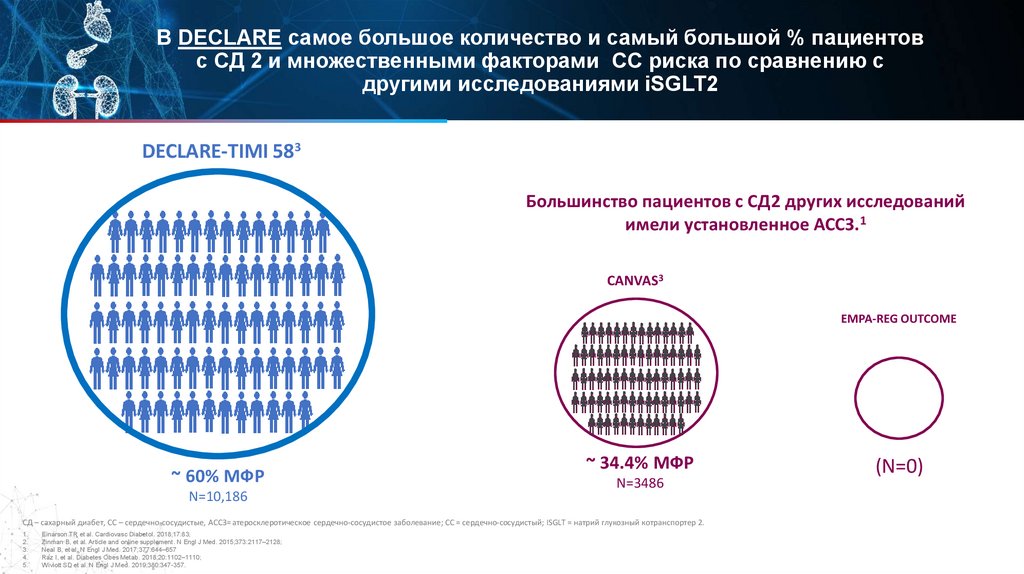
В DECLARE самое большое количество и самый большой % пациентовс СД 2 и множественными факторами СС риска по сравнению с
другими исследованиями iSGLT2
DECLARE-TIMI 583
Большинство пациентов с СД2 других исследований
имели установленное АССЗ.1
CANVAS3
EMPA-REG OUTCOME
~ 60% МФР
N=10,186
~ 34.4% МФР
N=3486
СД – сахарный диабет, СС – сердечно-сосудистые, АССЗ= атеросклеротическое сердечно-сосудистое заболевание; СС = сердечно-сосудистый; ISGLT = натрий глукозный котранспортер 2.
1.
2.
3.
4.
5.
Einarson TR et al. Cardiovasc Diabetol. 2018;17:83;
Zinman B, et al. Article and online supplement. N Engl J Med. 2015;373:2117–2128;
Neal B, et al. N Engl J Med. 2017;377:644–657
Raz I, et al. Diabetes Obes Metab. 2018;20:1102–1110;
Wiviott SD et al. N Engl J Med. 2019;380:347-357.
(N=0)
28.
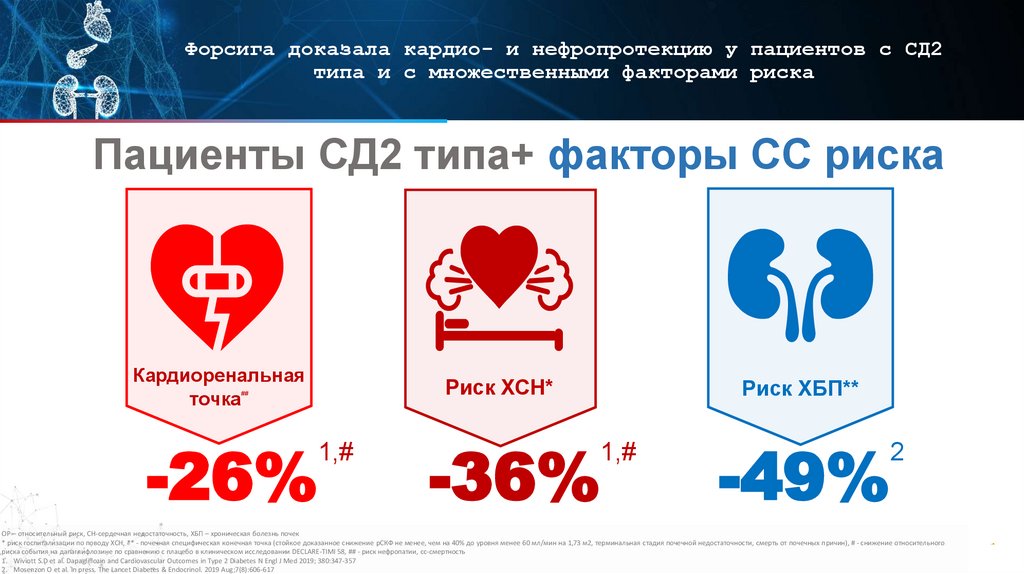
Форсига доказала кардио- и нефропротекцию у пациентов с СД2типа и с множественными факторами риска
Пациенты СД2 типа+ факторы СС риска
Кардиоренальная
точка
Риск ХСН*
##
-26%
1,#
-36%
Риск ХБП**
1,#
-49%
2
ОР – относительный риск, СН-сердечная недостаточность, ХБП – хроническая болезнь почек
* риск госпитализации по поводу ХСН, ** - почечная специфическая конечная точка (стойкое доказанное снижение рСКФ не менее, чем на 40% до уровня менее 60 мл/мин на 1,73 м2, терминальная стадия почечной недостаточности, смерть от почечных причин), # - снижение относительного
риска события на дапаглифлозине по сравнению с плацебо в клиническом исследовании DECLARE-TIMI 58, ## - риск нефропатии, сс-смертность
1. Wiviott S.D et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes N Engl J Med 2019; 380:347-357
2. Mosenzon O et al. In press. The Lancet Diabetes & Endocrinol. 2019 Aug;7(8):606-617
29.
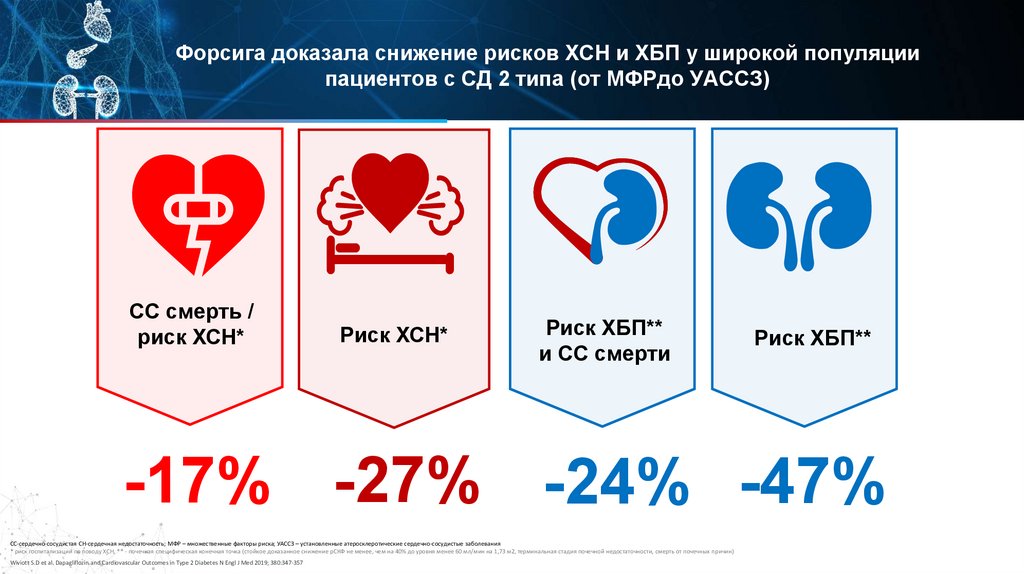
Форсига доказала снижение рисков ХСН и ХБП у широкой популяциипациентов с СД 2 типа (от МФРдо УАССЗ)
СС смерть /
риск ХСН*
Риск ХСН*
Риск ХБП**
и СС смерти
Риск ХБП**
-17% -27% -24% -47%
СС-сердечно-сосудистая СН-сердечная недостаточность; МФР – множественные факторы риска; УАССЗ – установленные атеросклеротические сердечно-сосудистые заболевания
* риск госпитализации по поводу ХСН, ** - почечная специфическая конечная точка (стойкое доказанное снижение рСКФ не менее, чем на 40% до уровня менее 60 мл/мин на 1,73 м2, терминальная стадия почечной недостаточности, смерть от почечных причин)
Wiviott S.D et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes N Engl J Med 2019; 380:347-357
30.
Эффективность Форсига по влиянию на СС исходыподтверждена в Реальной клинической практике
Nordic
40 908
пациентов (Дания, Швеция, Норвегия)
МАСЕ
-21%
Риск ХСН*
-38%
Факторы СС риска
Ассоциированные ССЗ
* риск госпитализации по поводу ХСН
СС- сердечно-сосудистый, ССЗ – сердечно-сосудистые заболевания, МАСE – комбинированная точка: СС смерть, инфаркт миокарда, ишемический инсульт
Persson F et al., Diabetes Obes Metab. 2018 Feb;20(2):344-351.
Смерть от всех причин
-41%
31.
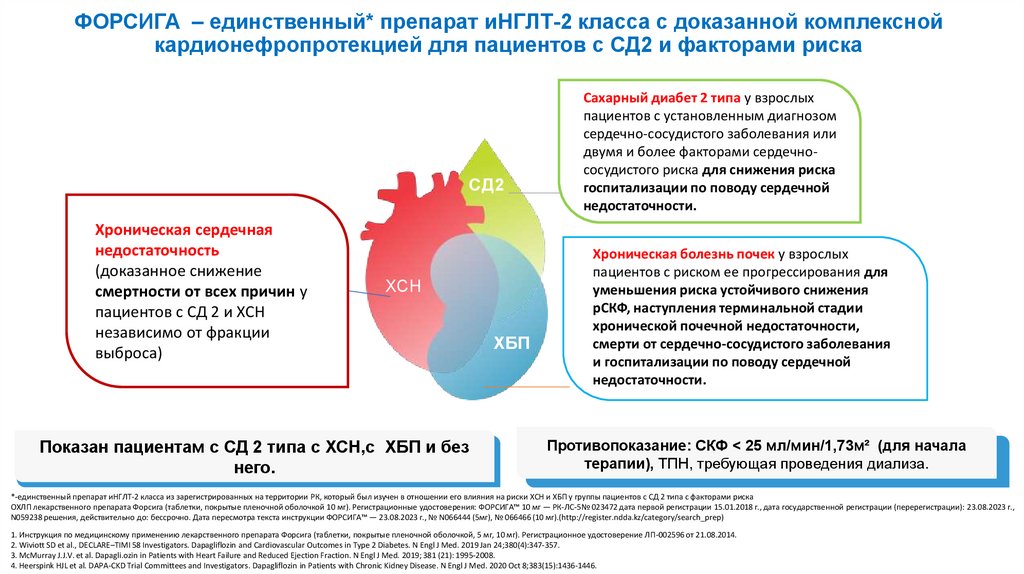
ФОРСИГА – единственный* препарат иНГЛТ-2 класса с доказанной комплекснойкардионефропротекцией для пациентов с СД2 и факторами риска
СД2
Хроническая сердечная
недостаточность
(доказанное снижение
смертности от всех причин у
пациентов с СД 2 и ХСН
независимо от фракции
выброса)
ХСН
Показан пациентам c СД 2 типа с ХСН,c ХБП и без
него.
ХБП
Сахарный диабет 2 типа у взрослых
пациентов с установленным диагнозом
сердечно-сосудистого заболевания или
двумя и более факторами сердечнососудистого риска для снижения риска
госпитализации по поводу сердечной
недостаточности.
Хроническая болезнь почек у взрослых
пациентов с риском ее прогрессирования для
уменьшения риска устойчивого снижения
рСКФ, наступления терминальной стадии
хронической почечной недостаточности,
смерти от сердечно-сосудистого заболевания
и госпитализации по поводу сердечной
недостаточности.
Противопоказание: СКФ < 25 мл/мин/1,73м² (для начала
терапии), ТПН, требующая проведения диализа.
*-единственный препарат иНГЛТ-2 класса из зарегистрированных на территории РК, который был изучен в отношении его влияния на риски ХСН и ХБП у группы пациентов с СД 2 типа с факторами риска
ОХЛП лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой 10 мг). Регистрационные удостоверения: ФОРСИГА™ 10 мг — РК-ЛС-5№ 023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023 г.,
N059238 решения, действительно до: бессрочно. Дата пересмотра текста инструкции ФОРСИГА™ — 23.08.2023 г., № N066444 (5мг), № 066466 (10 мг).(http://register.ndda.kz/category/search_prep)
1. Инструкция по медицинскому применению лекарственного препарата Форсига (таблетки, покрытые пленочной оболочкой, 5 мг, 10 мг). Регистрационное удостоверение ЛП-002596 от 21.08.2014.
2. Wiviott SD et al., DECLARE–TIMI 58 Investigators. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2019 Jan 24;380(4):347-357.
3. McMurray J.J.V. et al. Dapagli.ozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2019; 381 (21): 1995-2008.
4. Heerspink HJL et al. DAPA-CKD Trial Committees and Investigators. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020 Oct 8;383(15):1436-1446.
32.
Место дапаглифлозина в Национальных клиническихпротоколах
КП «Диагностика и лечение
СД2» 1
iSGLT2 входят в Перечень
лекарственных средств, имеющих
100% вероятность применения
КП «ХБП у взрослых» 2
КП «Диагностики и лечения ХСН» 3
iSGLT2 рекомендуют в качестве доказанной
нефропротективной и кардиопротективной
терапии первой линии у пациентов с СД2,
ХБП и рСКФ ≥30 мл/мин на 1,73 м2 (1A)
рекомендуют дапаглифлозин или
эмпаглифлозин всем пациентам с СНнФВ, независимо от наличия СД2 типа
ХБП – хроническая болезнь почек; ХСН – хроническая сердечная недостаточность, СД = сахарный диабет; iSGLT2- ингибиторы натрийглюкозного котраспортера 2 типа; KDIGO- Kidney Disease Improving Global Outcomes.
1. КП «Диагностика и лечение СД2 типа», Приказ №158 от 4.03.2022; 2. Клинический Протокол диагностики и лечения Хронической Болезни Почек у взрослых, Протокол №115, 23.12.2021; 3.КП ДИАГНОСТИКИ И ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ
НЕДОСТАТОЧНОСТИ МЗ РК, Приказ №179 от 09.02.2023
33.
Форсига (дапаглифлозин): простой способ дозирования и применения1Удобное дозирование один раз в день
без необходимости титрования * или коррекции
дозы
ПЕРВОНАЧАЛЬНОЕ
лечение
10 мг
таблетка
СКФ
≥25
1.
Форсига, 10 мг
Один раз в сутки.
Титрование не требуется
Регистрационные удостоверения: Форсига™ 10 мг - РК-ЛС-5№023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023г., NoN059238 решения, действительно до:
бессрочно. Дата пересмотра текста инструкции Форсига™ - 23. 08. 2023 г., №N066444 (5мг), №066466 (10 мг)
рСКФ = расчетная скорость клубочковой фильтрации; СКФ = скорость клубочковой фильтрации.
34.
Краткая общая характеристика лекарственного препаратаФорсига™
Краткая общая характеристика лекарственного препарата Форсига™
Торговое наименование Форсига™
Международное непатентованное название Дапаглифлозин
Показания к применению.
Cахарный диабет 2-го типа Препарат Форсига™ показан у взрослых пациентов с недостаточным контролем сахарного диабета 2-го типа в сочетании с диетой и физическими нагрузками в качестве:
монотерапии, когда применение метформина считается нецелесообразным или противопоказанным; комбинированной терапии в сочетании с другими лекарственными препаратами для лечения диабета 2-го
типа;
Сердечная недостаточность Препарат Форсига™ показан взрослым пациентам от 18 лет и старше для лечения симптоматической хронической сердечной недостаточности.
Хроническая болезнь почек Препарат Форсига показан взрослым пациентам от 18 лет и старше для лечения хронической болезни почек.
Способ применения и дозы
Режим дозирования Препарат Форсига™ применяется внутрь один раз в день независимо от приема пищи. Таблетки следует проглатывать целиком.
Способ применения.
Сахарный диабет 2-го типа Рекомендуемая доза дапаглифлозина составляет 10 мг один раз в сутки. С целью снижения риска гипогликемии при применении дапаглифлозина в комбинации с препаратами
инсулина или препаратами, повышающими секрецию инсулина, например, производными сульфонилмочевины, может потребоваться снижение дозы препаратов инсулина или препаратов, повышающих секрецию
инсулина.
Сердечная недостаточность Рекомендуемая доза дапаглифлозина составляет 10 мг один раз в сутки. В исследовании применения дапаглифлозина для предупреждения неблагоприятных исходов при сердечной
недостаточности (исследование DAPA-HF), дапаглифлозин применяется в сочетании с другими препаратами для лечения сердечной недостаточности.
Хроническая болезнь почек Рекомендуемая доза дапаглифлозина составляет 10 мг один раз в сутки. В исследовании влияния дапаглифлозина на почечные исходы у пациентов с хронической болезнью почек
(DAPA-CKD) дапаглифлозин применяется в сочетании с другими препаратами для лечения хронической болезни почек.
Основные побочные действия Очень часто (≥ 1/10): гипогликемия (при применении в комбинации с производным сульфонилмочевины или инсулином); Часто (≥ 1/100 ≤1/10): вульвовагинит, баланит и
сопутствующие инфекции половых органов, инфекции мочевыводящих путей; головокружение; сыпь; боль в спине; дизурия, полиурия; дислипидемия; сниженный почечный клиренс креатинина в начале терапии;
повышение значения гематокрита.
Противопоказания Повышенная индивидуальная чувствительность к любому компоненту препарата; сахарный диабет 1-го типа; диабетический кетоацидоз; почечная недостаточность, при которой расчетная СКФ
(рСКФ) ниже 25 мл/мин/1.73 м2 (для начала терапии); терминальная стадия заболевания почек, требующая диализа (из-за ограниченного опыта проведения клинических исследований); наследственная
непереносимость лактозы, недостаточность лактазы и глюкозо-галактозная непереносимость; беременность и период грудного вскармливания; детский и подростковый возраст до 18 лет (безопасность и
эффективность не изучены).
Особые указания
Беременность и период лактации. Отсутствуют данные об использовании дапаглифлозина у беременных женщин. При обнаружении беременности лечение дапаглифлозином должно быть прекращено. Из-за
возможного возникновения серьезных побочных реакций у детей применение препарата Форсига™ не рекомендуется во время кормления грудью.
Дети. Безопасность и эффективность дапаглифлозина у пациентов младше 18 лет не изучалась.
Условия отпуска по рецепту.
Название и адрес производителя АстраЗенека АБ, 18 СЕ-151 85, Содерталье, Швеция, тел.: +46 8 553 260 00 Факс: +46 8 553 290
Наименование, адрес и контактные данные организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств потребителей и ответственной за
пострегистрационное наблюдение за безопасностью лекарственного средства: Представительство ЗАК “АстраЗенека Ю-Кей Лимитед”, Республика Казахстан, г. Алматы, г. Алматы, 050000
ул. Кунаева, д. 77, офис 101, тел. +7 727 232 14 15;+7 701 0326745
e-mail: adverse.events.kz@astrazeneca.com или по ссылке https://contactazmedical.astrazeneca.com
Регистрационные удостоверения: Форсига™ 10 мг - РК-ЛС-5№023472 дата первой регистрации 15.01.2018 г., дата государственной регистрации (перерегистрации): 23.08.2023г., NoN059238 решения,
действительно до: бессрочно
Дата пересмотра текста инструкции Форсига™ - 23. 08. 2023 г., №N066444 (5мг), №066466 (10 мг)
Перед назначением и применением необходимо ознакомиться с инструкцией по медицинскому применению.
35.
Для лучшей и долгой жизни!Спасибо за внимание!









 medicine
medicine








