Similar presentations:
Таргетная терапия в онкологии
1.
УлГУМедицинский факультет
Кафедра онкологии и лучевой диагностики
Выполнил: Мухаметдинов
Айнур Раджапович ,
студент группы ЛД18/3
2024 г.
2.
ВВЕДЕНИЕ.Фундаментальным достижением последнего
десятилетия является образование нового
класса «таргетных,
молекулярно‐ориентированных препаратов»,
создаваемых для воздействия на определенные,
заранее установленные внутриклеточные
молекулярные мишени, имеющие ключевое
значение для жизнедеятельности опухолевой
клетки.
3.
Все эти мишени имеются и внормальной клетке, но при опухолевой
трансформации происходит их
гиперэкспрессия или гиперактивация,
что и является основанием для
применения определенных таргетных
препаратов.
4.
Большинство таргетных препаратов не обладаетспособностью убивать или выраженно повреждать
опухолевые клетки (цитотоксическое воздействие), а
лишь оказывают:
ингибирующее
влияние на
пролиферацию
и/или
(цитостатическое
воздействие)
стимулируют
дифференцировку опухолевых
клеток, за счет
выключения механизмов,
отвечающих за формирование
злокачественного фенотипа
5.
• В связи с этим основным эффектом при ихиспользовании является не излечение, а
длительное сдерживание опухолевого роста или,
в лучшем случае, уменьшение опухолевой массы.
Это никоим образом не уменьшает их потенциальной
значимости, т. к. перевод злокачественной опухоли в
состояние хронического заболевания, текущего
годами, является не менее привлекательной целью,
чем достижение полного излечения.
6.
В онкологии целями для воздействия таргетных препаратов являются:рецепторы к эпидермальным факторам роста (EGFR) и факторам роста
сосудов – VEGF (рецепторы ангиогенеза – VEGFR);
белки, осуществляющие проведение митогенных сигналов от
рецепторов;
молекулы, контролирующие запуск и течение программированной
смерти клеток;
гены, отвечающих за рост и деление раковых клеток;
перспективная новая технология направлена на «выключение» генов на основе механизма РНКинтерференции (механизма ингибирования экспрессии гена на стадии трансляции)
7.
По своей химической структуре таргетные средстваподразделяют на
антитела
«малые молекулы»
(низкомолекулярные
ингибиторы).
8.
антителаЭто продукты природного происхождения с
очень высокой специфичностью.
Они не проникают внутрь клетки, мишенью
являются мембранные рецепторы.
Процедура получения антител дорогостоящая и
всегда подразумевает иммунизацию какого-либо
животного, как правило, мыши.
9.
антителаВ-лимфоциты, полученные от иммунизируемой мыши,
иммортализуются посредством слияния с бессмертными
клетками – клетками миеломы.
«Чистые» мышиные антитела отторгаются иммунной системой
человека, поэтому для преодоления реакций межвидовой
несовместимости осуществляются генно-инженерные
манипуляции. В одном из технологических подходов активный
(противоопухолевый) эпитоп мышиных антител вырезается и
вставляется в «каркас» человеческого иммуноглобулина
10.
«малые молекулы» (низкомолекулярные ингибиторы).Это продукт химического синтеза с умеренной
специфичностью («мультитаргетные препараты»).
Они проникают внутрь клетки и имеют широкий спектр
мишеней.
Способность малых молекул проникать в ЦНС используется
для профилактики и лечения метастазов в головной мозг.
Стоимость производства – умеренная.
11.
АнтителаМалые молекулы
1. Продукт природного происхождения
2. Очень высокая специфичность
3. Не проникают внутрь клетки
(мишени: рецепторы)
4. Не проникают через
гематоэнцефалический барьер
5. Внутривенное введение
6. Высокая стоимость производства
1. Продукт химического синтеза
2. Умеренная специфичность
(«мультитаргетные препараты»)
3. Проникают внутрь клетки (широкий
спектр мишеней)
4. Проникают в ЦНС (профилактика и
лечение метастазов в мозг)
5. Пероральное введение
6. Умеренная стоимость производства
12.
• Рецепторы факторов роста представлены большим семействомразличных трансмембранных белков, локализованными в
поверхностных мембранах клеток.
13.
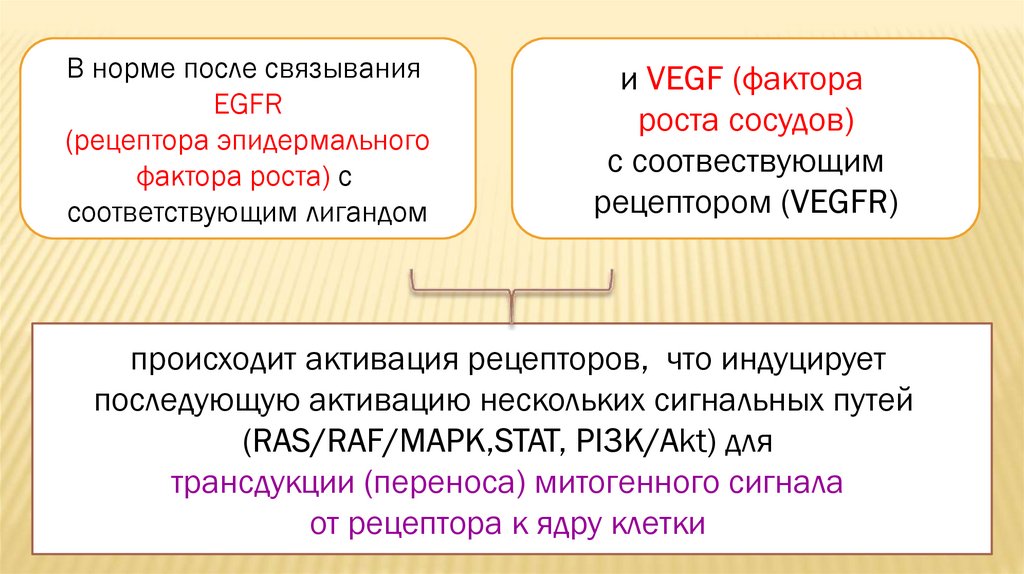
В норме после связыванияEGFR
(рецептора эпидермального
фактора роста) c
соответствующим лигандом
и VEGF (фактора
роста сосудов)
c соотвествующим
рецептором (VEGFR)
происходит активация рецепторов, что индуцирует
последующую активацию нескольких сигнальных путей
(RAS/RAF/MAPK,STAT, PI3K/Akt) для
трансдукции (переноса) митогенного сигнала
от рецептора к ядру клетки
14.
В опухолях часто встречается гиперактивация сигналаот этих рецепторов. Этот феномен является
результатом нескольких событий:
1. гиперэкспрессии рецептора,
2. аутокринной продукции самой опухолью
избыточных количеств лиганда,
3. мутации рецепторов, в результате которой они постоянно находятся в
активированном состоянии, независимо от связывания с лигандом.
15.
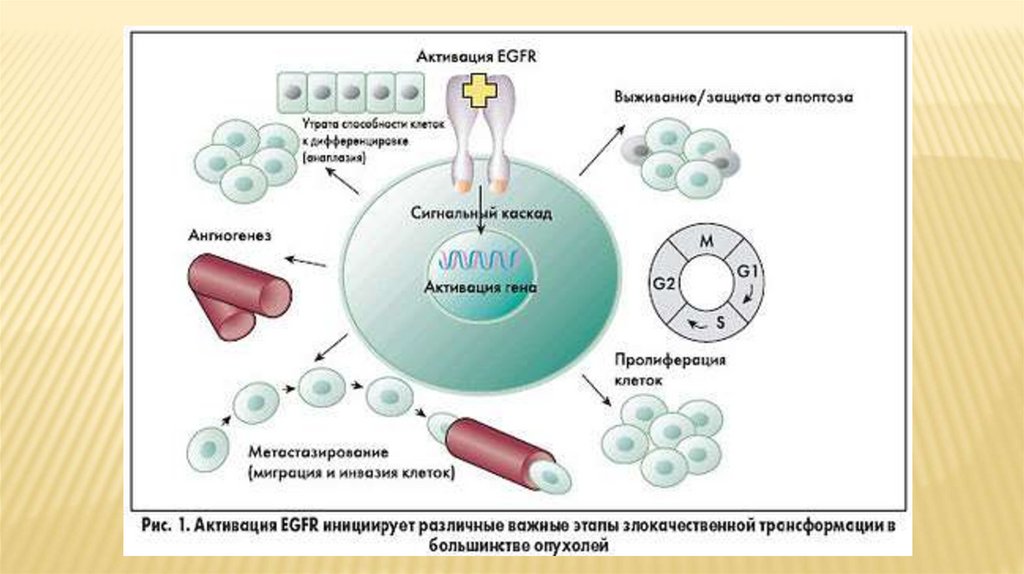
Результаты гиперактивации этих рецепторов вопухолевых клетках многообразны и включают:
1. неконтролируемую пролиферацию с
увеличением подвижности клеток,
2. метастазирование,
3. стимуляцию ангиогенеза,
4. подавление апоптоза.
16.
17.
В качестве противоопухолевых агентовпредложено использовать моноклональные
антитела к EGFR и VEGF, связывание которых с
рецептором или ростовым фактором должно
вести к блокированию сигнальных путей и
соответственно к гибели клеток.
18.
• Механизм действия препаратов: связываясь сэкстрацеллюлярным доменом EGFR, они препятствуют
его связыванию с природным лигандом и тем самым
предотвращают димеризацию рецептора и
последующее аутофосфорилирование тирозинкиназ
интрацеллюлярного домена рецептора.
• В результате не происходит активации белков,
входящих в сигнальный каскад, клетка не получает
пролиферативного сигнала, не делится, и в конечном
итоге наступает апоптоз.
19.
Неоангиогенез является важным патогенетическим фактором роста ипрогрессирования опухолей, т. к. опухоль при достижении определенного
размера (1–2 мм в диаметре) уже не может расти без дополнительного
поступления необходимых веществ. Для этого должен быть активирован
механизм неоангиогенеза, т. е. образование новых сосудов.
Этот момент является критическим для прогресса опухоли, т. к. в результате
неоангиогенеза она превращается из небольшого неопасного для организма
кластера мутантных клеток в опухоль, способную к злокачественному росту,
инвазии и метастазированию.
Поэтому, подавление неоангиогенеза является важным механизмом
противоопухолевого воздействия.
20.
Важнейшую роль в неоангиогенезе играетпролиферация эндотелиальных клеток, для развития
которой наибольшее значение имеет действие фактора
роста эндотелия сосудов (VEGF), который считаются
«прямым стимуляторам» ангиогенеза.
Высокий уровень экспрессии фактора роста эндотелия
сосудов найден во многих опухолях (рак толстой кишки,
рак молочной железы, рак желудка, рак легкого).
Причиной этого считают условия гипоксии и
оксидативного стресса, характерные для опухоли.
21.
• Рекомбинантное гуманизированное моноклональноеантитело против фактора роста эндотелия сосудов
(VEGF).
• Бевацизумаб реагирует с участком VEGF, ответственным
за связывание с соответствующим рецептором, что
блокирует образование ангиогенного сигнала и, как
следствие, подавляет неоангиогенез.
22.
Тирозинкиназы — одно из важнейших звеньев в системепередачи сигналов в клетке.
Одной из наиболее универсальных характеристик
процесса злокачественной трансформации является
активация процессов фосфорилирования белков. Поэтому
специфические инактиваторы протеинкиназ представляют
собой самый обширный класс таргетных препаратов.





















 medicine
medicine








