Similar presentations:
Изучение показателей жесткости водопроводной воды различных районов г. Смоленска
1. Изучение показателей жесткости водопроводной воды различных районов г. Смоленска Работу выполнили: Силенова Анастасия,
МБОУ «СШ № 25»Изучение показателей
жесткости водопроводной воды
различных районов
г. Смоленска
Работу выполнили: Силенова Анастасия,
Муравьева Виктория
Смоленск
2019 г
2. содержание
1. ВведениеАктуальность исследования
Значение воды для человека
Жесткость воды
2. Материалы и методики исследования
3. Результаты исследования и их анализ
4. Заключение
5. Литература
3. Цель работы
• Изучить параметры жесткости водывзятой из одних и тех же источников в
трех районах г. Смоленска:
Заднепровском, Ленинском и
Промышленном в динамике
наблюдения в течение зимне-весеннего
периода 2018 г.
4. Значение воды для человека
Химический аспект.Физиологический аспект.
Физический
аспект.
Санитарно - гигиенический
аспект.
Транспортный
аспект
Промышленный аспект.
Биологический
аспект.
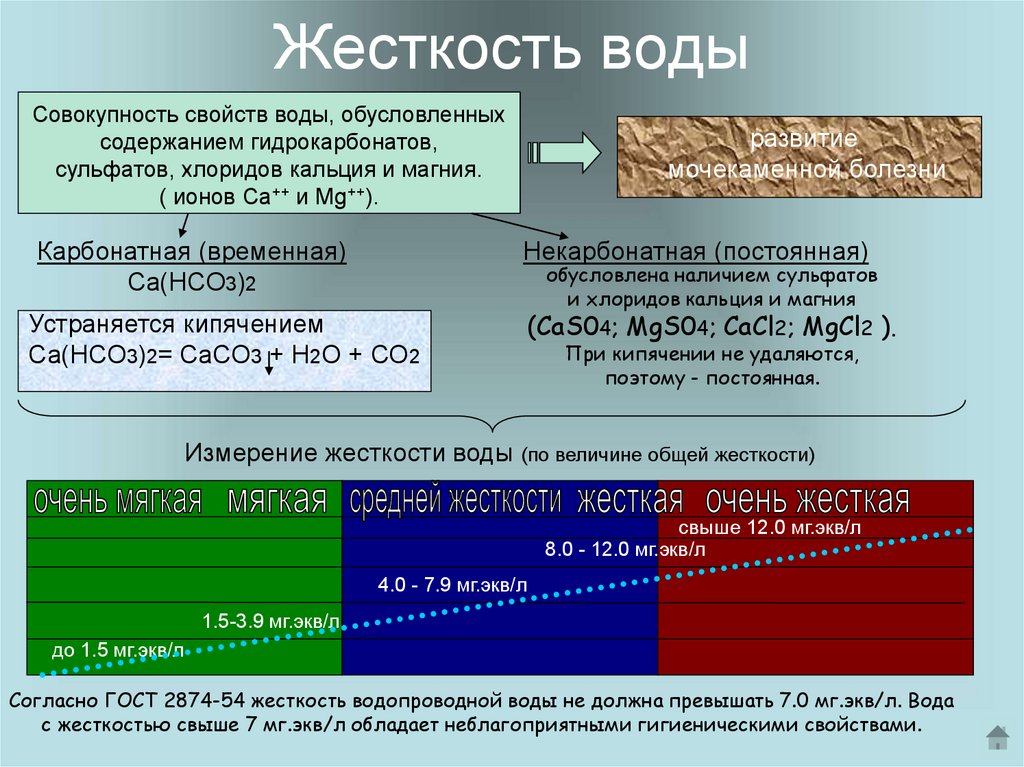
5. Жесткость воды
Совокупность свойств воды, обусловленныхсодержанием гидрокарбонатов,
сульфатов, хлоридов кальция и магния.
( ионов Са++ и Mg++).
Карбонатная (временная)
Ca(HCO3)2
развитие
мочекаменной болезни
Некарбонатная (постоянная)
Устраняется кипячением
Ca(HCO3)2= CaCO3 + H2O + CO2
обусловлена наличием сульфатов
и хлоридов кальция и магния
(CaS04; MgS04; CaCl2; MgCl2 ).
При кипячении не удаляются,
поэтому - постоянная.
Измерение жесткости воды (по величине общей жесткости)
свыше 12.0 мг.экв/л
8.0 - 12.0 мг.экв/л
4.0 - 7.9 мг.экв/л
1.5-3.9 мг.экв/л
до 1.5 мг.экв/л
Согласно ГОСТ 2874-54 жесткость водопроводной воды не должна превышать 7.0 мг.экв/л. Вода
с жесткостью свыше 7 мг.экв/л обладает неблагоприятными гигиеническими свойствами.
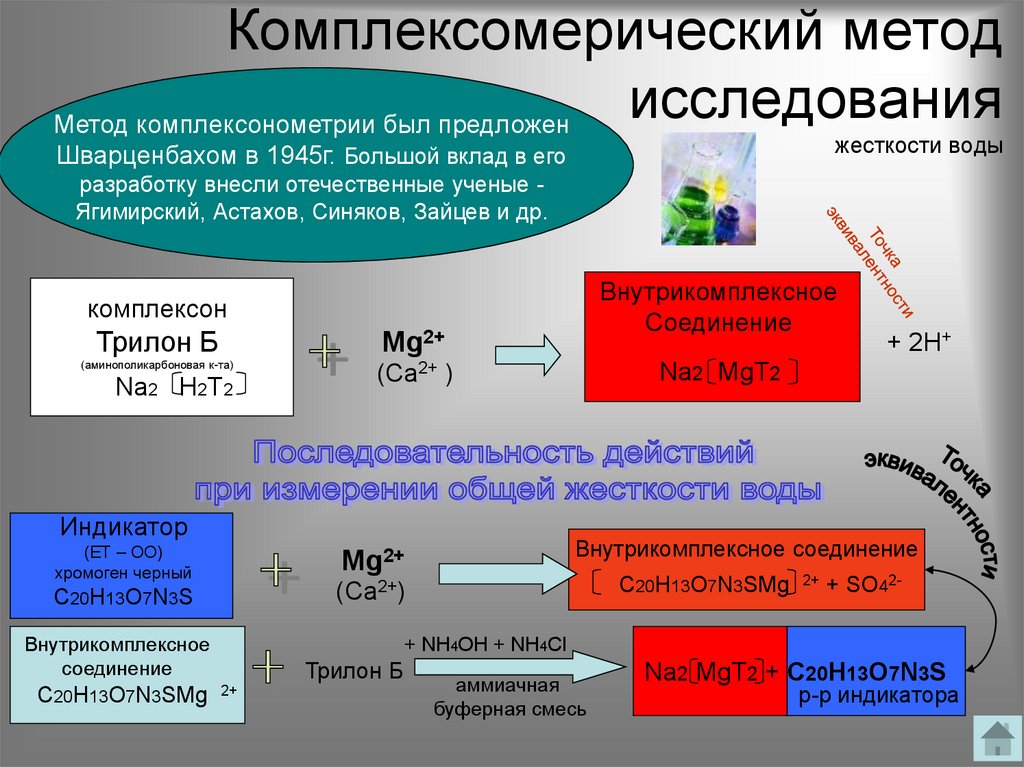
6. Комплексомерический метод исследования жесткости воды
Комплексомерический методисследования
Метод комплексонометрии был предложен
жесткости воды
Шварценбахом в 1945г. Большой вклад в его
разработку внесли отечественные ученые Ягимирский, Астахов, Синяков, Зайцев и др.
Внутрикомплексное
Соединение
комплексон
Трилон Б
Mg2+
(аминополикарбоновая к-та)
(Ca2+ )
Na2 H2T2
Индикатор
(ЕТ – ОО)
хромоген черный
C20H13O7N3SMg
(Ca2+)
Внутрикомплексное
соединение
C20H13O7N3SMg
Na2 MgT2
Внутрикомплексное соединение
Mg2+
C20H13O7N3S
+ 2H+
2+
+ SO42-
+ NH4OH + NH4Cl
Трилон Б
2+
аммиачная
буферная смесь
Na2 MgT2 + C20H13O7N3S
р-р индикатора
7.
В колбу для титрования отмеряли из бюретки 25 мл исследуемой воды,добавляли 10 мл аммиачно-буферной смеси, 6 капель индикатора
хромогена черного. Титровали раствором трилона Б до появления
серо-голубой окраски. Расчет общей жесткости воды определяется
по формуле: ОЖ = V х N х 1000
VI
Например:
ОЖ =4.7x0.05x1000 = 9.4 мг.экв/л
25
Где: ОЖ - общая жесткость воды (мг.экв/л)
V- число мл. трилона Б,
пошедшего на титрование
N - нормальность трилона Б
VI- объем воды, взятой для анализа в мл.
1000 - коэффициент для перерасчета
в литры
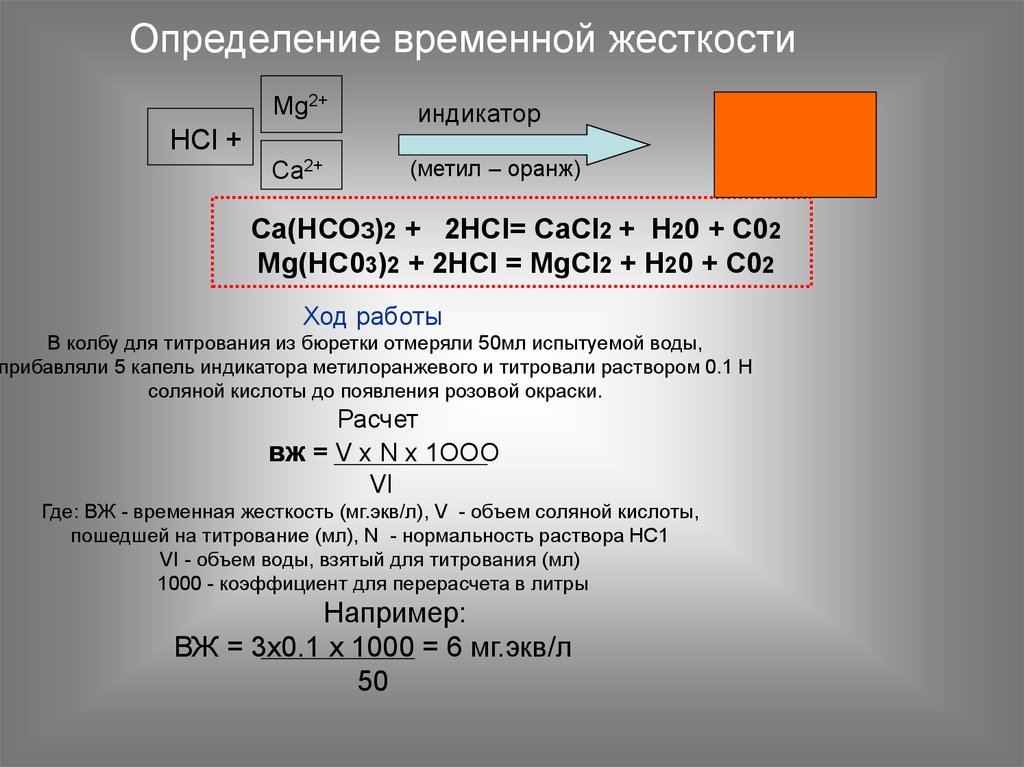
8.
Определение временной жесткостиMg2+
индикатор
HCl +
Ca2+
(метил – оранж)
Са(НСОЗ)2 + 2НСl= СаCl2 + Н20 + С02
Mg(HC03)2 + 2НСl = MgCl2 + Н20 + С02
Ход работы
В колбу для титрования из бюретки отмеряли 50мл испытуемой воды,
прибавляли 5 капель индикатора метилоранжевого и титровали раствором 0.1 Н
соляной кислоты до появления розовой окраски.
Расчет
вж = V x N x 1OOO
VI
Где: ВЖ - временная жесткость (мг.экв/л), V - объем соляной кислоты,
пошедшей на титрование (мл), N - нормальность раствора НС1
VI - объем воды, взятый для титрования (мл)
1000 - коэффициент для перерасчета в литры
Например:
ВЖ = 3x0.1 х 1000 = 6 мг.экв/л
50
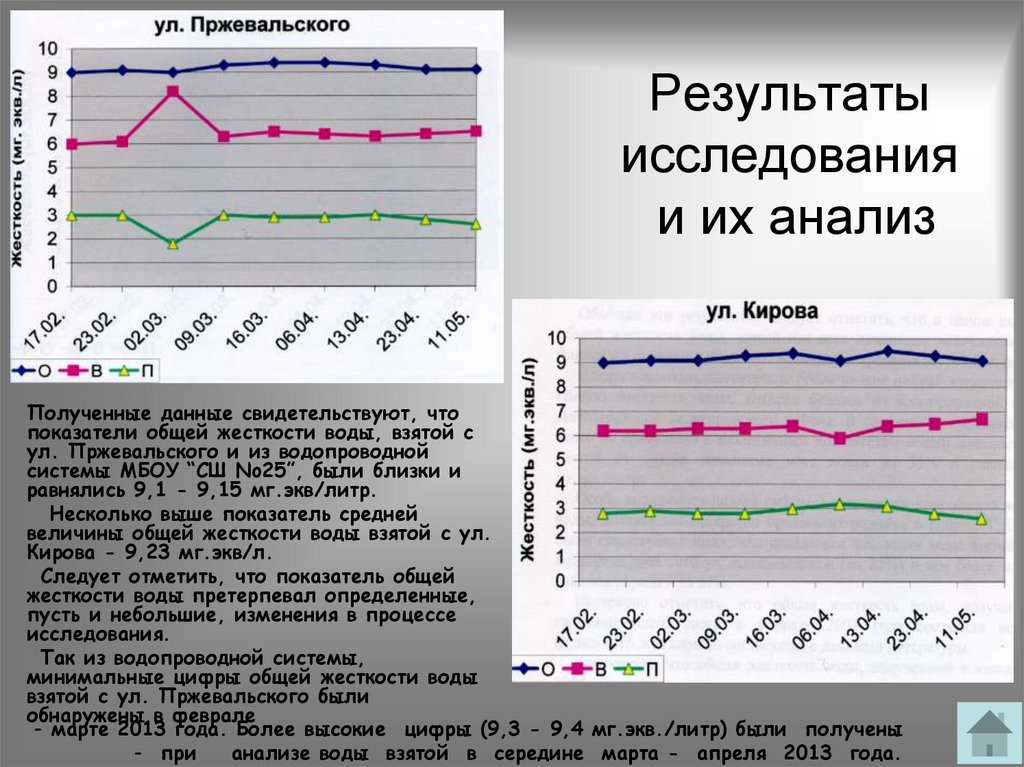
9. Результаты исследования и их анализ
Полученные данные свидетельствуют, чтопоказатели общей жесткости воды, взятой с
ул. Пржевальского и из водопроводной
системы МБОУ “СШ No25”, были близки и
равнялись 9,1 - 9,15 мг.экв/литр.
Несколько выше показатель средней
величины общей жесткости воды взятой с ул.
Кирова - 9,23 мг.экв/л.
Следует отметить, что показатель общей
жесткости воды претерпевал определенные,
пусть и небольшие, изменения в процессе
исследования.
Так из водопроводной системы,
минимальные цифры общей жесткости воды
взятой с ул. Пржевальского были
обнаружены в феврале
- марте 2013 года. Более высокие цифры (9,3 - 9,4 мг.экв./литр) были получены
- при
анализе воды взятой в середине марта - апреля 2013 года.
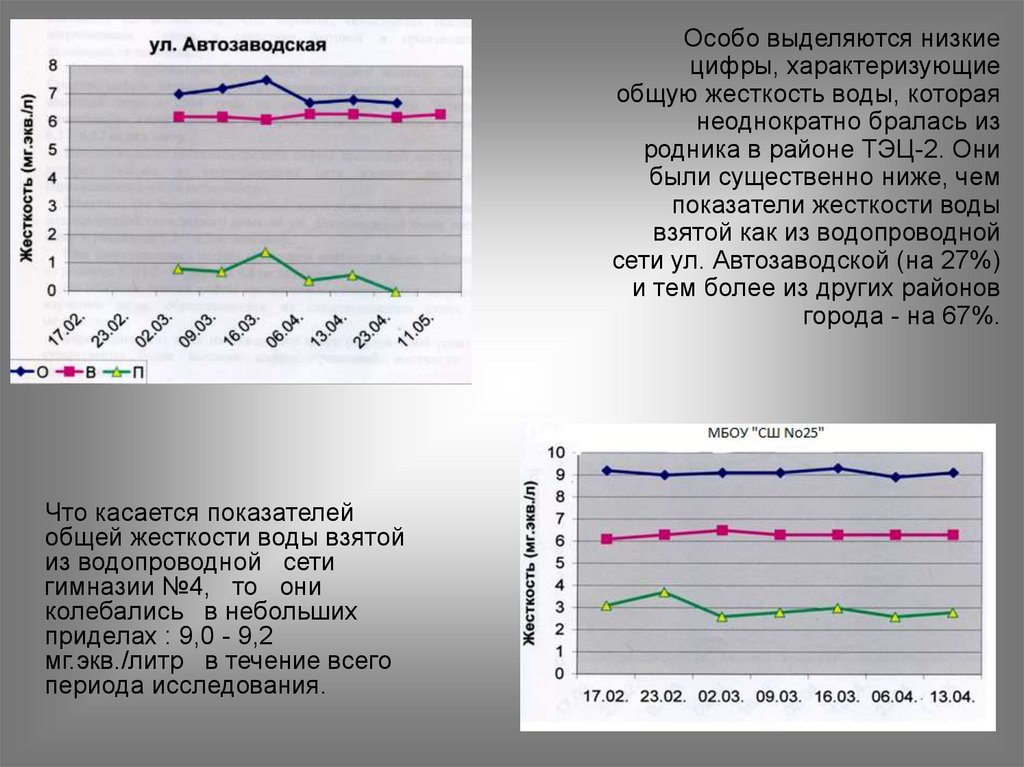
10.
Особо выделяются низкиецифры, характеризующие
общую жесткость воды, которая
неоднократно бралась из
родника в районе ТЭЦ-2. Они
были существенно ниже, чем
показатели жесткости воды
взятой как из водопроводной
сети ул. Автозаводской (на 27%)
и тем более из других районов
города - на 67%.
Что касается показателей
общей жесткости воды взятой
из водопроводной сети
гимназии №4, то они
колебались в небольших
приделах : 9,0 - 9,2
мг.экв./литр в течение всего
периода исследования.
11. Заключение
Результаты проведеннойработы свидетельствуют,
что показатели общей
жесткости воды, в течение
периода наблюдения
подвергались определенным
изменениям.
Наиболее низкие цифры,
характеризующие общую,
жесткость, были взяты из
водопроводной сети дома
по ул. Автозаводской
Заднепровского района
г.Смоленска.
28
источники
хим. очистка
время года
17
др.
43
10
12.
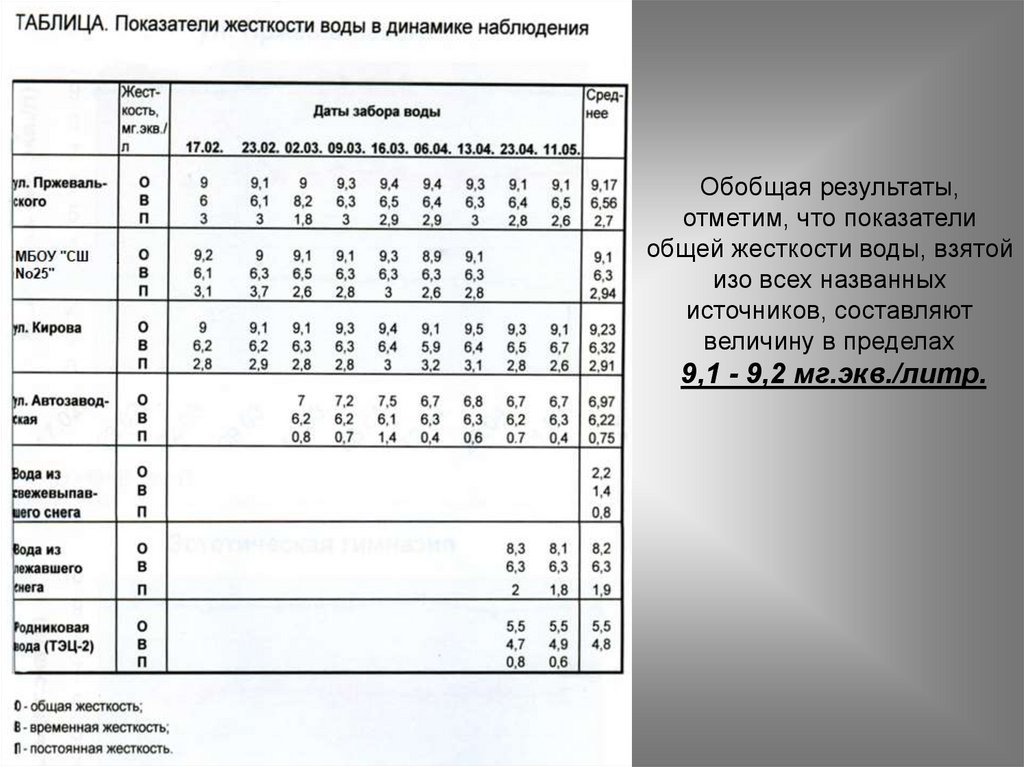
Обобщая результаты,отметим, что показатели
общей жесткости воды, взятой
изо всех названных
источников, составляют
величину в пределах
9,1 - 9,2 мг.экв./литр.
13.
• 1. Вода как природный ресурс. Метод.Материал в помощь лектор)
Смоленск, 1986, 25с
• 2. В.А.Гомфеклер. Питьевая вода. М.,1966, 36с
• 3. Ю.В.Новиков. Вода как фактор здоровья. М.
"Знание", 1982, 96с
• 4. Руководство по контролю качества
питьевой воды.. Изд2., Т.1
Рекомендации. ВОЗ, Женева, 1994г, 256с
• 5. 0.Л.Тиктинский, В.П.Александров. Мочекаменная
болезнь. С.П.,"Питер''
2000,384с
• 6.http://www.xumuk.ru
• 7.http://scalaria.narod.ru






 chemistry
chemistry








