Similar presentations:
Белки. Классификация белков
1.
Белки2.
Содержание• Определение
• Функции белков
• Источники аминокислот
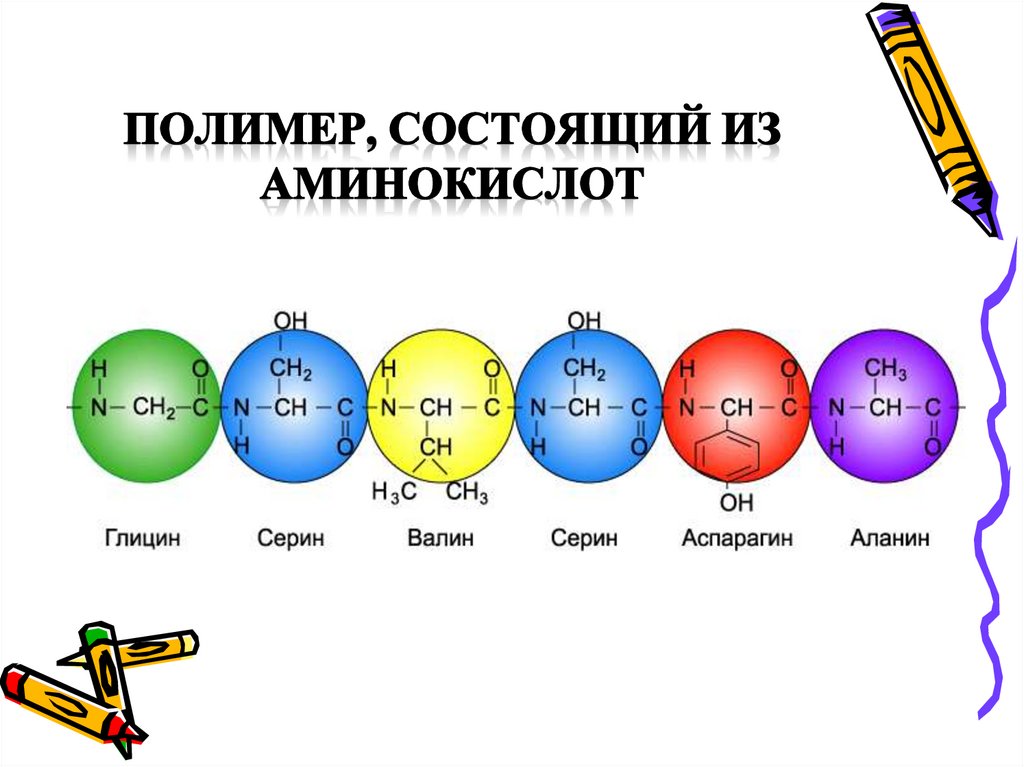
• Строение полипептидной цепи
• Структура белка
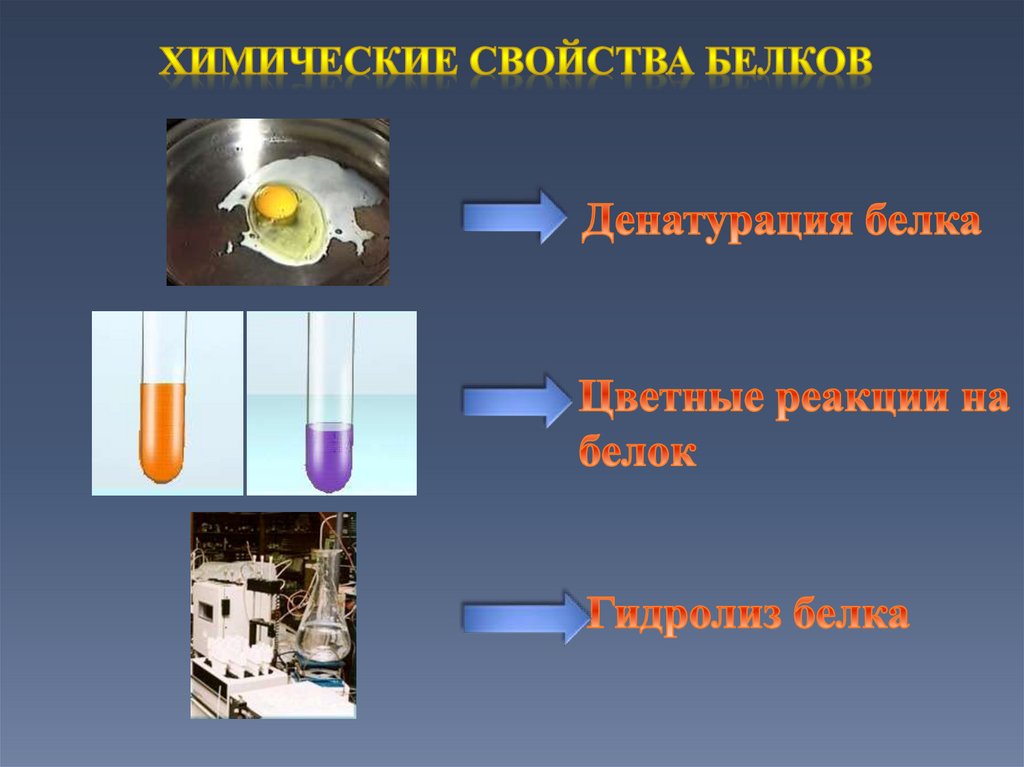
• Химические свойства
• Превращения белков в организме
• Источники информации
3.
История открытия белков1888г. – русский ученый
биохимик А.Я.Данилевский
на основании своих опытов
впервые высказал гипотезу о
пептидной связи между
остатками аминокислот в
белковой молекуле.
4.
1899г. – немецкие химики ЭмильФишер и Франц Гофмейстер высказали
предположение: в белках
аминокислоты связаны за счет
аминогруппы одной кислоты и
карбоксила другой.
Эта гипотеза в 1907г.
получила название
«полипептидной
теории».
Э. Фишер
5.
БелкиЭто природные высокомолекулярные
азотсодержащие органические
соединения, состоящие из α -аминокислот,
соединённых с помощью пептидных
связей и имеющие сложную структурную
организацию.
В состав большинства белков входит 300-500
остатков аминокислот, но есть и более
крупные белки, состоящие 1500 и более
аминокислот.
6.
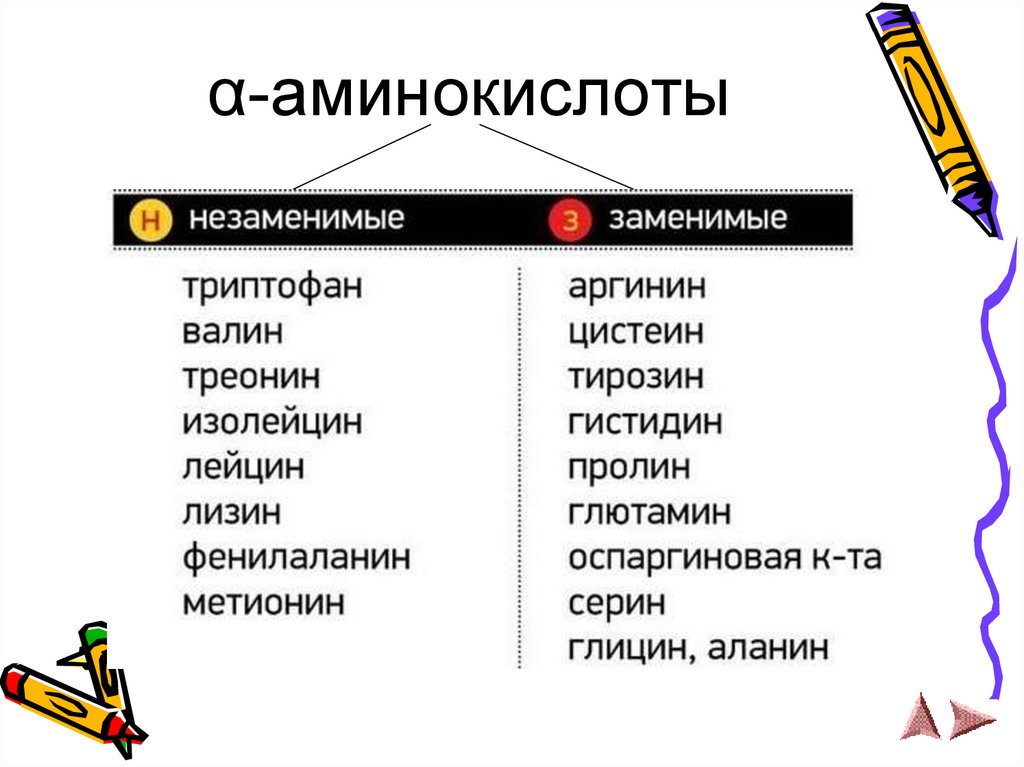
α-аминокислоты7.
Аминокислоты, участвующиев создании белков.
Глицин
Аланин
Валин
Лейцин
Изолейцин
Треонин
Серин
Цистеин
8.
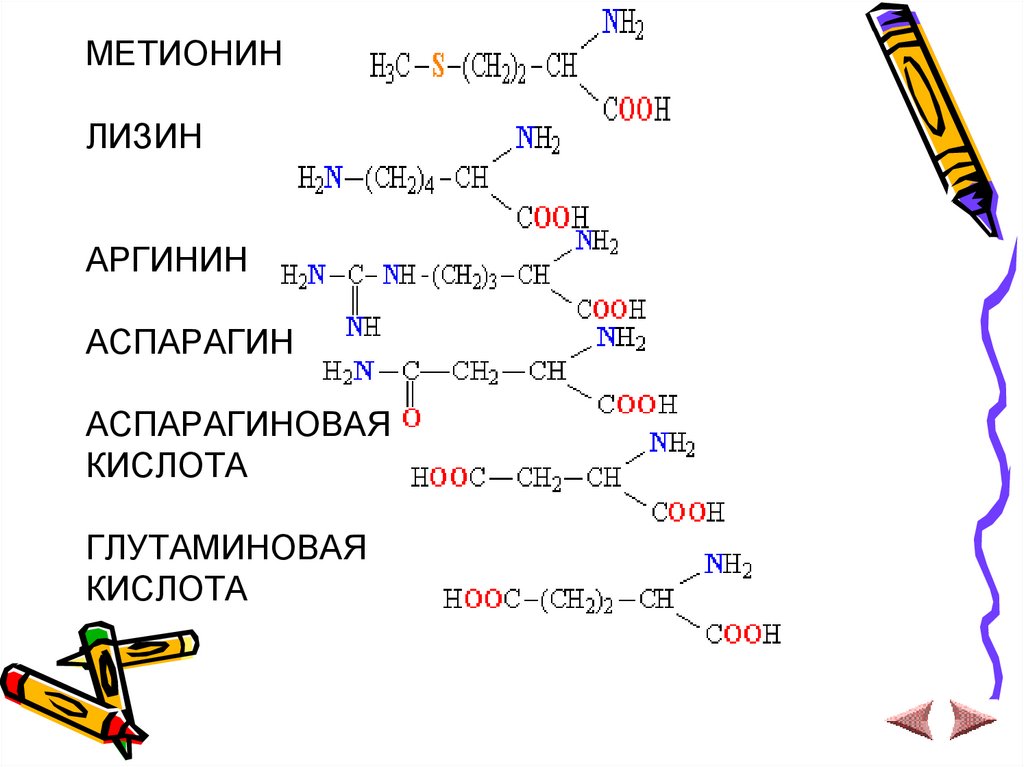
МЕТИОНИНЛИЗИН
АРГИНИН
АСПАРАГИН
АСПАРАГИНОВАЯ
КИСЛОТА
ГЛУТАМИНОВАЯ
КИСЛОТА
9.
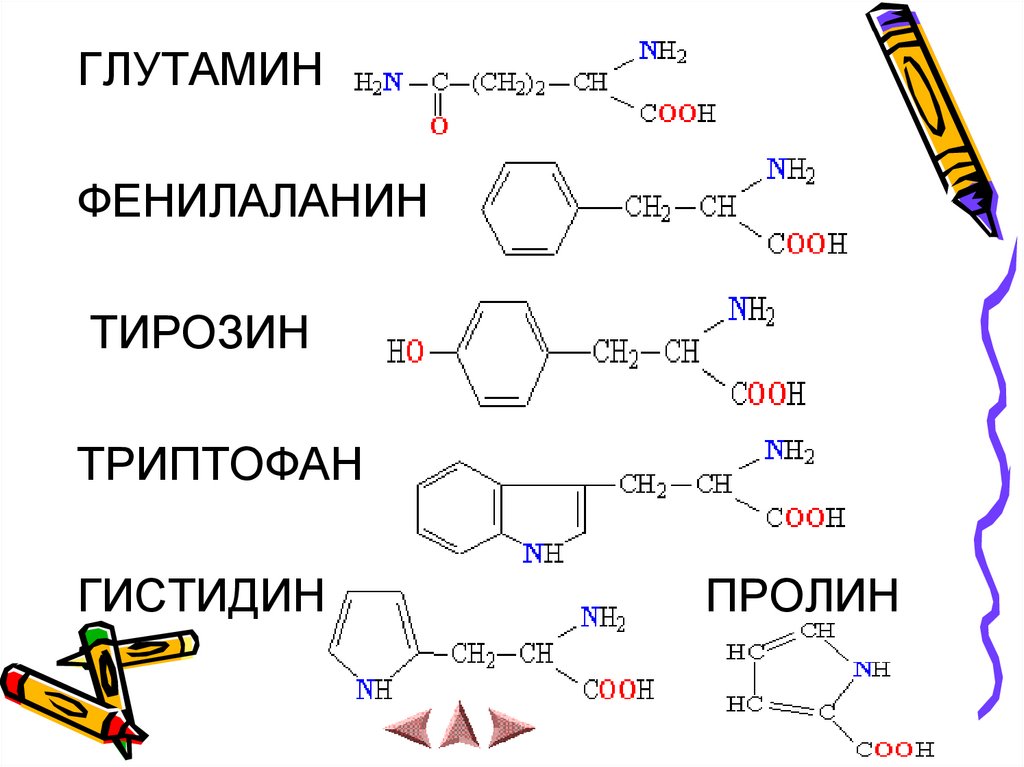
ГЛУТАМИНФЕНИЛАЛАНИН
ТИРОЗИН
ТРИПТОФАН
ГИСТИДИН
ПРОЛИН
10.
11.
12.
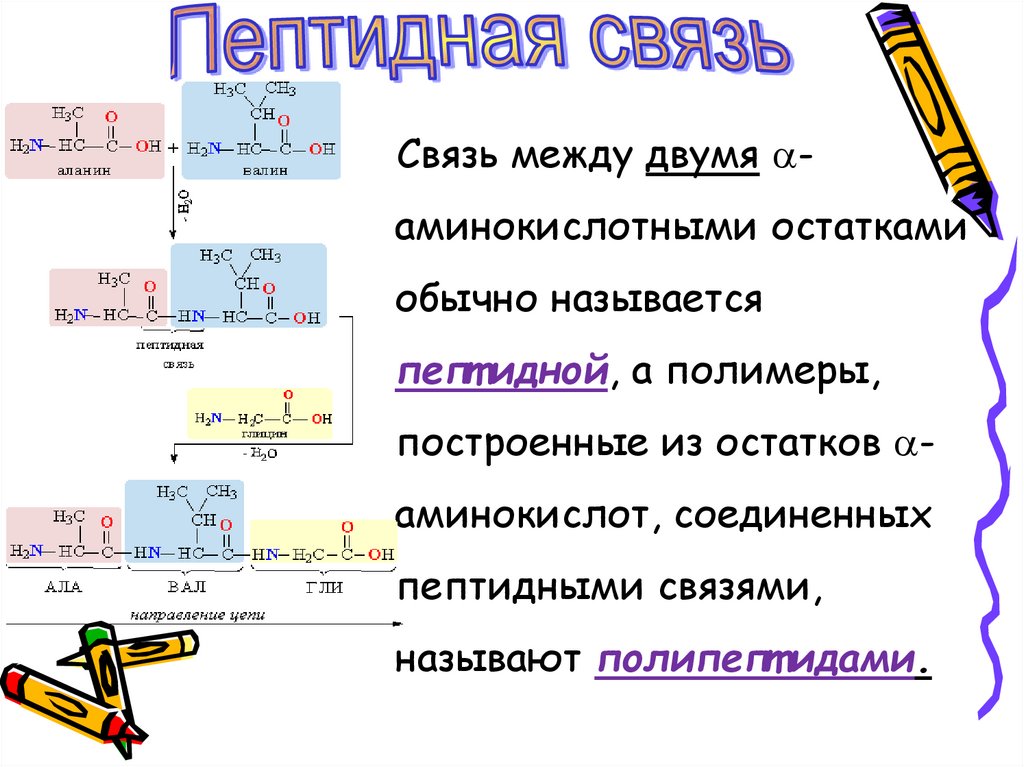
Связь между двумя аминокислотными остаткамиобычно называется
пепт идной, а полимеры,
построенные из остатков аминокислот, соединенных
пептидными связями,
называют полипепт идами.
13.
В их основе лежат разные признаки:степень сложности (простые и сложные);
форма молекул (глобулярные и
фибриллярные);
растворимость в отдельных растворителях;
выполняемая функция.
14.
Классификация белковБелки
Простые
гидролизуются
ТОЛЬКО
на аминокислоты
глобулярные
фибриллярные
Сложные
при гидролизе
дают не только
аминокислоты,
но и другие структуры –
ПРОСТЕТИЧЕСКИЕ группы
фосфопротеиды
металлопротеиды
хромопротеиды
липопротеиды
15.
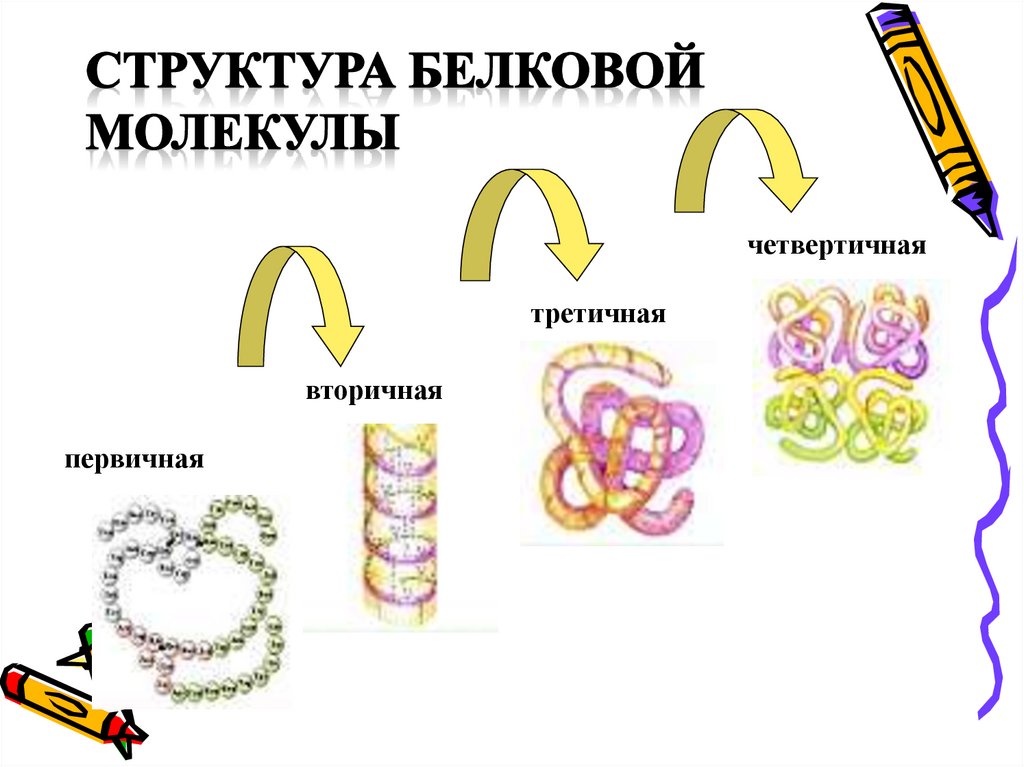
четвертичнаятретичная
вторичная
первичная
16.
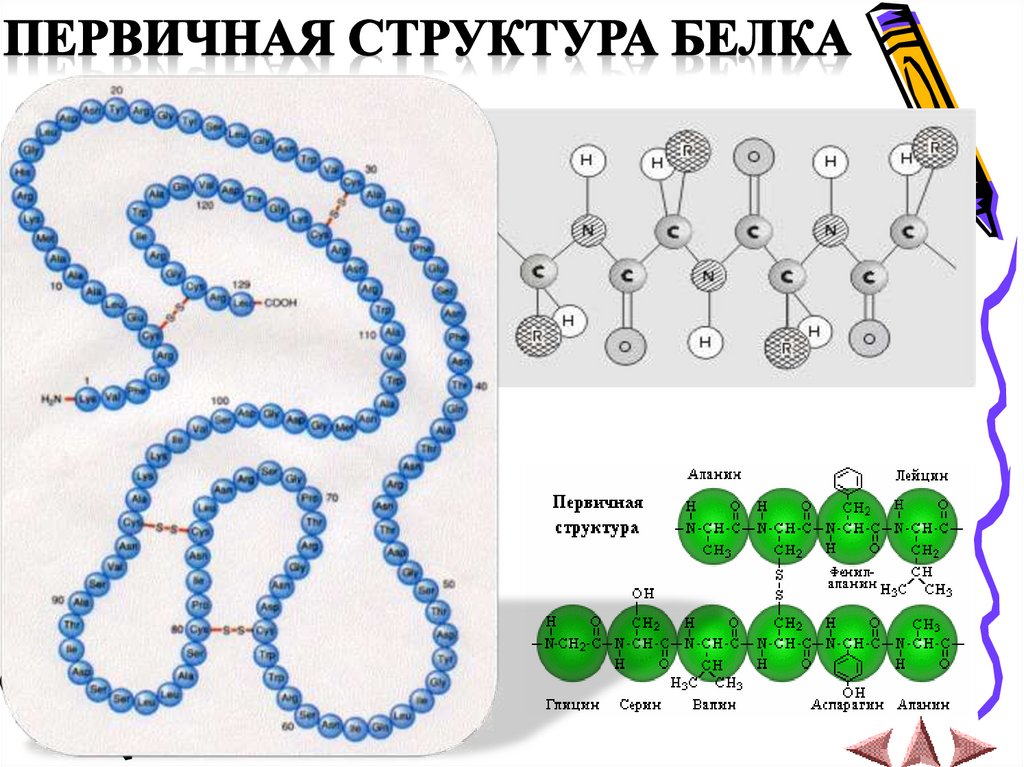
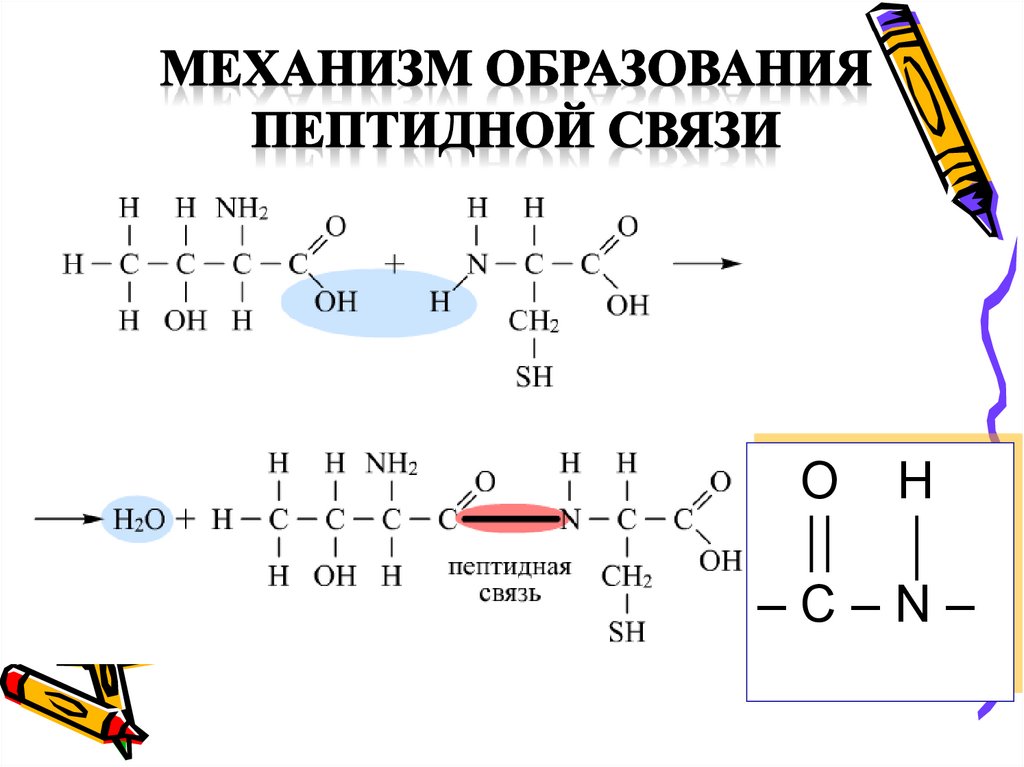
Представляет собой линейную цепьаминокислот, расположенных в
определенной последовательности и
соединенных между собой
пептидными связями. Пептидная
связь образуется за счет карбоксильной группы одной
аминокислоты и -аминной
группы другой.
17.
18.
OH
–С–N–
19.
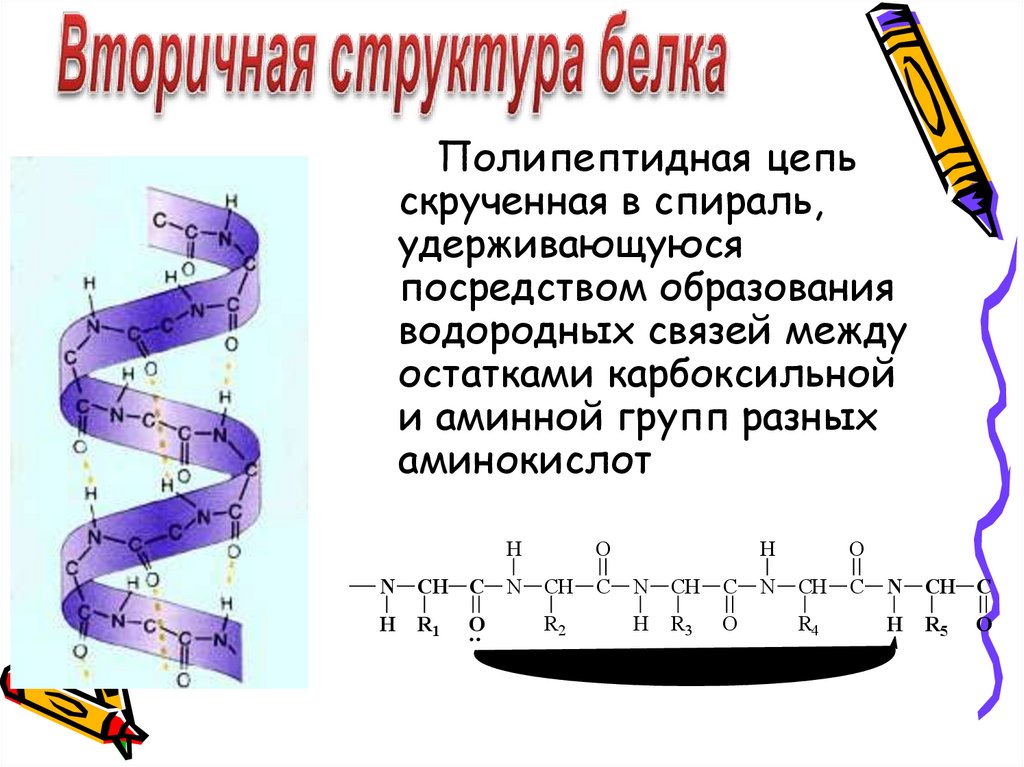
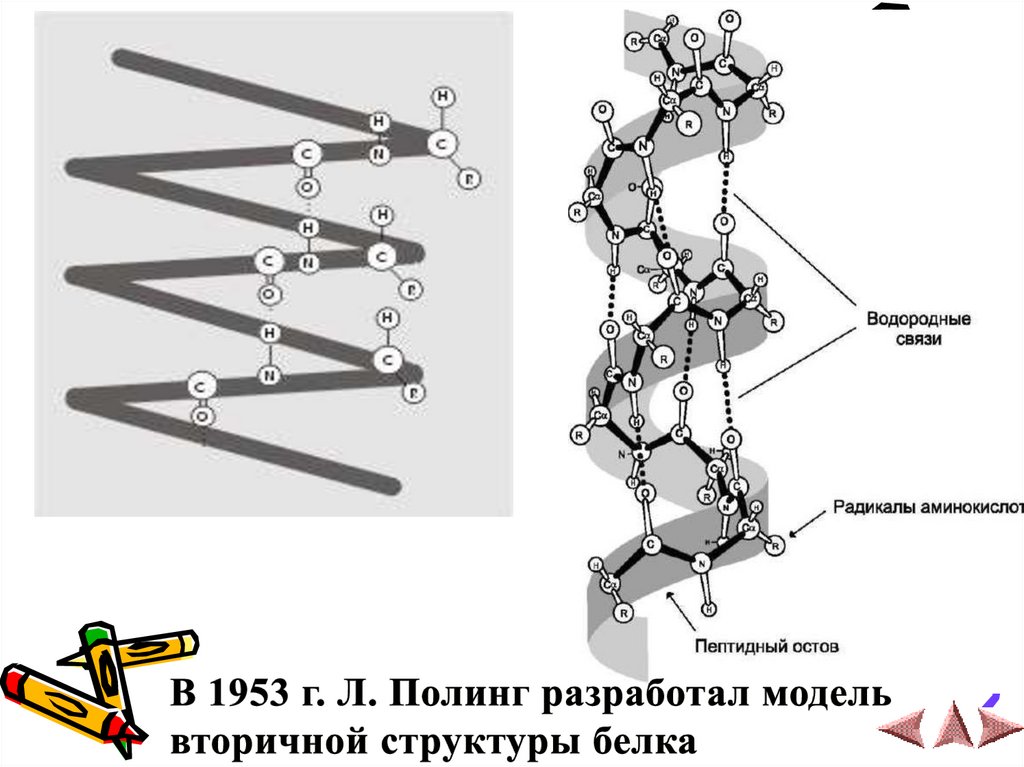
Полипептидная цепьскрученная в спираль,
удерживающуюся
посредством образования
водородных связей между
остатками карбоксильной
и аминной групп разных
аминокислот
H
N
CH C
H
R1
O
N
O
CH
R2
C
H
N
CH
C
H
R3
O
N
O
CH
R4
C
N
CH C
H
R5
O
20.
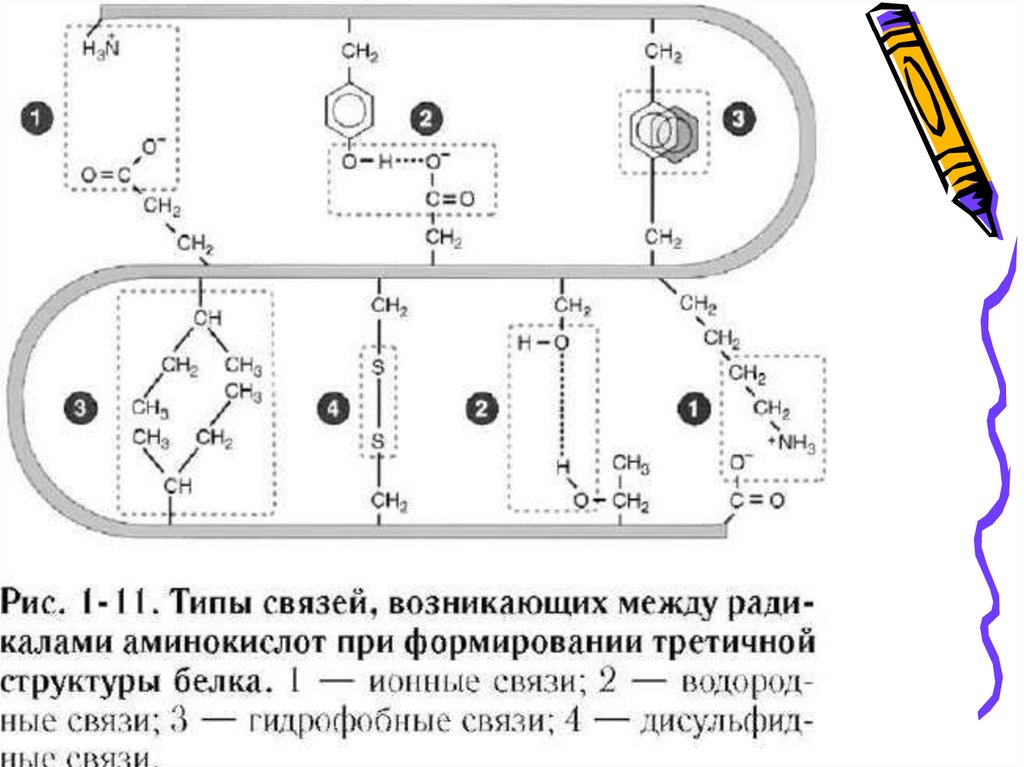
21.
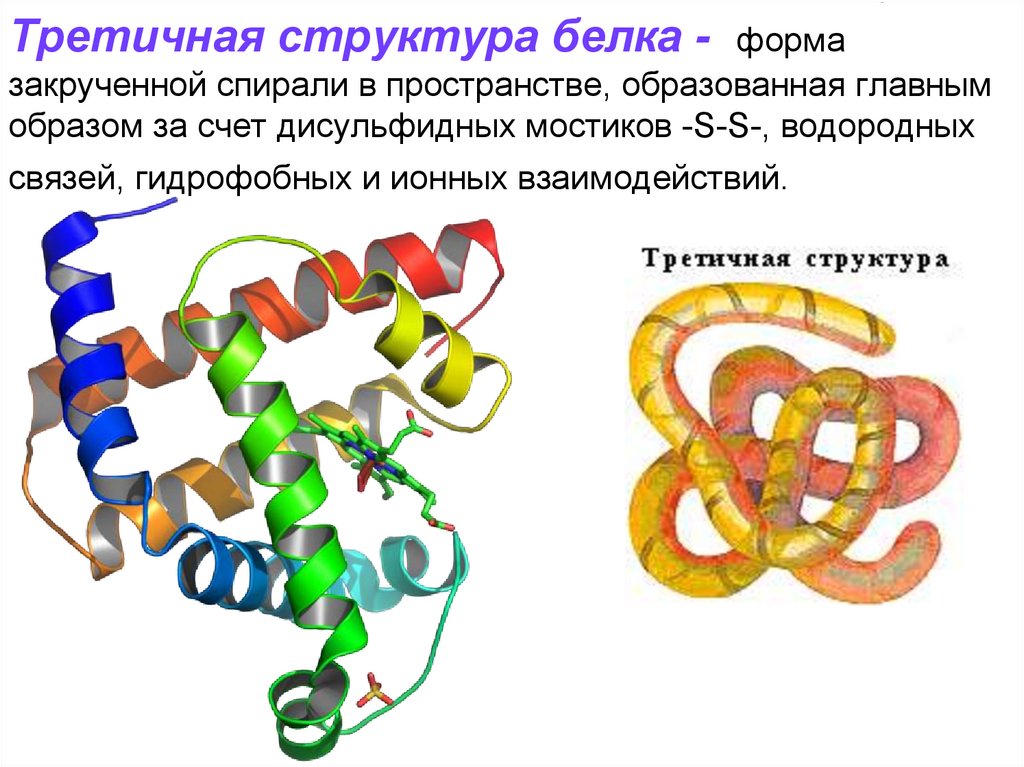
Третичная структура белка - формазакрученной спирали в пространстве, образованная главным
образом за счет дисульфидных мостиков -S-S-, водородных
связей, гидрофобных и ионных взаимодействий.
22.
23.
Четвертичная структура белка –агрегаты нескольких белковых макромолекул
(белковые комплексы), образованные за счет
взаимодействия разных полипептидных цепей
24.
25.
Глобулярные – глобула или клубок(растворимые)
Фибриллярные закрученная нить
(нерастворимые)
Гемоглобин (глобулярный)
Актин (фибриллярный)
26.
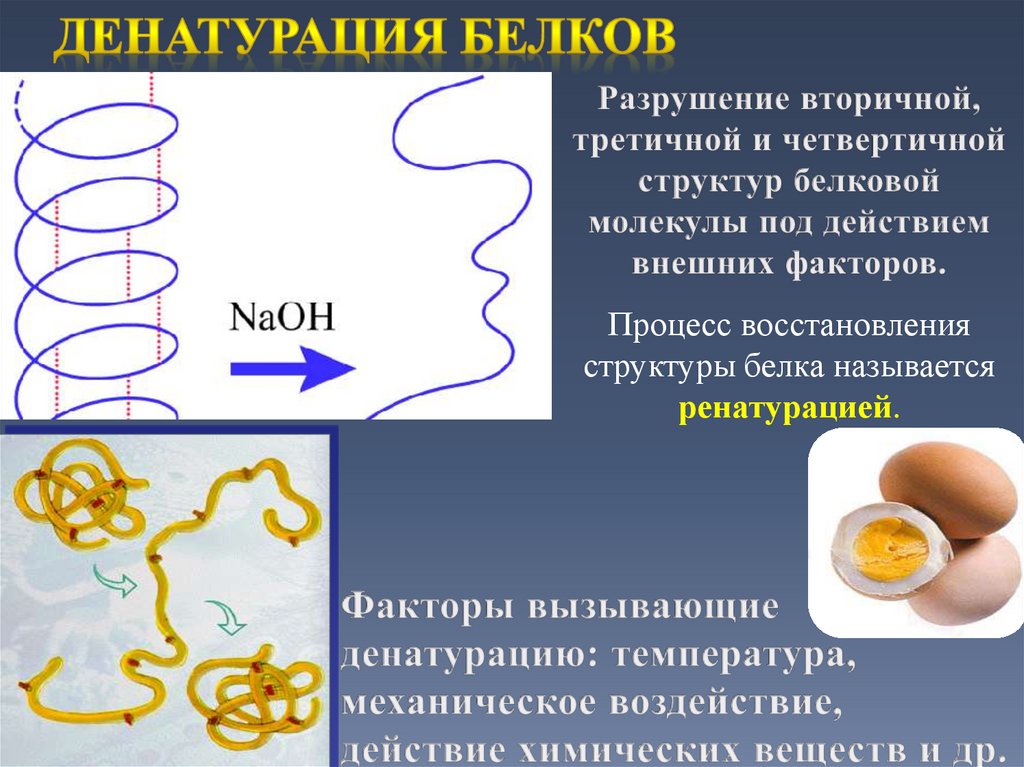
27.
Процесс восстановленияструктуры белка называется
ренатурацией.
28.
29.
30.
31.
32.
Биуретовая реакцияКсантопротеиновая
реакция
33.
34.
35.
36.
Качественные реакции на белки:1.Ксант опрот еиновая реакция (обнаружение
бензольных ядер в аминокислотных остатках
(фенилаланина, тирозина).
раствор белка + HNO3(конц)
желтое окрашивание
2. Биурет овая реакция (распознавание пептидных связей)
раствор белка + NaOH + CuSO4
окрашивание
фиолетовое
3. Осаждение белка солями тяжелых металлов.
раствор белка + CuSO4
выпадает осадок
раствор белка + AgNO3
выпадает осадок
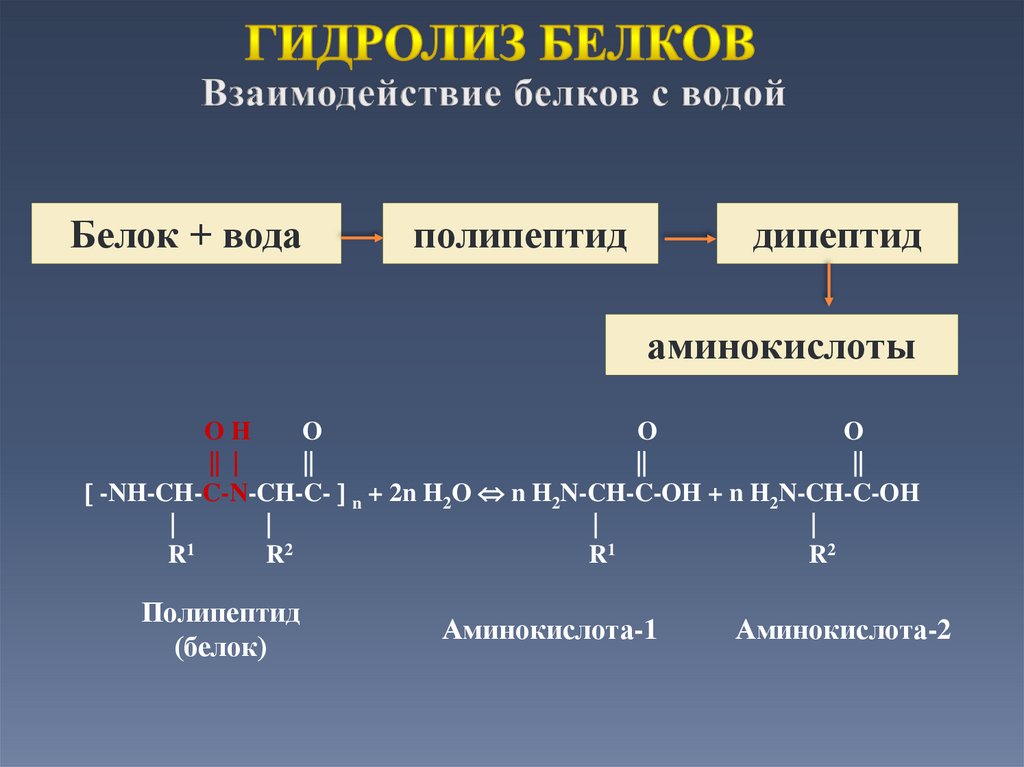
37.
Белок + водаполипептид
дипептид
аминокислоты
OH
O
O
O
|| |
||
||
||
-NH-CH-C-N-CH-C- n + 2n H2O n H2N-CH-C-OH + n H2N-CH-C-OH
|
|
|
|
R1
R2
R1
R2
Полипептид
(белок)
Аминокислота-1
Аминокислота-2
38.
кислотныйферментативный
39.
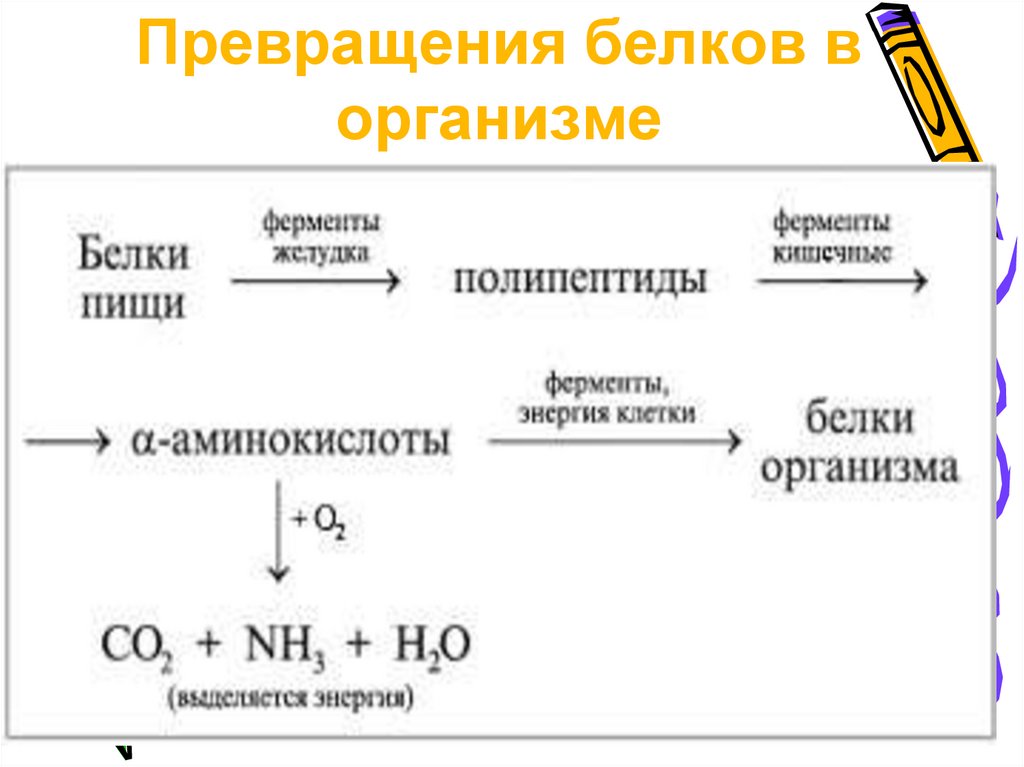
Превращения белков ворганизме
40.
41.
Проверь себя1. Для всех белков характерны свойства:
а) Растворимость и свертывание; б) Амфотерность и денатурация;
в) Гидролиз и растворимость в солях; г) Летучесть и горение.
2. При гидролизе белков образуются:
а) Углеводороды; б) Углеводы; в) Жирные кислоты; г) Аминокислоты.
3. Денатурация белков:
а) Осуществляется при действии ферментов или путем нагревания;
б) Приводит к нарушению вторичной структуры белка;
в) Приводит к нарушению третичной структуры белка;
г) Используется для получения углеводов.
4. При действии концентрированной азотной кислоты на белки
появляется окрашивание:
а) Фиолетовое; б) Желтое; в) Зеленое; г) Синее
5. Белки являются продуктом поликонденсации:
а) Углеводородов; б) Жирных кислот; в) Аминокислот; г) Сахаров
42.
Ответы1.
2.
3.
4.
5.
б)
г)
а)
б)
в)
43.
Домашнее заданиеНапишите формулу гексапептида
Лиз-Вал-Глу-Фен-Ала-Асп.


























 chemistry
chemistry








