Similar presentations:
Использование хлорофилла как флуорофора для визуализации и определения гидрофильных соединений
1. Использование хлорофилла как флуорофора для визуализации и определения гидрофильных соединений
Московский государственный университетим. М.В.Ломоносова
Химический факультет
Кафедра аналитической химии
Лаборатория биоаналитических методов анализа и оптических сенсорных систем
Видинчук Татьяна
Анатольевна
Студентка 6 курса
Руководитель
д.х.н., в.н.с. Беклемишев М.К.
Москва · 2023
2. Использование хлорофилла
Хлорофилл – зелёный пигмент растений, длинноволновый флуорофор (λem=680 нм)Применение
Литература
Определение низкомолекулярных
соединений
1. Отдельные работы (в основном, химически
модифицированный хлорофилл)
2. Определение неомицина*
Визуализация доставки
лекарственных веществ
Нет работ**
* Zakharenkova S.A. e.a. ACS Sustain. Chem. Eng. 2021, 9, 3408.
**Визуализация доставки изучена С.А. Захаренковой с использованием
карбоцианиновых флуорофоров: Zakharenkova S.A. e.a. Molecules,
2021, 26, 7426.
2
3. Цель работы:
Использование хлорофилла как флуорофора для определениялекарственных веществ и визуализации их доставки в
эукариотические клетки
Задачи:
• Показать возможность флуориметрического определения
цефтриаксона, блеомицина, винорелбина, метотрексата и
бензилпенициллина в воде и искуственной моче в виде тройных
агрегатов аналит-краситель-противоион.
• Выбрать системы для визуализации доставки этих соединений с
использований хитозанов и плюроников.
3
3
4. Структуры лекарственных веществ
ЦефтриаксонБензилпенициллин
Метотрексат
Блеомицин
Винорелбин
4
5. Методика работы. Схема визуализатора
Регистрация флуоресценции в БИК-диапазоне:1 – фотокамера, оснащенная светофильтром, пропускающим излучение с длиной волны более 700 нм,
2 – одиннадцать красных светодиодов с максимумом излучения 660 нм,
3 – алюминиевый радиатор (для охлаждения светодиодов),
4 – 96-луночный планшет с образцами,
5 – светонепроницаемый кожух.
5
6. Выделение хлорофилла из шпината
• Экстракция смесью ацетона и гексана (1:1 об.)• Удаление экстрагента испарением
• Растворение полученного остатка в ацетоне
• Разделение смеси на фракции методом ТСХ
• Десорбция ацетоном
5
7. Спектры выделенных фракций
Интенсивность поглощения, усл. ед.Спектры поглощения
Спектры флуоресценции
Хлорофилл а
Хлорофилл b
Феофитины
Хлорофилл а
Хлорофилл b
Феофитины
Длина волны поглощения, нм
Выделенные фракции распознавали,
сравнивая их спектры с литературными
данными
Хлорофилл а флуоресцирует, а хлорофилл b – нет.
Далее использовали хлорофилл а.
7
8. Структуры ПАВ
Цетилтриметиламмония бромид (ЦТАБ)Полигексаметиленгуанидин гидрохлорид (ПГМГ)
Додецилсульфат натрия (ДДС)
Лаурат натрия
Для определения лекарственных веществ
требовалось найти системы хлорофилл – ПАВ – аналит
с наибольшей разностью сигналов тройного агрегата и контрольного опыта
8
9. Выбор условий определения цефтриаксона
Зависимость флуоресценции тройного агрегатас цефтриаксоном от концентраций компонентов
Условия определения
цефтриаксона и получения
тройных агрегатов для
контейнеров:
• р-р хлорофилла 30-40 мкл;
• фосфатный буфер (рН 7,4) 30
мкл;
• вода до 300 мкл;
• ПГМГ (0,0056 М) 60 мкл;
• ЦТАБ (0,01 М) 10 мкл;
• анализируемый раствор 100
мкл.
а) ПГМГ, б) цефтриаксона, в) ЦТАБ, г) времени.
9
10. Выбор условий определения бензилпенициллина
Условия определениябензилпенициллина и получения
тройных агрегатов для контейнеров:
• р-р хлорофилла 10-20 мкл;
• фосфатный буфер (рН 7,4) 30 мкл;
• вода до 300 мкл;
• ЦТАБ (0,01 М) 10 мкл;
• анализируемый раствор 100 мкл.
Зависимость флуоресценции тройного агрегата с
бензилпенициллином от концентраций компонентов
а) природы ПАВ, б) бензилпенициллина.
10
11. Выбор условий определения винорелбина
Зависимость флуоресценции тройного агрегатас винорелбином от концентраций компонентов
Условия определения
винорелбина и получения
тройных агрегатов для
контейнеров:
• р-р хлорофилла15 мкл;
• фосфатный буфер (рН 7,4)
30 мкл;
• вода до 300 мкл;
• ЦТАБ (0,01 М) 10 мкл;
• анализируемый раствор 10
мкл.
а) ПГМГ, б) ЦТАБ, в)винорелбина, г) винорелбина и времени: измеряли
флуоресценцию каждой системы каждые 5 мин; стандартные отклонения означают
колебания флуоресценции в течение часа.
11
12. Возможность образования тройных агрегатов с одноимённо заряженными ПАВ
Зависимость флуоресценции тройного агрегата с винорелбином от природы ПАВ• Винорелбин способен образовывать тройные агрегаты как с катионными, так и с
анионным ПАВ (ЦТАБ и ДДС).
• Добавление ПГМГ в качестве коиона повышает разность сигнала и контрольного опыта.
12
13. Выбор условий определения блеомицина
Зависимость флуоресценции тройного агрегатас цефтриаксоном от концентраций компонентов
Условия определения
блеомицина и получения
тройных агрегатов для контейнеров:
• р-р хлорофилла 10 мкл;
• буфер боратный (рН 8,5/9,2) 30 мкл;
• вода до 300 мкл;
• ПГМГ (0,0056 М) 20 мкл;
• ДДС (0,008 м) 10 мкл;
• анализируемый раствор 10 мкл.
а) рН, б) ПГМГ, в) ДДС, г) блеомицина, д) метанола.
13
14. Зависимость сигналов от времени
Агрегаты хлорофилл-ПГМГ-ДДС-блеомицин и контрольный опыт• Сразу после приготовления сигналы различаются почти вдвое, однако через 7-10 мин
различие исчезает.
• Измерять флуоресценцию систем, где присутствует подобное сочетание, необходимо сразу
после приготовления (системы с блеомицином и винорелбином).
14
15. Эффект коиона в системе хлорофилл-ПГМГ-ДДС-блеомицин
Зависимость флуоресценции тройного агрегата с блеомицином от концентрации ПГМГ• Без ПГМГ тройные агрегаты хлорофилл-ПАВ-блеомицин флуоресцируют на уровне
контрольного опыта (без блеомицина).
• ПГМГ является коионом по отношению к блеомицину: флуоресценция возрастает в
диапазоне концентраций ПГМГ (0,0056 М) от 0 до 20 мкл.
• Эффект коиона наблюдается только с блеомицином и винорелбином.
15
16. Выбор условий определения метотрексата
Зависимость флуоресценции тройного агрегатас метотрексатом от концентраций компонентов
Условия определения
метотрексата и получения
тройных агрегатов для
контейнеров:
• р-р хлорофилла15-20 мкл;
• фосфатный буфер (рН 7,4)
30 мкл;
• вода до 300 мкл;
• ПГМГ (0,0056 М) 20-40 мкл;
• ЦТАБ (0,01 М) 10 мкл;
• анализируемый раствор
100 мкл.
а) природы ПАВ, б) ПГМГ, в) ЦТАБ, г) метотрексата.
16
17. Определение лекарственных веществ в водном растворе
Зависимость флуоресценции тройного агрегата от концентраций аналита:а) блеомицина, б) винорелбина, в) метотрексата, г) бензилпенициллина.
а)
б)
в)
г)
17
18. Определение метотрексата и бензилпенициллина в моче
Зависимость флуоресценции тройного агрегата от концентрацийаналита: а) метотрексата, б) бензилпенициллина.
а)
б)
18
19. - Показана возможность использования тройных агрегатов для определения - цефтриаксона, блеомицина, метотрексата, винорелбина,
Характеристики методик определения лекарственных веществв воде и искусственной моче
В воде
В искусственной моче
предел
обнаружения,
М
общее число
точек
линейный
диапазон, М
предел
обнаружения,
М
общее число
точек
линейный
диапазон, М
Блеомицин
1,1·10-4
12
(1,1-1,7)·10-4
-
-
-
Винорелбин
3,4·10-4
20
(3,4-6,5)·10-4
-
-
-
Метотрексат
1,4·10-4
12
(1,4-5,0)·10-4
7,6·10-4
14
(7,6-2,7)·10-4
4,5·10-5
15
(4,5-2,7)·10-5
1,0·10-3
22
-
Аналит
Бензилпенициллин
19
20.
Контейнеры для визуализации доставкилекарственных веществ
полимер – лекарственное вещество – ПАВ –
хлорофилл
20
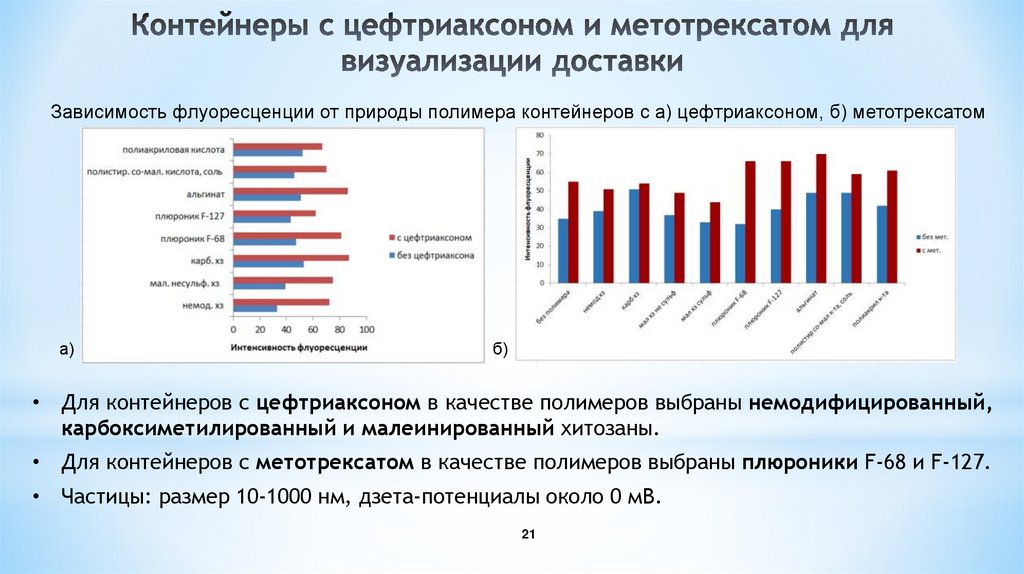
21. Контейнеры с цефтриаксоном и метотрексатом для визуализации доставки
Зависимость флуоресценции от природы полимера контейнеров с а) цефтриаксоном, б) метотрексатома)
б)
• Для контейнеров с цефтриаксоном в качестве полимеров выбраны немодифицированный,
карбоксиметилированный и малеинированный хитозаны.
• Для контейнеров с метотрексатом в качестве полимеров выбраны плюроники F-68 и F-127.
• Частицы: размер 10-1000 нм, дзета-потенциалы около 0 мВ.
21
22. Контейнеры с винорелбином для визуализации доставки
Зависимость флуоресценции контейнеров с винорелбином а) от природы полимера,б) природы полимера и осаждения
а)
б)
• Изучены плюроники F-68 и F-127 и анионированные хитозаны.
• Только контейнеры с карбоксиметилированным хитозаном сохраняют
флуоресценцию после выделения осаждением.
• Другие полимеры дают осадок, флуоресцирующий на уровне контрольного опыта.
22
23. Выбранные полимеры для получения контейнеров
АналитПолимер
Немодифицированный хитозан
Цефтриаксон
Метотрексат
Карбоксиметилированный хитозан
Малеинированный хитозан
Плюроник F-68
Плюроник F-127
Плюроник F-68
Плюроник F-127
Винорелбин
Малеинированный несульфатированный хитозан
Малеинированный сульфатированный хитозан
23
24. Ковалентная сшивка контейнеров с винорелбином с помощью эпихлоргидрина
Зависимость интенсивности флуоресценцииконтейнеров с винорелбином от природы хитозана
• В сшитых контейнерах с винорелбином и хитозанами нет
разности с контрольным опытом
• Переход к работе с несшитыми контейнерами
24
25. Стабильность флуоресценции тройных агрегатов и контейнеров с цефтриаксоном
Зависимость флуоресценции контейнеров от природы хитозана и времениИзменение сигнала (относительно контроля) во временем (в течение двух суток):
- тройные агрегаты (без полимера): уменьшается
- несшитые контейнеры с немод. хитозаном: сохраняется
- сшитые контейнеры с немод. хитозаном: возрастает (выталкивание цефтриаксона сшивателем из
агрегатов)
25
26. Сохранение флуоресценции в тройных агрегатах с винорелбином
Зависимость флуоресценции контейнеров с винорелбином от природы ПАВ и времени• Флуоресценция сохраняется в течение двух суток, если в качестве ПАВ использованы ПГМГ+ДДС или
лаурат в ацетоне
• В случае лаурата в воде разность с контрольным опытом появляется через сутки
• Принято решение далее работать с лауратом в воде
26
27. Сохранение флуоресценции в несшитых контейнерах с винорелбином
Зависимость флуоресценции контейнеров с винорелбином от природы ПАВ, природы хитозана и времени• Возможна замена токсичного ДДС на лаурат (в случае тройного агрегата с винорелбином и
контейнеров с винорелбином и карбоксиметилированным, малеинированным сульфатированным
хитозанами, плюроником F-68); принято решение далее работать с ними
• В системах с лауратом флуореценция через сутки возрастает
27
28. Устойчивость к диализу несшитых контейнеров
Состав контейнераВремя диализа до разрушения контейнера
Аналит
полимер
ПАВ
Плюроник F-68
Лаурат
1ч
Плюроник F-127
Лаурат
1ч
Карб. хит.
ЦТАБ-ПГМГ
45 мин
Плюроник F-68
ЦТАБ-ПГМГ
10 мин
Плюроник F-127
ЦТАБ-ПГМГ
10 мин
Винорелбин
Метотрексат
Контейнеры с винорелбином и плюрониками устойчивы к диализу в течение 1 ч
Контейнеры с метотрексатом и карбоксиметилированным хитозаном устойчивы к диализу по
крайней мере в течение 45 мин
Разрушение контейнеров с метотрексатом и плюрониками начинается в течение 10 мин
Все изученные системы потенциально пригодны для доставки в клетки
28
29. Методика работы с клетками аденокарциномы молочной железы человека
Живые клетки сорбированы на дне лунок при 37˚С:1) Промывка ячеек фосфатным буферно-солевым
раствором (PBS)
Ячейки для конфокального микроскопа
2) Заливание коллоидного раствора контейнеров
3) Инкубирование при 37˚С в течение 40 мин
4) Отбор раствора и промывка PBS
5) Фиксация (4%-формальдегид и выдерживание
без термостата 15 мин)
Работа с фиксированными клетками:
6) Промывка PBS
7) Заливка смеси глицерин – PBS (1:1 об.)
Фиксированные клетки могут храниться несколько
дней.
Далее исследование на конфокальном микроскопе.
29
30. Результаты поглощения контейнеров клетками
3031. Результаты эндоцитоза
1) Есть поглощение контейнеров клетками2) Флуоресценция наиболее заметна в цитоплазме, на ядерной мембране и в ядрышках ядра клеток
после интернализации контейнеров. Доставка в ядро интересна для визуализации доставки
противораковых веществ
3) Сигнал контейнеров тройного агрегата выше, чем сигнал в отсутствие аналита, это означает, что
переносится именно контейнер с тройным агрегатом.
Флуоресценция клеток после поглощения контейнеров
Винорелбин (лаурат, без
полимера)
Метотрексат (ПГМГ, ЦТАБ,
плюроник F-127)
Цефтриаксон (ПГМГ, ЦТАБ,
карб. хитоз.)
0
40
80
120
160
Интенсивность флуоресценции клеток
Контейнеры с лекарственным веществом
«Пустые» контейнеры (контроль)
31
32. Выводы
1. Получены флуоресцирующие тройные агрегаты хлорофилла а с аналитами и противоионом и показанавозможность их использования для определения цефтриаксона, блеомицина, метотрексата,
винорелбина, бензилпенициллина в водном растворе на уровне 0,1 мМ, а метотрексата и
бензилпенициллина – в искусственной моче на уровне 1 мМ.
2. Выявлено образование флуоресцирующего агрегата блеомицина с одноименно заряженным полимером
(блеомицин(2+) – полигексаметиленгуанидин(+) (ПГМГ) – додецилсульфат(–) – хлорофилл). В отсутствие
ПГМГ («коиона») флуоресценция агрегатов не отличается от флуоресценции контрольного опыта (без
блеомицина). Для ранее изученных модельных аналитов эффект «коиона» не наблюдали.
3. Взаимодействием тройных агрегатов (хлорофилла с модельными лекарственными веществами и
противоионами) с анионированными хитозанами или плюрониками получены контейнеры для
визуализации доставки цефтриаксона, метотрексата и винорелбина в эукариотические клетки.
4. Ковалентная сшивка контейнеров эпихлоргидрином не позволила получить устойчивого сигнала
модельных лекарственных веществ. Показана возможность длительного сохранения флуоресценции
выше сигнала контрольного опыта в тройных агрегатах без полиэлектролита и несшитых контейнерах
на основе карбоксиметилированного и малеинированного хитозана и плюроников F-68 и 128.
5. Показано сохранение флуоресценции контейнеров винорелбин – лаурат – плюроник F-68 (или F-128) во
время диализа против фосфатно-солевого буфера по крайней мере в течение 1 часа (в отличие от
аналогичных контейнеров с метотрексатом, ПГМГ и ЦТАБом, разрушающихся за 10 мин).
6. Показано проникнование контейнеров с винорелбином, цефтриаксоном и метотрексатом в клетки
аденокарциномы молочной железы человека с сохранением флуоресценции выше контрольного опыта.
Наблюдали распределение флуоресцирующих частиц в структуры цитоплазмы, ядерную мембрану и
ядрышко ядра.
32
































 chemistry
chemistry








