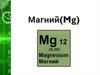Similar presentations:
Магний. Распространение в природе
1.
МАГНИЙЭЛЕМЕНТ 2 ГРУППЫ
ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
Выполнила ученица 11А класса Чачина Валерия
2.
Историяоткрытия
Магния
В конце 17 века Неемия Грю открыл
сернокислый магний (горькую соль) в
воде эпсомских минеральных
источников (Англия). Почти сразу же
сульфат магния стал употребляться как
лечебное средство и назывался тогда sal
anglicum или эпсомской солью.
Название элемента происходит от
латинского слова magnesia (Магнезия -местность в Фессалии)
3.
МагнийМагний -- элемент II группы
периодической системы Д. И.
Менделеева; третьего периода, главной
подгруппы, порядковый номер 12;
атомная масса 24,312
Магний -- металл серебристо-белого
цвета. по своему внешнему виду и
некоторым характерным свойствам
несколько напоминает алюминий.
Температура плавления 651° С.
Температура кипения 1120° С.
4.
Распространение в природе.
Получение
магния
Магний принадлежит к числу элементов,
наиболее распространённых в земной
коре, и занимает восьмое место по
распространению. Вымываемая при
выветривании окись магния скопляется
в морской воде, которая содержит в
среднем около 0,14% магния в виде
соединения с хлором (хлорида магния
MgCl)
5.
Распространение в природе.
Получение
магния
Самый распространенный из
магнийсодержащих минералов -доломит представляет собой
породообразующий минерал белого,
сероватого или других цветов. По своему
химическому составу это почти чистый
карбонат кальция и магния СаМg(СO).
Кроме производства магния, доломит
применяется также в качестве
огнеупорного материала и флюса в
металлургии и химической
промышленности, стекольном
производстве и других областях
промышленности.
Доломит
6.
Химические свойства магнияМагний - активный металл. Если разрушить оксидную пленку на его поверхности, он
легко окисляется кислородом воздуха. При нагревании магний энергично
взаимодействует с галогенами, серой, азотом, фосфором, углеродом, кремнием и
другими элементами:
2 Мg + O2 = 2 МgО (оксид магния);
Мg + Сl2 = МgСl2 (хлорид магния);
3 Mg + N2 = Мg3N2 (нитрид магния);
3 Мg + 2 Р= Мg3Р2 (фосфид магния);
2 Мg + Si = Мg2Si (силицид магния).
7.
Химические свойства магнияМагний не растворяется в воде, однако, при нагревании довольно активно
взаимодействует с парами воды:
Мg + Н2О = МgО + Н2.
Магний горит в атмосфере углекислого газа:
Мg + СО2 = МgО+ СО
и хорошо растворяется в кислотах:
Мg + Н2SO4 = МgSО4 + Н2;
4 Мg + 10 НNО3 = 4 Мg(NО3)2 + N2O + 5 Н2О.
8.
Наш организмВходит магний и в состав человеческого
организма. Так, магний найден в крови
(переутомление чаще всего вызвано
снижением количества магния в крови
человека), в зубах и в мозгу.
Установлено, что фермент,
способствующий переносу фосфора в
нашем организме, содержит магний.
Молекулы ферментов постепенно
разрушаются. Поэтому в организме
должны все время создаваться новые
молекулы. Отсюда постоянная
потребность организма в магнии. В
человеческом организме находится
примерно 60 г магния.
9.
ПрименениеГлавная область применения
металлического магния -- это получение
на его основе различных легких сплавов.
Прибавка к магнию небольших
количеств других металлов резко
изменяет его механические свойства,
сообщая сплаву значительную твердость,
прочность и сопротивляемость коррозии.
Высокая химическая активность
металлического магния позволяет
использовать его при получении таких
металлов, как титан, цирконий, ванадий,
уран.
10.
ИСТОЧНИКИ■ knowledge.allbest.ru/chemistry











 chemistry
chemistry