Similar presentations:
Электролитическая диссоциация
1.
Электролитическаядиссоциация
1
2.
Электролитическая диссоциация1. Электролиты и неэлектролиты
2.Электролитическая диссоциация
3. Механизм электролитической диссоциации
4. Сильные и слабые электролиты
5. Диссоциация кислот, оснований, солей
6. Значение электролитов
7. Проверка знаний
2
3.
11. Рис.1
Вещества
Электролиты
Неэлектролиты
Связь:
Ковалентная сильно
полярная,
ионная
Связь:
Ковалентная
неполярная,
малополярная
Примеры:
Кислоты, щелочи,
соли.
Примеры:
Большинство
органических
веществ, многие газы
3
4.
1. Электролиты и неэлектролитыЭлектролиты -
это вещества, растворы и
расплавы которых
проводят электрический
ток.
Кислоты: HCl; HNO3; H2SO4
Щелочи: NaOH; KOH; Ba(OH)2
Соли:
NaCl; CuSO4;
Al(NO3)3
4
5.
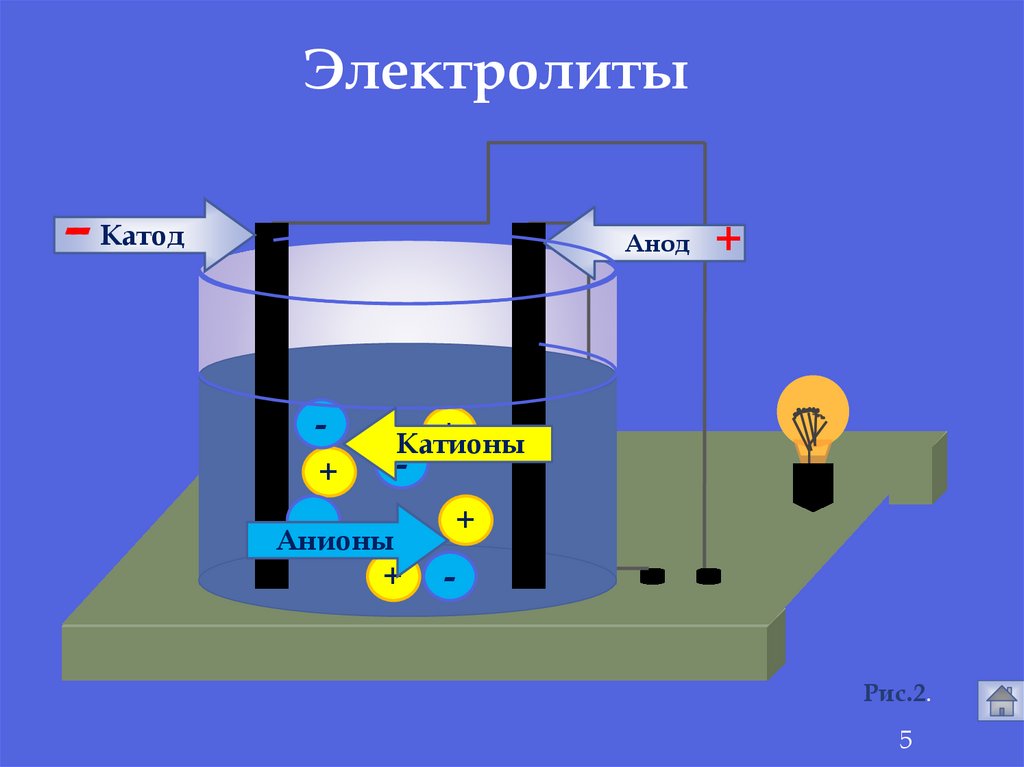
Электролиты-
Катод
Анод
+
-
+
+
Катионы
-
Анионы
+
+
Рис.2.
5
6.
1. Электролиты и неэлектролитыНеэлектролиты -
это вещества, растворы или
расплавы которых не
проводят электрический ток.
Органические вещества:
сахар, ацетон, бензин, керосин,
глицерин, этиловый спирт, бензол и
др.
Газы: кислород, водород, азот и др.
6
7.
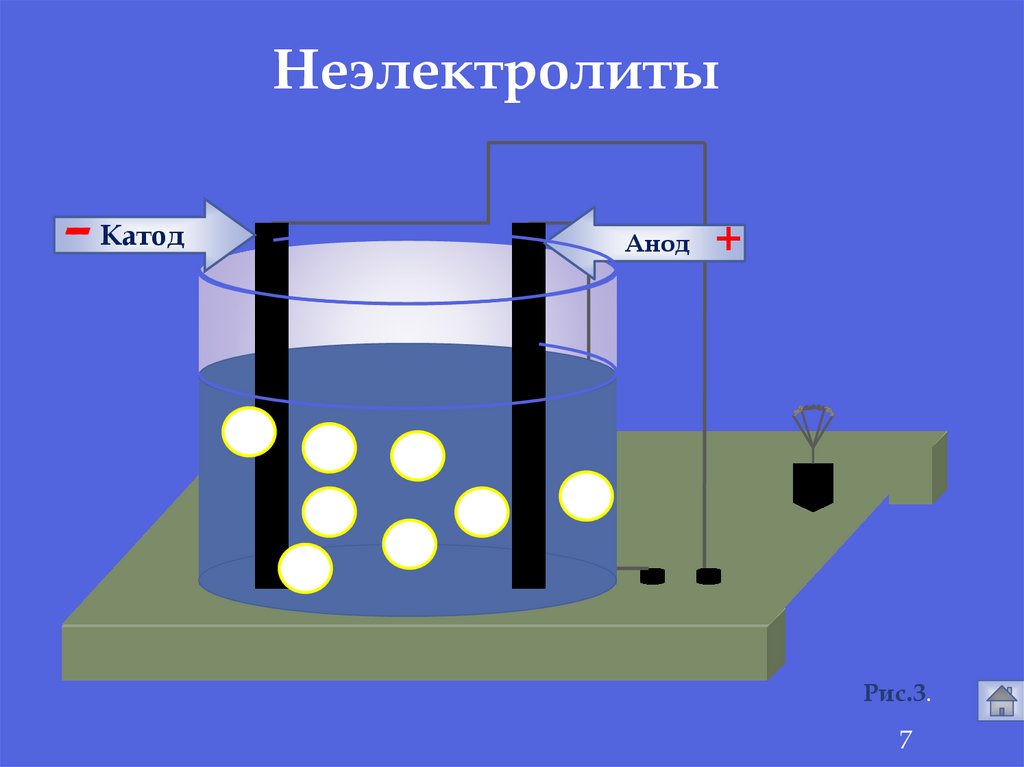
Неэлектролиты-
Катод
Анод
+
Рис.3.
7
8.
2.Электролитическая диссоциацияЭлектролитическая диссоциация процесс распада молекул
электролита на ионы в
растворе или расплаве.
С.Аррениус
Теория электролитической
диссоциации. 1887 г.
«Честь науке- ей дано уменье, выводить нас из заблужденья». М.Светлов
8
9.
Кратко обАррениусе Сванте
Августе
2.Электролитическая диссоциация
Шведский ученый, академик.
В 1887 году сформулировал
основные положения теории
электролитической
диссоциации.
В 1903 г. награжден
Нобелевской премией.
Проводил исследования во
многих других областях
науки.
С.Аррениус
(1859 – 1927)
«Честь науке- ей дано уменье, выводить нас из заблужденья».
9
10.
Основные положения теорииэлектролитической диссоциации
• 1. Электролиты при растворении в воде распадаются
(диссоциируют) на ионы – положительные и отрицательные.
• 2. Под действием электрического тока ионы приобретают
направленное движение: положительно заряженные частицы
движутся к катоду, отрицательно заряженные – к аноду.
Поэтому положительно заряженные частицы называются
катионами, а отрицательно заряженные – анионами.
• 3. Направленное движение происходит в результате
притяжения их противоположно заряженными электродами
(катод заряжен отрицательно, а анод – положительно).
• 4. Ионизация – обратимый процесс: параллельно с распадом
молекул на ионы (диссоциация) протекает процесс соединения
ионов в молекулы (ассоциация).
11.
Степень электролитическойдиссоциации (α) отношение числа диссоциированных
молекул к общему числу молекул,
находящихся в растворе.
Выражается в %
n
α=
N
11
12. Электролиты
СильныеСлабые
α=1
α<1
1. Растворимые соли
2. Сильные кислоты
(HCL, HI)
3. Щелочи (NaOH,
KOH)
1.
Слабые кислоты (HNO2)
2. Нерастворимые
основания и гидроксид
аммония (NH4OH)
3. Некоторые
малорастворимые и
нерастворимые соли
13. Неэлектролиты
α=01. Оксиды, не
взаимодействующие с H2O
2.
3.
Простые вещества
Большинство органических
веществ
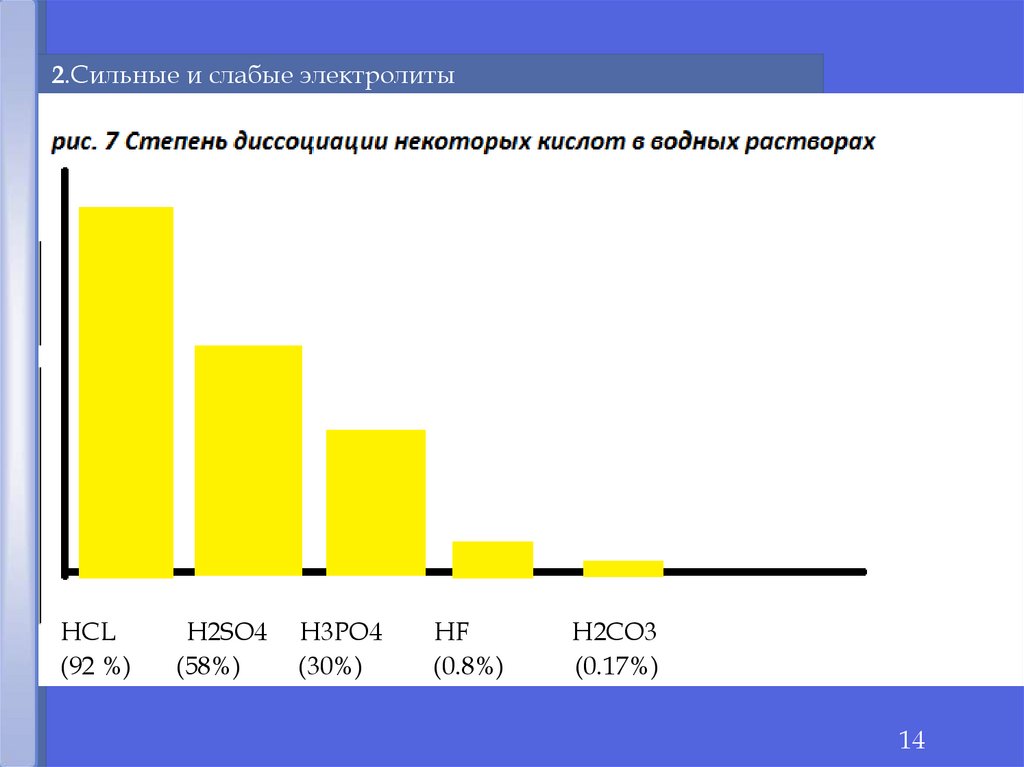
14. НСL H2SO4 H3PO4 HF H2CO3 (92 %) (58%) (30%) (0.8%) (0.17%)
2.Сильные и слабые электролиты%
НСL
(92 %)
H2SO4
(58%)
H3PO4
(30%)
HF
(0.8%)
H2CO3
(0.17%)
14
15.
Диссоциация кислот5. Диссоциация кислот, оснований, солей
Кислоты- это сложные вещества,
при диссоциации
которых в водных
-
растворах в качестве катионов
отщепляются только ионы водорода.
НCl + Н Cl -
Н+
Н2SO4 → 2 Н + SO4
Н2 CO3
2 Н + CO3
15
16.
Диссоциация основанийОснования - это сложные вещества,
при диссоциации которых в водных
растворах в качестве анионов
отщепляются только гидроксидионы.
KOH → K + OН
ОН-
Ca(OH)2
Ca + 2 OН
Мe(OH)n
Me +
OН
16
17.
Диссоциация солейСоли - это сложные вещества,
которые в водных растворах
диссоциируют на катионы металла и
анионы кислотного остатка.
NaCl →
Na +
K2SO4 → 2 K
Al(NO3)3 →Al
Me
+
Сl
SO4
+ 3NO
17
18.
Электролитическая диссоциация6. О значении электролитов для живых организмов
Электролиты – составная часть жидкостей и плотных
тканей живых организмов.
Ионы Na+,K+,Ca2+,Mg2+,H+; имеют большое
значение для физиологических и биохимических
процессов:
ионы H+; OH- играют большую роль в работе
ферментов, обмене веществ, переваривании пищи и
др.
при нарушении водно-солевого обмена в медицине
применяется физиологический раствор – 0,85%
раствор NaCl;
ионы I влияют на работу щитовидной железы.
18
19.
6. Рис.8. Характерные симптомы дефицита химических элементов в организмечеловека
Ионы
Типичный симптом
Са2+
Замедление роста скелета
Mg2+
Мускульные судороги
Fe2+
Анемия, нарушение иммунной
системы
Zn2+
Повреждение кожи, замедление
полового созревания
Mn2+
Учащение депрессий, дерматиты
19
20.
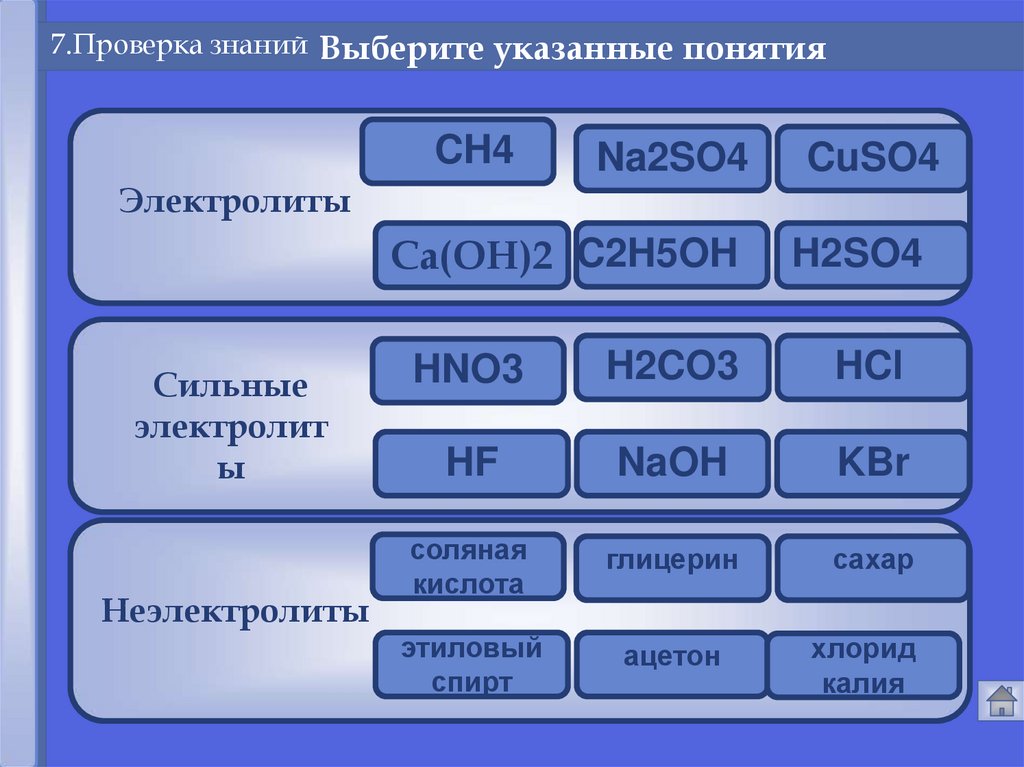
7.Проверка знаний Выберите указанные понятияCH4
Na2SO4
CuSO4
Ca(OH)2 C2H5OH
H2SO4
HNO3
H2CO3
HCl
HF
NaOH
KBr
соляная
кислота
глицерин
сахар
этиловый
спирт
ацетон
хлорид
калия
Электролиты
Сильные
электролит
ы
Неэлектролиты
21.
Электролитическая диссоциация7. Проверка знаний
Электролитическая
диссоциация
Под
каким действием
протекает
в растворах
электролитов
Слабым
Электролитами
электролитом
– это
в растворах
не
процесс
являются
является
распада
протекает
________
_______
под
.
.
электролитическая
диссоциация
электролита__________
действием
на __________
.
.
АЭлектрический
электрического
атомы
оксиды
KCl ток
тока
B
С молекул
Молекю
молекулы
NaOH
соли
растворителя
растворителя
D
температуры
электроны
Катализатора
катализатора
ионы
Температуры
кислоты
HNO3
21
21

















 chemistry
chemistry








