Similar presentations:
Кислоты. Лимонная кислота
1.
КИСЛОТЫ2.
Лимоннаякислота
Яблочная
кислота
Щавелевая
кислота
Муравьиная
кислота
Уксусная
кислота
Молочная
кислота
3.
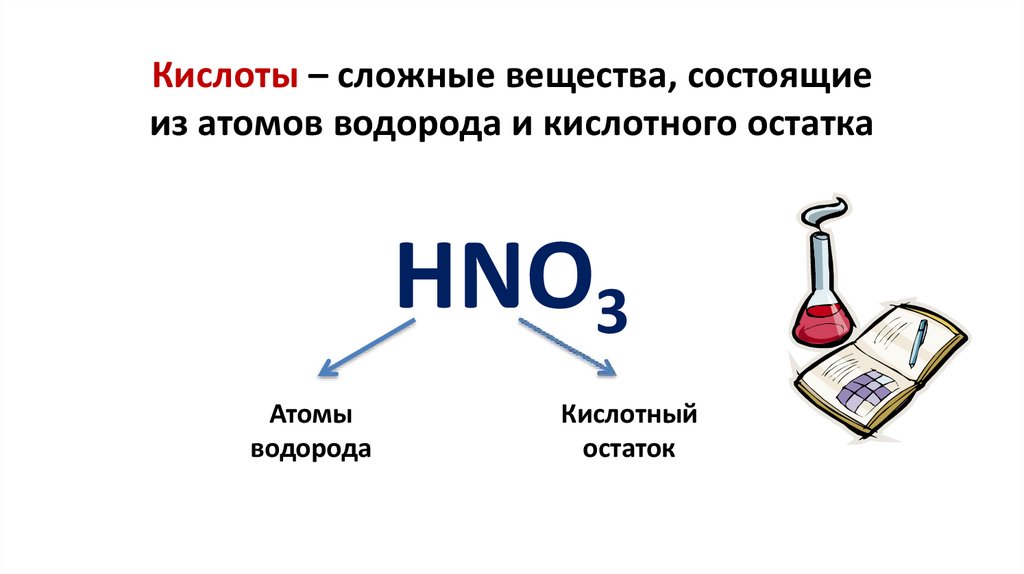
Кислоты – сложные вещества, состоящиеиз атомов водорода и кислотного остатка
HNO3
Атомы
водорода
Кислотный
остаток
4.
По содержаниюкислорода
По
растворимости
в воде
Кислородсодержащие
HNO3, H2SO4
Бескислородные
HCl, H2S
Растворимые в воде
Большинство кислот
Нерастворимые в воде
H2SiO3
5.
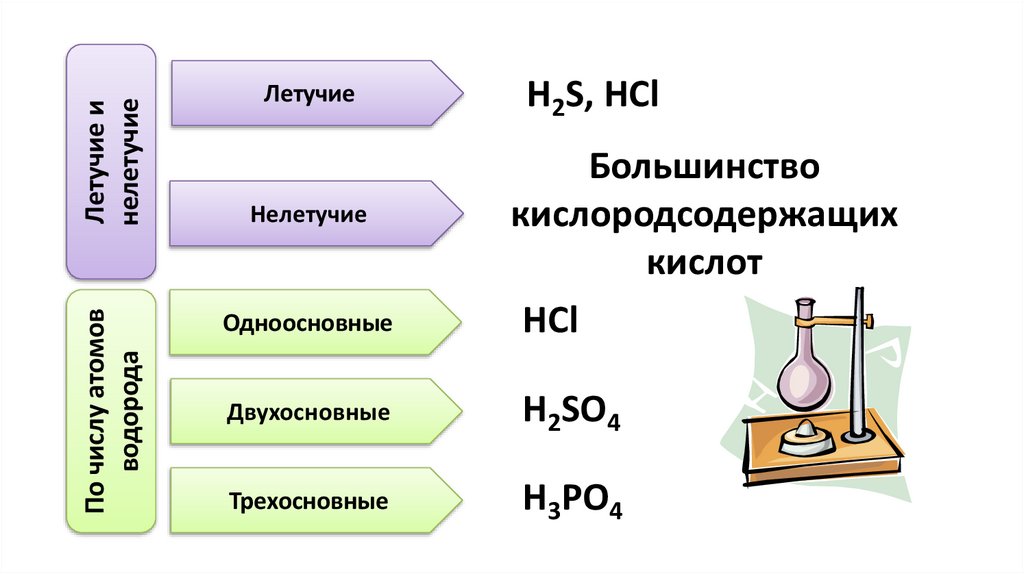
Летучие инелетучие
По числу атомов
водорода
Летучие
H2S, HCl
Одноосновные
Большинство
кислородсодержащих
кислот
HCl
Двухосновные
H2SO4
Трехосновные
H3PO4
Нелетучие
6.
1. Гидроксид-ионы (ОН-)2. Остальные атомы кислорода с кислотообразующим
элементом
7.
H2SO4SO42Сложный ион
HCl
ClПростой ион
8.
H2SO4Бесцветная, маслянистая жидкость
Не имеет запаха
Вдвое тяжелее воды
Поглощает влагу из воздуха и
других газов
Обугливает древесину, ткани, кожу
Применяют в производстве
удобрений и красителей, взрывчатых
веществ, медикаментов, моющих
средств, при очистке керосина,
нефтяных масел
Является электролитом в
аккумуляторах
9.
H2CO3 = H2O + CO2H2SO3 = H2O + SO2
10.
Окраска индикаторов в кислотахНазвание
индикатора
Лакмус
Метилоранж
Фенолфталеин
Окраска
индикатора в
нейтральной
среде
Окраска
индикатора в
растворах кислот
11.
Шкала рНУниверсальная
индикаторная бумага
Кислая среда
Нейтральная среда
рН = 7 – среда нейтральная
рН < 7 – среда кислая
рН > 7 – среда щелочная
Щелочная среда
12.
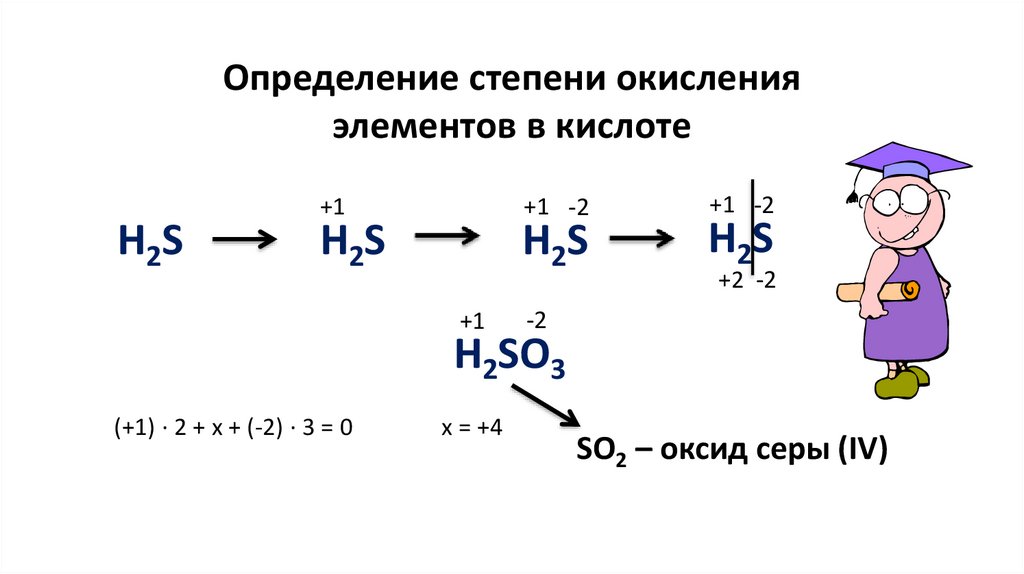
Определение степени окисленияэлементов в кислоте
H2S
+1 -2
+1
H2S
H2S
+1
+1 -2
H2S
+2 -2
-2
H2SO3
(+1) · 2 + x + (-2) · 3 = 0
x = +4
SO2 – оксид серы (IV)
13.
Название кислотыФормула
кислоты
Название
кислотного остатка
Хлороводородная (соляная)
Бромоводородная
Фтороводородная (плавиковая)
Азотная
Азотистая
Угольная
Кремниевая
Сероводородная
Сернистая
Серная
Ортофосфорная
(фосфорная)
HCI
HBr
HF
HNO3
HNO2
H2CO3
H2SiO3
H2 S
H2SO3
H2SO4
H3PO4
Хлорид
Бромид
Фторид
Нитрат
Нитрит
Карбонат
Силикат
Сульфид
Сульфит
Сульфат
Ортофосфат
(фосфат)










 chemistry
chemistry








