Similar presentations:
Виды кривых титрования
1.
Виды Кривые титрованияИботов Худойберди
Бобомуродоич
2.
Кривые титрованияЭто графическое изображение зависимости
концентрации определяемого компонента А или
пропорционального ей свойства системы от количества
прибавляемого титранта или степени оттитрованности.
Это график зависимости параметра системы, связанной
с концентрацией титруемого вещества или продукта, от
состава раствора в процессе титрования.
Степень оттитрованности (ƒ) – это отношение
количества оттитрованного в данный момент вещества
(nm) к исходному количеству его (n0):
nm C т Vm
f
n0
C 0 V0
3.
Классификация кривыхтитрования
Кривые
титрования
Теоретические
Линейные
Экспериментальные
Логарифмические
Дифференциальные
4.
Линейные кривые титрованияНа оси ординат
откладывают равновесную
концентрацию или
интенсивность
пропорционального ей
свойства системы.
5.
Дифференциальные кривыетитрования
На оси ординат
откладывают первую
производную от логарифма
равновесной концентрации
или интенсивности
пропорционального ей
свойства системы.
6.
Логарифмические кривыетитрования
На оси ординат
откладывают не
абсолютные значения
равновесной
концентрации или
интенсивности
пропорционального ей
свойства системы, а их
логарифмы.
7.
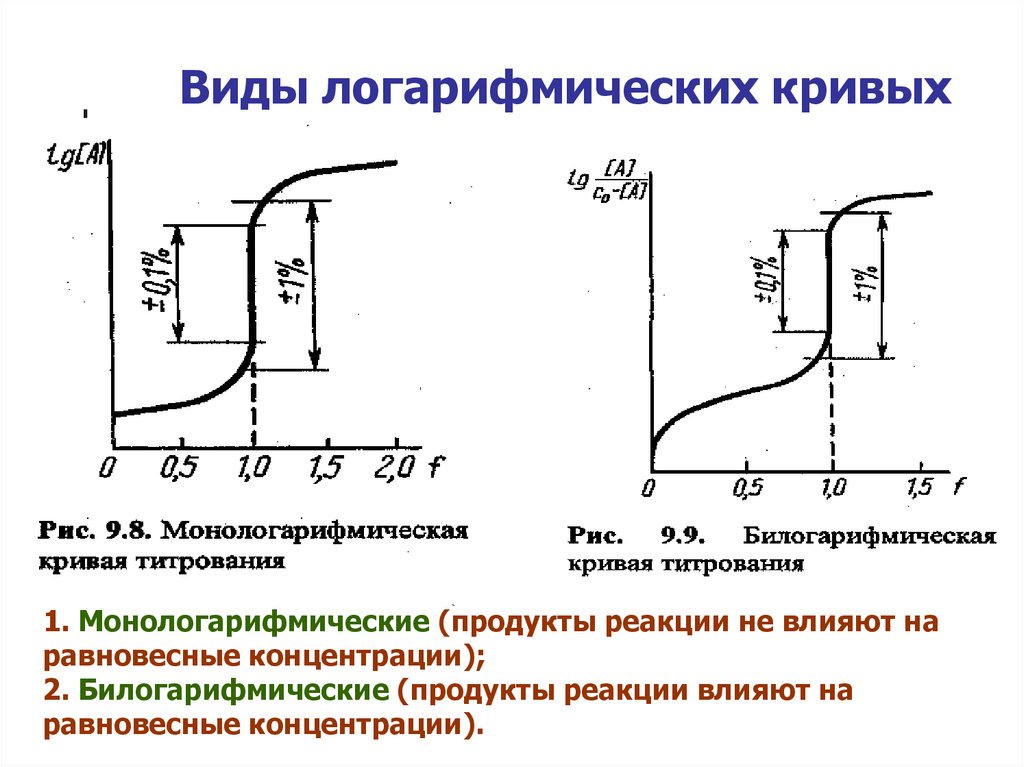
Виды логарифмических кривых1. Монологарифмические (продукты реакции не влияют на
равновесные концентрации);
2. Билогарифмические (продукты реакции влияют на
равновесные концентрации).
8.
Характеристики кривыхтитрования
1. Скачок титрования – область резкого изменения рассчитываемого
(измеряемого) параметра;
2. Крутизна кривой (η) – мера чувствительности и точности
титрования.
9.
Кривая титрованияКрива́ я титрова́ ния — графическое
изображение зависимости определяемой в
ходе титрования величины от объёма
добавленного стандартного раствора титранта.
Построение кривых проводится
в инструментальных методах аналитической
химии, где отсутствует возможность визуального
определения точки эквивалентности (например,
по индикатору). Кривые титрования помогают
выбрать индикатор, оценить погрешность,
наглядно проследить за ходом титрования
10.
Обработка данныхВажным
свойством
кривой
титрования
является
неравномерность изменения определяемой величины в
ходе анализа. Крутизна кривой является мерой
чувствительности и точности титрования. Сначала
величина меняется незначительным образом, формируя
пологую часть кривой. По мере приближения к точке
эквивалентности изменения становятся более резкими (не
редкостью являются моментальные, скачкообразные
изменения), а после прохождения точки они уменьшаются
и формируют вторую пологую часть кривой (аналогично
могут происходить второй, третий скачки — в случае
титрования многоосновных кислот). Именно на основе
этих изменений при помощи математической обработки
осуществляется определение точки эквивалентности —
обычно её рассчитывают как:
11.
первую производную от функции кривой — абсциссапикового значения будет соответствовать объёму
добавленного титранта;
вторую производную от функции кривой — объём
титранта является абсциссой в месте пересечения
производной оси X (Y=0). Расчёт по второй
производной предоставляет более точные
результаты.
12.
Кривая титрования в случае окислительновосстановительного титрования представляет собойзависимость электродного потенциала системы от
степени оттитрованности.
Пусть при титровании протекает химическая реакция
в которой Redi — определяемое вещество, Ох —
титрант.
2
13.
Изменение электродных потенциалов полуреакций сучастием определяемого вещества и титранта в процессе
титрования может быть описано, соответственно,
следующими уравнениями:
В процессе титрования после добавления каждой очередной порции
титранта в системе будет устанавливаться химическое равновесие.
Как было показано в предыдущей главе, если система находится в
состоянии равновесия, то E0xi ;Redl = Е0х2 Red2 • Такая величина
электродного потенциала, которую, кстати, можно определить
экспериментально, и называется потенциалом системы.
14.
При построении теоретическихкривых титрования рассчитывают
рН четырёх основных этапов:
1) до начала титрования;
2) титрование до точки эквивалентности;
3) точка эквивалентности;
4) после точки эквивалентности.
15.
В процессе титрования изменяются равновесныеконцентрации исходных веществ, титранта и
продуктов реакции. При этом пропорционально
концентрациям этих веществ изменяются свойства
раствора.
Например,
при
окислительновосстановительном
титровании
изменяются
равновесные
концентрации
окислителя
и
восстановителя и, следовательно, окислительновосстановительный потенциал (ОВП); при изменении
концентраций
компонентов
кислотно-основной
реакции изменяется pH раствора. График зависимости
параметра системы, связанного с концентрацией
титруемого вещества, титранта или продукта реакции,
от состава раствора в процессе титрования
называют кривой титрования.














 chemistry
chemistry








