Similar presentations:
Карбоновые кислоты. Сложные эфиры. Жиры
1. Карбоновые кислоты. Сложные эфиры. Жиры.
Параграф 56, выписать определения и общие формулыкарбоновых кислот, сложных эфиров, жиров.
Тесты.
Заполнить таблицу
Органические
соединения
Карбоновые кислоты
Сложные эфиры
Жиры
Применение
2.
3.
Карбоновые кислоты – производныеуглеводородов, в молекулах которых
имеется группа атомов –COOH
(карбоксильная группа)
-СООН функциональная группа. (Определяет
химические свойства класса веществ)
4.
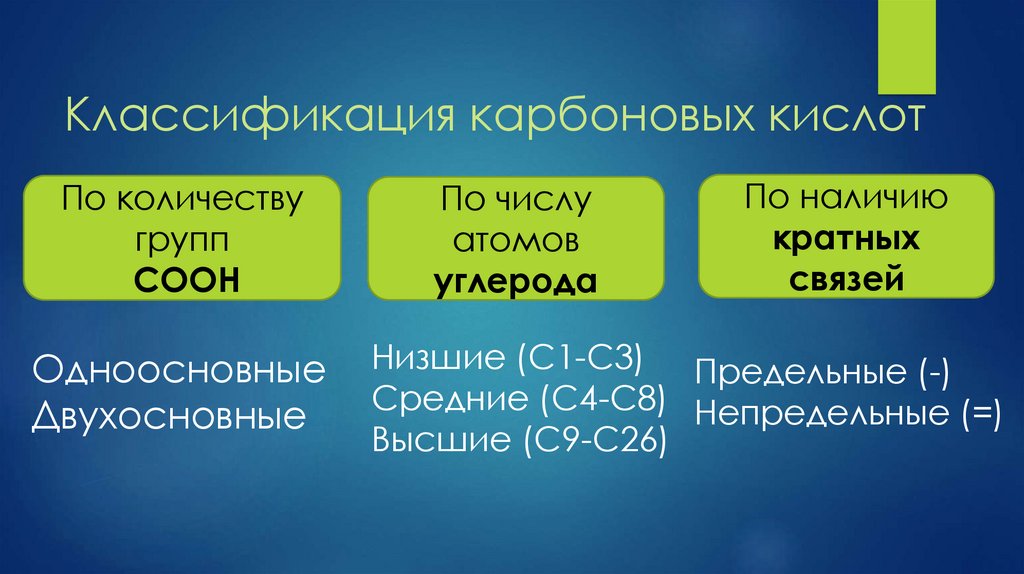
Классификация карбоновых кислотПо количеству
групп
СООН
Одноосновные
Двухосновные
По числу
атомов
углерода
По наличию
кратных
связей
Низшие (С1-С3) Предельные (-)
Средние (С4-С8) Непредельные (=)
Высшие (С9-С26)
5.
Некоторые предельные одноосновные кислотыФормула
НСООН
СН3СООН
С2Н5СООН
С3Н7СООН
С4Н9СООН
С15Н31СООН
С17Н35СООН
Название
По номенклатуре
Метановая
Этановая
Пропановая
Бутановая
Пентановая
Пентадекановая
Гептадекановая
Тривиальное
Муравьиная
Уксусная
Пропионовая
Масляная
Валериановая
Пальмитиновая
Стеариновая
6.
Краткие сведения о некоторыхкарбоновых кислотах
НСООН –метановая или муравьиная кислота
Вызывает ожоги
Содержится
Применяется
Органический синтез Медицина
Восстановитель
Текстильная
промышленность
Жидкость , без цвета, с резким запахом, хорошо растворима в воде
7.
Бесцветная жидкость с резким запахом.Хорошо растворима в воде
СН3СООН – этановая или уксусная кислота
содержание
применение
8.
С15Н31СООН – пентадекановая илипальмитиновая кислота
С17Н35СООН – гептадекановая или
стеариновая кислота
Соли щелочных металлов – основной
компонент мыла
применение
получение
Бесцветные
твердые вещества,
нерастворимые
в воде.
Растительные и животные
жиры. Парафин.
9.
Высшая непредельная одноосновнаякислота (=)
Маслянистая жидкость
С17Н33СООН – олеиновая кислота
Получают из природных жиров
Применение
Красители
Технические масла
Косметические средства
10.
Двухосновная кислотаБесцветное кристаллическое вещество,
растворимое в воде
Щавелевая кислота
применение
содержится
11.
Химические свойства карбоновых кислот1. Карбоновые кислоты диссоциируют
с образованием Н+
СН3СООН → СН3СОО- + Н+
этановая кислота
ацетат-ион
12.
2.Карбоновые кислоты взаимодействуютс активными металлами
2СН3СООН + 2К → 2СН3СООК + Н2
этановая кислота
ацетат калия
13.
3. Карбоновые кислоты взаимодействуютс основными оксидами
2СН3СООН + MgO → (CH3COO)2Mg + H2O
этановая кислота
ацетат магния
14.
4. Карбоновые кислоты взаимодействуютс основаниями
СH3COOH + NaOH → CH3COONa + H2O
этановая кислота
ацетат натрия
15.
5. Карбоновые кислоты взаимодействуютс солями более слабых кислот
2СH3COOH+CaCO3→(CH3COO)2Ca+CO2 + H2O
этановая кислота
ацетат кальция
16.
6. Карбоновые кислоты взаимодействуютсо спиртами, образуя сложные эфиры
CH3COOH + C2H5OH→ CH3CO-O-C2H5 + HOH
этановая кислота этанол
этилацетат
17.
Сложные эфиры низших кислот испиртов – летучие жидкости, с приятным
запахом.
Содержатся в цветах, ягодах и фруктах,
придавая характерный запах.
18.
Применение сложных эфировЯвляются хорошими растворителями
многих органических веществ, в том
числе полимеров
Применяются в пищевой
промышленности для
приготовления фруктовых
вод, эссенций,
кондитерских изделий ,
парфюмерии.
19.
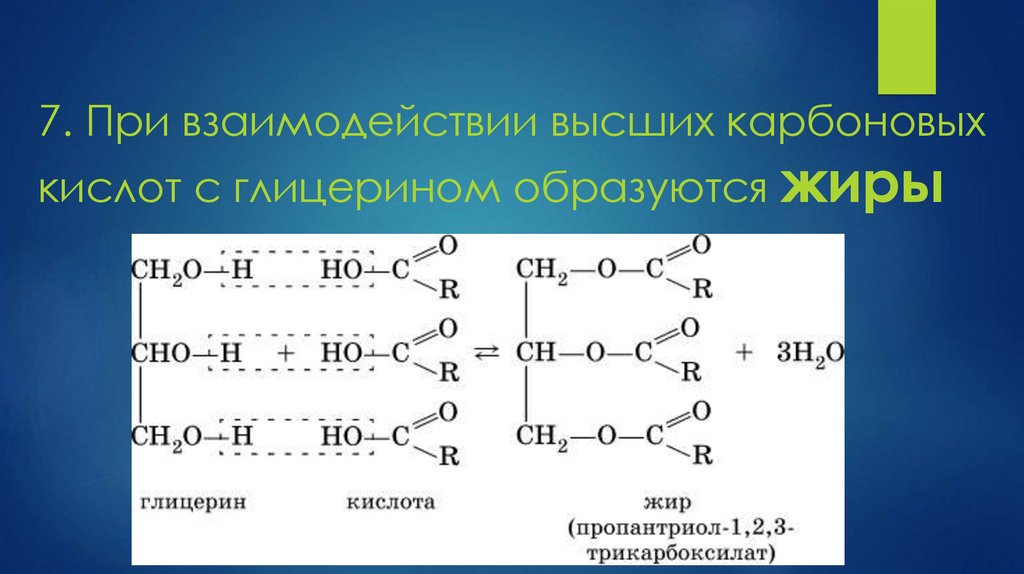
7. При взаимодействии высших карбоновыхкислот с глицерином образуются жиры
20.
Жиры являются составной частьюрастительных и животных организмов
Твердые жиры
Глицерин + высшие
предельные карбоновые
кислоты
Пальмитиновая С15Н31СООН
Стеариновая С17Н35СООН
Коровье масло
Свиное сало
Жидкие жиры
Глицерин + высшие
непредельные карбоновые
кислоты
Олеиновая С17Н33СООН
Линолевая С17Н29СООН
Подсолнечное масло
Оливковое масло
21.
Жиры легче воды, в воде не растворяются.Хорошо растворяются в органических
растворителях
Жиры хорошие растворители витамин (A,E,D)
22.
Жиры – источники энергии. (При окислениижиров выделяется энергия)
23.
Применение жировпродукты питания
лекарства
растворитель
смазочные материалы
косметические средства
мыло
24.
Ответьте на вопросы:• Какие соединения называются карбоновыми кислотами?
• Укажите функциональную группу карбоновых кислот.
• Как она называется?
• Что представляет собой муравьиная кислота?
• Где встречается в природе?
• Где используется?
• Что представляет собой столовый уксус и уксусная
эссенция?
Задания на слайдах 24-26 выполнять не нужно.
25.
• Какие кислоты называют высшими или жирными?• Сколько атомов углерода содержится в их молекулах?
• Что представляют собой натриевые и калиевые соли
этих кислот?
• Какие соединения называют жирами?
• Какие карбоновые кислоты образуют твердые жиры?
• Какие карбоновые кислоты образуют жидкие жиры?
26.
Домашнее задание:§56, записи в тетради – выучить.
Написать химические свойства для пропановой кислоты
(С2Н5СООН)- соль пропионат.
Решить задачу:
Определите массу вступившей в реакцию уксусной
кислоты, если
в ходе ее реакции с магнием выделилось:
А) 5,6 л (н.у.) водорода;
Б) 12 г водорода.
























 chemistry
chemistry








