Similar presentations:
Сложные эфиры. Жиры. Мыла
1.
Сложные эфиры.Жиры. Мыла.
2.
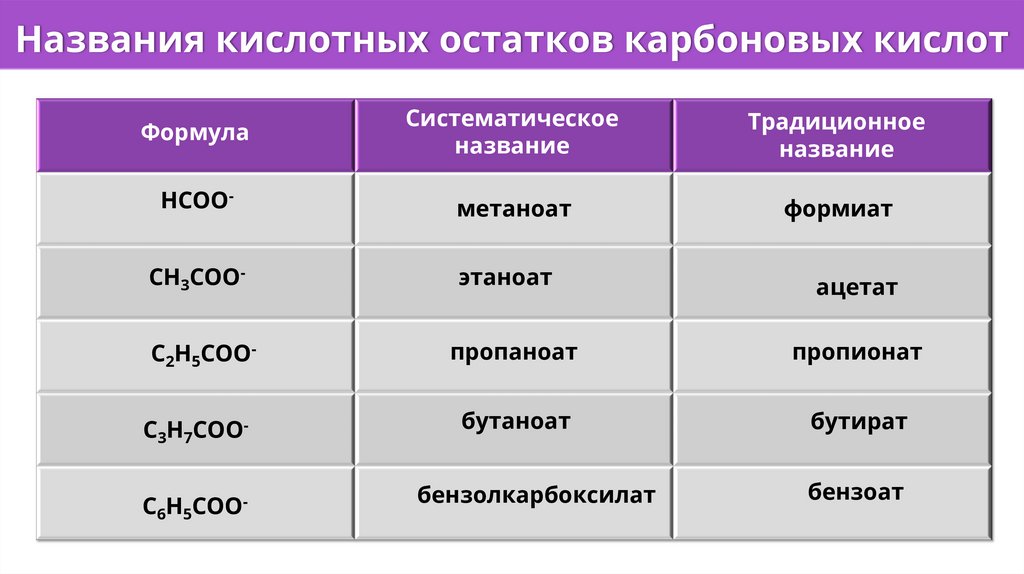
Названия кислотных остатков карбоновых кислотФормула
Систематическое
название
Традиционное
название
HCOO-
метаноат
формиат
CH3COO-
этаноат
ацетат
C2H5COO-
пропаноат
пропионат
C3H7COO-
бутаноат
бутират
C6H5COO-
бензолкарбоксилат
бензоат
3.
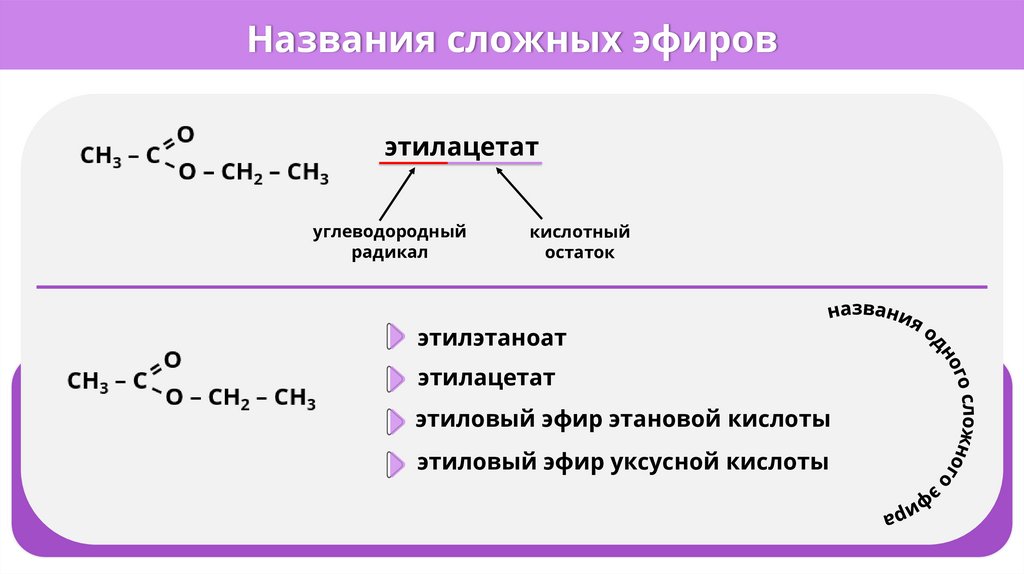
Названия сложных эфировэтилацетат
углеводородный
радикал
кислотный
остаток
этилэтаноат
этилацетат
этиловый эфир этановой кислоты
этиловый эфир уксусной кислоты
4.
Физические свойстваСложные эфиры бесцветные жидкости
летучие
плохо растворимы в воде
чаще с хорошим запахом
легче воды.
5.
Сложные эфиры в природеЭфирные масла
Воски
Эфиры низших карбоновых кислот и низших спиртов определяют
запах цветов, фруктов и ягод (эфирные масла).
Воски - сложные эфиры
жирных кислот и спиртов с
длинными углеводородными
радикалами.
СН3-СО-О-СН2-СН(СН3)2
Н-СО-О-СН2-(СН2)3-СН3
СН3-(СН2)14-СО-О-(СН2)29-СН3
СН3-СН2-СН2-СО-О-СН2-(СН2)3-СН3
СН3-СН2-СН2-СО-О-СН3
сложный эфир пальмитиновой
кислоты и мирицилового спирта
6.
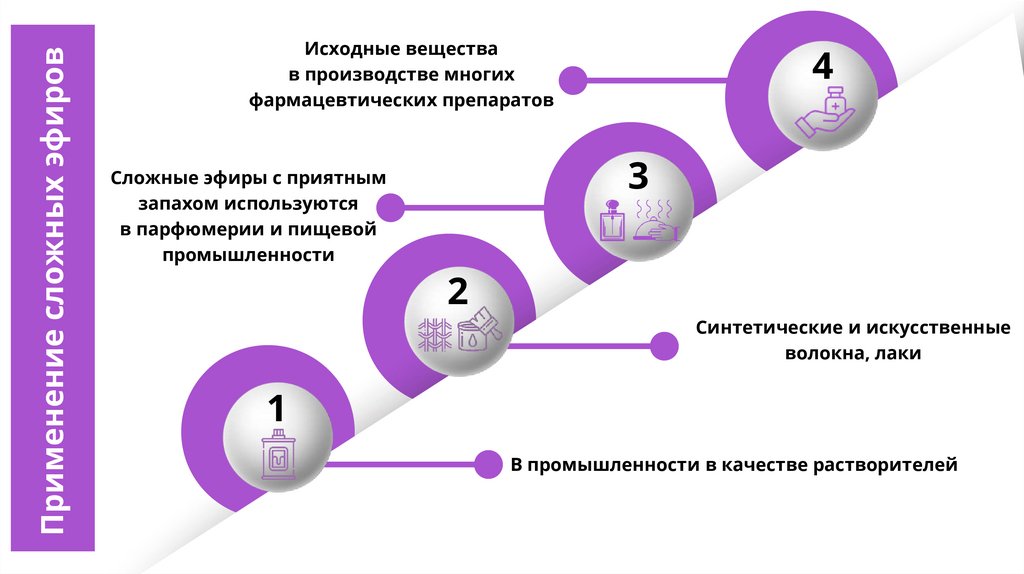
Применение сложных эфировИсходные вещества
в производстве многих
фармацевтических препаратов
Сложные эфиры с приятным
запахом используются
в парфюмерии и пищевой
промышленности
4
3
2
Синтетические и искусственные
волокна, лаки
1
В промышленности в качестве растворителей
7.
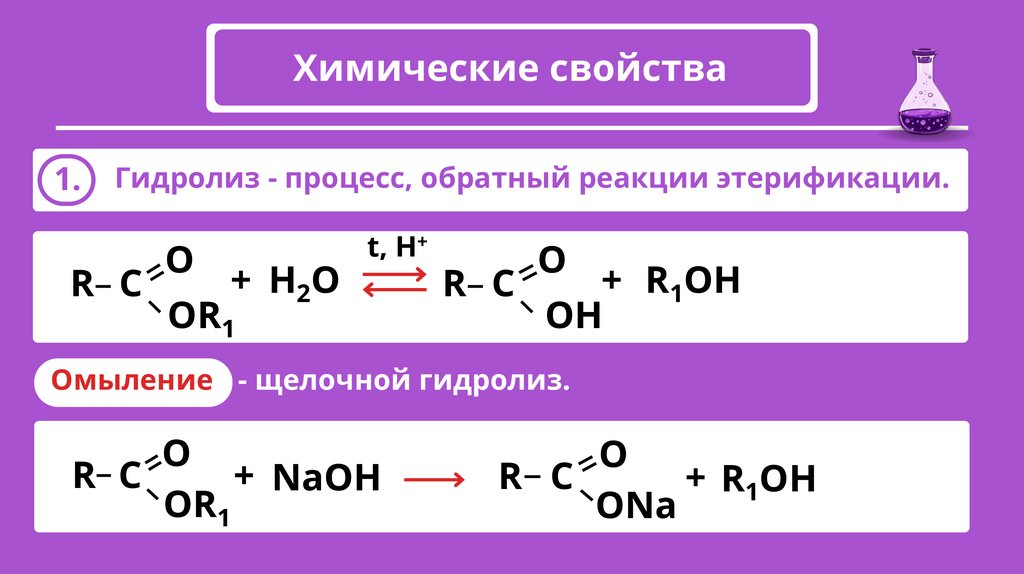
Химические свойства1.
Гидролиз - процесс, обратный реакции этерификации.
O
+ H2O
R C
OR1
t, H+
O
+ R1OH
R C
OН
Омыление - щелочной гидролиз.
O
R C
+ NaOH
OR1
O
R C
+ R1OH
ONa
8.
9.
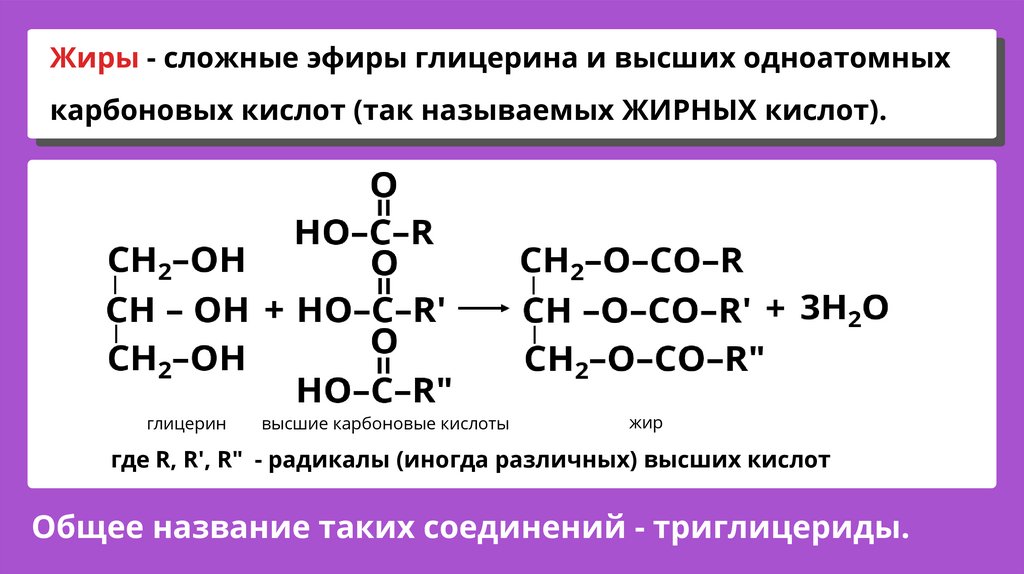
Жиры - сложные эфиры глицерина и высших одноатомныхкарбоновых кислот (так называемых ЖИРНЫХ кислот).
глицерин
высшие карбоновые кислоты
жир
где R, R', R" - радикалы (иногда различных) высших кислот
Общее название таких соединений - триглицериды.
10.
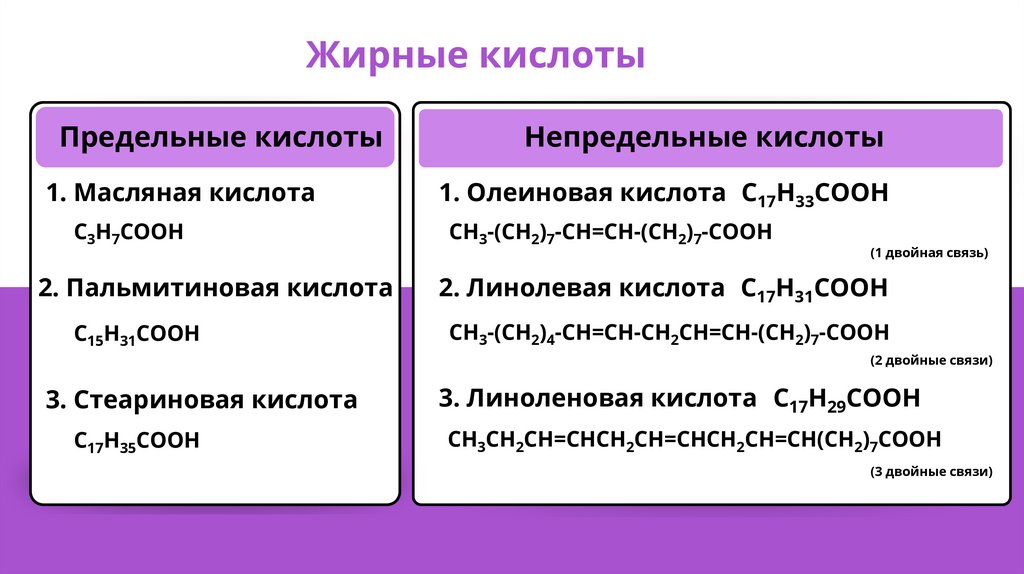
Жирные кислотыПредельные кислоты
1. Масляная кислота
С3Н7СООН
2. Пальмитиновая кислота
С15Н31СООН
Непредельные кислоты
1. Олеиновая кислота С17Н33СООН
СН3-(СН2)7-СН=СН-(СН2)7-СООН
(1 двойная связь)
2. Линолевая кислота С17Н31СООН
СН3-(СН2)4-СН=СН-СН2СН=СН-(СН2)7-СООН
(2 двойные связи)
3. Стеариновая кислота
С17Н35СООН
3. Линоленовая кислота С17Н29СООН
СН3СН2СН=СНСН2СН=СНСН2СН=СН(СН2)7СООН
(3 двойные связи)
11.
Физические свойстваЖиры
растворимы в органических
растворителях
нерастворимы в воде
Животные жиры
Растительные жиры (масла)
Твёрдые (кроме рыбьего), образованы
предельными кислотами.
Жидкие (кроме пальмового),
образованы непредельными кислотами.
говяжий
свиной
бараний
сливочное
масло
льняное
масло
подсолнечное оливковое
масло
масло
конопляное
масло
12.
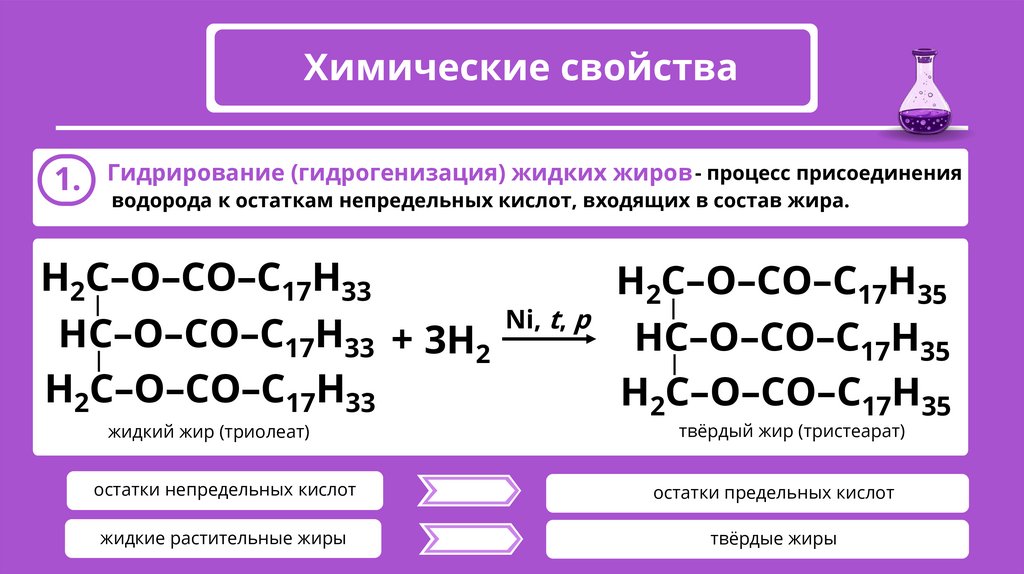
Химические свойства1.
Гидрирование (гидрогенизация) жидких жиров - процесс присоединения
водорода к остаткам непредельных кислот, входящих в состав жира.
Н2С–О–СО–С17Н33
Н2С–О–СО–С17Н35
Ni, t, p
НС–О–CO–С17Н33 + 3Н2
НС–О–CO–С17Н35
Н2С–О–CO–С17Н33
Н2С–О–CO–С17Н35
жидкий жир (триолеат)
твёрдый жир (тристеарат)
остатки непредельных кислот
остатки предельных кислот
жидкие растительные жиры
твёрдые жиры
13.
МаргаринПищевой жир, состоит из:
смеси гидрогенизированных
масел
и др.
животных жиров
молока
вкусовых добавок
и др.
14.
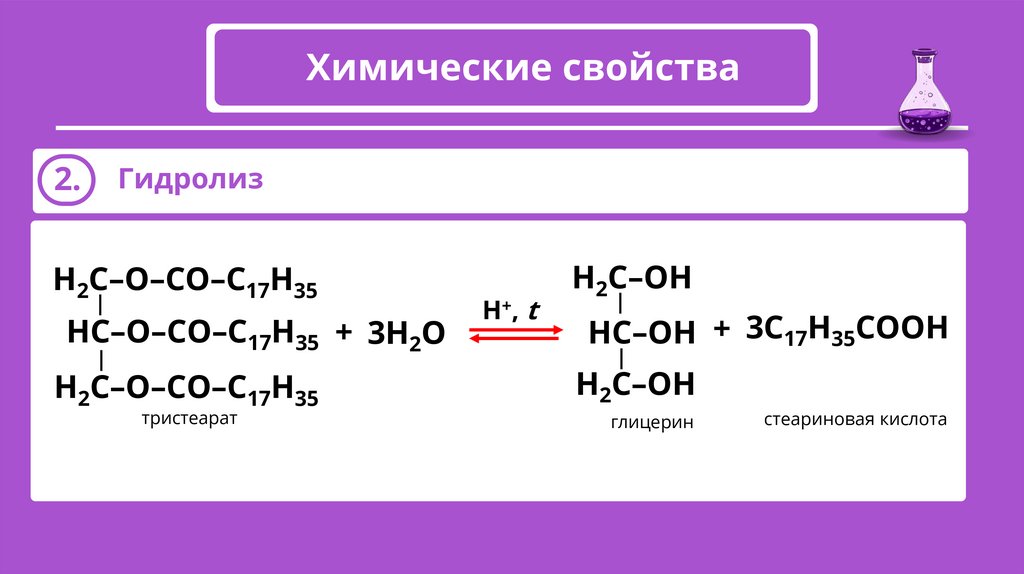
Химические свойства2.
Гидролиз
Н2С–О–СО–С17Н35
НС–О–CO–С17Н35 + 3Н2О
Н2С–О–CO–С17Н35
тристеарат
Н+, t
Н2С–ОН
НС–ОН + 3С17Н35СООН
Н2С–ОН
глицерин
стеариновая кислота
15.
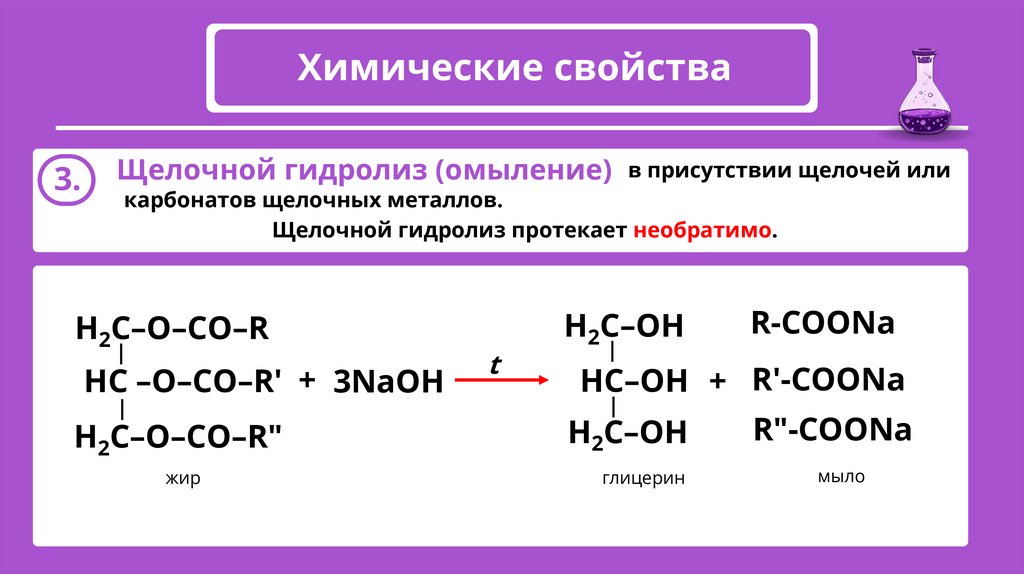
Химические свойства3.
Щелочной гидролиз (омыление) в присутствии щелочей или
карбонатов щелочных металлов.
Щелочной гидролиз протекает необратимо.
H2С–О–СО–R
HС –О–CO–R' + 3NaOH
H2С–О–CO–R"
жир
t
Н2С–ОН
R-СООNa
НС–ОН + R'-СООNa
Н2С–ОН
глицерин
R"-СООNa
мыло
16.
Мыла17.
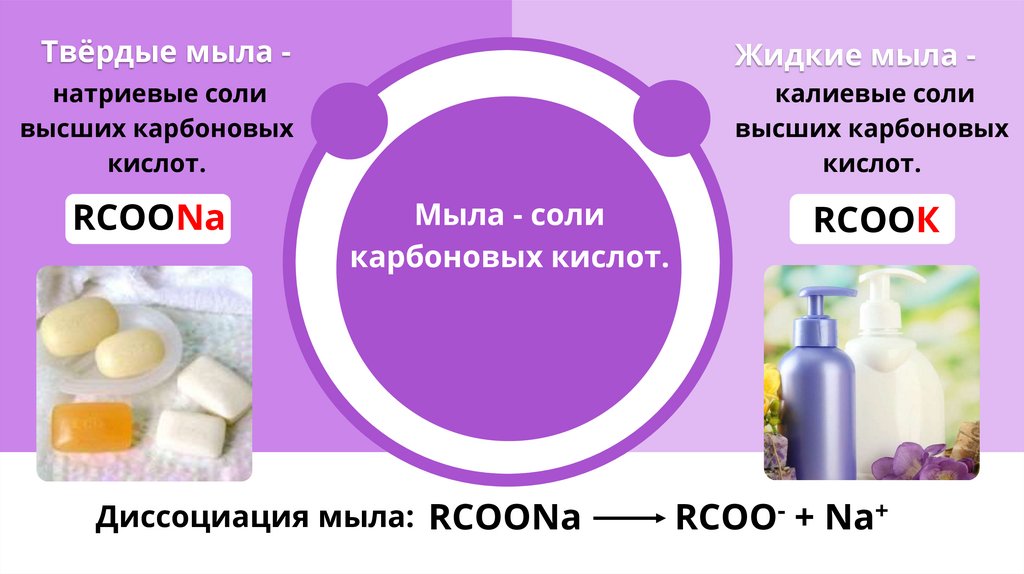
Твёрдые мыла -Жидкие мыла -
натриевые соли
высших карбоновых
кислот.
калиевые соли
высших карбоновых
кислот.
RCOONa
Мыла - соли
карбоновых кислот.
Диссоциация мыла: RCOONa
RCOOК
+
RCOO + Na
18.
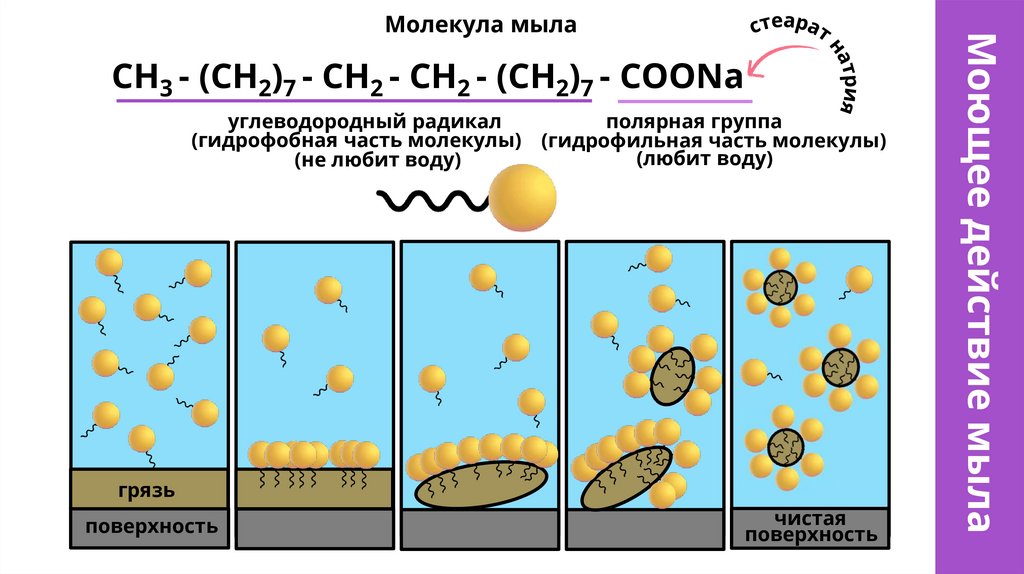
СН3 - (СН2)7 - СН2 - СН2 - (СН2)7 - СООNaполярная группа
углеводородный радикал
(гидрофобная часть молекулы) (гидрофильная часть молекулы)
(любит воду)
(не любит воду)
грязь
поверхность
чистая
поверхность
Моющее действие мыла
Молекула мыла
19.
Кальциевые и магниевые соли высшихкарбоновых кислот нерастворимы в воде.
2+
2+
В жёсткой воде, содержащей ионы Са и Mg ,
мыло теряет свою моющую способность.
2+
2С17Н35СОО + Са → (С17Н35СОО)2Са↓
20.
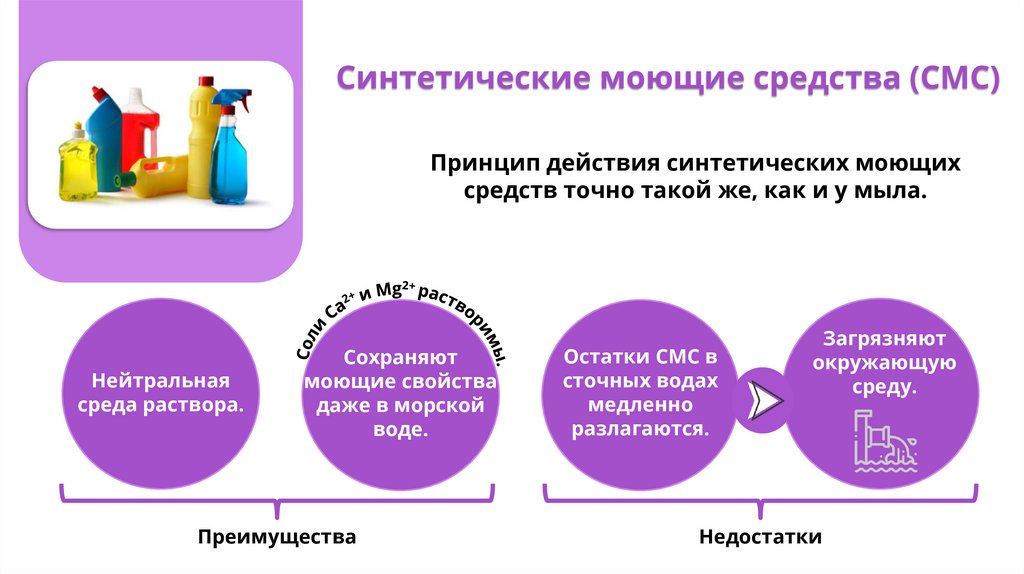
Синтетические моющие средства (СМС)Принцип действия синтетических моющих
средств точно такой же, как и у мыла.
Нейтральная
среда раствора.
Сохраняют
моющие свойства
даже в морской
воде.
Преимущества
Остатки СМС в
сточных водах
медленно
разлагаются.
Загрязняют
окружающую
среду.
Недостатки








 chemistry
chemistry








