Similar presentations:
Действие препарата «Золгенсма» при СМА
1.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ АВТОНОМНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ«БЕЛГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ НАЦИОНАЛЬНЫЙ
ИССЛЕДОВАТЕЛЬСКИЙ УНИВЕРСИТЕТ»
Действие препарата
«Золгенсма» при СМА
Студентки Медицинского института, направления подготовки
«Педиатрия», группы 03012137
Прижигалинской Лианы Отариевны
2.
СПИНАЛЬНЫЕ АМИОТРОФИИВКЛЮЧАЮТ В СЕБЯ НЕСКОЛЬКО
ВИДОВ ГРУППЫ НАСЛЕДСТВЕННЫХ
ЗАБОЛЕВАНИЙ,
ХАРАКТЕРИЗУЮЩИХСЯ
ПОРАЖЕНИЕМ СКЕЛЕТНЫХ МЫШЦ
ИЗ-ЗА ПРОГРЕССИРУЮЩЕЙ
ДЕГЕНЕРАЦИИ НЕЙРОНОВ
ПЕРЕДНИХ РОГОВ СПИННОГО
МОЗГА И ДВИГАТЕЛЬНЫХ ЯДЕР
СТВОЛА ГОЛОВНОГО МОЗГА.
ПРОЯВЛЕНИЯ МОГУТ НАЧАТЬСЯ В
МЛАДЕНЧЕСТВЕ ИЛИ ДЕТСТВЕ.
3.
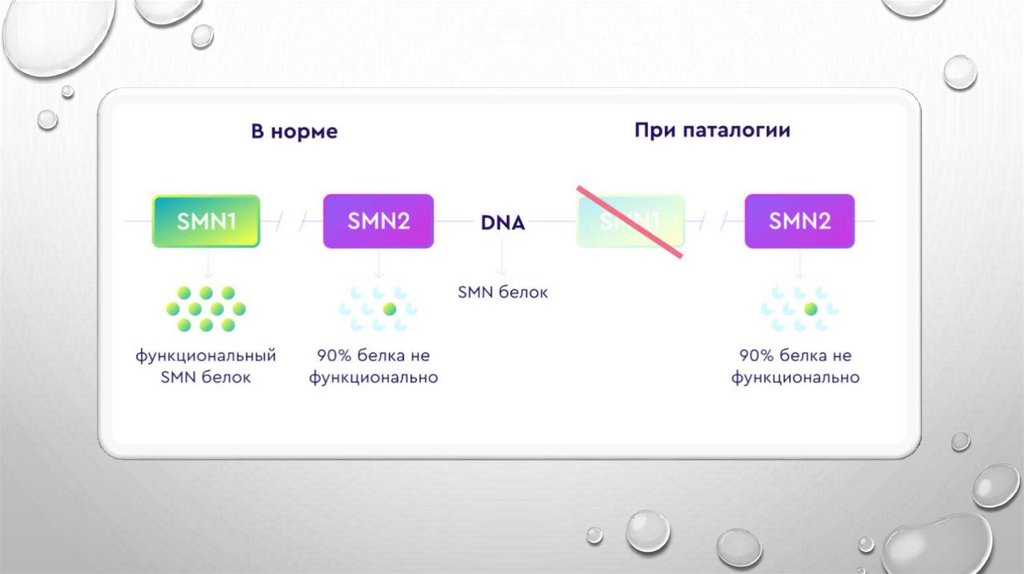
ПРИЧИНОЙ ЗАБОЛЕВАНИЯ ЯВЛЯЕТСЯВРОЖДЕННЫЙ ДЕФЕКТ В ГЕНЕ SMN1,
КОДИРУЮЩЕМ СООТВЕТСТВУЮЩИЙ БЕЛОК,
УЧАСТВУЮЩИЙ В ПОДДЕРЖАНИИ
ДВИГАТЕЛЬНЫХ (МОТОРНЫХ) НЕЙРОНОВ В
«ЖИВОМ» И НОРМАЛЬНО
ФУНКЦИОНИРУЮЩЕМ СОСТОЯНИИ.
ПРИ НЕДОСТАТКЕ ИЛИ ОТСУТСТВИИ БЕЛКА
SMN1 ДВИГАТЕЛЬНЫЕ НЕЙРОНЫ ОТМИРАЮТ,
ЧТО ПРИВОДИТ К ОСЛАБЛЕНИЮ МЫШЦ, А
ЗАТЕМ И ИХ АТРОФИИ, ЧТО ПРОИСХОДИТ ПРИ
ЗАБОЛЕВАНИИ SMA. В КОНЕЧНОМ ИТОГЕ
УСИЛЕНИЕ СИМПТОМОВ ПЕР,ЕРАСТАЕТ В
НЕСПОСОБНОСТЬ КОНТРОЛИРОВАТЬ ДАЖЕ
САМЫЕ ПРОСТЫЕ ДВИЖЕНИЯ ВКЛЮЧАЯ
ДЫХАНИЕ И ГЛОТАНИЕ, ЧТО БЕЗ ЛЕЧЕНИЯ
МОЖЕТ ПРИВЕСТИ К ТРАГИЧЕСКОМУ ИСХОДУ.
4.
5.
ТИПНАСЛЕДОВАНИЯ
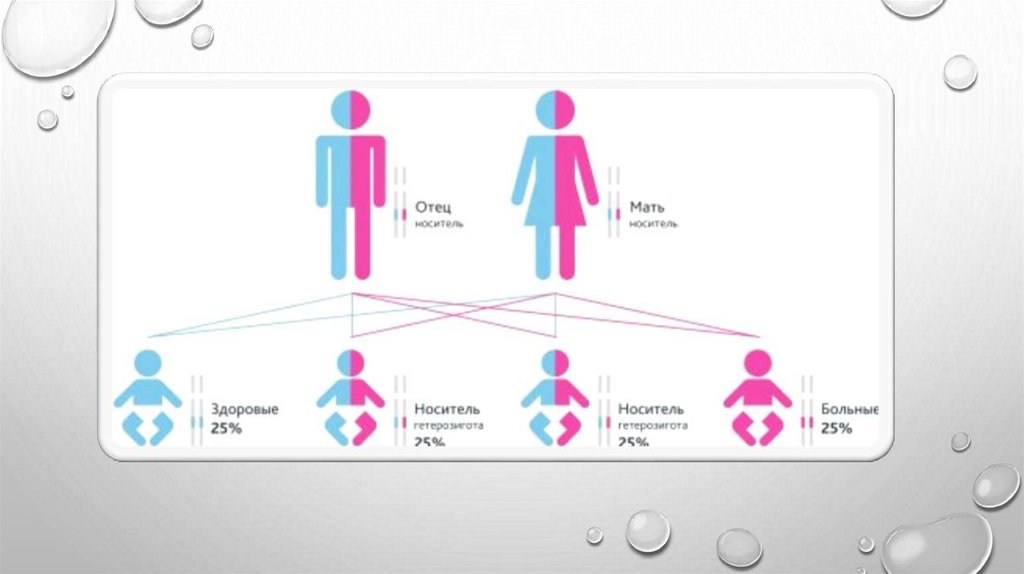
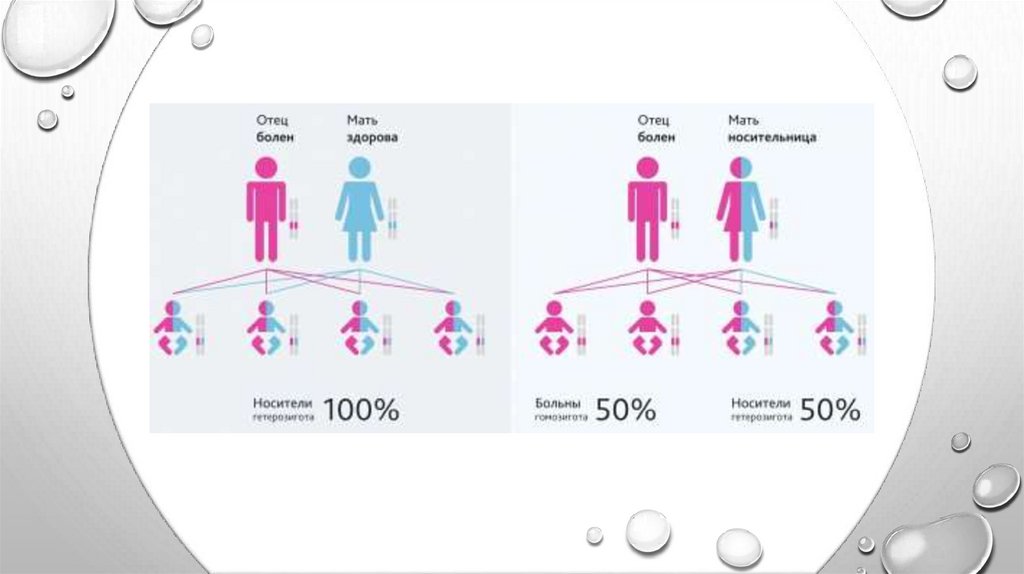
• СПИНАЛЬНАЯ МЫШЕЧНАЯ АТРОФИЯ
НАСЛЕДУЕТСЯ ПО АУТОСОМНОРЕЦЕССИВНОМУ ТИПУ. В БОЛЬШИНСТВЕ
СЛУЧАЕВ КАЖДЫЙ ИЗ РОДИТЕЛЕЙ
ЧЕЛОВЕКА С АУТОСОМНО-РЕЦЕССИВНЫМ
ЗАБОЛЕВАНИЕМ НЕСЕТ ПО ОДНОЙ КОПИИ
МУТИРОВАННОГО ГЕНА. НО ТАК КАК
МУТАЦИЯ КОМПЕНСИРОВАНА НАЛИЧИЕМ
ВТОРОЙ «ЗДОРОВОЙ» КОПИЕЙ ГЕНА,
НОСИТЕЛИ НЕ ПРОЯВЛЯЮТ ПРИЗНАКОВ
И СИМПТОМОВ БОЛЕЗНИ.
6.
7.
8.
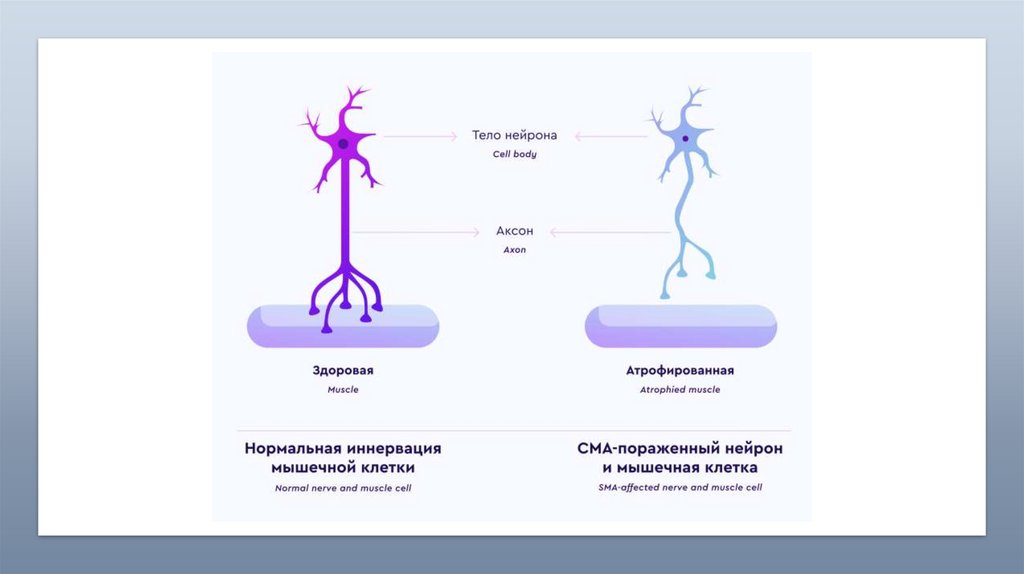
ОТМЕЧАЕТСЯ ДЕГЕНЕРАЦИЯ СПИНАЛЬНЫХ МОТОНЕЙРОНОВ И ПЕРЕДНИХКОРЕШКОВ, ЧАСТО – И В ДВИГАТЕЛЬНЫХ ЯДРАХ И КОРЕШКАХ V, VI, VII,IХ, Х,
ХI И ХII ЧЕРЕПНЫХ НЕРВОВ. В СКЕЛЕТНЫХ МЫШЦАХ ВТОРИЧНЫЕ
НЕЙРОДЕГЕНЕРАТИВНЫЕ ИЗМЕНЕНИЯ (ПУЧКОВАЯ АТРОФИЯ И ДР).
9.
10.
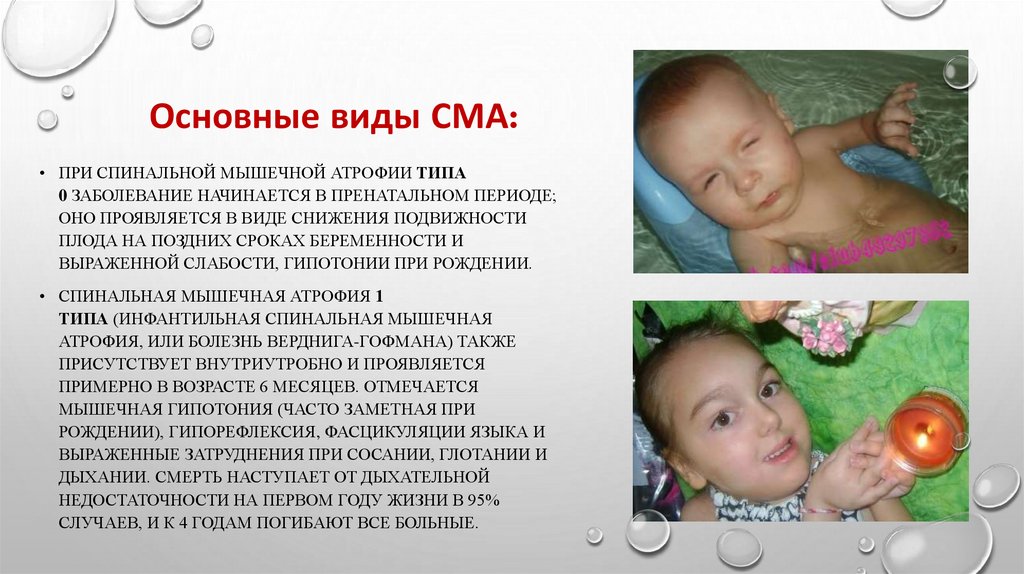
Основные виды СМА:• ПРИ СПИНАЛЬНОЙ МЫШЕЧНОЙ АТРОФИИ ТИПА
0 ЗАБОЛЕВАНИЕ НАЧИНАЕТСЯ В ПРЕНАТАЛЬНОМ ПЕРИОДЕ;
ОНО ПРОЯВЛЯЕТСЯ В ВИДЕ СНИЖЕНИЯ ПОДВИЖНОСТИ
ПЛОДА НА ПОЗДНИХ СРОКАХ БЕРЕМЕННОСТИ И
ВЫРАЖЕННОЙ СЛАБОСТИ, ГИПОТОНИИ ПРИ РОЖДЕНИИ.
• СПИНАЛЬНАЯ МЫШЕЧНАЯ АТРОФИЯ 1
ТИПА (ИНФАНТИЛЬНАЯ СПИНАЛЬНАЯ МЫШЕЧНАЯ
АТРОФИЯ, ИЛИ БОЛЕЗНЬ ВЕРДНИГА-ГОФМАНА) ТАКЖЕ
ПРИСУТСТВУЕТ ВНУТРИУТРОБНО И ПРОЯВЛЯЕТСЯ
ПРИМЕРНО В ВОЗРАСТЕ 6 МЕСЯЦЕВ. ОТМЕЧАЕТСЯ
МЫШЕЧНАЯ ГИПОТОНИЯ (ЧАСТО ЗАМЕТНАЯ ПРИ
РОЖДЕНИИ), ГИПОРЕФЛЕКСИЯ, ФАСЦИКУЛЯЦИИ ЯЗЫКА И
ВЫРАЖЕННЫЕ ЗАТРУДНЕНИЯ ПРИ СОСАНИИ, ГЛОТАНИИ И
ДЫХАНИИ. СМЕРТЬ НАСТУПАЕТ ОТ ДЫХАТЕЛЬНОЙ
НЕДОСТАТОЧНОСТИ НА ПЕРВОМ ГОДУ ЖИЗНИ В 95%
СЛУЧАЕВ, И К 4 ГОДАМ ПОГИБАЮТ ВСЕ БОЛЬНЫЕ.
11.
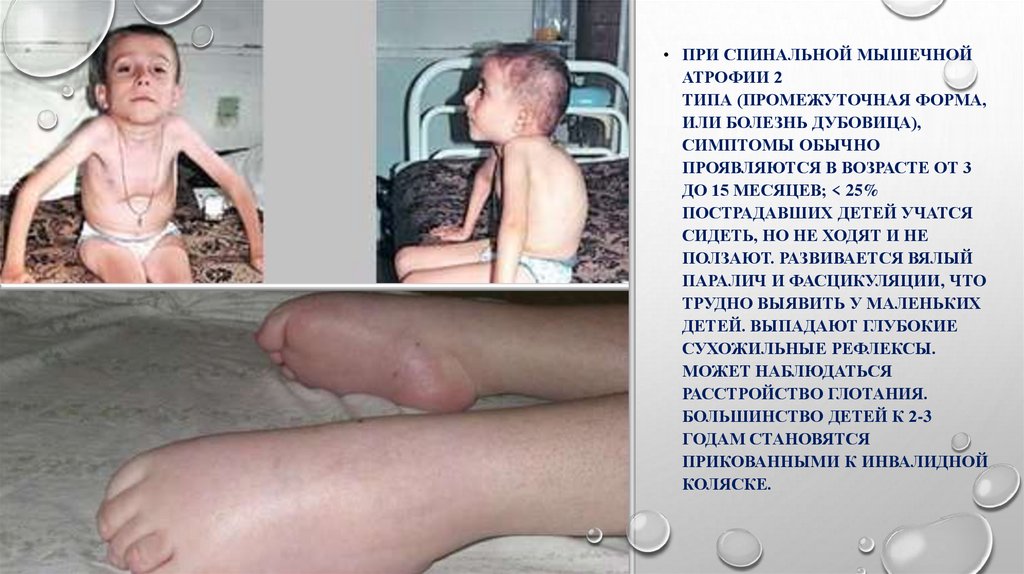
• ПРИ СПИНАЛЬНОЙ МЫШЕЧНОЙАТРОФИИ 2
ТИПА (ПРОМЕЖУТОЧНАЯ ФОРМА,
ИЛИ БОЛЕЗНЬ ДУБОВИЦА),
СИМПТОМЫ ОБЫЧНО
ПРОЯВЛЯЮТСЯ В ВОЗРАСТЕ ОТ 3
ДО 15 МЕСЯЦЕВ; < 25%
ПОСТРАДАВШИХ ДЕТЕЙ УЧАТСЯ
СИДЕТЬ, НО НЕ ХОДЯТ И НЕ
ПОЛЗАЮТ. РАЗВИВАЕТСЯ ВЯЛЫЙ
ПАРАЛИЧ И ФАСЦИКУЛЯЦИИ, ЧТО
ТРУДНО ВЫЯВИТЬ У МАЛЕНЬКИХ
ДЕТЕЙ. ВЫПАДАЮТ ГЛУБОКИЕ
СУХОЖИЛЬНЫЕ РЕФЛЕКСЫ.
МОЖЕТ НАБЛЮДАТЬСЯ
РАССТРОЙСТВО ГЛОТАНИЯ.
БОЛЬШИНСТВО ДЕТЕЙ К 2-3
ГОДАМ СТАНОВЯТСЯ
ПРИКОВАННЫМИ К ИНВАЛИДНОЙ
КОЛЯСКЕ.
12.
• СПИНАЛЬНАЯ АМИОТРОФИЯ 3 ТИПА (БОЛЕЗНЬКУГЕЛЬБЕРГА–ВЕЛАНДЕР) ОБЫЧНО ПРОЯВЛЯЕТСЯ В
ВОЗРАСТЕ МЕЖДУ 15 МЕСЯЦЕВ И 19 ГОДАМИ. ПРИЗНАКИ
ПОХОЖИ НА СИМПТОМЫ I ТИПА ЗАБОЛЕВАНИЯ, НО
БОЛЕЗНЬ ПРОГРЕССИРУЕТ МЕДЛЕННЕЕ, А
ПРОДОЛЖИТЕЛЬНОСТЬ ЖИЗНИ БОЛЬШЕ (ИНОГДА
НОРМАЛЬНА). СИММЕТРИЧНАЯ СЛАБОСТЬ И АТРОФИИ,
НАЧИНАЯСЬ С ЧЕТЫРЕХГЛАВОЙ МЫШЦЫ БЕДРА И
СГИБАТЕЛЕЙ БЕДРА, ПОСТЕПЕННО РАСПРОСТРАНЯЮТСЯ
ДИСТАЛЬНЕЕ, СТАНОВЯСЬ НАИБОЛЕЕ ВЫРАЖЕННЫМИ НА
ГОЛЕНЯХ.
• СПИНАЛЬНАЯ АМИОТРОФИЯ 4 ТИПА (ПРИ ПОЗДНЕМ
ПРОЯВЛЕНИИ) МОЖЕТ НАСЛЕДОВАТЬСЯ ПО
РЕЦЕССИВНОМУ, ДОМИНАНТНОМУ ИЛИ Х-СЦЕПЛЕННОМУ
ТИПУ; С ДЕБЮТОМ В ЗРЕЛОМ ВОЗРАСТЕ (30–60 ЛЕТ) И
МЕДЛЕННО ПРОГРЕССИРУЮЩЕЙ СЛАБОСТЬЮ И АТРОФИЕЙ
В ОСНОВНОМ ПРОКСИМАЛЬНЫХ МЫШЦ.
13.
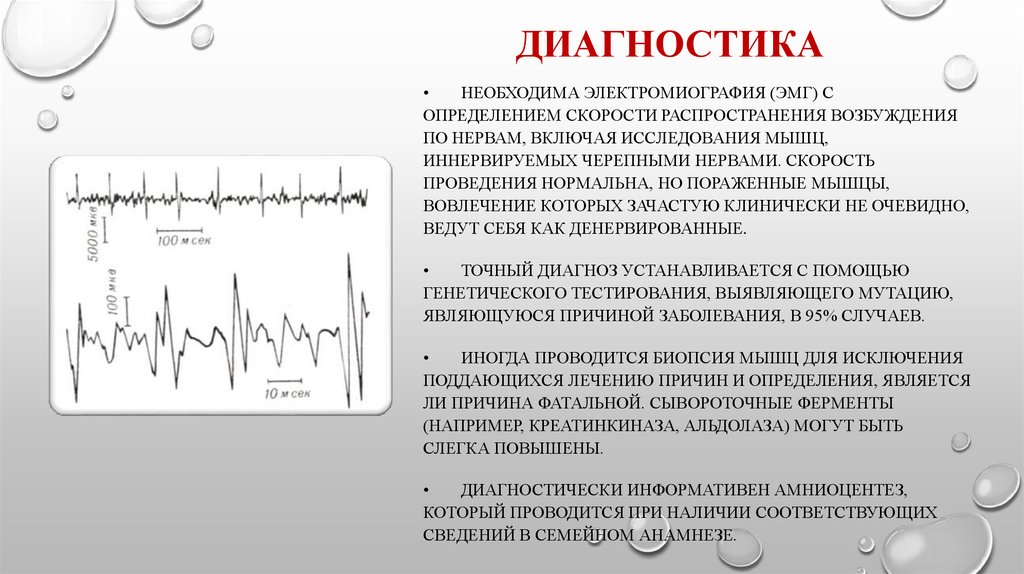
ДИАГНОСТИКАНЕОБХОДИМА ЭЛЕКТРОМИОГРАФИЯ (ЭМГ) С
ОПРЕДЕЛЕНИЕМ СКОРОСТИ РАСПРОСТРАНЕНИЯ ВОЗБУЖДЕНИЯ
ПО НЕРВАМ, ВКЛЮЧАЯ ИССЛЕДОВАНИЯ МЫШЦ,
ИННЕРВИРУЕМЫХ ЧЕРЕПНЫМИ НЕРВАМИ. СКОРОСТЬ
ПРОВЕДЕНИЯ НОРМАЛЬНА, НО ПОРАЖЕННЫЕ МЫШЦЫ,
ВОВЛЕЧЕНИЕ КОТОРЫХ ЗАЧАСТУЮ КЛИНИЧЕСКИ НЕ ОЧЕВИДНО,
ВЕДУТ СЕБЯ КАК ДЕНЕРВИРОВАННЫЕ.
ТОЧНЫЙ ДИАГНОЗ УСТАНАВЛИВАЕТСЯ С ПОМОЩЬЮ
ГЕНЕТИЧЕСКОГО ТЕСТИРОВАНИЯ, ВЫЯВЛЯЮЩЕГО МУТАЦИЮ,
ЯВЛЯЮЩУЮСЯ ПРИЧИНОЙ ЗАБОЛЕВАНИЯ, В 95% СЛУЧАЕВ.
ИНОГДА ПРОВОДИТСЯ БИОПСИЯ МЫШЦ ДЛЯ ИСКЛЮЧЕНИЯ
ПОДДАЮЩИХСЯ ЛЕЧЕНИЮ ПРИЧИН И ОПРЕДЕЛЕНИЯ, ЯВЛЯЕТСЯ
ЛИ ПРИЧИНА ФАТАЛЬНОЙ. СЫВОРОТОЧНЫЕ ФЕРМЕНТЫ
(НАПРИМЕР, КРЕАТИНКИНАЗА, АЛЬДОЛАЗА) МОГУТ БЫТЬ
СЛЕГКА ПОВЫШЕНЫ.
ДИАГНОСТИЧЕСКИ ИНФОРМАТИВЕН АМНИОЦЕНТЕЗ,
КОТОРЫЙ ПРОВОДИТСЯ ПРИ НАЛИЧИИ СООТВЕТСТВУЮЩИХ
СВЕДЕНИЙ В СЕМЕЙНОМ АНАМНЕЗЕ.
14.
Клинические проявления СМА:БУЛЬБАРНЫЕ НАРУШЕНИЯ: ОСЛАБЛЕННЫЙ КРИК У ДЕТЕЙ, ФАСЦИКУЛЯЦИИ ЯЗЫКА;
НАРУШЕНИЯ ДЫХАНИЯ;
НАРУШЕНИЯ ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ СЕРДЦА И ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА;
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС;
ЗАПОР, ПОТЕРЯ МАССЫ ТЕЛА;
КОНТРАКТУРЫ СУСТАВОВ;
СНИЖЕНИЕ ИЛИ ОТСУТСТВИЕ ГЛУБОКИХ РЕФЛЕКСОВ;
АТРОФИЯ МЫШЦ, ИХ СЛАБОСТЬ И ГИПОТОНИЯ;
У РЯДА ПАЦИЕНТОВ МОЖЕТ НАБЛЮДАТЬСЯ ГРУБЫЙ ПОСТУРАЛЬНЫЙ ТРЕМОР – МИНИПОЛИМИОКЛОНУС.
15.
ЗОЛГЕНСМА(ОНАСЕМНОГЕН
АБЕПАРВОВЕК)
16.
ПРЕПАРАТЫ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ СМАПРИМЕНЯЮТСЯ В МИРЕ С 2016 ГОДА, ДО ЭТОГО
МОМЕНТА ЛЕЧЕНИЕ БЫЛО СИМПТОМАТИЧЕСКИМ.
ПЕРВЫЕ ДВА – СПИНРАЗА (НУСИНЕРСЕН ОТ BIOGEN) И
ЭВРИСДИ (РИСДИПЛАМ ОТ ROCHE).
17.
РАЗРАБОТКАNOVARTIS И AVEXIS (ПРИОБРЕТЕНА NOVARTIS В 2018 ГОДУ ЗА
8,7 МЛРД ДОЛЛАРОВ США) ЗАНИМАЛИСЬ РАЗРАБОТКОЙ
ОНАСЕМНОГЕНА АБЕПАРВОВЕКА БОЛЕЕ 23 ЛЕТ. ЗА ЭТО
ВРЕМЯ КОМПАНИИ СМОГЛИ РАСШИРИТЬ ПРОГРАММУ
КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ ПРЕПАРАТА С ПЕРВОГО
ИССЛЕДОВАНИЯ В ОДНОМ МЕДИЦИНСКОМ ЦЕНТРЕ ДО 6
ИССЛЕДОВАНИЙ БОЛЕЕ ЧЕМ В 17 ЦЕНТРАХ В США, ЧТОБЫ
ПРОВЕСТИ ЛИЦЕНЗИРОВАНИЕ ТЕХНОЛОГИЙ, РАЗРАБОТАТЬ
ПРОИЗВОДСТВЕННЫЙ ПРОЦЕСС, ПОСТРОИТЬ
ПРОИЗВОДСТВЕННУЮ ПЛОЩАДКУ, СООТВЕТСТВУЮЩУЮ
ТРЕБОВАНИЯМ ПРАВИЛ ПРОИЗВОДСТВА И КОНТРОЛЯ
КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ FDA, А ТАКЖЕ НАНЯТЬ
И ОБУЧИТЬ КОМАНДУ ВЫСОКОКВАЛИФИЦИРОВАННЫХ
СПЕЦИАЛИСТОВ, ОТВЕЧАЮЩИХ ЗА ВЫПУСК И ДОСТАВКУ
ПРЕПАРАТА.
18.
КЛИНИЧЕСКИЕИСПЫТАНИЯ
НА МОМЕНТ ОДОБРЕНИЯ FDA (УПРАВЛЕНИЕ
ПО НАДЗОРУ ЗА КАЧЕСТВОМ ПИЩЕВЫХ
ПРОДУКТОВ И МЕДИКАМЕНТОВ США) В МАЕ
2019 ГОДА БЫЛИ ДОСТУПНЫ ДАННЫЕ ПО 36
ПАЦИЕНТАМ С СМА I ТИПА В ВОЗРАСТЕ ОТ
0,5 ДО 7,2 МЕСЯЦЕВ. ИЗ НИХ ТРОЕ ПОЛУЧИЛИ
НИЗКУЮ ДОЗУ ПРЕПАРАТА, А 33 —
ВЫСОКУЮ. ИЗ ПОЛУЧИВШИХ ВЫСОКУЮ
ДОЗУ 31 ПАЦИЕНТ НА МОМЕНТ ОДОБРЕНИЯ
(4-28 МЕС. ПОСЛЕ НАЧАЛА ТЕРАПИИ) НЕ
НУЖДАЛСЯ В ПОСТОЯННОЙ ВЕНТИЛЯЦИИ
ЛЁГКИХ. 19 ПАЦИЕНТОВ, ПОЛУЧИВШИХ
ВЫСОКУЮ ДОЗУ, БЫЛИ СПОСОБНЫ СИДЕТЬ
БЕЗ ПОДДЕРЖКИ. СЧИТАЕТСЯ, ЧТО БЕЗ
ЛЕЧЕНИЯ В ЖИВЫХ К ЭТОМУ МОМЕНТУ
ОСТАЛОСЬ БЫ ПРИМЕРНО 8-9 ПАЦИЕНТОВ И
СИДЕТЬ
НЕ
МОГ
БЫ
НИКТО.
МАКСИМАЛЬНЫЙ СРОК НАБЛЮДЕНИЯ ЗА
ПАЦИЕНТАМИ
СОСТАВИЛ
4,6
ЛЕТ,
НЕКОТОРЫЕ
ИЗ
НИХ
НАЧИНАЮТ
САМОСТОЯТЕЛЬНО СТОЯТЬ И ХОДИТЬ.
19.
ДЕЙСТВИЕОНАСЕМНОГЕН АБЕПАРВОВЕК ПРЕДСТАВЛЯЕТ СОБОЙ ГЕННО-ТЕРАПЕВТИЧЕСКОЕ
ЛЕЧЕНИЕ, ОБЕСПЕЧИВАЮЩЕЕ ЗАМЕНУ ОТСУТСТВУЮЩЕГО ИЛИ ДЕФЕКТНОГО ГЕНА
SMN1 НА ЕГО ФУНКЦИОНАЛЬНУЮ КОПИЮ, ЧТО ПРИВОДИТ К НОРМАЛИЗАЦИИ
ВЫРАБОТКИ БЕЛКА ВЫЖИВАЕМОСТИ МОТОНЕЙРОНОВ (SMN).
ПОЛНОЦЕННЫЙ ГЕН SMN1 НАХОДИТСЯ ВНУТРИ ВЕКТОРА
АДЕНОАССОЦИИРОВАННОГО ВИРУСА (ADENO-ASSOCIATIVE VIRUS 9, ИЛИ AAV9).
ПРЕПАРАТЫ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ СМА ПРИМЕНЯЮТСЯ В МИРЕ С 2016 ГОДА,
ДО ЭТОГО МОМЕНТА ЛЕЧЕНИЕ БЫЛО СИМПТОМАТИЧЕСКИМ. ПЕРВЫЕ ДВА –
СПИНРАЗА (НУСИНЕРСЕН ОТ BIOGEN) И ЭВРИСДИ (РИСДИПЛАМ ОТ ROCHE).
20.
КЛИНИЧЕСКИ ДОКАЗАНО, ЧТО ОДНОКРАТНАЯ ИНФУЗИЯ ПРЕПАРАТА
СПОСОБНА ВОССТАНОВИТЬ SMN-ЭКСПРЕССИЮ В МОТОРНЫХ НЕЙРОНАХ,
ЛИШЁННЫХ ФУНКЦИОНАЛЬНОГО ГЕНА SMN1.
ОДНОКРАТНАЯ ВНУТРИВЕННАЯ ИНФУЗИЯ В ТЕЧЕНИЕ 1 Ч. ДО НАЧАЛА
ИНФУЗИИ ПРОВОДИТСЯ ОЦЕНКА ФУНКЦИИ ПЕЧЕНИ,
УРОВНЯ ТРОМБОЦИТОВ И ТРОПОНИНА-I, ПРОВЕРКА
НАЛИЧИЯ АНТИТЕЛ ПРОТИВ ВИРУСА AAV9. ЗА 1 ДЕНЬ ДО ИНФУЗИИ НАЧИНАЮТ
ПРИМЕНЯТЬ СИСТЕМНЫЕ КОРТИКОСТЕРОИДЫ В ДОЗЕ, ЭКВИВАЛЕНТНОЙ 1
МГ/КГ МАССЫ ТЕЛА В СУТКИ, И ПРОДОЛЖАЮТ ПРИМЕНЯТЬ ИХ В ОБЩЕЙ
СЛОЖНОСТИ В ТЕЧЕНИЕ 30 ДНЕЙ.
21.
В СЕРЕДИНЕ ИЮЛЯ 2020 ГОДА NOVARTISПОДАЛА ДОСЬЕ НА РЕГИСТРАЦИЮ
ПРЕПАРАТА ЗОЛГЕНСМА
В МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ
РФ. ПОКА ЗОЛГЕНСМА НЕ БЫЛА
ЗАРЕГИСТРИРОВАНА ДЛЯ КЛИНИЧЕСКОГО
ПРИМЕНЕНИЯ В РОССИИ, ЕЁ ВВОЗ НА
ТЕРРИТОРИЮ СТРАНЫ МОГ
ОСУЩЕСТВЛЯТЬСЯ ТОЛЬКО ПО
ЖИЗНЕННЫМ ПОКАЗАНИЯМ ДЛЯ
КОНКРЕТНЫХ ПАЦИЕНТОВ В
СООТВЕТСТВИИ С ТРЕБОВАНИЯМИ,
ОПРЕДЕЛЁННЫМИ ФЕДЕРАЛЬНЫМ
ЗАКОНОМ № 61-Ф3 (ОБ ОБРАЩЕНИИ
ЛЕКАРСТВЕННЫХ СРЕДСТВ). ДЛЯ ЭТОГО
НЕОБХОДИМО БЫЛО РЕШЕНИЕ ВРАЧЕБНЫХ
КОМИССИЙ МЕДУЧРЕЖДЕНИЙ, А ТАКЖЕ
ОДОБРЕНИЕ НА ВВОЗ СО СТОРОНЫ
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РФ.
ОСУЩЕСТВЛЯТЬ ПРИМЕНЕНИЕ ЭТОГО
ПРЕПАРАТА В РОССИИ МОГЛИ ДВА
ФЕДЕРАЛЬНЫХ ЦЕНТРА, КОТОРЫЕ
ПОЛУЧИЛИ ПОЛНОМОЧИЯ ПОСЛЕ
ПРОХОЖДЕНИЯ НЕОБХОДИМОГО
ОБУЧЕНИЯ, ОРГАНИЗОВАННОГО NOVARTIS.













 medicine
medicine








