Similar presentations:
Скорость химической реакции. Химическое равновесие
1.
Материалы тестовогоконтроля
Тема: «Скорость химической
реакции. Химическое
равновесие»
2.
Выберите номер правильного ответа1 вариант
2 вариант
Поле с вариантами ответов
1……..
2……..
3……..
4……..
3.
1.Скорость реакции разложения Н2О2• С катализатором
• Без катализатора
1.Уменьшается
2.Не изменяется
3.увеличивается
4.
2.Скорость реакцииэкзотермической
эндотермической
при
понижении
повышении
температуры
1.Уменьшается
2.Не изменяется
3.увеличивается
5.
3. Реакция междуСульфатом натрия
и хлоридом бария
Оксидом серы (IV) и
кислородом
1.Обратимая
2.Необратимая
6.
Установите соответствиеВарианты ответов:
1…….А.
2…….В.
3…….Б.
7.
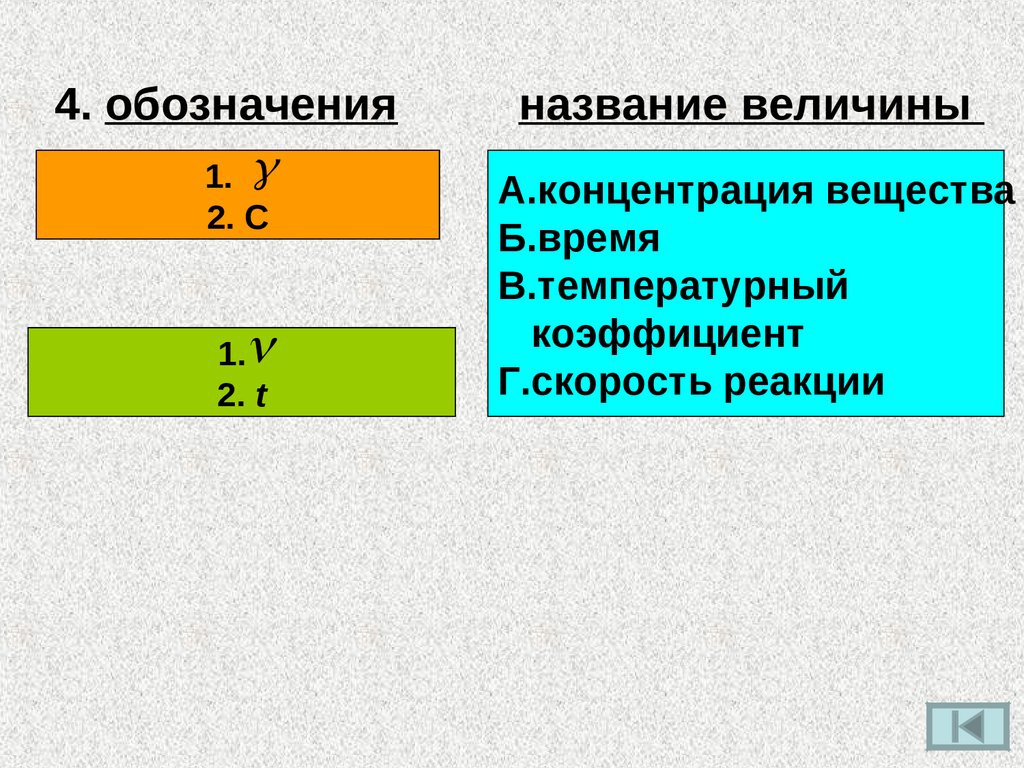
4. обозначения1.
2. С
1.
2. t
название величины
А.концентрация вещества
Б.время
В.температурный
коэффициент
Г.скорость реакции
8.
5. Физическаявеличина
1. ɫ тау
2. t
1.v
2. С
единица измерения
А.моль/л
Б.секунда
В.безразмерная
Г. моль/л*с
9.
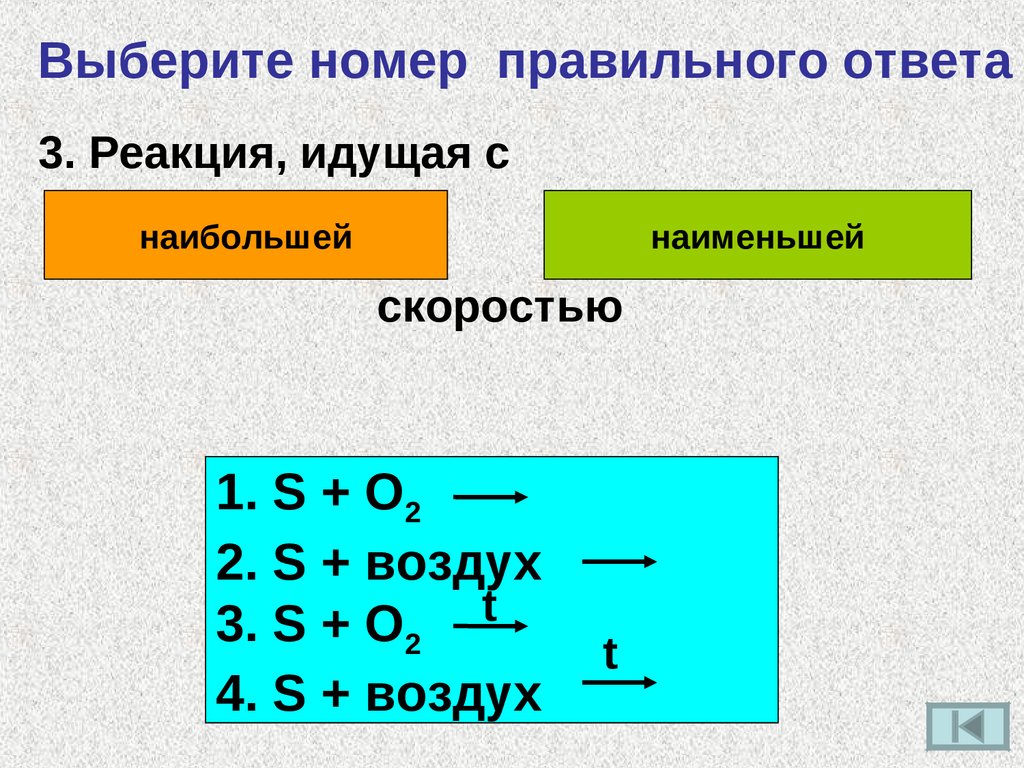
Выберите номер правильного ответа3. Реакция, идущая с
наибольшей
наименьшей
скоростью
1. S + O2
2. S + воздух
3. S + O2 t
4. S + воздух
t
10.
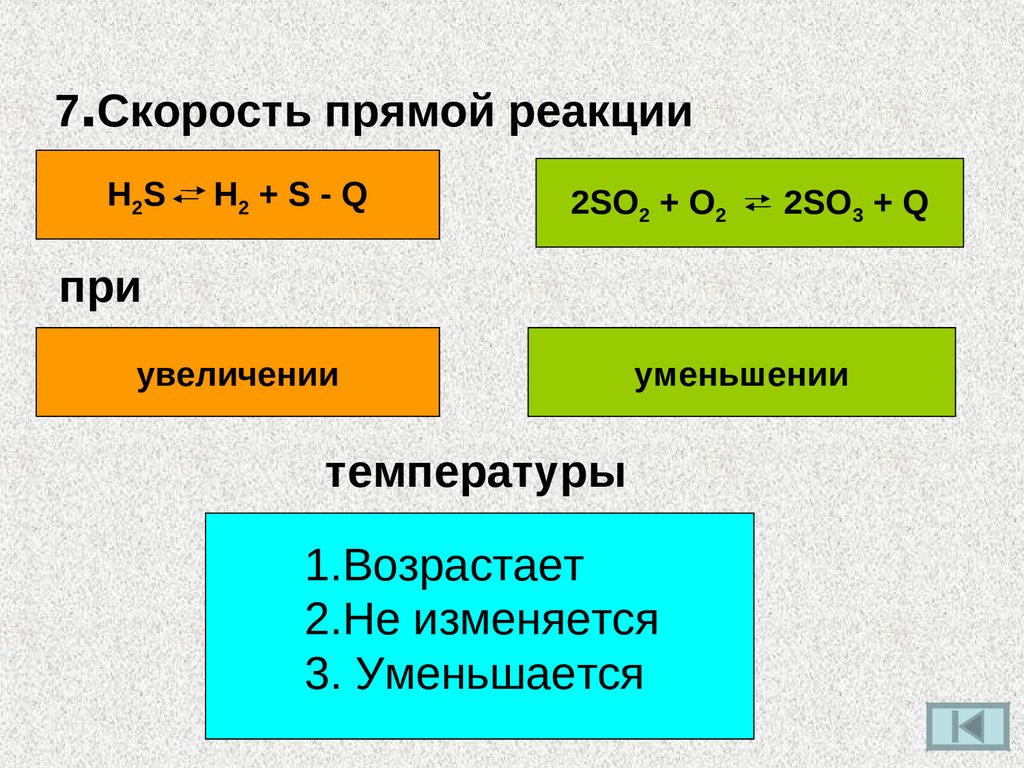
7.Скорость прямой реакцииH2S
H2 + S - Q
2SO2 + O2
2SO3 + Q
при
увеличении
уменьшении
температуры
1.Возрастает
2.Не изменяется
3. Уменьшается
11.
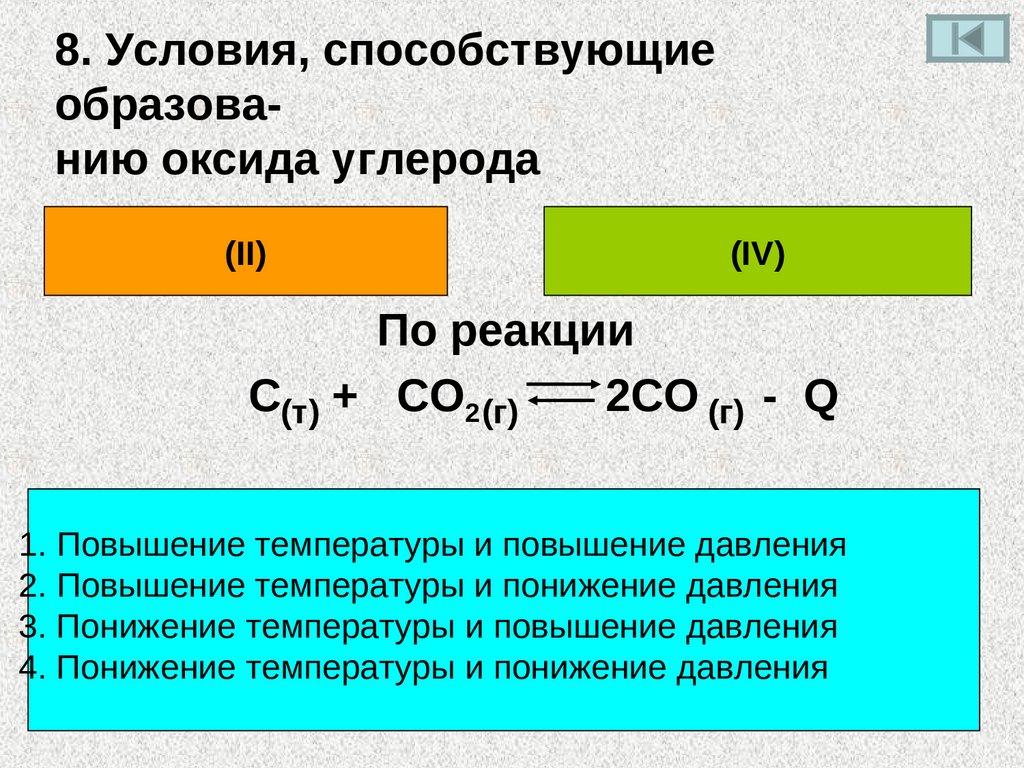
8. Условия, способствующиеобразованию оксида углерода
(II)
(IV)
По реакции
C(т) + CO2 (г)
2CO (г) - Q
1. Повышение температуры и повышение давления
2. Повышение температуры и понижение давления
3. Понижение температуры и повышение давления
4. Понижение температуры и понижение давления
12.
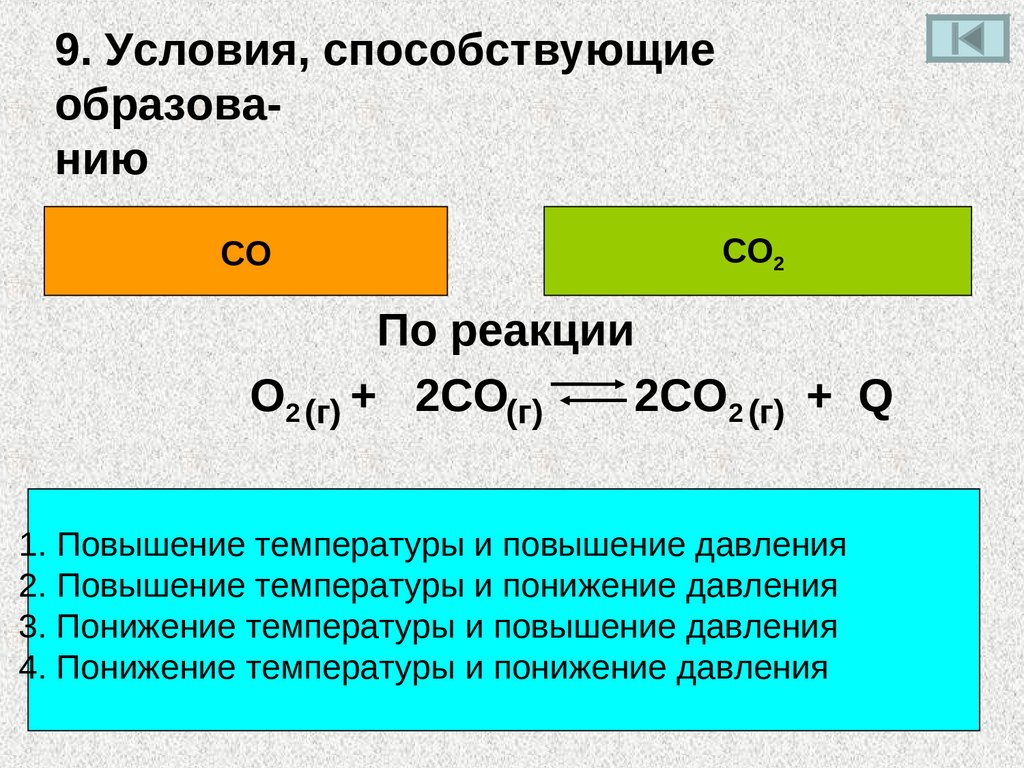
9. Условия, способствующиеобразованию
СО
СО2
По реакции
О2 (г) + 2CO(г)
2CO2 (г) + Q
1. Повышение температуры и повышение давления
2. Повышение температуры и понижение давления
3. Понижение температуры и повышение давления
4. Понижение температуры и понижение давления
13.
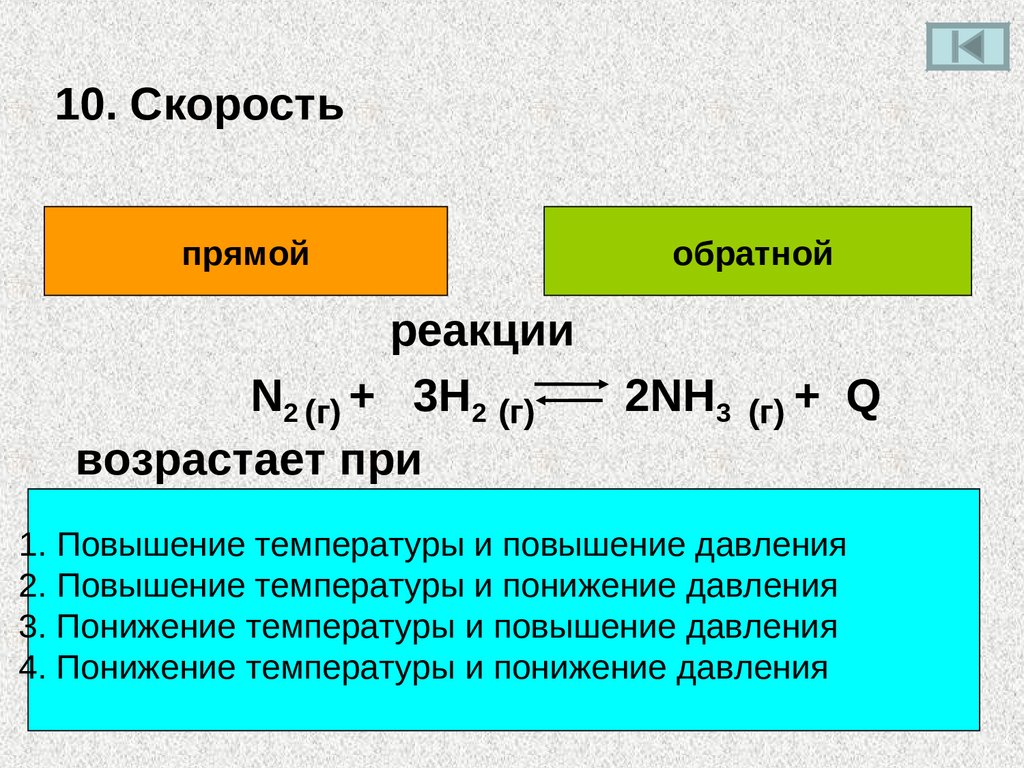
10. Скоростьпрямой
реакции
N2 (г) + 3H2 (г)
возрастает при
обратной
2NH3
(г) +
Q
1. Повышение температуры и повышение давления
2. Повышение температуры и понижение давления
3. Понижение температуры и повышение давления
4. Понижение температуры и понижение давления
14.
Установите соответствие11. Тип реакции
1. каталитическая
2. обратимая
1. гетерогенная
2. необратимая
исходные вещества
А. N2 + O2
Б. Cu + O2
(т)
В. H2 + N2
Г. CaCO3
(г)
t
кат
15.
Дополните:12. Формула вещества _____________,
образующегося при
уменьшении
увеличении
концентрации водорода в реакции
С4Н10 (г)
С4Н6
+
(г)
2Н2
Q
(г)
16.
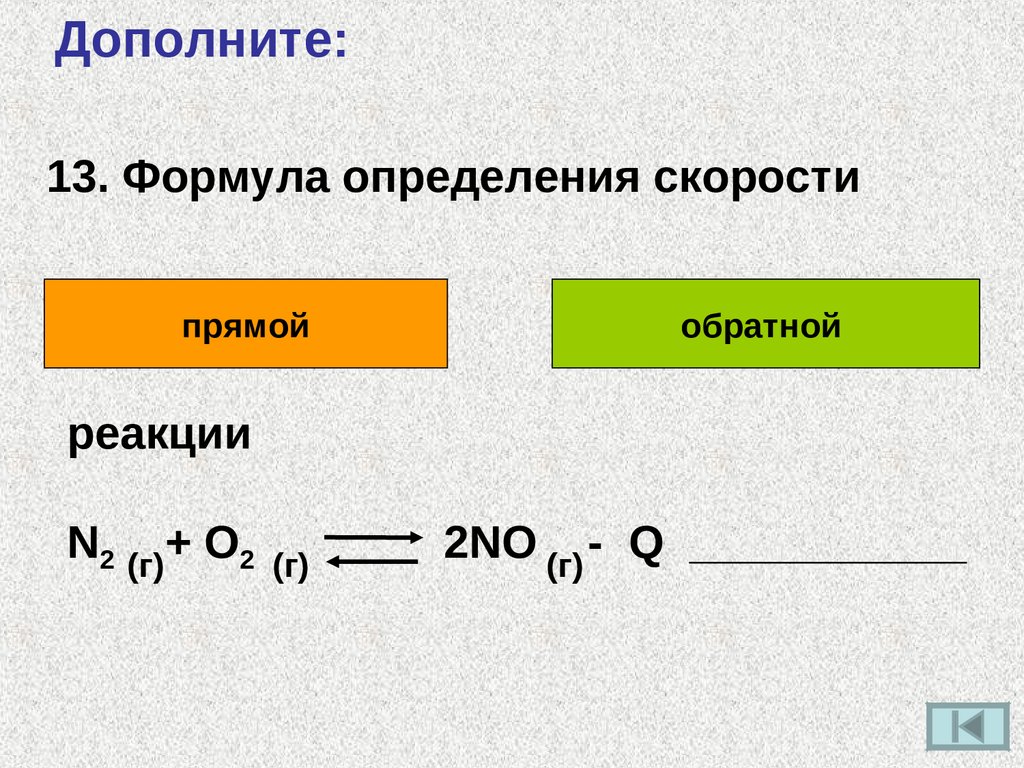
Дополните:13. Формула определения скорости
прямой
обратной
реакции
N2 (г)+ O2
(г)
2NO (г) - Q ___________
17.
Дополните:14. Формула определения скорости
обратной реакции
2HBr
H2 + Br2
2H2O
___________
2H2 + O2
18.
Дополните:15. Формула определения скорости
прямой
обратной
реакции
2SO2 (г) + O2
(г)
2SO3
(г)
___________
19.
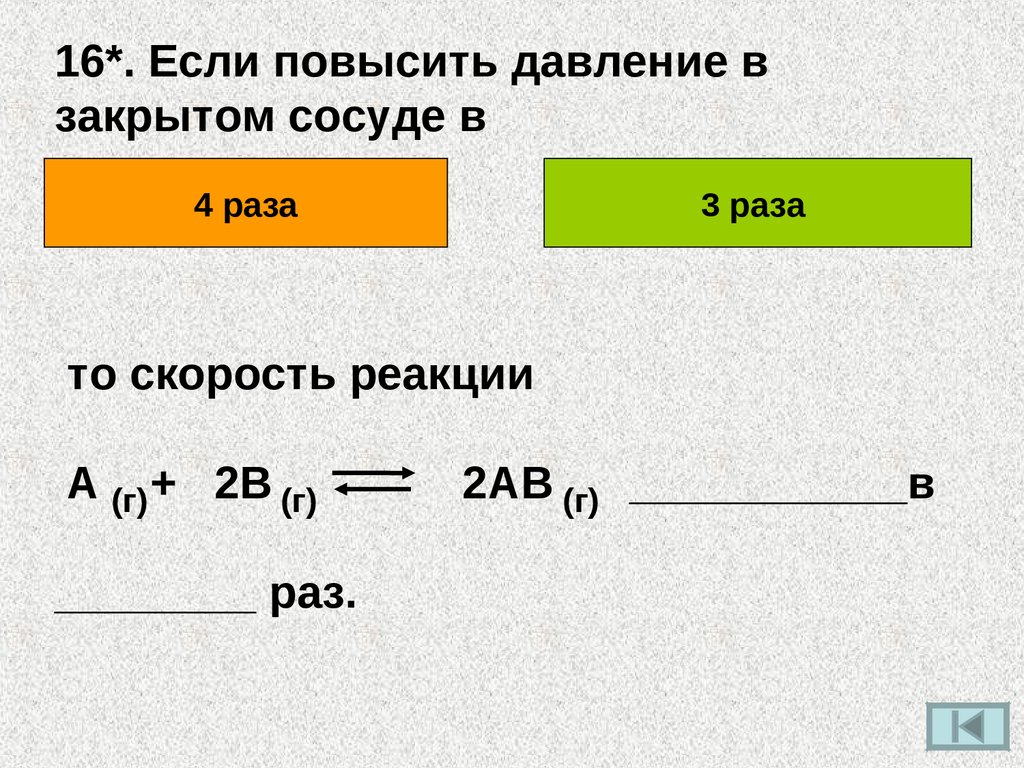
16*. Если повысить давление взакрытом сосуде в
4 раза
3 раза
то скорость реакции
А (г) + 2В (г)
________ раз.
2АВ (г) ___________в
20.
17*. Скорость реакции возрастает приповышении температуры на
300 С
500 С
в ________ раз, если температурный
коэффициент равен
3
2
21.
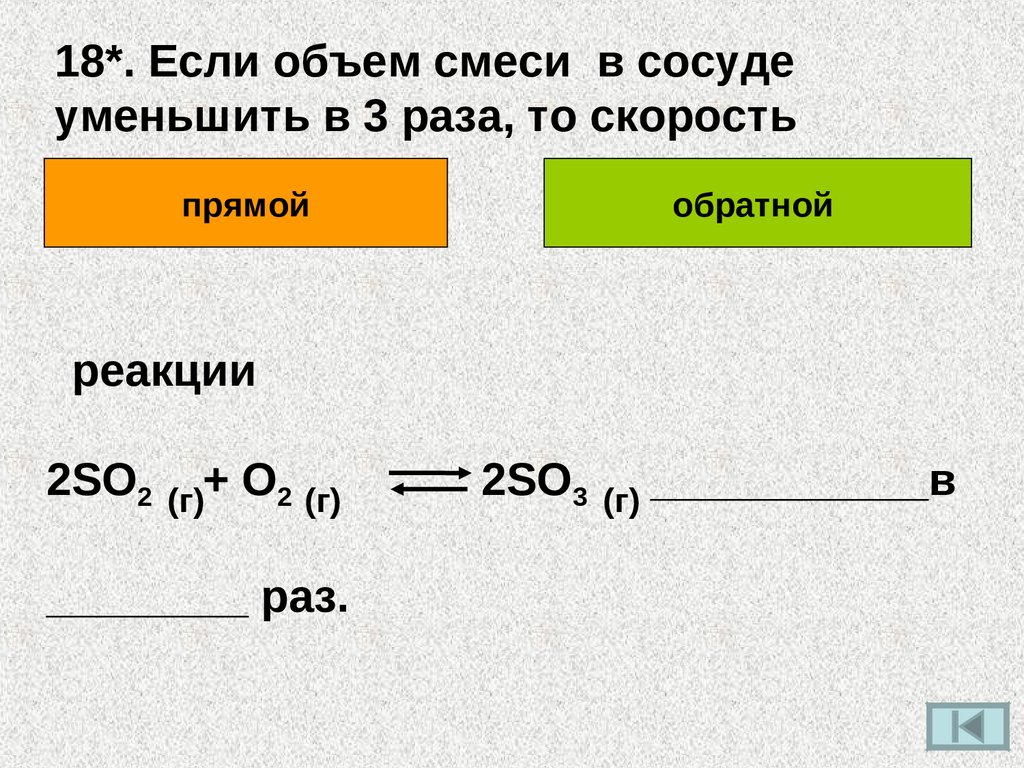
18*. Если объем смеси в сосудеуменьшить в 3 раза, то скорость
прямой
обратной
реакции
2SO2
+
O
2 (г)
(г)
________ раз.
2SO3
___________в
(г)
22.
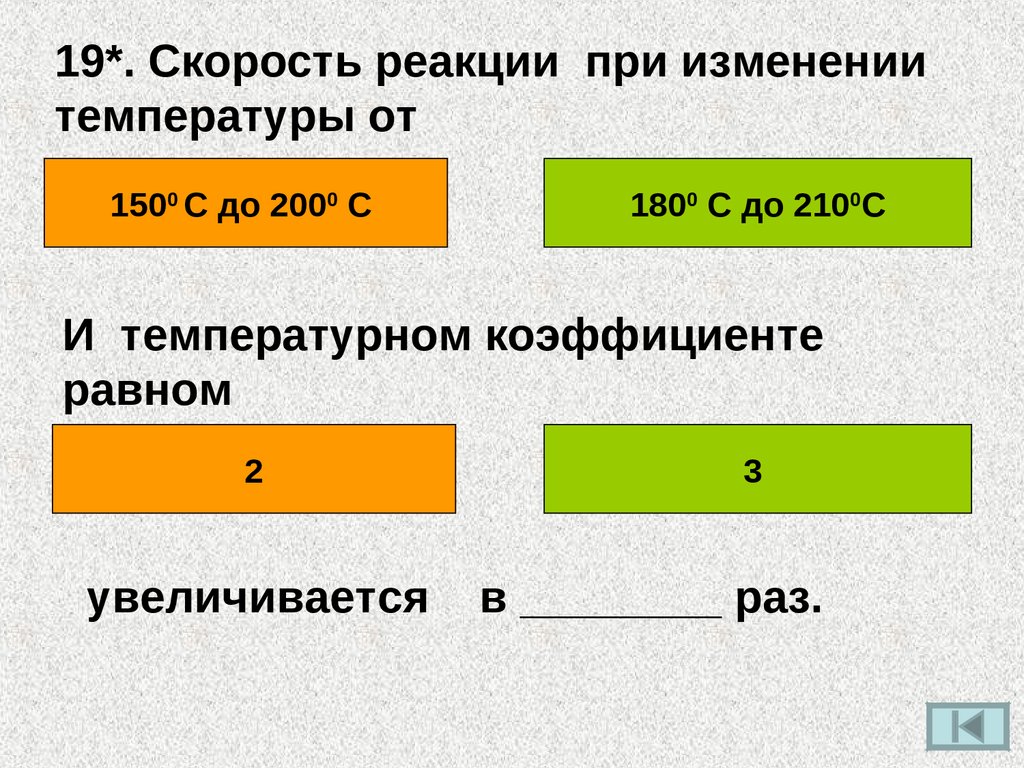
19*. Скорость реакции при изменениитемпературы от
1500 С до 2000 С
1800 С до 2100С
И температурном коэффициенте
равном
2
увеличивается
3
в ________ раз.
23.
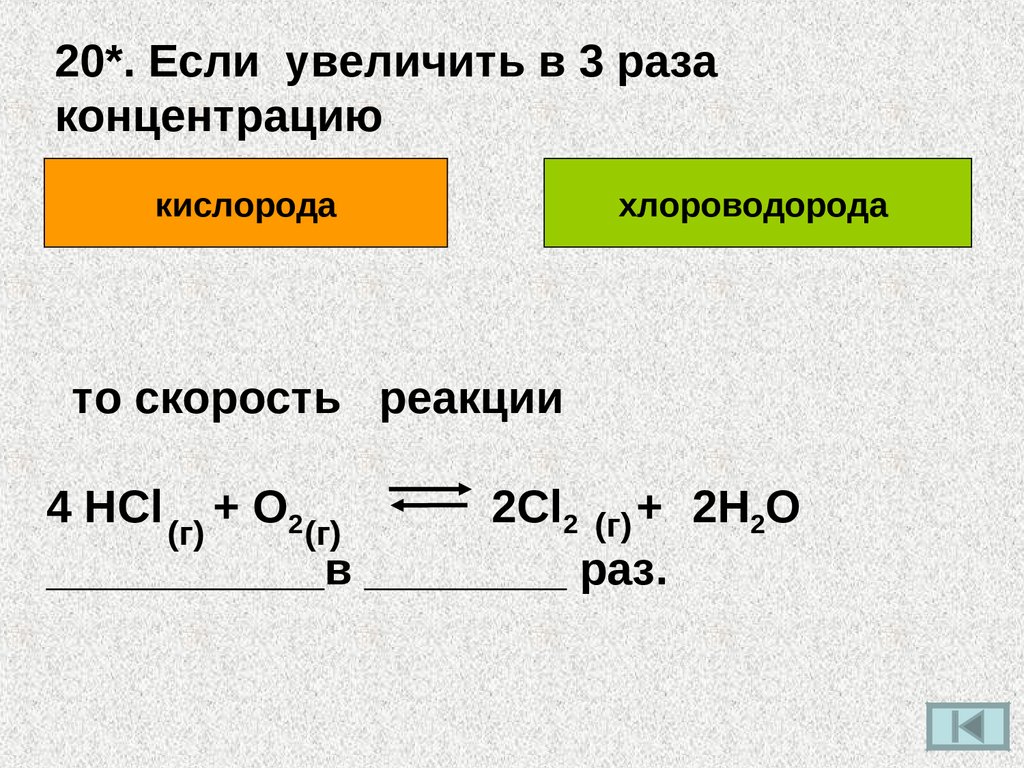
20*. Если увеличить в 3 разаконцентрацию
кислорода
хлороводорода
то скорость реакции
4 HCl (г) + O2 (г)
2Cl2 (г) + 2H2O
___________в ________ раз.








 chemistry
chemistry








