Similar presentations:
Гидролиз солей. 9 класс
1.
ГИДРОЛИЗ СОЛЕЙ9 класс
2.
Тема: Гидролиз солейЦель: изучить сущность гидролиза солей в водных
растворах.
Задачи :
сформулировать определение понятия «гидролиз»
научиться
объяснять
химические
процессы,
протекающие в водных растворах солей
записывать уравнения реакций гидролиза
предсказывать и объяснять изменение кислотности
среды и образование кислых и основных солей в
этом процессе
познакомиться с ролью гидролиза солей в природе,
хозяйственной деятельности и повседневной жизни
человека.
3.
«ГИДРОЛИЗ» от греческого«гидро» - вода
«лизис» - разложение
4.
ОКРАСКА ЛАКМУСАВ РАЗЛИЧНЫХ СРЕДАХ
Окраска
лакмусово
й бумаги
Среда
Ионы
Раствор щелочи
Синяя
Щелочная
ОН-
Раствор кислоты
Красная
Кислотная
Н+
Дистиллированная
вода
Бесцветная
Нейтральная
Н+ = ОН-
5.
ТипыСоли, образованные
сильной кислотой и
сильным основанием
Примеры
Na2SO4, CsCl, CaBr2, KNO3
Соли, образованные
Na2CO3, Na2SiO3, K2SO3
слабой кислотой и сильным
основанием
Соли, образованные
ZnCl2, CuSO4, AlCl3,
сильной кислотой и слабым NH4ClO4
основанием
Соли, образованные
слабой кислотой и слабым
основанием
NH4CN, (NH4)2S, Al2S3
6.
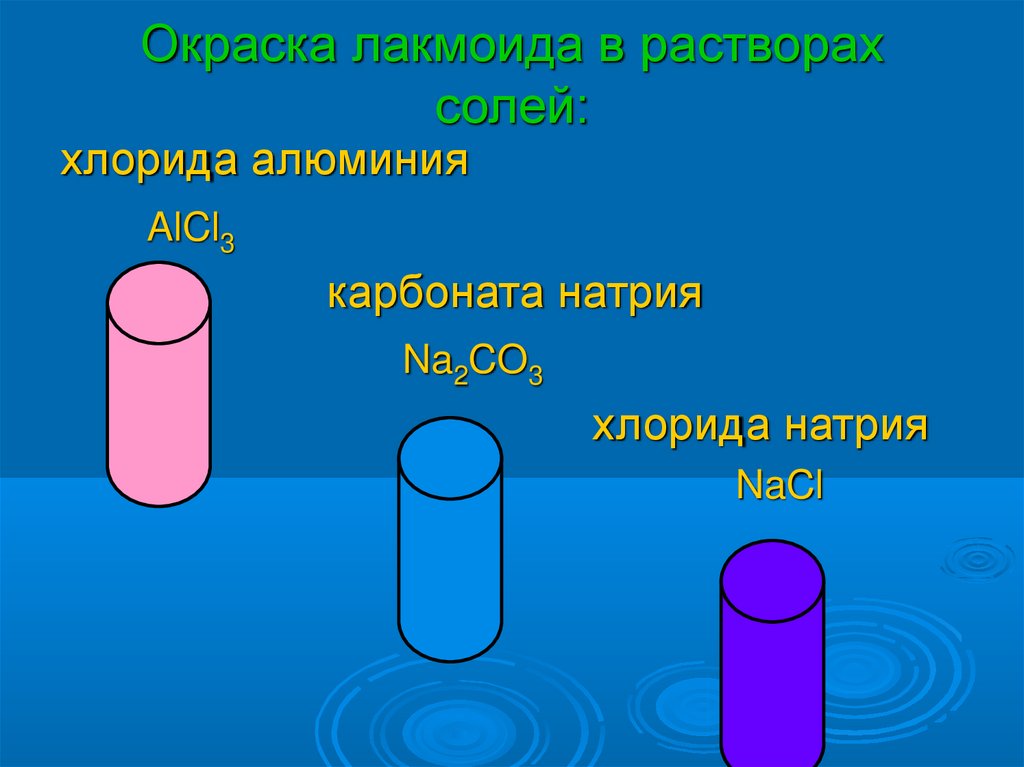
Окраска лакмоида в растворахсолей:
хлорида алюминия
AlCl3
карбоната натрия
Na2CO3
хлорида натрия
NaCl
7.
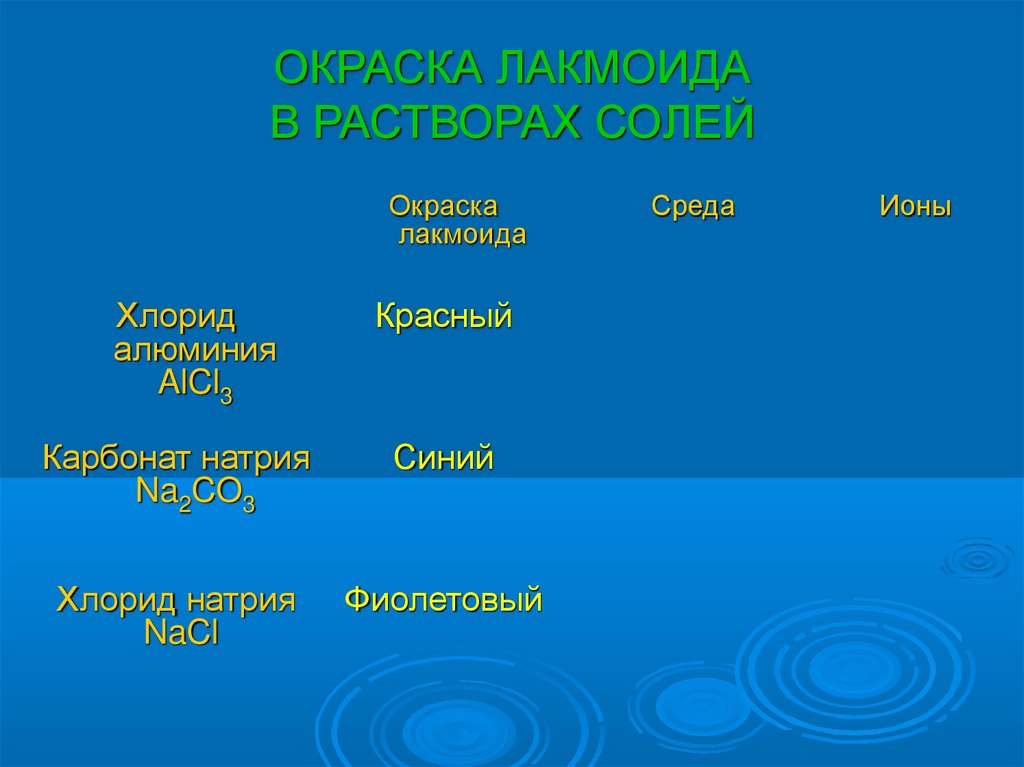
ОКРАСКА ЛАКМОИДАВ РАСТВОРАХ СОЛЕЙ
Окраска
лакмоида
Хлорид
алюминия
AlCl3
Красный
Карбонат натрия
Na2CO3
Синий
Хлорид натрия
NaCl
Фиолетовый
Среда
Ионы
8.
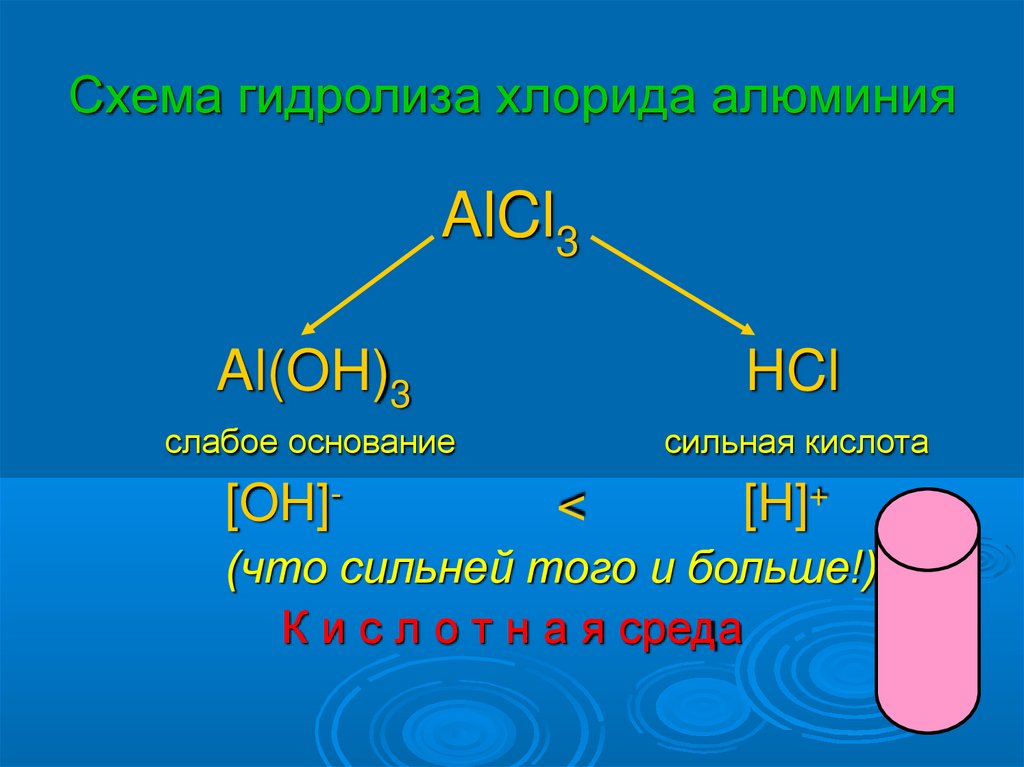
Схема гидролиза хлорида алюминияAlCl3
Al(OH)3
HCl
слабое основание
сильная кислота
[OH]-
<
[H]+
(что сильней того и больше!)
К и с л о т н а я среда
9.
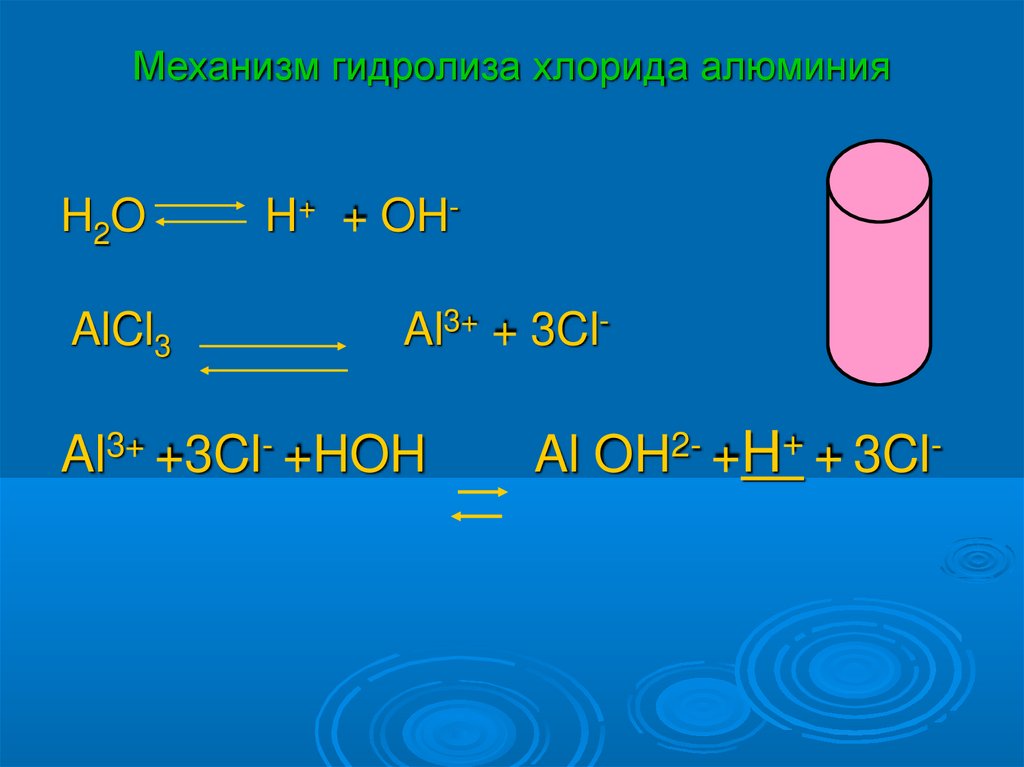
Механизм гидролиза хлорида алюминияH2 O
AlCl3
H+ + OHAl3+ + 3Cl-
Al3+ +3Cl- +HOH
Al OH2- +H+ + 3Cl-
10.
АЛГОРИТМСОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ
Определить состав соли, то есть указать, каким по
силе основанием и какой по силе кислотой
образована данная соль.
Взять ион слабого электролита и написать
уравнение взаимодействия его с составными
частями одной молекулы воды; в результате получить
краткое ионное уравнение гидролиза.
Написать на основании краткого ионного уравнения
молекулярное уравнение.
Исходные вещества известны – соль и вода.
Продукты гидролиза составить, связывая
образовавшиеся ионы с теми ионами соли, которые
не участвуют в реакции гидролиза.
11.
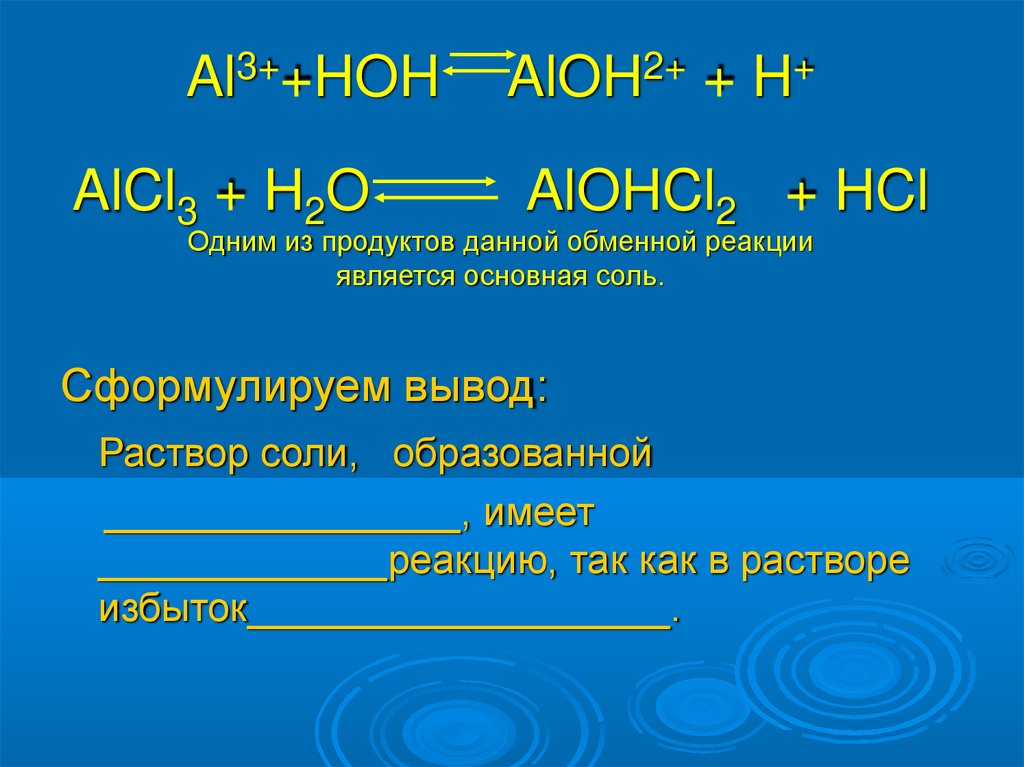
Al3++HOHAlCl3 + H2O
AlOH2+ + H+
AlOHCl2 + HCl
Одним из продуктов данной обменной реакции
является основная соль.
Сформулируем вывод:
Раствор соли, образованной
________________, имеет
_____________реакцию, так как в растворе
избыток___________________.
12.
Схема гидролиза карбоната натрияNa2CO3
NaOH
H2CO3
сильное основание
[OH]-
слабая кислота
>
[H]+
(что сильней того и больше!)
Щ е л о ч н а я среда
13.
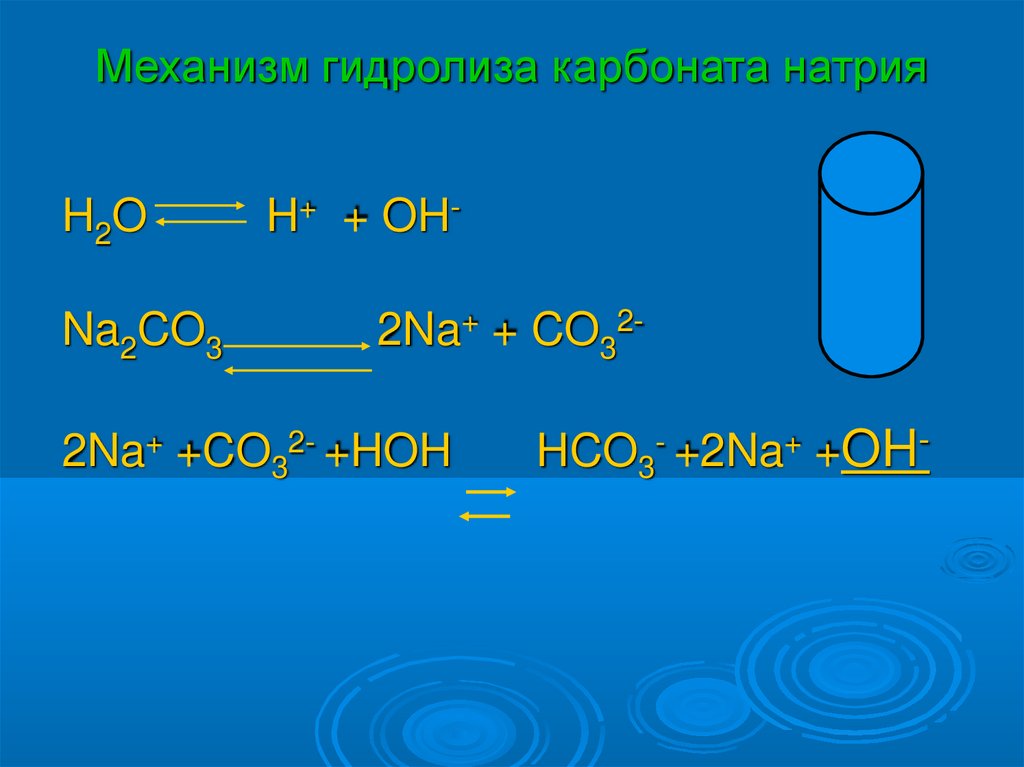
Механизм гидролиза карбоната натрияH2O
Na2CO3
H+ + OH2Na+ + CO32-
2Na+ +CO32- +HOH
HCO3- +2Na+ +OH-
14.
АЛГОРИТМСОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ
Определить состав соли, то есть указать, каким по
силе основанием и какой по силе кислотой
образована данная соль.
Взять ион слабого электролита и написать
уравнение взаимодействия его с составными
частями одной молекулы воды; в результате получить
краткое ионное уравнение гидролиза.
Написать на основании краткого ионного уравнения
молекулярное уравнение.
Исходные вещества известны – соль и вода.
Продукты гидролиза составить, связывая
образовавшиеся ионы с теми ионами соли, которые
не участвуют в реакции гидролиза.
15.
CO32- +HOHHCO3- +OHNa2CO3 +H2O NaHCO3 +NaOH
Одним из продуктов данной обменной реакции
является кислая соль.
Сформулируем вывод:
Раствор соли, образованной
________________,
имеет__________реакцию, так как в растворе
избыток ________________.
16.
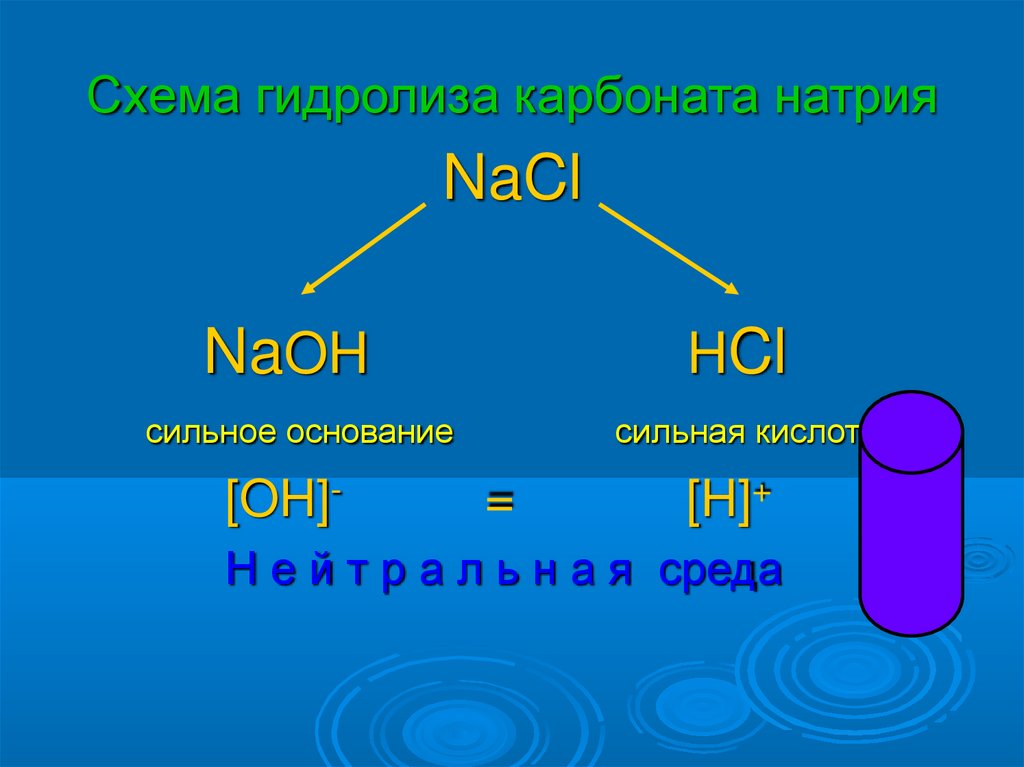
Схема гидролиза карбоната натрияNaCl
NaOH
HCl
сильное основание
[OH]-
сильная кислота
=
[H]+
Н е й т р а л ь н а я среда
17.
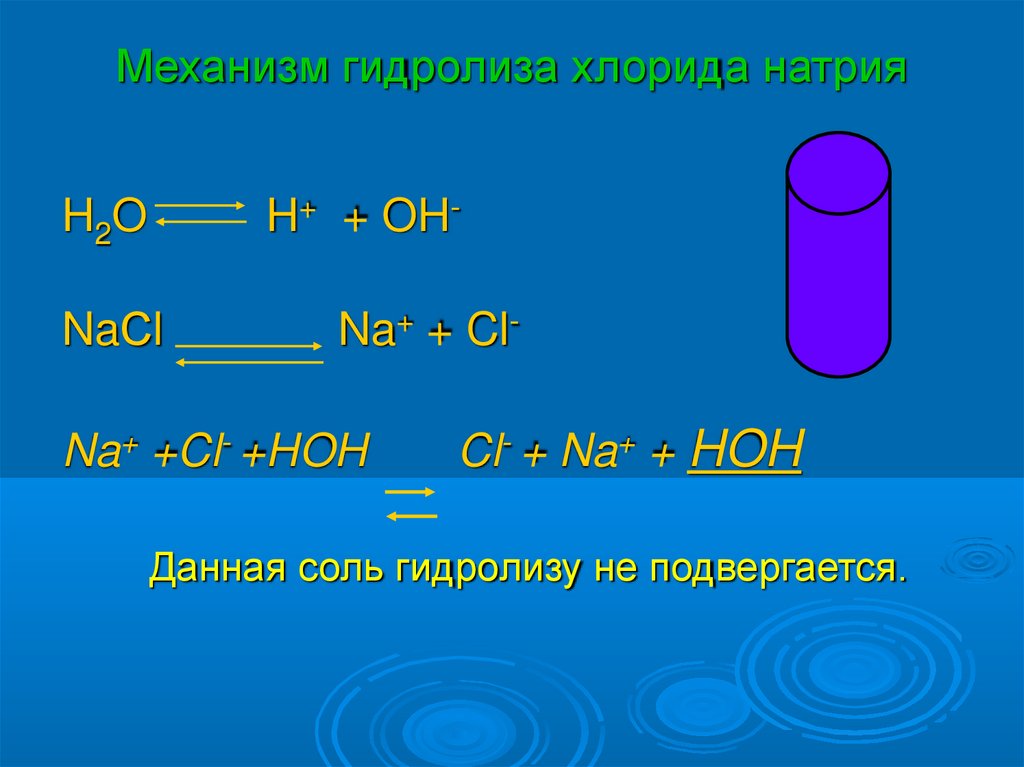
Механизм гидролиза хлорида натрияH+ + OH-
H2O
NaСl
Na+ + Cl-
Na+ +Cl- +HOH
Cl- + Na+ + HOH
Данная соль гидролизу не подвергается.
18.
NaCl + Н2О =Сформулируем вывод:
Раствор соли, образованной__________________,
имеет________________________реакцию, так как в
растворе__________________________________.
19.
Сформулируемопределение понятия «гидролиз»:
К какому типу мы отнесем данные реакции?
Какие вещества в них участвуют?
В чем заключается сущность гидролиза?
Какие продукты данных взаимодействий с
точки зрения теории электролитической
диссоциации мы получили
20.
ГИДРОЛИЗ –это реакция обмена между
некоторыми солями и водой
приводящая к образованию
слабого электролита.
21.
Самостоятельно заполните таблицуНазвание соли
Карбонат
калия
Нитрат
железа (II)
Хлорид
бария
Уравнение гидролиза
Среда
раствора
Окраска
лакмуса
22.
Роль гидролиза в природеПреобразование
Обеспечение
земной коры
слабощелочной среды
морской воды
23.
Роль гидролиза в народном хозяйствеПорча производственного оборудования
Выработка из непищевого сырья ценных
продуктов (бумага, мыло, спирт, глюкоза,
белковые дрожжи)
Очистка промышленных стоков и питьевой воды
(сульфат алюминия + вода
гидроксид
алюминия)
Подготовка тканей к окрашиванию
Известкование почв основано на гидролизе
24.
Роль гидролизав повседневной жизни человека
Стирка
Мытье посуды
Умывание с мылом
Процессы пищеварения

















 chemistry
chemistry