Similar presentations:
Соли (8 класс)
1. СОЛИ
8 классАвтор: Сметанникова Г.П.
МБОУ СОШ №12
2. О чём идет речь? 1
1) Я, конечно, очень нужен,Без меня не сваришь ужин,
Не засолишь огурца,
Не заправишь холодца,
Но не только лишь в еде,
Я живу в морской воде.
Если льется слеза из глаза,
Вкус припомните вы сразу.
Кто догадлив, говорит –
Это….
3. 2
Предложитеспособы получения с
солей?
Изучите химические свойства солей (
выполните их в виде презентации – 6
слайдов
1, 2 слайды - 2 уравнения реакции на
способы получения солей
3, 4, 5, 6 слайды – химические свойства
солей)
4. Названия солей 3
Солибезкислородных кислот
Соли кислородсодержащих кислот
5. медная зелень- ? 4
6. Нахождение в природе 5
Приведитепримеры известных вам
солей в природе и их использование
человеком?
7. Д / З Распределите вещества по основным классам и дайте им названия 6
1)NaCl,
1)
Ba(OH)2, 2) H 2SO4,
1)
HF,
2) NaOH,
2) SO3,
1) Li2O,
2) MgCl2,
1) Na2CO 3,
2) K3PO4,
3) CO2,
3) Cu(OH)2,
3) MgCO3,
3) HNO3,
3) K2S.
8. Ответ 1
СолиФормула: NaCl
Класс:
9. Ответ 2
1.кислота + металл
2. кислота + основный оксид
3. кислота + основание
4. кислота + соль
5. щелочь + кислотный оксид
6. щелочь + соль
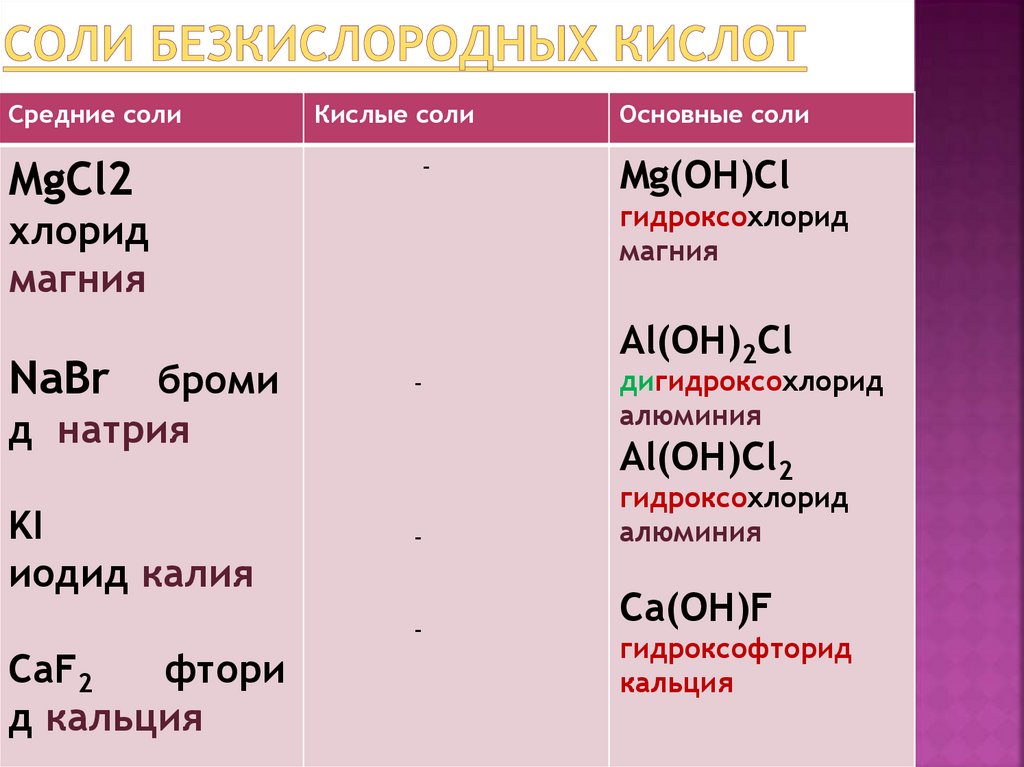
10. Соли безкислородных кислот
Средние солиMgCl2
Кислые соли
-
броми
д натрия
KI
иодид калия
-
Al(OH)2Cl
дигидроксохлорид
алюминия
Al(OH)Cl2
-
CaF2
фтори
д кальция
Mg(OH)Cl
гидроксохлорид
магния
хлорид
магния
NaBr
Основные соли
гидроксохлорид
алюминия
Сa(OH)F
гидроксофторид
кальция
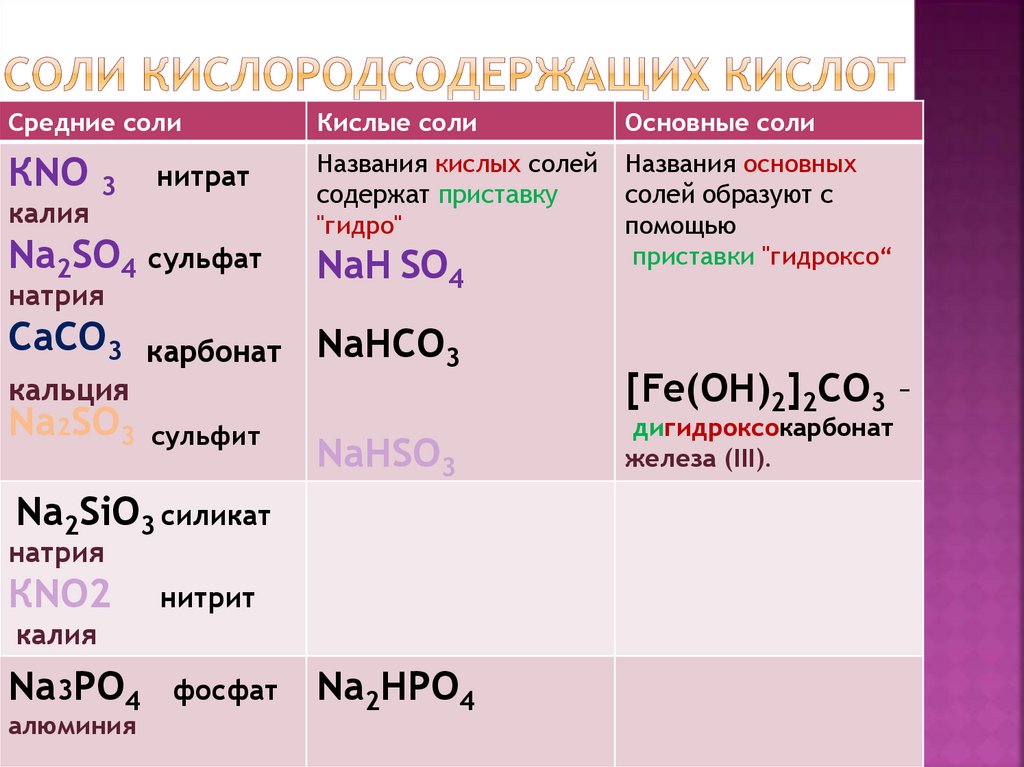
11. Соли кислородсодержащих кислот
Средние солиКислые соли
Основные соли
КNO
Названия кислых солей
содержат приставку
"гидро"
Названия основных
солей образуют с
помощью
приставки "гидроксо“
калия
3
нитрат
Na2SO4
сульфат
NaH SO4
CaCO3
карбонат
NaHCO3
натрия
кальция
Na2SO3
cульфит
NaHSO3
Na2SiO3 силикат
натрия
КNO2
нитрит
калия
Na3PO4
алюминия
фосфат
Na2HPO4
[Fe(OH)2]2CO3 –
дигидроксокарбонат
железа (III).
12. Класс: карбонаты. Формула: CuCO3 . Cu(OH)2 ! 4
дигидроксокарбонатмеди
Состоит из 71.9% CuO оксид меди (Cu 57% ),
19,9% CO2углекислоты и 8,2% H2O воды.
Выражается химической формулой
Cu2(CO3)(OH)2 или (CuOH)2CO3.
Устаревшее химическое название —
медная зелень углекислая.
13. ! 4
Принагревании в колбе выделяет воду,
углекислый газ и становится чёрным:
(CuOH)2CO3 =2CuO +CO2 +H2O
Характерна
растворимость малахита
в кислотах с выделением углекислого
газа, а также в аммиаке, который
окрашивается при этом в красивый
голубой цвет.
14. ! 4
Сглубокой древности известен способ
получения из малахита свободной меди. В
условиях неполного сгорания угля, при
котором образуется угарный газ,
происходит реакция:
(CuOH)2CO3 + 2 CO=3CO2+2Cu +H2O












 chemistry
chemistry








