Similar presentations:
Тепловое движение. Модель идеального газа
1. Тепловое движение. Модель идеального газа
2.
Тепловое движение — беспорядочное(хаотическое) движение атомов и молекул, из
которых состоят все тела. Все молекулы любого
вещества непрерывно и беспорядочно
(хаотически) движутся.
ТЕМПЕРАТУРА – это мера «нагретости» тела.
3. Идеальный газ
Идеальный газ – простейшая физическаямодель реального газа.
Идеальный газ – это газ, взаимодействие между
молекулами которого пренебрежимо мало
Ек >>Ep.
4. Идеальный газ
1.2.
3.
4.
5.
Расстояние между молекулами >d.
Молекулы - упругие шары.
Силы притяжения стремятся к нулю.
Отталкивание – только при ударах.
Движение по законам Ньютона
И
Д
Е
А
Л
Ь
Н
Ы
Й
Г
А
З
5. Идеальный газ Реальный газ
Идеальный газ1. Совокупность
большого числа
молекул массой m0, размерами
молекул пренебрегают.
2. Молекулы находятся на больших
расстояниях друг от друга и
движутся хаотически.
3. Молекулы взаимодействуют по
законам упругих столкновений ,
силами притяжения между
молекулами пренебрегают.
4. Скорости молекул
разнообразны, но при
определенной температуре
средняя скорость молекул
остается постоянной.
Реальный газ
1. Молекулы реального газа не
являются точечными
образованиями, диаметры
молекул лишь в десятки раз
меньше расстояний между
молекулами.
2. Молекулы не взаимодействуют
по законам упругих
столкновений.
6. Зависимость давления идеального газа от:
Массы молекулКонцентрации
молекул
Скорости движения
молекул
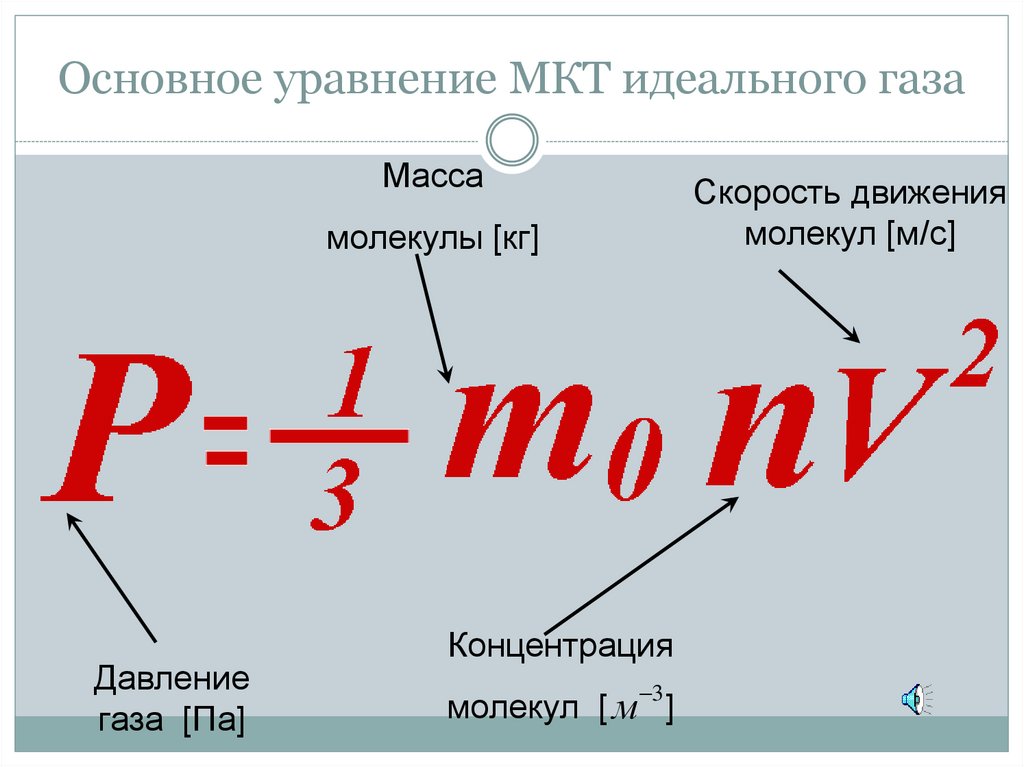
7. Основное уравнение МКТ идеального газа
МассаСкорость движения
молекул [м/с]
молекулы [кг]
Давление
газа [Па]
Концентрация
3
молекул [ м ]
8. Основное уравнение МКТ
Давление идеального газа прямо пропорциональнопроизведению массы молекулы, концентрации
молекул и среднему квадрату скорости молекул.
Концентрация молекул – это число молекул в
единице объема
9. Зависимость давления от кинетической энергии
Т.к. средняя кинетическая энергия поступательнодвижения молекул
,где
- плотность газа
10. Задача.
Каково давление азота, если средняяквадратичная скорость его молекул 500 м/с, а
его плотность 1,35?
Какова средняя квадратическая скорость
движения молекул газа, если имея массу 6 кг,
он занимает объем 5 м3 при давлении 200кПа?
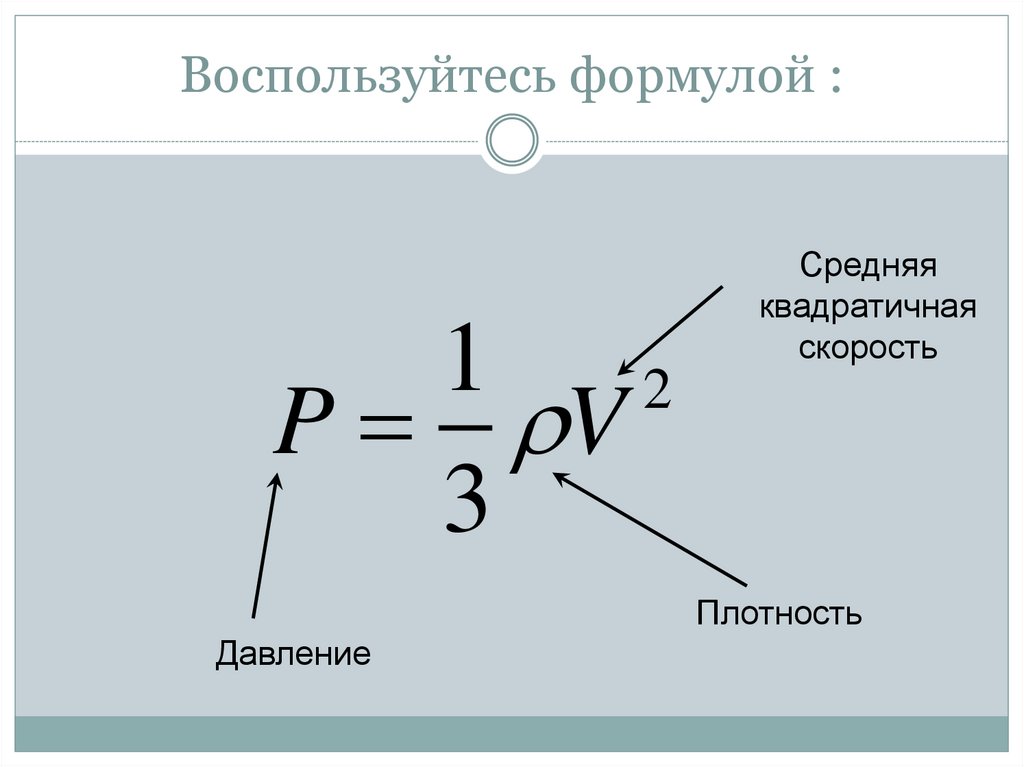
11. Воспользуйтесь формулой :
12
P V
3
Средняя
квадратичная
скорость
Плотность
Давление
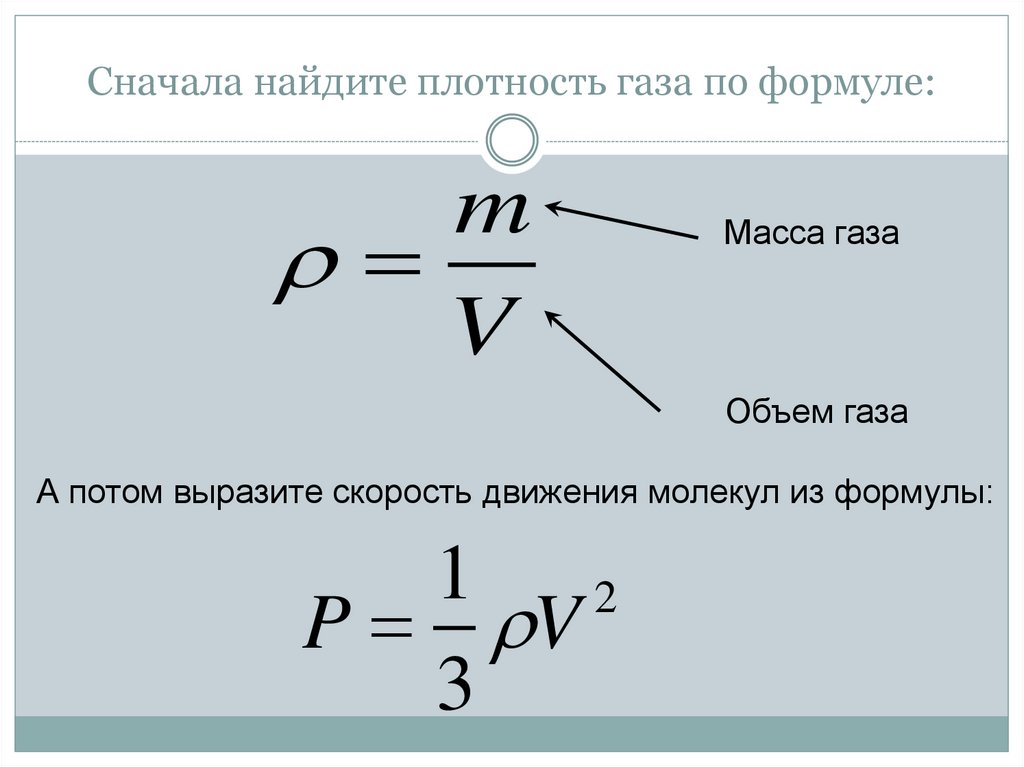
12. Сначала найдите плотность газа по формуле:
mV
Масса газа
Объем газа
А потом выразите скорость движения молекул из формулы:
1
2
P V
3








 physics
physics








