Similar presentations:
Идеальный газ
1. Повторение
1. Что такое МКТ?(Из чего состоитвещество).
2. Почему молекулы обладают только
кинетической энергией?(Формула).
3. При нагревании вещества, молекулы…
и поэтому тело….
4. Что такое броуновское движение? (Опыт)
5. Что такое диффузия?
2. Установите соответствие:
1. Молекулы движутся с огромнымискоростями.
2. Тела сохраняют форму и объем.
3. Атомы колеблются около
положения равновесия.
4.Расстояние между молекулами
превышает размер молекул.
5.Молекулы колеблются, периодически перескакивая на новое
место.
6. Тела сохраняют форму, но не
сохраняют объем.
Ответы: 1-В
2-А
3-А
4-В
А. Твердые
тела.
Б. Жидкости.
В. Газы.
5-Б
6-Б
3. Идеальный газ в МКТ Основы МКТ
4.
ИДЕАЛЬНЫЙ ГАЗИзвестно, что частицы в газах, в отличие от
жидкостей и твердых тел, располагаются друг
относительно друга на расстояниях,
существенно превышающих их собственные
размеры. В этом случае взаимодействие
между молекулами пренебрежимо мало и
кинетическая энергия молекул много больше
энергии межмолекулярного взаимодействия.
Для выяснения наиболее общих свойств,
присущих всем газам, используют упрощенную
модель реальных газов идеальный газ
5.
Идеальный газ(модель)
Реальный газ
1. Совокупность большого числа
молекул массой m0, размерами
молекул пренебрегают (принимают
молекулы за материальные точки).
2. Молекулы находятся на больших
расстояниях друг от друга и
движутся хаотически.
3. Молекулы взаимодействуют по
законам упругих столкновений ,
силами притяжения между
молекулами пренебрегают.
4. Скорости молекул разнообразны,
но при определенной температуре
средняя скорость молекул остается
постоянной.
1. Молекулы реального газа не
являются точечными
образованиями, диаметры
молекул лишь в десятки раз
меньше расстояний между
молекулами.
2. Молекулы не взаимодействуют по законам
упругих столкновений.
6. Реальный газ можно считать идеальным, если он сильно разрежен и хорошо нагрет
7. Скорости движения молекул
При одной и той же температуревсе молекулы одного газа движутся
с разными скоростями
Средняя скорость
хаотического движения
нулю:
1 равна
молекул
2
N
ср
0
N
Средняя арифметическая
скорость:
1 2 N
N
Средняя квадратичная
скорость:
2
1
2
2
N
2
N
8.
Микропараметры(характеризуют одну
молекулу)
Макропараметры
(можно измерить приборами)
m0
ЕК
r0
р
m
V
T
p
п
9. В модели «идеальный газ» все молекулы движутся с одинаковыми скоростями равной средней квадратичной
N3
N
6
— молекула
движется по
каждой оси.
— молекул
движутся в одном
направлении
вдоль каждой оси
Все направления движения хаотического движения
молекул равновероятны:
2
х
2
у
2
z
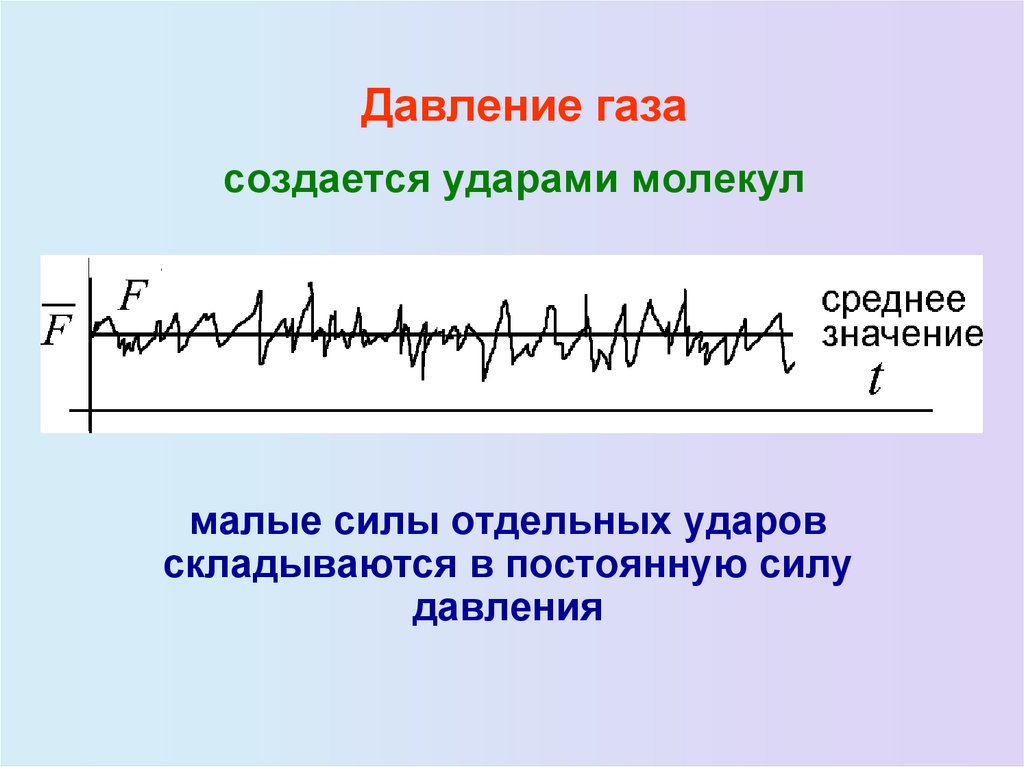
10. Давление газа создается ударами молекул
малые силы отдельных ударовскладываются в постоянную силу
давления
11.
От чего зависит давление идеального газа?12.
13.
14.
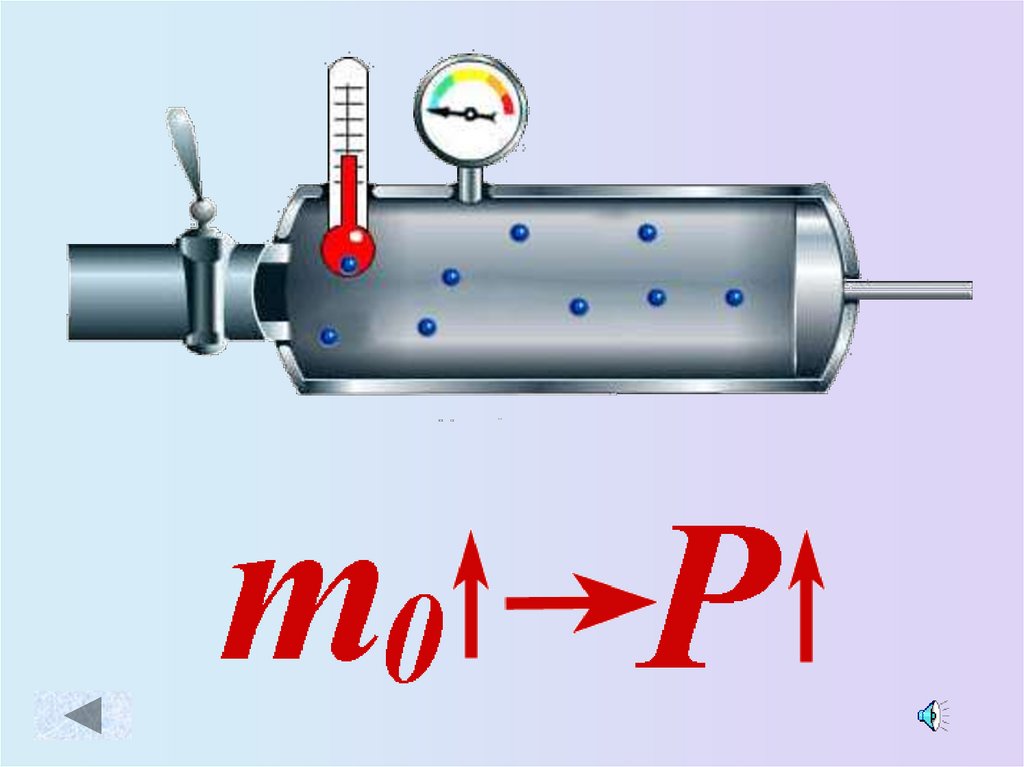
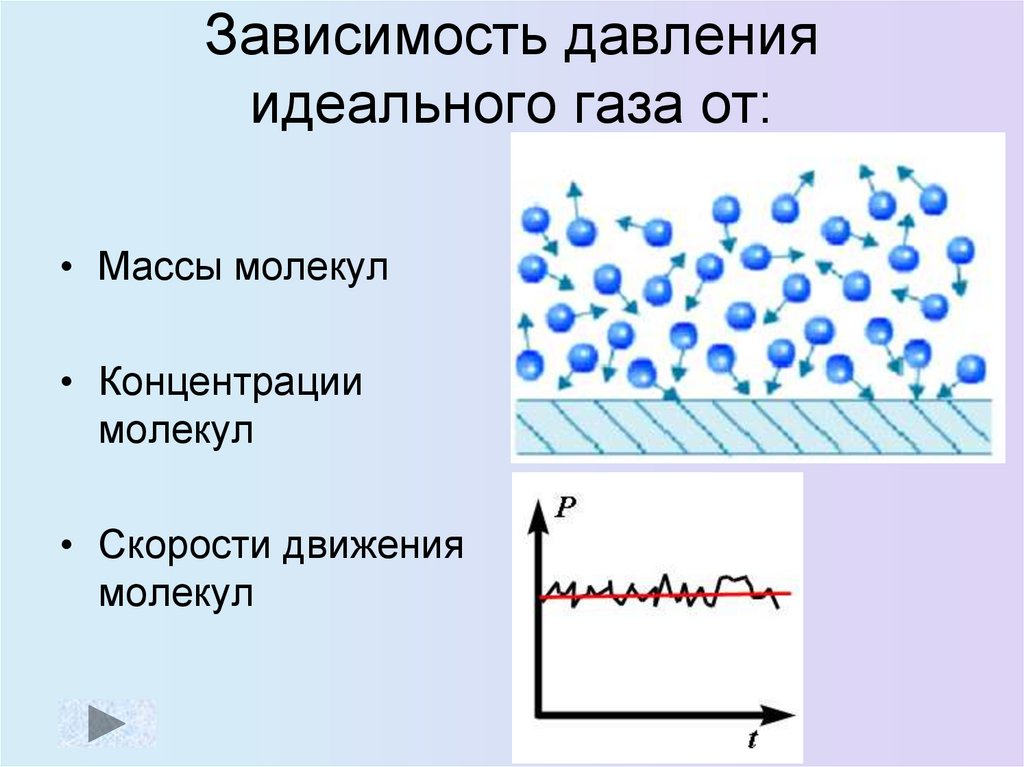
15. Зависимость давления идеального газа от:
• Массы молекул• Концентрации
молекул
• Скорости движения
молекул
16.
12
p nm0
3
- основное
уравнение МКТ
идеального
газа.
2
p nЕК
3
- связь давления со
средней кинетической
энергией
1
2
p
3
[p] = Па(паскаль)
17.
mo- масса молекулы, [m ] = кг0
n
концентрация молекул, [n] = м-3
- средняя квадратичная скорость, [υ]=м/с
Е К - средняя кинетическая энергия, [Е
К
]=Дж
18.
Подведем итоги занятия:1. Что такое идеальный газ?
2. От чего зависит давление идеального
газа?
3. Где можно применить полученные
знания на практике в быту?
19. Как изменится давление газа на стенки сосуда, если:
масса молекулы увеличится в 3 раза
концентрация молекул уменьшится в 4 раза
скорость движения молекул увеличится в 2 раза
объем увеличится в 5 раз
масса молекулы уменьшится в 4 раза, а
концентрация увеличится в 2 раза
• масса молекулы увеличится в 2 раза, а скорость
движения молекул увеличится в 3 раза
• концентрация молекул увеличится в 3 раза,
скорость движения молекул уменьшится в 3 раза
20. Связь давления со средней кинетической энергией
21.
m0 VЕ
2
2
Средняя кинетическая
энергия
поступательного
движения молекулы
m
V
2
2
1
0
2
n
P m0 nV nE
3
2
2
3
2
22.
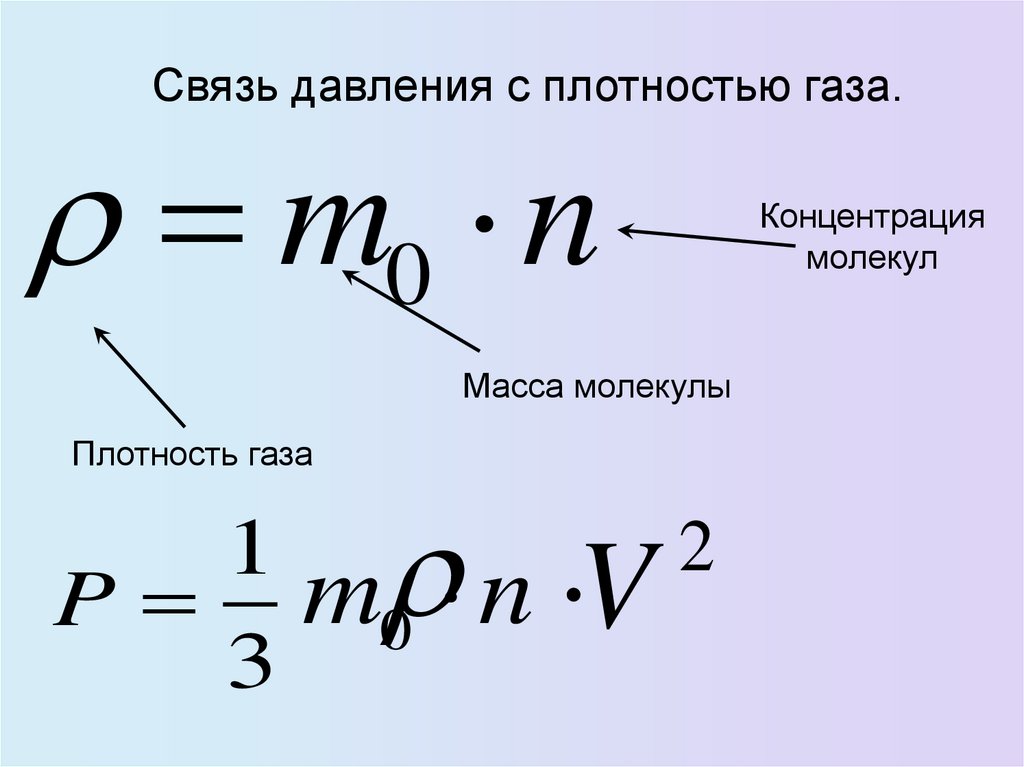
Связь давления с плотностью газа.m0 n
Концентрация
молекул
Масса молекулы
Плотность газа
1
P
3
m0 n V
2
23. Задача.
• №468 Каково давление азота, если средняяквадратичная скорость его молекул 500 м/с, а его
3
плотность 1,35 кг / м ?
подсказка
решение
•№469 Какова средняя квадратическая скорость
движения молекул газа, если имея массу 6 кг, он
3
занимает объем 5 м при давлении 200кПа?
подсказка
решение
24.
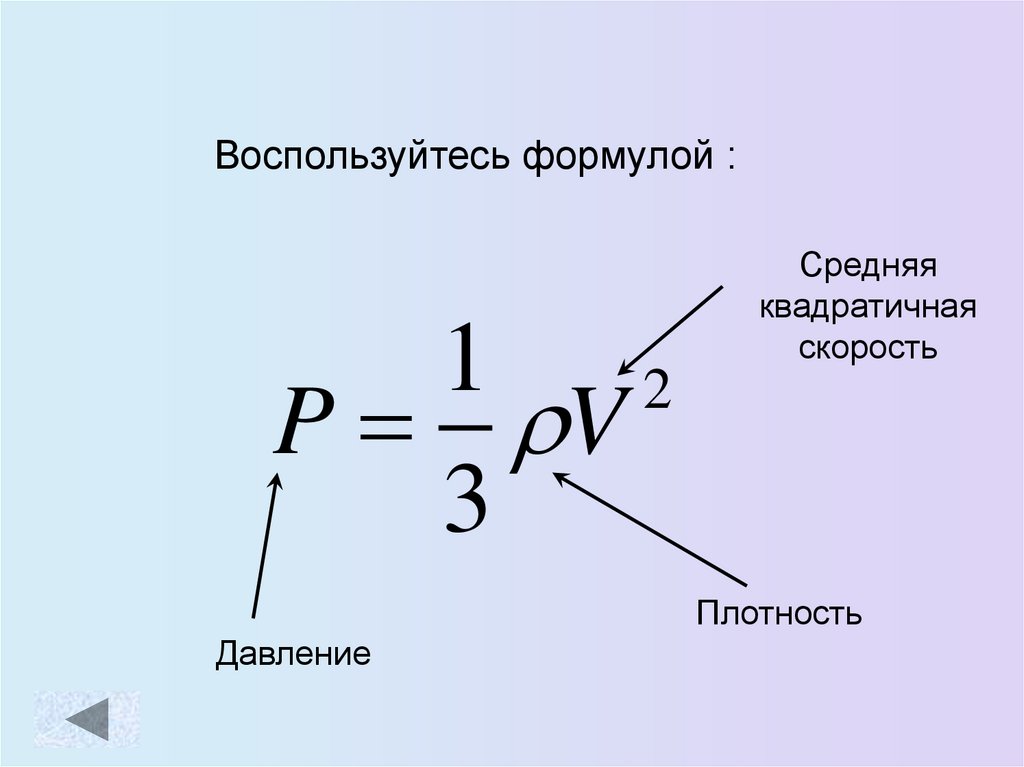
Воспользуйтесь формулой :1
2
P V
3
Средняя
квадратичная
скорость
Плотность
Давление
25.
Дано :Решение:
V 500 м / с
1,35кг / м
Найти :
Р ?
3
1
2
P V
3
1
2
P 1,35 500
3
112500 Па
112,5кПа
Ответ: 112,5кПа
26. Сначала найдите плотность газа по формуле:
mV
Масса газа
Объем газа
А потом выразите скорость движения молекул из формулы:
1
2
P V
3
27.
Решение:Дано :
6
m
5
V
3
1, 2 кг / м
m 6кг
V 5м
3
P 2 10 Па
5
Найти :
V=?
V=
3P
3 2 10
1, 2
707 м / с
Ответ: 707 м/с
5





















 physics
physics








