Similar presentations:
Ионные уравнения реакций
1. Ионные уравнения реакций.
2. ВОПРОСЫ
. Какиевещества называются
Что
называется
электролитической
Что
называется
солью
в свете
ТЭД?
Какие
Что
Что
Что
называется
называется
вещества
называется
называются
основанием
кислотой
ионом?
в
электролитами?
в
свете
свете
ТЭД?
ТЭД?
неэлектролитами?
диссоциацией?
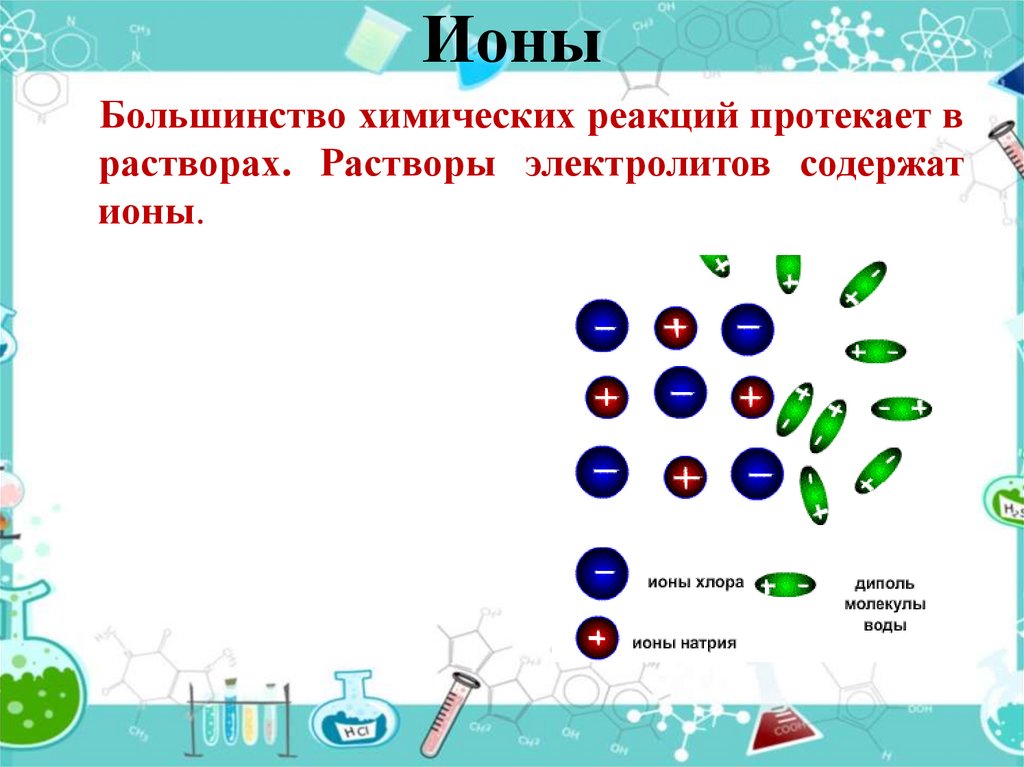
3. Ионы
Большинство химических реакций протекает врастворах. Растворы электролитов содержат
ионы.
4.
НСl + AgNO3 → AgCl + НNO35. .
Реакции ионного обмена записываюттремя уравнениями:
молекулярное
полное ионно-молекулярное
сокращенное ионно-молекулярное
6. .
Ионные реакции – это реакции между ионами.Ионные уравнения – это уравнения ионных реакций.
Например:
2Na+ + CO32- + 2H+ + 2Cl- = 2Na+ +2 Cl- + H2O + CO2
2K+ + CO32-+ 2H+ + 2NO3- =2K+ + 2NO3- + H2O + CO2
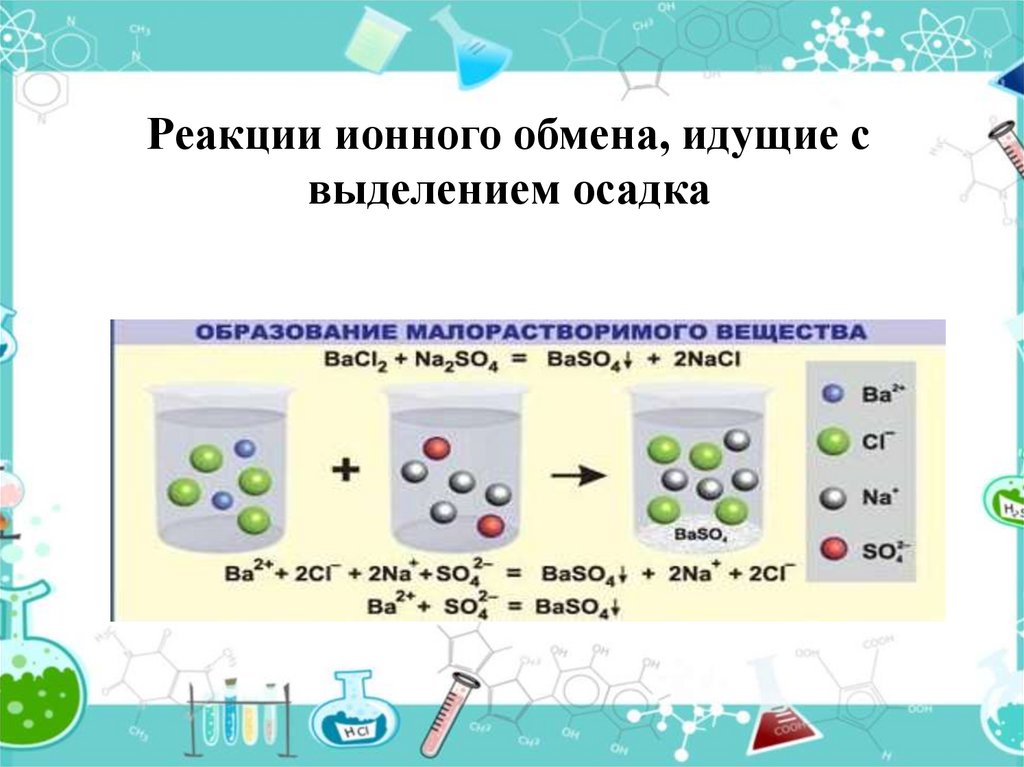
7. Реакции ионного обмена, идущие с выделением осадка
8.
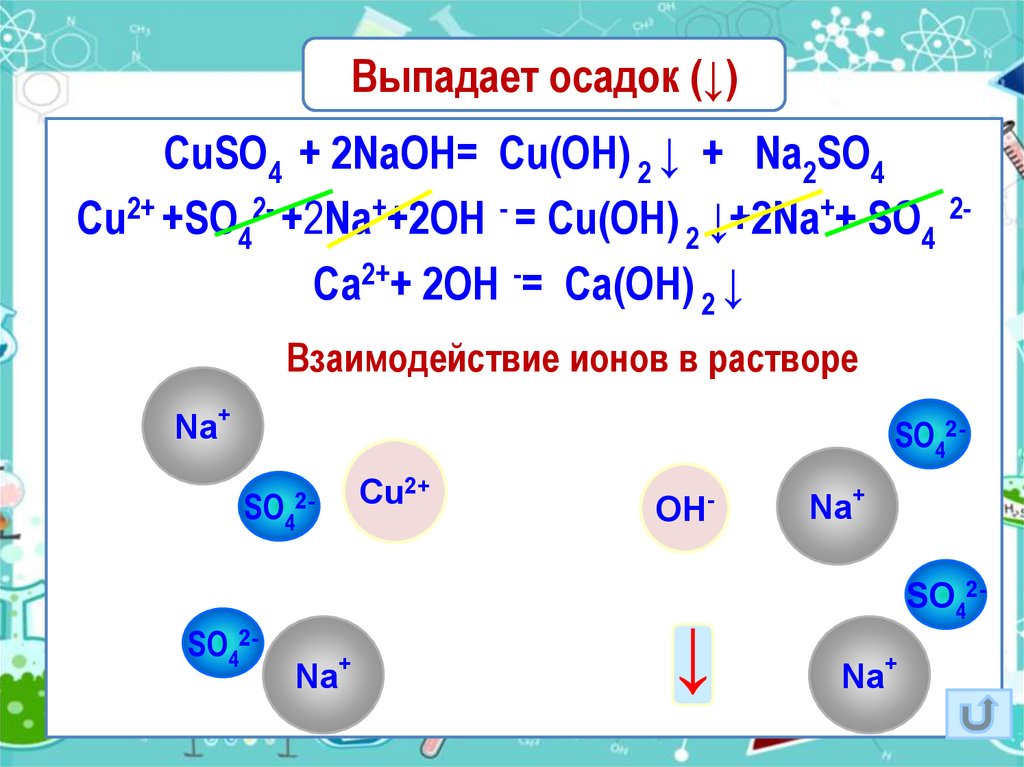
Выпадает осадок (↓)CuSO4 + 2NaOH= Cu(OH) 2 ↓ + Na2SO4
Cu2+ +SO42- +2Na++2OH - = Cu(OH) 2 ↓+2Na++ SO4
Ca2++ 2OH -= Ca(OH) 2 ↓
2-
Взаимодействие ионов в растворе
Na+
SO42SO4
SO42-
2-
Na+
Cu2+
OH-
↓
Na+
SO42Na+
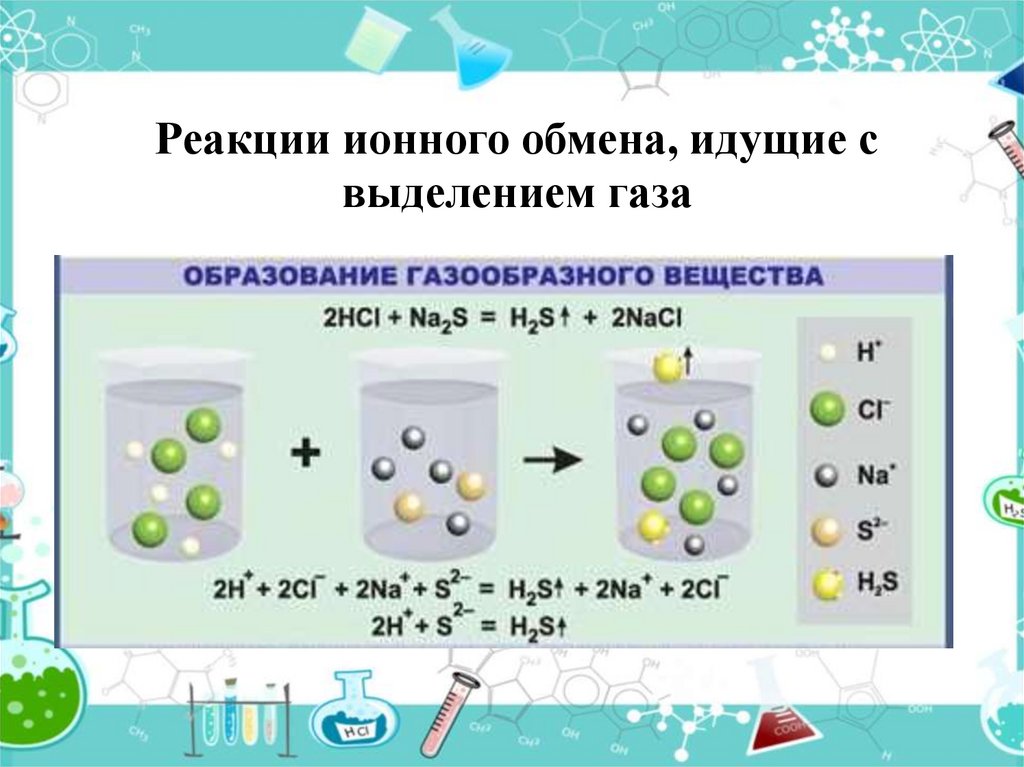
9. Реакции ионного обмена, идущие с выделением газа
10.
Выделяется газ (↑)2HCl + Na2CO3 = H2CO3 + 2 NaCl
H2O + CO2 ↑
2H+ +2Cl-+2Na++CO32- = H2O+CO2↑+2Na++2Cl 2H+ + CO32- = H2O + CO2 ↑
Взаимодействие ионов в растворе
Cl-
Na+
H+
Cl-
2-
CO3
ClNa+
H+
H2O
CO2
Na+
Cl-
Na+
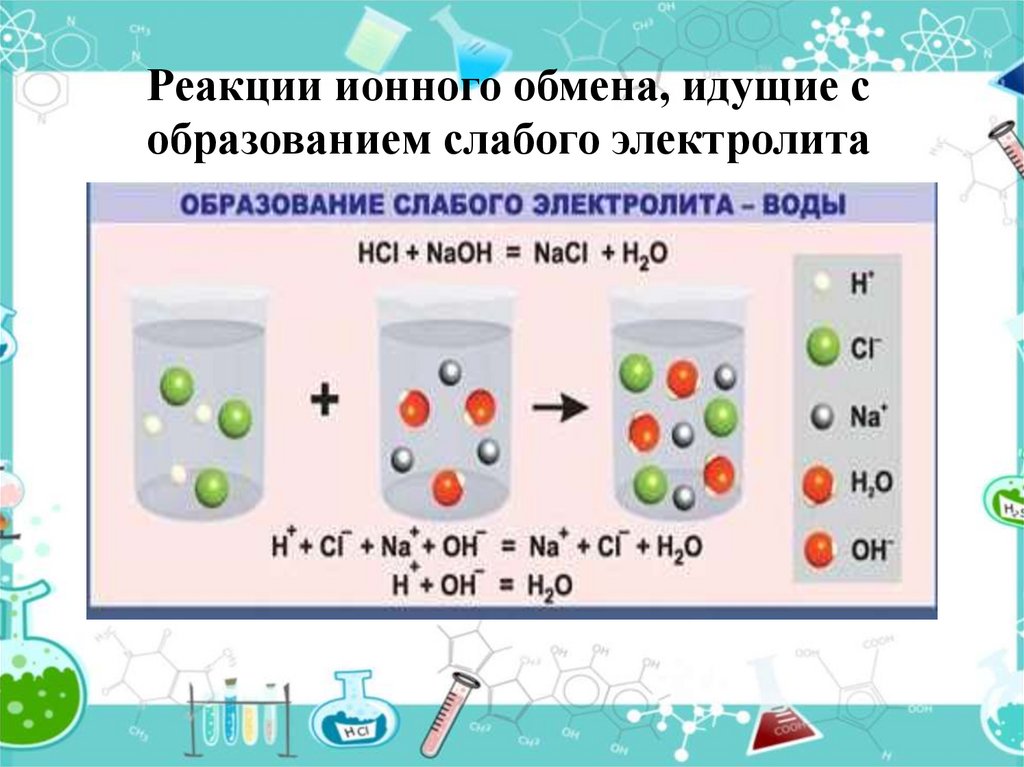
11. Реакции ионного обмена, идущие с образованием слабого электролита
12.
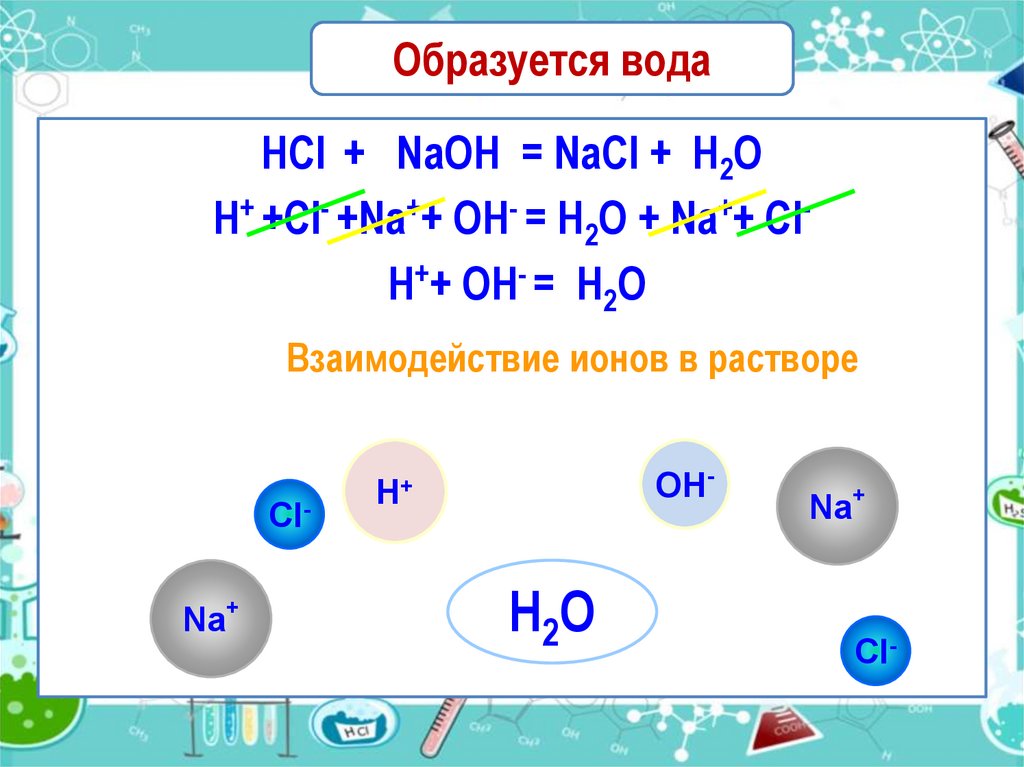
Образуется водаHCl + NaOH = NaCl + H2O
H+ +Cl- +Na++ OH- = H2O + Na++ ClH++ OH- = H2O
Взаимодействие ионов в растворе
ClNa+
OH-
H+
H2O
Na+
Cl-
13. Обратимые реакции
Na2SO4 + KI1.Нет осадка
2.Не выделяется газ
3.Не образуется
слабый электролит
K+
Na+
I-
SO42-
14.
В соответствии с правилом Бертолле ионныереакции протекают практически необратимо:
I случай
III случай
II случай
В остальных случаях реакции обратимы!
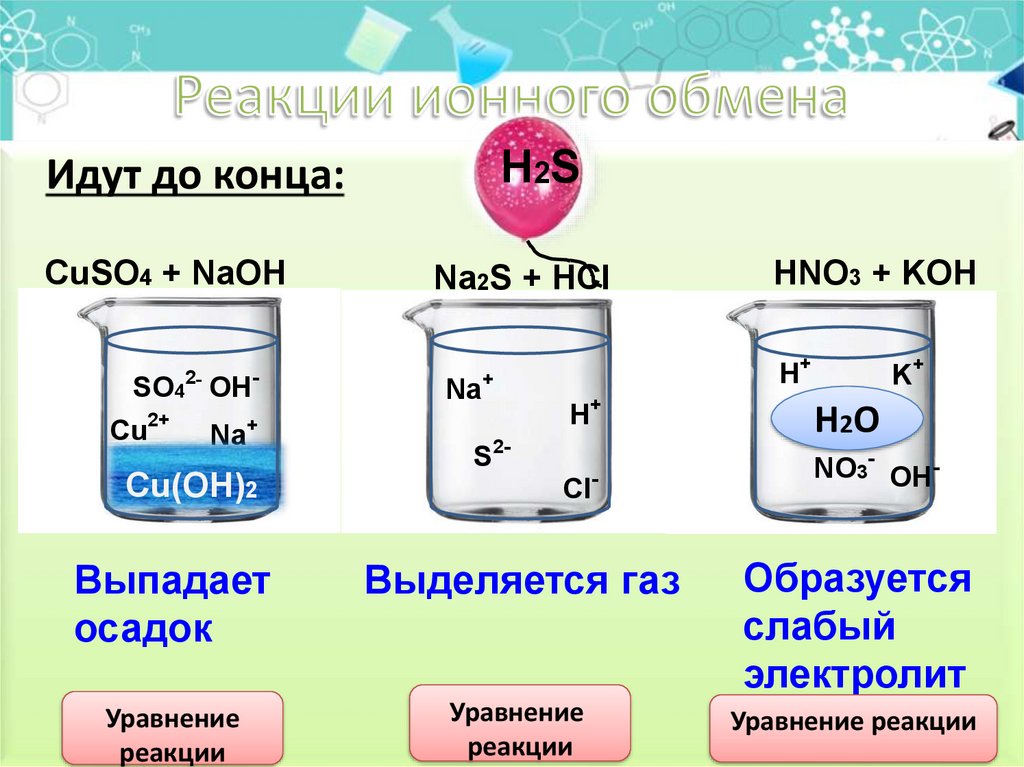
15. Реакции ионного обмена
H2SИдут до конца:
CuSO4 + NaOH
2-
-
SO4 OH
Cu2+ Na+
Сu(OH)2
Na2S + HCl
Na
H+
+
S2-
HNO3 + KOH
K+
H+
H2O
Cl-
NO3- OH-
Выпадает
осадок
Выделяется газ
Образуется
слабый
электролит
Уравнение
реакции
Уравнение
реакции
Уравнение реакции








 chemistry
chemistry








