Similar presentations:
Ионная полимеризация
1.
Ионная полимеризация1. Катионная полимеризация
2. Анионная полимеризация
3. Ионно-координационная полимеризация
2.
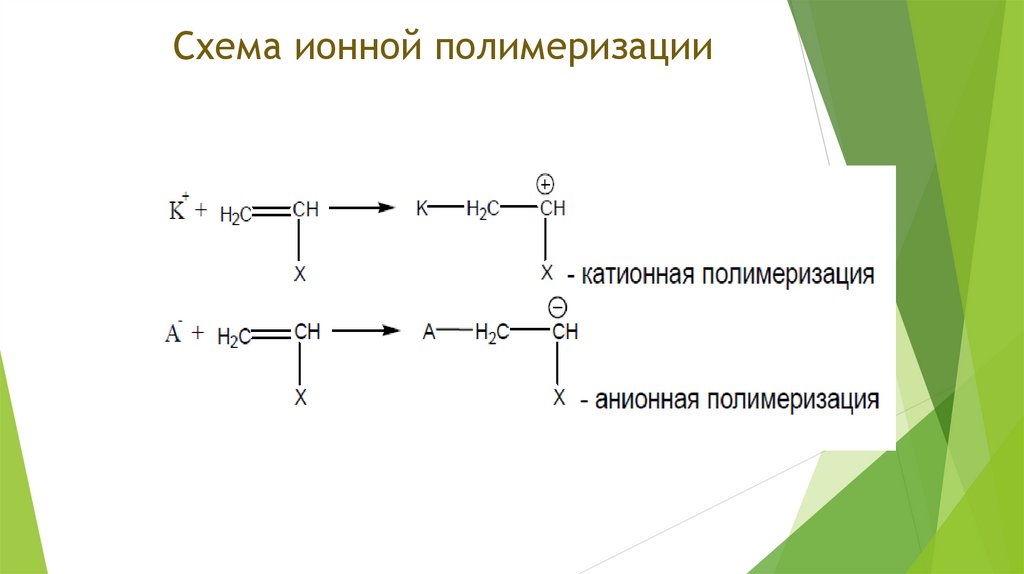
Схема ионной полимеризации3.
Общие черты у радикальной иионной полимеризации
И
те
и
другие
процессы
протекают
по
цепному
механизму:
имеется стадия инициирования цепи
стадия роста цепи
стадия обрыва цепи
Но - Во многих случаях реакции ионной полимеризации могут протекать и
без стадии обрыва цепи («живые макромолекулы»)
4.
Катионная полимеризацияВ процессе катионной полимеризации инициатором процесса являются
катионы.
Поэтому в процесс вступают мономеры с кратной связью С=С, имеющие
избыточную электронную плотность на двойной связи
• Виниловые эфиры активны в
катионной полимеризации
5.
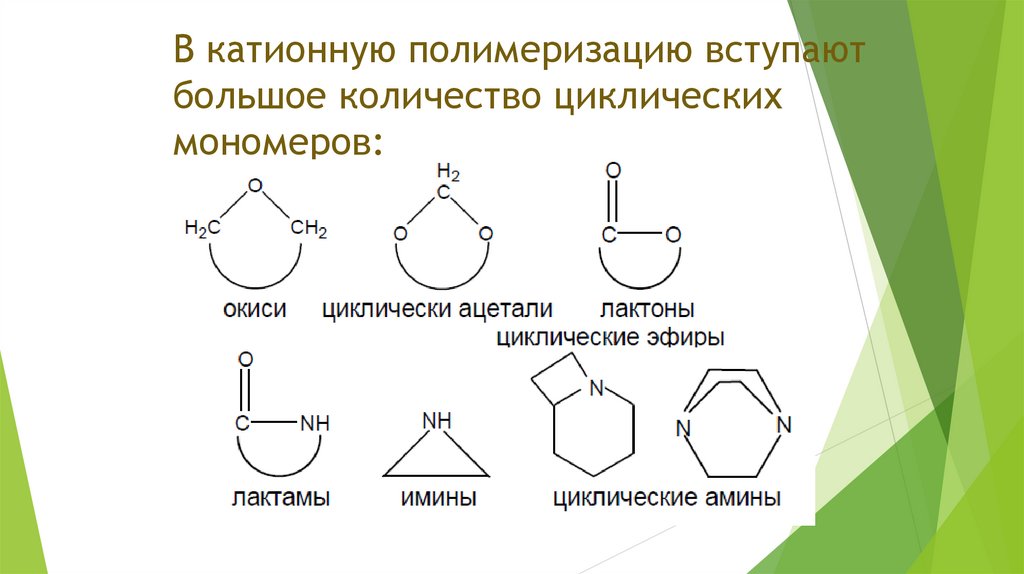
В катионную полимеризацию вступаютбольшое количество циклических
мономеров:
6.
Механизм катионной полимеризации1 стадия. Инициирование
1. Инициирование протонными кислотами.
К наиболее употребляемым для инициирования относятся:
СFзСООН
НСlО4
HI
7.
2. Инициирование кислотами Льюисакислоты Льюиса
доноры протона
ВFз, FеСl3, SnCl4, TiCl4, AlCl3, AlRnClm, PОСl3
Н2О, ROH, RCOOH
доноры карбкатиона (СНз)зСС1, (С6Н5)зСС1
Образование комплекса катализатор-сокатализатор
8.
3. Инициирование ионизирующим излучением.Образование катион-радикалов под действием ионизирующего излучения
Димеризация
Реакция катион-радикала с мономером
9.
4. Фотоинициирование катионной полимеризациисоли диарилиодония
соли триарилсульфония
Ar2 I PF6
Ar3 S SbF6
Воздействие УФ-излучения
Окислительно-восстановительная реакция с сокатализатором
Собственно инициирование катионной полимеризации
10.
Элементарные реакции катионнойполимеризации на примере изопрена
1. Инициирование
2. Рост цепи
11.
3. Передача и обрыв цепиРеакции передачи цепи (без обрыва кинетической цепи).
• бимолекулярная реакция передачи цепи на мономер
• спонтанная мономолекулярная реакция передачи цепи на противоионы
• путем переноса гидрид-иона от мономера к активному центру
12.
3. Передача и обрыв цепиРеакции обрыва кинетической цепи.
• присоединения противоиона или его фрагмента к карбкатиону
13.
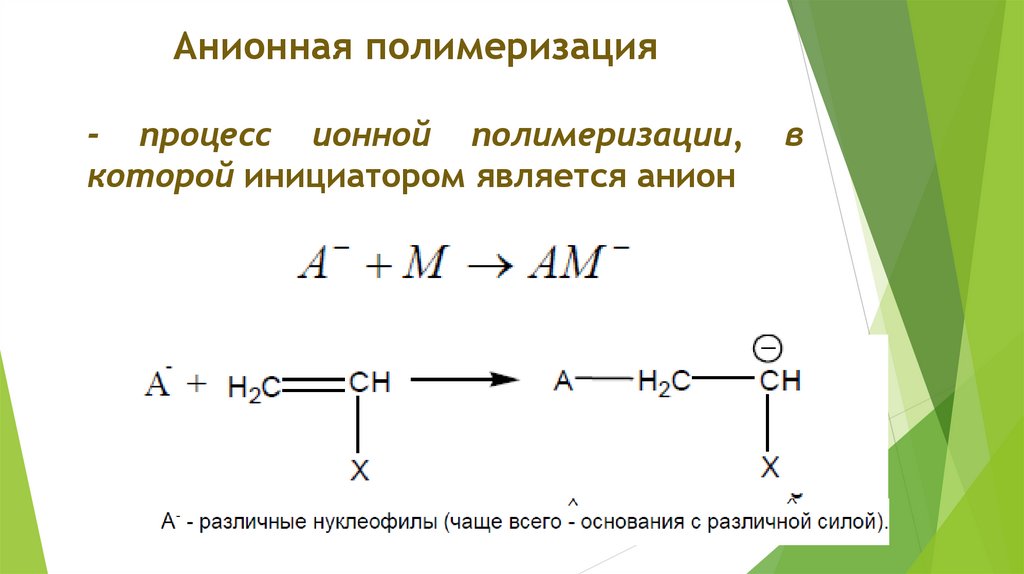
Анионная полимеризация- процесс ионной полимеризации,
которой инициатором является анион
в
14.
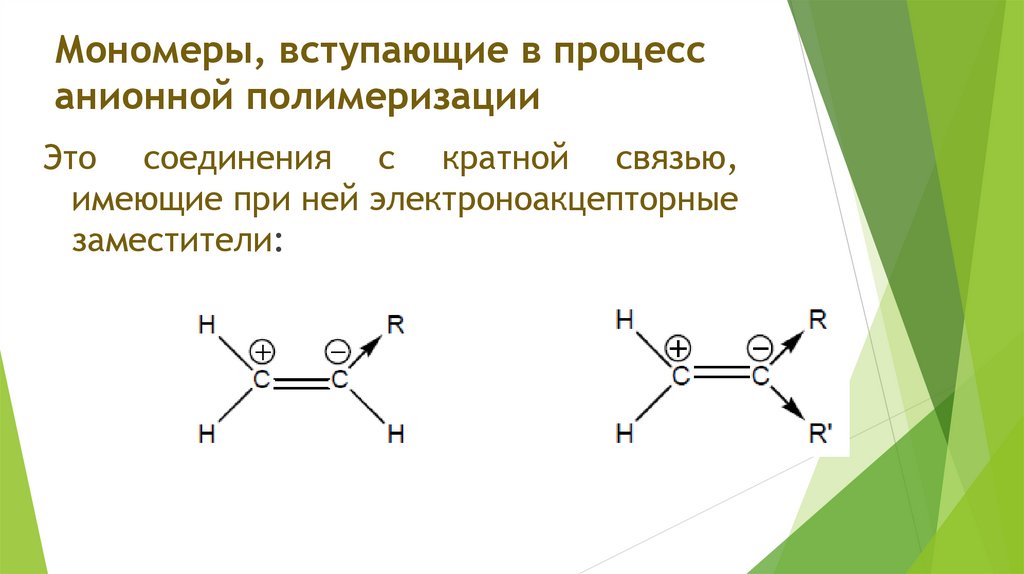
Мономеры, вступающие в процессанионной полимеризации
Это соединения с кратной связью,
имеющие при ней электроноакцепторные
заместители:
15.
По анионному механизму полимеризуетсятакже ряд циклических мономеров:
16.
Инициаторы анионной полимеризацииТребования к инициаторам – «генераторы» анионов в
неполярной среде
1.
Слабые основания:
NH3, NR2H
2. Основания средней силы: к этой группе относятся соединения,
имеющие карбоксильную группу, аминогруппу (-NH2), алкоголяты
щелочных металлов, гидроксиды щелочных металлов.
3. Сильные основания алкилы щелочных или щелочноземельных металлов.
17.
18.
ПОЛИКОНДЕНСАЦИЯ– процесс образования макромолекул в результате
ступенчатого
химического
взаимодействия
функциональных групп многофункциональных мономеров
и n-меров (олигомеров, например), накапливающихся в
ходе реакции, а также молекул n-меров между собой
19.
Механизм поликонденсации1. Рост цепи
По типу участвующих в реакции мономеров поликонденсацию
подразделяют на:
1. ГОМОПОЛИКОНДЕНСАЦИЮ (1 мономер)
Оразование простых полиэфиров
n CH2
CH2
OH
OH
H+
CH2
O
R
CO
TC
полиамиды
n NH2
CH2
o
R COOH
H+
o
NH
TC
n NH2
R COCl
H+
o
TC
n H2O
n +
n H2O
n +
O
NH
R
CO
O
n HCl
n +
20.
2. СОПОЛИКОНДЕНСАЦИЮ (2 и более мономеров)простые полиэфиры
OH R OH + OH R"
OH
O R O R"
n+
n H2O
полиамиды
NH2
R COOH + NH2
R" COOH
NH
R
CO
NH R"
O
NH2
R COCl + NH2
R" COCl
NH
R
CO
O
CO
+ n H2O
n
O
NH R"
CO
O
+ n HCl
n
21.
полиамидыNH2
R
O
C
+
NH2
O
Кат., To
Cl
- HCl
C
R'
Cl
O
NH2
R
C
+
NH2
O
C
R'
RO
NH
R
Кат., To
- ROH
OR
NH
C
C
R'
O
O
сложные полиэфиры
O
HO
R
OH
+
O
C
R'
C
Cl
Cl
O
HO
R
+
OH
O
C
R'
C
OH
R"O
R
OR"
OH
O
+
O
C
R'
HO
O
R
C
OH
O
C
O
R'
Кат., To
- HCl
Кат., To
- H2O
Кат., To
- R"OH
C
O
n
21
22.
3. ИНТЕРСОПОЛИКОНДЕНСАЦИЮ (3 мономера)полиамиды
O
NH2
R
NH2
+ NH2
O
C
R" NH2 +
R'
OH
NH
R
NH
C
O
R'
C
O
C
OH
NH R" NH C
O n
23.
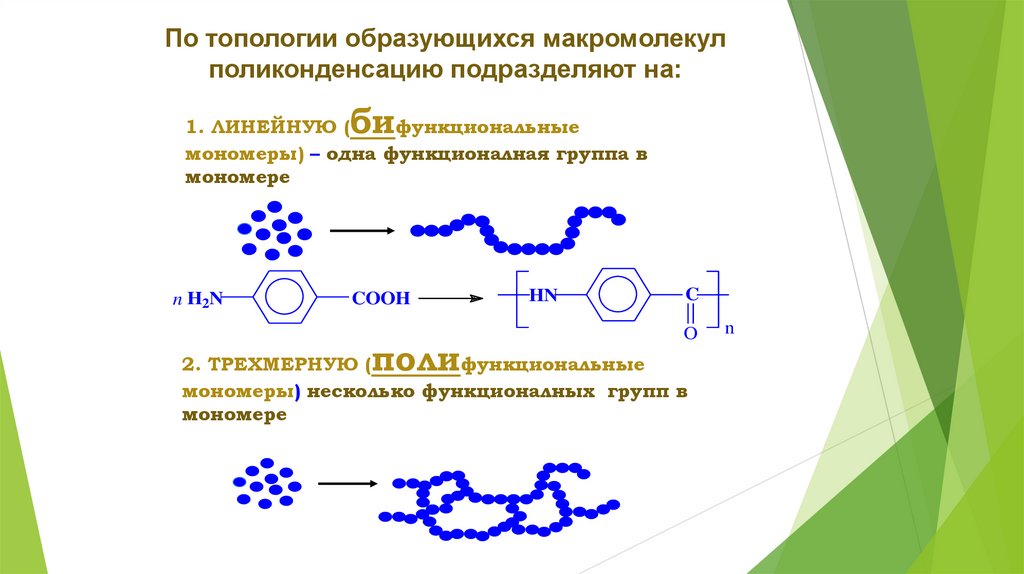
По топологии образующихся макромолекулполиконденсацию подразделяют на:
би
1. ЛИНЕЙНУЮ (
функциональные
мономеры) – одна функционалная группа в
мономере
n H2N
COOH
поли
HN
C
O
2. ТРЕХМЕРНУЮ (
функциональные
мономеры) несколько функционалных групп в
мономере
n
24.
Побочные химические реакции , в результате которых функциональныегруппы утрачивают способность участвовать в реакции роста.
1. обрыв цепи происходит при взаимодействии функциональных групп мономеров с
монофункциональным соединением, присутствующим в виде примеси
или специально введенной добавки .
2. Химическое превращение функциональных групп вследствие
протекания побочных реакций:
HOOC–R-COOH HR-COOH + CO2
ClOC-R-COCl + 2H2O HOOC-R-COOH + 2HCl
3. Циклизация
а) внутримолекулярная
NH
CH2 CH2
C
CH2 CH2
NH2(CH2)5COOH
CH2
O
б) межмолекулярная (реагируют функциональные группы разных
молекул)
CH2 CH2
HOCH2CH2OH + C2H5OOC-COOC2H5
O
C
C
O
O
O
+ 2C2H5OH
25.
КИНЕТИКА ПОЛИКОНДЕНСАЦИИДля поликонденсации характерно исчезновение
мономера уже на ранних стадиях процесса, когда
молекулярная масса продукта реакции ещё очень
мала.
Дальнейший
рост
цепи
происходит
при
практически полном отсутствии мономера в
системе (при полимеризации на ВСЕХ стадиях) наряду
с
макромолекулами,
активными
макрорадикалами
(анионами
и
катионами)
присутствует мономер).
26.
ПОЛИПРИСОЕДИНЕНИЕРеакции проходят без выделения низкомолекулярного продукта
диамин
диизоцианат
NH2
R
NH2
+
NH2
R
NH
C
O
C
NH
N
R'
R'
N
N
C
C
O
O
NH2
R
NH2
Полимочевины
O
NH2
R
NH
C
NH
R'
NH
C
O
HO
R
диизоцианат
+
OH
O
C
N
R'
N
C
O
HO
R
NH2
R
O
гликоль
OH
NH
O
C
NH
R'
N
C
R
O
OH
O
NH2
R
O
C
O
NH
R'
NH
C
O
O
R
OH
Полиуретаны
27.
Сравнительные характеристики реакцийполимеризации и поликонденсации
полимеризация
1.
цепная
реакция
присоединения
активных
центров (радикалов, анионов ,
катионов) к кратным связям
мономеров.
2.
не
выделяется
низкомолекулярное вещество.
3.
молекулярная
масса
образующегося
полимера
практически не зависит от
конверсии.
4.
практически
нет
промежуточных олигомеров.
поликонденсация
1. ступенчатая реакция между
функциональными
группами
многофункциональных
мономеров.
2.
выделяется
низкомолекулярное
вещество,
которое необходимо удалять из
реакционной среды.
3. молекулярная масса полимера
зависит от конверсии и от
концентрации
низкомолекулярного вещества.
4. промежуточные олигомеры
стабильны
и способны к
дальнейшим реакциям.






















 chemistry
chemistry








