Similar presentations:
Галогенидные и полигалогенидные комплексы висмута и теллура: синтез и физико-химические свойства
1.
ГАЛОГЕНИДНЫЕ И ПОЛИГАЛОГЕНИДНЫЕ КОМПЛЕКСЫ ВИСМУТА ИТЕЛЛУРА: СИНТЕЗ И ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Усольцев Андрей Николаевич
02.00.01 – неорганическая химия
Диссертация на соискание ученой степени кандидата химических наук
Научный руководитель:
с.н.с., к.х.н. Адонин Сергей Александрович
Новосибирск 2019 г.
2.
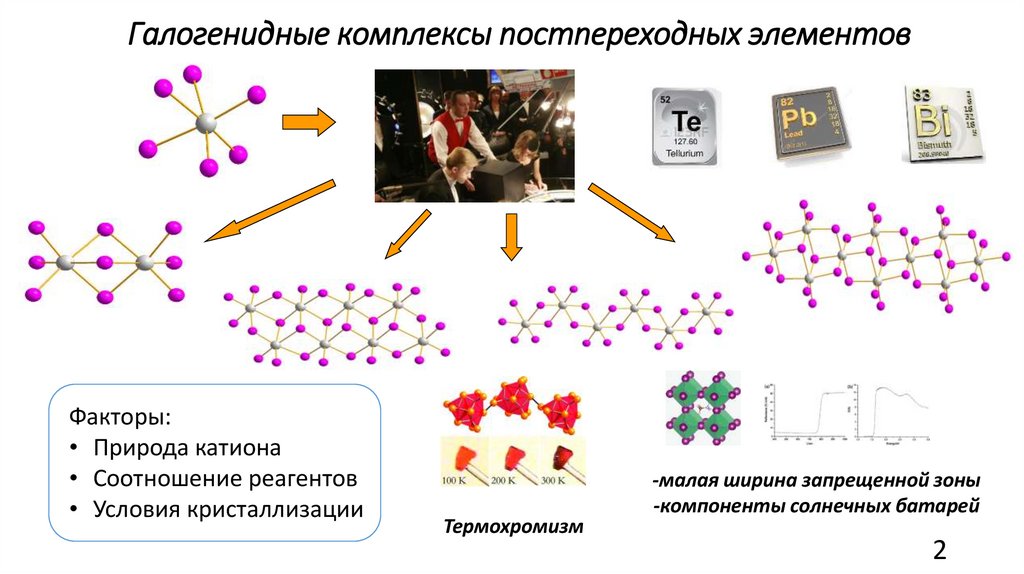
Галогенидные комплексы постпереходных элементовФакторы:
• Природа катиона
• Соотношение реагентов
• Условия кристаллизации
Термохромизм
-малая ширина запрещенной зоны
-компоненты солнечных батарей
2
3.
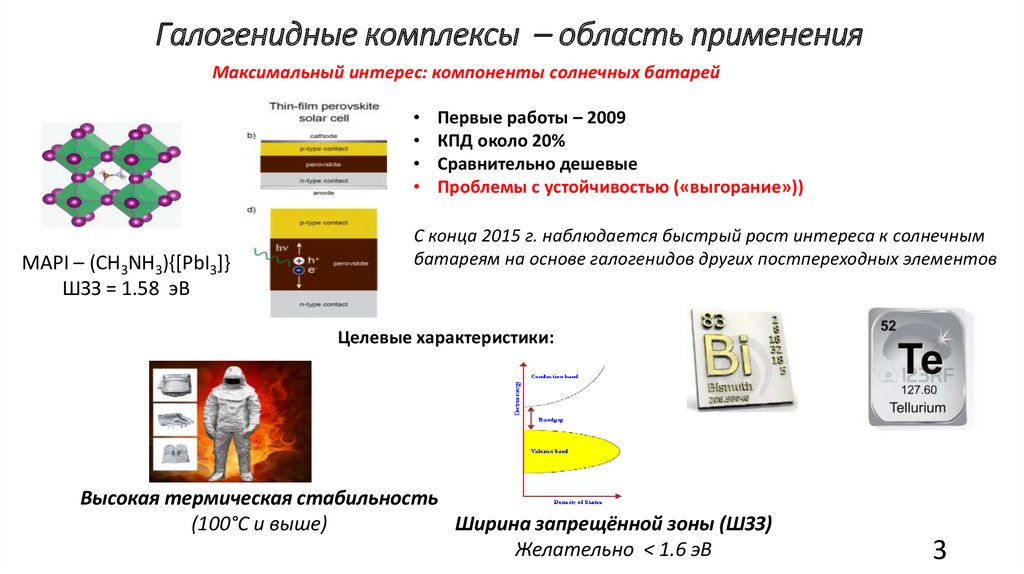
Галогенидные комплексы – область примененияМаксимальный интерес: компоненты солнечных батарей
MAPI – (CH3NH3){[PbI3]}
ШЗЗ = 1.58 эВ
Первые работы – 2009
КПД около 20%
Сравнительно дешевые
Проблемы с устойчивостью («выгорание»))
С конца 2015 г. наблюдается быстрый рост интереса к солнечным
батареям на основе галогенидов других постпереходных элементов
Целевые характеристики:
Высокая термическая стабильность
(100°С и выше)
Ширина запрещённой зоны (ШЗЗ)
Желательно < 1.6 эВ
3
4.
Цель:Изучение закономерностей образования галогенидных и полигалогенидных
комплексов висмута и теллура и изучение их физико-химических свойств
Задачи:
разработка и оптимизация методик синтеза новых галогенидных комплексов
висмута(III) и теллура(IV);
определение структуры полученных соединений методом РСА;
изучение термической стабильности бромо- и иодотеллуратов(IV), а также
полибромид- и полииодид-галогентеллуратов(IV);
изучение оптических свойств полученных соединений, в том числе термохромных
свойств иодовисмутатов(III) и бромотеллуратов(IV).
4
5.
1. Иодовисмутаты: Синтез, структурнаяхарактеризация и оптические свойства
5
6.
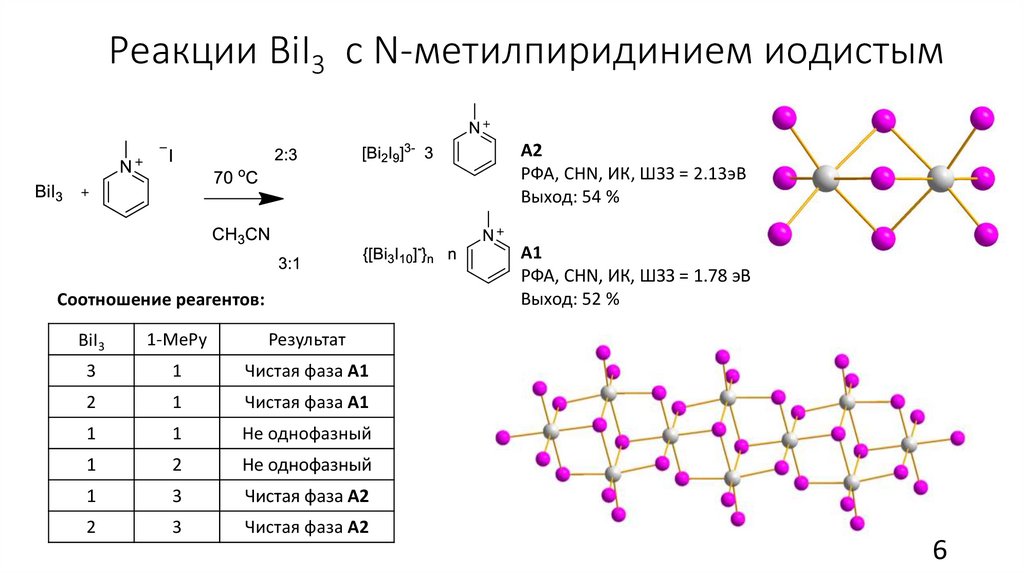
Реакции BiI3 с N-метилпиридинием иодистымА2
РФА, CHN, ИК, ШЗЗ = 2.13эВ
Выход: 54 %
А1
РФА, CHN, ИК, ШЗЗ = 1.78 эВ
Выход: 52 %
Соотношение реагентов:
BiI3
1-MePy
Результат
3
1
Чистая фаза А1
2
1
Чистая фаза А1
1
1
Не однофазный
1
2
Не однофазный
1
3
Чистая фаза А2
2
3
Чистая фаза А2
6
7.
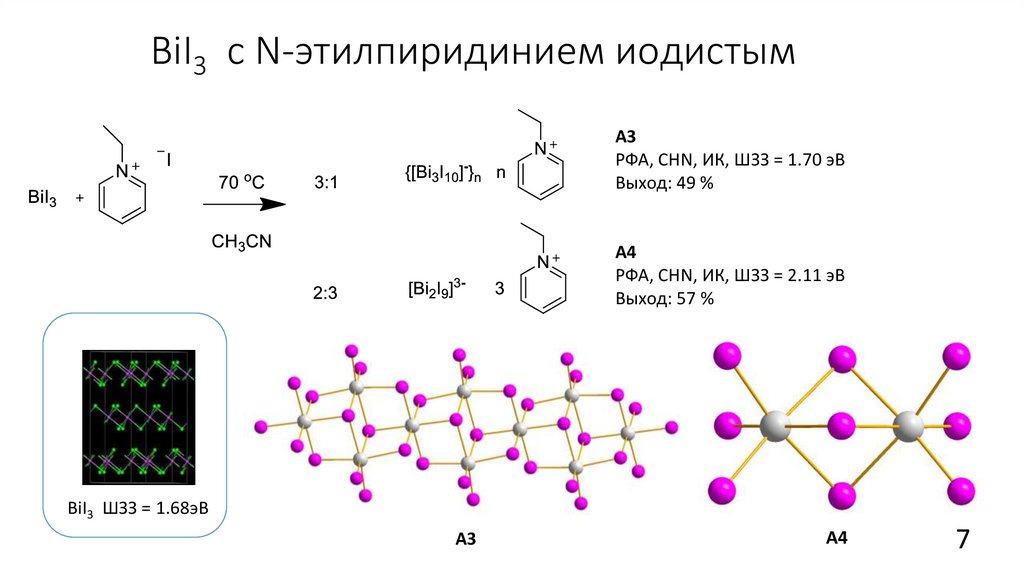
BiI3 с N-этилпиридинием иодистымА3
РФА, CHN, ИК, ШЗЗ = 1.70 эВ
Выход: 49 %
А4
РФА, CHN, ИК, ШЗЗ = 2.11 эВ
Выход: 57 %
BiI3 ШЗЗ = 1.68эВ
А3
А4
7
8.
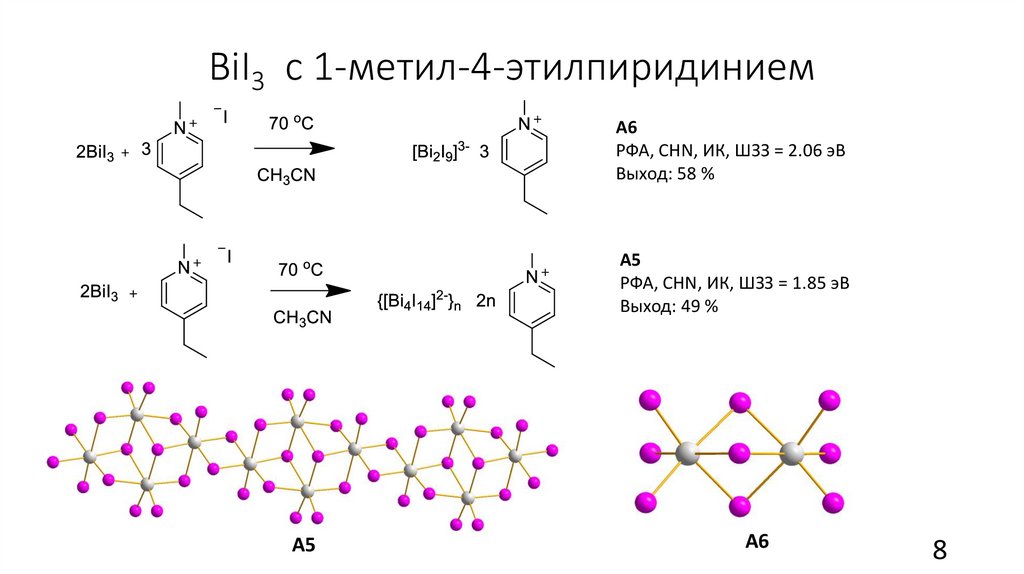
BiI3 с 1-метил-4-этилпиридиниемА6
РФА, CHN, ИК, ШЗЗ = 2.06 эВ
Выход: 58 %
А5
РФА, CHN, ИК, ШЗЗ = 1.85 эВ
Выход: 49 %
А5
А6
8
9.
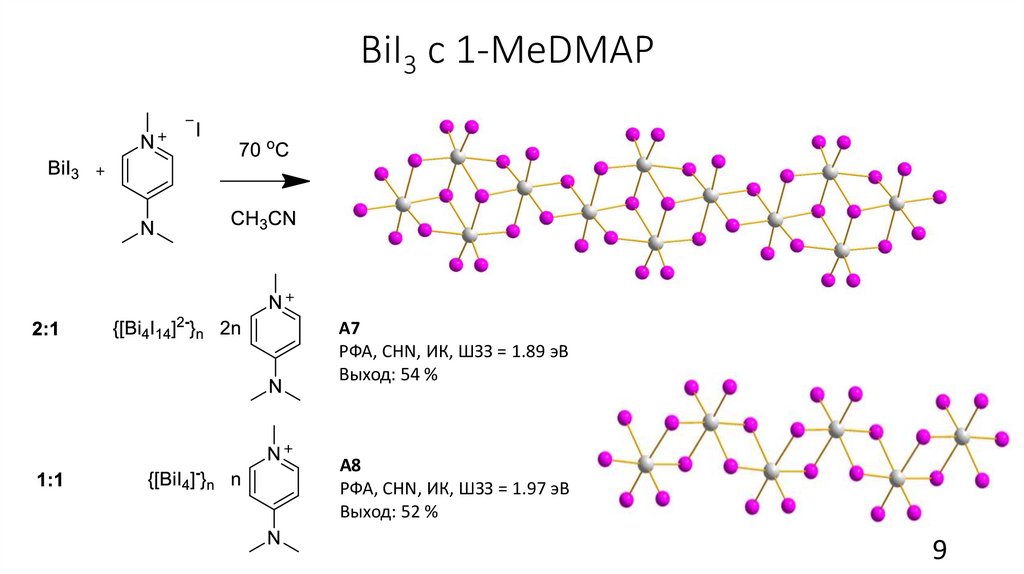
BiI3 с 1-MeDMAPА7
РФА, CHN, ИК, ШЗЗ = 1.89 эВ
Выход: 54 %
А8
РФА, CHN, ИК, ШЗЗ = 1.97 эВ
Выход: 52 %
9
10.
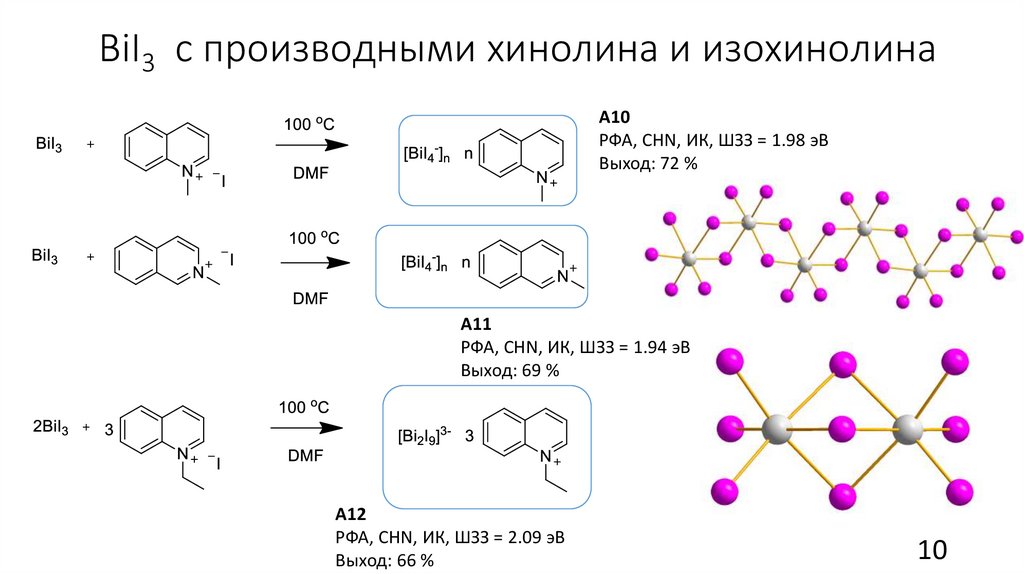
BiI3 с производными хинолина и изохинолинаА10
РФА, CHN, ИК, ШЗЗ = 1.98 эВ
Выход: 72 %
А11
РФА, CHN, ИК, ШЗЗ = 1.94 эВ
Выход: 69 %
А12
РФА, CHN, ИК, ШЗЗ = 2.09 эВ
Выход: 66 %
10
11.
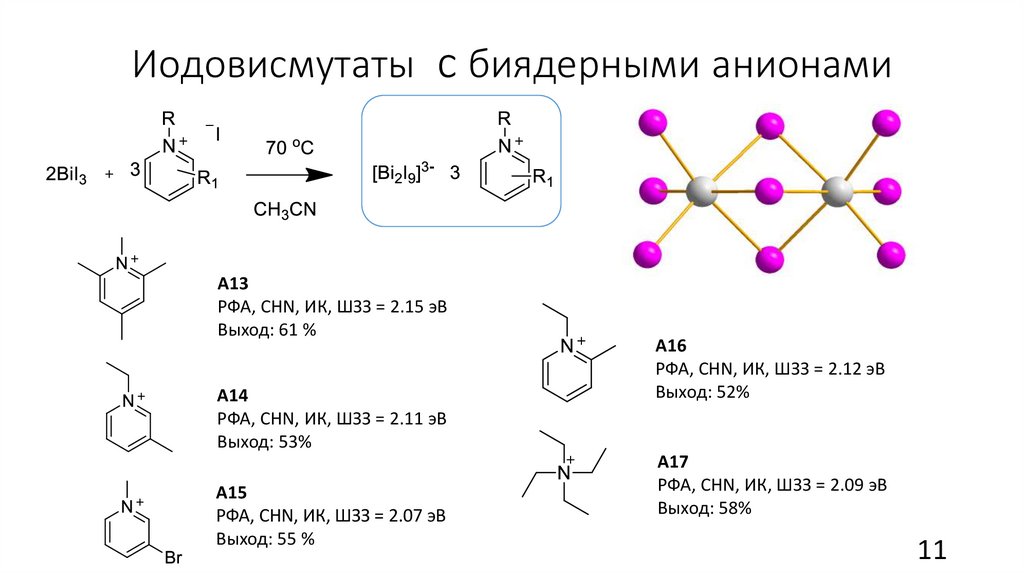
Иодовисмутаты c биядерными анионамиА13
РФА, CHN, ИК, ШЗЗ = 2.15 эВ
Выход: 61 %
А14
РФА, CHN, ИК, ШЗЗ = 2.11 эВ
Выход: 53%
А15
РФА, CHN, ИК, ШЗЗ = 2.07 эВ
Выход: 55 %
А16
РФА, CHN, ИК, ШЗЗ = 2.12 эВ
Выход: 52%
А17
РФА, CHN, ИК, ШЗЗ = 2.09 эВ
Выход: 58%
11
12.
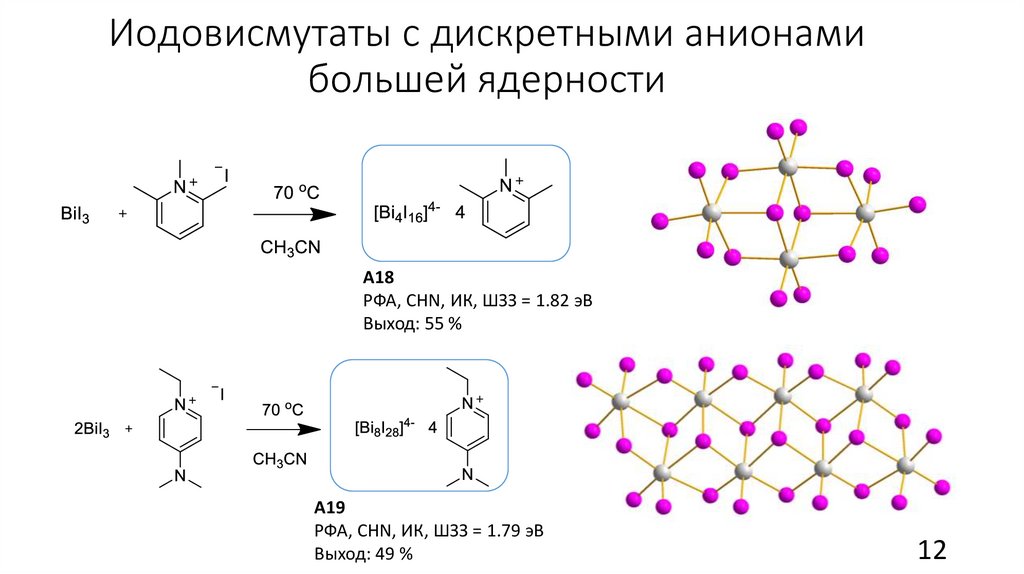
Иодовисмутаты с дискретными анионамибольшей ядерности
А18
РФА, CHN, ИК, ШЗЗ = 1.82 эВ
Выход: 55 %
А19
РФА, CHN, ИК, ШЗЗ = 1.79 эВ
Выход: 49 %
12
13.
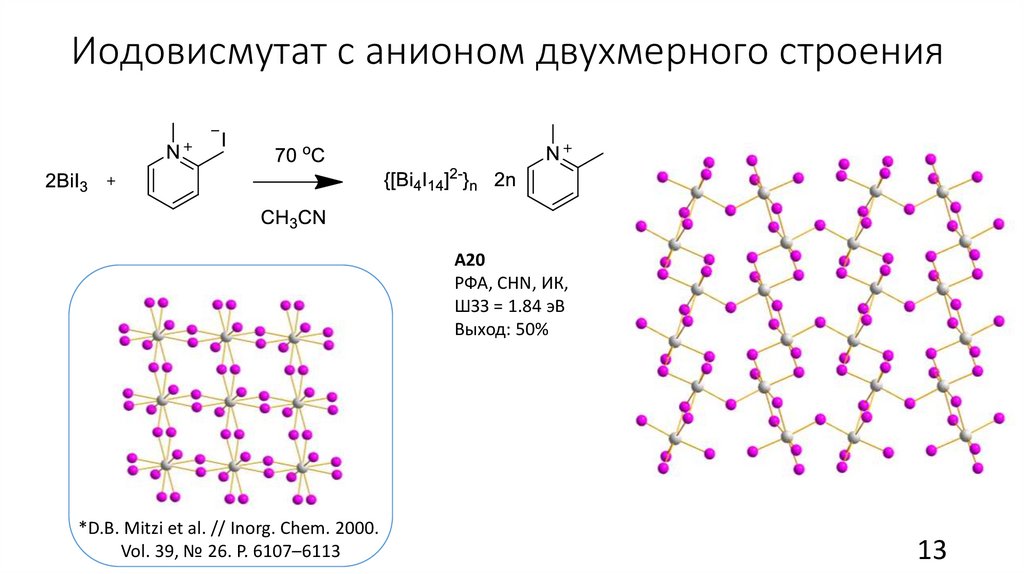
Иодовисмутат с анионом двухмерного строенияА20
РФА, CHN, ИК,
ШЗЗ = 1.84 эВ
Выход: 50%
*D.B. Mitzi et al. // Inorg. Chem. 2000.
Vol. 39, № 26. P. 6107–6113
13
14.
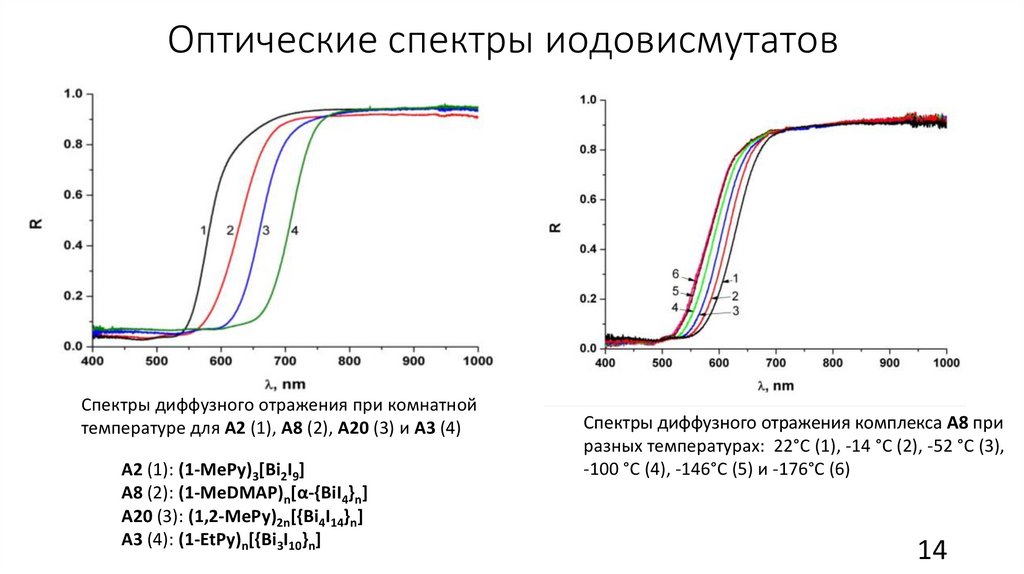
Оптические спектры иодовисмутатовСпектры диффузного отражения при комнатной
температуре для A2 (1), A8 (2), A20 (3) и A3 (4)
A2 (1): (1-MePy)3[Bi2I9]
A8 (2): (1-MeDMAP)n[α-{BiI4}n]
A20 (3): (1,2-MePy)2n[{Bi4I14}n]
A3 (4): (1-EtPy)n[{Bi3I10}n]
Спектры диффузного отражения комплекса A8 при
разных температурах: 22°C (1), -14 °C (2), -52 °C (3),
-100 °C (4), -146°C (5) и -176°C (6)
14
15.
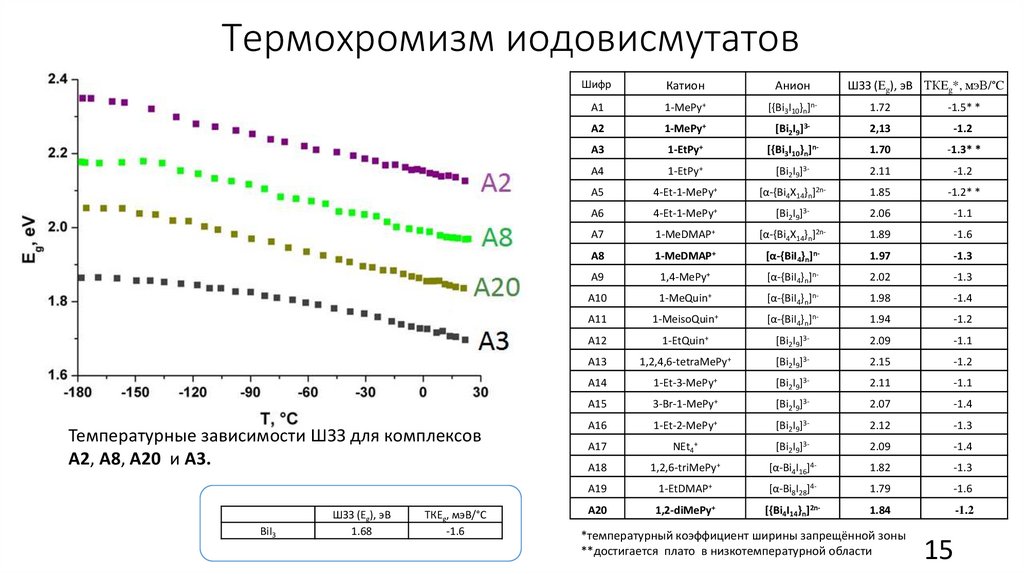
Термохромизм иодовисмутатовТемпературные зависимости ШЗЗ для комплексов
А2, А8, А20 и А3.
BiI3
ШЗЗ (Eg), эВ
1.68
ТКEg, мэВ/°C
-1.6
ШЗЗ (Eg), эВ ТКEg*, мэВ/°C
Шифр
Катион
Анион
A1
1-MePy+
[{Bi3I10}n]n-
1.72
-1.5* *
A2
1-MePy+
[Bi2I9]3-
2,13
-1.2
A3
1-EtPy+
[{Bi3I10}n]n-
1.70
-1.3* *
A4
1-EtPy+
[Bi2I9]3-
2.11
-1.2
A5
4-Et-1-MePy+
[α-{Bi4X14}n]2n-
1.85
-1.2* *
A6
4-Et-1-MePy+
[Bi2I9]3-
2.06
-1.1
A7
1-MeDMAP+
[α-{Bi4X14}n]2n-
1.89
-1.6
A8
1-MeDMAP+
[α-{BiI4}n]n-
1.97
-1.3
A9
1,4-MePy+
[α-{BiI4}n]n-
2.02
-1.3
A10
1-MeQuin+
[α-{BiI4}n]n-
1.98
-1.4
A11
1-MeisoQuin+
[α-{BiI4}n]n-
1.94
-1.2
A12
1-EtQuin+
[Bi2I9]3-
2.09
-1.1
A13
1,2,4,6-tetraMePy+
[Bi2I9]3-
2.15
-1.2
A14
1-Et-3-MePy+
[Bi2I9]3-
2.11
-1.1
A15
3-Br-1-MePy+
[Bi2I9]3-
2.07
-1.4
A16
1-Et-2-MePy+
[Bi2I9]3-
2.12
-1.3
A17
NEt4+
[Bi2I9]3-
2.09
-1.4
A18
1,2,6-triMePy+
[α-Bi4I16]4-
1.82
-1.3
A19
1-EtDMAP+
[α-Bi8I28]4-
1.79
-1.6
A20
1,2-diMePy+
[{Bi4I14}n]2n-
1.84
-1.2
*температурный коэффициент ширины запрещённой зоны
**достигается плато в низкотемпературной области
15
16.
2. Галогенидные и полигалогенидныекомплексы теллура: Синтез, структурная
характеризация, термические стабильность и
оптические свойства
16
17.
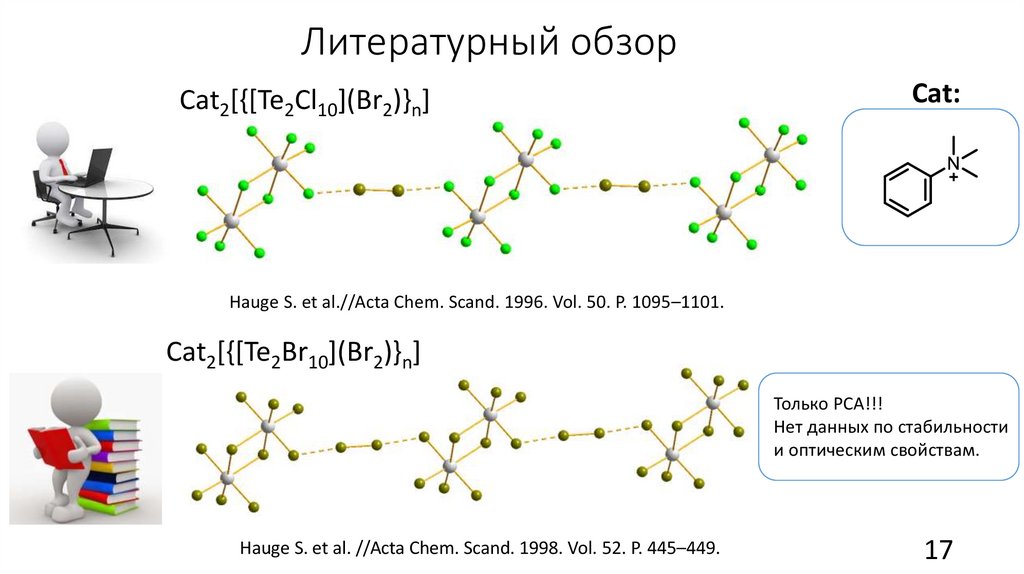
Литературный обзорCat2[{[Te2Cl10](Br2)}n]
Cat:
Hauge S. et al.//Acta Chem. Scand. 1996. Vol. 50. P. 1095–1101.
Cat2[{[Te2Br10](Br2)}n]
Только РСА!!!
Нет данных по стабильности
и оптическим свойствам.
Hauge S. et al. //Acta Chem. Scand. 1998. Vol. 52. P. 445–449.
17
18.
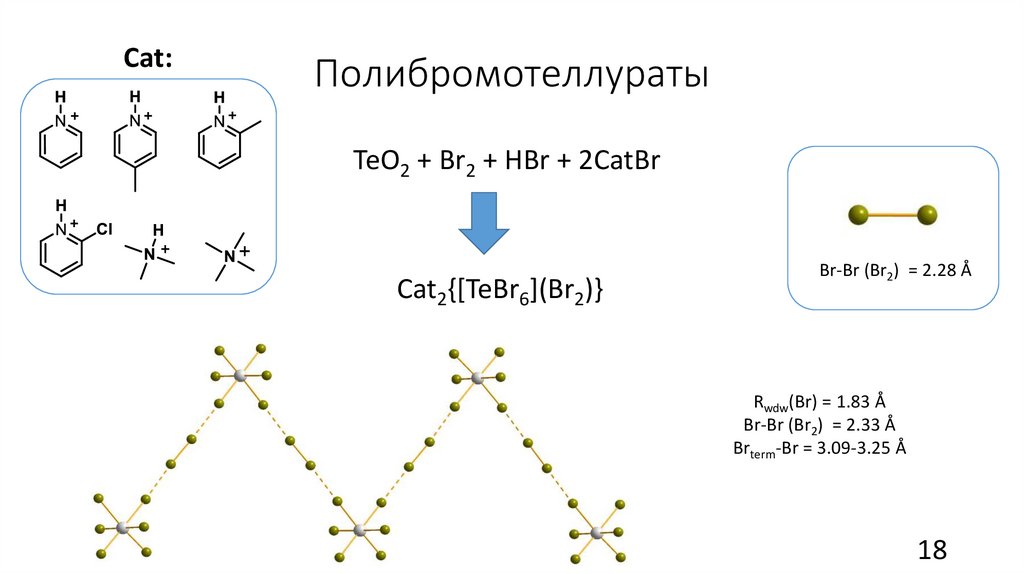
Cat:Полибромотеллураты
TeO2 + Br2 + HBr + 2CatBr
Cat2{[TeBr6](Br2)}
Br-Br (Br2) = 2.28 Å
Rwdw(Br) = 1.83 Å
Br-Br (Br2) = 2.33 Å
Brterm-Br = 3.09-3.25 Å
18
19.
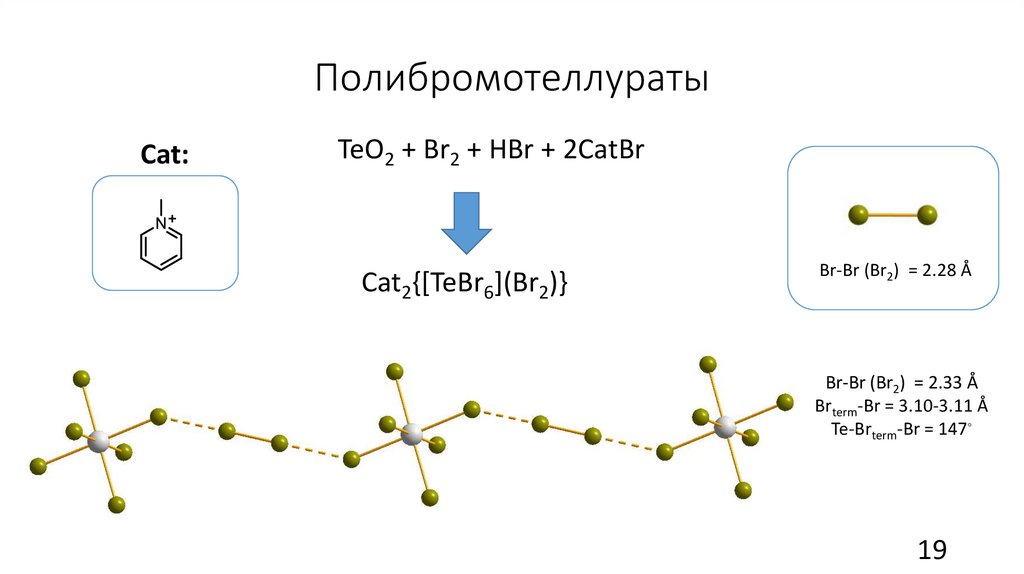
ПолибромотеллуратыCat:
TeO2 + Br2 + HBr + 2CаtBr
Cat2{[TeBr6](Br2)}
Br-Br (Br2) = 2.28 Å
Br-Br (Br2) = 2.33 Å
Brterm-Br = 3.10-3.11 Å
Te-Brterm-Br = 147◦
19
20.
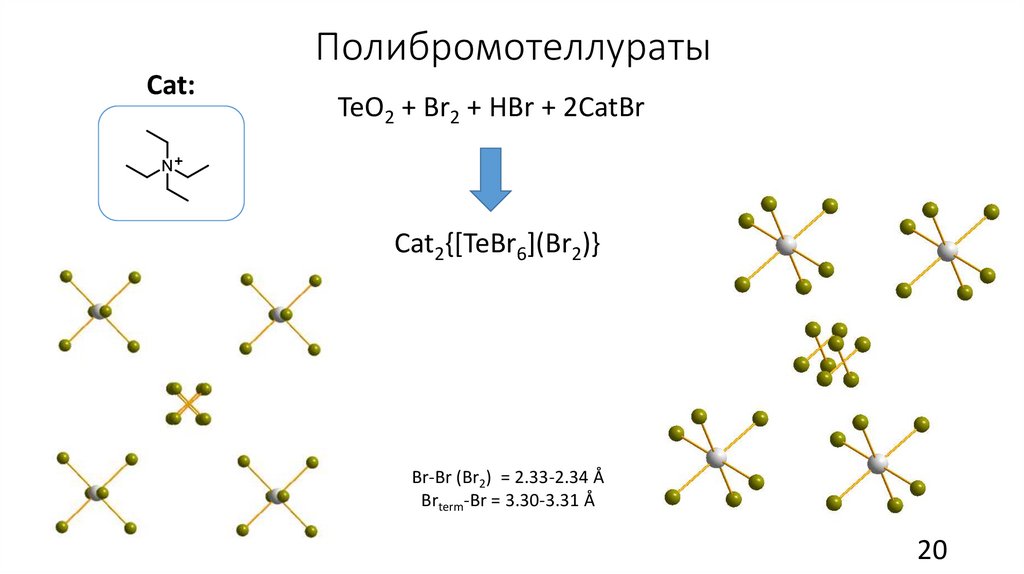
ПолибромотеллуратыCat:
TeO2 + Br2 + HBr + 2CatBr
Cat2{[TeBr6](Br2)}
Br-Br (Br2) = 2.33-2.34 Å
Brterm-Br = 3.30-3.31 Å
20
21.
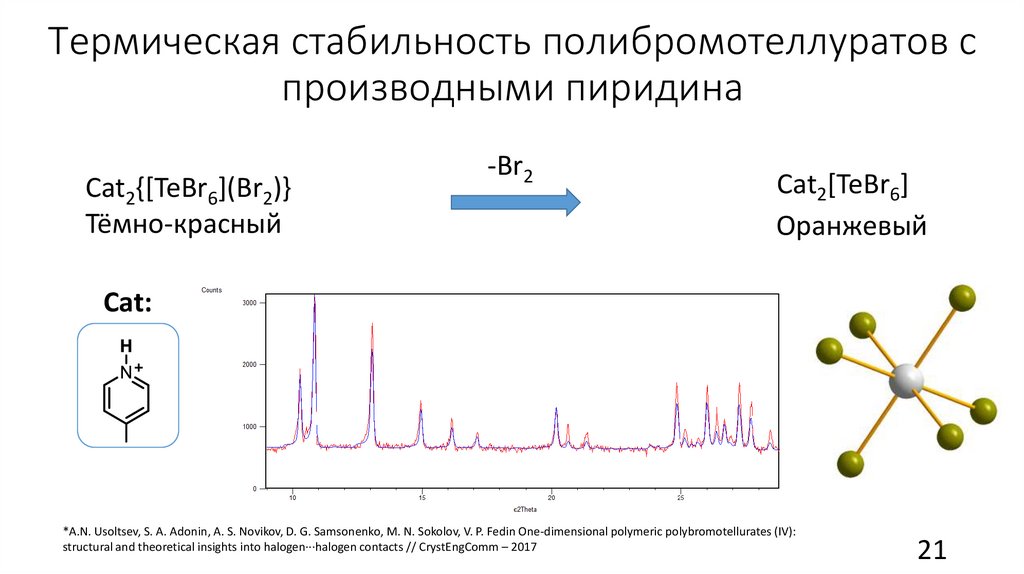
Термическая стабильность полибромотеллуратов спроизводными пиридина
Cat2{[TeBr6](Br2)}
Тёмно-красный
-Br2
Cat2[TeBr6]
Оранжевый
Cat:
*A.N. Usoltsev, S. A. Adonin, A. S. Novikov, D. G. Samsonenko, M. N. Sokolov, V. P. Fedin One-dimensional polymeric polybromotellurates (IV):
structural and theoretical insights into halogen···halogen contacts // CrystEngComm – 2017
21
22.
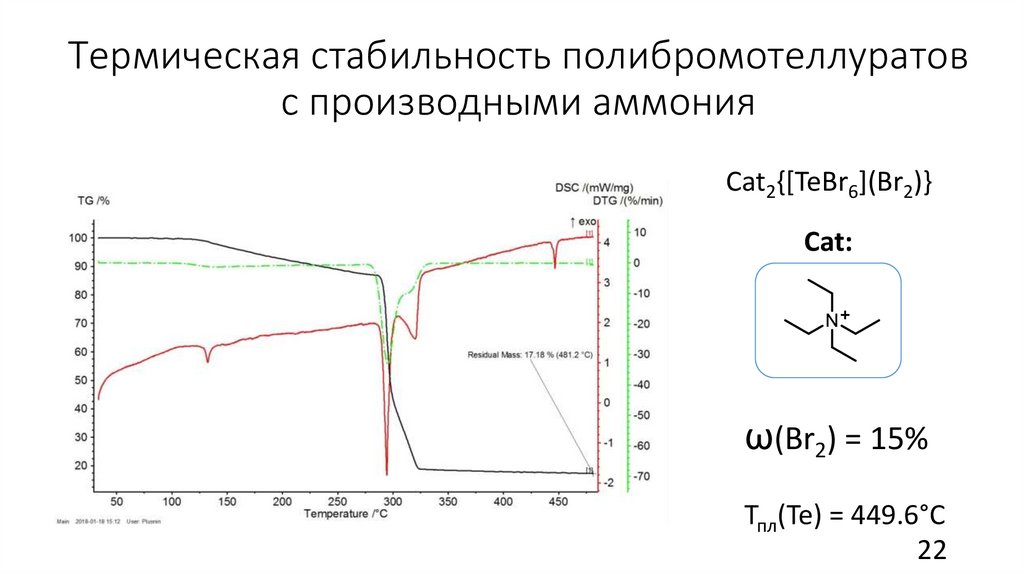
Термическая стабильность полибромотеллуратовс производными аммония
Cat2{[TeBr6](Br2)}
Cat:
ω(Br2) = 15%
Тпл(Te) = 449.6°C
22
23.
Характеризация веществ состава: Сat2{[TeBr6](Br2)}Шифр
B1
B2
B3
B4
B5
B6
B7
B8
Сat\Катион ШЗЗ (эВ) Начало потери
массы (°C)
PyH+
4-MePyH+
N(Me)4+
1,92
200
N(Et)4+
1,86
130
1-MePy+
2-MePyH+
HN(Me)3+
1,95
110
2-ClPyH+
-
Выход
(%)
48
43
42
-
23
24.
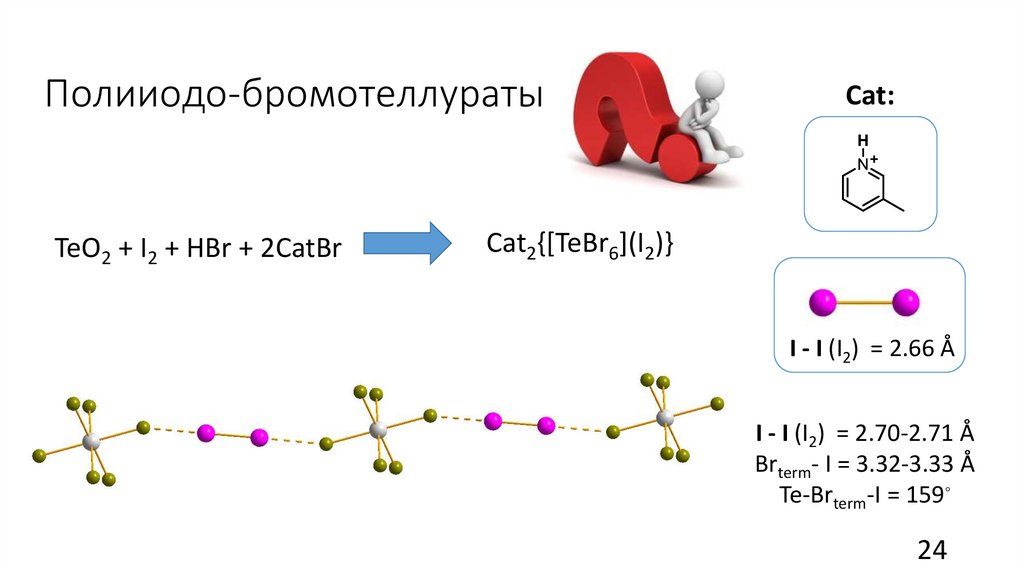
Полииодо-бромотеллуратыTeO2 + I2 + HBr + 2СatBr
Cat:
Сat2{[TeBr6](I2)}
I - I (I2) = 2.66 Å
I - I (I2) = 2.70-2.71 Å
Brterm- I = 3.32-3.33 Å
Te-Brterm-I = 159◦
24
25.
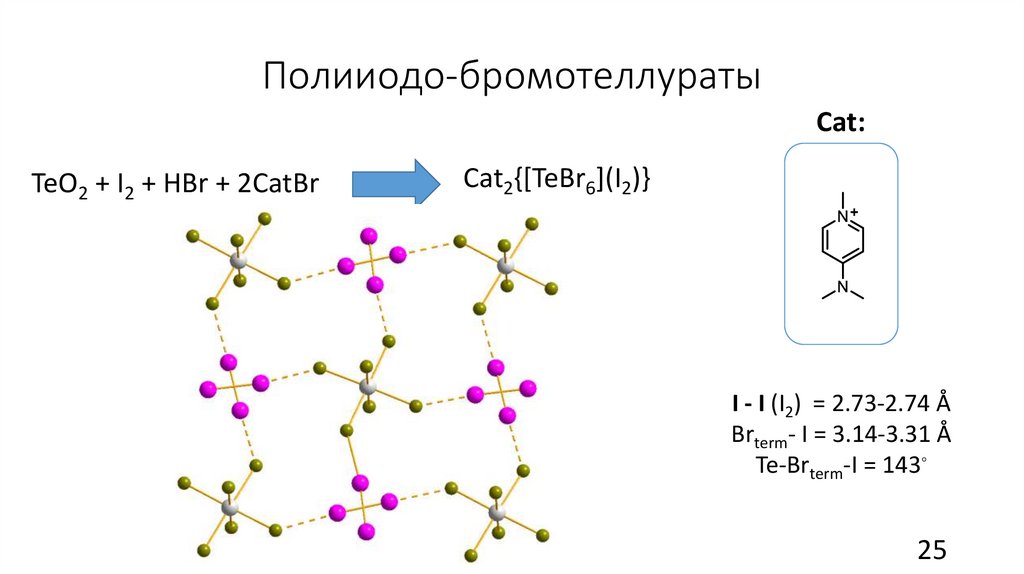
Полииодо-бромотеллуратыCat:
TeO2 + I2 + HBr + 2CatBr
Cat2{[TeBr6](I2)}
I - I (I2) = 2.73-2.74 Å
Brterm- I = 3.14-3.31 Å
Te-Brterm-I = 143◦
25
26.
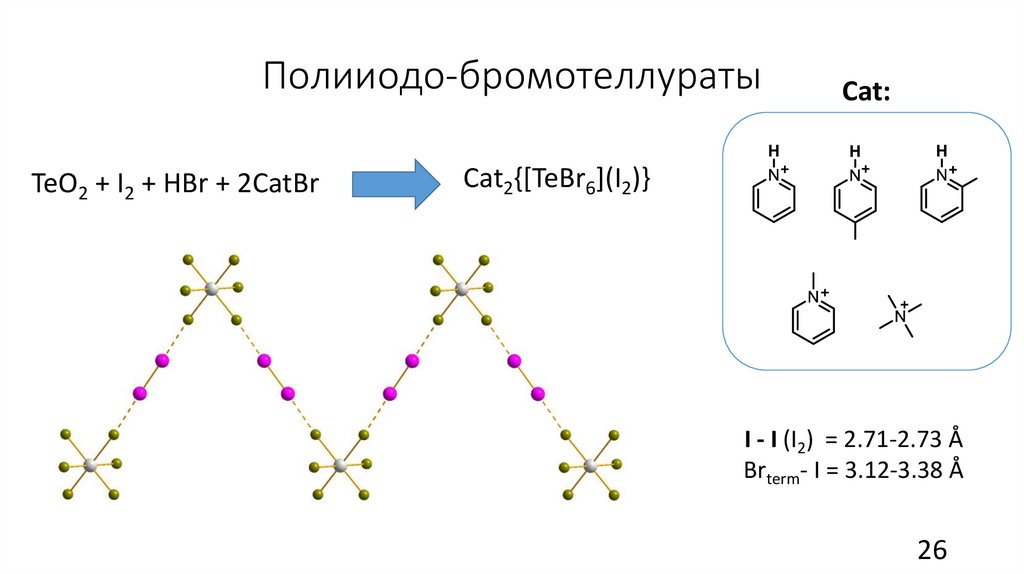
Полииодо-бромотеллуратыTeO2 + I2 + HBr + 2СatBr
Cat:
Сat2{[TeBr6](I2)}
I - I (I2) = 2.71-2.73 Å
Brterm- I = 3.12-3.38 Å
26
27.
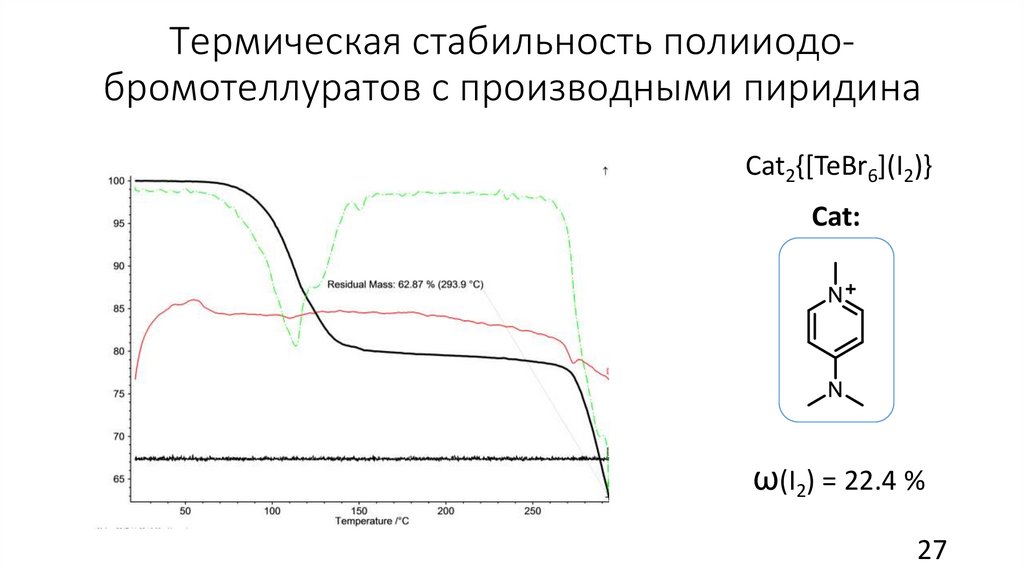
Термическая стабильность полииодобромотеллуратов с производными пиридинаСat2{[TeBr6](I2)}
Cat:
ω(I2) = 22.4 %
27
28.
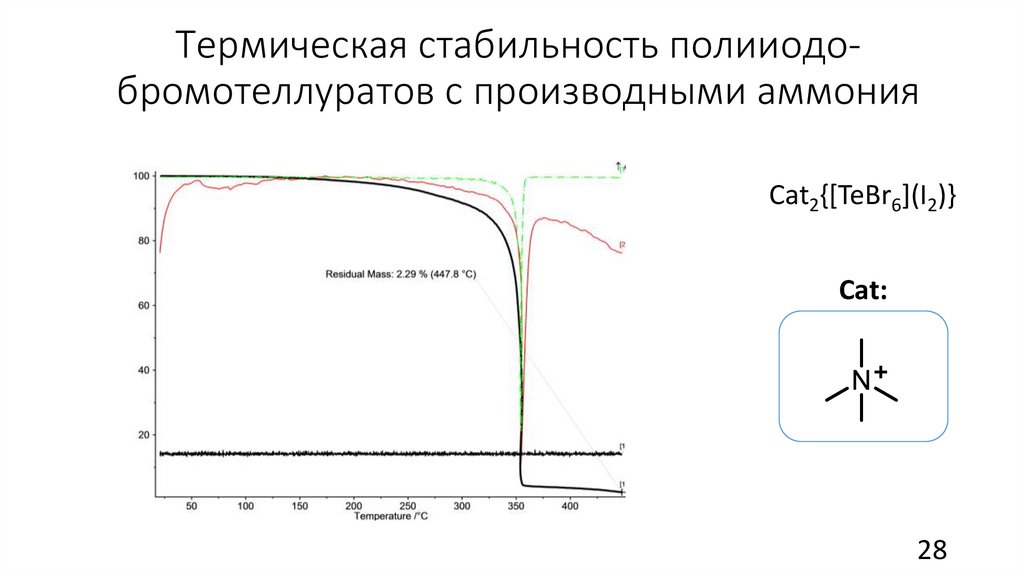
Термическая стабильность полииодобромотеллуратов с производными аммонияСat2{[TeBr6](I2)}
Cat:
28
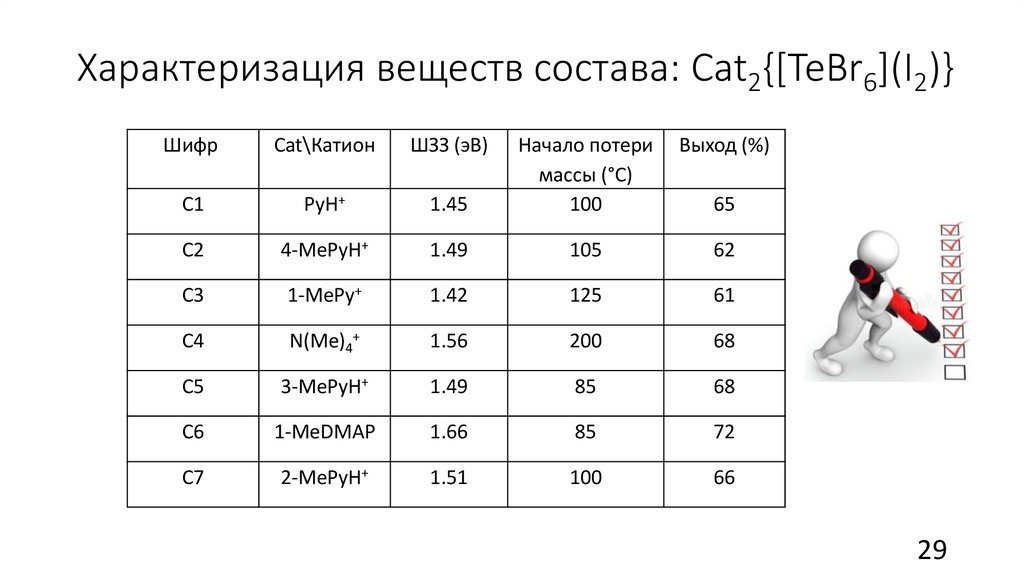
29.
Характеризация веществ состава: Сat2{[TeBr6](I2)}Шифр
Cat\Катион
ШЗЗ (эВ)
Выход (%)
1.45
Начало потери
массы (°C)
100
C1
PyH+
C2
4-MePyH+
1.49
105
62
C3
1-MePy+
1.42
125
61
C4
N(Me)4+
1.56
200
68
C5
3-MePyH+
1.49
85
68
C6
1-MeDMAP
1.66
85
72
C7
2-MePyH+
1.51
100
66
65
29
30.
Бромидные комплексы теллураTeO2 + X2 + HBr + 2CatBr
Cat2[TeBr6]
E1-E16
Cat2{[TeBr6](X2)}
Шифр
Е1
Е2
Е3
Е4
Е5
Е6
Е7
Е8
Е9
Е10
Е11
Е12
Е13
Е14
Е15
Е16
Сat
2-MePyH
3-MePyH+
4-MePyH+
1-EtPy+
2-IPyH+
3-ClPyH+
3-BrPyH+
3-IPyH+
2-Br-5-MePyH+
3,5-diClPyH+
1,2-diMePy+
1,3-diMePy+
1,4-diMePy+
2,6-diMePyH+
2,4,6-triMePyH+
2-ClPyH+
Te-Br, Å
2.694-2.714
2.621-2.775
2.691-2.712
2.696-2.701
2.703-2.707
2.690-2.705
2.648-2.737
2.652-2.741
2.677-2.697
2.687-2.697
2.692-2.702
2.696-2.729
2.695-2.709
2.685-2.703
2.651-2.737
2.692-2.702
Выход (%)
76
79
77
78
74
73
77
68
69
63
81
84
79
75
75
71
30
31.
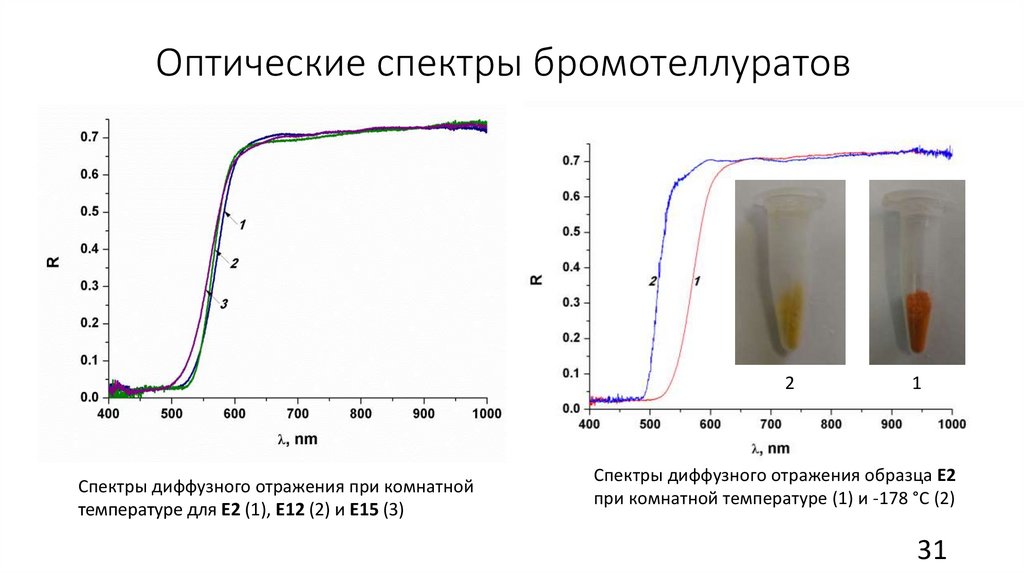
Оптические спектры бромотеллуратов2
Спектры диффузного отражения при комнатной
температуре для Е2 (1), Е12 (2) и Е15 (3)
1
Спектры диффузного отражения образца Е2
при комнатной температуре (1) и -178 °C (2)
31
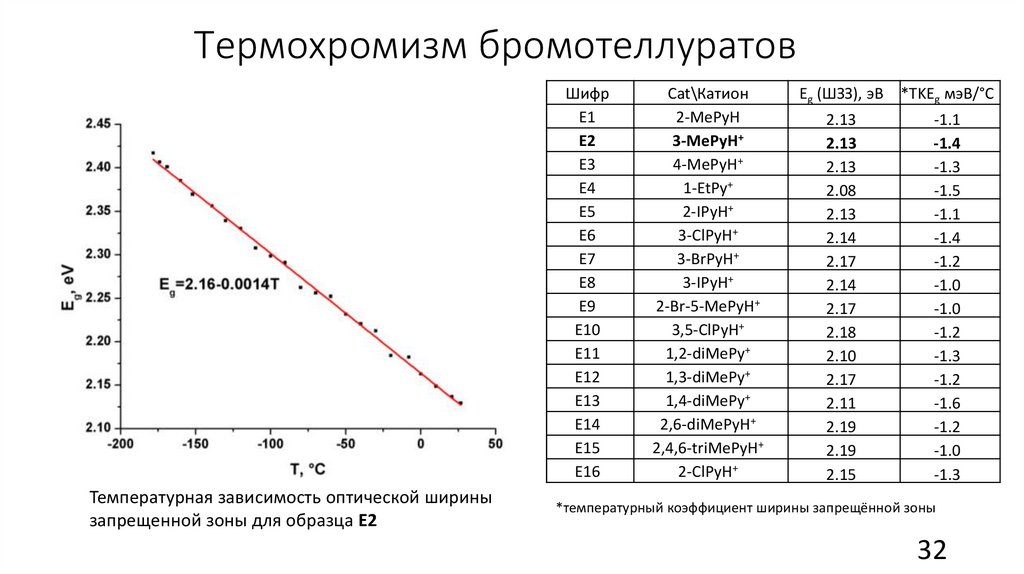
32.
Термохромизм бромотеллуратовШифр
Е1
Е2
Е3
Е4
Е5
Е6
Е7
Е8
Е9
Е10
Е11
Е12
Е13
Е14
Е15
Е16
Температурная зависимость оптической ширины
запрещенной зоны для образца Е2
Сat\Катион
2-MePyH
3-MePyH+
4-MePyH+
1-EtPy+
2-IPyH+
3-ClPyH+
3-BrPyH+
3-IPyH+
2-Br-5-MePyH+
3,5-ClPyH+
1,2-diMePy+
1,3-diMePy+
1,4-diMePy+
2,6-diMePyH+
2,4,6-triMePyH+
2-ClPyH+
Eg (ШЗЗ), эВ
*TKEg мэВ/°C
2.13
2.13
2.13
2.08
2.13
2.14
2.17
2.14
2.17
2.18
2.10
2.17
2.11
2.19
2.19
2.15
-1.1
-1.4
-1.3
-1.5
-1.1
-1.4
-1.2
-1.0
-1.0
-1.2
-1.3
-1.2
-1.6
-1.2
-1.0
-1.3
*температурный коэффициент ширины запрещённой зоны
32
33.
Выводы:1) Разработаны методы синтеза серии новых иодовисмутатных комплексов с
анионами различного строения, в том числе соединений, содержащих два ранее
неизвестных структурных типа – одномерный полимер [β-{Bi3I10}n]n- и двухмерный
полимер [{Bi4I14}n]2n-. Показано, что при получении иодовисмутатов(III) в органических
растворителях на состав продуктов оказывает влияние как строение органического
противоиона, так и соотношение реагентов. Показано, что при соотношении CatI/BiI3
равному 3:2, как правило, образуются комплексы состава Cat3[Bi2I9].
2) Синтезировано 8 полибромид-бромотеллуратных комплексов Cat2{[TeBr6](Br2)},
принадлежащих к 3 различным структурным типам. Комплексы, содержащие катионы
– производные пиридиния, менее стабильны по сравнению с алкиламмонийными
катионами.
33
34.
Выводы:3) Получено 7 полииодид-бромотеллуратных комплексов состава Сat2{[TeBr6](I2)}.
Показано, что термическая стабильность полигалогенидных комплексов теллура при
замене мостикового фрагмента {Br2} на {I2} увеличивается, а ШЗЗ уменьшается.
4) Было показано, что природа катиона в общем случае не оказывает влияния на
термохромные свойства иодовисмутатов(III) и бромотеллуратов(IV). Ключевым
фактором, определяющим оптические свойства, является отношение Bi/I или Te/Br,
соответственно.
34
35.
Основное содержание диссертации изложено в следующих работах:1) Usoltsev A.N., Adonin S.A., Novikov A.S., Samsonenko D.G., Sokolov M.N., Fedin V.P. One-dimensional
polymeric polybromotellurates(IV): Structural and theoretical insights into halogen⋯halogen contacts //
CrystEngComm. 2017. V. 19. N 39. P. 5934-5939.
2) Usoltsev A.N., Adonin S.A., Abramov P.A., Novikov A.S., Shayapov V.R., Plyusnin P.E., Korolkov I. V., Sokolov
M.N., Fedin V.P. 1D and 2D Polybromotellurates(IV): Structural Studies and Thermal Stability // Eur. J. Inorg.
Chem. 2018. V. 2018. N 27. P. 3264-3269.
3) Usoltsev A.N., Adonin S.A., .Plyusnin P.E., Abramov P.A., Korolkov I.V., Sokolov M.N., Fedin V.P. Mononuclear
bromotellurates(IV) with pyridinium-type cations: structures and thermal stability // Polyhedron. 2018. V. 151.
N 4. P. 498-502.
4) Usoltsev A.N., Elshobaki M., Adonin S.A., Frolova L.A., Derzhavskaya T., Abramov P.A., Anokhin D. V.,
Korolkov I. V., Luchkin S.Y., Dremova N.N., Stevenson K.J., Sokolov M.N., Fedin V.P., Troshin P.A. Polymeric
iodobismuthates {[Bi3I10]} and {[BiI4]} with N-heterocyclic cations: promising perovskite-like photoactive
materials for electronic devices // J. Mater. Chem. A. 2019. V. 7. N 11. P. 5957-5966
5) Shayapov V.R., Usoltsev A.N., Adonin S.A.,. Sokolov M.N., Samsonenko D.G., Fedin V.P. Thermochromism of
bromotellurates (IV): experimental insights // New J. Chem. 2019. V. 43. N 9. P. 3927-3930.
В 5 тезисах докладов на российских и международных конференциях.
35
36.
Благодарность!Работа была выполнена при поддержке Российского Научного Фонда
(грант № 14-23-00013 и № 18-73-10040)
36
37.
Благодарность!Адонину С.А. (Науч. Рук.)
Соколову М.Н. (Зав. Лаб.)
Абрамову П.А. (РСА)
Самсоненко Д.Г. (РСА)
Плюснину П.Е. (ТГ)
Королькову И.В. (РФА)
Шаяпову В.Р. (ШЗЗ)
Колесову Б.А. (КР)
Алферовой Н.И. (ИК)
Ведущей организации:
ФГБУН Институту элементоорганических
соединений им. А.Н. Несмеянова РАН
Доктору химических наук,
Перекалину Дмитрию Сергеевичу
Официальным оппонентам:
кандидату химических наук,
научному сотруднику
Николаевскому Станиславу Александровичу
доктору химических наук, профессору,
заведующему кафедрой неорганической
химии МГУ
Шевелькову Андрею Владимировичу
37
38.
ФГБУН Институт элементоорганических соединений им. А.Н. Несмеянова РАНДоктор химических наук, Перекалин Дмитрий Сергеевич
1) Одной из важных целей работы является накопление объема структурных данных для установления корреляций
между строением органического катиона и структурой образующихся галогенид- или полигалогенидных комплексов.
Однако, было бы полезно и интересно проанализировать, насколько возможны такого рода корреляции в принципе,
учитывая, что кристаллическая упаковка в данном случае определяется большим количеством слабых
взаимодействий. Известны ли какие-либо подобные корреляции для других родственных классов соединений,
например, для органических полигалогенидов или, в более общем виде, солей органических катионов со сложными
неорганическими анионами?
2) Насколько надежно воспроизводятся полученные кристаллические фазы? При каких отклонений от соотношения
исходных реагентов начинает образовываться другая кристаллическая фаза или смесь фаз? Если полученные
кристаллы растворить и подвергнуть повторной кристаллизации – будет получена та же фаза или другая?
3) В большинстве случаев соединения в работе получают кристаллизацией из раствора и выход продуктов
колеблется в рамках 50–80%. Если продолжить кристаллизацию (постепенным упариванием маточного раствора или
добавлением осаждающего растворителя) можно ли увеличить выход до практически количественного или с какогото момента начнет образоваться другая кристаллическая фаза?
38
39.
Кандидат химических наук, научный сотрудник Николаевский Станислав АлександровичФГБУН Институт общей и неорганической химии им. Н.С. Курнакова РАН, г. Москва
1) В заключении литературного обзора на с. 40 диссертационной работы сказано, что для полигалогенидных
комплексов теллура в литературе отсутствуют данные о термической стабильности и оптических свойствах.
Здесь же автор указывает на отсутствие в литературе информации о систематических исследованиях
температурной зависимости оптических свойств галогенидных комплексов как висмута, так и теллура. Однако,
в тексте литературного обзора обсуждаются только структурные данные, а информация об оптических
свойствах рассматриваемых типов галогенометаллатов отсутствует. Таким образом, вывод об отсутствии
опубликованных данных по оптическим свойствам полигалогенидных комплексов теллура и висмута выглядит
не совсем убедительно.
2) Одним из немногих методических недостатков диссертационной работы является отсутствие обобщённых
схем синтеза. Учитывая однотипность методик синтеза в рамках каждого отдельно взятого класса
галогенометаллатов, несколько графических схем могли бы украсить работу и облегчить восприятие её
экспериментальной части.
3) При обосновании выбора растворителя на с. 61 диссертации сказано, что ДМФА и ДМСО не были
использованы, т.к. целью работы являлось получение гомолигандных галогенометаллатов. Тем не менее, в
разделе «Цели и задачи работы» такая конкретизация отсутствует. Чем плохи гетеролигандные
галогенометаллаты?
39
40.
Кандидат химических наук, научный сотрудник Николаевский Станислав АлександровичФГБУН Институт общей и неорганической химии им. Н.С. Курнакова РАН, г. Москва
4) В работе не хватает рассуждений о возможности модификации полученных полигалогенидных соединений
галогенпроизводными углеводородов – донорами галогенной связи. Такая модификация могла бы оказать
заметное влияние на оптические свойства соединений.
5) При исследовании термической стабильности полибромид-бромотеллуратов(IV) (с. 75–78 диссертационной
работы) получены интересные результаты. Экспериментально обнаружена значительная разница значений
температур, при которых от комплексов B4 и B7 отщепляется молекулярный бром. Было бы интересно
попытаться объяснить эту разницу с помощью квантовохимической оценки энергетических параметров
отщепления молекулярного брома от указанных комплексов. Такие DFT расчёты могли бы стать хорошим
дополнением к результатам, полученным в рамках теории Бейдера.
40
41.
Доктор химических наук, профессор, заведующий кафедрой неорганической химии МГУШевельков Андрей Владимирович
ФГБОУ ВО «Московский государственный университет им. М.В. Ломоносова»
1) При описании кристаллических структур и затем при описании химической связи в новых соединениях
совершенно обходится стороной вопрос взаимодействия катиона с анионом, хотя даже из анализа состава
катионов становится понятно, что в некоторых случаях должна играть существенную роль не галогенная, а
водородная связь. Было бы интересно знать, какова энергия водородных связей, насколько она
сопоставима с энергией галогенных связей, исследованных в работе, и как водородная связь влияет (или не
влияет) на порядок относительного расположения катионов и анионов в кристаллической структуре.
2) Некоторые данные в работе приводятся без указания ошибок, например, в таблицах 4 и 9. В частности,
интересно знать, разными или одинаковыми следует принимать ширины запрещенных зон в соединениям
Е5, Е6 и Е7, если они равны соответственно 2.13, 2.14 и 2.17 эВ?
41
42.
Отзывы на автореферат без замечаний поступили от:1) Ассистента института химии Санкт-Петербургский государственный университет,
к.х.н. Иванова Даниила Михайловича
2) Главного научного сотрудника, заведующего лабораторией Металоорганических и координационных
соединений ИОФХ им. А.Е. Арбузова – обособленного структурного подразделения ФИЦ КазНЦ РАН,
д.х.н., профессора РАН Яхфарова Дмитрия Григорьевича
3) Ведущего научного сотрудника лаборатории биоэлементоорганической химии химического факультета
Московского государственного университета имени М.В. Ломоносова
к.х.н. Назарова Алексея Анатольевича
4) Научного сотрудника лаборатории многоспиновых координационных соединений
Института «Международный томографический центр» СО РАН,
к.х.н. Марюниной Ксении Юрьевны
5) Профессора кафедры физической и коллоидной химии ФГБОУ ВО «Иркутский государственный
университет», директора НИИ Нефте-углехимического синтеза ФГБОУ ВО «Иркутский государственный
университет»
д.х.н., доцента Суслова Дмитрия Сергеевича
42
43.
Отзыв на автореферат с замечаниям поступил от:Профессора кафедры физической органической химии Инстутута химии ФГБОУВО
«Санкт-Петербургский государственный унисерситет», доктора химических наук, доцента
Боярского Вадима Павловича
-Лишь для соедининения В4, В5 и В7 указаны препаративные выходы , а для остальных
соединений в том же ряду полибромтеллуратов они отсутствуют ввиду их нестабильности. В
таком случае, неясно, что вкладывается в понятие «были получены». Насколько воспроизводима
методика получения для указанных соединений? Каким образом определялся
стехиометрический и фазовый состав полученных соединений? Что ещё образуется в ходе
реакции? Из-за недостатка данной информации становится сложно оценить практическую
применимость предложенных методов синтеза. Возможно, эта информация присутствует в
работе.
43
44.
Галогенидные комплексы висмута и теллура как компоненты солнечныхбатарей.
С конца 2015 г. наблюдается быстрый рост интереса к
солнечным батареям на основе галогенидов других
постпереходных элементов
Галогенидный комплекс выступает в роли поглотителя света
Новиков Артем
Аспирант
Сколтех
П.А. Трошин
Профессор
Сколтех
44
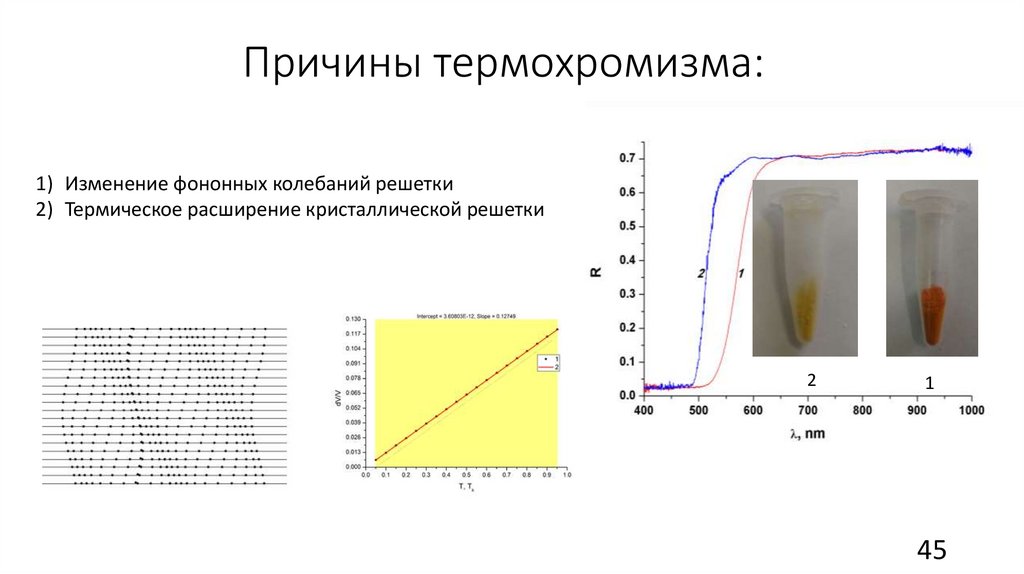
45.
Причины термохромизма:1) Изменение фононных колебаний решетки
2) Термическое расширение кристаллической решетки
2
1
45
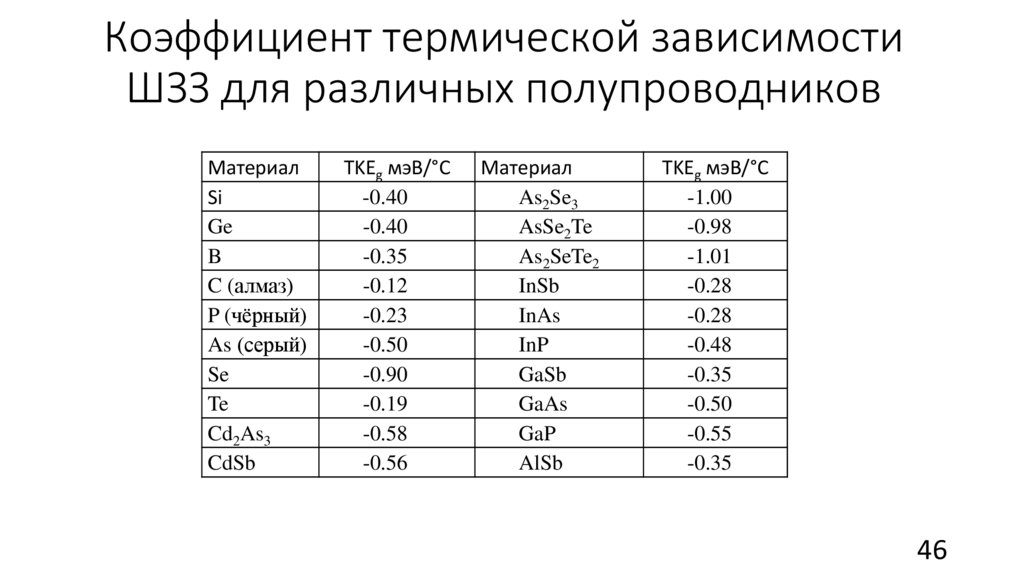
46.
Коэффициент термической зависимостиШЗЗ для различных полупроводников
Материал
Si
Ge
B
C (алмаз)
P (чёрный)
As (серый)
Se
Te
Cd2As3
CdSb
TKEg мэВ/°C
-0.40
-0.40
-0.35
-0.12
-0.23
-0.50
-0.90
-0.19
-0.58
-0.56
Материал
As2Se3
AsSe2Te
As2SeTe2
InSb
InAs
InP
GaSb
GaAs
GaP
AlSb
TKEg мэВ/°C
-1.00
-0.98
-1.01
-0.28
-0.28
-0.48
-0.35
-0.50
-0.55
-0.35
46
47.
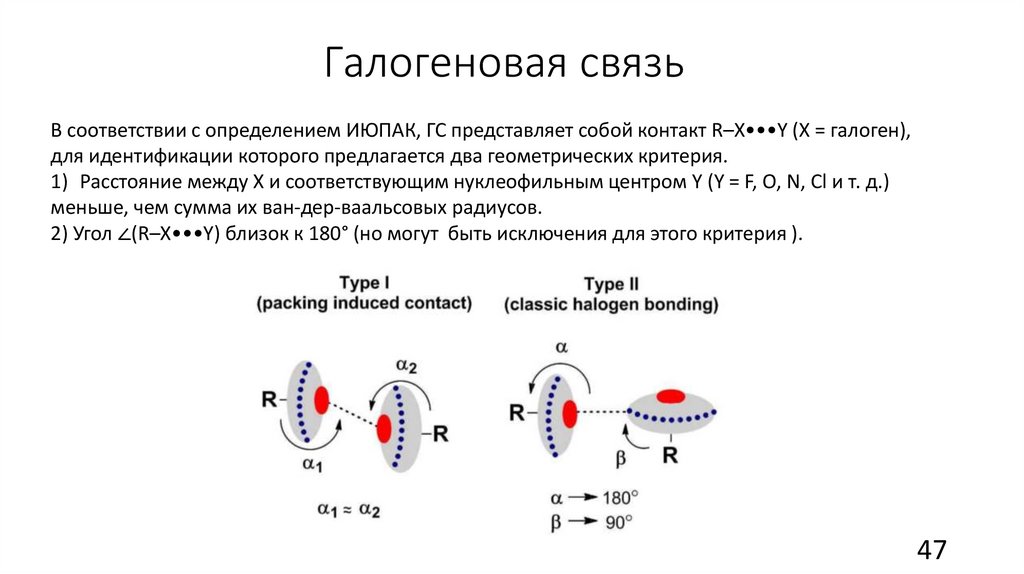
Галогеновая связьВ соответствии с определением ИЮПАК, ГС представляет собой контакт R–X•••Y (X = галоген),
для идентификации которого предлагается два геометрических критерия.
1) Расстояние между X и соответствующим нуклеофильным центром Y (Y = F, O, N, Cl и т. д.)
меньше, чем сумма их ван-дер-ваальсовых радиусов.
2) Угол ∠(R–X•••Y) близок к 180° (но могут быть исключения для этого критерия ).
47
48.
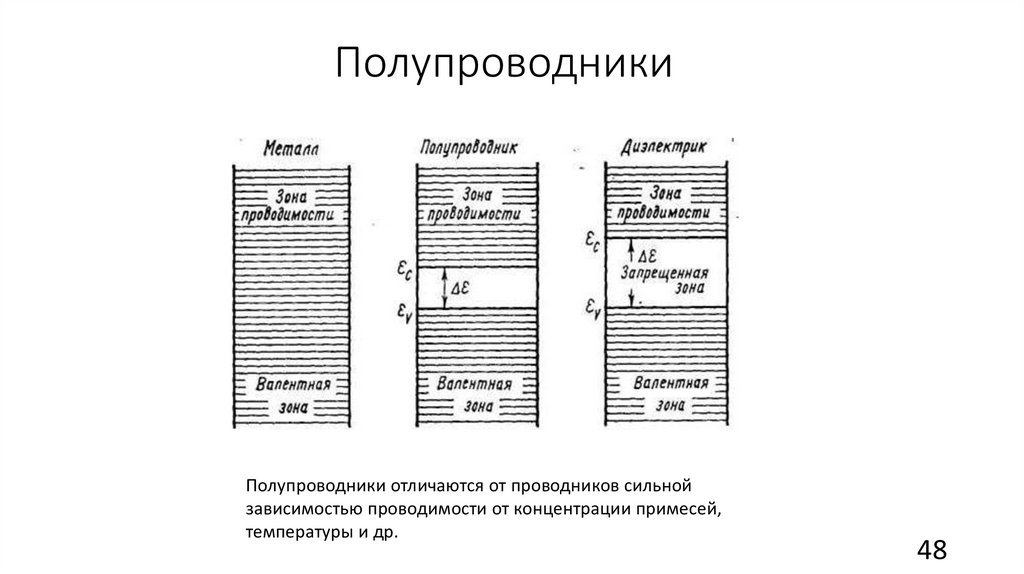
ПолупроводникиПолупроводники отличаются от проводников сильной
зависимостью проводимости от концентрации примесей,
температуры и др.
48
49.
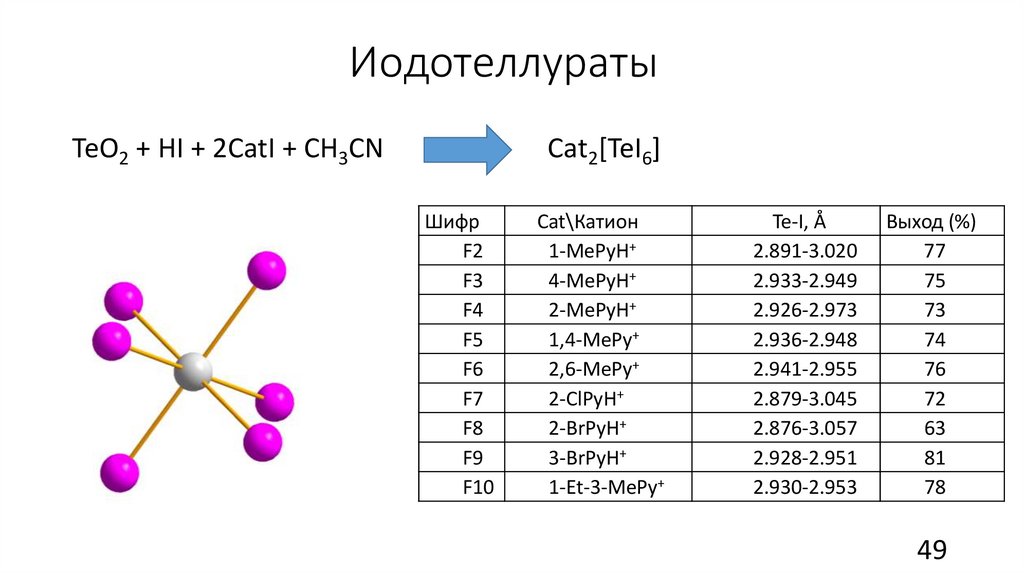
ИодотеллуратыTeО2 + HI + 2CatI + CH3CN
Cat2[TeI6]
Шифр
F2
F3
F4
F5
F6
F7
F8
F9
F10
Сat\Катион
1-MePyH+
4-MePyH+
2-MePyH+
1,4-MePy+
2,6-MePy+
2-ClPyH+
2-BrPyH+
3-BrPyH+
1-Et-3-MePy+
Te-I, Å
2.891-3.020
2.933-2.949
2.926-2.973
2.936-2.948
2.941-2.955
2.879-3.045
2.876-3.057
2.928-2.951
2.930-2.953
Выход (%)
77
75
73
74
76
72
63
81
78
49
50.
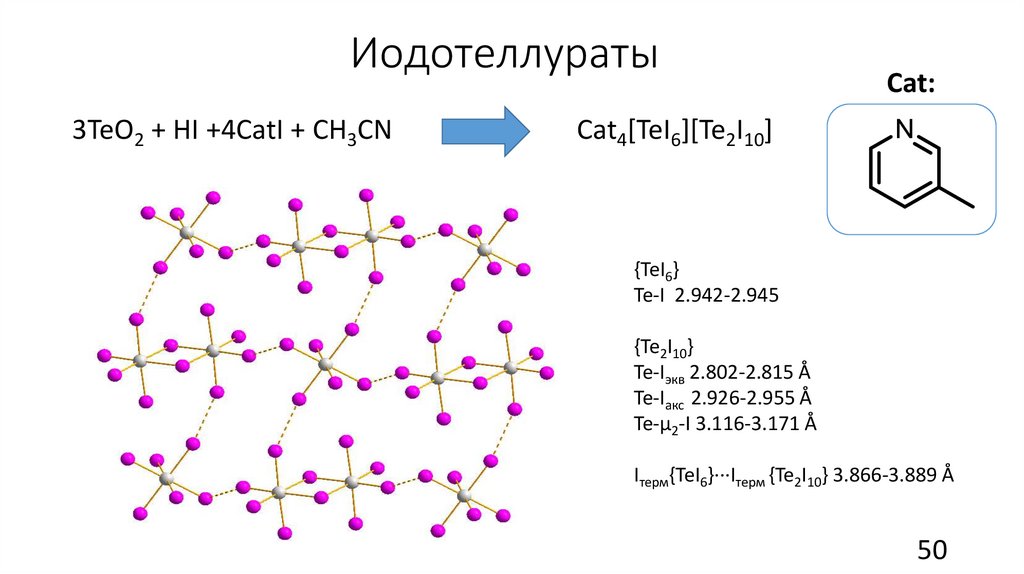
Иодотеллураты3TeО2 + HI +4CatI + CH3CN
Cat:
Cat4[TeI6][Te2I10]
{TeI6}
Te-I 2.942-2.945
{Te2I10}
Te-Iэкв 2.802-2.815 Å
Te-Iакс 2.926-2.955 Å
Te-µ2-I 3.116-3.171 Å
Iтерм{TeI6}···Iтерм {Te2I10} 3.866-3.889 Å
50
51.
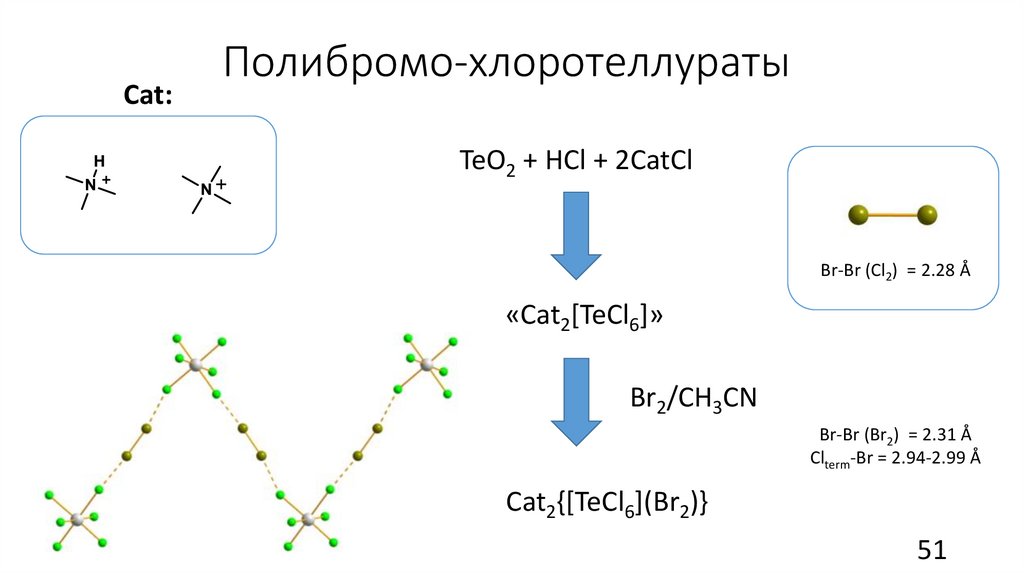
Cat:Полибромо-хлоротеллураты
TeO2 + HCl + 2CatCl
Br-Br (Cl2) = 2.28 Å
«Cat2[TeCl6]»
Br2/CH3CN
Br-Br (Br2) = 2.31 Å
Clterm-Br = 2.94-2.99 Å
Cat2{[TeCl6](Br2)}
51
52.
Фотовольтаические элементы на основе галогенидныхкомплексов висмута
Кристаллическая структура Cs3Bi2I9 была первоначально изучена в 1960-х годах. Почти 50 лет спустя, Парк
и др. впервые включил иодидные комплексы висмута в солнечные элементы, демонстрируя
эффективность преобразования энергии 1,09% для Cs3Bi2I9 и 0,12% для (CH3NH3)3Bi2I9.
Несмотря на свою скромную эффективность, эти материалы
обладали высокими коэффициентами поглощения и были
более устойчивыми к воздуху, чем их свинцовые аналоги.
Примеры галогенидных комплексов висмута с ЩМ:
K4Bi2Br10; (NH4)4Bi2Br10; Na7(BiBr6)(Bi2Br10); Cs2NaBiCl6 ;
(CH3NH2)4BiCl6Cl; Rb5 (BiI6)(I3)I; Cs3Bi2Br9…
* Park B.-W., Philippe B., Zhang X., Rensmo H., Boschloo G., Johansson E.M.J. Bismuth Based Hybrid
Perovskites A3Bi2I9 (A: Methylammonium or Cesium) for Solar Cell Application // Adv. Mater. 2015. N
43. P. 6806–6813.
52
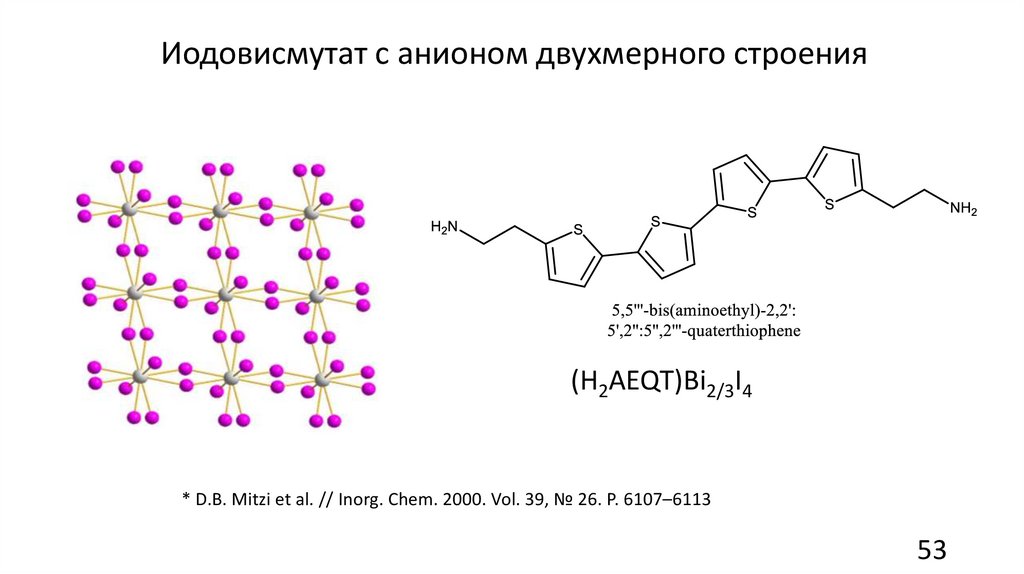
53.
Иодовисмутат с анионом двухмерного строения(H2AEQT)Bi2/3I4
* D.B. Mitzi et al. // Inorg. Chem. 2000. Vol. 39, № 26. P. 6107–6113
53
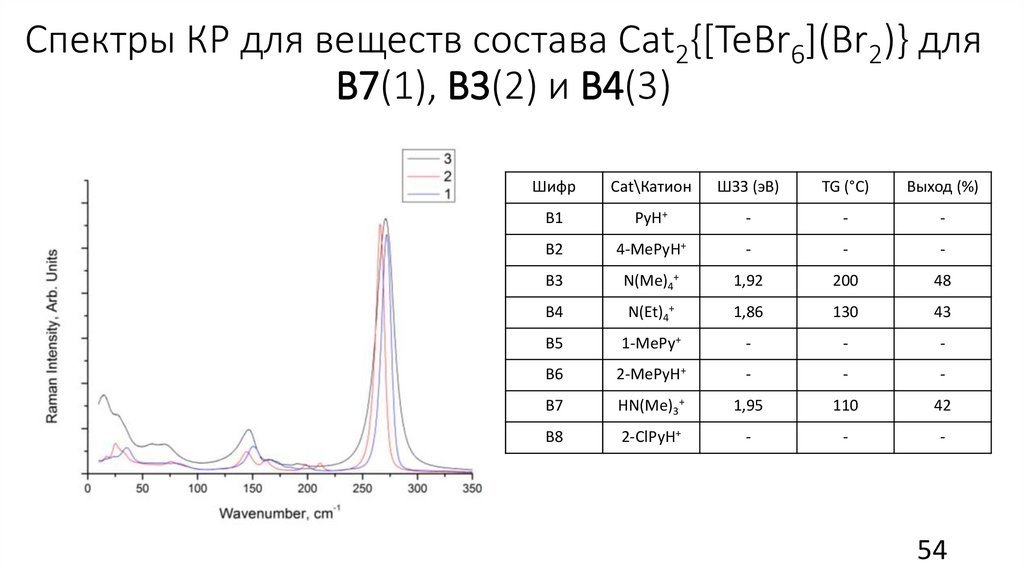
54.
Спектры КР для веществ состава Сat2{[TeBr6](Br2)} дляВ7(1), В3(2) и В4(3)
Шифр
Сat\Катион
ШЗЗ (эВ)
TG (°C)
Выход (%)
B1
PyH+
-
-
-
B2
4-MePyH+
-
-
-
B3
N(Me)4+
1,92
200
48
B4
N(Et)4+
1,86
130
43
B5
1-MePy+
-
-
-
B6
2-MePyH+
-
-
-
B7
HN(Me)3+
1,95
110
42
B8
2-ClPyH+
-
-
-
54
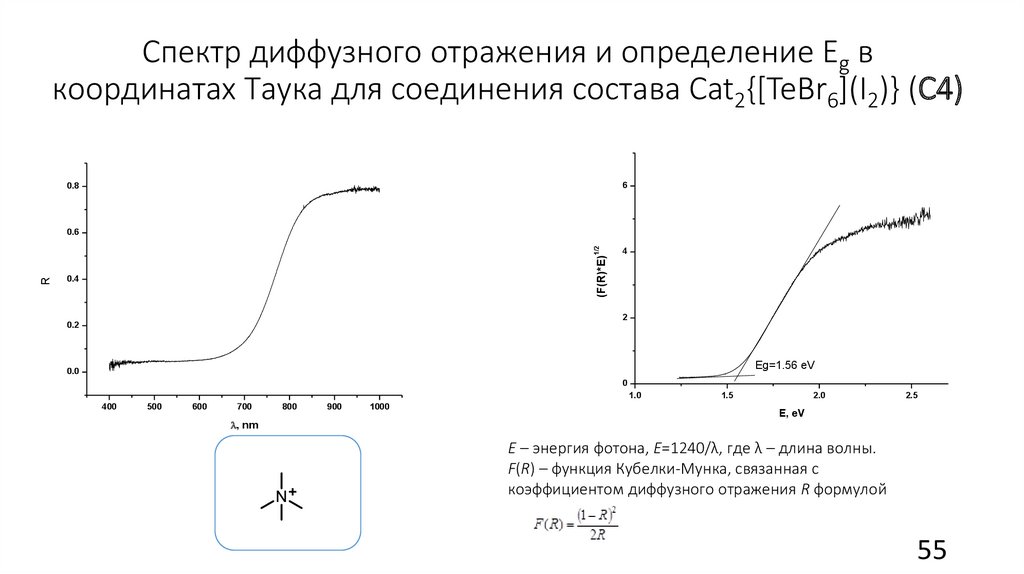
55.
Спектр диффузного отражения и определение Eg вкоординатах Таука для соединения состава Сat2{[TeBr6](I2)} (С4)
6
0.8
(F(R)*E)
R
1/2
0.6
0.4
4
2
0.2
Eg=1.56 eV
0.0
0
1.0
400
500
600
700
, nm
800
900
1000
2.0
1.5
2.5
E, eV
E – энергия фотона, E=1240/λ, где λ – длина волны.
F(R) – функция Кубелки-Мунка, связанная с
коэффициентом диффузного отражения R формулой
55
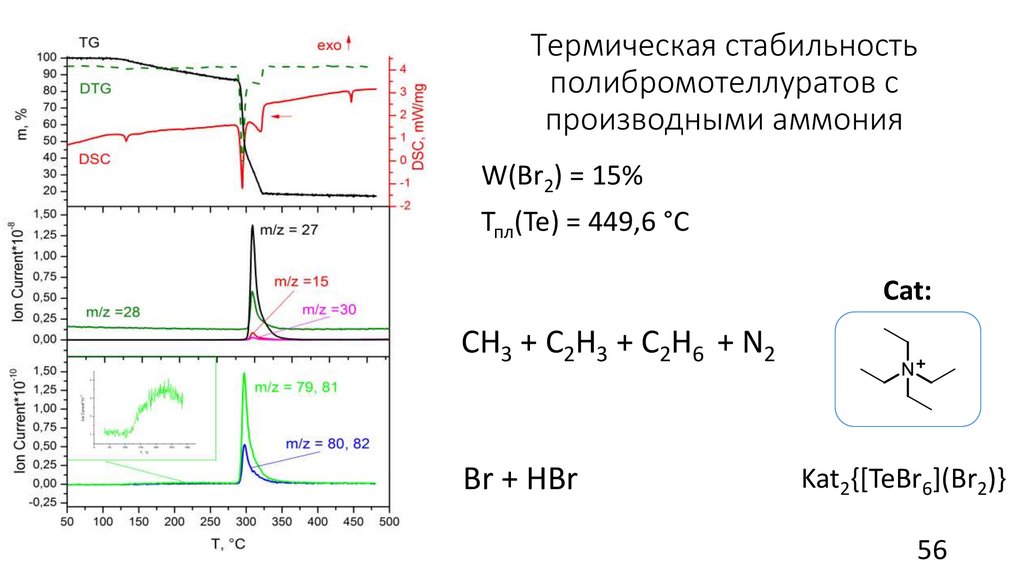
56.
Термическая стабильностьполибромотеллуратов с
производными аммония
W(Br2) = 15%
Тпл(Te) = 449,6 °С
Cat:
CH3 + C2H3 + С2H6 + N2
Br + HBr
Kat2{[TeBr6](Br2)}
56



















 chemistry
chemistry








