Similar presentations:
Белок биосинтезі Көмірсу Нуклеин қышқылы синтезі
1. Белок биосинтезі Көмірсу Нуклеин қышқылы синтезі
Орындаған:Қабылдаған:
2. ЖОСПАР
КіріспеНегізгі бөлім
• Белок биосинтезі
• Көмірсу құрылымы
• Нуклеин қышқылы синтезі
Қорытынды
Пайдаланылған әдебиеттер
3. КІРІСПЕ
• Белок биосинтезі тіршіліктің ең маңызды қасиеттерінің бірі, себебітіршілік процесінде белок молекулалары әртүрлі биохимиялық
реакцияларға түсіп ыдырап жойылып отырады, ал олардың орнын
толтыру тек жаңа белок молекулаларының синтезделуі нәтижесінде
жүзеге асады. Мұнда ДНҚ, РНҚ, АТФ және белоктардың қызметі
бірігеді.
• Көмірсулар (моносахаридтер – қарапайым қанттар,
гидролизденбейді, бұлар глюкоза, фруктоза; дисахаридтер-әр
молекуласы 2 моносахаридтерден тұрады: сахароза, лактоза;
полисахаридтер - өте күрделі заттар: крахмал, клетчатка) табиғатта
өте көп таралған, оның адам өмірінде маңызы өте зор. Организмге
қажет қуаттың (энергия) көбі көмірсулар арқылы жүреді.
• Нуклеин қышқылы - пішіні жіп тәрізді, жоғарғы молекулалы,
ерітінділерінің тұтқырлығы жоғары қосылыс. Нуклеин қышқылдары нуклеотид полимерлерінен құралған. Нуклеотидтердің химиялық
құрамы - пиримидиндік немесе пуриндік негіздер, пентоз, фосфор
қышқылының қалдығы.
4. Клеткадағы зат және энергия алмасулар
• Тірі организмдердің ерекше қасиеті — олар зат алмасуға(метаболизмге) және көптеген әр түрлі химиялық реакцияларға
қатысуға кабілетті болады. Сырткы ортамен үнемі зат алмасып отыру
— тірі жүйелердің негізгі қасиеттерінің бірі. Клеткаларда
биологиялық синтез және ыдырау процестері үздіксіз жүріп отырады.
Синтез процесі жалпы анаболизм (гр. "ана" — тірі дене), ал ыдырау
процесі катаболизм (гр. "ката" — өлі дене) деп аталады.
• Синтез — бұл жай заттардың энергия жұмсау аркылы күрделі заттар
түзу процесі. Мысалы, аминқышқылдарынан белоктар,
моносахаридтерден күрделі көмірсулар, нуклеотидтерден нуклеин
қышқылдары синтезделеді. Синтезделген заттар өсу процесі кезінде
клетка мен оның органоидтерінің түзілуі үшін және жұмсалған немесе
зақымданған молекулаларды қалпына келтіру үшін пайдаланылады.
• Ыдырау процесі кезінде күрделі заттардан жай заттар түзіліп, энергия
бөлініп шығады. Мысалы, қанттар органикалық қышқыл мен спиртке
ыдыраса, органикалық қышкылдар өз кезегінде көмірқышқыл газы
мен суға ыдырайды. Зат алмасудың ерекше белгісі сол, мұнда
анаболизм және катаболизм процестері бірдей уакытта сыртқы
ортамен өзара тура байланыста жүреді.
5.
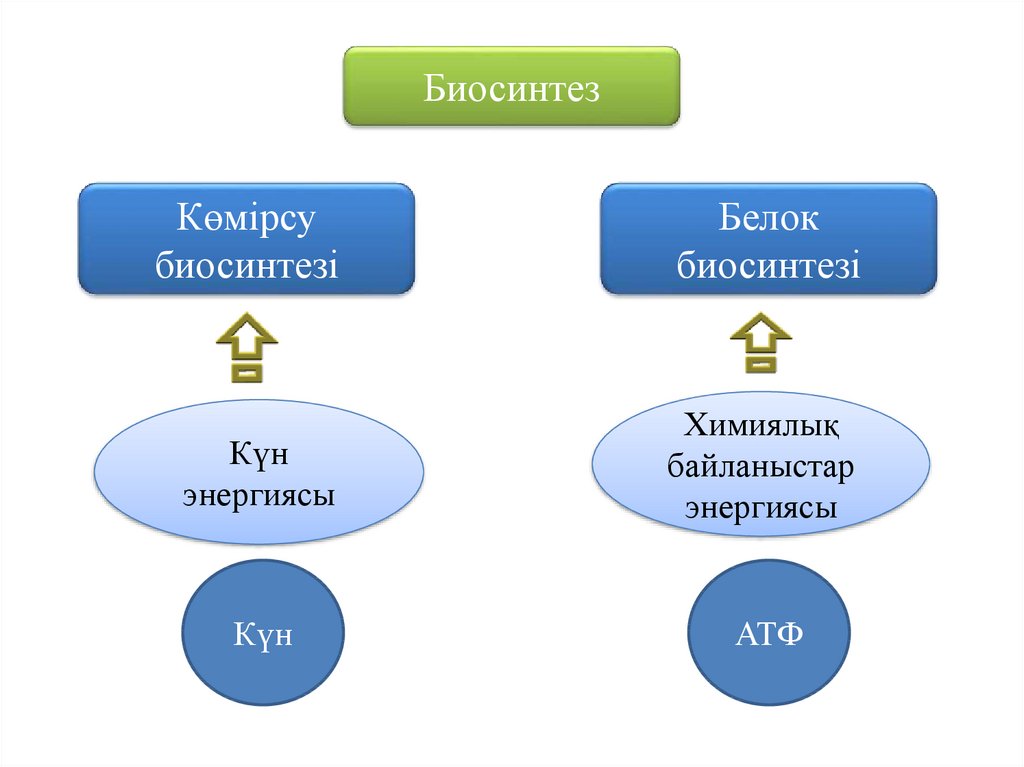
БиосинтезКөмірсу
биосинтезі
Белок
биосинтезі
Күн
энергиясы
Химиялық
байланыстар
энергиясы
Күн
АТФ
6. Негізгі бөлім
НЕГІЗГІ БӨЛІМБелок биосинтезі
Генетикалық код
7.
Я.БеккориБелок туралы алғашқы мәліметтер XVIII
ғасырдан белгілі. 1745 ж. италиялық
ғалым Беккори бидай ұнынан лейковина
деген белокты бөліп шығарған. 19
ғасырдың
30жылдарында ет, жұмыртқа, сүт, өсімдік
тұқымдарында белоктық заттар бар екені
анықталды. Ғалымдарың содан бергі
зерттеулері нәтижесінде барлық тірі
организмдер клеткасында болатын тірі
материя – протоплазма, негізінен,
белоктан құралатыны анықталды. белок
тірі организмнің негізін құрайды, онсыз
өмір жоқ.
Фридрих Энгельс пікірі бойынша:
«Тіршілік — белок заттарының
өмір сүру формасы».
8. Ақуыз құрамы
• Ақыздардың қасиеттерін олардың құрамы мен құрылымыанықтайды.
Ақуыз
молекуласындағы
а-аминқышқылдары
қалдықтарының саны әр түрлі болады, кейде бірнеше мыңға дейін
жетеді. Әр ақуызда а-аминқышқылдары тек осы ақуызға ғана тән
ретімен орналасады. Олардың молекулалық массалары бірнеше
мыңнан миллионға дейін жетеді. Мысалы, жұмыртқа ақуызының
молекулалық массасы 36000, бұлшық ет ақуызының молекулалық
массасы — 150000, адам гемоглобині 67000, ал көптеген ақуыздардікі
> 300000 шамасында. Олар, негізінен, көміртек (50—55%), оттек
(20—24%), азот (15—19%), сутектен (6—7%) тұрады.
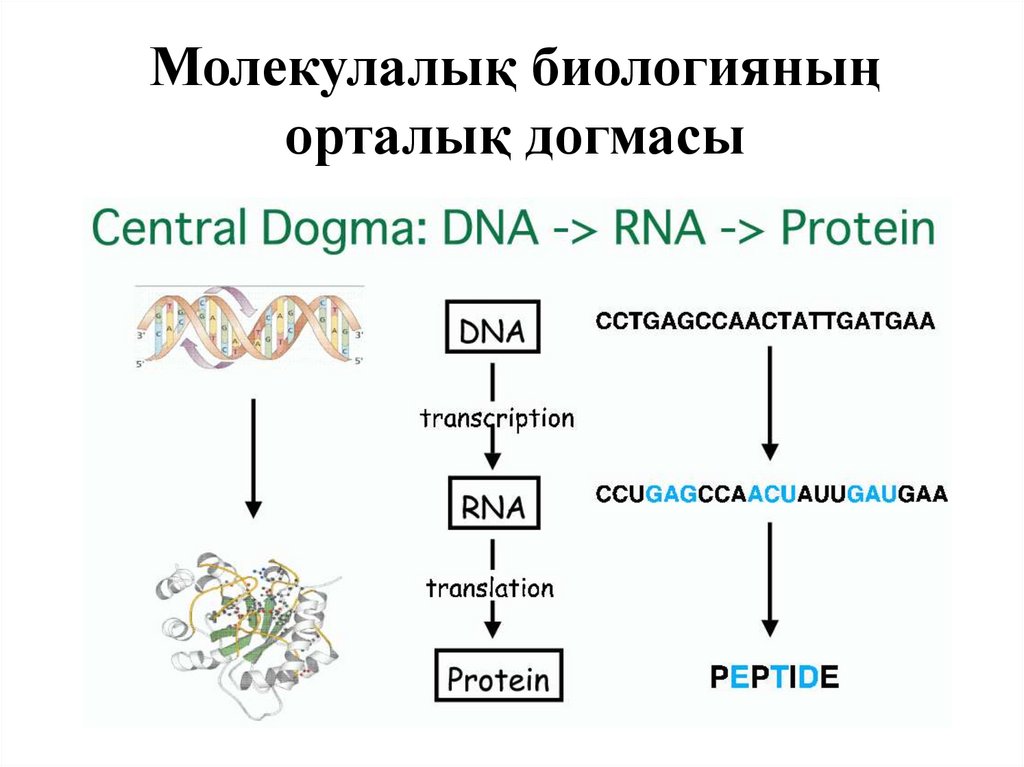
9. Молекулалық биологияның орталық догмасы
10. Клеткадағы рибосомалар локализациясы
11. Рибосома морфологиясы
12. Про- және эукариоттар рибосомалары
Прокариоттық:70S = 30S + 50S
Эукариоттық:
80S = 40S + 60S
13. Рибосома суббірліктері
14.
Белоктардың синтезі рибосомада жүредіБелоктардың синтезі үшін қажет энергия АТФ және ГТФ
арқылы қамтамасыз етіледі, айта кету керек, бір пептидтік
байланыс түзілу үшін 4 макроэргтік қосылыс қажет:
20-ға жуық амин қышқылдары;
20-дан астам аминоацил - т-РНҚ синтетаза ферменті;
20-ға жуық т-РНҚ;
Мg2+ ионы, конц 5-8 тМ қажет.
Сонымен барлығы 200-ге жуық макромолекулалар, белоктық
факторлар қажет.
15.
Рибосоманың негізгі қызметі – белок молекуласын синтездеуКіші бөлігінде
трансляция (көшіріп
аудару) процессі жүреді
Үлкен бөлігінде
аминқышқылдары жинақталып,
белок молекуласы түзіледі.
Эндоплазмалық
тордың
мембранасында
орналасқан
рибосомалар белоктың биосинтезі жүретін және оларды
тасымалдайтын бірыңғай жүйе болып есептеледі.
16. РНҚ-ның құрылысы мен функциясы
Әрбір жасушада ДНҚ-ға қарағанда РНҚ-ныңмөлшері 5-10 есе көп кездеседі.
РНҚ-ның бастапқы рөлі- ақуыздар түзіп,
генетикалық ақпаратты трянсляциялау және де
әр түрлі ген экспрессиясының кезеңдерінде
қатысатын эндонуклеазалық функцияларды
реттейді.
Кейбір вирустардың (ретровирустарда және
көптеген жануарлар вирусында)
өсімдіктер мен жәндіктерде РНҚ бір және екі
тізбекті молекула күйінде кездеседі.
17.
• РНҚ-ның ерекшеліктері – бірполинуклеотидтік тізбектен тұрады.
• 2-жіпшелік РНҚ өте сирек кездеседі. Бірақ,
РНҚ -РНҚ деген екі құрылымның
«шпилка» деп аталатын құрылымы жиі
кездеседі. Бұл құрылымның
комплементарлы азоттық негіздер болады.
• (А-Ц-Г-С) – осы құрылымдарды үшінші
реттік құрылым деп атайды.
• Т-РНҚ - беде жапырағы деп аталатын
екінші ретті құрылымдар кездеседі
18. РНҚ-ның түрлері.
• Көптеген жасушада мынадай РНҚ-ныңтүрлері кездеседі:
рибосомды (рРНҚ)
транспортты (тРНҚ)
ақпараттық немесе матрицалық (мРНҚ).
• Көбінесе клеткада кіші цитоплазмалық
РНҚ-лар (мцРНК), ал эукариот
жасушаларында кіші ядролы РНҚ-лар
кездеседі (мяРНК).
19. и-РНҚ құрылысы
ГЕНЕТИКАЛЫҚ КОД20.
Биологиялық код - ақуыздардың бірінші реттікқұрылысы туралы ақпаратты нуклеин қышқылдары
арқылы анықтау әдісі
Генетикалық кодтың касиеттері:
• триплеттік (әрбір амин қышқылы үш нуклеотидпен
кодталады);
• барлық тірі ағзаларда әмбебап;
• қайталанушылық (яғни бір амин қышқылын бірнеше
триплет кодтайды).
Амин қышқылдарын кодтайтын нуклеодитер
триплет немесе кодон деп аталады, олар т-РНҚ-дағы
антикодонға комплементарлы.
21.
• Төрт түрлі нуклеотидтен 64 кодон түзіледі,ондағы 61-і амин қьшқылдарын кодтайды
және
бірі метионинді кодтайтын АУГ-триплеті
инициациялаушы болып табылады.
Қалған 3 триплет (УАА, УАГ, УГА) амин
қышқылдарын кодтамайды, оны терминациялаушы
триплеттер деп атайды. Терминациялаушы
триплеттер ақуыздың синтезін аяқтайды.
22.
• Маңызы қызметі: триплеттілігі, биологиялықкодта код саны - 3. Үш нуклеотидтік қалдықтан бір
амин қышкылы қолданылады.
аяқтаушы триплеттер - УАА, УАГ, УГА ақуыз
синтезінің аяқталғанынын көрсетеді
• Ерекшелігі: әр триплет бір ғана амин қышқылын
кодтайды
• Әмбебаптылығы: биологиялық код барлық
ағзада бірдей
23. 1. Ядролық кезең немесе транскрипция. Мұнда ДНҚ қос тізбегінің біреуінің комплементарлы көшірмесі болып табылатын и-РНҚ синтезі
Белоктардың синтезделуі негізіненекі кезеңнен тұрады:
1. Ядролық кезең немесе транскрипция. Мұнда ДНҚ қос тізбегінің
біреуінің комплементарлы көшірмесі болып табылатын и-РНҚ
синтезі жүреді. Осы жолмен синтезделген и-РНҚ әрі қарай
синтезделетін
белоктың
негізі
болып
табылады.
2. Цитоплазмалық кезең яғни трансляция. Цитоплазмада 4 әріптік
генетикалық информацияның триплеттік кодтың көмегімен 20 әріптік
амин қышқылдарынан тұратын белоктың тізбегіне айналу процесі
жүреді. Сонымен бірге онда белоктардың үшінші, төртінші реттік
құрылысының кеңістікте орын алуы және олардың клетка
метаболизміне тікелей қатынасуына мүмкіндік туады.
24.
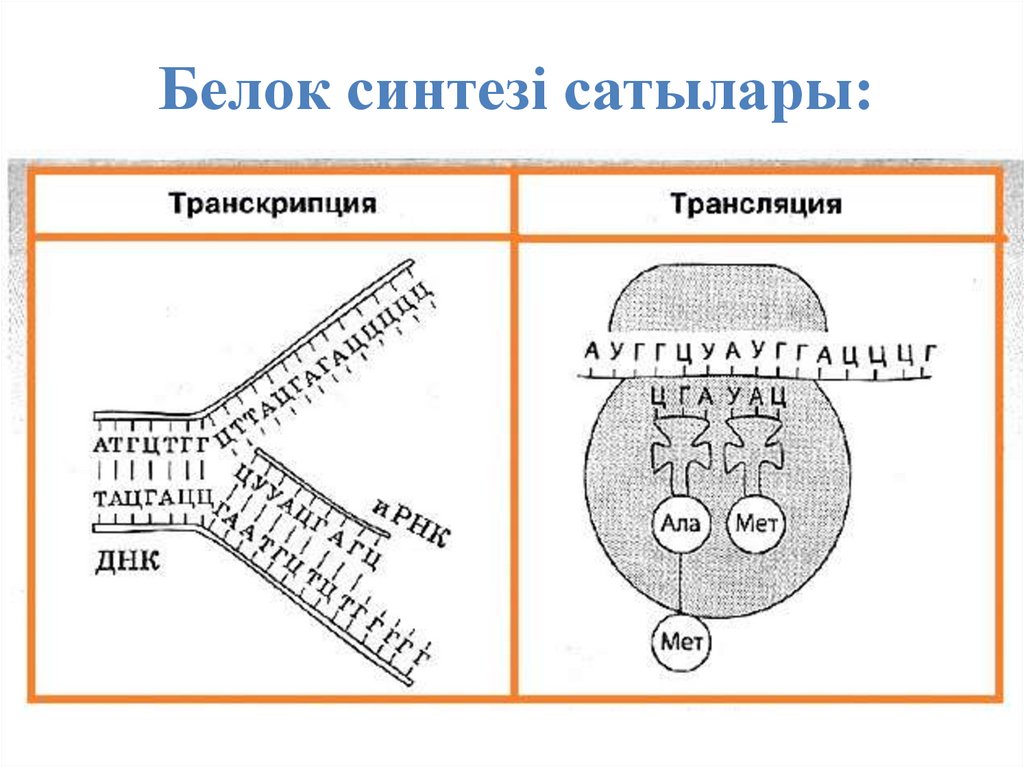
Белок синтезі сатылары:25.
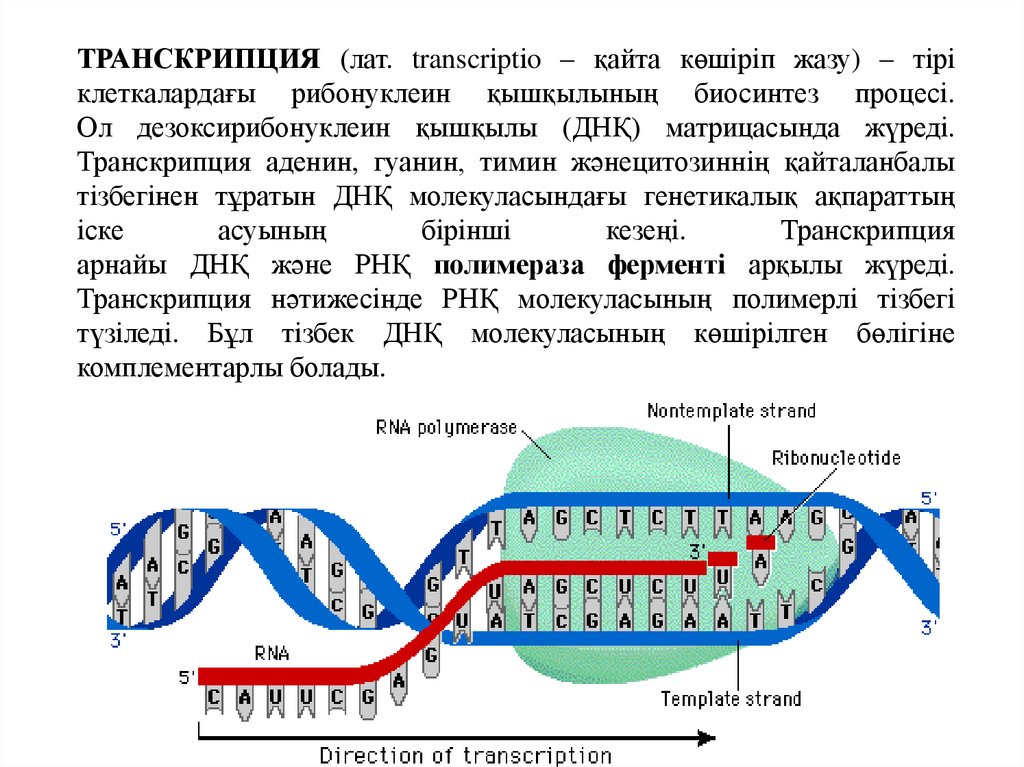
ТРАНСКРИПЦИЯ (лат. transcrіptіo – қайта көшіріп жазу) – тіріклеткалардағы рибонуклеин қышқылының биосинтез процесі.
Ол дезоксирибонуклеин қышқылы (ДНҚ) матрицасында жүреді.
Транскрипция аденин, гуанин, тимин жәнецитозиннің қайталанбалы
тізбегінен тұратын ДНҚ молекуласындағы генетикалық ақпараттың
іске
асуының
бірінші
кезеңі.
Транскрипция
арнайы ДНҚ және РНҚ полимераза ферменті арқылы жүреді.
Транскрипция нәтижесінде РНҚ молекуласының полимерлі тізбегі
түзіледі. Бұл тізбек ДНҚ молекуласының көшірілген бөлігіне
комплементарлы болады.
26.
27.
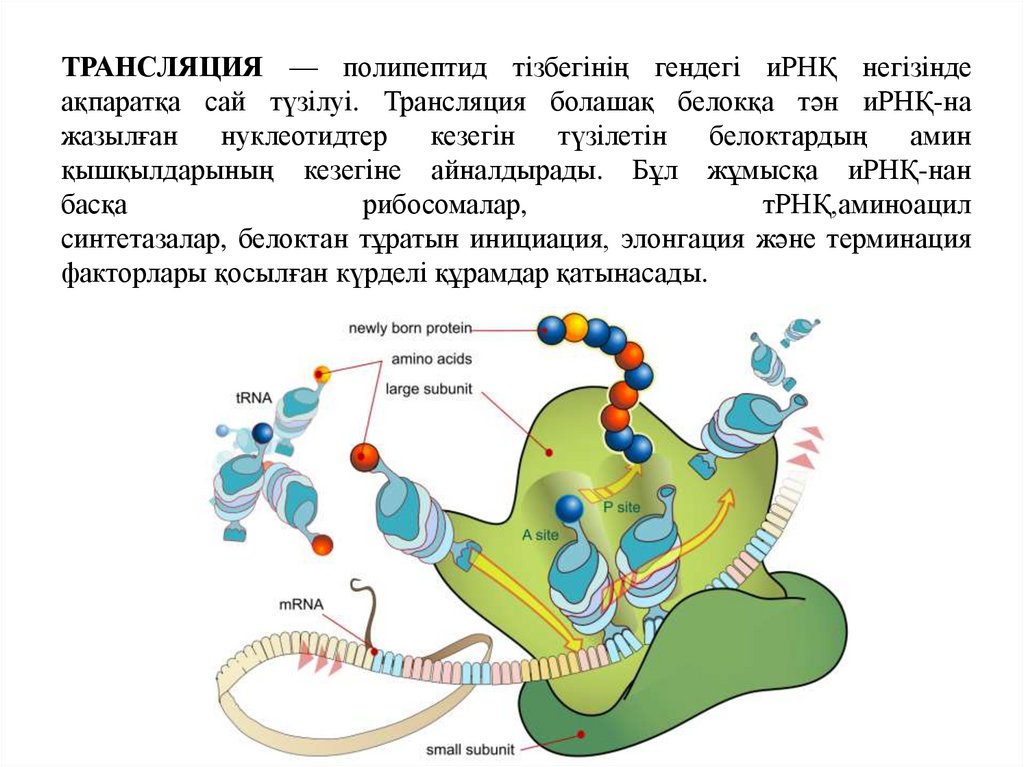
ТРАНСЛЯЦИЯ — полипептид тізбегінің гендегі иРНҚ негізіндеақпаратқа сай түзілуі. Трансляция болашақ белокқа тән иРНҚ-на
жазылған
нуклеотидтер
кезегін
түзілетін белоктардың
амин
қышқылдарының кезегіне айналдырады. Бұл жұмысқа иРНҚ-нан
басқа
рибосомалар,
тРНҚ,аминоацил
синтетазалар, белоктан тұратын инициация, элонгация және терминация
факторлары қосылған күрделі құрамдар қатынасады.
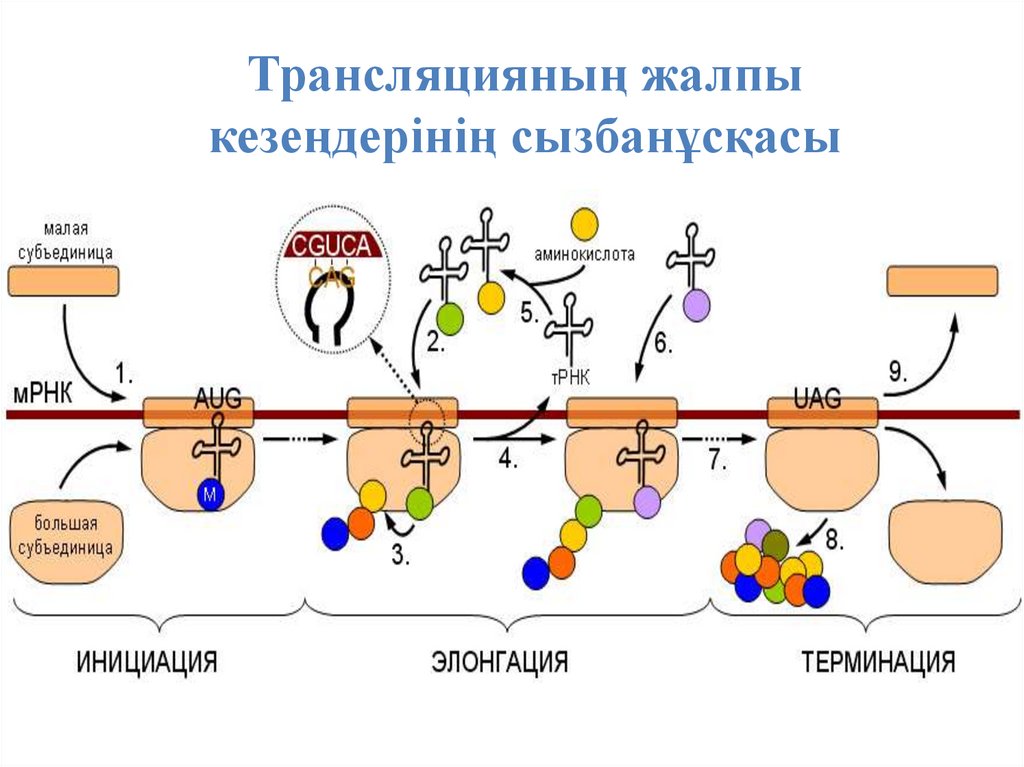
28.
Трансляцияның жалпыкезеңдерінің сызбанұсқасы
29.
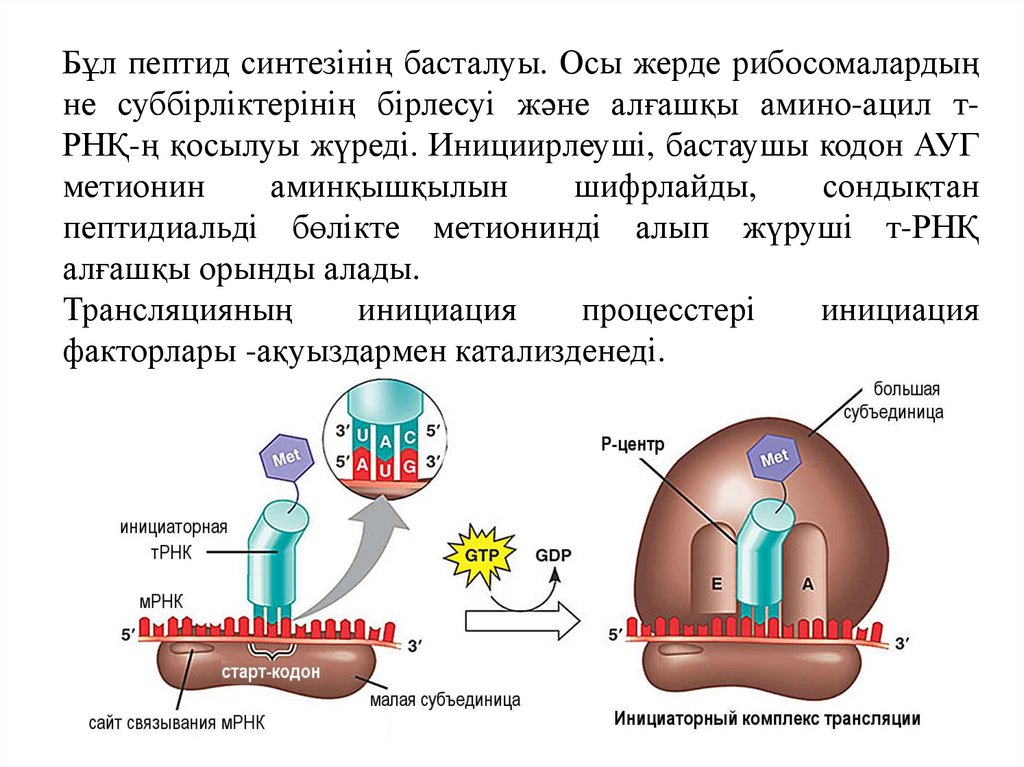
Бұл пептид синтезінің басталуы. Осы жерде рибосомалардыңне суббірліктерінің бірлесуі және алғашқы амино-ацил тРНҚ-ң қосылуы жүреді. Инициирлеуші, бастаушы кодон АУГ
метионин
аминқышқылын
шифрлайды,
сондықтан
пептидиальді бөлікте метионинді алып жүруші т-РНҚ
алғашқы орынды алады.
Трансляцияның
инициация
процесстері
инициация
факторлары -ақуыздармен катализденеді.
30.
Инициация кезінде РНҚ полимераза промотормен қосылып ДНҚшынжырын тарқатады. М-РНҚ бір шынжырлы. ДНҚ –да РНҚ-ның
орналасуы комплементарлық принциппен өтеді. Мұндай бірізділік
трансляцияның терминациялы кодоны деп аталынады.
ДНҚ транскрипциялы аймағы, яғни промотор мен терминтатор
арасында орналасса транскрипция бірілігі немесе транскриптоном деп
аталынады. ДНҚ транскрипциялы аймағы, яғни промотор мен
терминтатор арасында орналасқан транскрипция бірлігі немес
транскриптон деп аталынады, ал түзілген РНҚ алғашқы транскриптат
делінеді.
Прокариоттарда алғашқы транскриптатта РНҚ-ның көшірмесі
бірнеше гендерден тұрады, ал эукариоттарда – біреу ғана.
РНҚ полимеразаның бірнеше типтері белгілі. РНҚ-ның
транскриптаттың 5/ - соңы синтезделінеді, содан кейін кэпирленеді.
Кэпирлену – бұл белгі нуклеотидтердің бірізділігінің қосылуы.
Кэпирлену қызметі – РНҚ транскриптатаны бұзылудан қорғау және
рибосомамен байланысады. Одан трансляция басталады,сосын кэп
алынып тасталынады.
31.
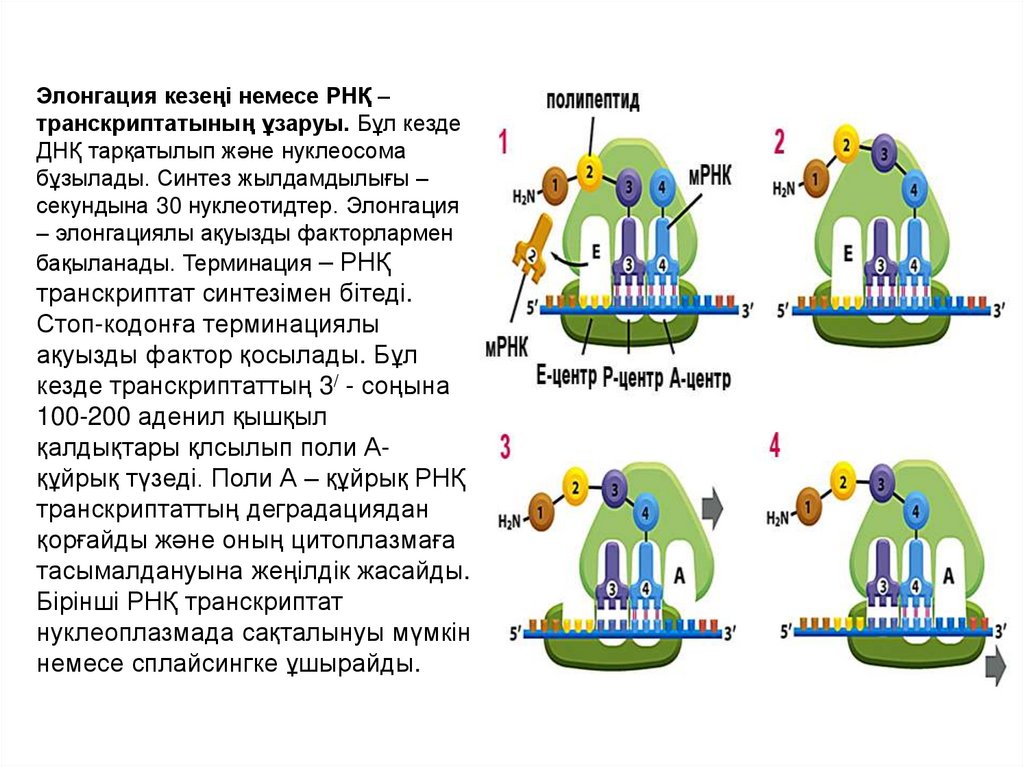
Элонгация кезеңі немесе РНҚ –транскриптатының ұзаруы. Бұл кезде
ДНҚ тарқатылып және нуклеосома
бұзылады. Синтез жылдамдылығы –
секундына 30 нуклеотидтер. Элонгация
– элонгациялы ақуызды факторлармен
бақыланады. Терминация – РНҚ
транскриптат синтезімен бітеді.
Стоп-кодонға терминациялы
ақуызды фактор қосылады. Бұл
кезде транскриптаттың 3/ - соңына
100-200 аденил қышқыл
қалдықтары қлсылып поли Ақұйрық түзеді. Поли А – құйрық РНҚ
транскриптаттың деградациядан
қорғайды және оның цитоплазмаға
тасымалдануына жеңілдік жасайды.
Бірінші РНҚ транскриптат
нуклеоплазмада сақталынуы мүмкін
немесе сплайсингке ұшырайды.
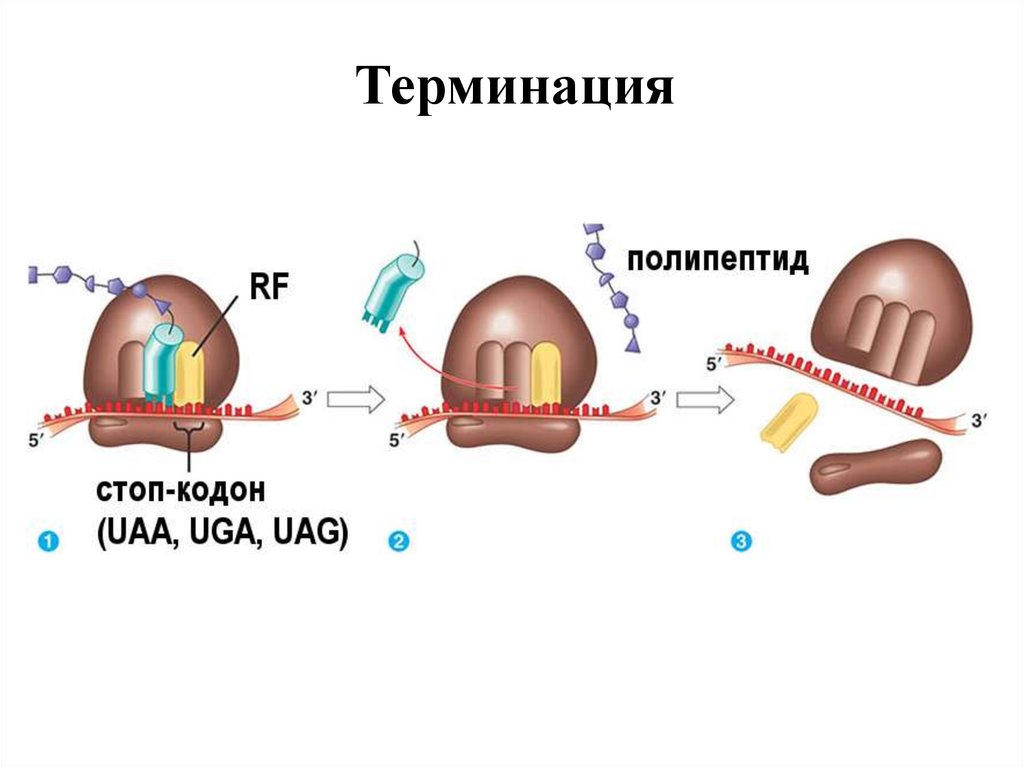
32. Терминация
33.
• Трансляцияның 4-ші кезеңі – Терминация, яғни синтездің бітуі,аяқталу кезеңі, керекті эаттар:
1)АТФ;
2) Белок синтезінің біткенін білдіруші и-РНҚ-дағы кодондар;
3) Полипептидтің рибосомадан босап шығуына қажет белоктық
факторлар, и-РНҚ-да соңғы амин қышқылын көрсететін кодон
біткен соң, мағынасыз, мәнсіз кодондар басталады. Олардың саны
үшеу: УАА, УАГ, УГА. Міне осы кодондардың басталуы,
полипептидттің синтезінің біткенін хабарлайды. Сонан соң,
синтезді бітіруші факторлар /Ғ1, Ғ2/ өздерінің әрекетін бастайды.
Бұл факторлар: I/ полипептидтің соңғы т-РНҚ-дан гидролиздік
жолмен ыдырап шығуын және т-РНҚ-ның босауын; 2/ соңғы т-РНҚның пептидилдік бөлімнің "бос" күйінде бөлінуін; 3/ рибосоманың
305 жане 505 суббірліктерге диссоциациялануын қамтамасыз етеді.
34.
• Трансляцияның 5-ші кезеңі - кеңістіктегі полипептидтік тізбектіңорналасуы және процессинг. Бұл кезеңде полипептид өзінің
кеңістіктегі екінші- , үшінші - реттік құрылысын түзіп, биологиялық
активті түріне көшеді. Сонымен қатар бұл кезеңде бірінші амин
қышқылы метиониннен және кейбір керек емес амин қышқылдарынан
ажырап, кейбір амин қышқылдарының қалдықтары өзіне фосфат, метил - , карбоксил - , ацетил топтарын қосып алуы мүмкін. Ал кейде
белоктар өзіне олигосахаридтер мен коферменттерді қосып, өзінің
биологиялық қызметін атқаруға дайын болады. Белоктардың синтезі
көптеген антибиотиктер әсерінен тежеуге ұшырауы мүмкін. Кейбір
микроорганизмдер үшін қорғаныш антибиотиктер, басқа организмдер
үшін өте улы болып табылады. Мысалы: пурамицин - элонгация
кезеңінде әсер етсе, тетрациклин аминоацил - т-РНҚ-ның рибосомадағы
аминоацилдік центрімен байланысуына кедергі жасайды; стрептомицин
- рибосоманың кіші суббірлігімен қосылып оның қызметін
нашарлатады; дифтерия токсині-элонгация факторын тежейді;
левомицетин - пептидилтрансфераза ферментінің активтілігін
нашарлатады; эритромицин - үлкен суббірлікпен қосылып, транслоказа
ферментінің жұмысын тежейді.
35.
• Белоктар синтезінің реттелуі. Белок синтезінің реттелуі иРНҚ-ның синтезі және трансляция (яғни белок синтезі)кезеңінде жүреді. Бұл бағытта аса көп жұмыс істеген француз
ғалымдары Жакоб және Моно болды. Бұл ғалымдар осы
жұмысы үшін Нобель сыйлығына ие болды. Олар белоктарды
синтездеу теориясын оперон теориясы деп атады. Бұл
ғалымдардың пікірі бойынша бактерияларда ең кемінде геннің
үш түрі болады: 1) оператор гені (0-ген); 2) реттеуші ген ( R –
ген); 3) белоктардың бірінші реттік құрылысын анықтайтын
құрылымдық ген (S – ген).
ДНҚ молекуласының осы үш ген орналасқан бөлімін опероң
деп атайды да, бірімен-бірі тығыз байланысты болады.
Реттеуші ген оператор геніне репрессор арқылы әсер етіп
отырса, оператор гені құрылымдық генге әсер етеді
36. Негізгі бөлім
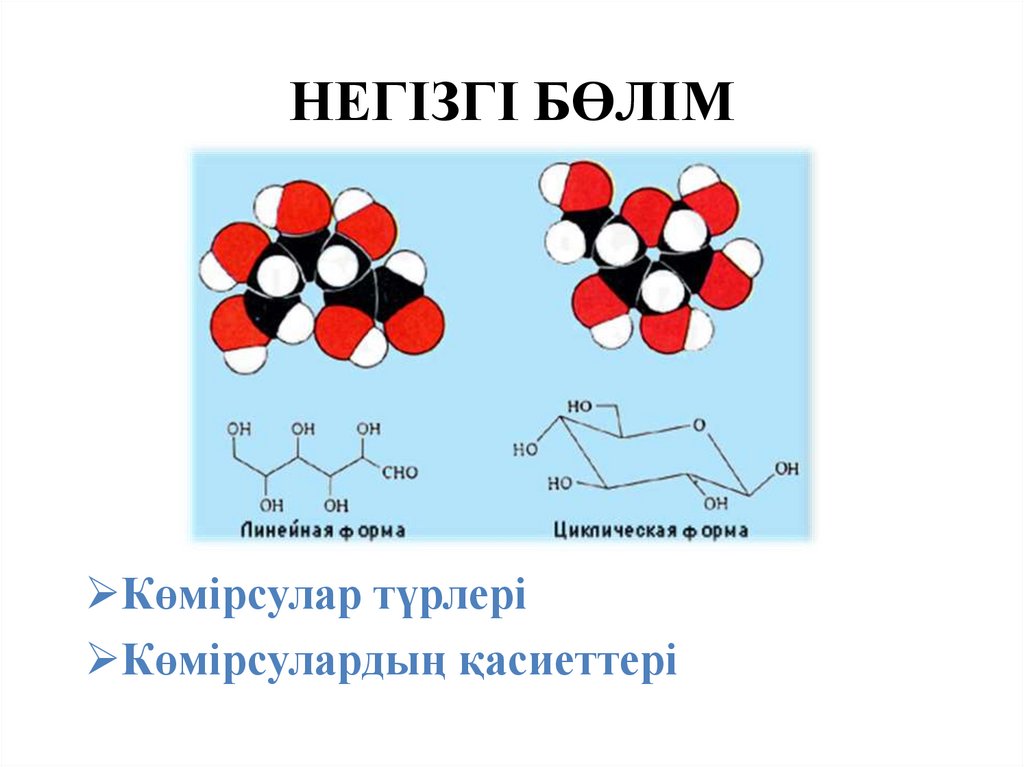
НЕГІЗГІ БӨЛІМКөмірсулар түрлері
Көмірсулардың қасиеттері
37. Көмірсулар – барлық тірі ағзада энергия беретін органикалық зат және көміртек көзі
жалпы формуласыCn(H2O)m
38.
Таза күйінде қызылша қанты 1747 жылынеміс химигі А. Маргграф ашқан болатын
2. 1811 жылы орыс химигі Кирхгоф алғаш
рет глюкозаны крахмал гидролизі арқылы
бөліп алған
3. 1837жылы швед химигі Я. Берцеллиус
глюкозаның дұрыс эмпирикалық
формуласын С6Н12О6 ұсынды
4. 1861 жылы формальдегидтен Са(ОН)2
қатысында көмурсулар синтезін А.М. Бутлеров
жүргізген
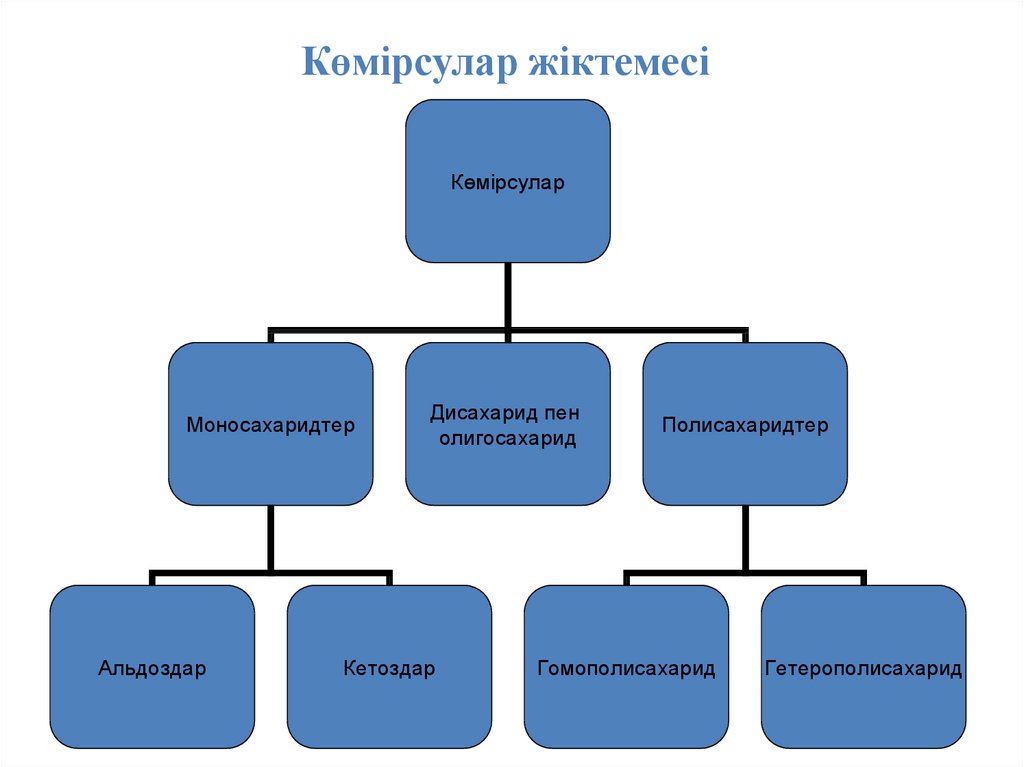
39. Көмірсулар жіктемесі
КөмірсуларМоносахаридтер
Альдоздар
Дисахарид пен
олигосахарид
Кетоздар
Полисахаридтер
Гомополисахарид
Гетерополисахарид
40. Көмірсулар биологиялық қызметтері
Энергетикалық
Тіректік қызмет
Қорғаныштық (майлау)қызметі
Гидросмостық және ионды реттеушілік
Кофакторлық
41. Моносахаридтердің физикалық қасиеттері
Түссіз
Кристалды заттар
Суда ериді
Дәмі тәтті
Cn(H2O)m
42. Моносахаридтер изомериясы. Оптикалық изомерия
HH
HO
С
O
С * OH
С* H
H
С * OH
H
С * OH
СH2OH
D-(+)-глюкоза
Көмірсу молекуласы оптикалы белсенді және құрамынды
бірнеше ассиметриялы көміртегі атомдары бар. ОНтоптардың және сутегі атомдарының кеңістіктегі орналасуы
моносахаридтердің диастереоизомерлердің бар екендігін
көрсетеді. Альдогексоздарда 8 диастереоизомер, ал
кетогексоздарда 4 диастереоизомер болады.
Әрбір диастереоизомер екі оптикалық изомер D- және Lэнантиамерлер түрінде бола алады.
Тірі ағзалар D қатарын ғана бойына сіңіре алады
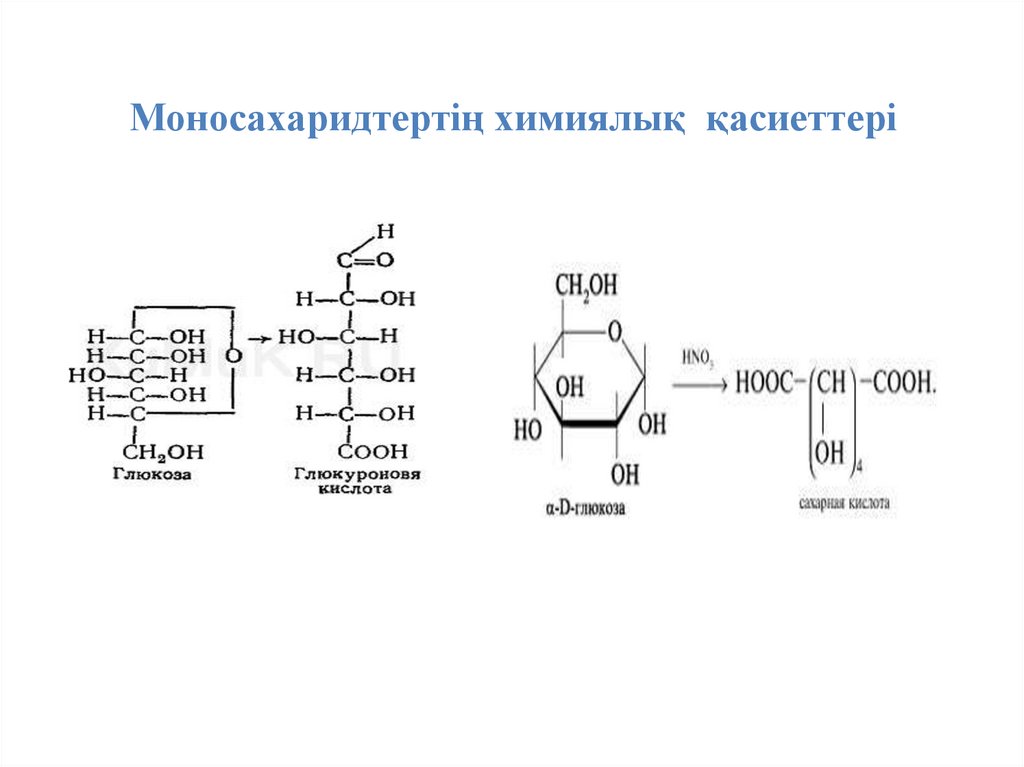
43. Моносахаридтертің химиялық қасиеттері
1. Альдегидтер мен кетондарсияқты сутегі атомдары әсерінен оңай тотықсызданады.
C6H12O6 + НАД-Н + Н+→ С6Н14О6 +НАД+
D-глюкоза
D-сорбит (алты атомды спирт)
2.
Моносахаридтер тотығуы жағдайға байланысты альдегидтік немесе бірінші
спирттік
бойынша жүреді. Альдегидтік топ тотыққан кезде альдон қышқылдары түзіледі.
C6H12O6
D-глюкоза
→ С6Н12О7
D-глюкон қышқылы
3. Моносахаридтердің бірінші спирттік бойынша тотығу өнімдері урон қышқылдар
(альдегид қышқылдар) деп аталады. М: D-глюкоза D-глюкурон қышқылын, Dгалактоза Dгалактурон қышқылын береді. альдегидтік топ пен бірінші спирттік топтың екеуі де
тотықса,онда Альдар қышқылдары түзіледі. М: D-глюкоза осындай тотығу кезінде екі
негізді қант қышқылын береді.
44. Моносахаридтертің химиялық қасиеттері
45.
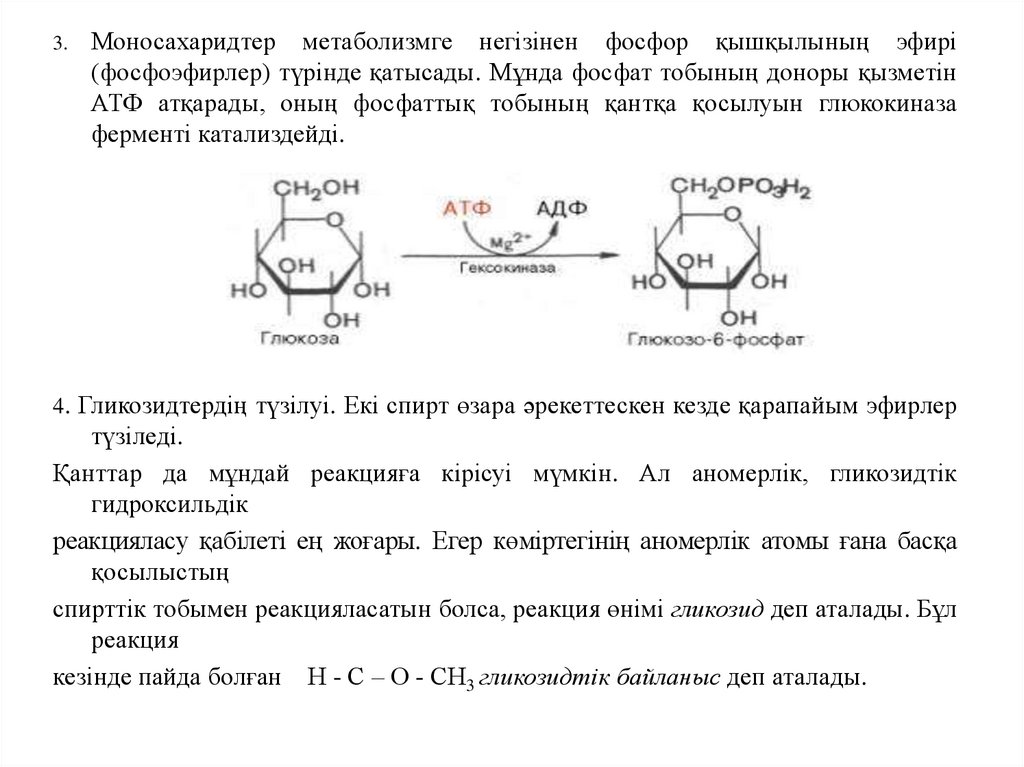
3.Моносахаридтер метаболизмге негізінен фосфор қышқылының эфирі
(фосфоэфирлер) түрінде қатысады. Мұнда фосфат тобының доноры қызметін
АТФ атқарады, оның фосфаттық тобының қантқа қосылуын глюкокиназа
ферменті катализдейді.
4. Гликозидтердің түзілуі. Екі спирт өзара әрекеттескен кезде қарапайым эфирлер
түзіледі.
Қанттар да мұндай реакцияға кірісуі мүмкін. Ал аномерлік, гликозидтік
гидроксильдік
реакцияласу қабілеті ең жоғары. Егер көміртегінің аномерлік атомы ғана басқа
қосылыстың
спирттік тобымен реакцияласатын болса, реакция өнімі гликозид деп аталады. Бұл
реакция
кезінде пайда болған Н - С – О - СН3 гликозидтік байланыс деп аталады.
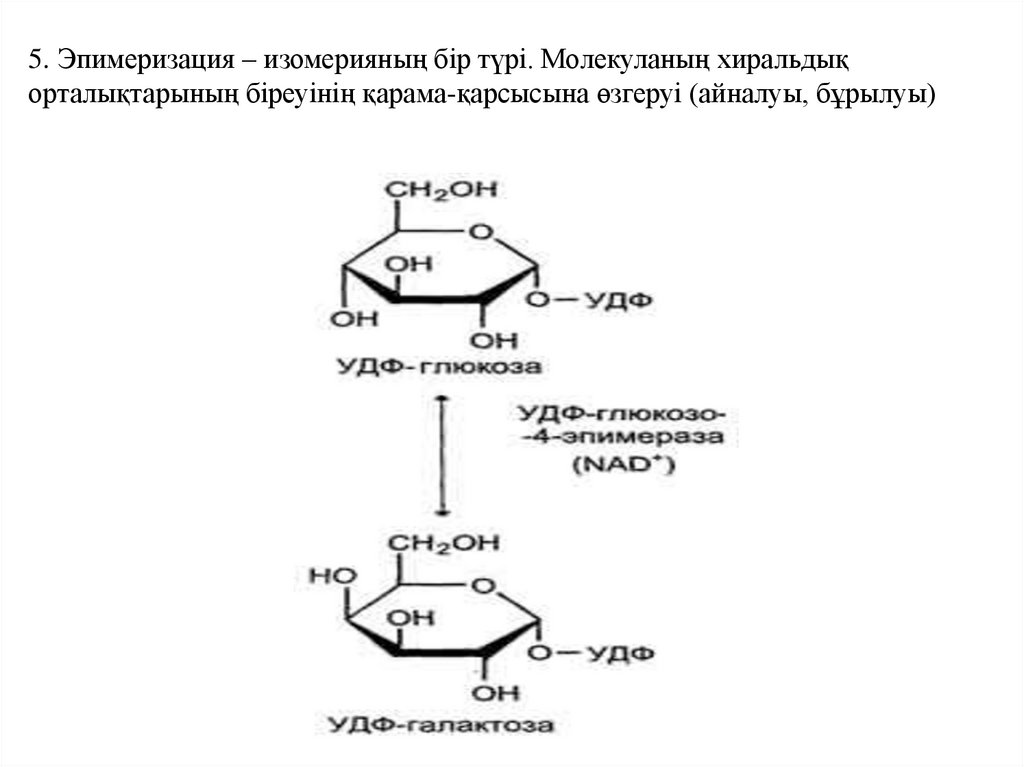
46.
5. Эпимеризация – изомерияның бір түрі. Молекуланың хиральдықорталықтарының біреуінің қарама-қарсысына өзгеруі (айналуы, бұрылуы)
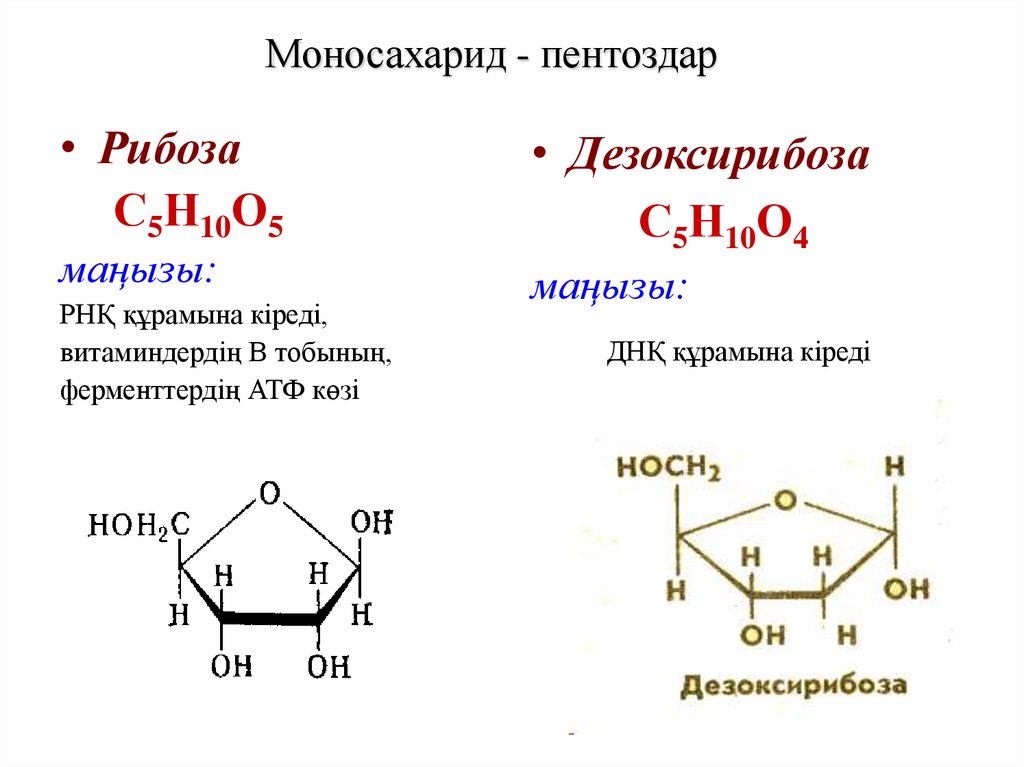
47. Моносахарид - пентоздар
• РибозаС5Н10О5
маңызы:
РНҚ құрамына кіреді,
витаминдердің В тобының,
ферменттердің АТФ көзі
• Дезоксирибоза
С5Н10О4
маңызы:
ДНҚ құрамына кіреді
48.
• ГлюкозаС6Н12О6
маңызы: Энергия көзі;
гликозидтердің құрамына кіреді,
бос күйінде өсімдіктер,
жануарлар және адам
тканьдерінде болады;
полисахаридтердің, гликоген,
крахмал, клетчатканың мономері.
49.
• ФруктозаС6Н12О6
Маңызы:
Жеміс қанты; бос күйінде бал
құрамында болады; сахарозамен
салыстырғанда тәттілеу, байланысқан
күйде сахарозада, полисахарид
инулинде кездеседі.
• Галактоза
С6Н12О6
Маңызы:
Бос күйінде кездеспейді, липоидтер –
цереброзидтер құрамында, нерв ткані
ганглиозидтерінде болады және ми
жасушаларының түзілуінде маңызды
роль атқарады.
50. Дисахаридтер
Молекулалық формуласы С12Н22О11, судың бір молекуласын бөліп
шығару
арқылы
гликозидтік
байланыспен
байланысқан
моносахаридтердің екі молекуласынан құралған.
Табиғатта бос күйінде екі дисахарид – сахароза мен лактоза
кездеседі. Ал крахмал, гликоген және целлюлоза полисахаридтері
шала гидролизденгенде мальтоза, изомальтоза және целлобиоза
түзіледі.
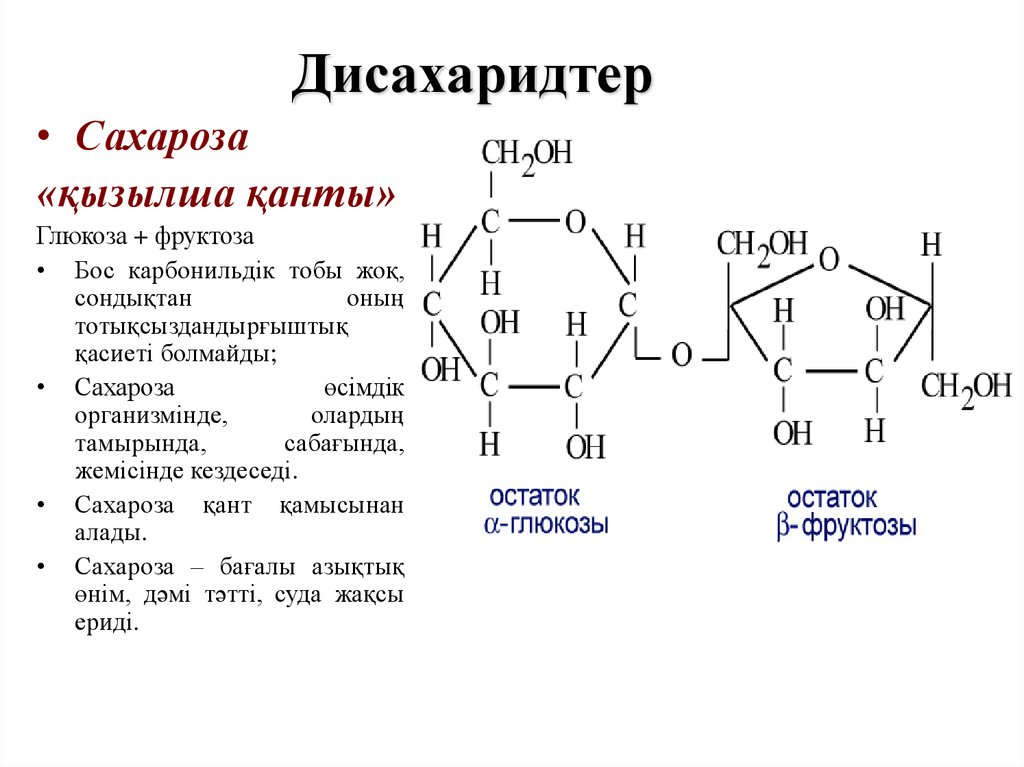
51. Дисахаридтер
• Сахароза«қызылша қанты»
Глюкоза + фруктоза
• Бос карбонильдік тобы жоқ,
сондықтан
оның
тотықсыздандырғыштық
қасиеті болмайды;
• Сахароза
өсімдік
организмінде,
олардың
тамырында,
сабағында,
жемісінде кездеседі.
• Сахароза қант қамысынан
алады.
• Сахароза – бағалы азықтық
өнім, дәмі тәтті, суда жақсы
ериді.
52.
• МальтозаГлюкоза + Глюкоза
Крахмал мен гликогеннің
шала гидролизденуі
нәтижесінде алынатын өнім
болап табылады.
Ячмень солодында, басқа да
дәнді дақылдар құрамында
болады. Томаттарда, кейбір
жемістердің нектарында да
табылған.
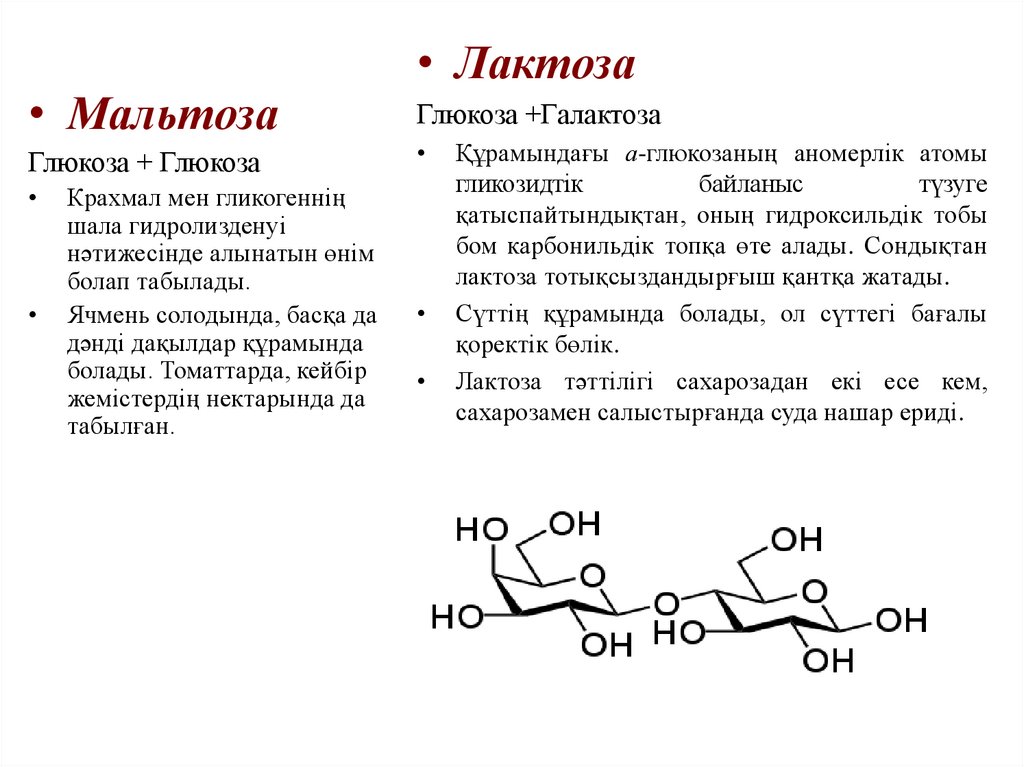
• Лактоза
Глюкоза +Галактоза
Құрамындағы а-глюкозаның аномерлік атомы
гликозидтік
байланыс
түзуге
қатыспайтындықтан, оның гидроксильдік тобы
бом карбонильдік топқа өте алады. Сондықтан
лактоза тотықсыздандырғыш қантқа жатады.
Сүттің құрамында болады, ол сүттегі бағалы
қоректік бөлік.
Лактоза тәттілігі сахарозадан екі есе кем,
сахарозамен салыстырғанда суда нашар ериді.
53. Полисахаридтер
• Күрделі көмірсулар, олар гликозидтік байланыстарменжалғасқан 1000 дейін, тіпті одан да көп
моносахаридтерден құралады.
• Полисахаридтерге жататындар: крахмал, гликоген,
целлюлоза, инулин, гемицеллюлоза, пентозандар, т.б.
• Кейбір полисахаридтер мукополисахаридтер деп
аталады, олар аминосахаридтер мен урон қышқылынан
тұрады. Оларға: гиалурон қышқылы, хитин, лигнин,
гепарин, т.б. жатады.
• Гомополисахаридтер
құрамында
бір
түрдің
моносахаридтері бар заттар. Мысалы, крахмал мен
гликоген тек қана глюкоза молекуларынан тұрады.
• Гетерополисахаридтер әр түрлі моносахаридтерден
және
олардың
туындыларынан
құралатын
биополимерлер. Мысалы, камеди.
54. Крахмал (С6Н10О5)n
• Өсімдіктердің негізгі қоры болатын көмірсу және адамға азық-түлік,малға жемшөп болатын аса маңызды полисахарид.
• Екі бөліктен тұрады: амилоза мен амилопектиннен тұрады
• Амилопектин крахмал дәнінің сыртқы қабығын құрайды.
Амилопектин құрылымы тармақталған, мұнда негізгі тізбек а(1→4)
байланысы арқылы жалғасқан глюкоза қалдықтарынан тұрады.
• Амилоза құрылымы тармақталмаған созылыңқы келеді, мұнда глюкоза
молекуласының қалдықтары (1000-4000) а(1→4) байланысы арқылы
жалғасқан.
• Крахмал ақ ұнтақ, суда ерімейді, ісінеді, ыстық суға салса клейстер
береді.
• Амилоза суда ериді, иодпен әсер еткенде көк түске боялады.
Амилопектин суда ерімейді, иодпен әсер еткенде күлгін түске енбейді.
55. Крахмал
CH 2OHамилозы (10-20%) және
амилопектина (80-90%),
D-глюкозаға
дейін
гидролизденеді.
O
HO
OH
CH 2OH
O
O
HO
OH
CH 2OH
O
O
спирализация
HO
OH
Амилоза
a -Glc-(1
4)
n
n = 6000 - 6000000
n = 1000-3000
O
Амилоза
Амилопектин
56.
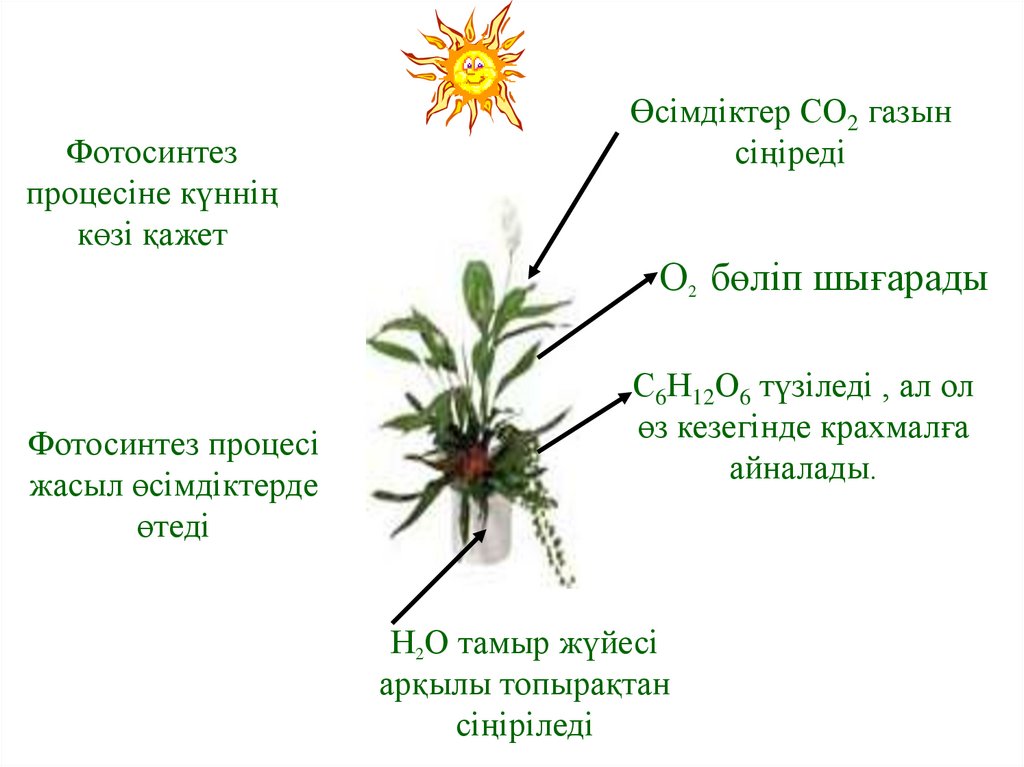
Фотосинтезпроцесіне күннің
көзі қажет
Өсімдіктер СО2 газын
сіңіреді
О2 бөліп шығарады
Фотосинтез процесі
жасыл өсімдіктерде
өтеді
С6Н12О6 түзіледі , ал ол
өз кезегінде крахмалға
айналады.
Н2О тамыр жүйесі
арқылы топырақтан
сіңіріледі
57. Гликоген
• Жануарлардың полисахарид қоры. Бауырмен бұлшық еттерде, қанда да жиналады.
Ол – организмге қуат беретін заттық қор.
• Крахмал
молекуласына
қарағанда,
гликоген молекуласының тармағы көп
және құрылымы ашық.
• Таза гликоген – ақ түсті ұнтақ, суда ериді
де коллоидты ерітінді түзеді. Иодпен әсер
еткенде қызыл түске немесе қызыл-қоңыр
түске боялады.
• Бауырдың беткі жағында түйіршік түрінде
болады.
• Молекулалық массасы өте жоғары – 1-1,5
млн шамасындай.
• Гликогеннің құрылымы амилопектинге
ұқсас.
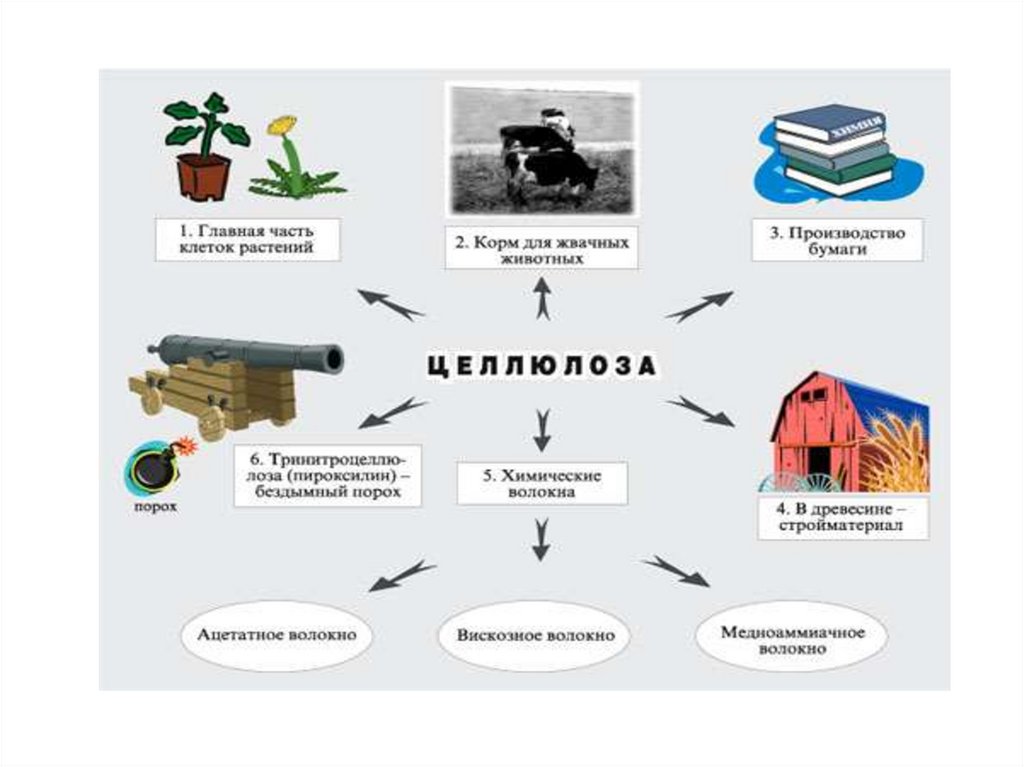
58. Целлюлоза
• Өсімдіктер жасушасының негізгі материалы.• Таза целлюлозаның талшықтанған құрылымы бар және
органикалық еріткіштерде ерімейді. Ол Швейцар
реактивінде (мыс гидрототығының аммиак ерітіндісі)
ериді.
• Молекулалық массасы толық анықталмаған, шамамен
10млн.
• Химиялық реакцияда спирттік қасиет көрсетеді,
қышқылдармен
эфирлер
түзеді.
Бұл
қасиеті
нитроцеллюлоза, түтінсіз оқ-дәрі, вискоз жібегін алу
үшін пайдаланады.
59.
60.
Хитин целлюлозаға жақын; ол саңырауқұлақтардың кейбіртүрлерінде кездеседі; және де кейбір жануарлардың сыртқы
қаңқасының маңызды бөлігі болып табылады.
61.
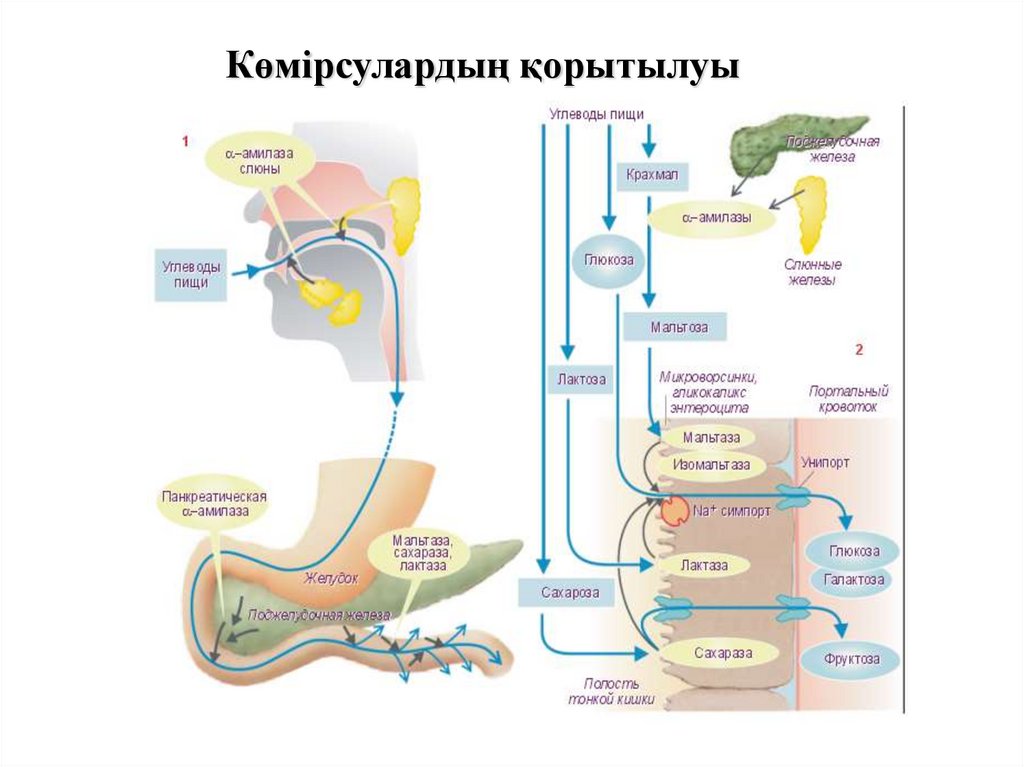
62. Көмірсулардың қорытылуы
63. Негізгі бөлім
НЕГІЗГІ БӨЛІМНуклеин қышқылы синтезі
Нуклеин қышқылы қасиеттері
64.
• Швейцария биологы Э.Мишер (1868) іріңжасушалары ядросынан құрамында фосфоры
бар зат бөліп алды.Ядродан бөліп алынған бұл
зат нуклеин деп аталды.
• Нуклеин екі: қышқылдық ДНҚ және негіздік
ақуыздық компоненттен тұрады.
• ДНҚ жасушаның тұқым қуалаушылығына
қатысты және генетикалық ақпарат
тасушы.(1943)
• ДНҚ негізінен жасушаның ядросында
жинақталған. Оның негізгі қызметі ген
тасымалдаушылық.
65.
• РНҚ жасуша ядросында және цитоплазмада(РНҚ-ның 90%-ға жуығы цитоплазмада)
орналасқан және ақуыз синтезінің
белсенділігі РНҚ мөлшеріне тікелей
байланысты.
• Жасушада рибонуклеин қышқылдары РНҚ:
ақпараттық РНҚ (а-РНҚ),
тасымалдаушы немесе ерігіш РНҚ (т-РНҚ),
рибосомалық (р-РНҚ) түрінде кездеседі.
Үшеуі де белгілі бір молекулаық массасы мен
арнайы нуклеотидтік құрамы бойынша
ерекшеленеді.
66.
• Нуклеин қышқылы - пішіні жіп тәрізді,жоғарғы молекулалы, ерітінділерінің
тұтқырлығы жоғары қосылыс.
• Адамның 23 жұп хромасомасында ДНҚ
ұзындығы 1,5 м.
РНҚ молекуласы өте қысқа, ұзындығы 0,01
мм
ДНҚ негізгі бөлігі жасуша ядросындахроматин негізінде аздаған мөлшері
митохондрияда орналасқан.
РНҚ жасушаның барлық жерінде кездеседі.
67.
• ДНҚ геннің материалдық негізі, ол генніңкелесі қасиеттеріне ие болады:
• 1. Өз-өзін дәл қайталау, соның арқасында
генетикалық ақпаратты ұрпақтан ұрпаққа
жеткізу.
• 2. Жасуша метаболизмін басқару үшін
ферменттердің синтезін бағыттау.
68.
• Дезоксирибонуклеотидтер - ағзадағы ДНҚ-ңтүзілуіне қатысады.
• Рибонуклеотидтер РНҚ- түзілуіне
жүмсалады. Рибонуклеотидтердің кейбірі
трансферазалық реакцияларда коферменттік
қызмет атқарады. Аденильді
рибонуклеотидтер НАД+ , НАДФ+ ФАД,
КоА ферментінің құрамына кіреді.
69.
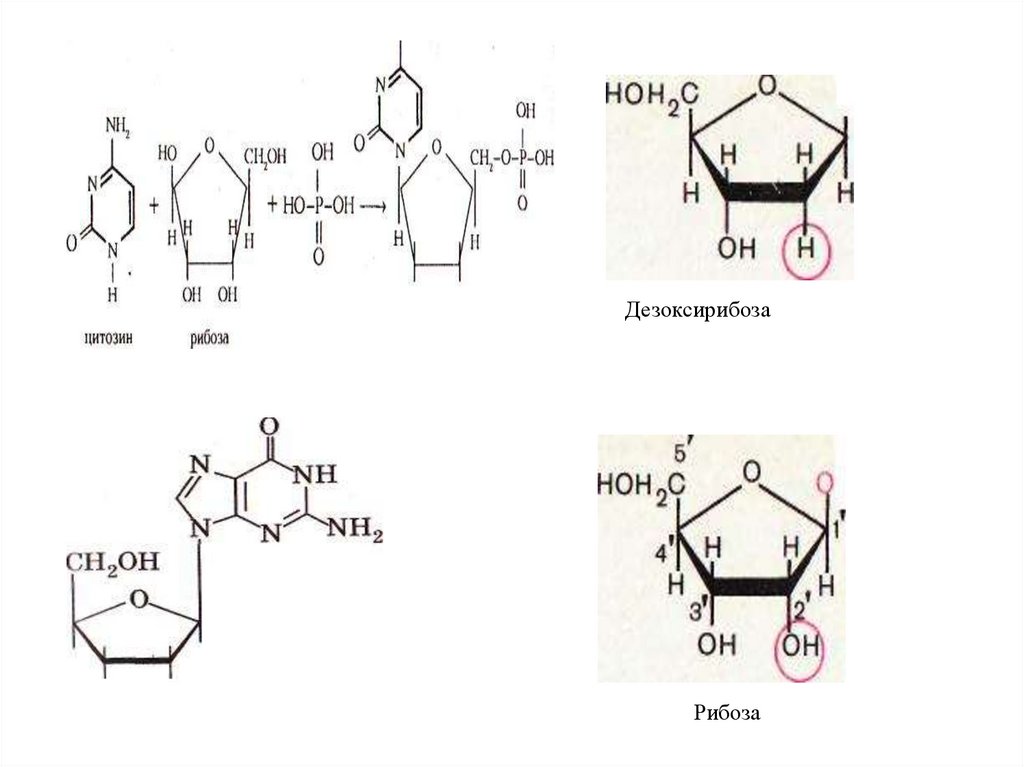
• Нуклеин қышқылдары - нуклеотидполимерлерінен құралған.
• Нуклеотидтердің химиялық құрамы пиримидиндік немесе пуриндік негіздер,
пентоз, фосфор қышқылының қалдығы.
• Нуклеотидтер пентоздың (рибоза,
дезоксирибоза), пуриндік (аденин, гуанин)
және пиримидиндік (тимин, цитозин, урацил)
негіздерге байланысты екі топқа бөлінеді.
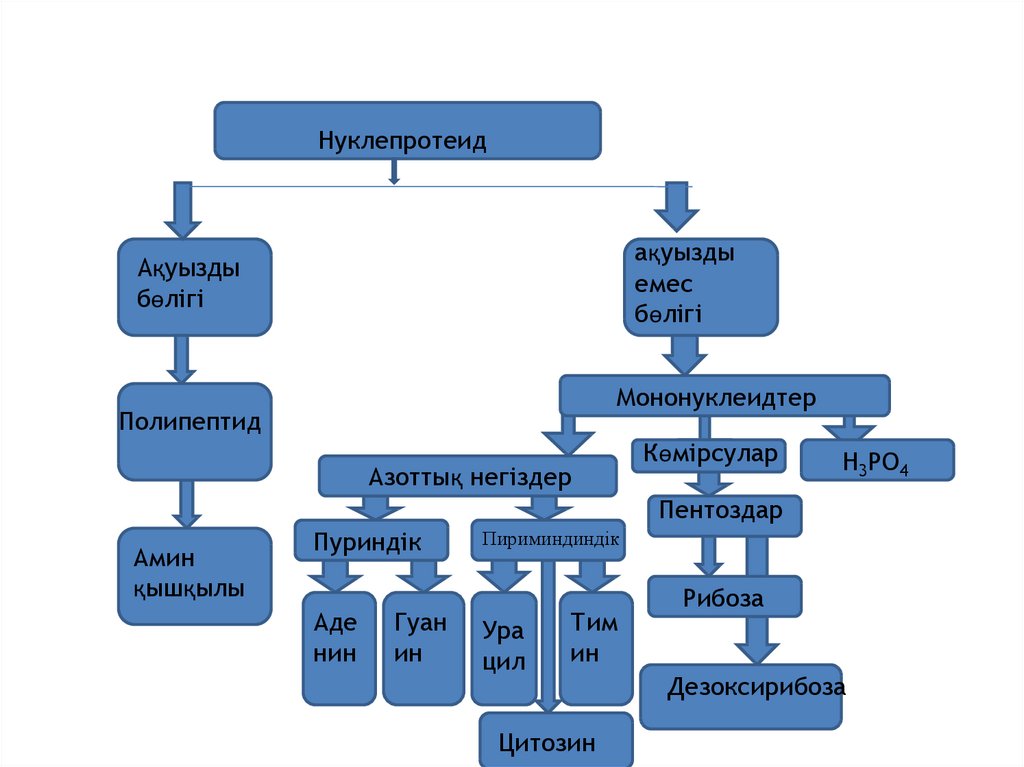
70.
Нуклепротеидақуызды
емес
бөлігі
Ақуызды
бөлігі
Мононуклеидтер
Полипептид
Азоттық негіздер
Көмірсулар
H3PO4
Пентоздар
Амин
қышқылы
Пуриндік
Аде
нин
Гуан
ин
Пириминдиндік
Ура
цил
Тим
ин
Цитозин
Рибоза
Дезоксирибоза
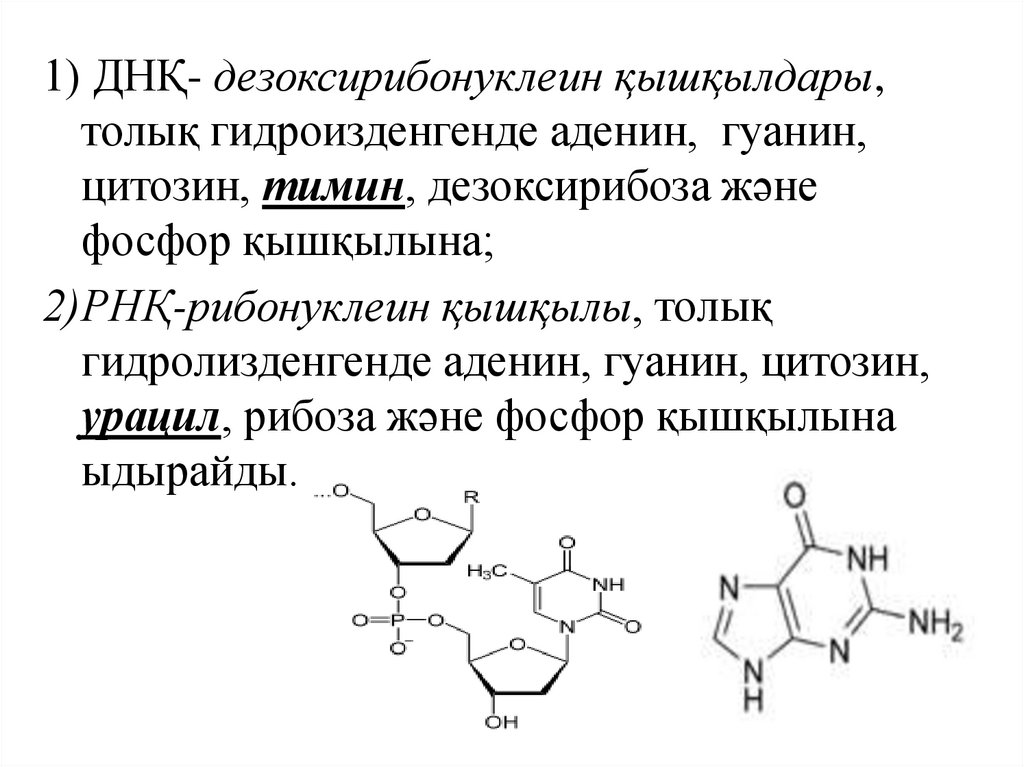
71.
1) ДНҚ- дезоксирибонуклеин қышқылдары,толық гидроизденгенде аденин, гуанин,
цитозин, тимин, дезоксирибоза және
фосфор қышқылына;
2)РНҚ-рибонуклеин қышқылы, толық
гидролизденгенде аденин, гуанин, цитозин,
урацил, рибоза және фосфор қышқылына
ыдырайды.
72.
Алтымүшелі бір гетероатомдыгетероциклдердің өкілі – пиридин;
алтымүшелі екі гетероатомды
гетероциклдердің өкілі – пиримидин.
• Пиридин
пиримидин
N1 6 5
N
23 4
N
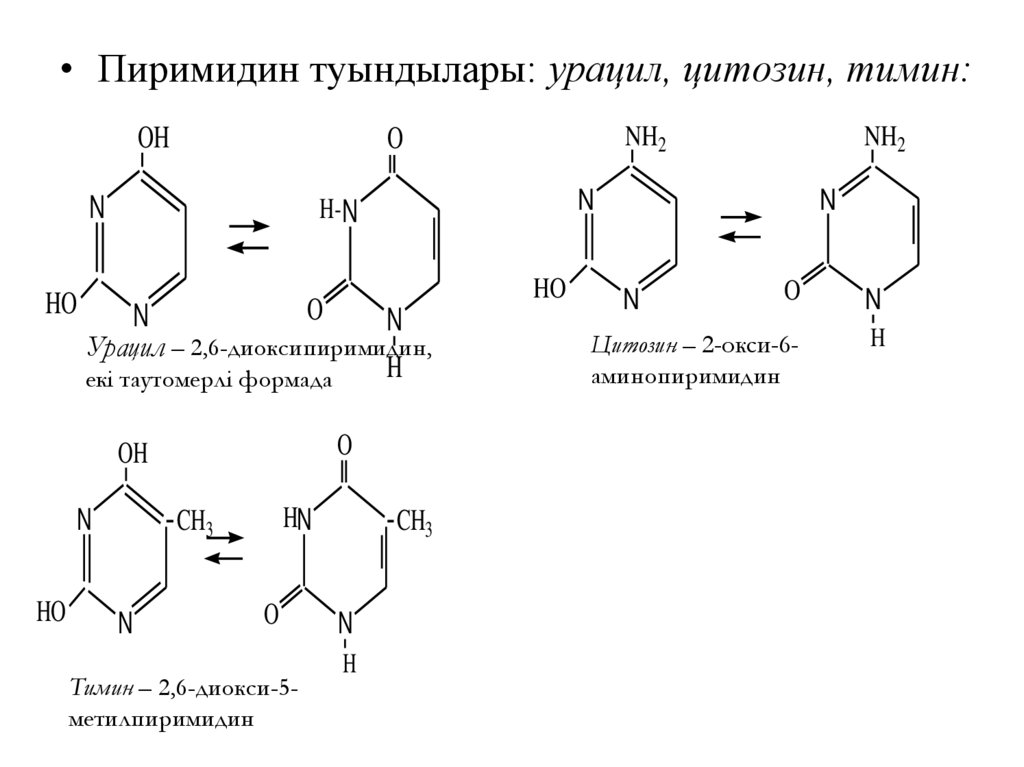
73.
• Пиримидин туындылары: урацил, цитозин, тимин:OH
N
HO
HO
O
N
N
Урацил – 2,6-диоксипиримидин,
H
екі таутомерлі формада
N
O
HN
CH3
N
O
Тимин – 2,6-диокси-5метилпиримидин
CH3
N
H
NH2
N
H- N
OH
HO
NH2
O
N
O
N
Цитозин – 2-окси-6аминопиримидин
H
N
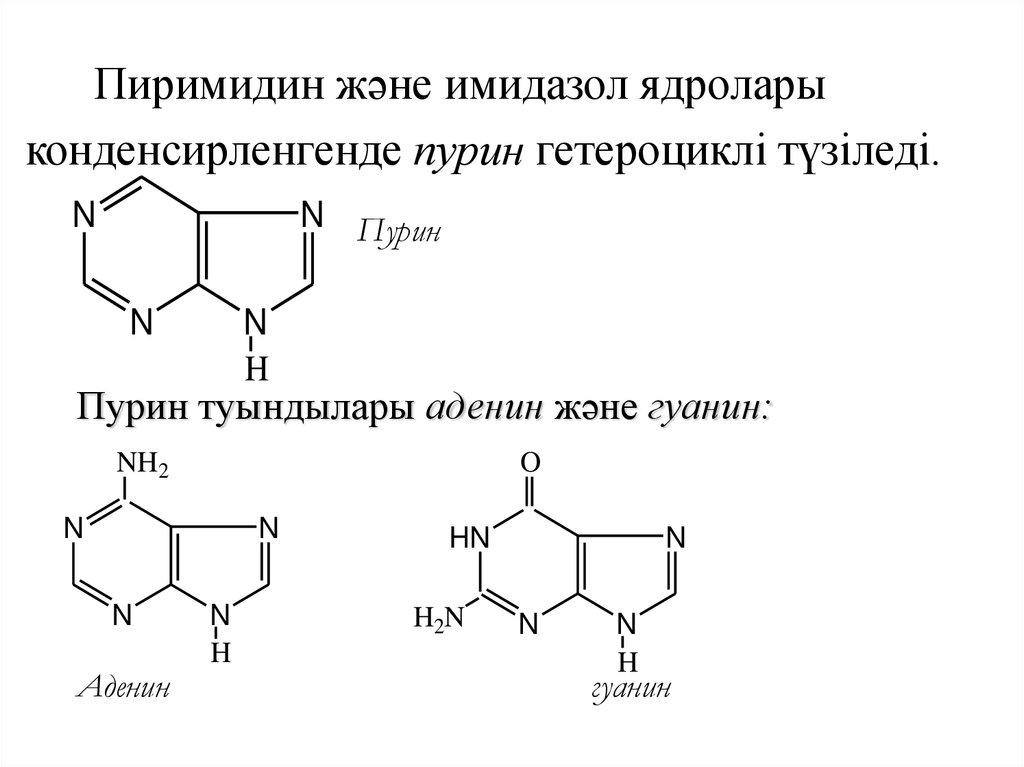
74.
Пиримидин және имидазол ядроларыконденсирленгенде пурин гетероциклі түзіледі.
N
N Пурин
N
N
H
Пурин туындылары аденин және гуанин:
NH2
O
N
N
N
Аденин
N
H
HN
H2N
N
N
N
H
гуанин
75.
ДезоксирибозаРибоза
76.
• Нуклеопротеидтердің гидролизденуі сатылайжүреді және бұл тізбек кез-келген сатыда тоқтауы
мүмкін.
• Азоттық негізді трифосфор қышқылы ағзада
маңызды қызмет атқарады, өйткені олар энергияға
бай макроэргиялық қосылыстар болып табылады.
Макроэргиялық қосылыстардағы, мысалы АТФ
молекуласында, энергия химиялық байланыстағы
үшінші фосфор қышқылының қалдығы мен АТФ
молекуласының қалған бөлігі арасында жинақталған.
Сондықтан мұндай байланыс макроэргиялық
байланыс деп те аталады.
77.
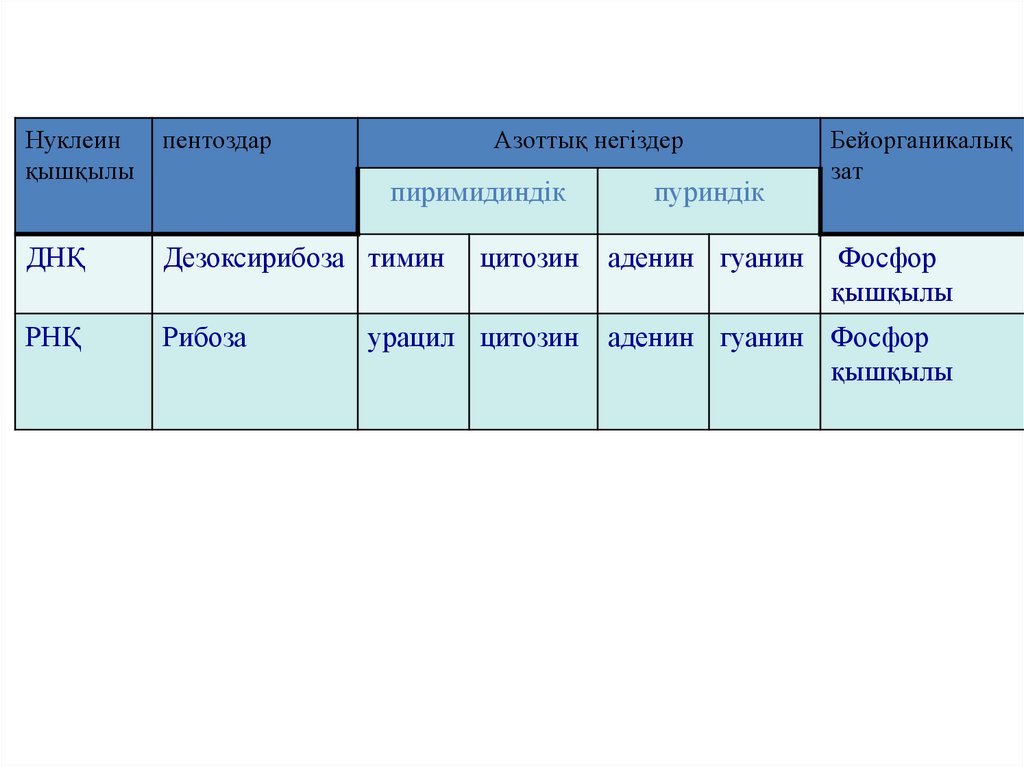
Нуклеинқышқылы
пентоздар
Азоттық негіздер
ДНҚ
Дезоксирибоза тимин
РНҚ
Рибоза
пиримидиндік
цитозин
урацил цитозин
пуриндік
аденин гуанин
Бейорганикалық
зат
Фосфор
қышқылы
аденин гуанин Фосфор
қышқылы
78.
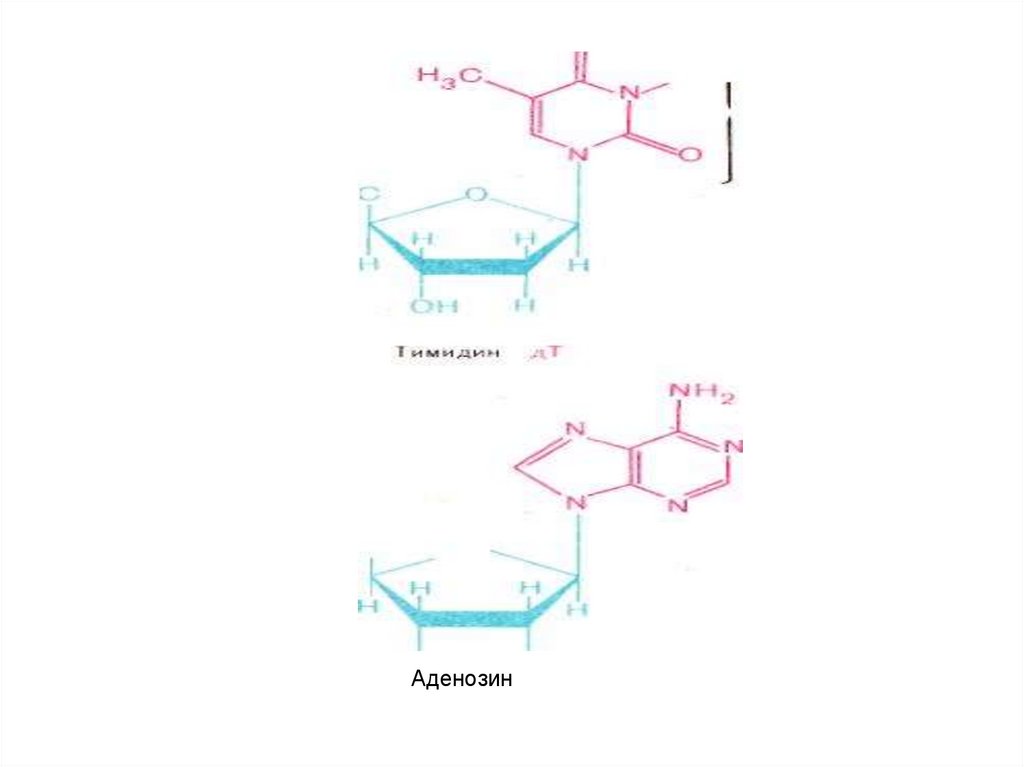
• РНҚ (рибонуклеозидтер) құрамына кіретіннуклеозидтер:
аденил қышқылы (аденозин),
гуанин қышқылы (гуанозин),
цитидил қышқылы (цитидин) т.б.
79.
• Нуклеотидтердің атауы:нуклеин негіздердің тривиалды атауына
сәйкес жалғаулар “идин” пиримидиндік
және “озин”пуринді нуклеозидтерге
жалғанады:
Цитозин+рибоза = цитидин
Цитозин+дезоксирибоза=дезокцитидин
Аденин+Рибоза=аденозин
Аденин+Дезоксирибаза=дезоксиаденозин
80.
Аденозин81.
• Нуклеин қышқылдарының құрамындағымононуклеотидтер бір-бірімен оттектік көпірше
арқылы, яғни пентоздардың гидроксил тобы (-ОН)
(үшінші көміртегінің жанындағы) және келесі
мононуклеотидтің фосфор қышқылының гидроксил
тобының (-ОН) арасынан бір су молекуласының
түзілуі нәтижесінде негізгі байланыс күрделі
эфирлік байланыс,ал пуринді және пиримдинді
негіздер мен пентоздар арасындағы байланыс
N-гликозидтік байланыс деп аталады.
82.
• Нуклеин қышқылдарының бірінші реттікқұрылымы: мононуклеотидтер бір-бірімен
«3́-5́ ́ байланыс» арқылы, мұнда фосфор
қышқылының қалдығы 5 - фосфатты топ пен
екінші соңы 3 -бос- гидроксил тобы, яғни
Оказаки фрагменттері (жапон ғалымы
Оказакидің құрметіне), яғни 3'(ОН) және
5'(ОН) топтарының фосфодиэфирлік
байланыс арқылы ДНҚ-лигаза ферменттерінің
қатысуымен 3'-5' фосфодиэфирлік байланыспен
тізбек құрайды.
83.
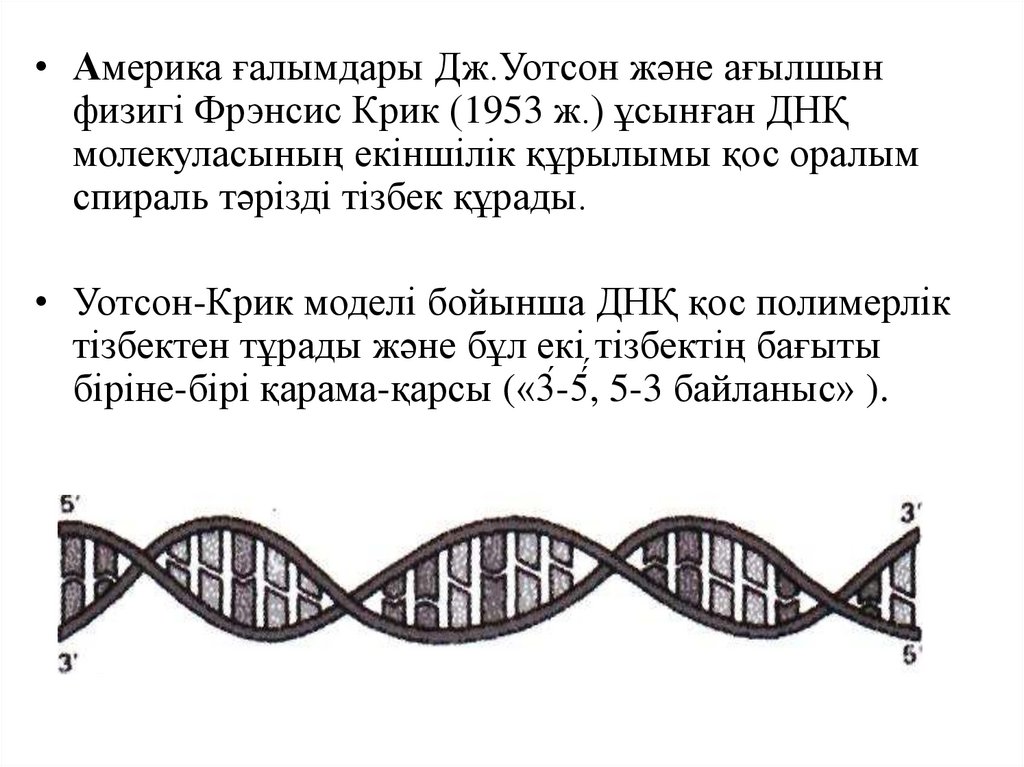
• Америка ғалымдары Дж.Уотсон және ағылшынфизигі Фрэнсис Крик (1953 ж.) ұсынған ДНҚ
молекуласының екіншілік құрылымы қос оралым
спираль тәрізді тізбек құрады.
• Уотсон-Крик моделі бойынша ДНҚ қос полимерлік
тізбектен тұрады және бұл екі тізбектің бағыты
біріне-бірі қарама-қарсы («3́-5́,́ 5-3 байланыс» ).
84.
• ДНҚ-ның екінші реттік құрылымында молекулаоралым спираль тәрізді тізбек құрады.
• ДНҚның екіншілік құрылымында пуриндік негіз
міндетті түрде белгілі бір пириминдік негізбен
қосылады.
Аденин-тимин,гуанин- цитозин;
• Нуклнотидтердің өзара қатынасы: адениннің саны
тиминнің санына, гуаниннің саны цитозиннің санына
тең:
А= T, Г=Ц
• Аденин мен цитозиннің жалпы саны гуанинмен
тиминнің жалпы санына тең:
А+Ц=Г+Т
• Комплементарлы жұп аденин мен тиминнің арасында
екі сутектік (=) байланыс,ал цитозин мен гуаниннің
арасында үш (=)сутектік байланыс түзіледі
85.
86.
• Бір тізбектегі нуклеотидтің орналасуы өз бетінменеркінірек болғанымен, екінші тізбектегі
нуклеотидтердің орны бірінші тізбектің нуклеотидтік
құрамына тәуелді болып келеді.
• ДНҚ тізбегіндегі нуклеотидтер біріне-бірі
комплементарлық принципке (Чаргафф ережесі
бойынша) негізделген:
• Адениннің саны тиминнің санына, гуаниннің саны
цитозиннің санына тең:
А = Т, Г = Ц.
• Аденин мен цитозиннің жалпы саны гуанин мен
тиминнің жалпы санына тең:
А + Ц = Г + Т.
87.
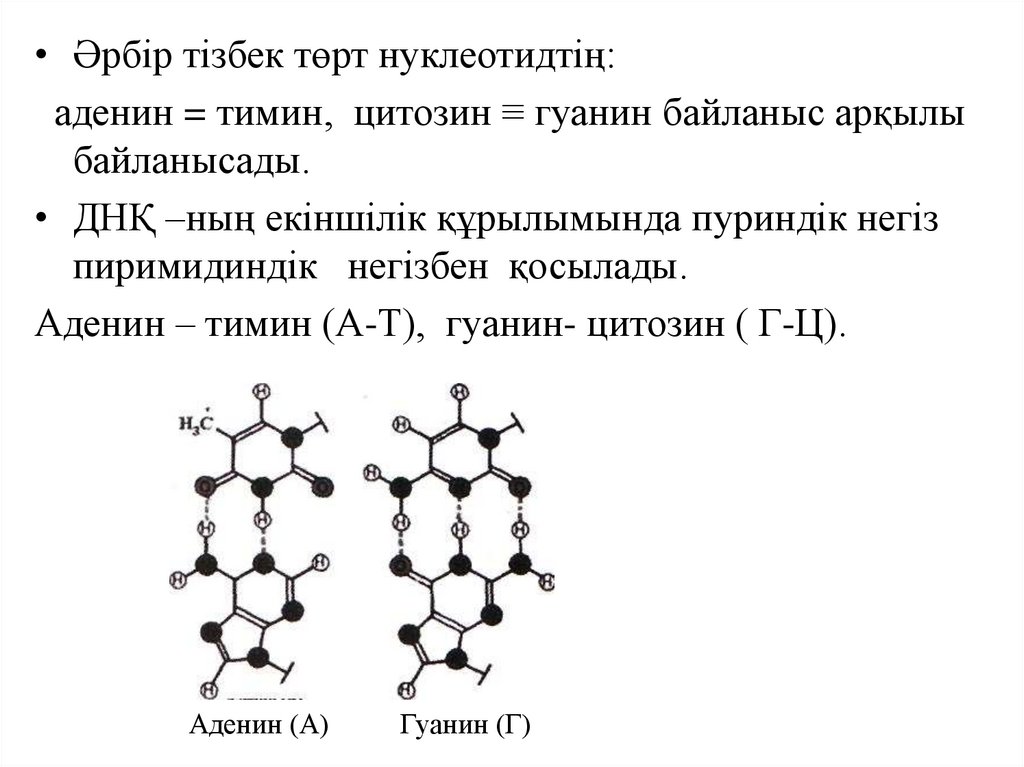
• Әрбір тізбек төрт нуклеотидтің:аденин = тимин, цитозин ≡ гуанин байланыс арқылы
байланысады.
• ДНҚ –ның екіншілік құрылымында пуриндік негіз
пиримидиндік негізбен қосылады.
Аденин – тимин (А-Т), гуанин- цитозин ( Г-Ц).
Аденин (А)
Гуанин (Г)
88.
89.
• ДНҚ синтезіне қатысатын негізгі фермент ДНҚ-на тәуелді ДНҚ полимераза.• ДНҚ молекуласының синтезіне қажетті негізгі
компоненттер:
1. Субстрат есебінде дезокси- қатарын жататын төрт
трифосфо-нуклеотидтер (d - АТФ, d - ГТФ, d ЦТФ. d – ТТФ).
2. Ферменттің оптималды белсенділігі үшін Mg2+
қатысуы кажет.
3. Аналық ДНҚ-ның болуы міндетті, себебі
генетикалық акпараттың көзі қажет.
4. Нуклеотидтердің біріне-бірі қосылу бағыты 5'
3' бойынша жүреді.
90.
• ДНҚ синтезіне қатысатын ферменттер:• 1. ДНҚ-на тәуелді ДНҚ-полимеразасы (I, П, III). III ДНҚполимеразасы элонгацияға тікелей қатысатын фермент.
• 2. ДНҚ-полимераза өз бетінше синтезді бастай алмайды,
сондықтан ДНҚ-праймаза ферменті праймерлерді түзуге
көмектеседі, ал III ДНҚ полимеразасы әрі қарай тізбектің
өсуіне мүмкіндік береді.
• 3. Гираза- қос тізбектің бір-бірінен ажырауын, ал хеликаза
ферменті қос тізбектегі сутектік байланыстардың бірбірінен ажырауын қамтамасыз етеді.
• 4. ДНҚ-ның лигазасы үзіктерді өзара жалғастырады. Бұл
Оказаки фрагменттері (жапон ғалымы Оказакидің
құрметіне), яғни 3'(ОН) және 5'(ОН) топтарының
бірімен-бірін фосфодиэфирлік байланыс арқылы ДНҚлигаза ферменттерінің қатысуымен тізбек құрайды.
• 5. 20-ға жуық ақуыздық факторлар қажет.
91.
• ДНҚ-ның биосинтезі үш кезеңнен түрады:• 1. Инициация. ДНҚ-на тәуелді РНҚ-полимеразасы жұмыс істейді,
сннтездің басы. ДНҚ-ны екі түрлі қызмет атқарады: 1) матрицалық
(арқаулық), 2) ұйытқы (затравка).
• ДНҚ-полимеразасы ДНҚ-ның басы болып табылатын тізбектің
нуклеотидінің З'-OH тобына нуклеотидтердің қосылуына мүмкіндік
береді, сондықтан синтездің бағыты 5'—»3'-ке қарай бағытталған
болады.
• II. Элонгация. Комплементарлы жұптардың репликациясы жеке-жеке
фрагменттердің 5' 3' бағытында түзілуі, осы фрагментердің ДНҚ-лигаза
ферменттерінің қатысуымен бірімен-бірінің қосылуы.
• III. Терминация. Синтездің аяқталуы. Арқаулық ДНҚ-ның толық
жұмсалуына сәйкес полимерлік реакцияның аяқталуы.
• ДНҚ синтезі РНҚ матрицасында да жүруі мүмкін. Оған ревертаза
(америка ғалымдары Бальтимор, Темин, 1974 ж. рак ауруын туғызатын
вирустан тапқан) ферменті қатысады. Рефертаза ДНҚ синтезін РНҚматрицада жүргізетін фермент, демек РНҚ-нан ақпараттың ДНҚ-ға өтуі
қайтымды үрдіс болғаны.
92. ҚОРЫТЫНДЫ
• Белок биосинтезі тіршіліктің ең маңызды қасиеттерінің бірі, себебітіршілік процесінде белок молекулалары әртүрлі биохимиялық
реакцияларға түсіп ыдырап жойылып отырады, ал олардың орнын
толтыру тек жаңа белок молекулаларының синтезделуі нәтижесінде
жүзеге асады. Мұнда ДНҚ, РНҚ, АТФ және белоктардың қызметі
бірігеді.
• Көмірсулар (моносахаридтер – қарапайым қанттар,
гидролизденбейді, бұлар глюкоза, фруктоза; дисахаридтер-әр
молекуласы 2 моносахаридтерден тұрады: сахароза, лактоза;
полисахаридтер - өте күрделі заттар: крахмал, клетчатка) табиғатта
өте көп таралған, оның адам өмірінде маңызы өте зор. Организмге
қажет қуаттың (энергия) көбі көмірсулар арқылы жүреді.
• Нуклеин қышқылы - пішіні жіп тәрізді, жоғарғы молекулалы,
ерітінділерінің тұтқырлығы жоғары қосылыс. Нуклеин қышқылдары нуклеотид полимерлерінен құралған. Нуклеотидтердің химиялық
құрамы - пиримидиндік немесе пуриндік негіздер, пентоз, фосфор
қышқылының қалдығы.
93. Пайдаланылған әдебиеттер
• Тұртабаев С. Қ. және т.б. Биохимия негіздері: Оқулық./С. Қ. Тұртабаев, А. К. Кабдрахимова, А. Ж. Еримова/
Биология мамандықтарының студенттеріне арналған. –
Алматы: ЖШС РПБК «Дәуір», 2012. – 336 б.
• Сеитов З.С. Биологиялық химия. – Алматы, 1992
• Сейтмбетова А.Ж., Лиходий С.С. Биологиялық химия. –
Алматы: Білім, 1994 – 304 б.
• Сеитов З.С. Биохимия. – Алматы: Агроуниверситет,
2000. – 897 с.
• С. Ж. Стамбеков, В. Л. Петухов. Молекулалық биология.
Новосибирск-2003г.
• Н. Кенесарина. Өсімдіктер физиологиясы және
биохимия негіздері. Алматы «Мектеп»-1988ж.




























































 medicine
medicine








