Similar presentations:
Аминокислоты и белки
1. Аминокислоты и белки
Спирали встречаются во многихобластях:
в архитектуре, в макромолекулах
белков, нуклеиновых кислот и даже в
полисахаридах
1
2. Аминокислоты
Соединение, которое содержитодновременно и кислотную
функциональную группу, и аминогруппу,
является аминокислотой
H2N CH COOH
R
2
3.
НазваниеСокращение
Структурная формула
Глицин ЕГЭ!!!
gly
H2NCH2COOH
Аланин ЕГЭ!!!
ala
CH3CHCOOH
NH2
Валин
Лейцин
val
(CH3)2CHCHCOOH
leu
NH2
(CH3)2CHCH2CHCOOH
NH2
NH
Пролин
pro
Фенилаланин
phe
COOH
C6H5CH2CHCOOH
NH2
Триптофан
try
C6H5CH2CHCOOH
NH2
3
4.
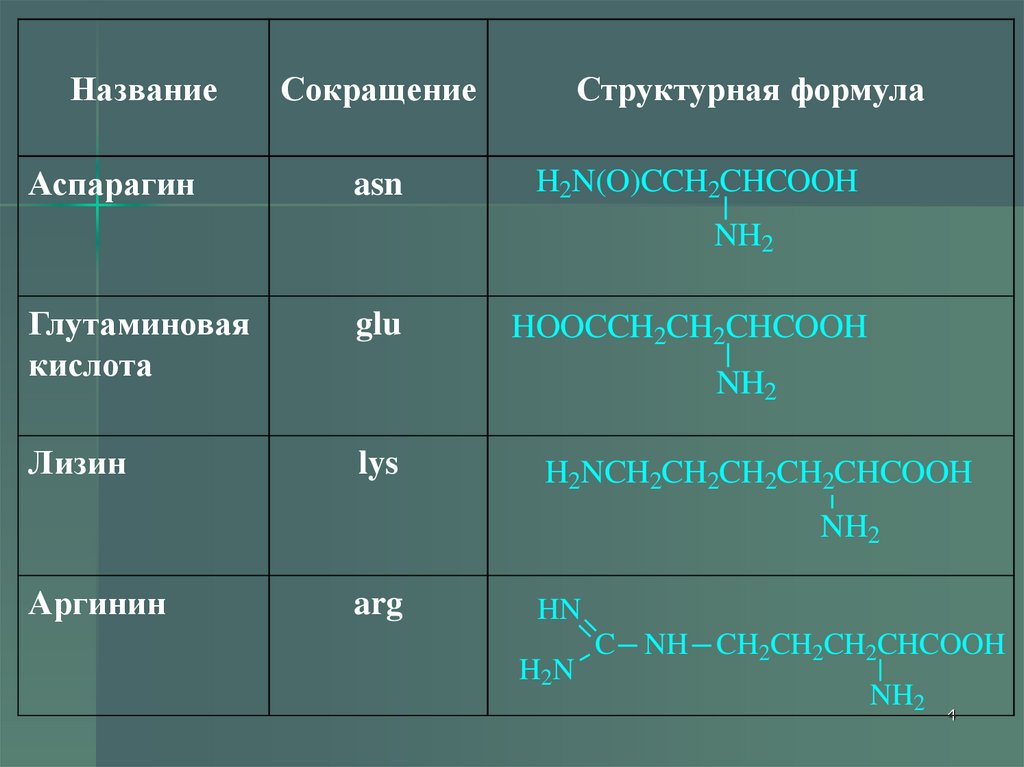
НазваниеАспарагин
Сокращение
asn
Структурная формула
H2N(O)CCH2CHCOOH
NH2
Глутаминовая
кислота
glu
Лизин
lys
HOOCCH2CH2CHCOOH
NH2
H2NCH2CH2CH2CH2CHCOOH
NH2
Аргинин
arg
HN
H2N
C NH CH2CH2CH2CHCOOH
NH2
4
5.
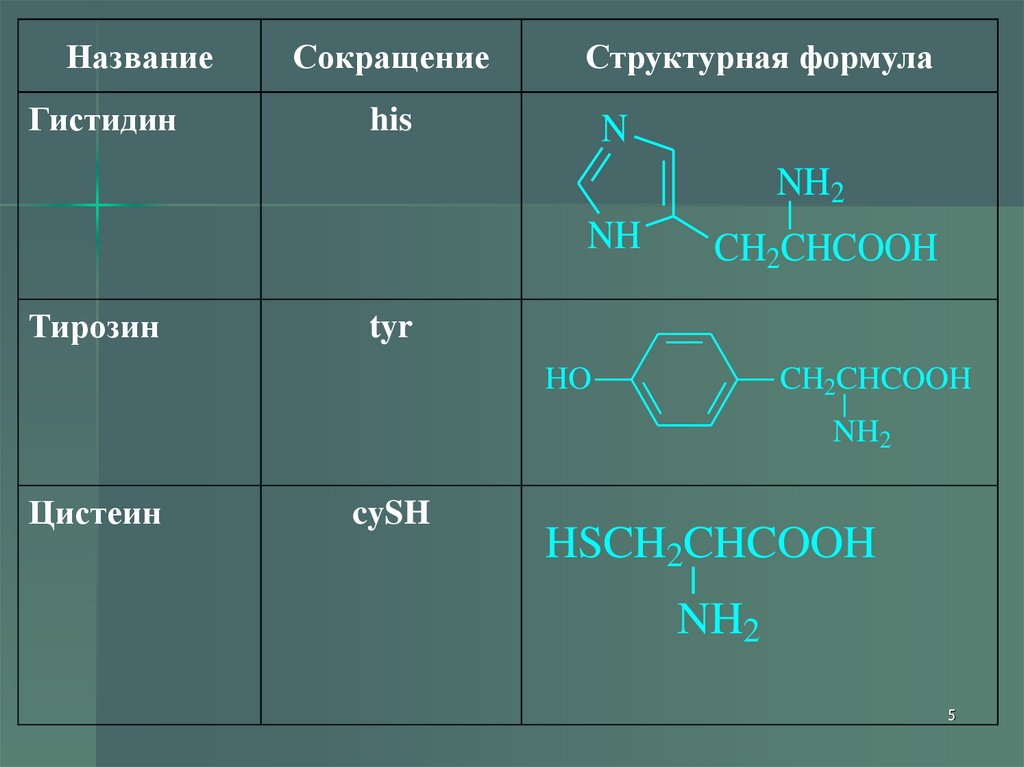
НазваниеГистидин
Сокращение
Структурная формула
his
N
NH2
NH
Тирозин
CH2CHCOOH
tyr
HO
CH2CHCOOH
NH2
Цистеин
cySH
HSCH2CHCOOH
NH2
5
6. Незаменимые аминокислоты
Незаменимыми называютсяаминокислоты, которые не могут
быть синтезированы организмом из
веществ, поступающих с пищей, в
количествах, достаточных для того,
чтобы удовлетворить
физиологические потребности
организма.
6
7. Незаменимые аминокислоты
Следующие аминокислоты принятосчитать незаменимыми для
организма человека:
изолейцин, лейцин, лизин,
метионин, фенилаланин,
треонин, триптофан и валин,
гистидин (для детей)
7
8. Кислотно-основные свойства
H 2NCH
COO
-
H+
OH
-
H 3N
R
щелочной раствор
CH
COO
+
- H
R
H2N
CH
OH-
H 3N
CH
COOH
R
COOH
кислый раствор
R
8
9. Способы получения аминокислот Аминирование -галогензамещенных кислот
Способы получения аминокислотАминирование -галогензамещенных кислот
RCH2COOH + Br2
PBr3
1) NH3 (изб.)
RCHCOOH 2) разб. кисл.
Br
RCHCOOH
NH2
9
10. Пептиды
Пептиды — соединения,построенные из нескольких
остатков -аминокислот,
связанных амидной (пептидной)
связью.
O
Ñ
NH
10
11. Пептиды
OH2N
CH
O
C
OH + H
NH
R
CH
O
C
OH + H
NH
R'
CH
C
OH
R''
Пептидная группа
O
-2H2O
H 2N
CH
R
N-конец
C
O
NH
CH
C
R'
Пептидная связь
NH
CH
COOH
R''
C-конец
11
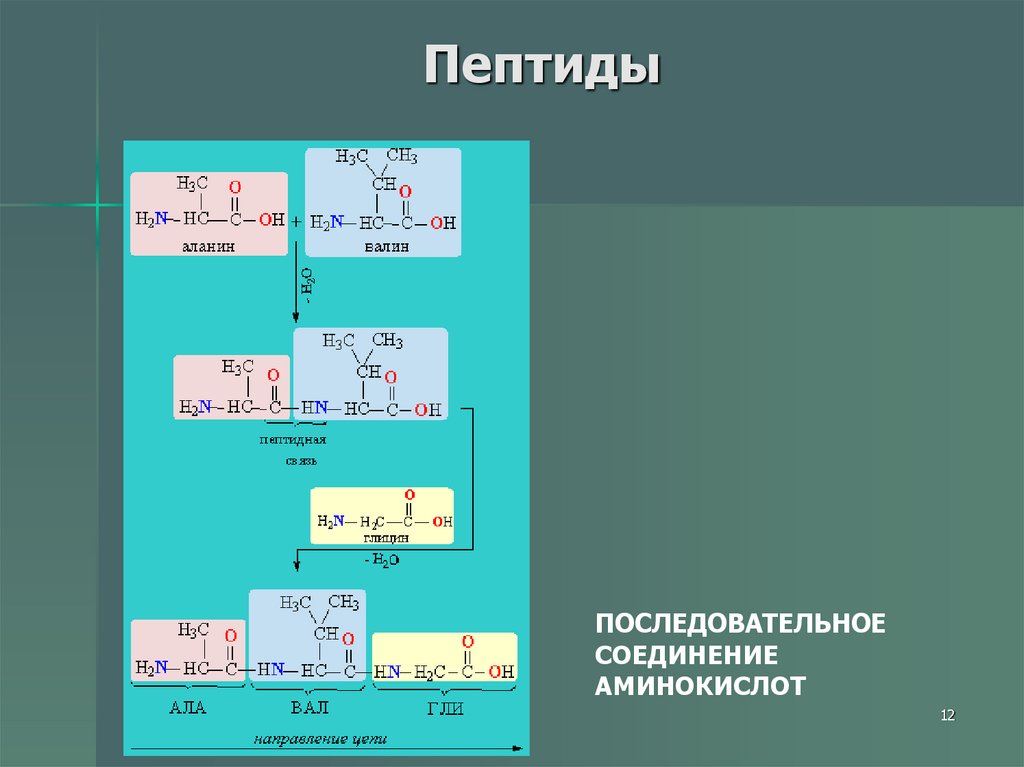
12. Пептиды
ПОСЛЕДОВАТЕЛЬНОЕСОЕДИНЕНИЕ
АМИНОКИСЛОТ
12
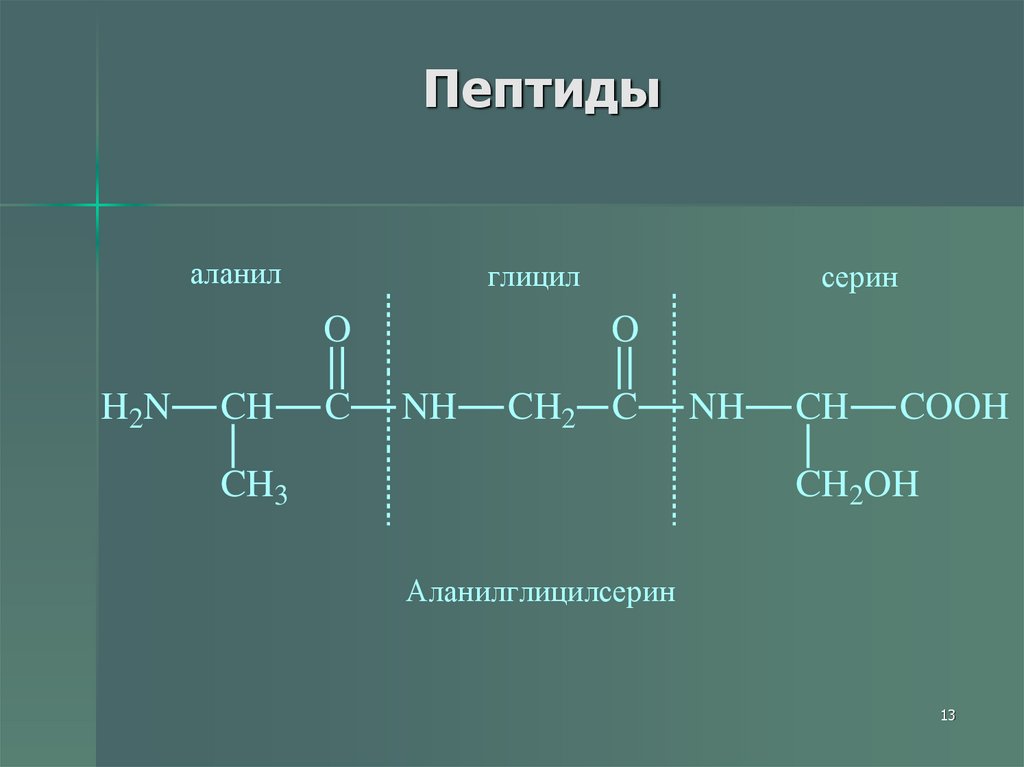
13. Пептиды
аланилглицил
O
O
H2N
CH
C
серин
NH
CH2 C
NH
CH
COOH
CH2OH
CH3
Аланилглицилсерин
13
14. Белки
Белки – это биоорганическиеполимеры, образованные
аминокислотами; имеют
строго определённые
элементный состав и
пространственную структуру.
14
15. Белки
1516. Белки: структура
Первичная структура пептидов ибелков — это последовательность
аминокислотных остатков в
полипептидной цепи.
16
17. Белки: структура
Первичная структура белка инсулина.17
18. Белки: структура
Вторичная структура белка — этоболее высокий уровень структурной
организации, в котором закрепление
конформации происходит за счет
водородных связей между пептидными
группами.
18
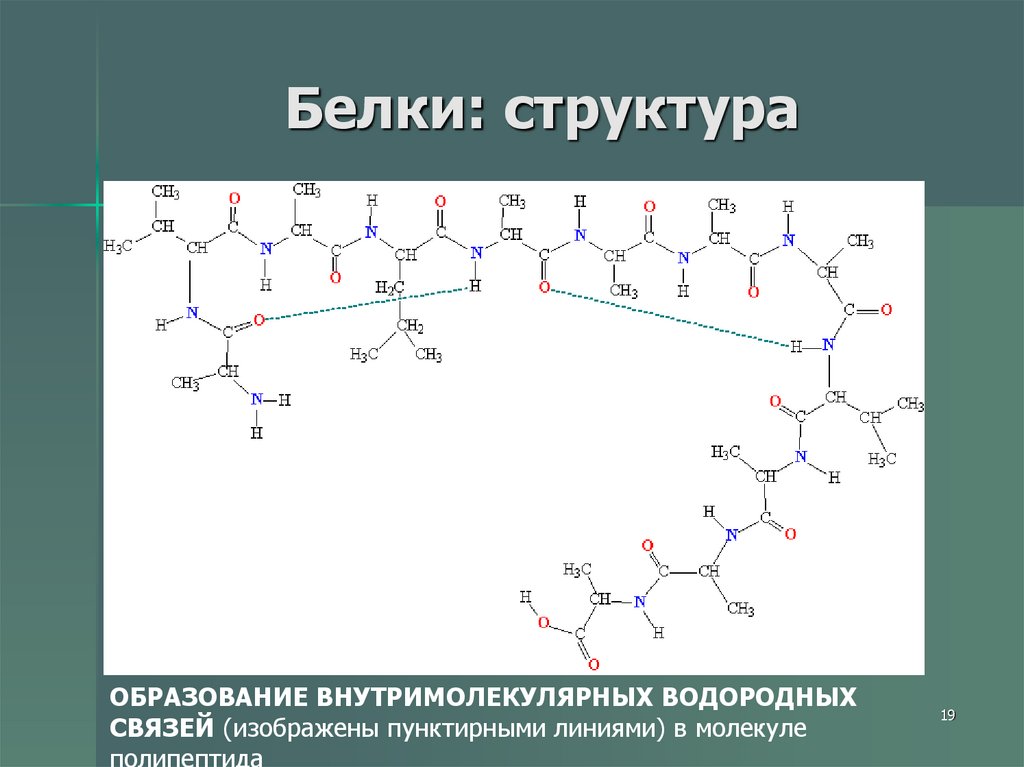
19. Белки: структура
ОБРАЗОВАНИЕ ВНУТРИМОЛЕКУЛЯРНЫХ ВОДОРОДНЫХСВЯЗЕЙ (изображены пунктирными линиями) в молекуле
полипептида
19
20. Белки: структура
-спиральмолекулы белка
20
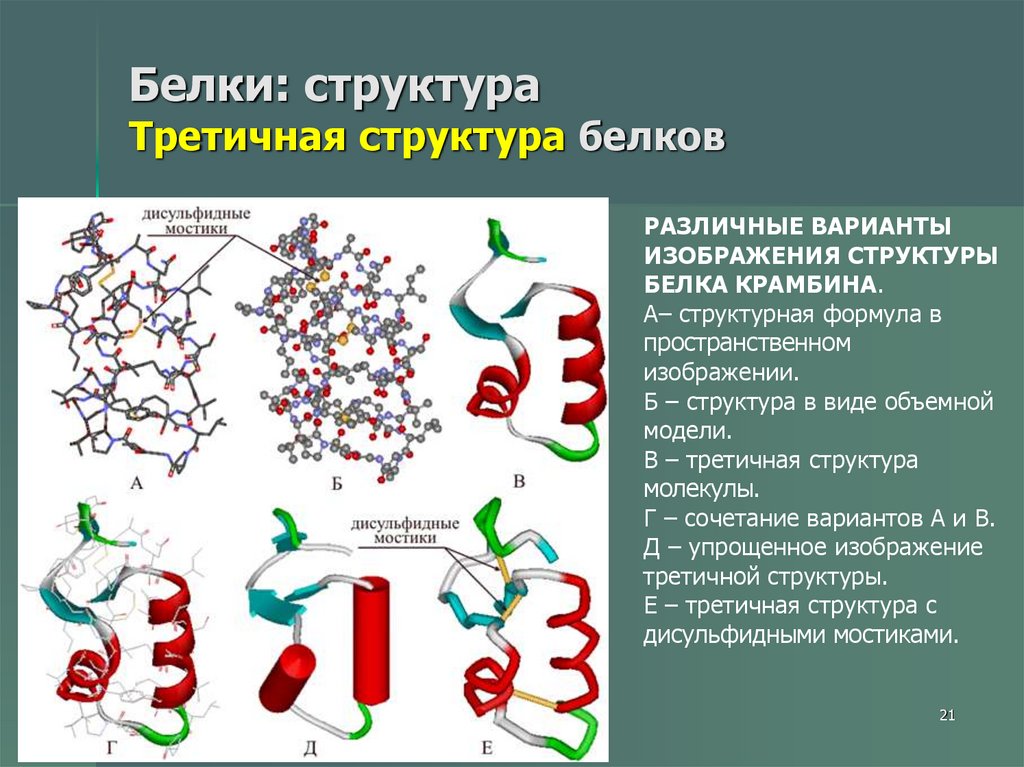
21. Белки: структура Третичная структура белков
РАЗЛИЧНЫЕ ВАРИАНТЫИЗОБРАЖЕНИЯ СТРУКТУРЫ
БЕЛКА КРАМБИНА.
А– структурная формула в
пространственном
изображении.
Б – структура в виде объемной
модели.
В – третичная структура
молекулы.
Г – сочетание вариантов А и В.
Д – упрощенное изображение
третичной структуры.
Е – третичная структура с
дисульфидными мостиками.
21
22. Белки: структура Глобулярные белки
ГЛОБУЛЯРНАЯСТРУКТУРА
АЛЬБУМИНА (белок
куриного яйца). В
структуре помимо
дисульфидных мостиков
присутствуют свободные
сульфгидридные HSгруппы цистеина, которые
в процессе разложения
белка легко образуют
сероводород – источник
запаха тухлых яиц.
Дисульфидные мостики
намного более устойчивы
и при разложении белка
сероводород не образуют
22
23. Белки: структура Фибриллярные белки
ФИБРИЛЛЯРНЫЙ БЕЛОК ФИБРОИН – основной компонентнатурального шелка и паутины
23
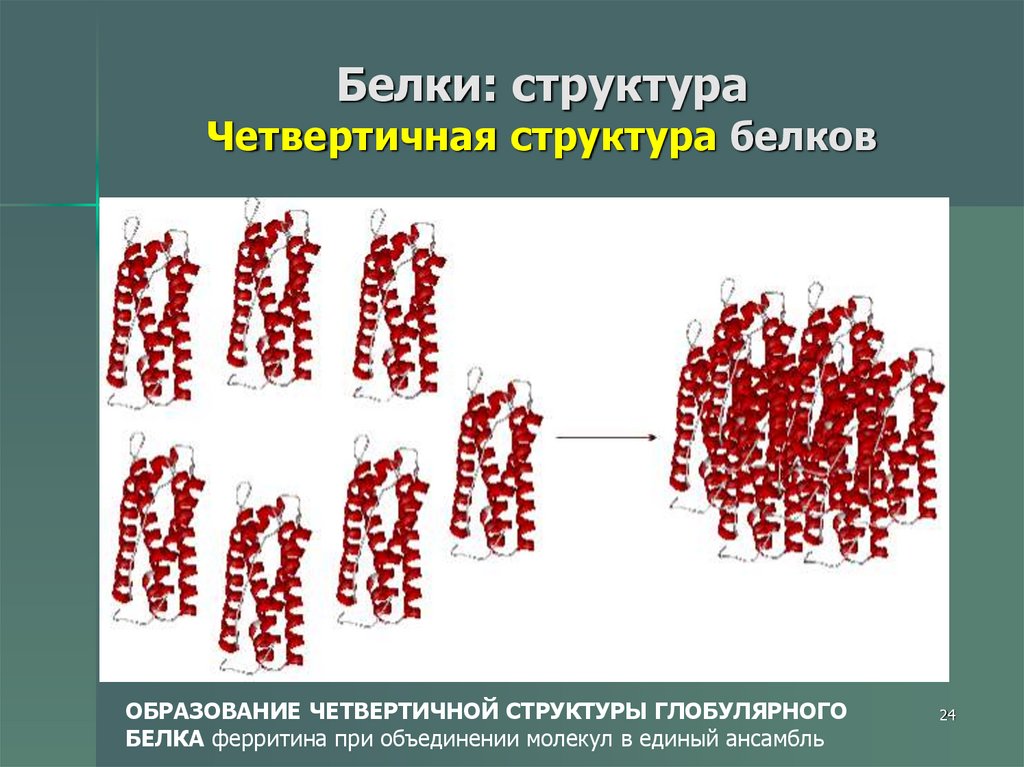
24. Белки: структура Четвертичная структура белков
ОБРАЗОВАНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ ГЛОБУЛЯРНОГОБЕЛКА ферритина при объединении молекул в единый ансамбль
24
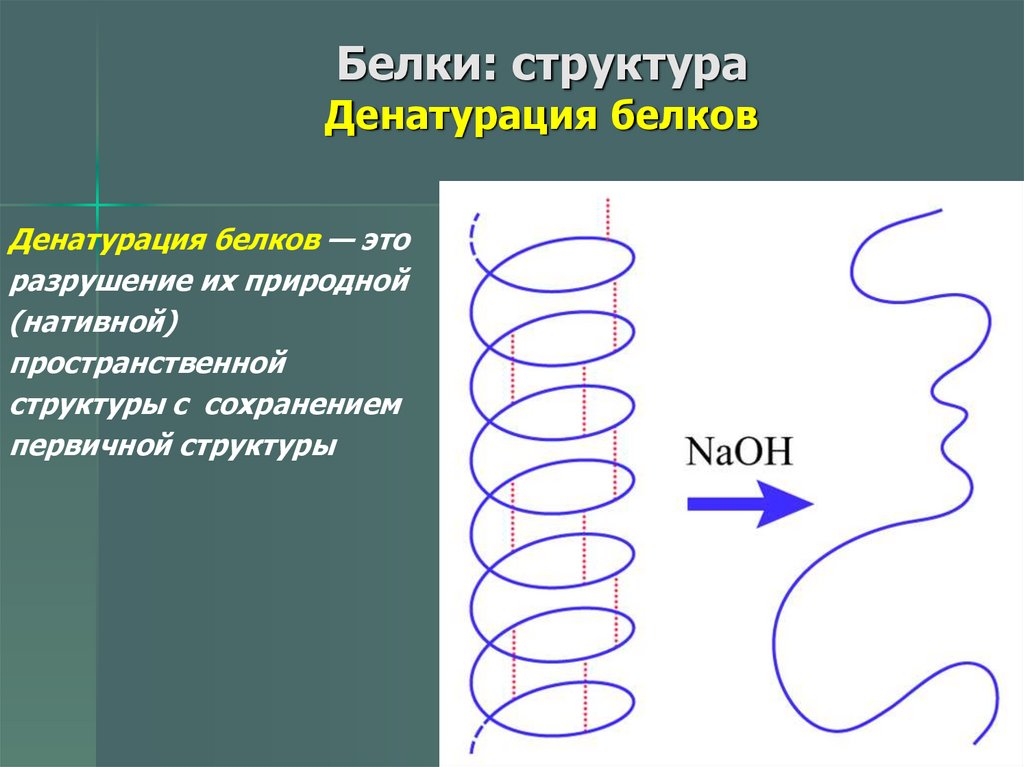
25. Белки: структура Денатурация белков
Денатурация белков — эторазрушение их природной
(нативной)
пространственной
структуры с сохранением
первичной структуры
25




















 chemistry
chemistry








