Similar presentations:
Соли. Определение солей
1. Соли
Химия8 класс
И. Жикина
2. Определение солей
Мех(КО)уСульфат
натрия
Na2SO4
КО - кислотный
остаток
CaCl2
Хлорид
кальция
Na2SO4 2Na+ +SO42CaCl2 Ca2+ + 2ClСоли – сложные вещества, состоящие из катионов
металла и анионов кислотного остатка
3. Классификация солей
СредниеОсновные
Кислые
КHCO3
Na2SO3
Сульфит
натрия
Гидрокарбонат
калия
Н - гидро
Mg(OH)Cl
Гидроксохлорид
магния
Кислотный
остаток
ОН - гидроксо
4. Химические свойства солей
Растворимыесоли
Сильные
электролиты
Полностью
распадаются
на ионы
Растворы
солей
проводят ток
5.
Электролитырастворимые
Кислоты
Соли
Основания
Реакции в растворах электролитов
протекают между ионами
Признак
реакции
•Осадок
•Газ
•Вода
6.
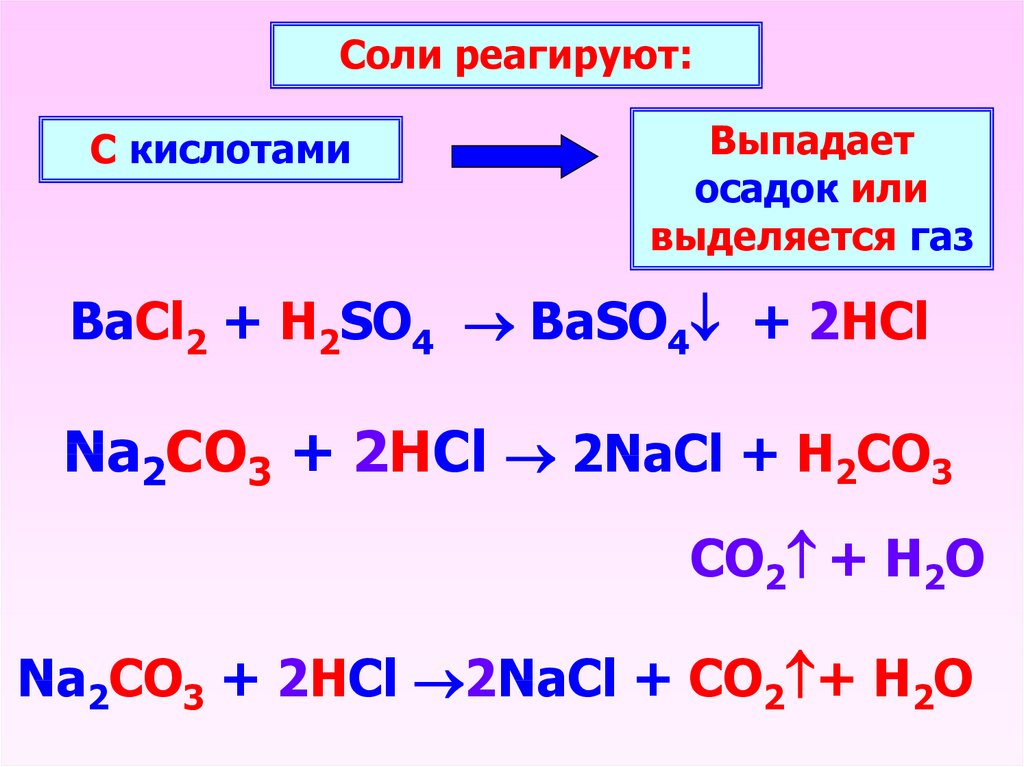
Соли реагируют:С кислотами
Выпадает
осадок или
выделяется газ
BaCl2 + H2SO4 BaSO4 + 2HCl
Na2CO3 + 2HCl 2NaCl + H2CO3
CO2 + H2O
Na2CO3 + 2HCl 2NaCl + CO2 + H2O
7.
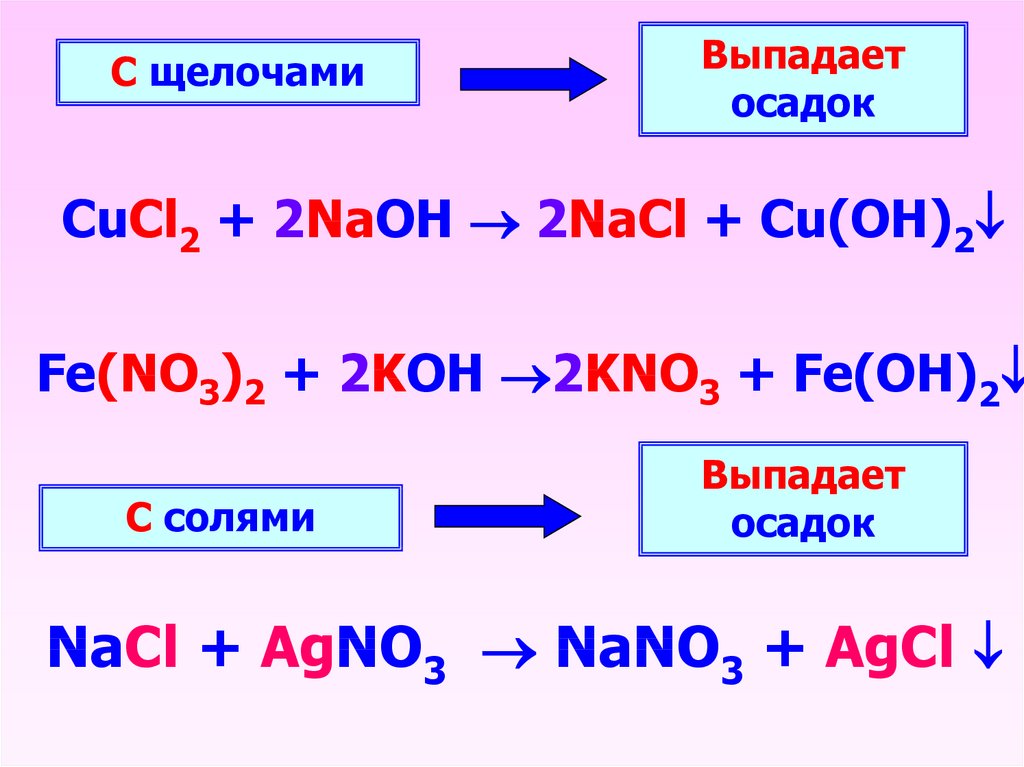
С щелочамиВыпадает
осадок
CuCl2 + 2NaOH 2NaCl + Cu(OH)2
Fe(NO3)2 + 2KOH 2KNO3 + Fe(OH)2
С солями
Выпадает
осадок
NaCl + AgNO3 NaNO3 + AgCl
8.
9. pH растворов солей
КислаяНейтральная
рН < 7
красный
рН = 7
фиолетовый
Щелочная
рН > 7
синий
Лакмус
бесцветный
малиновый
Фенолфталеин
розовый
Метилоранж
оранжевый
желтый
10.
Универсальный индикаторСильно
кислая
Слабо
кислая
Слабо
щелочная
Сильно
щелочная
Нейтральная
Усиление
кислотности среды
Усиление
основности среды
11.
12. Соль сильного основания и сильной кислоты
K2SO4KOH
рН = 7
H2SO4
BaCl2
Ba(OH)2
HCl
Сильное основание + сильная кислота
Полная нейтрализация
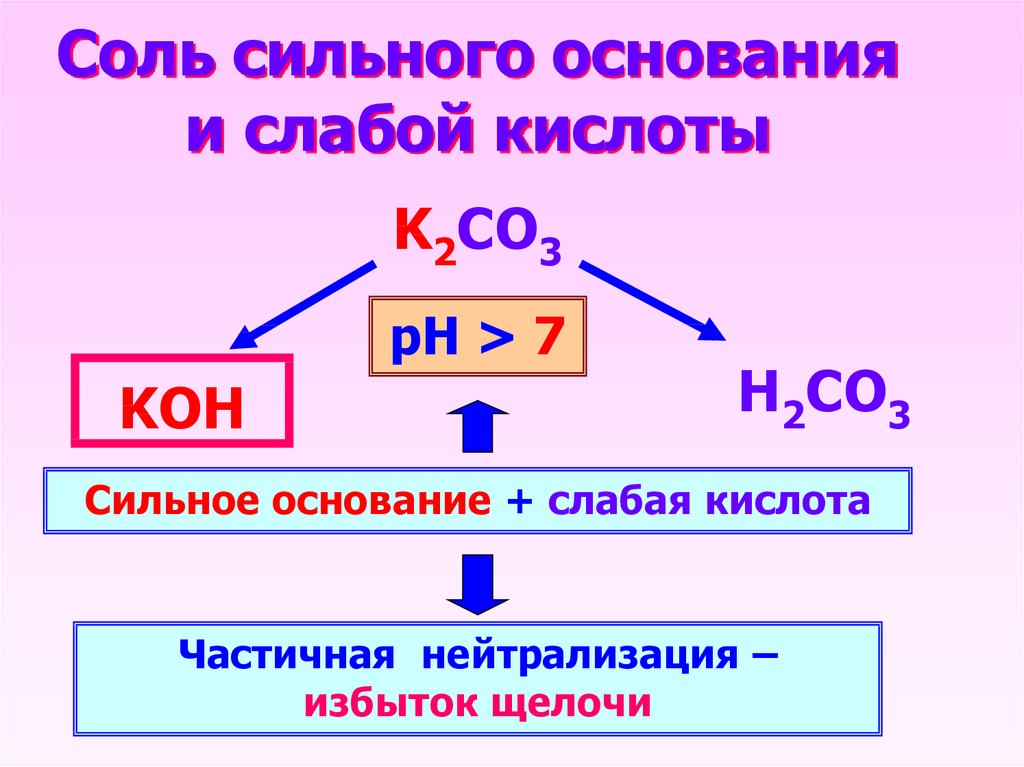
13. Соль сильного основания и слабой кислоты
K2CO3рН > 7
KОН
Н2CO3
Сильное основание + слабая кислота
Частичная нейтрализация –
избыток щелочи
14. Соль слабого основания и сильной кислоты
Al(NO3)3рН < 7
Al(OН)3
НNO3
Слабое основание + сильная кислота
Частичная нейтрализация –
избыток кислоты
15.
ОксидыОсновные
Кислотные
Кислоты
Бескислородные
Кислородсодержащие
Сложные
вещества
Щелочи
Основания
Нерастворимые
Кислые
Соли
Средние
Основные
16. Генетическая связь между классами неорганических соединений
Генетическая связь между классаминеорганических соединений
17. Примеры
1. Металл + неметалл сольHg + S HgS
2Al + 3I2 2AlI3
2. Основной оксид + кислотный оксид соль
Li2O + CO2 Li2CO3
CaO + SiO2 CaSiO3
18.
2. Основание + кислота сольCu(OH)2 + 2HCl CuCl2 + 2H2O
Fe(OH)2 + H2SO4 FeSO4 + 2H2O
KOH + HNO3 KNO3 + H2O
Нейтрализация
19.
металл основной оксид4Li + O2 2Li2O
основной оксид основание
Li2O + H2O 2LiOH
металл основной оксид основание соль
Генетический ряд металла
20.
неметалл кислотный оксидS + O2 SO2
кислотный оксид кислота
SO3 + H2O H2SO4
неметалл кислотный кислота соль
Генетический ряд неметалла















 chemistry
chemistry








