Similar presentations:
Основания, кислоты, соли в свете ТЭД
1.
Основания, кислоты ,соли
в свете ТЭД.
2. Электролитическая диссоциация
процессраспада электролита на ионы
3.
Теорияэлектролитической диссоциации
( С. Аррениус, 1887 г.) – веществаэлектролиты в растворах распадаются на
ионы.
Вещества-электролиты, которые
проводят электрический ток
4. Электролиты и неэлектролиты
Сильныеэлектролиты – при растворении
полностью распадаются на ионы
(растворимые соли, сильные кислоты,
щелочи)
Слабые электролиты – незначительно
диссоциируют на ионы (слабые кислоты,
нерастворимые основания и гидроксид
амония NH4OH, малорастворимые соли)
Неэлектролиты – не распадаются на ионы
(простые вещества, нерастворимые оксиды,
большинство органических веществ)
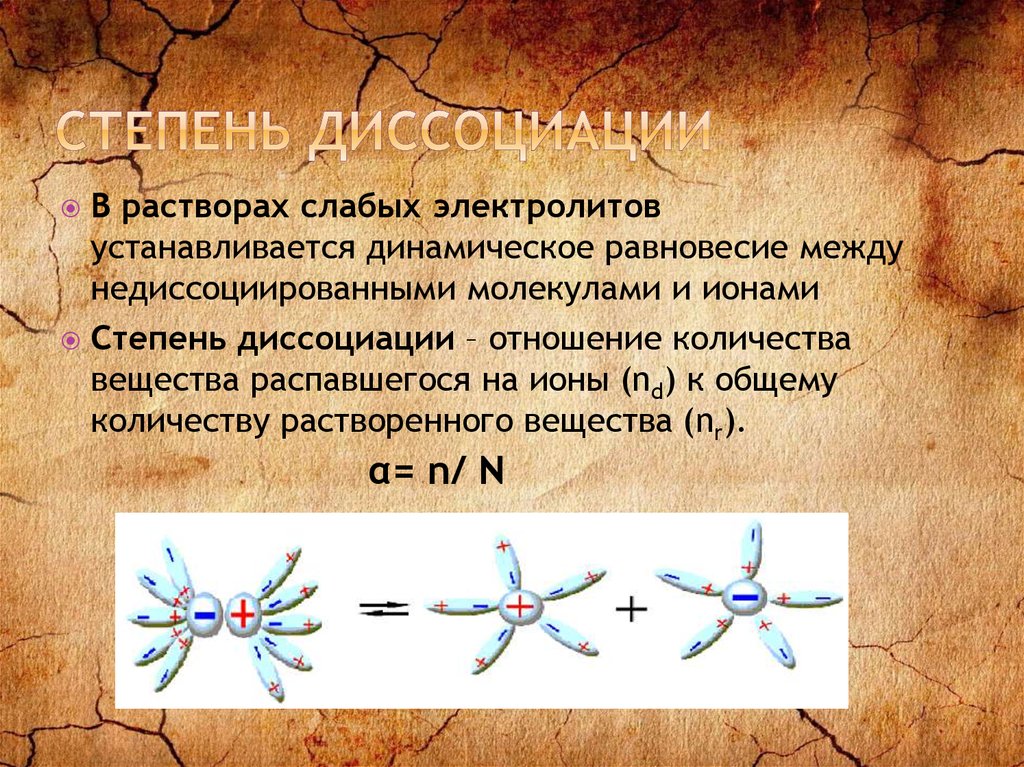
5. степень диссоциации
В растворах слабых электролитовустанавливается динамическое равновесие между
недиссоциированными молекулами и ионами
Степень диссоциации – отношение количества
вещества распавшегося на ионы (nd) к общему
количеству растворенного вещества (nr).
α= n/ N
6. Константа диссоциации
– показываетотношение концентрации ионов к
концентрации недиссоциированных молекул
Константа
1.
2.
3.
диссоциации зависит от:
Природы (силы)электролита
Температуры
Концентрации
Видеотека:
Электролиты
Влияние температуры на диссоциацию
Влияние концентрации на диссоциацию
7. Основные положения ТЭД
Электролитыпри растворении
гидратируются и распадаются на ионы
(катионы+ и анионы-).
Под действием электрического тока
катионы+ движутся к катоду(-), анионыдвижутся к аноду(+).
Диссоциация это обратимый процесс:
наряду с распадом вещества на ионы идет
процесс обратной ассоциации в молекулы
и кристаллы.
8. Основания в свете ТЭД
Основанияминазываются вещества, в которых
атомы металла связаны с гидроксильными
группами Me(ОН)n
Основания
- электролиты, при диссоциации
которых в качестве анионов образуются
только гидроксид-ионы.
KOH
K+ + OH—
NH4OH
NH+4 + OH—
9. Виды оснований
1. Щелочи - растворимые в воде основания(гидроксиды металлов I и II групп).
Кристаллические вещества, устойчивы к
разложению.
2. Нерастворимые и малорастворимые основания
(большинство оснований ,гидроксиды металлов
побочных подгрупп: Cu(OH)2, Fe(OH) 3 и др.
Твердые вещества, легко разлагаются на оксид и
воду:
Cu(OH)2 CuO + H2 О
10. Кислотность оснований
Кислотность основания определяется числомгидроксильных групп (равно количеству молекул
кислоты, необходимой для нейтрализации).
NН4ОН — однокислотное основание,
Са(ОН)2 — двухкислотное,
Fе(ОН)3 — трехкислотное (многокислотное)
Двух и многокислотные основания
диссоциируют ступенчато:
Ca(ОН)2
Са(ОН)+ + OH— (первая ступень)
Ca(OH)+
Ca2++OH— (вторая ступень)
Константа диссоциации второй и третьей
ступени значительно ниже первой.
11. Сильные и слабые основания
Сильные основанияСлабые основания
NaOH гидроксид натрия
(едкий натр)
KOH гидроксид калия
(едкое кали)
LiOH гидроксид лития
Ba(OH)2 гидроксид бария
Ca(OH)2 гидроксид кальция
(гашеная известь)
Mg(OH)2 гидроксид магния
Fe(OH)2 гидроксид железа (II)
Zn(OH)2 гидроксид цинка
NH4OH гидроксид аммония
Fe(OH)3 гидроксид железа (III)
и т.д. (большинство
гидроксидов металлов)
12. Кислоты в свете ТЭД
Кислота– это сложное вещество, в молекуле
которого имеется один или несколько атомов
водорода и кислотный остаток Hn(Ac).
Кислота
- электролит, при диссоциации
которого в качестве катионов образуются
только катионы водорода (Н+).
HCl
Н+ + Cl—
H2SO4 Н+ + НSО—4
13. Виды кислот
Безкислородныекислоты: HCl, HBr, HF, H2S и
др. (образуют сильные неметаллы VI и VII
гр.). Представляют растворы газов в воде.
Кислородсодержащие
кислоты : H2SO4 ;
H2СO3; H3PO4. – Как правило жидкости.
14. Основность кислот
определяется количествомионов водорода Н+, равно количеству молекул
простого основания необходимого для
нейтрализации.
Диссоциация многоосновной кислоты
протекает ступенчато.
Константа диссоциации второй и третьей ступени
значительно ниже чем первой.
Н3РО4
Н+ + Н2РО—4 - первая ступень
Н2РО—4
Н+ + НРO2-4
- вторая ступень
НРО2-4
Н+ PОЗ—4
- третья ступень
15. Сильные и слабые кислоты
Сильные кислотыСлабые кислоты
HI иодоводородная
HBr бромоводородная
HCl хлороводородная
H2SO4 серная
HNO3 азотная
HF фтороводородная
H3PO4 фосфорная
H2SO3 сернистая
H2S сероводородная
H2CO3 угольная
H2SiO3 кремниевая
16. Соли в свете ТЭД
Соли– это сложные вещества, образованные
атомами металлов и кислотных остатков
МеnАс.
Соли
- электролиты, при диссоциации
которых образуются катионы металлов, а
также катион аммония ( NH+4) и анионы
кислотных остатков.
(NH4)2SO4
2NH+4 + SO2-4
Na3PO4
3Na+ + PO3-4
17. Виды солей
Средние соли – все атомы кислорода замещеныметаллом. KCl, FeSO4, Na3PO4
Кислые соли – содержат Н+ диссоциируют
ступенчато:
KHSO4
K+ + HSO—4
HSO—4
H++SO2-4
Основные соли – содержат гидроксильную
группу ОН—, диссоциируют ступенчато:
Mg(OH)Cl
Mg(OH)++Cl—
Mg(OH)+
Mg2++OH—
18. Водородный показатель
– характеризуетконцентрацию свободных ионов водорода в воде или
водном растворе: pH = -log[H+].
Диссоциация воды (очень незначительно):
Н 2O
Н+ + ОН—
[H+] = [ОН—] = 10 —7 моль/л.
pH = - lg [H+] = 7 - нейтральная среда
При добавлении кислоты:
Н2O + HCl = Н2O + H+ + Cl—
0 ≤ рН <7 – кислая среда
При добавлении основания:
Н2O + КОН = Н2O + К+ + ОН—
7< рН ≤14 – щелочная среда
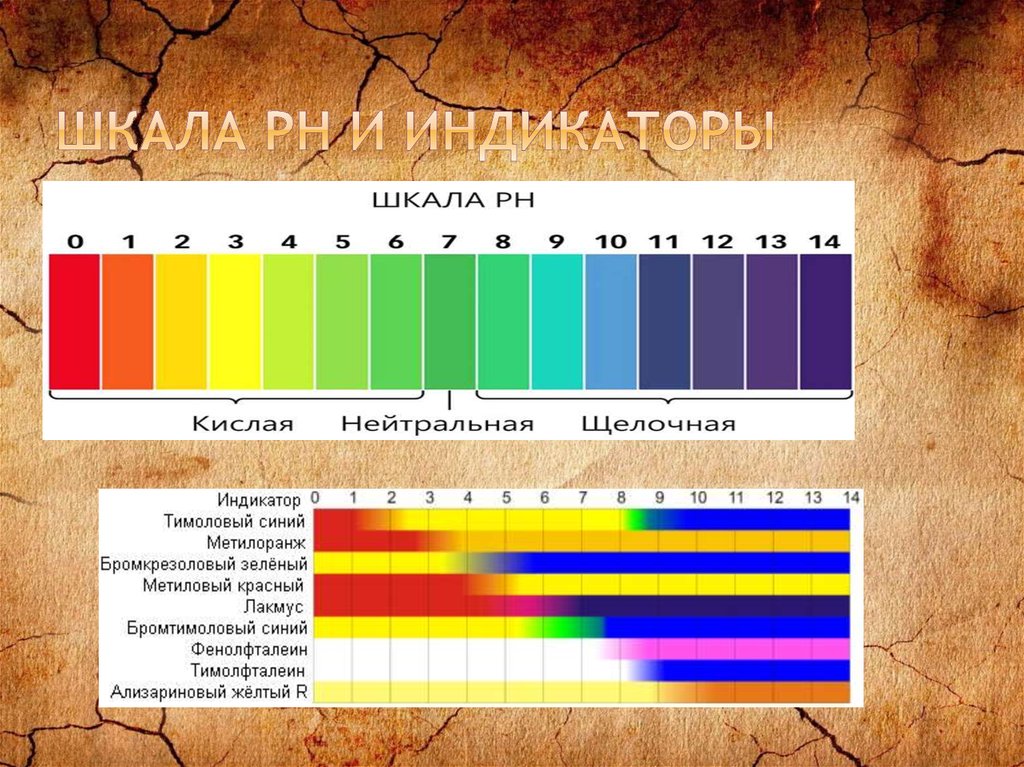
19. Шкала Ph и индикаторы
20.
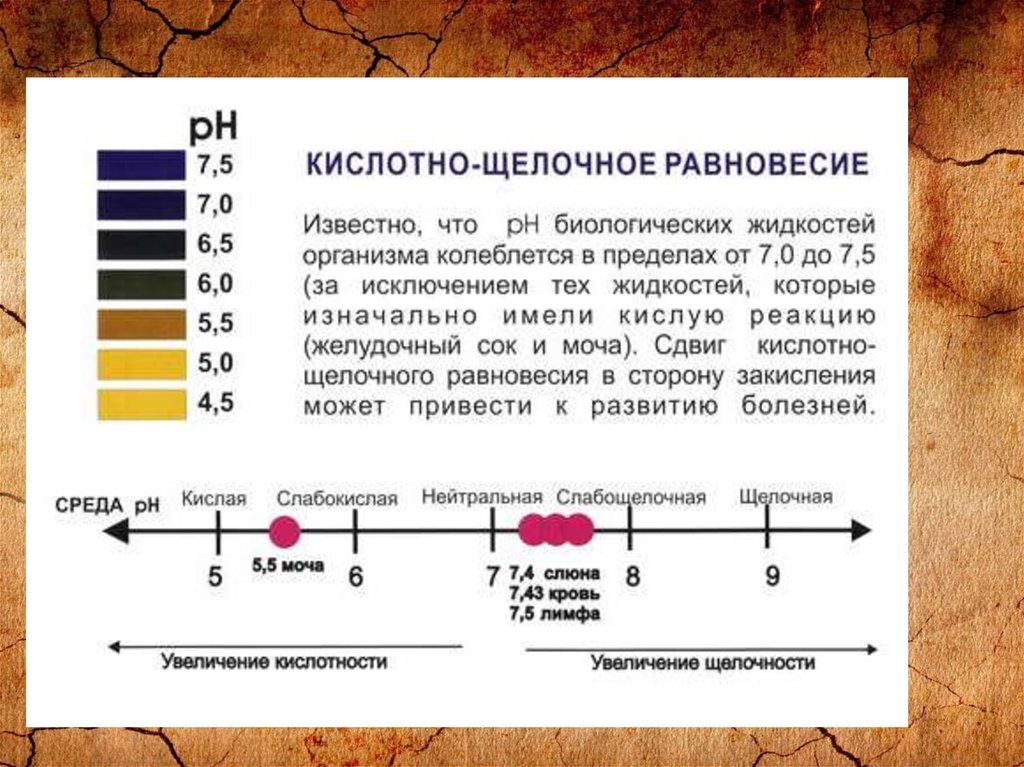
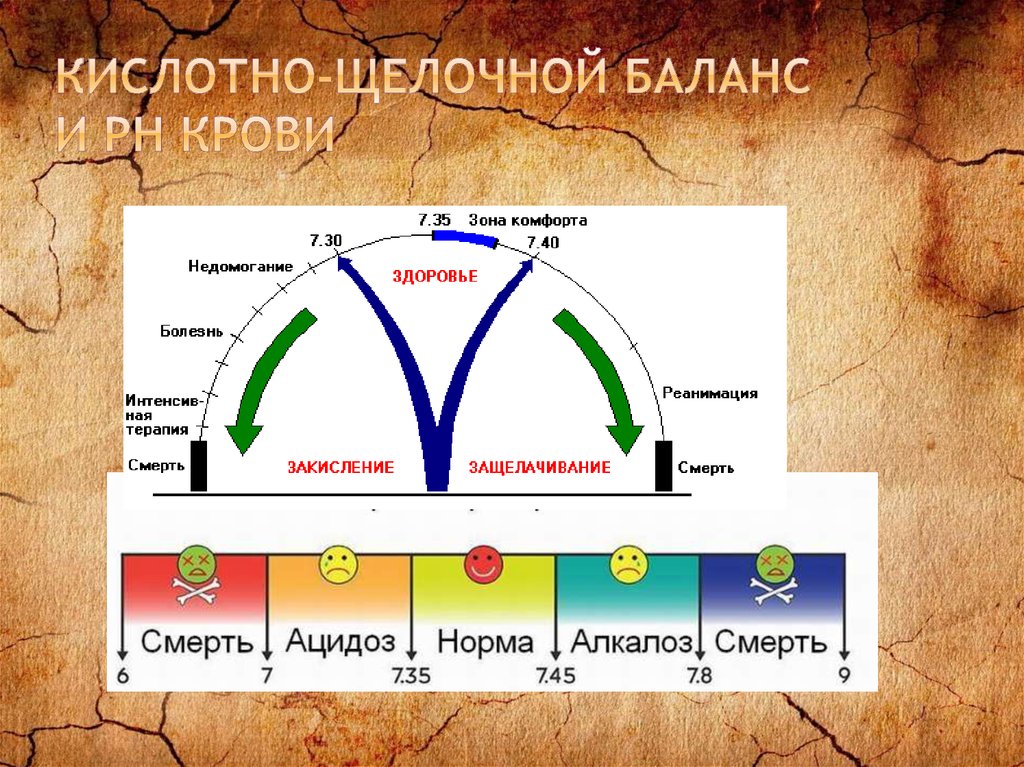
21. Кислотно-щелочной баланс и рн крови
22.
Проверьте свой кислотно-щелочной баланс спомощью pH тест-полосок
С помощью pH тест-полосок можно легко, быстро и
точно определить уровень pH, не выходя из дома. Если
уровень pH мочи колеблется в пределах 6,0-6,4 утром и
6,4-7,0 вечером, то ваш организм функционирует
нормально. Если в слюне отметка уровня pH остается
между 6,4-6,8 в течение всего дня – это также
свидетельствует о здоровье ва-шего организма.
Наиболее оптимальный уровень pH слюны и мочи
слегка кислый, в пределах 6,4-6,5. Лучшее время для
определения уровня pH – за 1 час до еды или спустя 2
часа после еды. Регулярно проверяйте уровень вашего
pH.
23.
24. Электролиз
– окислительновосстановительные реакции, которыепротекают на электродах при прохождении
электрического тока через расплав или
раствор электролита.
Электрический ток – самый сильный
окислитель и восстановитель!
В процессе электролиза восстанавливаются
даже ионы щелочных металлов и окисляются
ионы галогенов и кислорода.
25. Электролизер
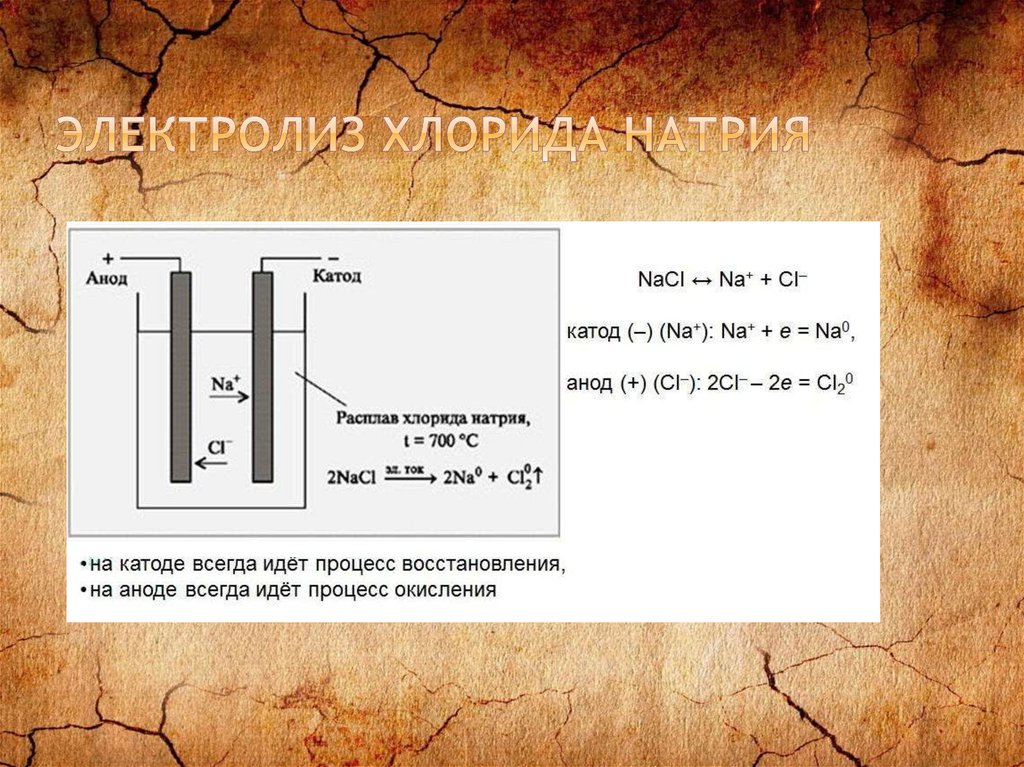
26. Электролиз хлорида натрия
27. Электролиз воды
Видеотека: Электролиз воды28. Электролиз раствора сульфата меди
Видеотека: Электролиз сульфата меди29. Применение электролиза
Получениещелочных и щелочно-земельных
металлов и аллюминия
Получение галогенов, водорода и кислорода
Нанесение металлических покрытий –
никелирование, хромирование, золочение
(гальваностегия)
Изготовление рельевных металлических
копий (гальванопластика)
Очистка цветных металлов от примесей
(рафинирование)
























 chemistry
chemistry








