Similar presentations:
Окисли́тельно-восстанови́тельные реа́кции
1.
Когда электрон улетает, степень окисления________________________Когда электрон присоединяется, степень окисления _______________
2.
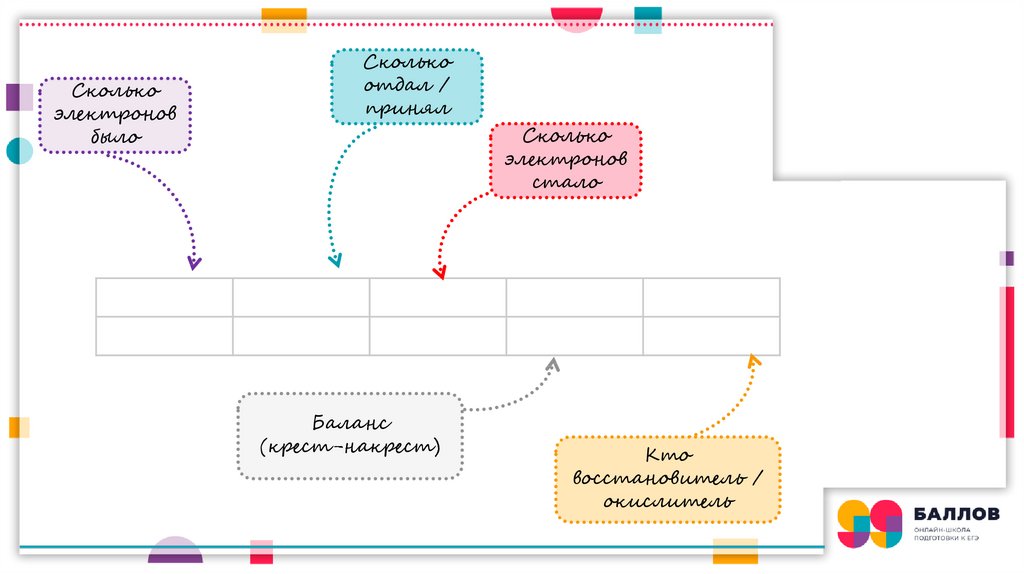
Cколькоэлектронов
было
Сколько
отдал /
принял
Cколько
электронов
стало
Баланс
(крест-накрест)
Кто
восстановитель /
окислитель
3.
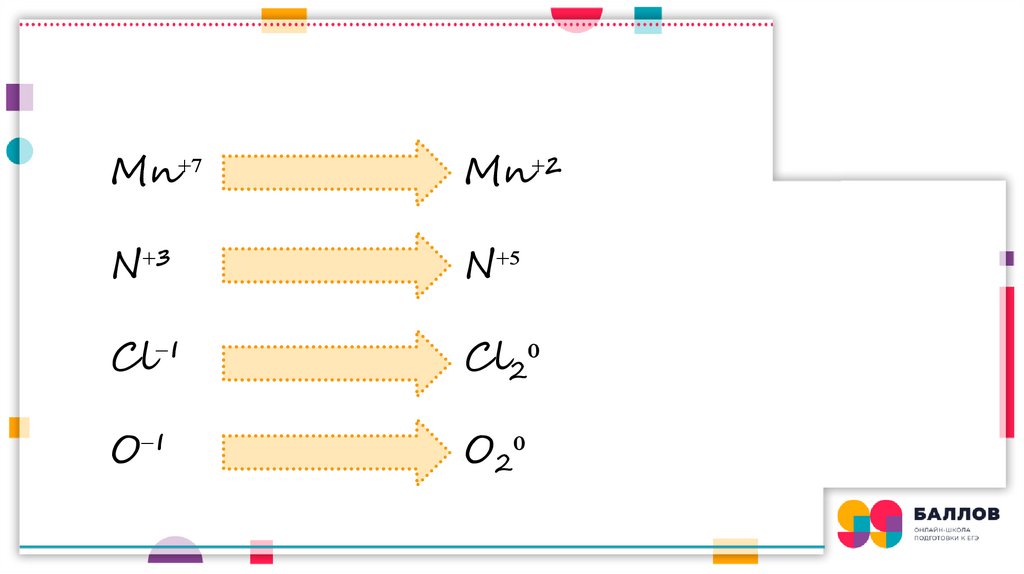
Mn⁺⁷Mn⁺²
N⁺³
N⁺⁵
Cl⁻¹
Cl2⁰
O⁻¹
O2⁰
4.
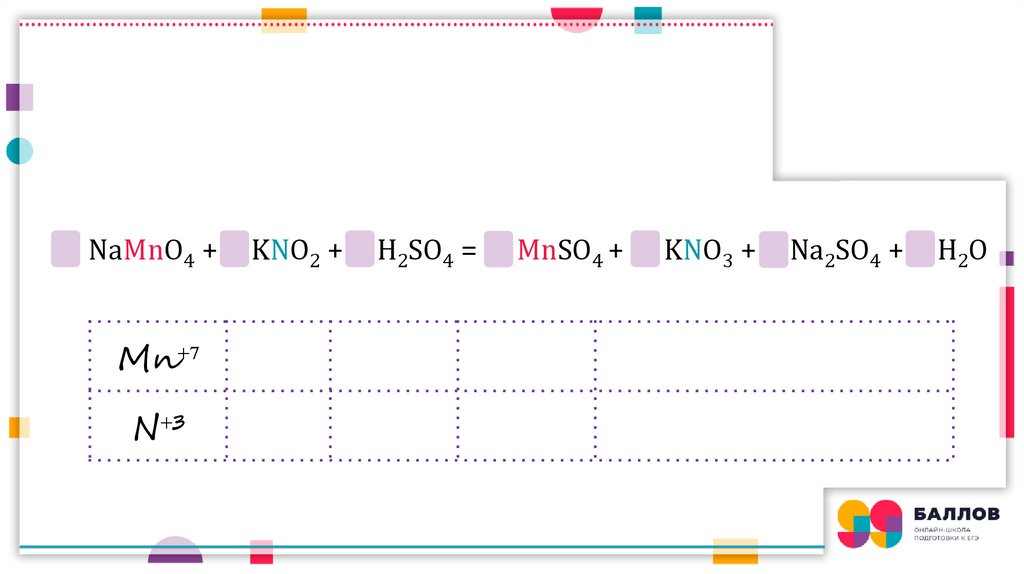
NaMnO4 +Mn⁺⁷
N⁺³
KNO2 +
H2SO4 =
MnSO4 +
KNO3 +
Na2SO4 +
H2O
5.
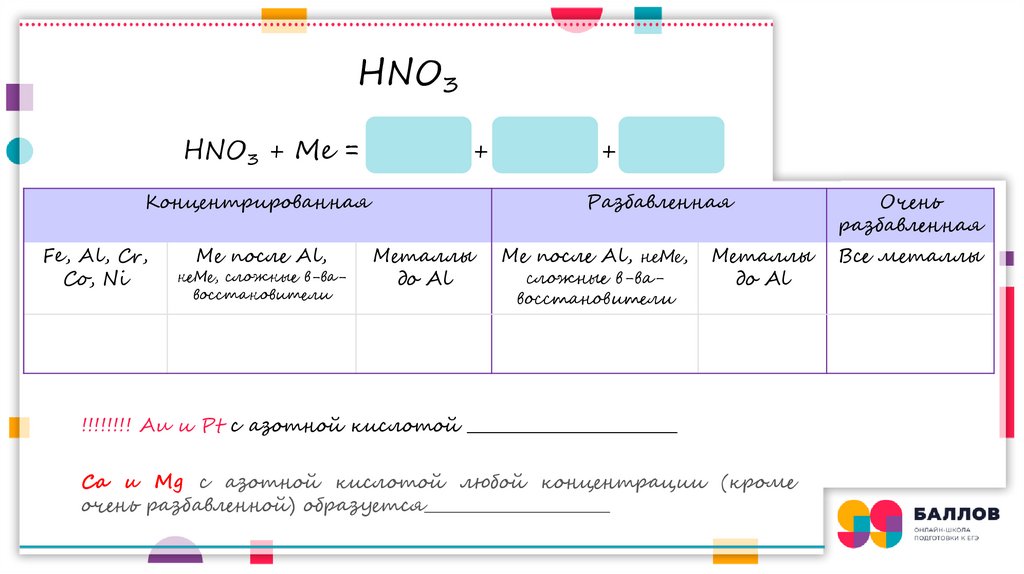
HNO3HNO3 + Me =
+
Концентрированная
Fe, Al, Cr,
Co, Ni
Ме после Al,
неМе, сложные в-вавосстановители
+
Разбавленная
Металлы
до Al
Ме после Al, неМе,
сложные в-вавосстановители
Металлы
до Al
!!!!!!!! Au и Pt с азотной кислотой __________________________
Ca и Mg с азотной кислотой любой концентрации (кроме
очень разбавленной) образуется_______________________
Очень
разбавленная
Все металлы
6.
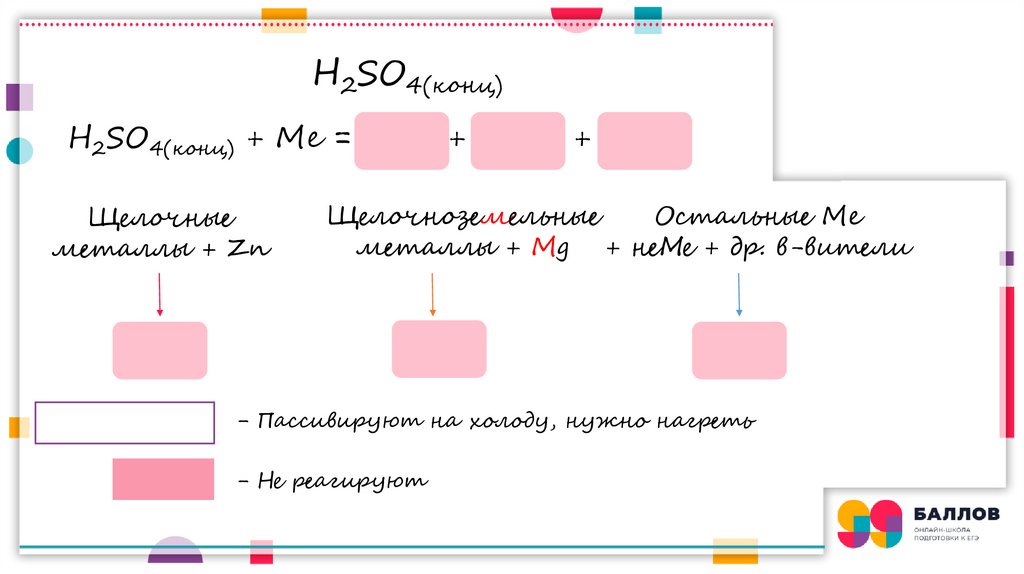
H2SO4(конц)H2SO4(конц) + Me =
Щелочные
металлы + Zn
+
+
Щелочноземельные
Остальные Me
металлы + Mg + неМе + др. в-вители
- Пассивируют на холоду, нужно нагреть
- Не реагируют
7.
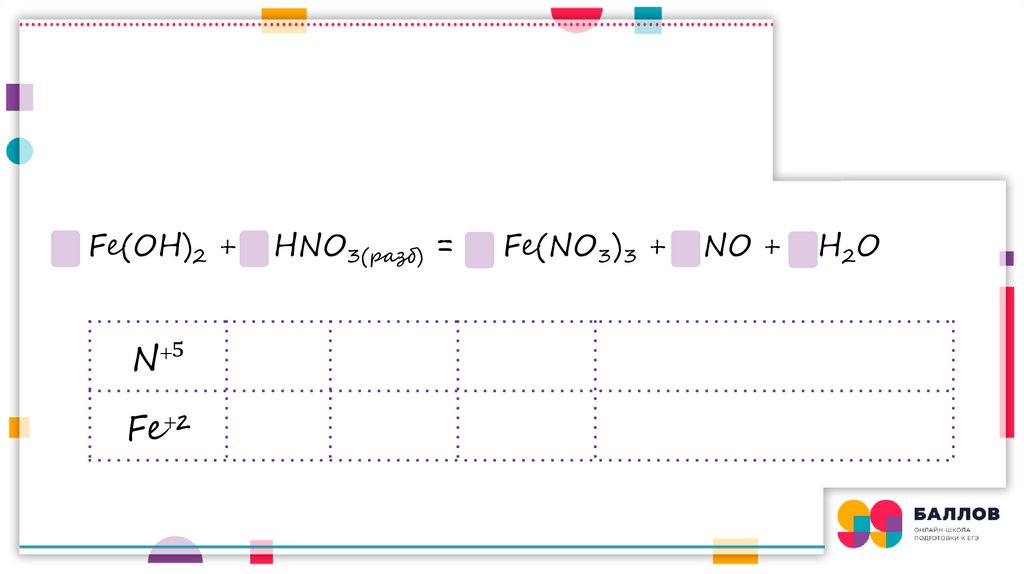
Fe(OH)2 +N⁺⁵
Fe⁺²
HNO3(разб) =
Fe(NO3)3 +
NO +
H2O

 chemistry
chemistry