Similar presentations:
Маркировка Лекарственных препаратов. Обеспечение учета лекарственных препаратов
1.
Маркировка Лекарственных препаратовОбеспечение учета лекарственных
препаратов и взаимодействие с ФГИС
МДЛП
Корпорация «ПАРУС»
2.
План презентацииОбзор актуальных НПА
Основания для разработки программного обеспечения
Архитектура решения Корпорации Парус
Поддержка оборудования (2D-сканеры, РВ КМ и ККТ)
Взаимодействие с внешними системами
Дорожная карта по подготовке организаций к
работе с ФГИС МДЛП
Демонстрация решения
3.
Актуальные НПАФедеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств»
Постановление Правительства Российской Федерации от 24.01.2017 № 62
«О проведении эксперимента по маркировке контрольными (идентификационными)
знаками и мониторингу за оборотом отдельных видов лекарственных препаратов для
медицинского применения»
–
Проект изменений № 02/07/05-19/00091535 от 22 мая 2019г.
Постановления Правительства Российской Федерации от 14 декабря 2018 года:
• №1556 «Об утверждении Положения о системе мониторинга движения
лекарственных препаратов для медицинского применения»
–
–
–
Требования к структуре кода маркировки
Требования по порядку и составу информации о ЛП предоставляемой субъектами обращения в ФГИС МДЛП
• Вывод из оборота для медицинского применения
• Операции с групповыми упаковками
• Оборот и внутреннее перемещение
Причины блокировки принятия ФГИС МДЛП сведений о движении ЛП
№1557 «Об особенностях внедрения системы мониторинга движения лекарственных
препаратов для медицинского применения»
–
–
Распространяется на организации - субъекты обращения ЛП по программе «7 нозологий»
См. Приложение N 3 к распоряжению Правительства Российской Федерации от 10 декабря 2018 г. N 2738-р
4.
Актуальные НПАФедеральный закон от 15.04.2019 № 58-ФЗ «О внесении изменений в Кодекс Российской
Федерации об административных правонарушениях»
• Статья 6.34. Несвоевременное внесение данных в систему мониторинга движения
лекарственных препаратов для медицинского применения либо внесение в нее
недостоверных данных.
–
Для должностных лиц штраф составит 5-10 тыс. рублей, для юр.лиц – 50-100 тыс. рублей.
Нормативно-методические материалы и техническая документация на сайте оператора
системы маркировки (https://честныйзнак.рф/business/projects/medicines/):
«Паспорта процессов v1.30» и «Статусная модель v1.28»
«Схемы и форматы для разработчиков учётных систем v1.30»
«API. Протокол обмена интерфейсного уровня v2.30»
«Формат записи данных о выбытии ЛП в ФФД»
«Инструкция по подключению медицинских организаций и аптек к ИС МДЛП»
«Руководство пользователя личного кабинета субъекта обращения лекарственных препаратов»
«Регламент подключения к API и рекомендуемый алгоритм освоения интеграции с МДЛП…»
FAQ и другие материалы:
– … Партнёры –> Протестированные решения –>
Протестированные сканеры штрих-кода
Региональные отраслевые приказы и распоряжения
5.
Ожидаемые измененияМихаил Мурашко,
Руководитель Федеральной службы по надзору в сфере
здравоохранения (Росздравнадзор):
• «… Что важно: маркировка и работа в системе маркировки будут лицензионными
требованиями, и это автоматический контроль. То есть реестр лицензий
накладывается на реестр подключенных организаций к системе маркировки, и те,
кто отсутствует, или те, по которым отсутствует движение лекарственных
препаратов, будут фактическими объектами контроля»
«….в текущем году уже стартовала подготовка к внедрению системы маркировки
медицинских изделий»
*Заявление в рамках конференции Фармедобращение-2019
6.
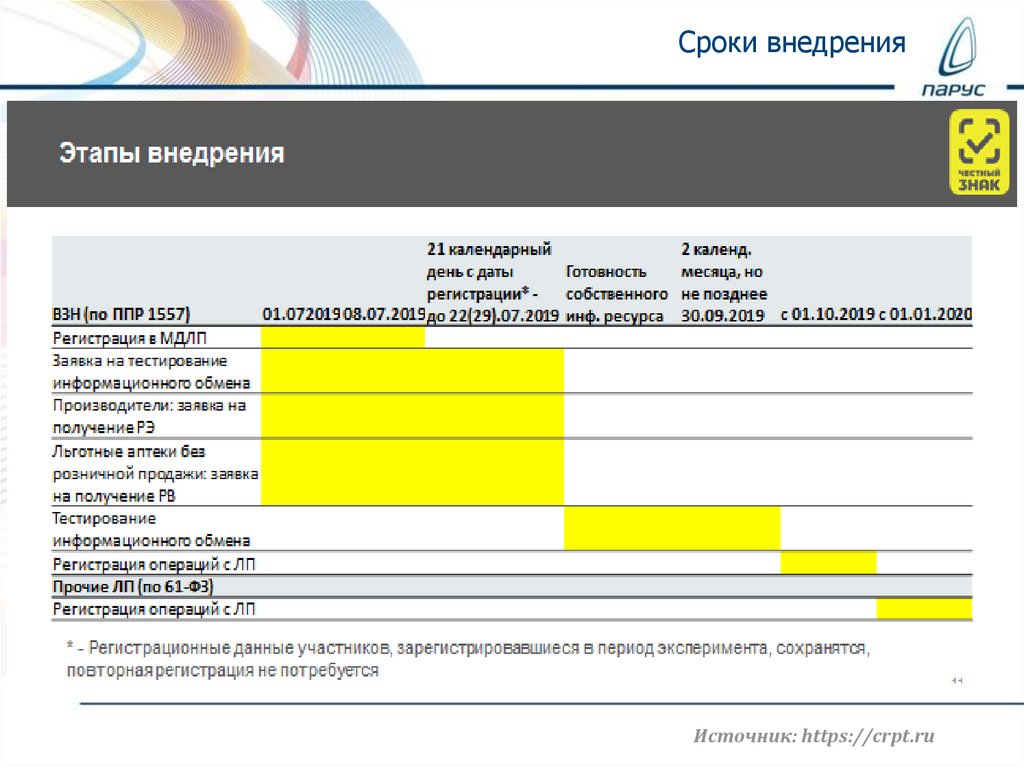
Сроки внедренияИсточник: https://crpt.ru
7.
Регистратор выбытия8.
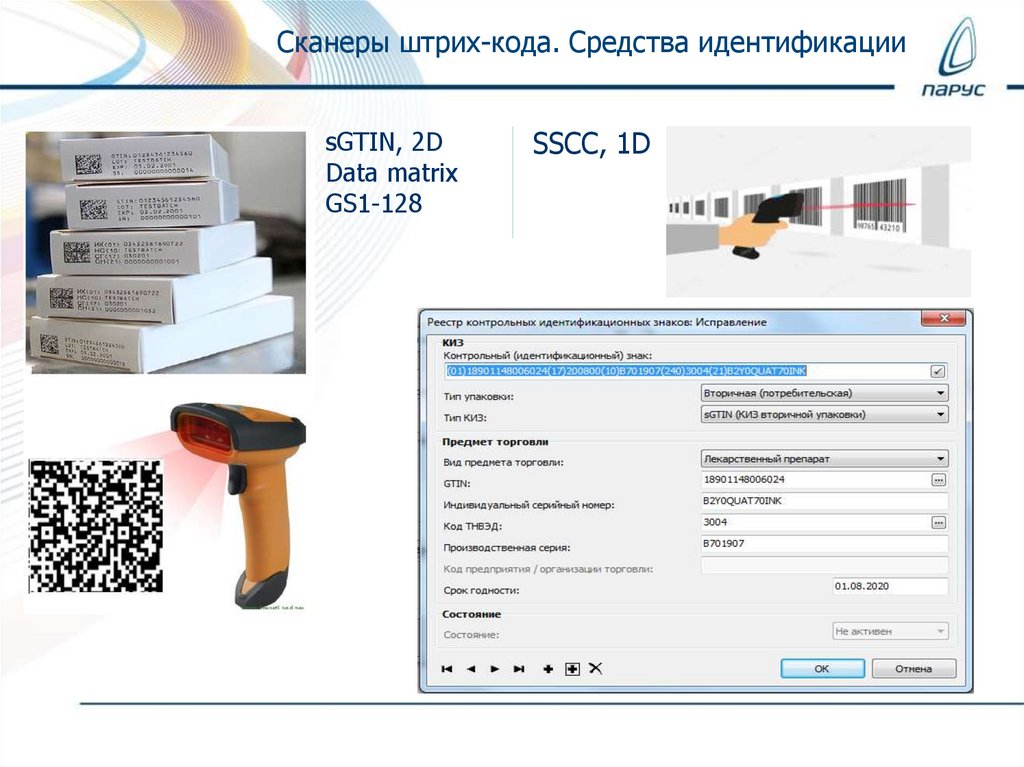
Сканеры штрих-кода. Средства идентификацииsGTIN, 2D
Data matrix
GS1-128
SSCC, 1D
9.
Компетенции «Корпорации «ПАРУС»» по работе с ИС МДЛП• Начало работ по проектированию и созданию модуля «Учёт
маркированных товаров» с 2017 года
• Члены рабочей группы Росздравнадзора по организации работы
медицинских организаций (в том числе взаимодействие с
разработчиками ПО) во ФГИС МДЛП
Члены постоянной рабочей группы «Оператор-ЦРПТ» по
взаимодействию информационных систем с регистраторами
выбытия КМ
• Реализация информационной системы для всероссийского центра
компетенции ГБУЗ ГКБ им. М. П. Кончаловского
• Реализация региональных проектов в сфере МДЛП более чем в 10
субъектах РФ
10.
Дорожная карта по подготовке МО к работе с маркированными ЛПДля успешной подготовки к регистрации медицинской организации в
ИС МДЛП и дальнейшей работе с маркированными ЛП необходимо:
1. Иметь лицензию на фармацевтическую/медицинскую деятельность
2. Заказать и получить электронную подпись в аккредитованных удостоверяющих центрах
3. Обеспечить полное соответствие ФИО руководителя и ИНН организации, указанные в
УКЭП, сведениям, внесенным в ЕГРЮЛ/ЕГРИП
4. Пройти регистрацию в ИС МДЛП на https://mdlp.crpt.ru
5. Подготовить учетную систему медицинской организации
6. Подготовить рабочее место сотрудника медицинского склада
7. Пройти тестовый стенд «Песочница»
8. Получить регистратор выбытия КМ
11.
Регистрация в ИС МДЛП1.
(Мониторинг движения лекарственных препаратов)
Установить на рабочем месте сертификат ключа УКЭП, программы, обеспечивающие работу
с электронной подписью и защиту информации (КриптоПро, Плагин КриптоПро для браузеров)
2.
Открыть информационный ресурс Маркировка лекарственных средств
https://sb.mdlp.crpt.ru (проверка поддерживаемости версий ОС, браузера, КриптоПро, Плагина
КриптоПро выполняется автоматически при регистрации МО)
3.
Заполнить заявление (появится автоматически при выборе пункта «Зарегистрируйтесь» и
указании типа участника – Резидент РФ)
4.
Получить подтверждение о регистрации на электронную почту, указанную в
заявлении
5.
Войти с помощью УКЭП в личный кабинет МДЛП https://sb.mdlp.crpt.ru (для первого
входа необходимо использовать УКЭП руководителя организации)
6.
Зарегистрировать места деятельности и пользователей
7.
Обратиться в СТП МДЛП с просьбой дать доступ к API тестового стенда «Песочница»
8.
Пройти тестовую цепочку на тестовом стенде «Песочница» и заполнить чек-лист
9.
Повторить шаги 2, 3, 4, 5, 6, 7 для подключения к промышленному контуру по адресу:
https://mdlp.crpt.ru
12.
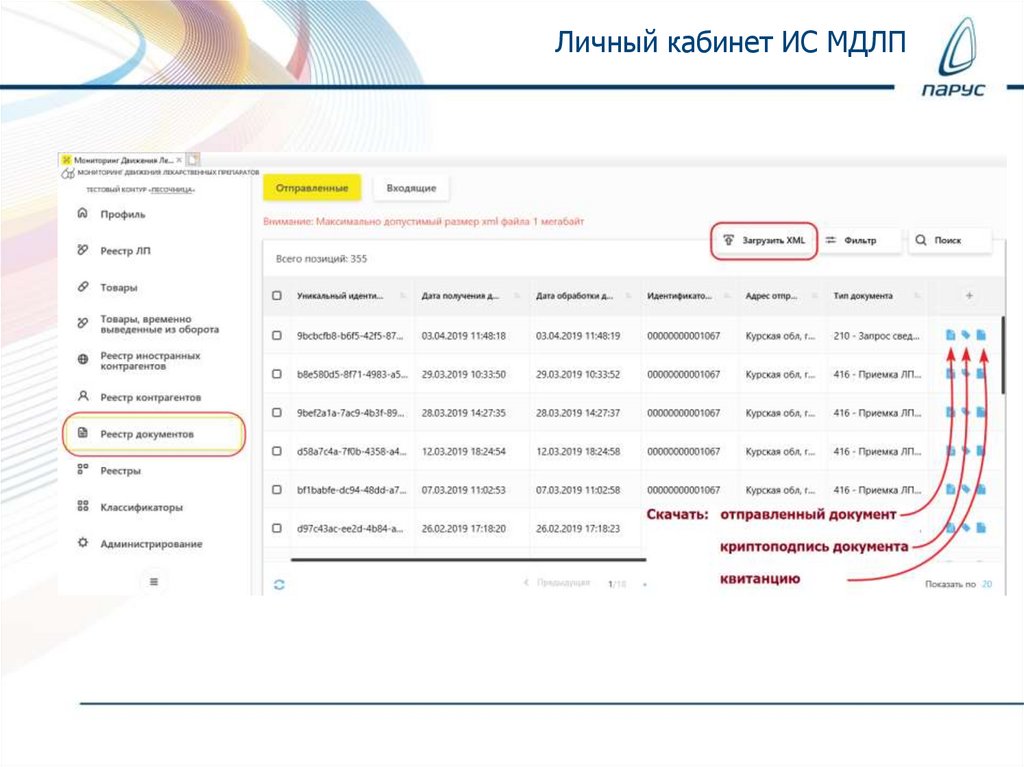
Личный кабинет ИС МДЛП13.
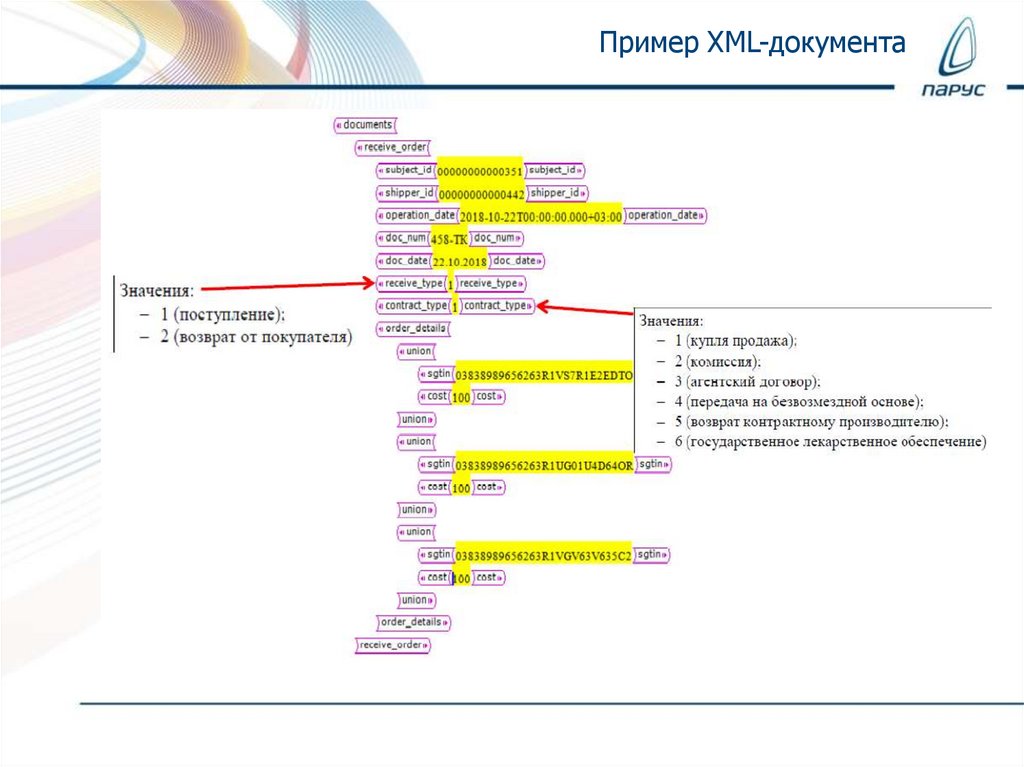
Пример XML-документа14.
Требования к информационной системе МОНа базе ПП «Парус – Бюджет 8» было разработано решение, автоматизирующее учет
движения маркированных товаров и передачу всех необходимых данных в систему
мониторинга движения лекарственных препаратов.
Решение обеспечивает:
Ведение реестра контрольных идентификационных знаков лекарственных
препаратов;
Учет операций с упаковками лекарственных препаратов, включая приемку на
склад, перемещение по местам деятельности, вывод лекарственных препаратов из
оборота и др.;
Учет лекарственных препаратов, лекарственных форм, дозировок и
международных непатентованных наименований;
Считывание средств идентификации лекарственных препаратов с использованием
сканеров 2-мерных штрих кодов;
Взаимодействие с регистраторами выбытия.
15.
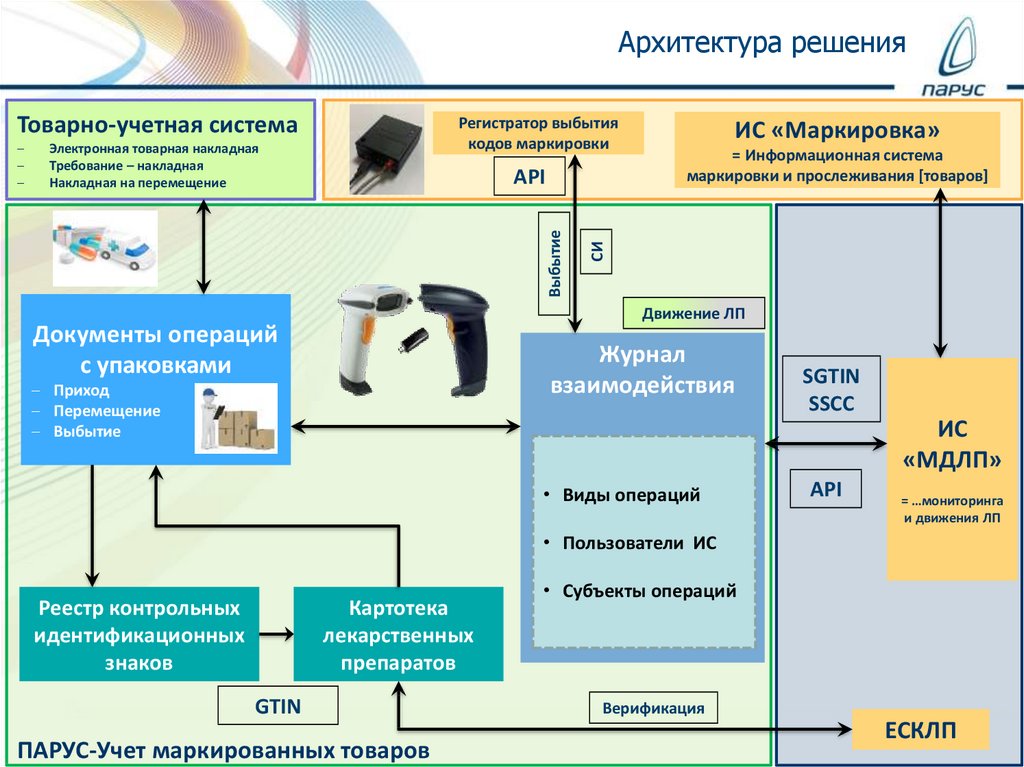
Архитектура решенияТоварно-учетная система
Электронная товарная накладная
Требование – накладная
Накладная на перемещение
ИС «Маркировка»
= Информационная система
маркировки и прослеживания [товаров]
СИ
API
Выбытие
Регистратор выбытия
кодов маркировки
Движение ЛП
Документы операций
с упаковками
Журнал
взаимодействия
Приход
Перемещение
Выбытие
SGTIN
SSCC
ИС
«МДЛП»
• Виды операций
API
= …мониторинга
и движения ЛП
• Пользователи ИС
Реестр контрольных
идентификационных
знаков
Картотека
лекарственных
препаратов
GTIN
ПАРУС-Учет маркированных товаров
• Субъекты операций
Верификация
ЕСКЛП
16.
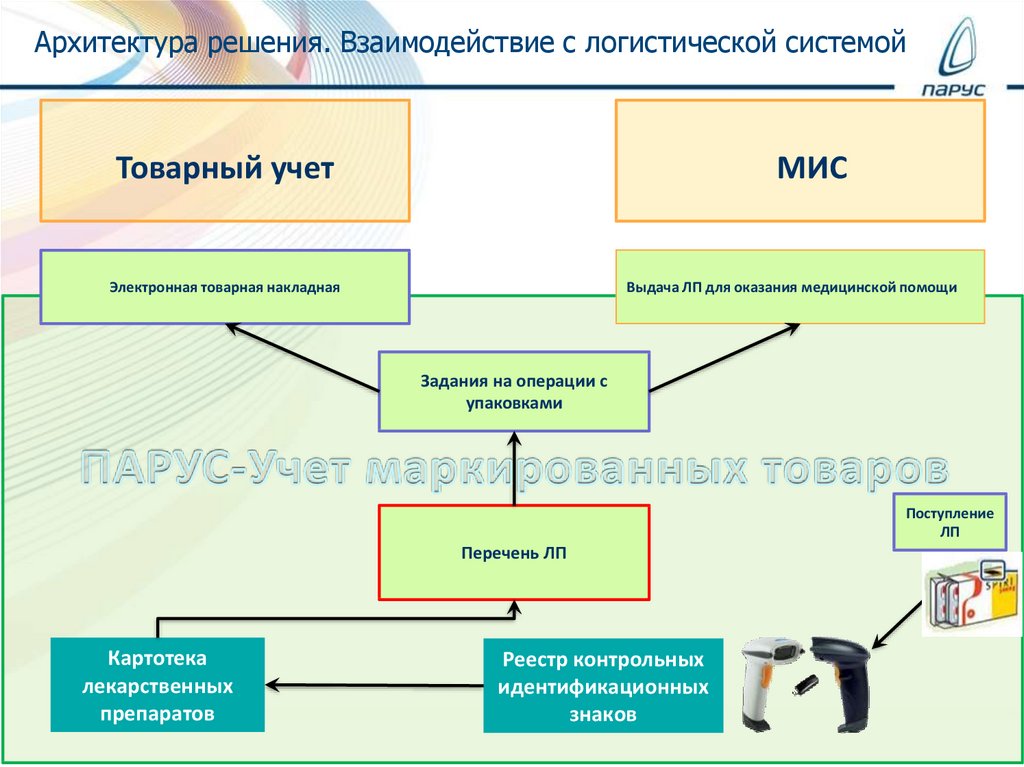
Архитектура решения. Взаимодействие с логистической системойТоварный учет
МИС
Выдача ЛП для оказания медицинской помощи
Электронная товарная накладная
Задания на операции с
упаковками
Поступление
ЛП
Перечень ЛП
Картотека
лекарственных
препаратов
Реестр контрольных
идентификационных
знаков
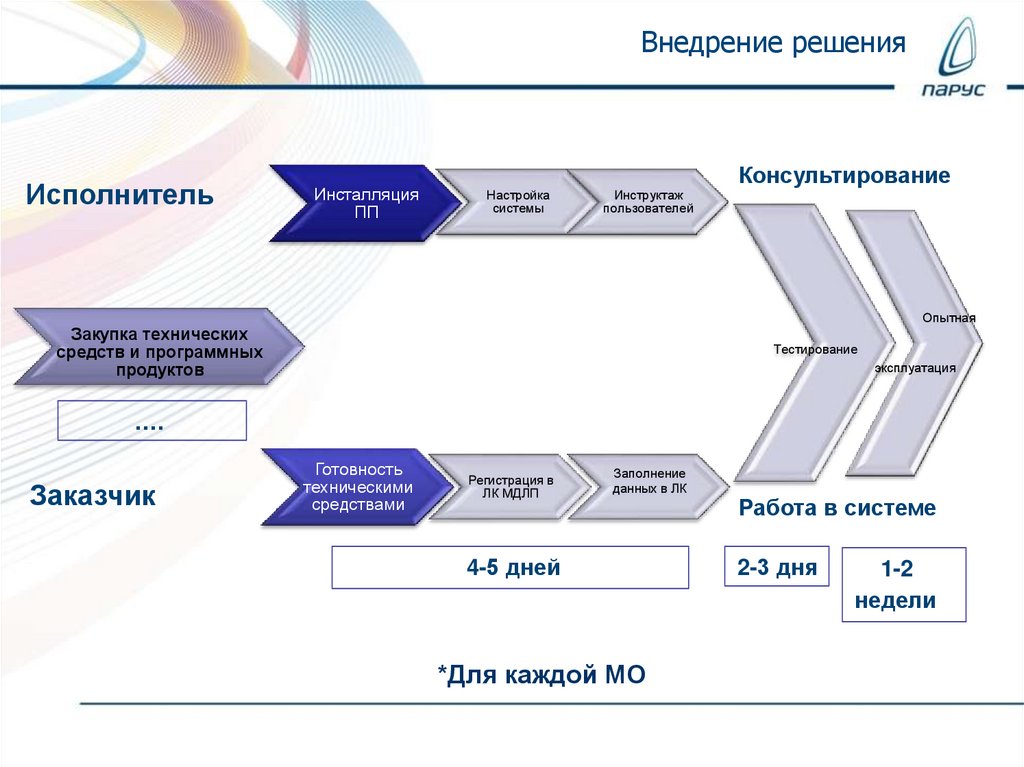
17.
Внедрение решенияИсполнитель
Инсталляция
ПП
Консультирование
Настройка
системы
Инструктаж
пользователей
Опытная
Закупка технических
средств и программных
продуктов
Тестирование
эксплуатация
….
Заказчик
Готовность
техническими
средствами
Регистрация в
ЛК МДЛП
Заполнение
данных в ЛК
4-5 дней
*Для каждой МО
Работа в системе
2-3 дня
1-2
недели
18. Варианты развертывания решения
Автоматизируемые бизнес-процессыПриемка ЛП с прямым и обратным порядком акцептирования
получение сведений (уведомления) об отгрузке ЛП со склада продавца
сверка фактически полученных ЛП сведениям об отгрузке
подтверждение (акцептование) сведений об отгрузке
отказ получателя от приёмки товара (полностью либо частично)
Использование ЛП при оказании медицинской помощи
Перемещение между местами осуществления деятельности
Продажа ЛП в рамках розничной торговли
Отпуск ЛП по льготному рецепту
Передача на уничтожение ЛП
Факт (в т.ч. способ и адрес) уничтожения ЛП
Вывод ЛП из оборота [по различным причинам]
Отзыв/отмена ранее совершенной операции
19.
Практическое использование решенияЦентры компетенции и МО, уже подключившиеся к процессу интеграции с системой
МДЛП через API:
ГБУЗ ГКБ им. М.П.Кончаловского ДЗМ г. Москвы + другие МО субъекта
ФГУ НМХЦ им. Н.И.Пирогова Минздрава России
ОБУЗ «Курская городская больница №2» + другие МО субъекта
ГБУЗ Свердловской области «Свердловский областной онкологический диспансер» +
другие МО субъекта
БУЗ Омской области «Клинический медико-хирургический центр Министерства
здравоохранения Омской области» + другие МО субъекта
ГБУЗ Республики Башкортостан «Городская клиническая больница №21 города Уфа» +
БУЗ Орловской области «Орловский онкологический диспансер»
ГУП «Фармация» Республика Алтай
ОГБУЗ «Городская больница города Костромы» + другие МО субъекта
ГБУ Рязанской области «Областная клиническая больница» + другие МО субъекта
другие МО субъекта
В настоящее время более 60 организаций выбрали наше решение
20.
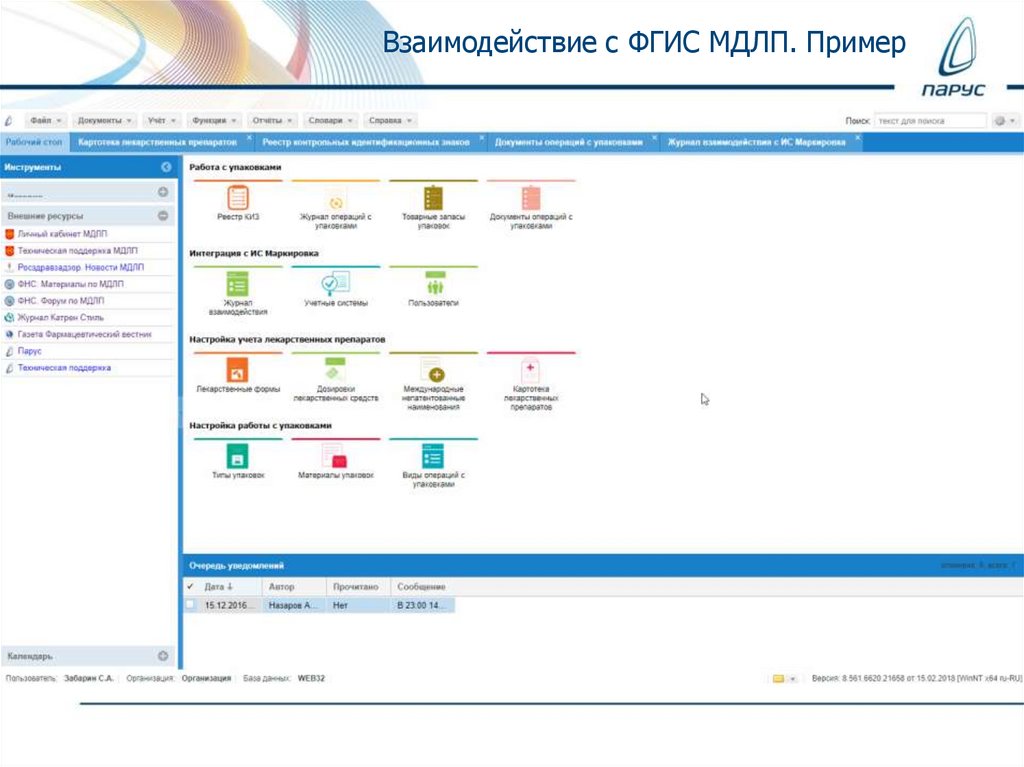
Взаимодействие с ФГИС МДЛП. Пример21.
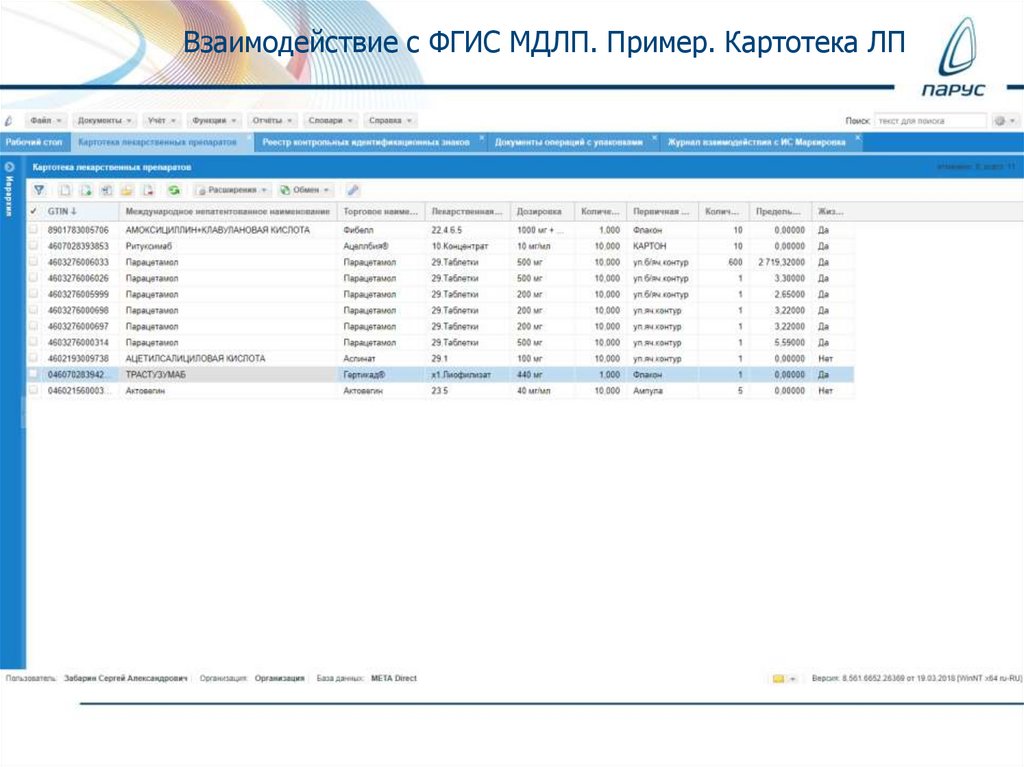
Взаимодействие с ФГИС МДЛП. Пример. Картотека ЛП22.
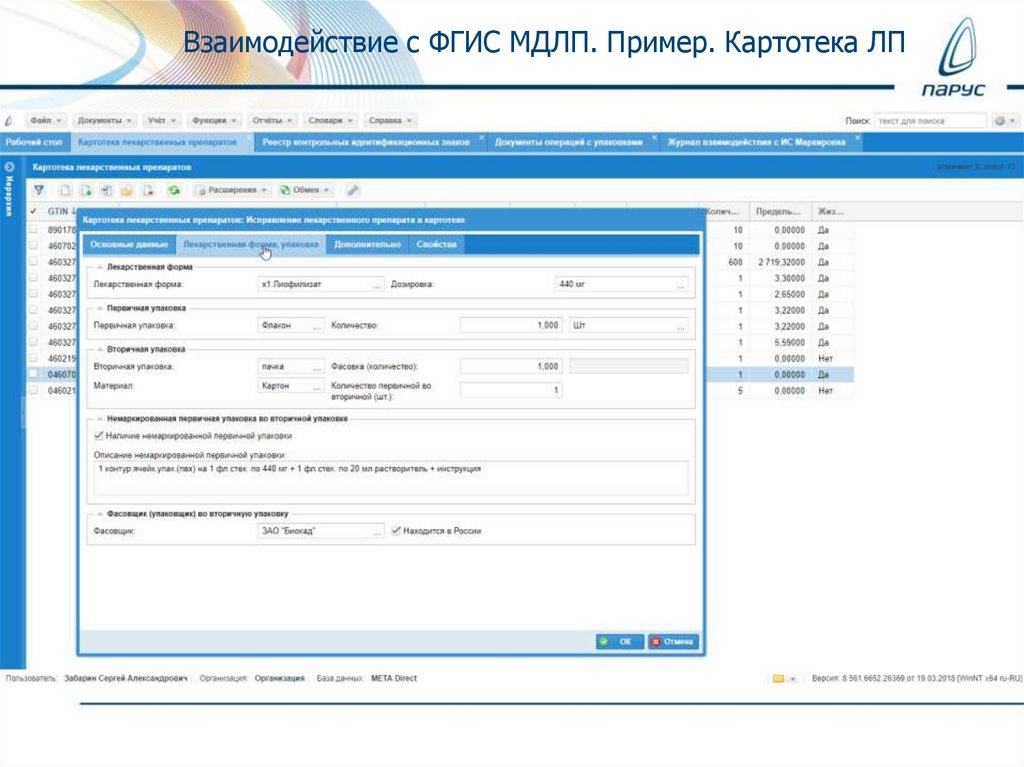
Взаимодействие с ФГИС МДЛП. Пример. Картотека ЛП23.
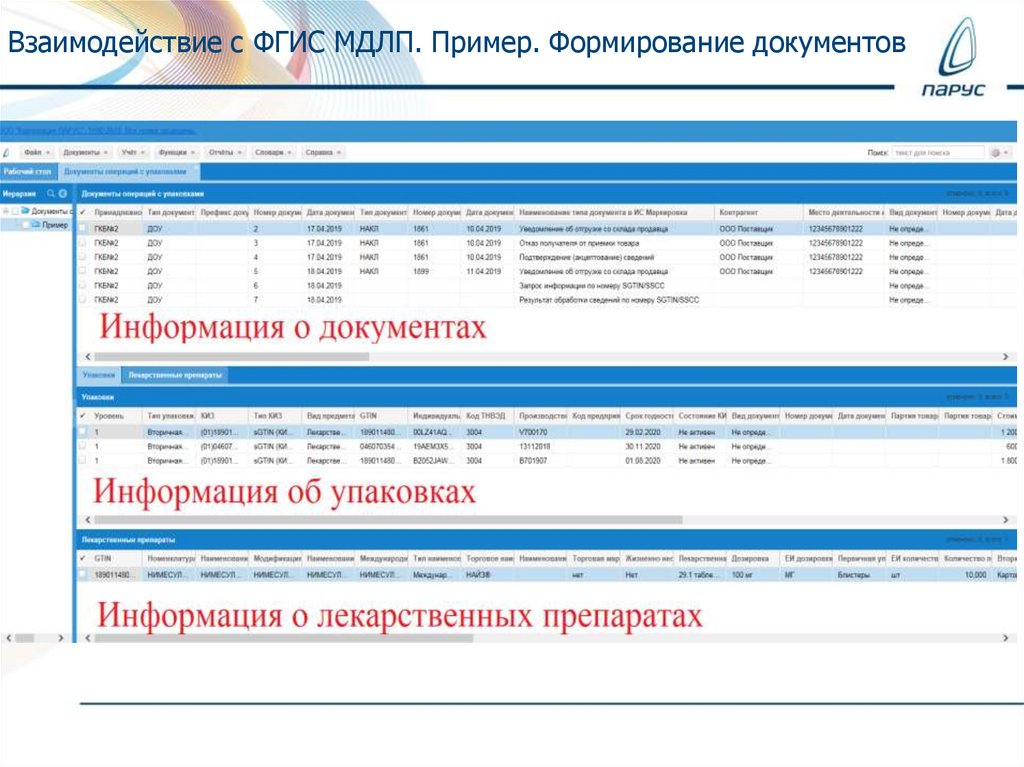
Взаимодействие с ФГИС МДЛП. Пример. Формирование документов24.
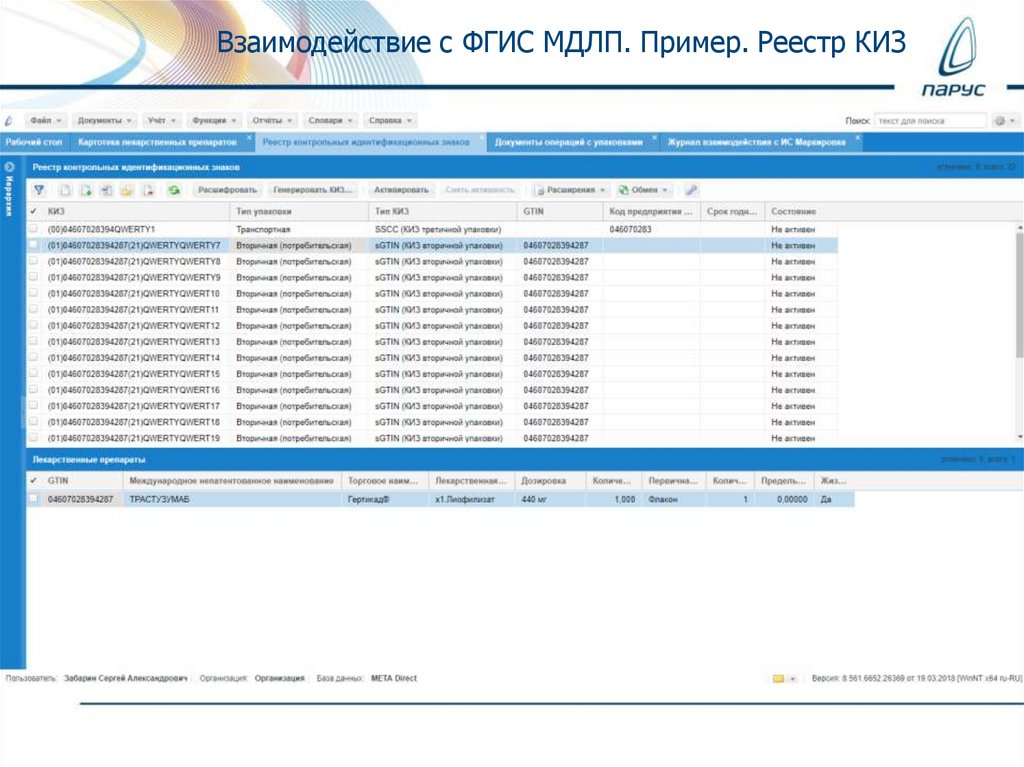
Взаимодействие с ФГИС МДЛП. Пример. Реестр КИЗ25.
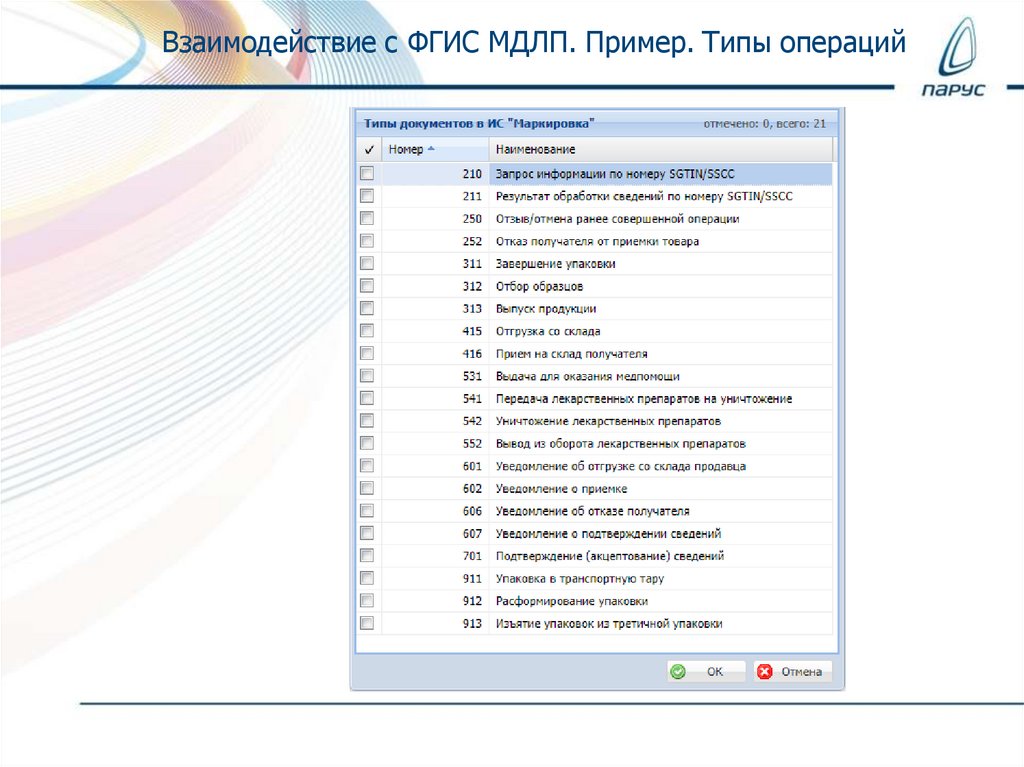
Взаимодействие с ФГИС МДЛП. Пример. Типы операций26.
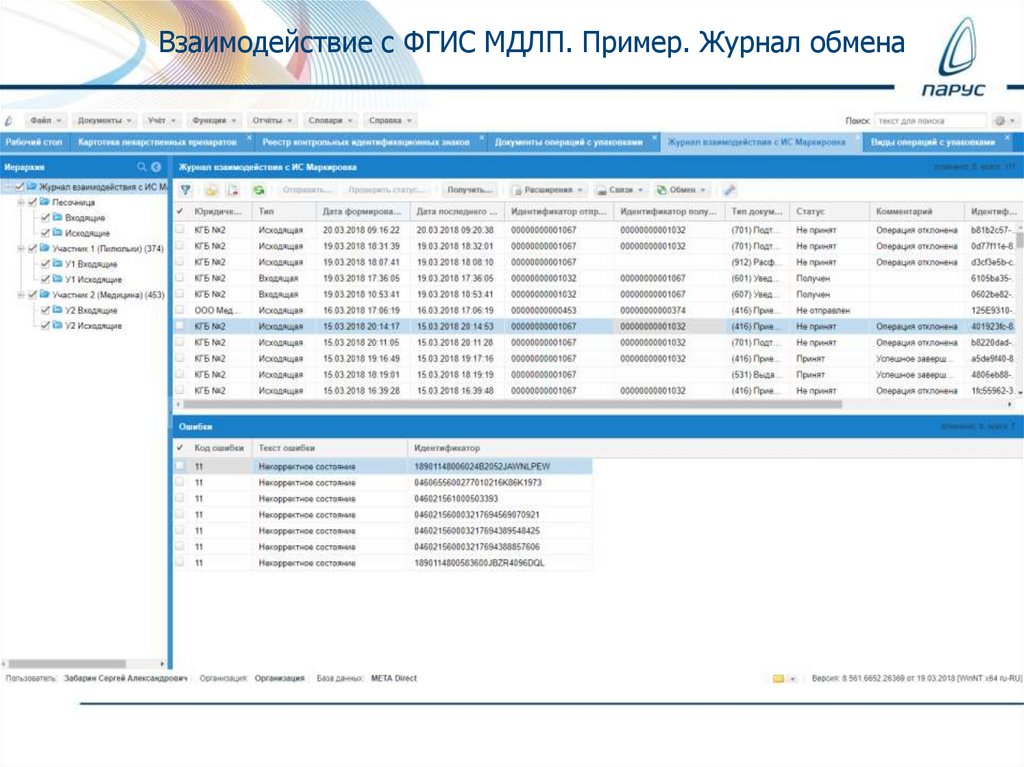
Взаимодействие с ФГИС МДЛП. Пример. Журнал обмена27.
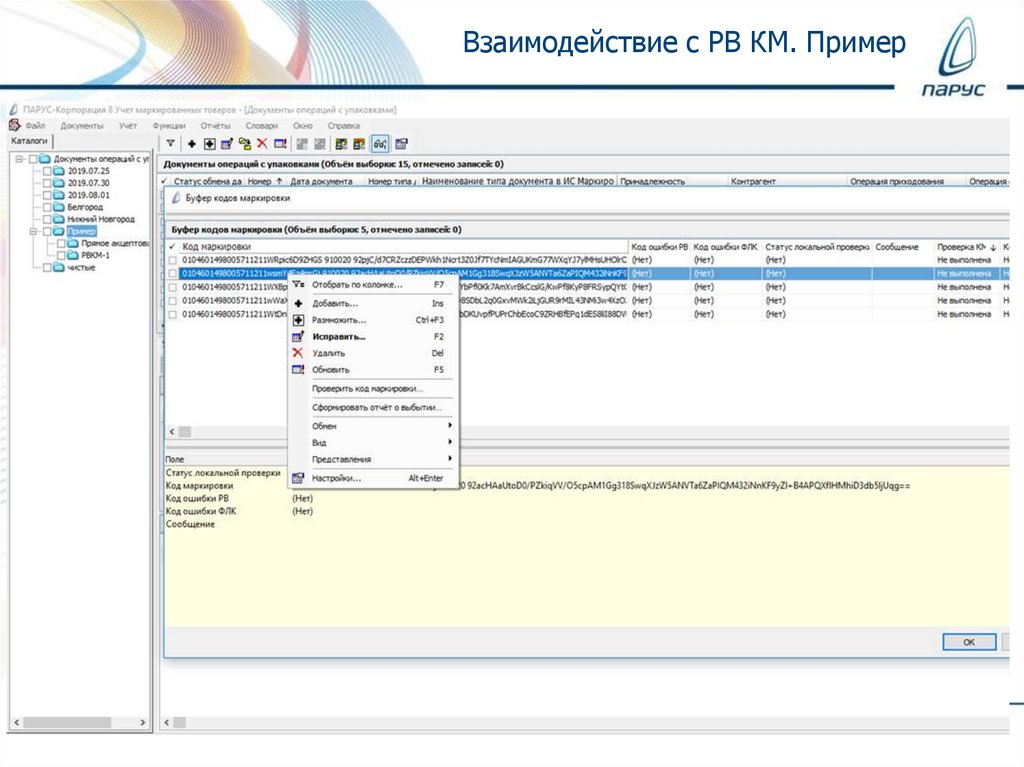
Взаимодействие с РВ КМ. Пример28.
ПоддержкаКонтактные данные
Центр компетенции «Корпорации «Парус»
по маркировке лекарственных препаратов
129366, Москва, ул. Ярославская, д.10 корп.4,
8 (495) 797-89-90 доб. 341
www.parus.com
office@parus.com
СПАСИБО ЗА ВНИМАНИЕ













 medicine
medicine








