Similar presentations:
Составление уравнений химических реакций
1. Составление уравнений химических реакций
Учитель химии МБОУСОШ №13
Ромашка В.В.
2. Химические уравнения
Масса веществ, вступивших в химическую реакцию,равна массе веществ, образовавшихся в результате нее.
Химическое уравнение – это условная запись химической
реакции с помощью химических формул и
математических знаков.
3. Определение количества атомов
SO2 Fe2O3 H2CO3 Mg(OH)2 Al2(SO4)3S -1 Fe -2
H -2
Mg -1
Al -2
O -2 O -3
C -1
O -2
S – 1*3
O -3
H -2
O – 4*3
2CO2
3NaOH
2H3PO4 2Mg(NO3)2
C -2*1 Na -3*1
H -2*3 Mg -2*1
O -2*2 O -3*1
P -2*1
N -1*2*2
H -3*1
O -2*4 O -2*3*2
4. Водород реагирует с кислородом с образованием воды
Слева записать исходные вещества (вещества, вступающие вреакцию). Слово «реагирует» заменить знаком «+».
H2 + O2
H2O
Справа записать продукт реакции (вещество, которое
образуется). Между правой и левой частью поставить
стрелку.
Мы получили схему реакции
Дальше
5.
Уравнять количество атомов каждого элемента с помощьюкоэффициентов.
2 H2 + O2
= 2 H2O
До реакции (слева) два атома кислорода, а после реакции
(справа) – один атом. Чтобы уравнять количество, нужно
поставить коэффициент «2» перед формулой воды.
Теперь проверим количество атомов водорода на данный
момент. До реакции (слева) – 2 атома, а справа – 4 атома
(2*2). Чтобы уравнять, поставим коэффициент «2» перед
формулой H2.
Т.к. мы уравняли количество атомов всех элементов, наша схема
стала уравнением, поэтому заменим стрелку на знак =
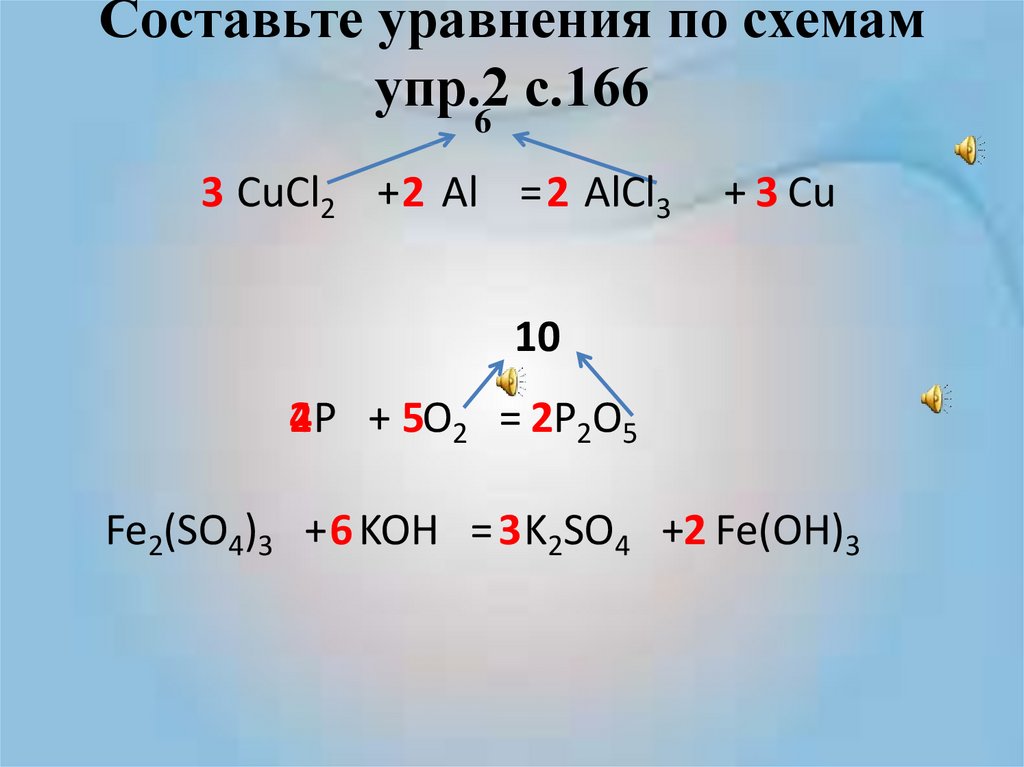
6. Составьте уравнения по схемам упр.2 с.166
63 CuCl2 + 2 Al = 2 AlCl3
+ 3 Cu
10
4P + 5O2 = 2P2O5
2
Fe2(SO4)3 + 6 KOH = 3 K2SO4 +2 Fe(OH)3
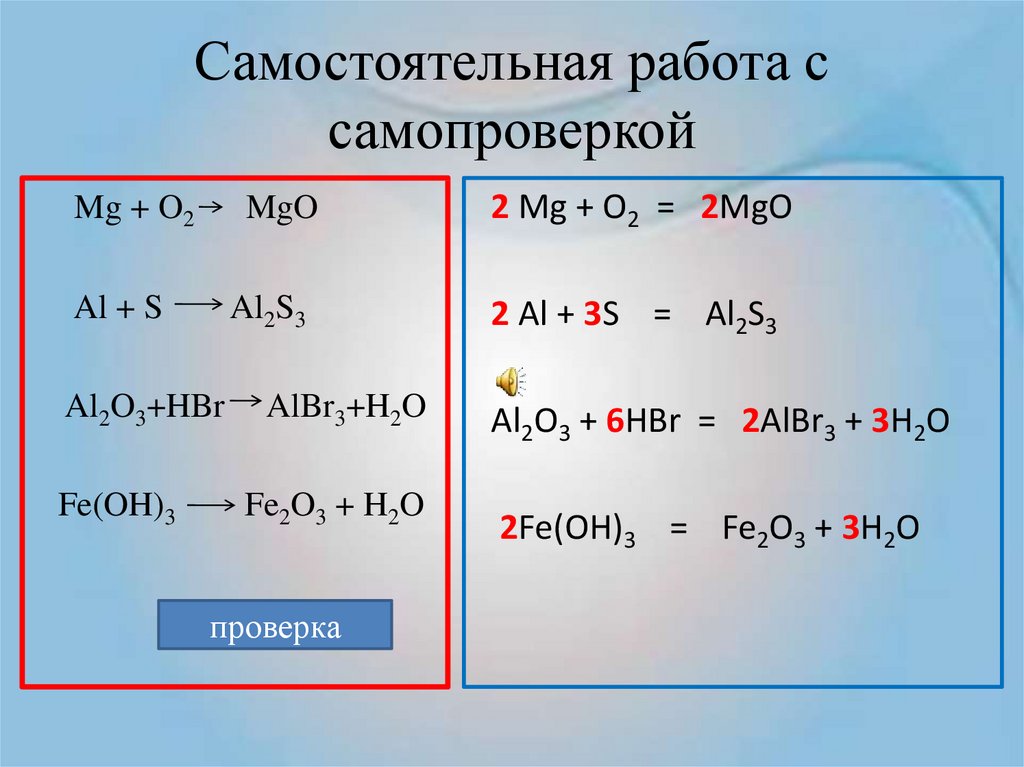
7. Самостоятельная работа с самопроверкой
Mg + O2MgO
Al + S
Al2S3
Al2O3+HBr
Fe(OH)3
AlBr3+H2O
Fe2O3 + H2O
проверка
2 Mg + O2 = 2MgO
2 Al + 3S = Al2S3
Al2O3 + 6HBr = 2AlBr3 + 3H2O
2Fe(OH)3 = Fe2O3 + 3H2O
8. Записать уравнения реакций по словесным схемам упр.3 с.167
Фосфорная кислота + гидроксид натрияфосфат натрия + вода
+
-
+
3=
H3PO4 + 3NaOH
Na3PO4 +3H2O
Оксид
натрия + вода
-2
+
Na O + H2O =2NaOH
+
2
гидроксид натрия
проверка
9. Составьте уравнения реакций
Серная кислота + гидроксид алюминия =сульфат алюминия + вода проверка
+
2-
3+
-
3+
2-
3H2SO4 + 2 Al(OH)3 = Al2(SO4)3 + 6 H2O
дальше
Фосфат натрия + нитрат кальция
фосфат
проверка
кальция + нитрат натрия
+
3-
2+
-
2+
3-
+
-
2 Na3PO4 + 3 Ca(NO3)2 = Ca3(PO4)2 + 6NaNO3
10. Вставьте в уравнения формулы пропущенных веществ и расставьте коэффициенты
MgO + HNO3 = … + H2OFe(OH)3 + HCl = … + …
Al2O3 + … = Al2(SO4)3 + H2O
Al2O3 + H2 = Al + …
проверка
11.
MgO + 2HNO3 = Мg(NO3)2 + H2OFe(OH)3 + 3HCl = FeCl3 + 3H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
Al2O3 + 3H2 = 2Al + 3H2O
12. Использованная литература
Химия 8 класс О.С.Габриелян Москва, изд.Дрофа, 2013г.
Настольная книга учителя химии
Москва, изд. Дрофа, 2002г.










 chemistry
chemistry








