Similar presentations:
Подготовительные курсы для абитуриентов химического факультета БГУ
1. Подготовительные курсы «Абитуриент химического факультета БГУ»
ст. преподаватель кафедрынеорганической химии БГУ Цобкало
Жанна Анатольевна
Тел.7797097 мтс и вел
Vk. com
2. ЗАНЯТИЯ БЕСПЛАТНЫЕ!
Осенью: 1 день- 31октябряЗимой: 2 дня (22 декабря)+ День открытых дверей.
ОВР, кинетика и катализ,
избранные главы неорганической химии;
избранные главы органической химии;
решение комбинированных задач по химии;
ЗАПИШИТЕ или вышлите ТЕМЫ ДЛЯ РАССМОТРЕНИЯ!
Весной: 30 марта+ День открытых дверей.
решение нестандартных задач и конкурсных
заданий.
Возможна переписка!
3. Особенности ЦТ по химии
• Часть А – 1 правильный ответ 38 заданийУбираем НЕ!; сначала отвечаем, потом ищем
ответ; исключаем неправильные; все время
отвечаем себе на вопросы Что это? и Почему?
• Часть Б – открытый ответ 12 заданий
Правильно пишем
Округляем до целого, в каждую клеточку по 1
заглавному символу или цифре. ☺ «пратон»
С
А
3
(
Р
О
4
)
2
4. Какой признак процесса НЕ может сопровождать физическое явление:
1) образование осадка3) изменение цвета
2) появление запаха
4) образование нового
вещества
5. При температуре 800С массовая доля вещества в насыщенном водном растворе составляет 32,8%, а при температуре 00С – 13,5%.
Укажите название вещества:1) аммиак ;
3) сера ;
2)сульфат железа (II);
4) хлорид серебра(I).
6. Укажите сумму коэффициентов в реакции окисления этина оксидом меди(II)
7. C2H2+ CuO → CO2 + H2O + Cu
8. 1C2H2+5CuO → 2CO2 + 1H2O + 5Cu
9. Особенности ЦТ по химии
• ЭКОНОМИМ ВРЕМЯ:черновик, М,
быстрая запись, min коэффициентов…
• Справочные материалы на ЦТ:
таблица ПСХЭ;
таблица растворимости: не смотрим _____
ЭХРНМ: после водорода _____
Ряд ЭО!!!: Сl N O F
Калькулятор, черновик, 1-2 гелевые ручки
Нижний порог – до 15 б.
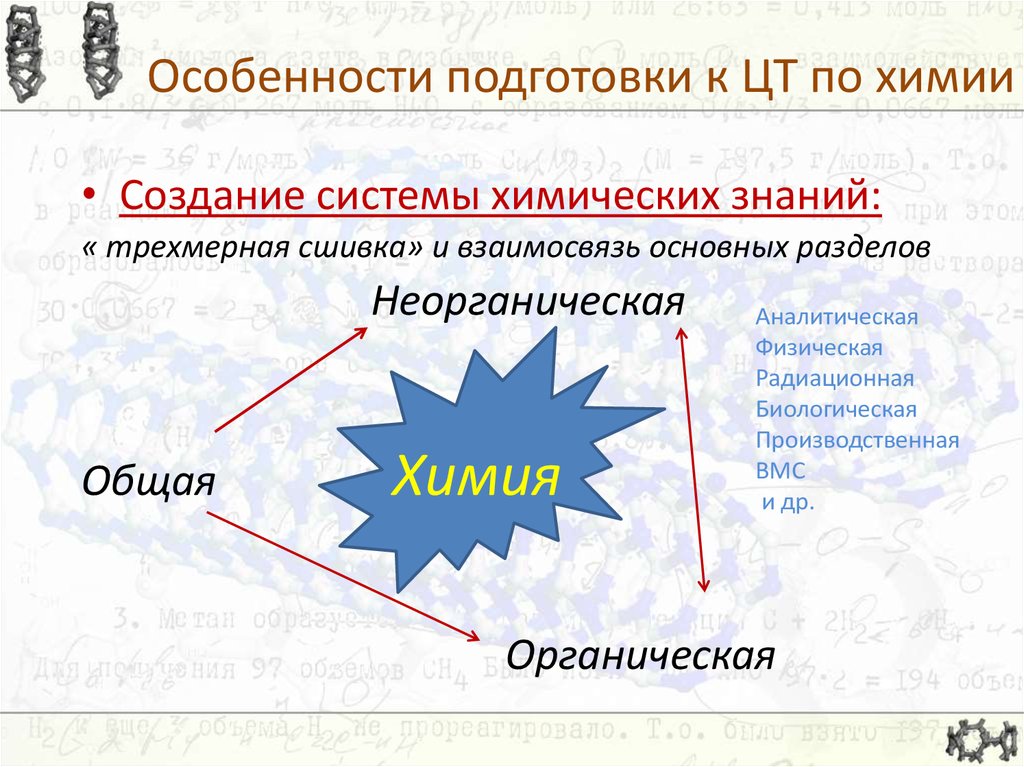
10. Особенности подготовки к ЦТ по химии
• Создание системы химических знаний:« трехмерная сшивка» и взаимосвязь основных разделов
Неорганическая
Общая
Химия
Аналитическая
Физическая
Радиационная
Биологическая
Производственная
ВМС
и др.
Органическая
11.
Почему химию многие«боятся?»
12. Почему химию многие «боятся?»
• Химию невозможно «вызубрить»- ее необходимо понять!!!!
Развитие логического, абстрактного и
математического мышления
• Чтобы химию понять –
необходимо кое-что «вызубрить»
Тривиальные названия,
латинские названия некоторых элементов, числительных,
постоянные (Мвозд, NA, Vm н.у., Ar (Cl), R, ρHOH, ___),
ИСКЛЮЧЕНИЯ! (в каком случае их нет?)
13. Развитие мышления
логического –построение логических рассуждений, схем;
абстрактного – моделирование;
математического – устный счет.
ПРАКТИКА не менее 25 решенных!!! задач в
неделю
+ min 50 заданий тестов.
14.
тривиальные названия (рассылка)Развесить на все видимые места,
ежедневно просматривать
Сода кристаллическая – …кальцинированная –…
питьевая – …
каустическая – …
Числительные
1 – моно, 2- ди, 3-три, 4-тетра, 5- пента,
6- гекса, 7-гепта, 8-окта, 9-нано, 10 – дека(дец-)
15. ПРИЕМЫ ЗАПОМИНАНИЯ
• Опорные конспекты и графическиеизображения
• Укрупнение фактов и закономерностей
• Мнемонические правила
16. Графическое отображение информации
ХИМИЯ АЗОТА17.
Только восстановительные свойства за счетатома азота проявляет:
1) гидразин;
2) оксид азота (III);
3) аммиак;
4) гидроксиламин.
Аммиак бывает кислотой? окислителем?
18. Укрупнение информации
ТЕРМИЧЕСКОЕ РАЗЛОЖЕНИЕ НИТРАТОВПРОДУКТЫ ЭЛЕКТРОЛИЗА В РАСТВОРЕ
?
19.
На катодеДо Аl
Ион
H2O
(от Al до H]
Ме не восст-ся
2HOH+2ē →H2 + 2OH-
На аноде
После Н
Men+ + nē→Me
не восст-ся
-ид (кроме F-)
-ит
До ПВ
Сl2, Br2, I2, S
не окисл-ся
-ат
не окисляется
до –ат
2HOH-4ē →O2 +4H+
Вывод:
На катоде металл (кроме тех, кто реагирует с водой)
+ Н2 (кроме тех, кто «важнее водорода»)
На аноде Сl2, Br2, I2, S ИЛИ О2
20.
При электролизе растворов каких веществна катоде выделяется водород?
При электролизе растворов каких веществ
на аноде выделяется кислород?
а) сульфид натрия б) бромид меди
в) нитрат цинка
г) серная кислота д) гидроксид калия
21. МНЕМОНИКА в химии
• экзо- и эндотермические процессы:с термином «экзо» ассоциируются экзотические
страны, в которых обычно тепло, а эн-д-д-до холодно
• по гласным и согласным буквам для электролиза и ГЭ
на Аноде Окисление, на Катоде Восстановление,
• Амфотерные оксиды: вода БЕсЦеНный ЖАХ!!!
ЖАХ – еще и пассивируется в конц HNO3 и H2SO4
• PV=nRT («пора вставать на работу»)
• Написание циклической
формулы глюкозы
22. Комбинируем приемы
окислитель(Ox) –грабительвосстановитель(Red)
Взял ē – Восстановился
-4
-3
-2
Отдал ē –Окислился
Атом
-1
0
+1
+2
+3
+4
• Восстановление
MnO4• KMnO4 +H2SO4 + KNO2→
• KMnO4 +С2Н4 →
+5
+6
+7
+8
23. Комбинируем приемы
NH4NO3N2
N2O
NO
NO2 НNО3(конц)
НNО3(разб)
Продукты восстановления азотной кислоты
Слабые восстановители – неметаллы,
металлы после Н
Сильные восстановители – щел. и щ/зем
металлы
Пассивируются в конц ЖАХ!!!
24. Указать, в каком случае продуктом реакции является оксид азота (IV)
а) электролиз нитрата натрия;б) взаимодействие конц. азотной кислоты с
серебром;
в) самопроизвольное разложение оксида азота (III);
г) длительное взаимодействие азота с изб.
кислорода;
д) термическое разложение нитрата меди;
е) взаимодействие разб. азотной кислоты с магнием.
Правильные ответы:
25. б, в, Г?, д
26.
Цобкало Ж. А., Сечко О. И. Домашний исследовательский эксперимент в 10классе // Хiмiя: праблемы выкладання.– 2003.– №3.– С. 46–61






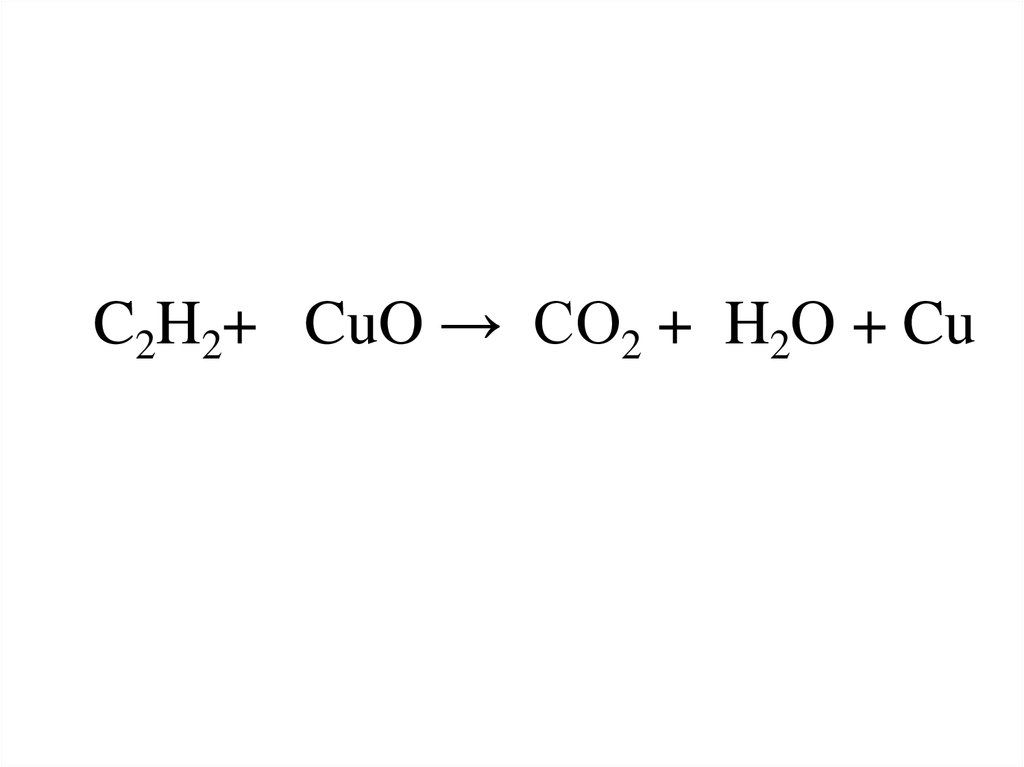
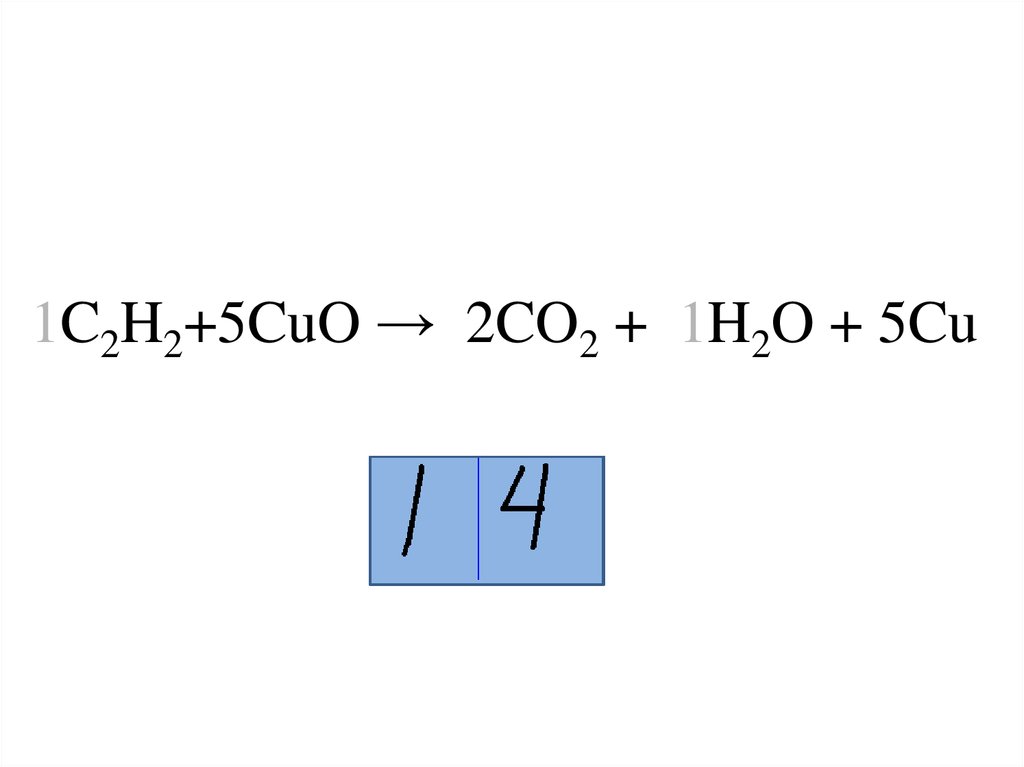

















 chemistry
chemistry education
education








