Similar presentations:
Гликоконъюгаты: структура и функции протеогликанов и гликопротеинов
1. Гликоконъюгаты: структура и функции протеогликанов и гликопротеинов.
Санкт-Петербургский государственный университетГликоконъюгаты: структура и
функции протеогликанов и
гликопротеинов.
Презентацию выполнил:
Кренев Илья, 2 курс
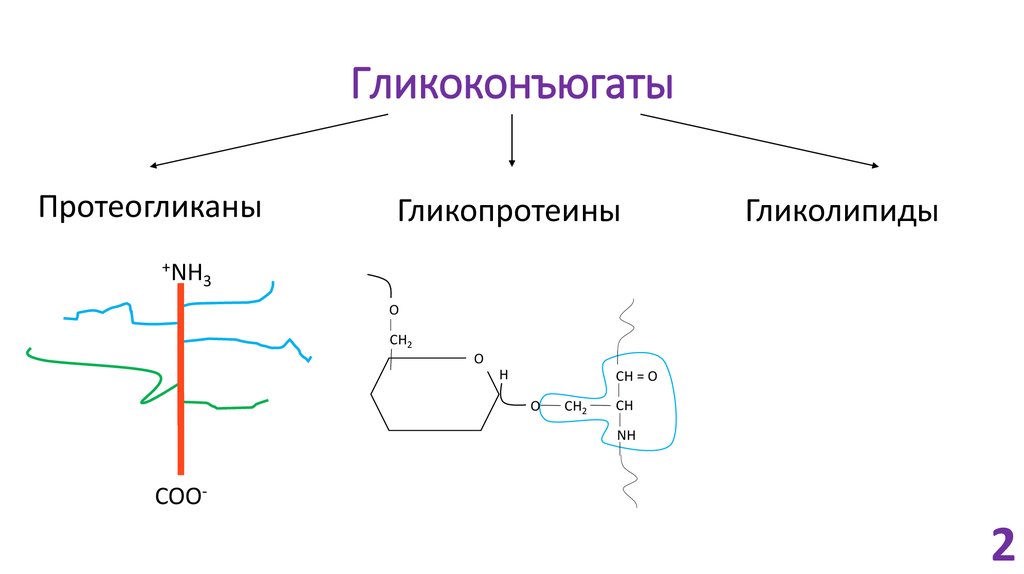
2. Гликоконъюгаты
Протеогликаны+NH
Гликопротеины
Гликолипиды
3
O
CH2
O
H
CH = O
O
CH2
CH
NH
COO-
2
3. Протеогликаны
• На поверхности клеток и во внеклеточном матриксе (основнойкомпонент);
• Одна или несколько цепей ГАГ связаны ковалентной связью с
мембранным или секретируемым белком;
• Цепь ГАГ может прикрепляться к внеклеточным белкам за счёт
электростатических взаимодействий;
• Клетки млекопитающих синтезируют около 40 типов ПГ.
3
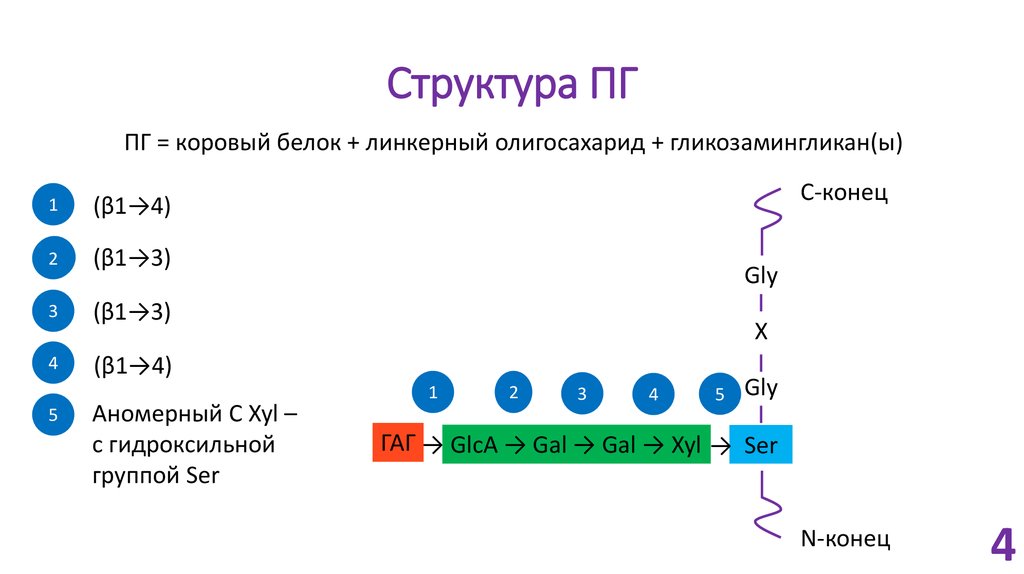
4. Структура ПГ
ПГ = коровый белок + линкерный олигосахарид + гликозамингликан(ы)1
(β1→4)
21
(β1→3)
3
(β1→3)
4
(β1→4)
5
Аномерный C Xyl –
с гидроксильной
группой Ser
C-конец
Gly
X
1
2
3
4
5
Gly
ГАГ → GlcA → Gal → Gal → Xyl → Ser
N-конец
4
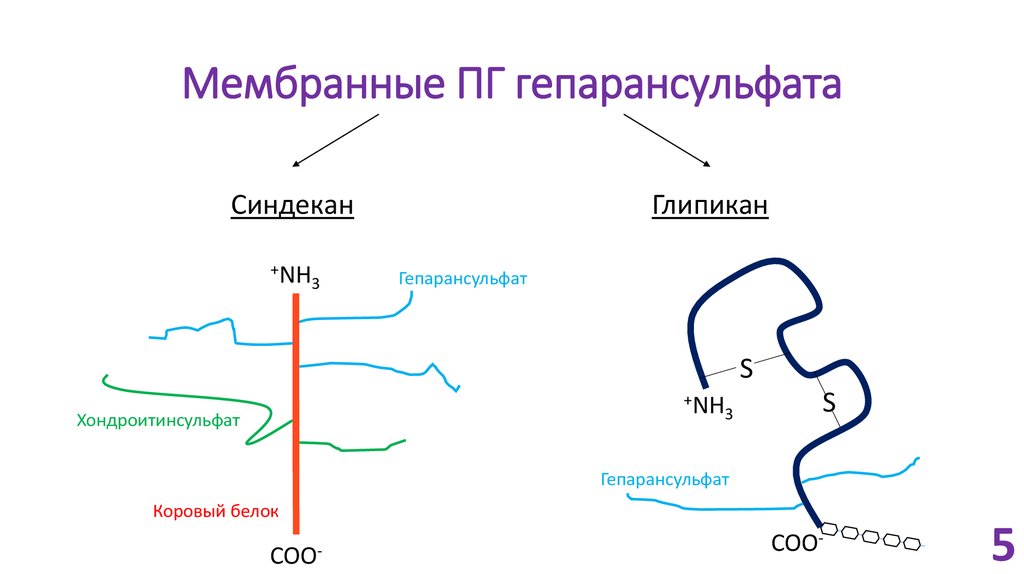
5. Мембранные ПГ гепарансульфата
Синдекан+NH
3
Глипикан
Гепарансульфат
S
+NH
Хондроитинсульфат
3
S
Гепарансульфат
Коровый белок
COO-
COO-
5
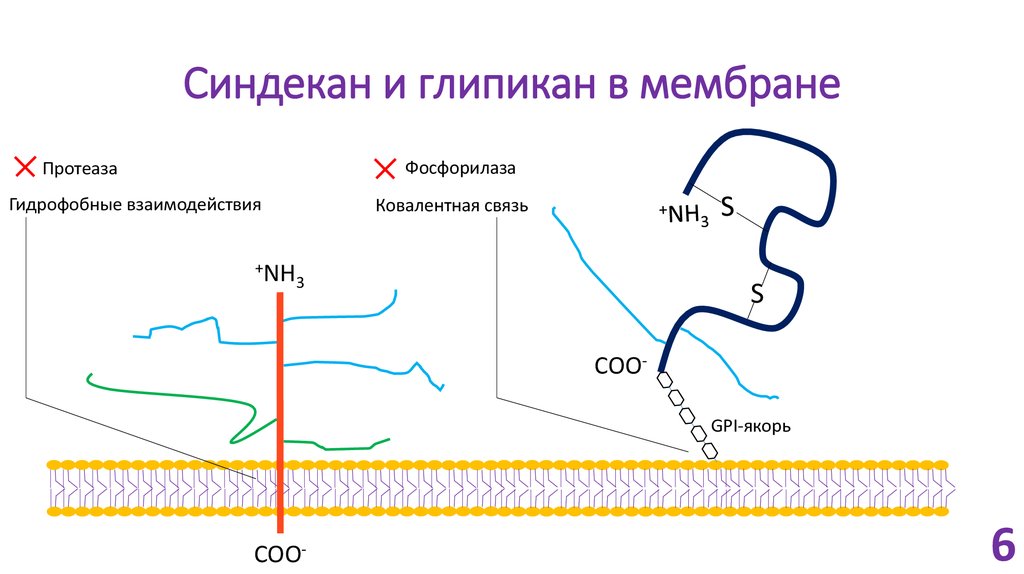
6. Синдекан и глипикан в мембране
ФосфорилазаПротеаза
Гидрофобные взаимодействия
+NH
Ковалентная связь
3
S
COOGPI-якорь
COO-
6
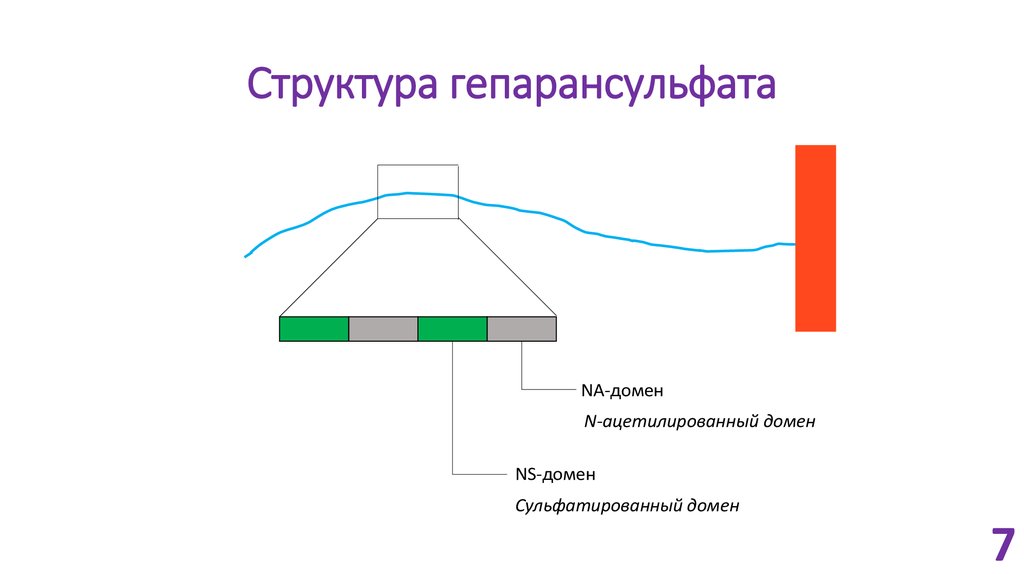
7. Структура гепарансульфата
NA-доменN-ацетилированный домен
NS-домен
Сульфатированный домен
7
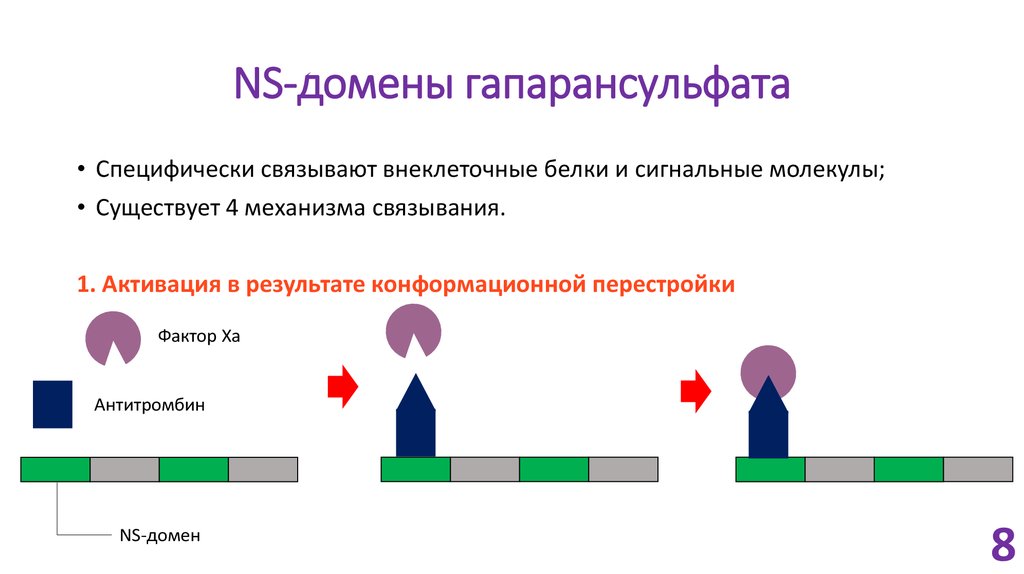
8. NS-домены гапарансульфата
• Специфически связывают внеклеточные белки и сигнальные молекулы;• Существует 4 механизма связывания.
1. Активация в результате конформационной перестройки
Фактор Xa
Антитромбин
NS-домен
8
9.
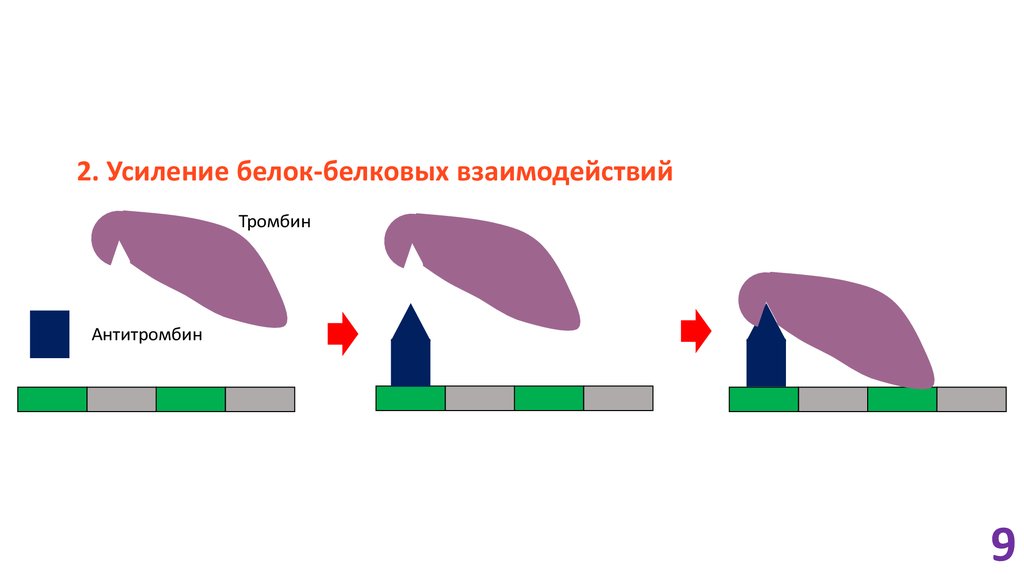
2. Усиление белок-белковых взаимодействийТромбин
Антитромбин
9
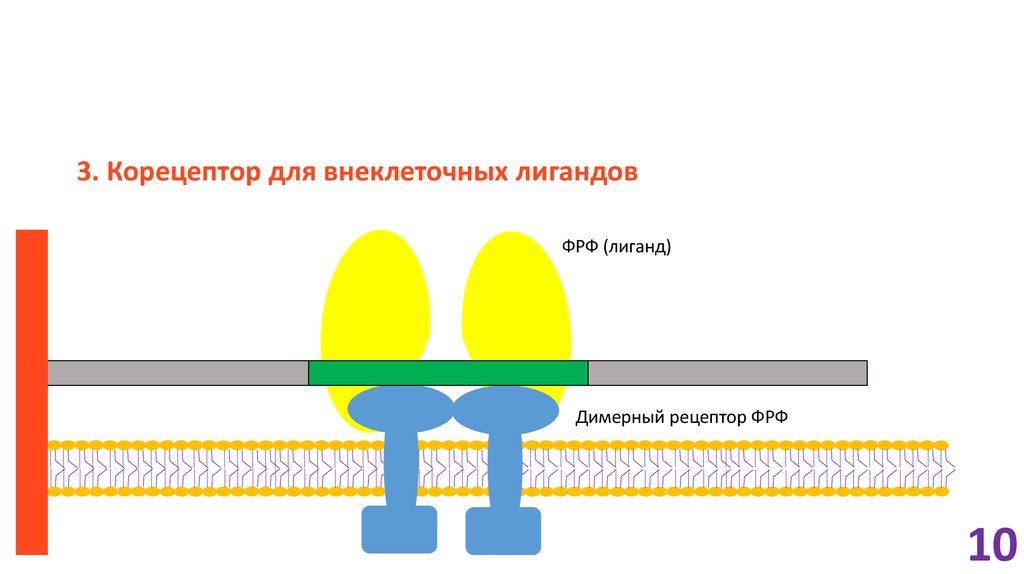
10.
3. Корецептор для внеклеточных лигандовФРФ (лиганд)
Димерный рецептор ФРФ
10
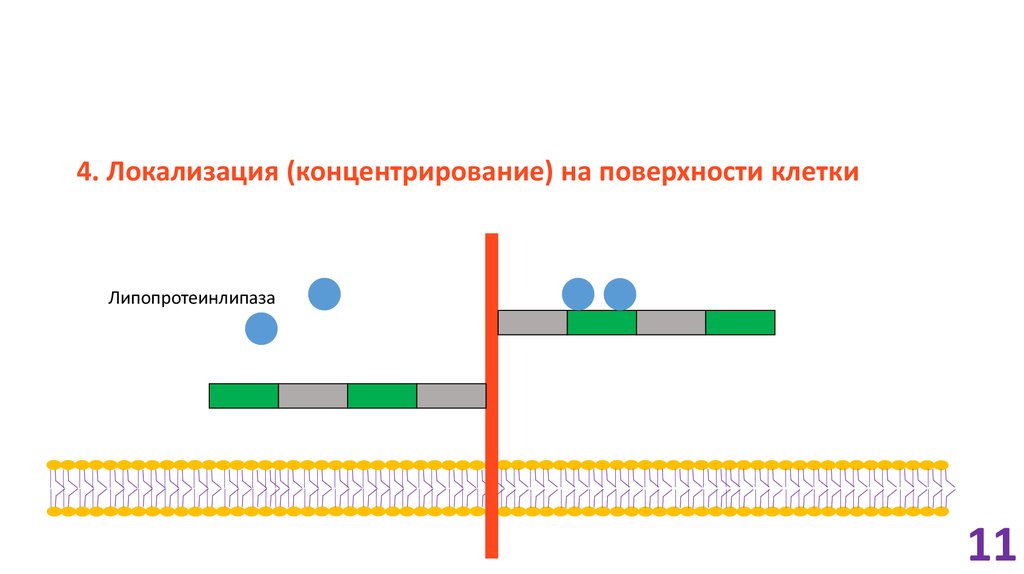
11.
4. Локализация (концентрирование) на поверхности клеткиЛипопротеинлипаза
11
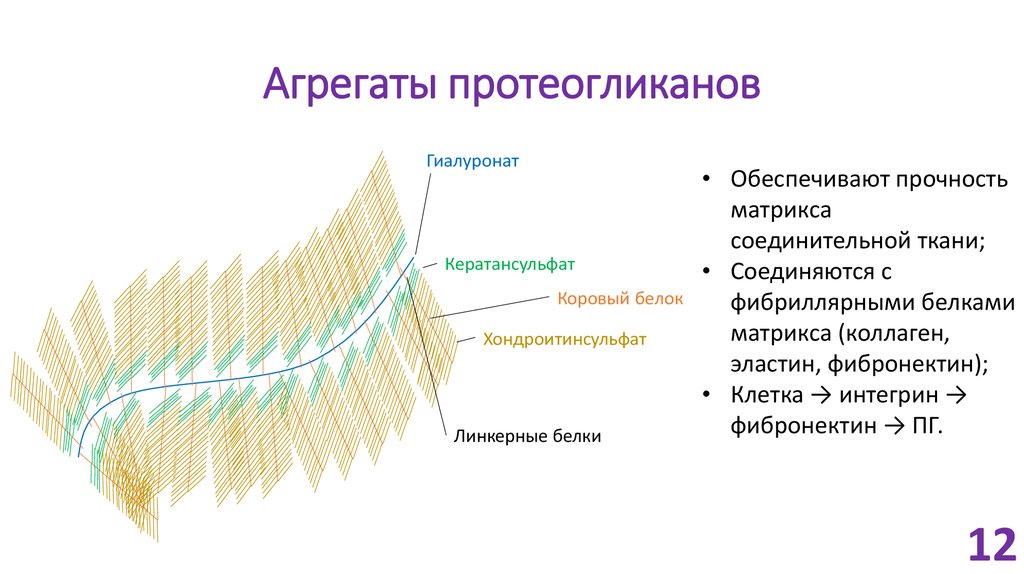
12. Агрегаты протеогликанов
ГиалуронатКератансульфат
Коровый белок
Хондроитинсульфат
Линкерные белки
• Обеспечивают прочность
матрикса
соединительной ткани;
• Соединяются с
фибриллярными белками
матрикса (коллаген,
эластин, фибронектин);
• Клетка → интегрин →
фибронектин → ПГ.
12
13. Гликопротеины
• Конъюгаты белков и углеводов (ковалентная связь);• На внешней поверхности ЦПМ, во внеклеточном матриксе и в
крови;
• Углеводные цепи короче и разнообразнее, чем цепи ГАГ в ПГ;
• Углеводная часть может составлять от 1 до 70% массы ГП;
• Олигосахариды ГП несут много информации, образуют
высокоспецифичные сайты узнавания и высокоафинные центры
связывания лектинов;
• Примерно половина белков Mm гликозилированы;
• Около 1% генов Mm: ферменты синтеза и прикрепления
олигосахаридов.
13
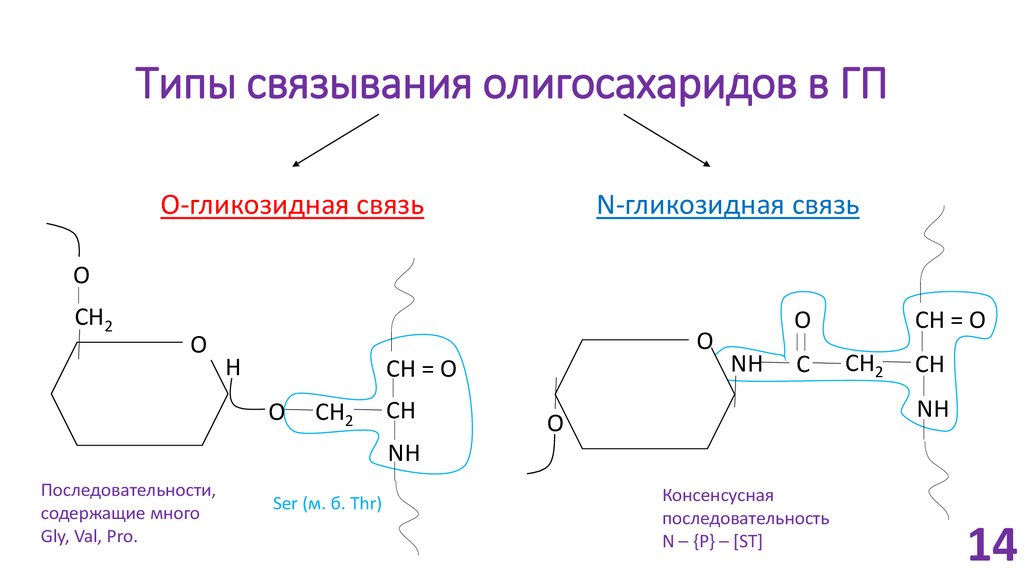
14. Типы связывания олигосахаридов в ГП
O-гликозидная связьN-гликозидная связь
O
CH2
O
O
H
CH = O
O
CH2
CH
O
NH
C
CH = O
CH2
CH
NH
O
NH
Последовательности,
содержащие много
Gly, Val, Pro.
Ser (м. б. Thr)
Консенсусная
последовательность
N – {P} – [ST]
14
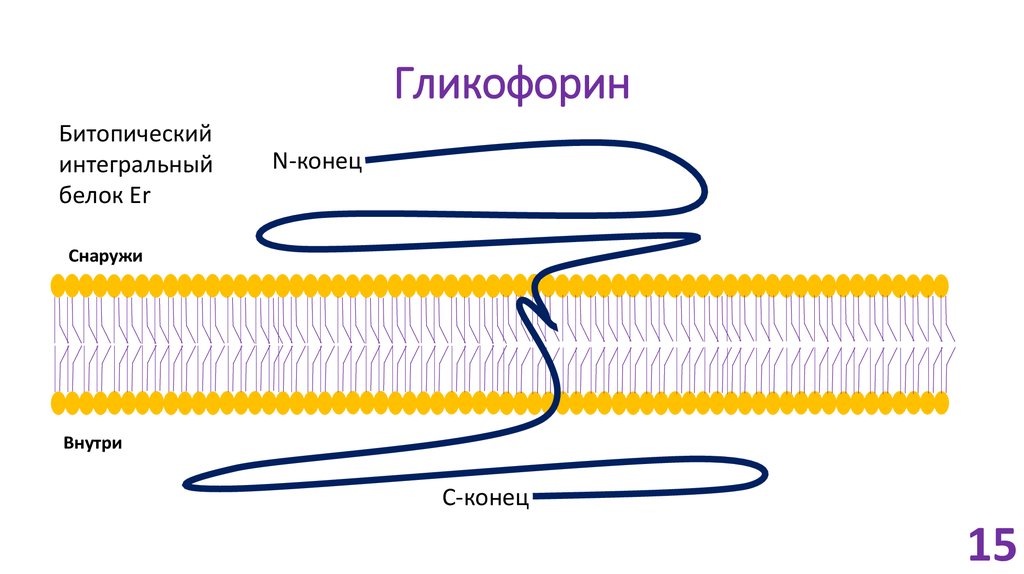
15. Гликофорин
Битопическийинтегральный
белок Er
N-конец
Снаружи
Внутри
C-конец
15
16. Гликофорин
16 олигосахаридных цепей (все – к внешнему домену).N-гликозидная связь:
O-гликозидная связь:
2S
3T
4T
10 T
11 T
12 T
13 S
14 S
15 S
22 S
25 T
37 T
44 S
47 S
50 T
26 N
16
17. Примеры гликопротеинов
• Большинство белков крови (в т. ч. Ig);• Гормоны: фолликулостимулирующий, лютеинизирующий,
тиреостимулирующий;
• Многие белки молока (в т. ч. лактальумин);
• Некоторые белки поджелудочной железы (в т. ч. рибонуклеаза);
• Большинство белков лизосом.
17
18. Функции гликозилирования белков
• Углеводородные кластеры гидрофильны → изменениерастворимости;
• Указывают на подлежащие уничтожению неправильно свёрнутые
белки;
• Отрицательно заряженные олигосахариды кластера из-за
взаимного отталкивания способствуют формированию на данном
участке вытянутой структуры;
• Иногда – защита от действия протеаз;
• Формируют «код сахаров».
18
19. Гликолипиды
• Мембранные сфинголипиды;• Гидрофильная головка, образованная олигосахаридами,
распознаёт лектины;
• В мозге и нервной ткани: проведение нервного импульса и
образование миелиновой оболочки;
• Участвуют в передаче клеточных сигналов.
19








 chemistry
chemistry