Similar presentations:
Морфологические изменения в хрусталике при катаракте
1. Свободные радикалы и болезни человека
Биофизические основыпатологии клетки
Свободные радикалы и болезни человека
Ю.А. Владимиров, А.Н. Осипов
2018
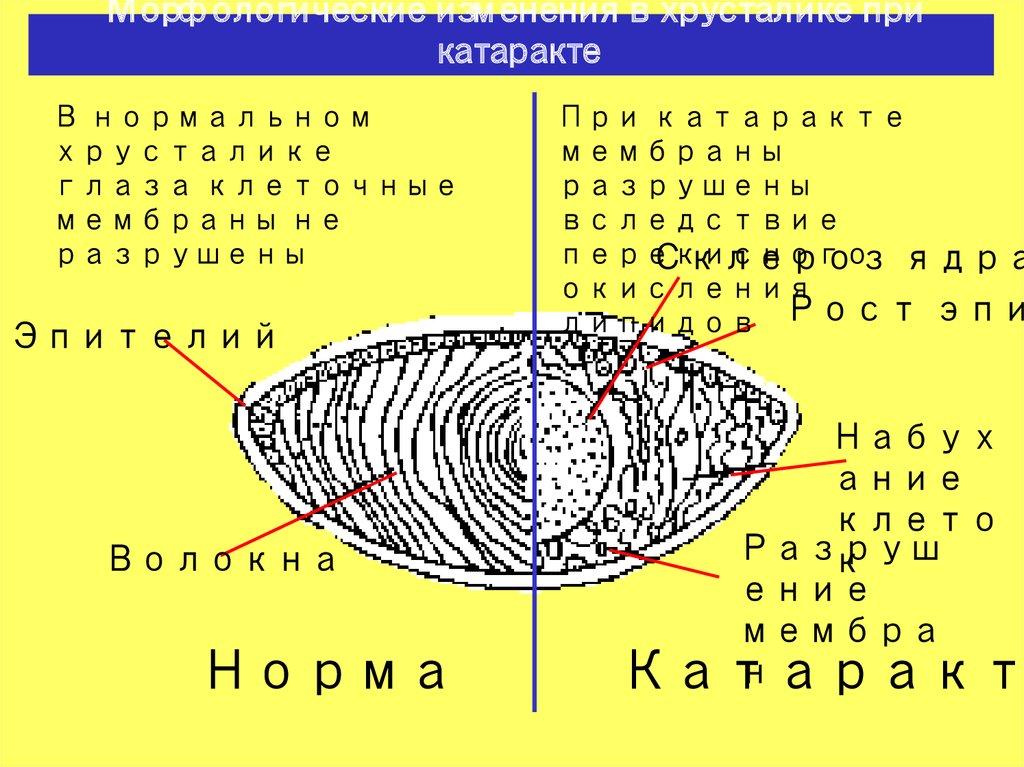
2. Морфологические изменения в хрусталике при катаракте
Морфологическиеиз
менениявхруст
аликепри
кат
аракт
е
В нормальном
хрусталике
глаза клеточные
мембраны не
разрушены
Эпителий
Волокна
Норма
При катаракте
мембраны
разрушены
вследствие
перекисного
Склероз ядра
окисления
липидов Рост эпи
Набух
ание
клето
Разруш
к
ение
мембра
н
Катаракт
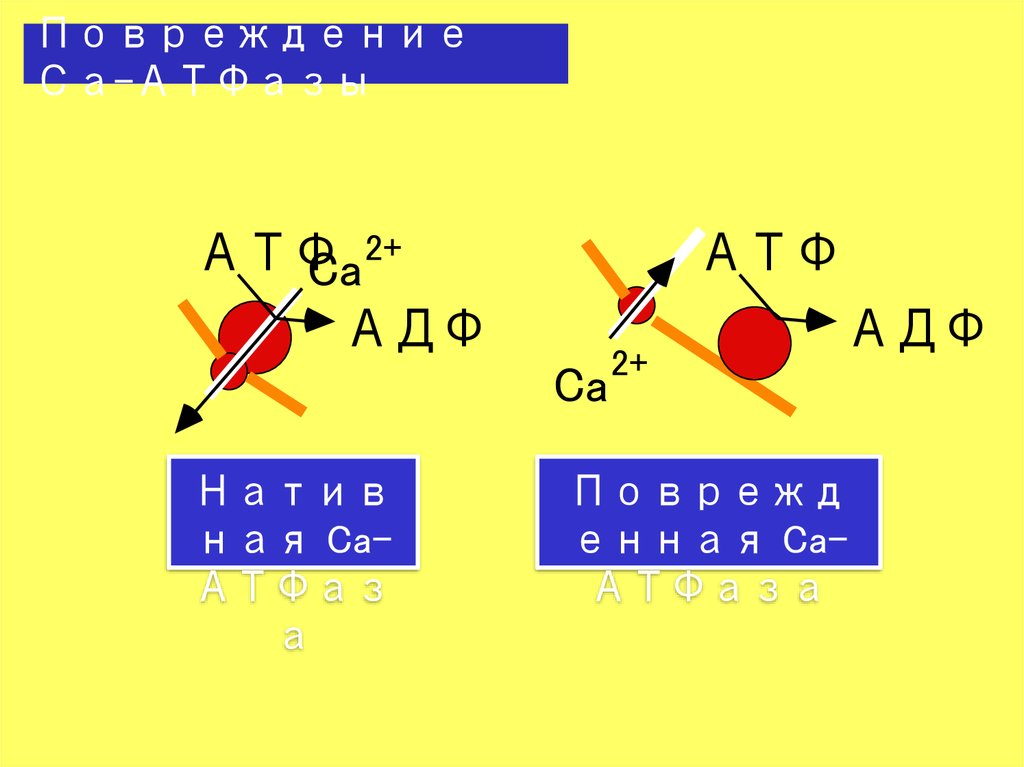
3. Повреждение Са-АТФазы
2+АТФ
Ca
АДФ
АТФ
Ca
Натив
ная CaАТФаз
а
2+
АДФ
Поврежд
енная CaАТФаза
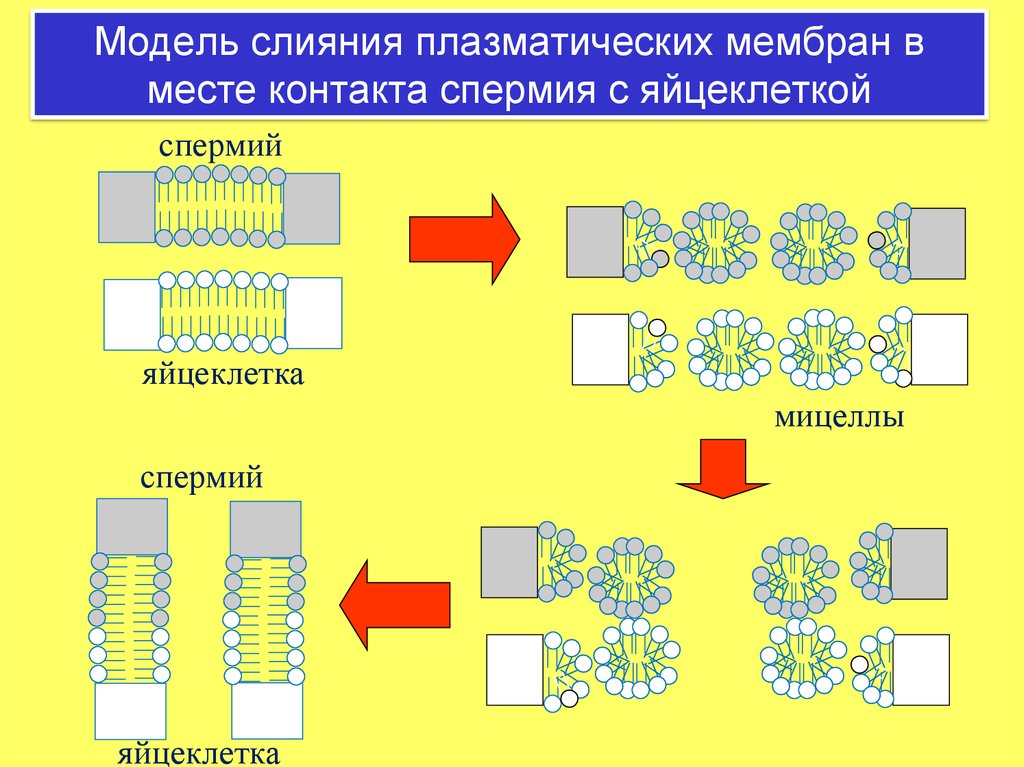
4. Модель слияния плазматических мембран в месте контакта спермия с яйцеклеткой
спермийяйцеклетка
мицеллы
спермий
яйцеклетка
5. Методы изучения реакций с участием свободных радикалов
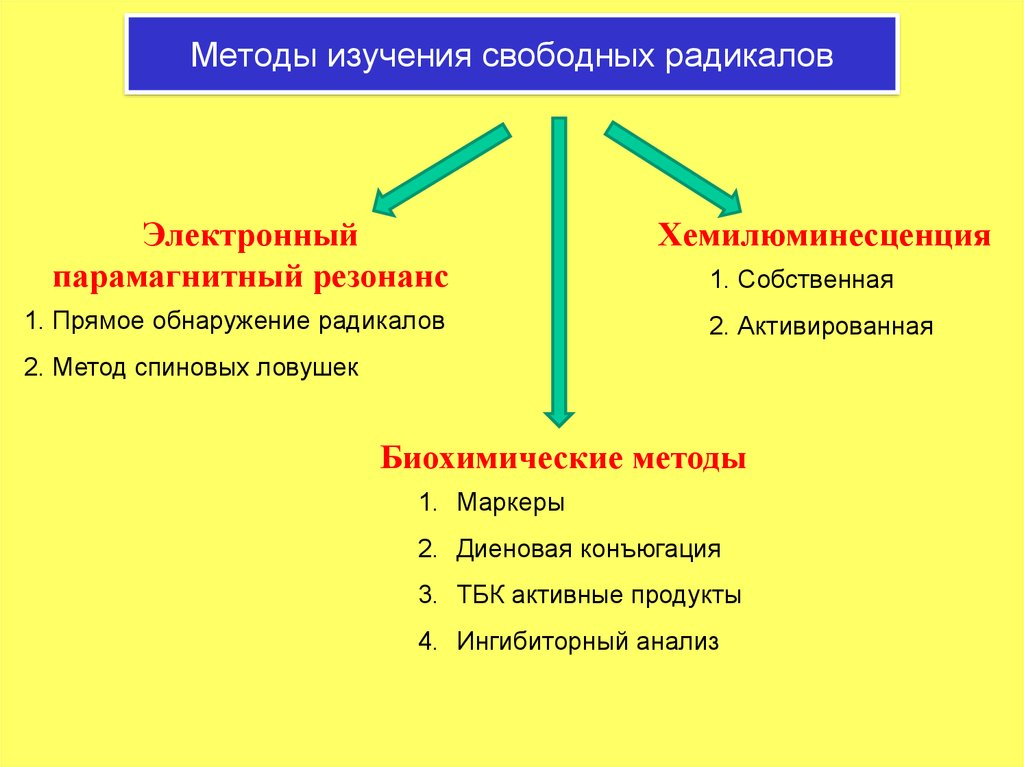
6. Методы изучения свободных радикалов
Электронныйпарамагнитный резонанс
1. Прямое обнаружение радикалов
Хемилюминесценция
1. Собственная
2. Активированная
2. Метод спиновых ловушек
Биохимические методы
1. Маркеры
2. Диеновая конъюгация
3. ТБК активные продукты
4. Ингибиторный анализ
7.
Метод электронногопарамагнитного резонанса (ЭПР)
• Прямое измерение сигнала радикалов
Сигналы стабильных радикалов
Метод быстрого смешивания
Стабилизация радикалов при низких
температурах
• Метод спиновых ловушек
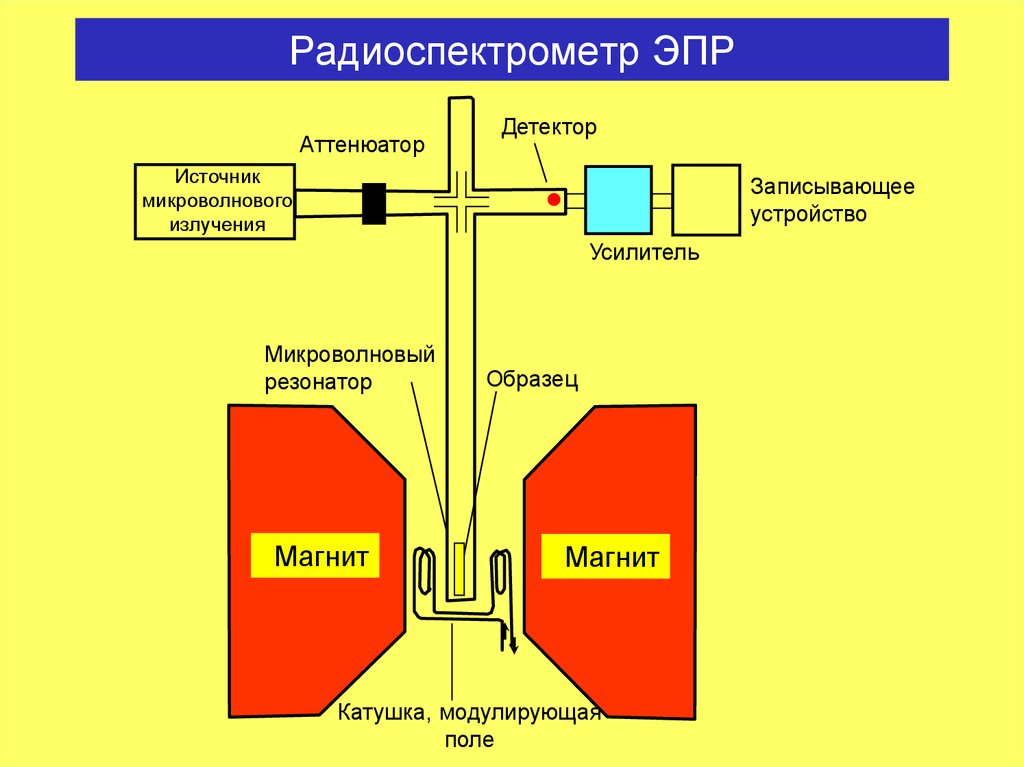
8. Радиоспектрометр ЭПР
АттенюаторДетектор
Источник
микроволнового
излучения
Записывающее
устройство
Усилитель
Микроволновый
резонатор
Магнит
Образец
Магнит
Катушка, модулирующая
поле
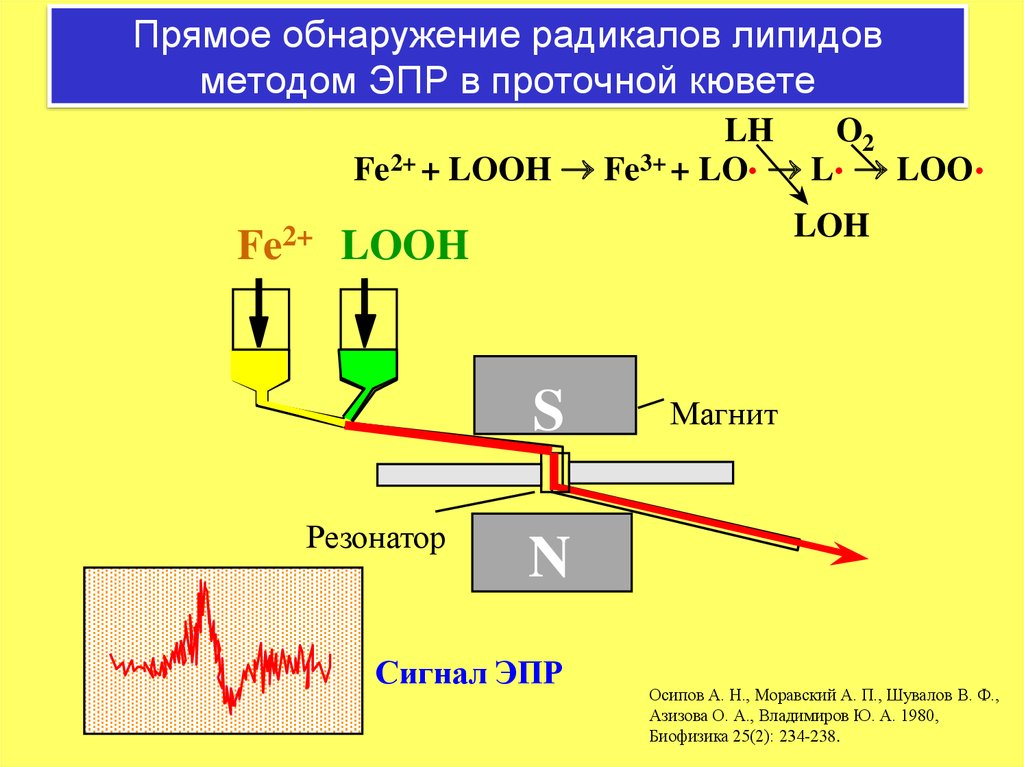
9. Прямое обнаружение радикалов липидов методом ЭПР в проточной кювете
LHO2
Fe2+ + LOOH Fe3+ + LO. L. LOO .
Fe2+
LOH
LOOH
S
Резонатор
Магнит
N
Сигнал ЭПР
Осипов А. Н., Моравский А. П., Шувалов В. Ф.,
Азизова О. А., Владимиров Ю. А. 1980,
Биофизика 25(2): 234-238.
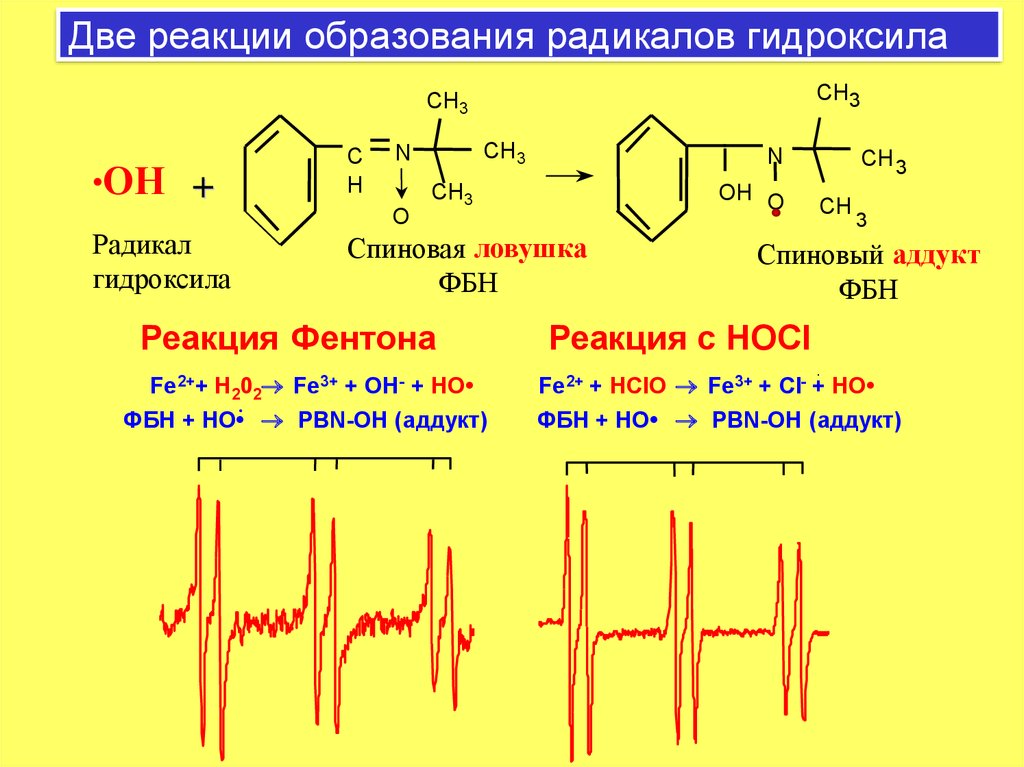
10. Две реакции образования радикалов гидроксила
CH3CH3
.ОН +
Радикал
гидроксила
C
H
CH3
N
O
N
CH3
OH O
Спиновая ловушка
ФБН
Реакция Фентона
Fe2++ H202 Fe3+ + OH- + HO
.
ФБН + HO• PBN-OH (аддукт)
CH 3
CH
3
Спиновый аддукт
ФБН
Реакция c HOCl
.
Fe2+ + HClO Fe3+ + Cl- + HO
.
.
PBN-OH (аддукт)
ФБН + HO
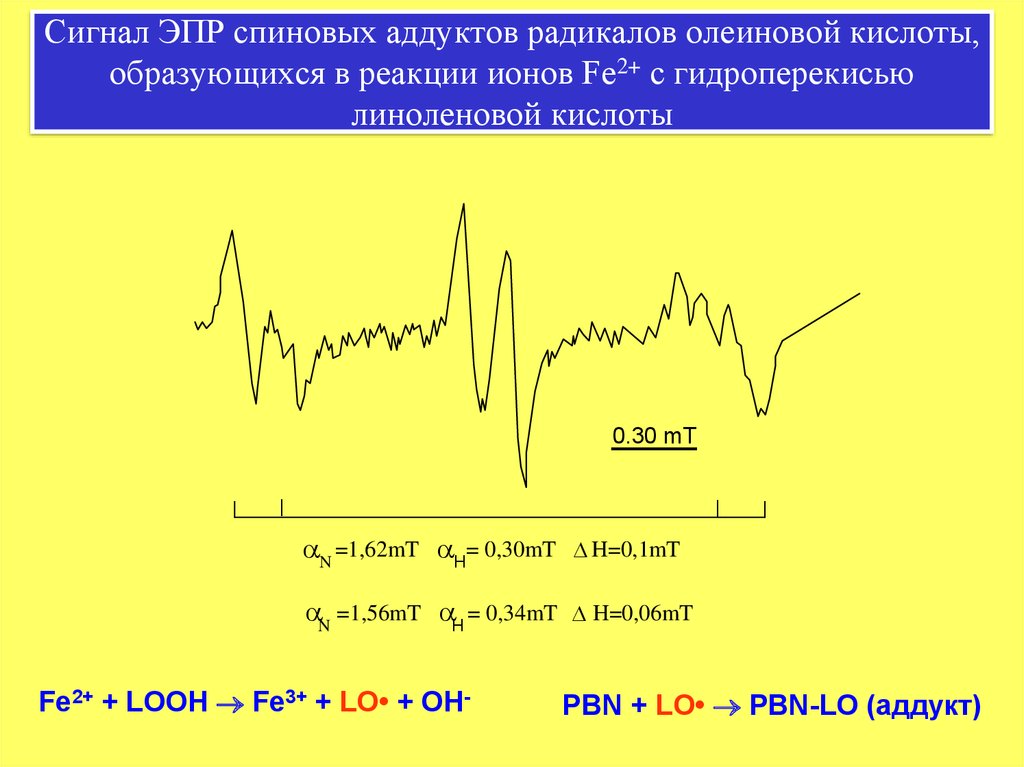
11. Сигнал ЭПР спиновых аддуктов радикалов олеиновой кислоты, образующихся в реакции ионов Fe2+ с гидроперекисью линоленовой
кислоты0.30 mT
aN =1,62mT aH= 0,30mT
D H=0,1mT
aN =1,56mT aH = 0,34mT
D H=0,06mT
Fe2+ + LOOH Fe3+ + LO• + OH-
PBN + LO• PBN-LO (аддукт)
12.
Метод хемилюминесценции• Собственная
• Активированная
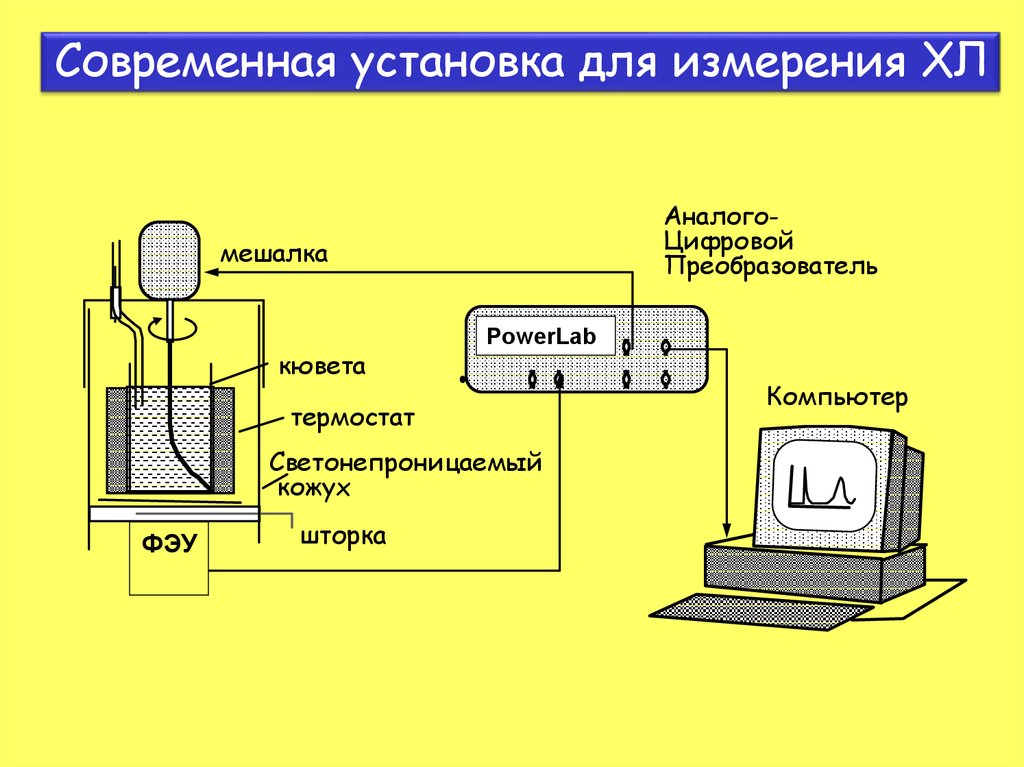
13. Современная установка для измерения ХЛ
АналогоЦифровойПреобразователь
мешалка
кювета
PowerLab
термостат
Светонепроницаемый
кожух
ФЭУ
шторка
Компьютер
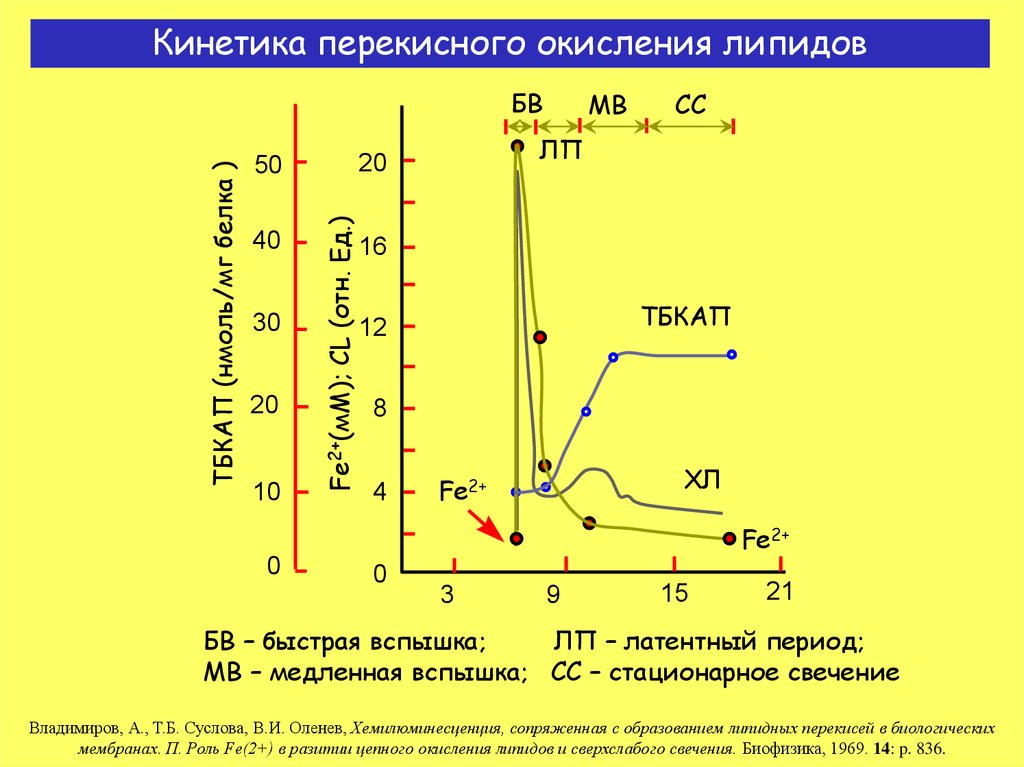
14. Кинетика перекисного окисления липидов
4030
20
10
МВ
СС
ЛП
20
50
Fe2+(мМ); CL (отн. Ед.)
ТБКАП (нмоль/мг белка )
БВ
16
ТБКАП
12
8
4
ХЛ
Fe2+
Fe2+
0
0
3
9
15
21
БВ – быстрая вспышка;
ЛП – латентный период;
МВ – медленная вспышка; СС – стационарное свечение
Владимиров, А., Т.Б. Суслова, В.И. Оленев, Хемилюминесценция, сопряженная с образованием липидных перекисей в биологических
мембранах. П. Роль Fe(2+) в разитии цепного окисления липидов и сверхслабого свечения. Биофизика, 1969. 14: p. 836.
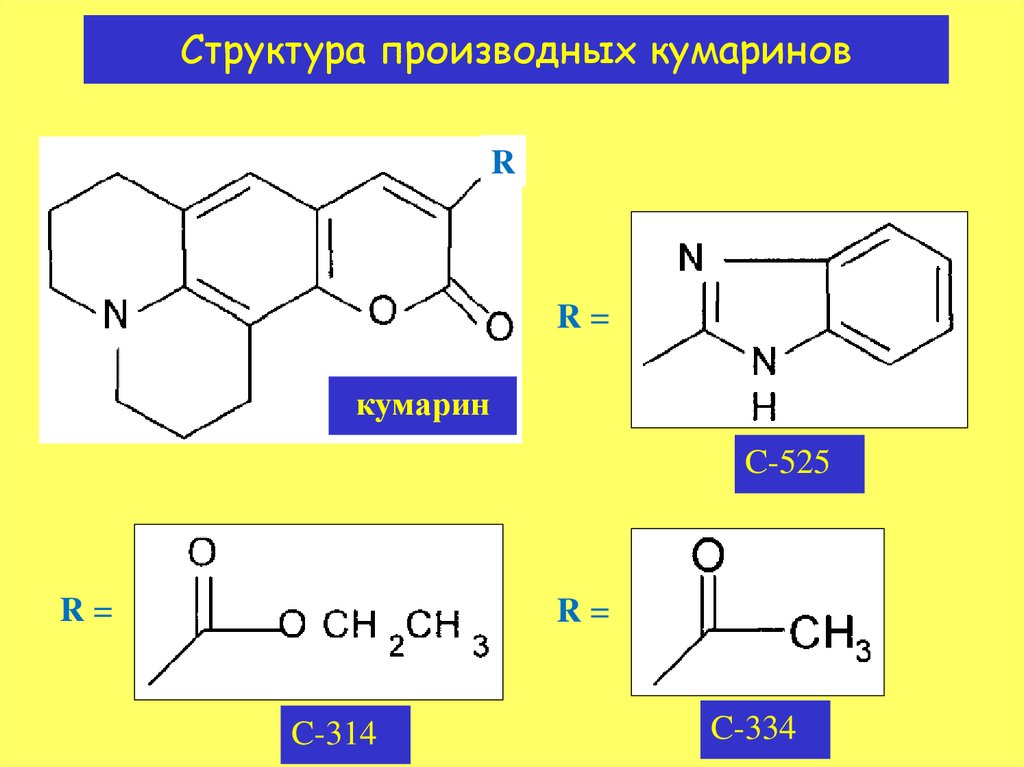
15. Структура производных кумаринов
RR=
кумарин
C-525
R=
R=
C-314
C-334
16. Биохимические методы изучения свободных радикалов
•Биомаркеры•Диеновая конъюгация
•ТБК активные продукты
•Ингибиторный анализ
17.
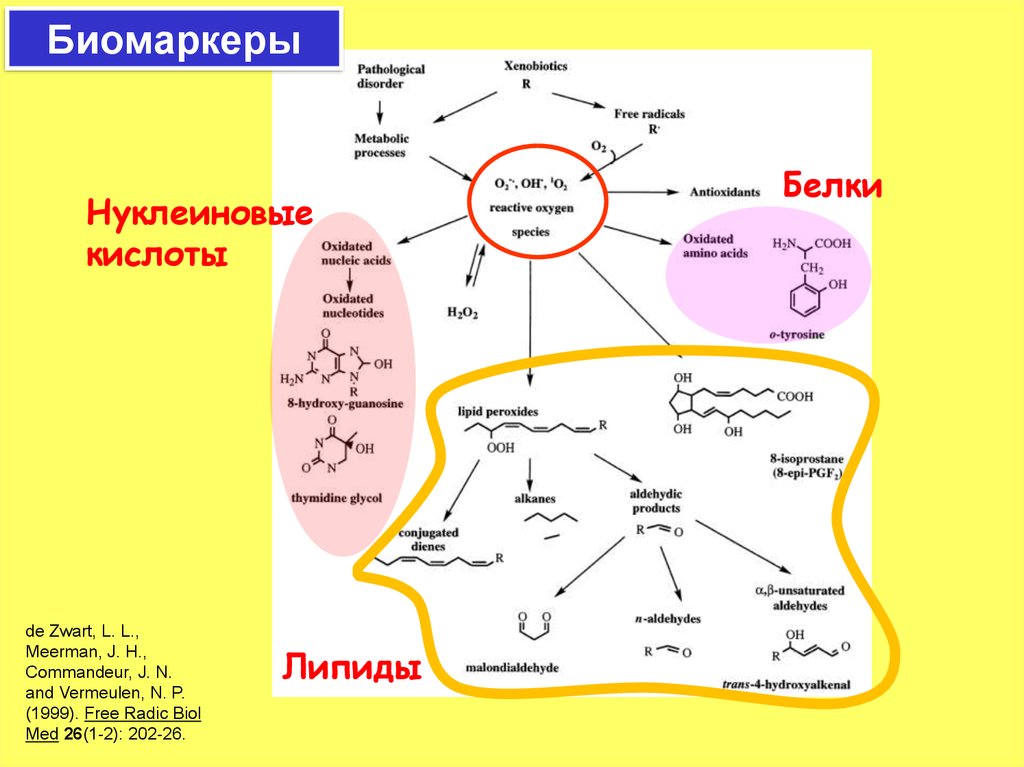
Биомаркеры18. Биомаркеры
Нуклеиновыекислоты
de Zwart, L. L.,
Meerman, J. H.,
Commandeur, J. N.
and Vermeulen, N. P.
(1999). Free Radic Biol
Med 26(1-2): 202-26.
Липиды
Белки
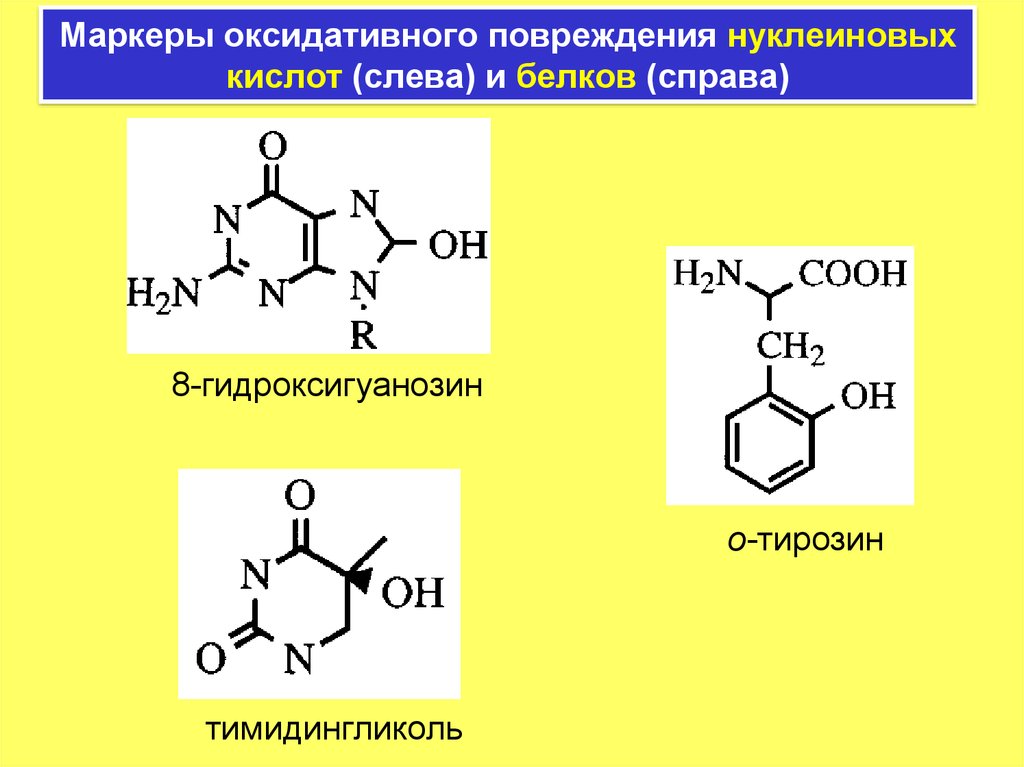
19. Маркеры оксидативного повреждения нуклеиновых кислот (слева) и белков (справа)
8-гидроксигуанозино-тирозин
тимидингликоль
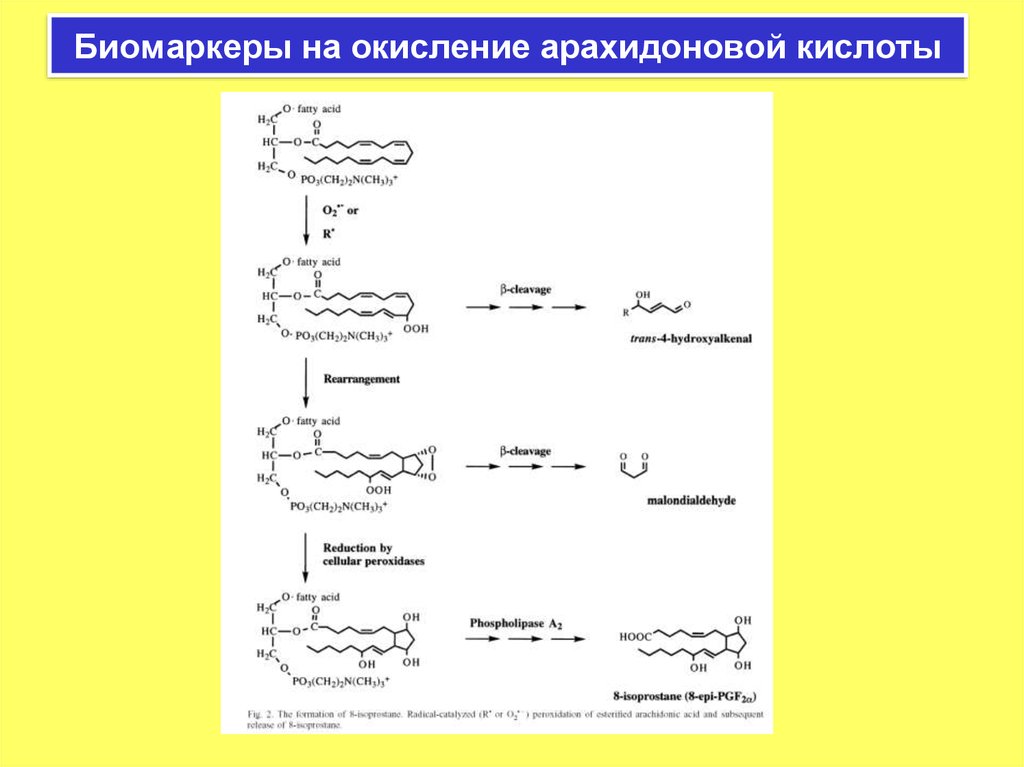
20. Биомаркеры на окисление арахидоновой кислоты
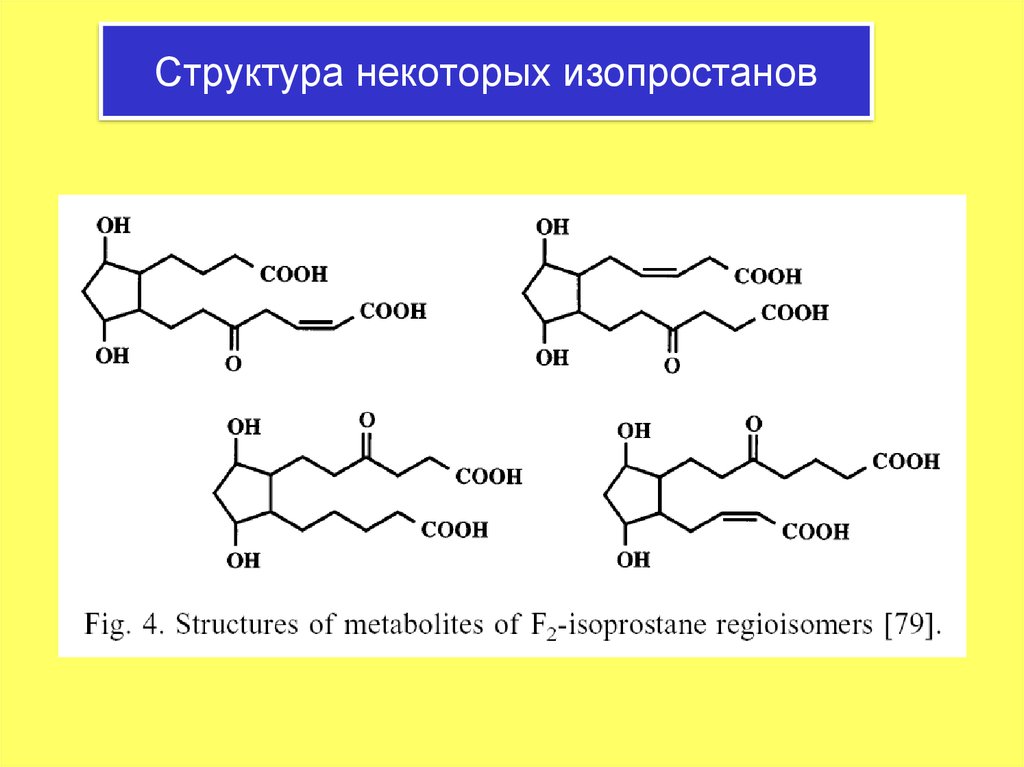
21. Структура некоторых изопростанов
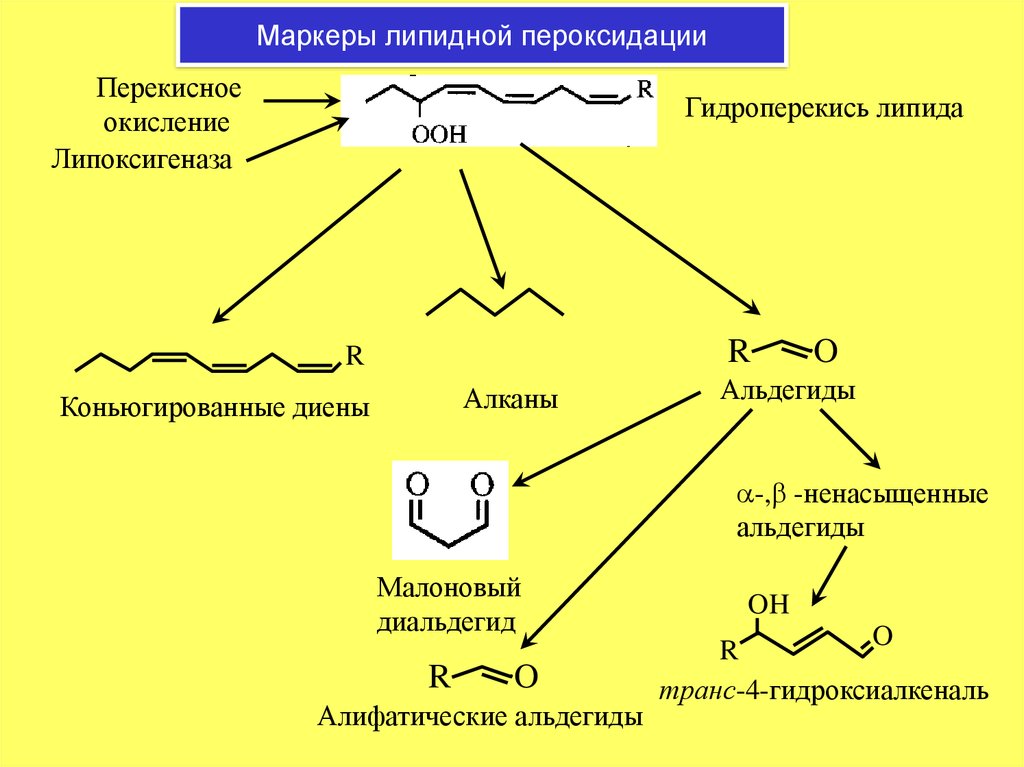
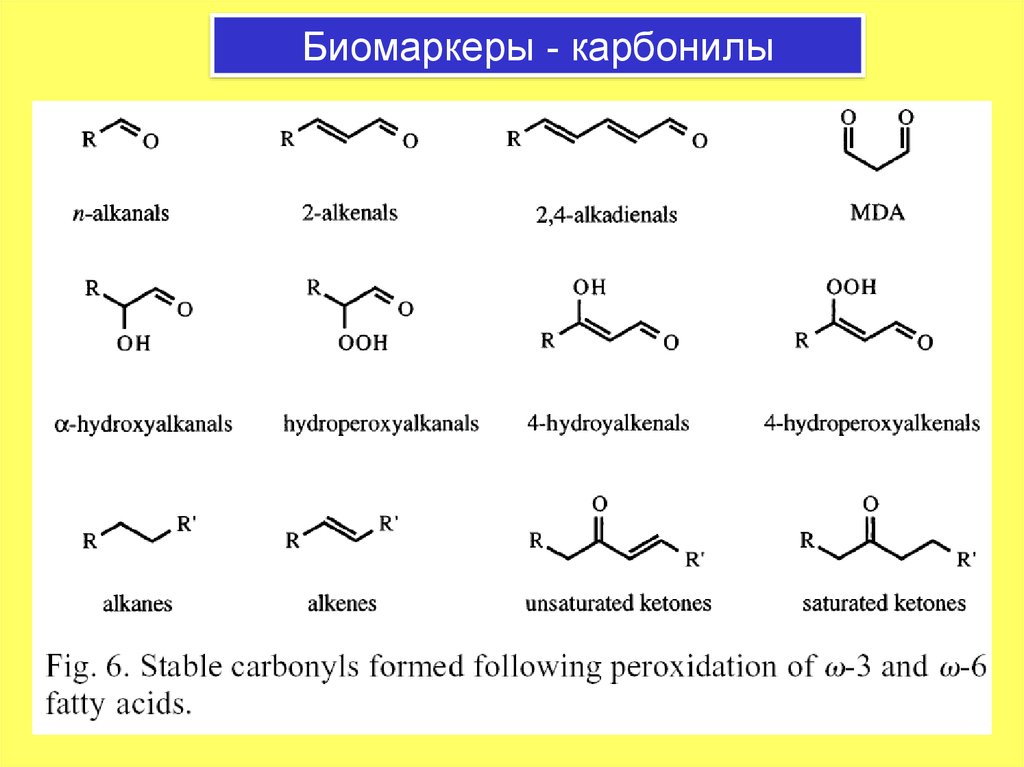
22. Маркеры липидной пероксидации
Перекисноеокисление
Липоксигеназа
Гидроперекись липида
R
R
Алканы
Коньюгированные диены
O
Альдегиды
a-,b -ненасыщенные
альдегиды
Малоновый
диальдегид
R
O
Алифатические альдегиды
OH
O
R
транс-4-гидроксиалкеналь
23. Биомаркеры - карбонилы
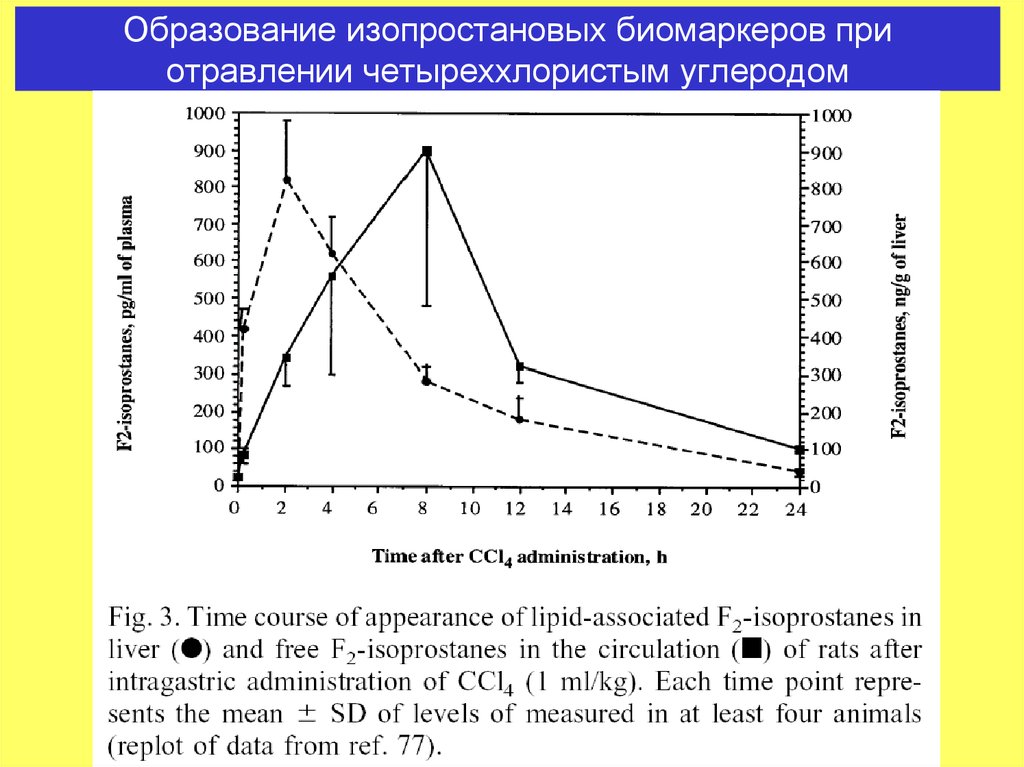
24. Образование изопростановых биомаркеров при отравлении четыреххлористым углеродом
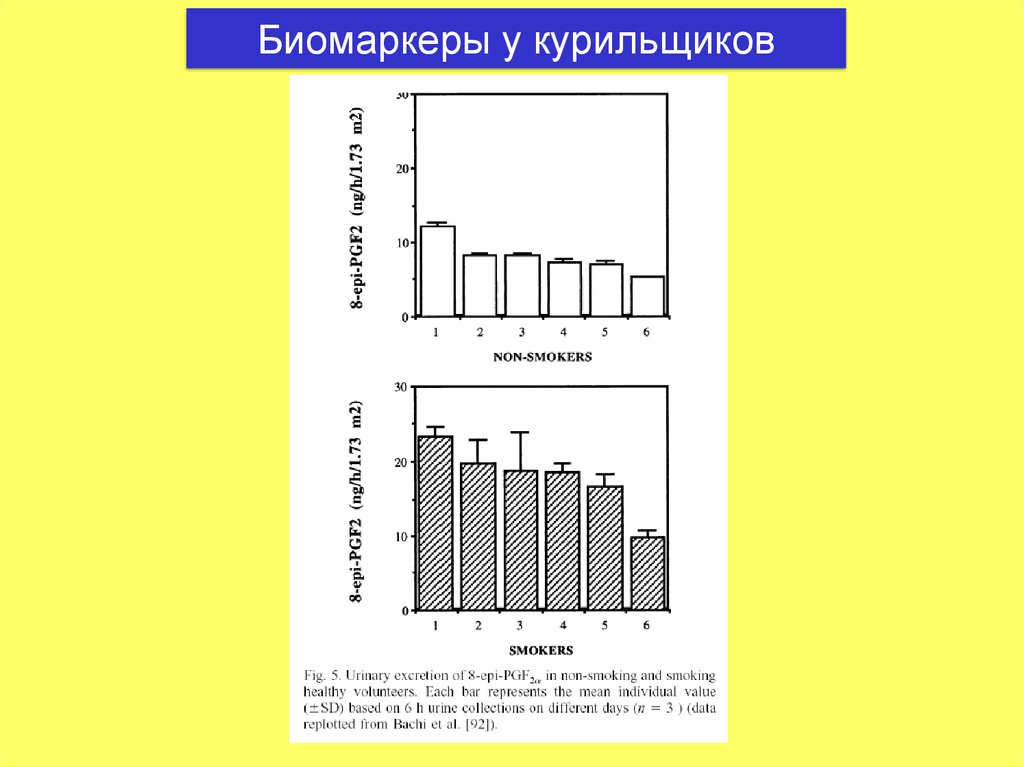
25. Биомаркеры у курильщиков
26.
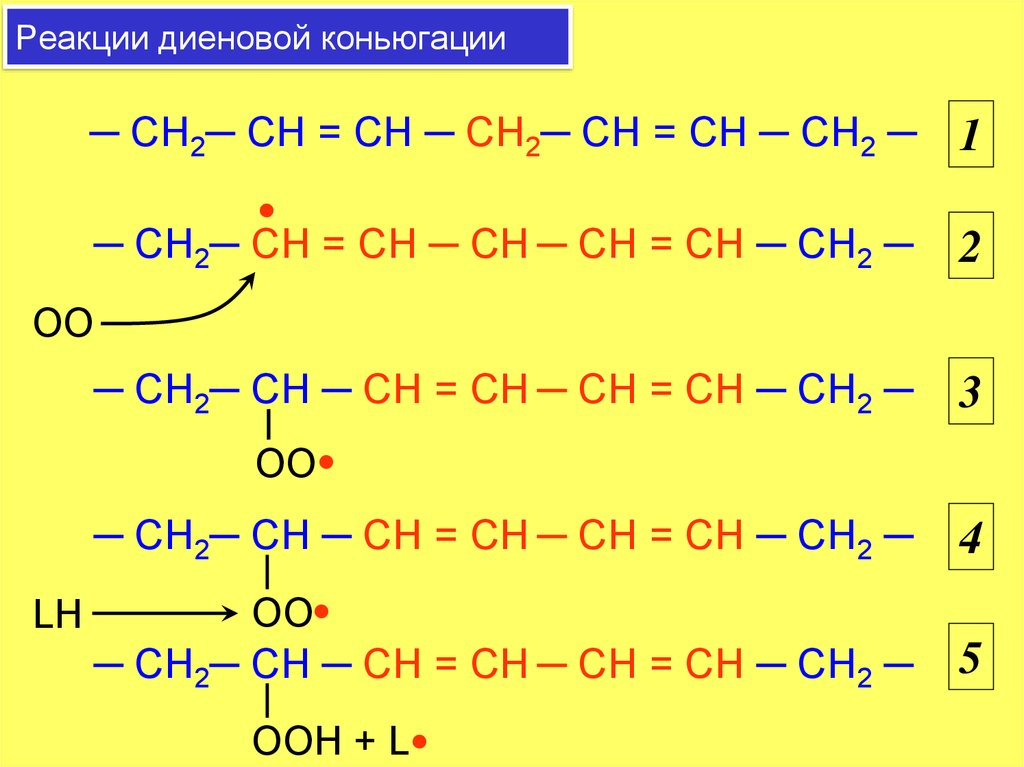
Диеновая коньюгация27. Реакции диеновой коньюгации
─ CH2─ CH = CH ─ CH2─ CH = CH ─ CH2 ─1
─ CH2─ CH = CH ─ CH ─ CH = CH ─ CH2 ─
2
OO
─ CH2─ CH ─ CH = CH ─ CH = CH ─ CH2 ─
3
OO
LH
─ CH2─ CH ─ CH = CH ─ CH = CH ─ CH2 ─
4
OO
─ CH2─ CH ─ CH = CH ─ CH = CH ─ CH2 ─
5
OOH + L
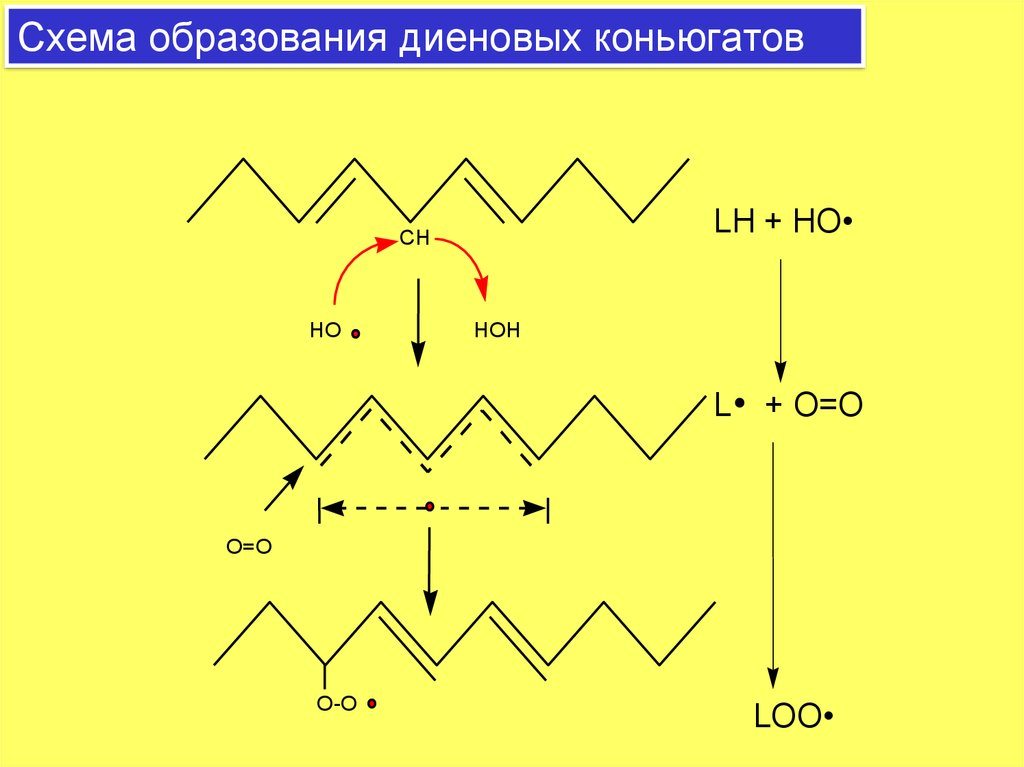
28. Схема образования диеновых коньюгатов
LH + HOCH
HO
HOH
L
+ O=О
O=O
O-O
LOO
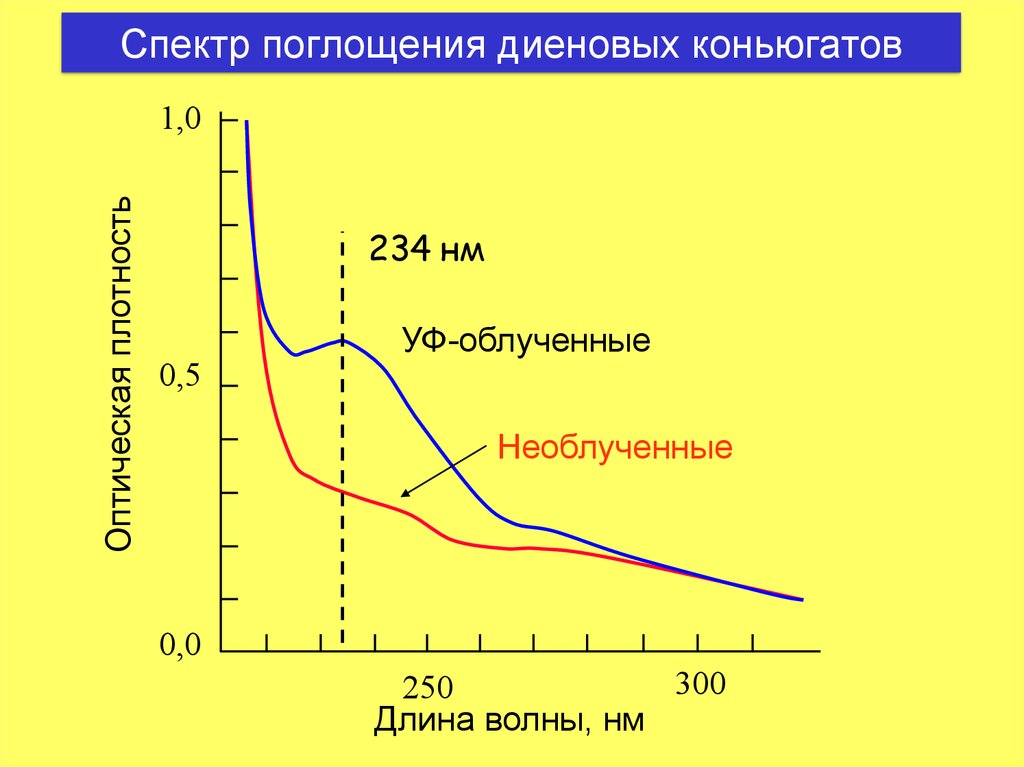
29. Спектр поглощения диеновых коньюгатов
Оптическая плотность1,0
234 нм
0,5
УФ-облученные
Необлученные
0,0
300
250
Длина волны, нм
30.
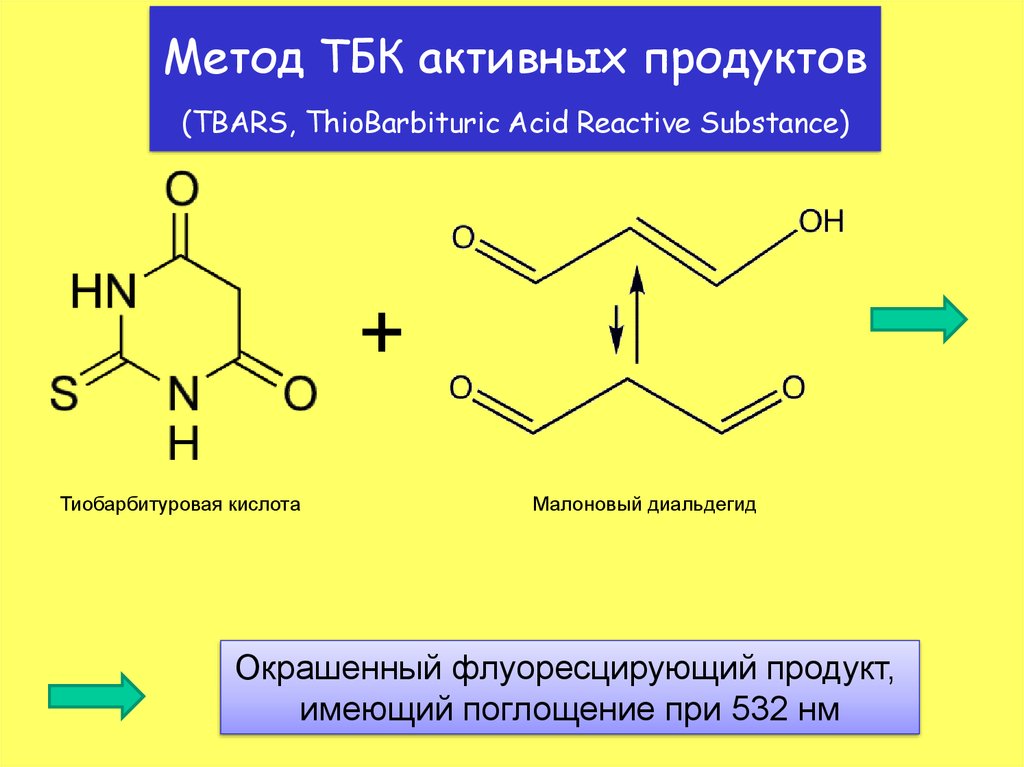
Метод с тиобарбитуровой кислотой31.
Метод ТБК активных продуктов(TBARS, ThioBarbituric Acid Reactive Substance)
+
Тиобарбитуровая кислота
Малоновый диальдегид
Окрашенный флуоресцирующий продукт,
имеющий поглощение при 532 нм
32.
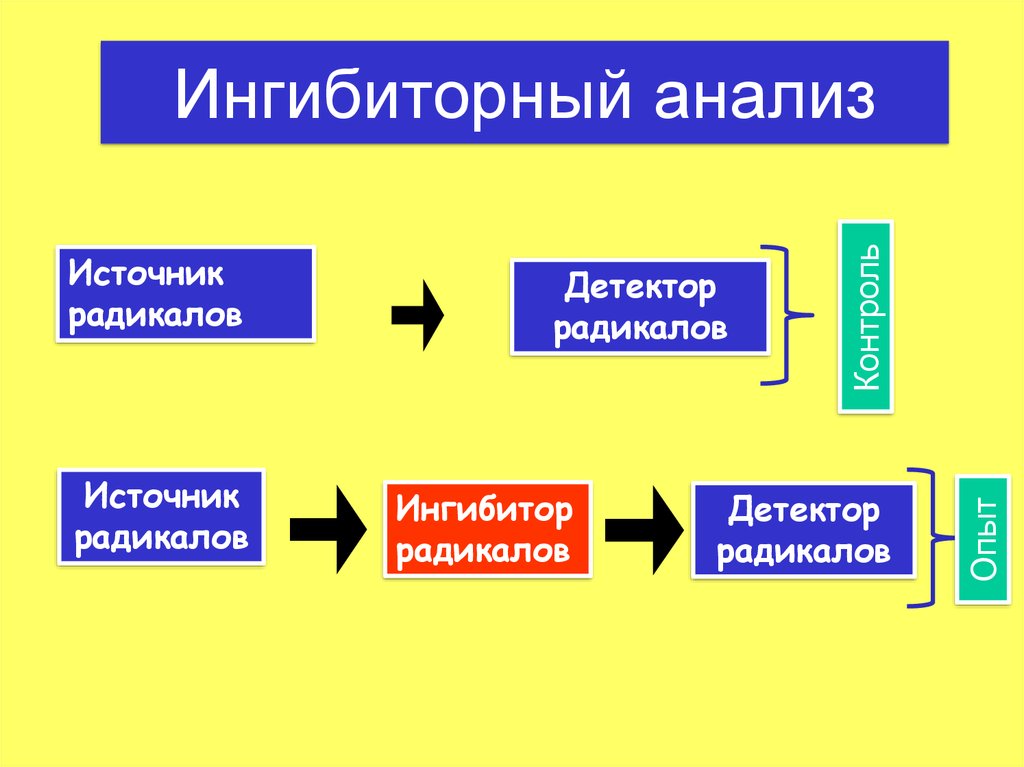
Ингибиторный анализ33. Ингибиторный анализ
Источникрадикалов
Детектор
радикалов
Ингибитор
радикалов
Детектор
радикалов
Опыт
Источник
радикалов
Контроль
Ингибиторный анализ
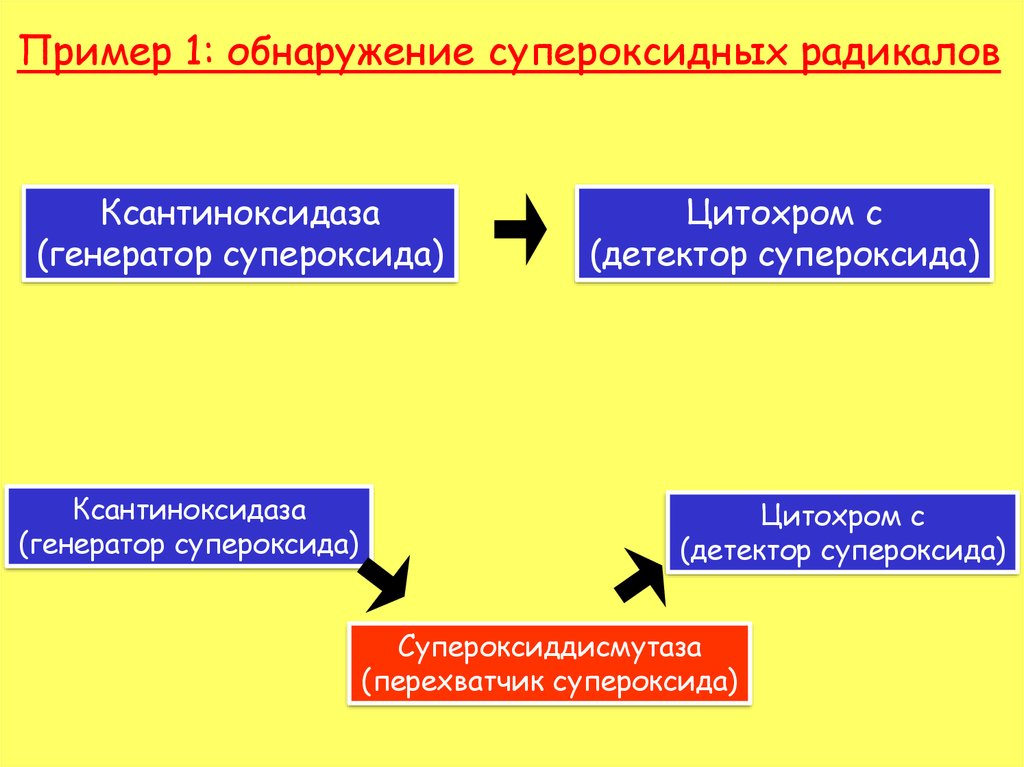
34. Пример 1: обнаружение супероксидных радикалов
Ксантиноксидаза(генератор супероксида)
Ксантиноксидаза
(генератор супероксида)
Цитохром с
(детектор супероксида)
Цитохром с
(детектор супероксида)
Супероксиддисмутаза
(перехватчик супероксида)
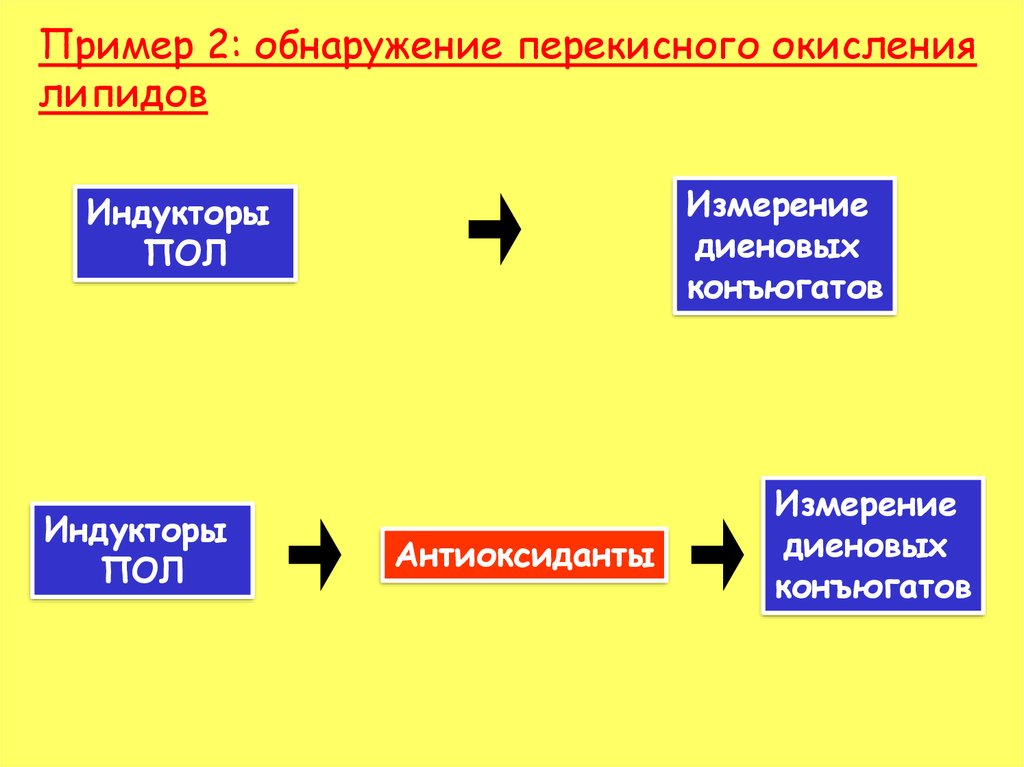
35. Пример 2: обнаружение перекисного окисления липидов
Измерениедиеновых
конъюгатов
Индукторы
ПОЛ
Индукторы
ПОЛ
Антиоксиданты
Измерение
диеновых
конъюгатов









 biology
biology chemistry
chemistry








