Similar presentations:
Аминокислоты, пептиды, белки, нуклеиновые кислоты. Их биологическая роль
1. Аминокислоты, пептиды, белки, нуклеиновые кислоты. Их биологическая роль
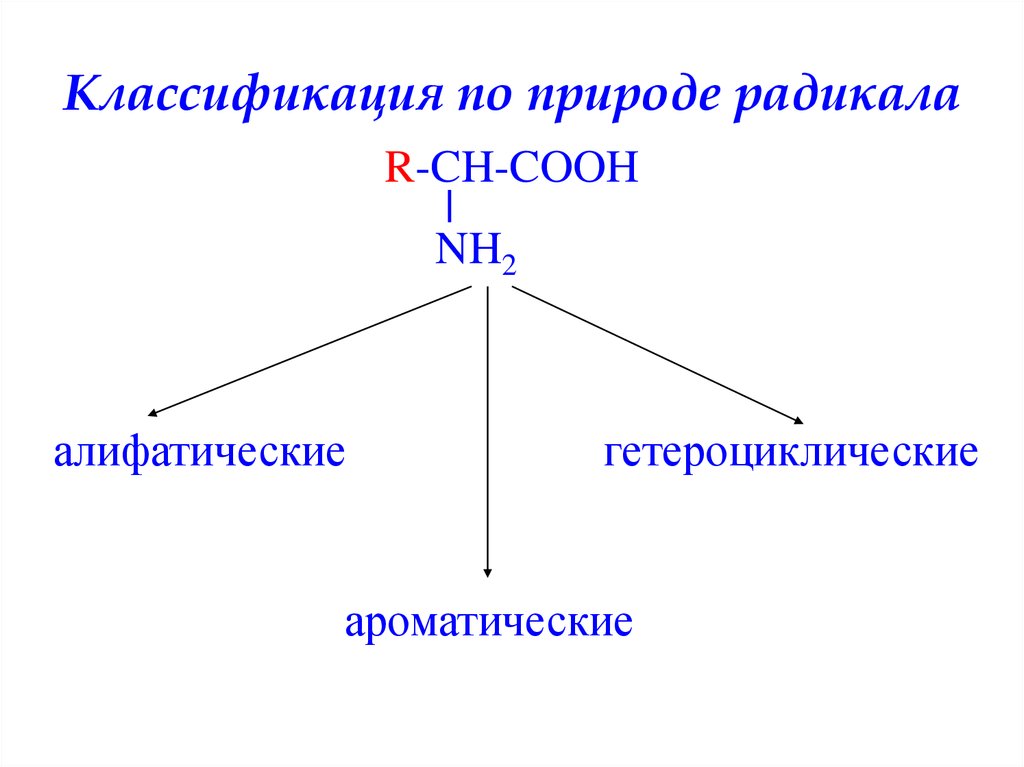
2. Классификация по природе радикала
R-CH-COOHNH2
алифатические
гетероциклические
ароматические
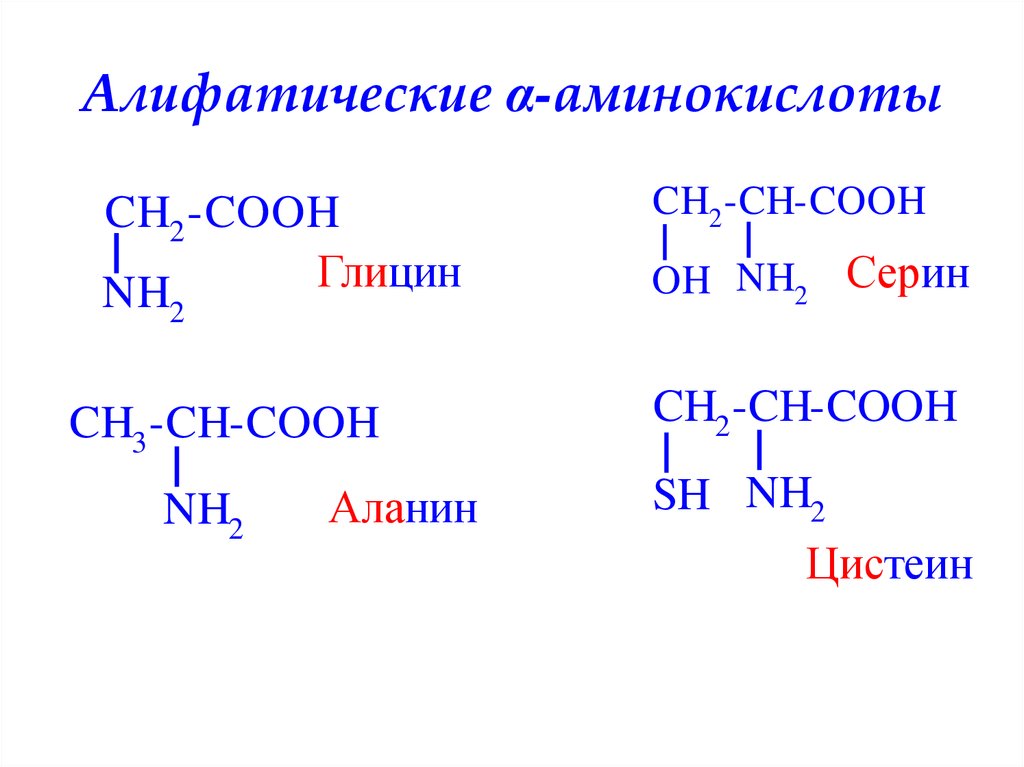
3. Алифатические α-аминокислоты
CH2 -COOHГлицин
NH
2
CH3 -CH-COOH
NH2
Аланин
CH2 -CH-COOH
OH NH2 Серин
CH2 -CH-COOH
SH NH2
Цистеин
4. Ароматические α-аминокислоты
CH2 -CH-COOHФенилаланин
NH2
HO
CH2 -CH-COOH
NH2
Тирозин
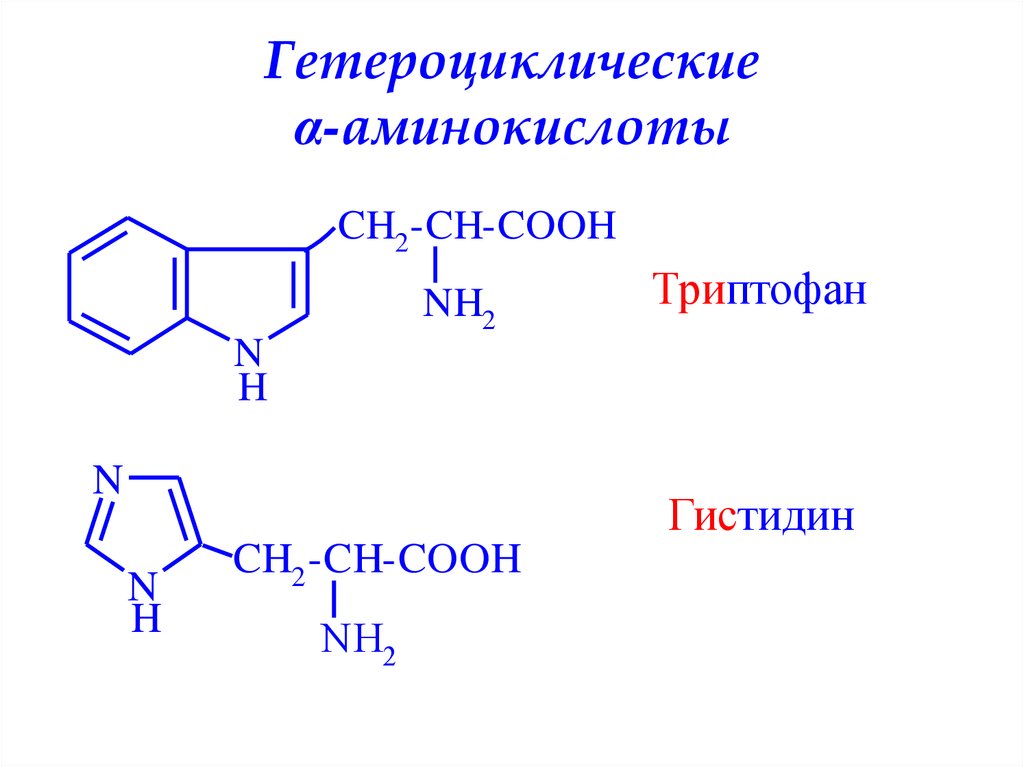
5. Гетероциклические α-аминокислоты
CH2 -CH-COOHNH2
Триптофан
N
H
N
Гистидин
N
H
CH2 -CH-COOH
NH2
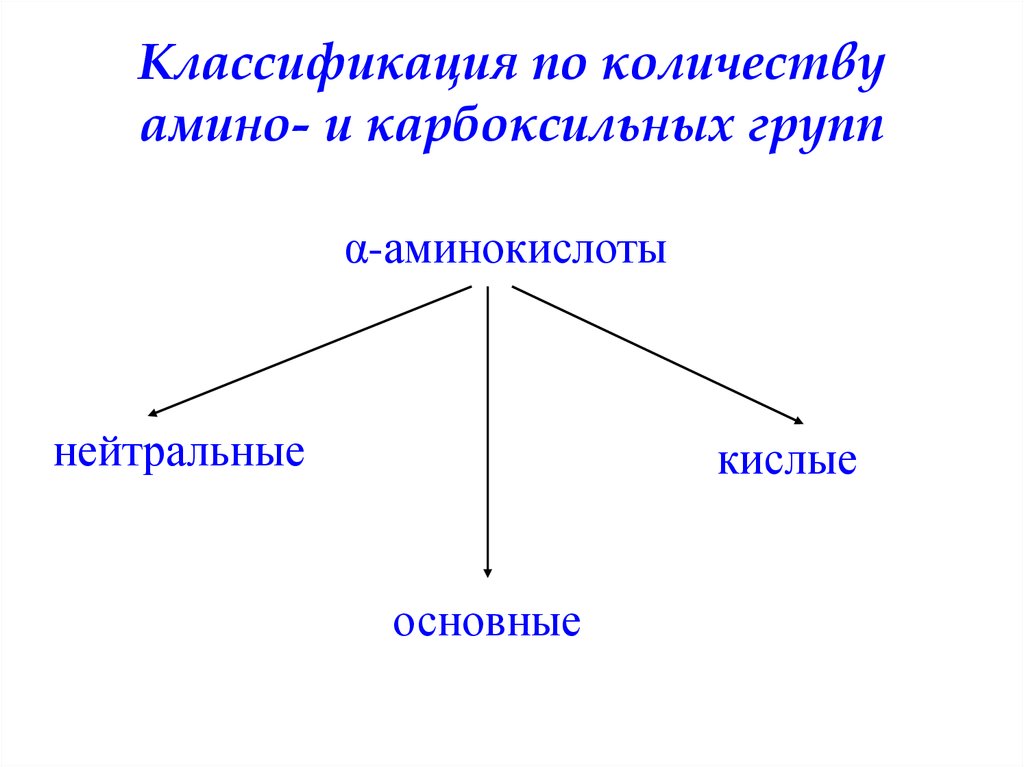
6. Классификация по количеству амино- и карбоксильных групп
α-аминокислотынейтральные
кислые
основные
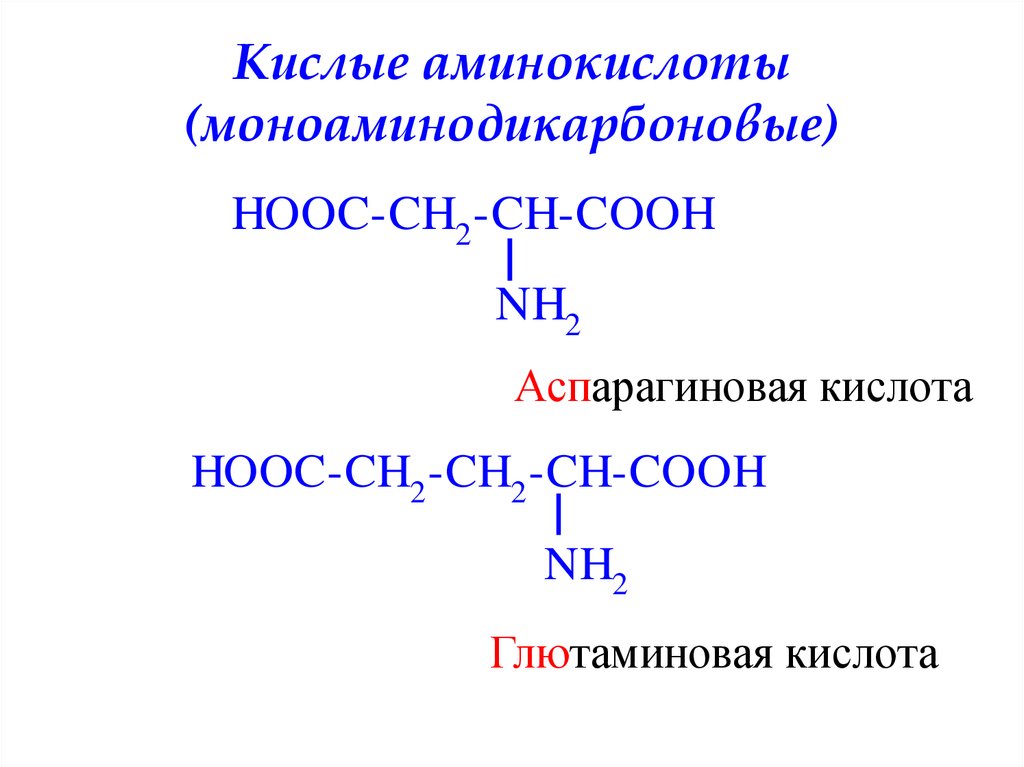
7. Кислые аминокислоты (моноаминодикарбоновые)
HOOC-CH2 -CH-COOHNH2
Аспарагиновая кислота
HOOC-CH2 -CH2 -CH-COOH
NH2
Глютаминовая кислота
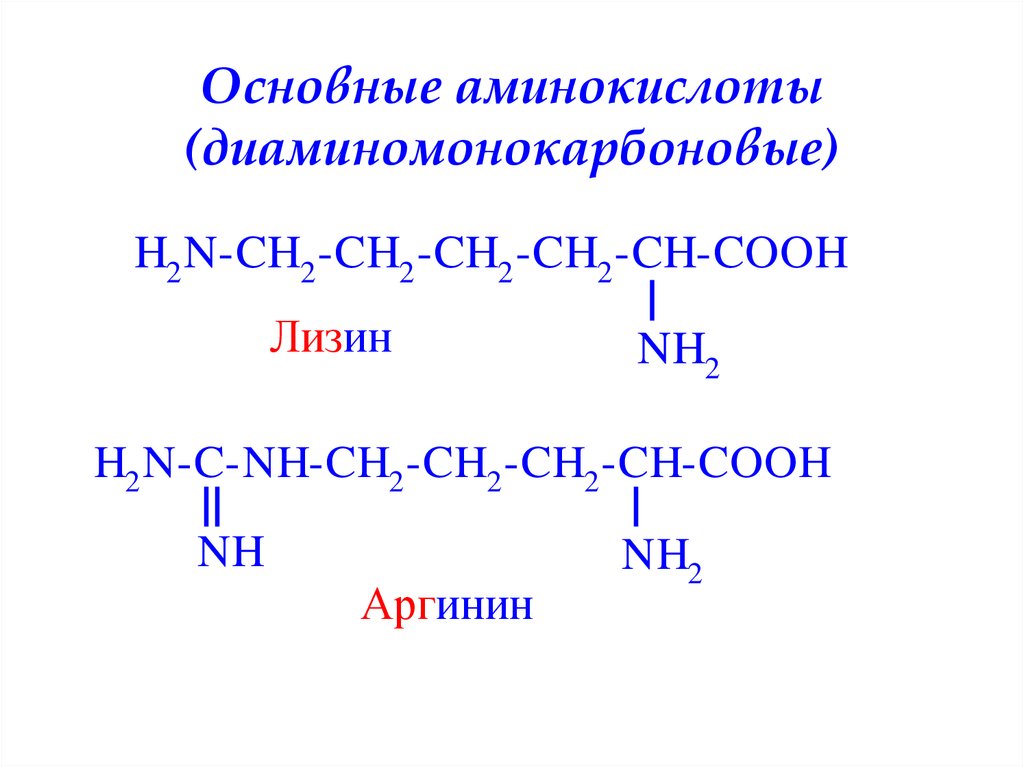
8. Основные аминокислоты (диаминомонокарбоновые)
H2 N-CH2 -CH2 -CH2 -CH2 -CH-COOHЛизин
NH2
H2 N-C-NH-CH2 -CH2 -CH2 -CH-COOH
NH
Аргинин
NH2
9. Незаменимые α-аминокислоты
Валин
Лейцин
Изолейцин
Метионин
Треонин
Фенилаланин
Триптофан
Лизин
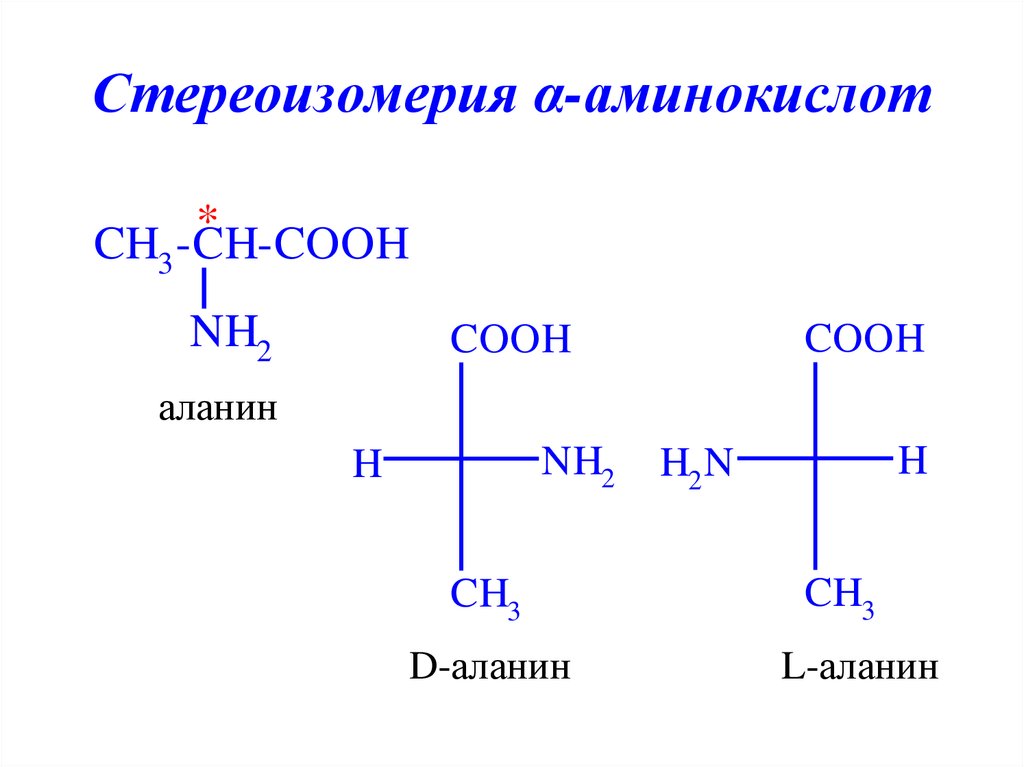
10. Стереоизомерия α-аминокислот
*CH3 -CH-COOH
NH2
COOH
COOH
аланин
NH2
H
CH3
D-аланин
H
H2 N
CH3
L-аланин
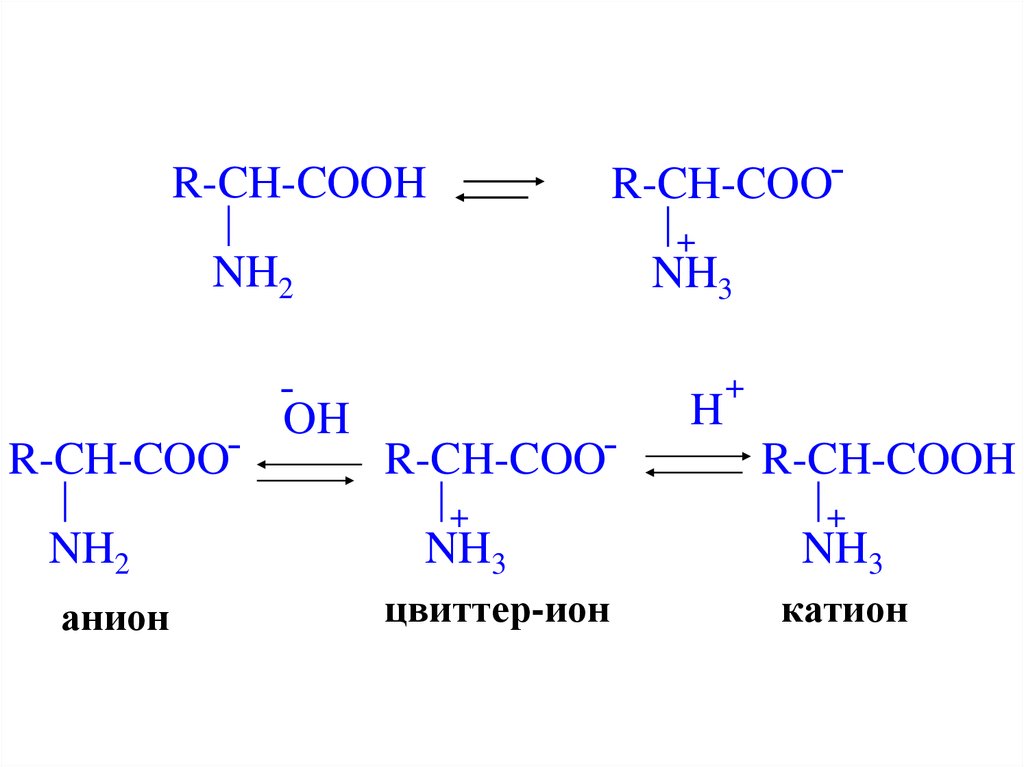
11.
R-CH-COO-R-CH-COOH
+
NH2
R-CH-COONH2
анион
OH
NH3
R-CH-COO+
NH3
цвиттер-ион
H
+
R-CH-COOH
+
NH3
катион
12.
Изоэлектрическая точка α-аминокислоты – это тозначение pH раствора, при котором большинство
молекул существуют в виде биполярных ионов, а
концентрации катионной и анионной форм
минимальны и равны.
13.
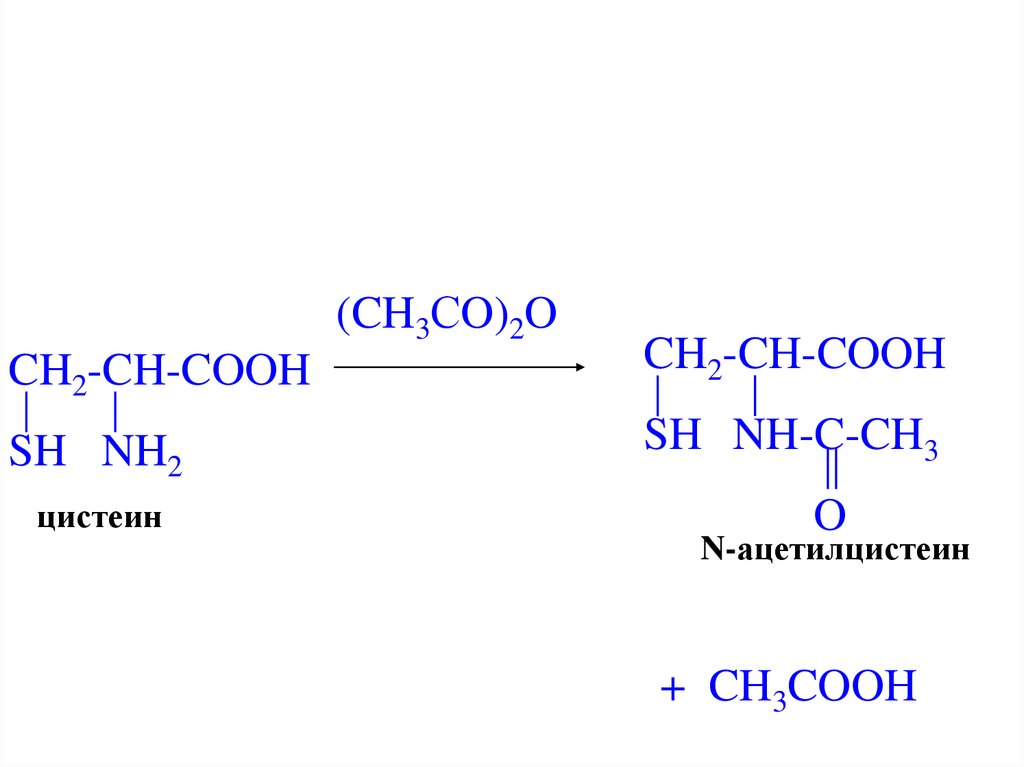
(CH3СO)2OCH2-CH-COOH
CH2-CH-COOH
SH NH2
SH NH-C-CH3
цистеин
O
N-ацетилцистеин
+ CH3COOH
14.
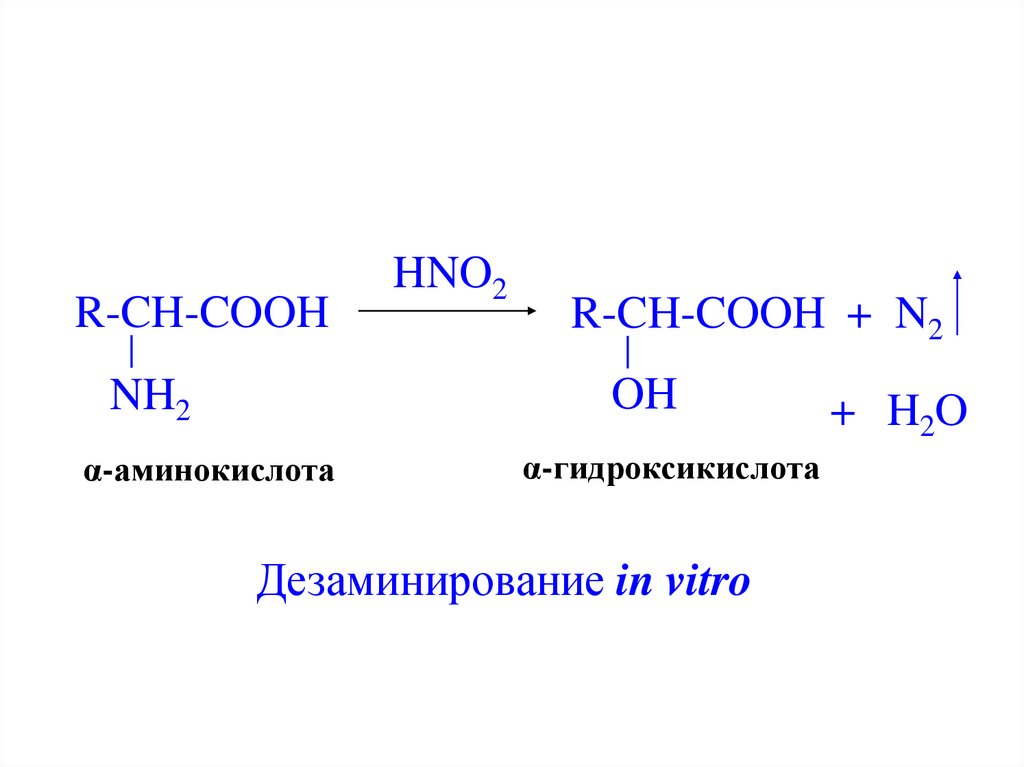
R-CH-COOHHNO2
R-CH-COOH + N2
OH
NH2
α-аминокислота
α-гидроксикислота
Дезаминирование in vitro
+ H 2O
15.
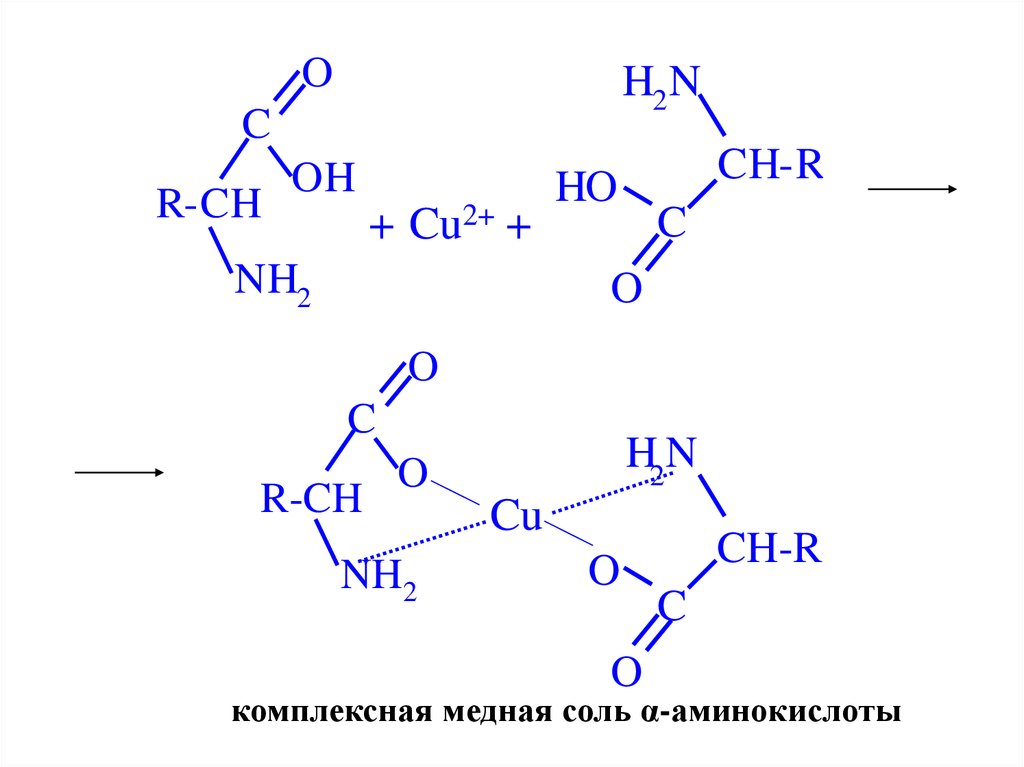
OH2 N
C
R-CH
OH
+ Cu2+ +
NH2
CH-R
HO
C
O
O
C
R-CH
H2N
O
NH2
Cu
O
O
CH-R
C
комплексная медная соль α-аминокислоты
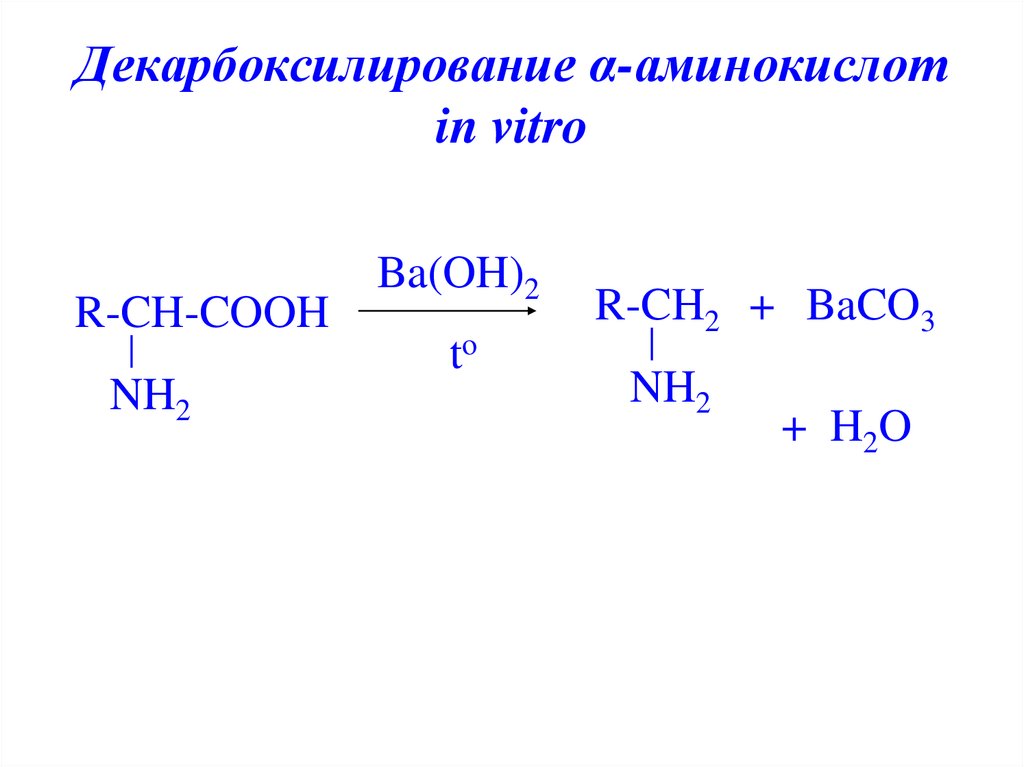
16. Декарбоксилирование α-аминокислот in vitro
R-CH-COOHNH2
Ba(OH)2
to
R-CH2 + BaCO3
NH2
+ H2O
17.
OOH
OH
+ H2 N-CH-COOH
R
O
нингидрин
O
O
O
N
+ R-C
+ CO2
H
O
OH
продукт сине-фиолетового цвета
18. Реакция на ароматические α-аминокислоты (ксантопротеиновая)
HNO3CH2 -CH-COOH
HO
тирозин
to
NH2
NaOH
HO
O2 N
CH2 -CH-COOH
NH2
продукт нитрования
продукт
оранжевого
цвета
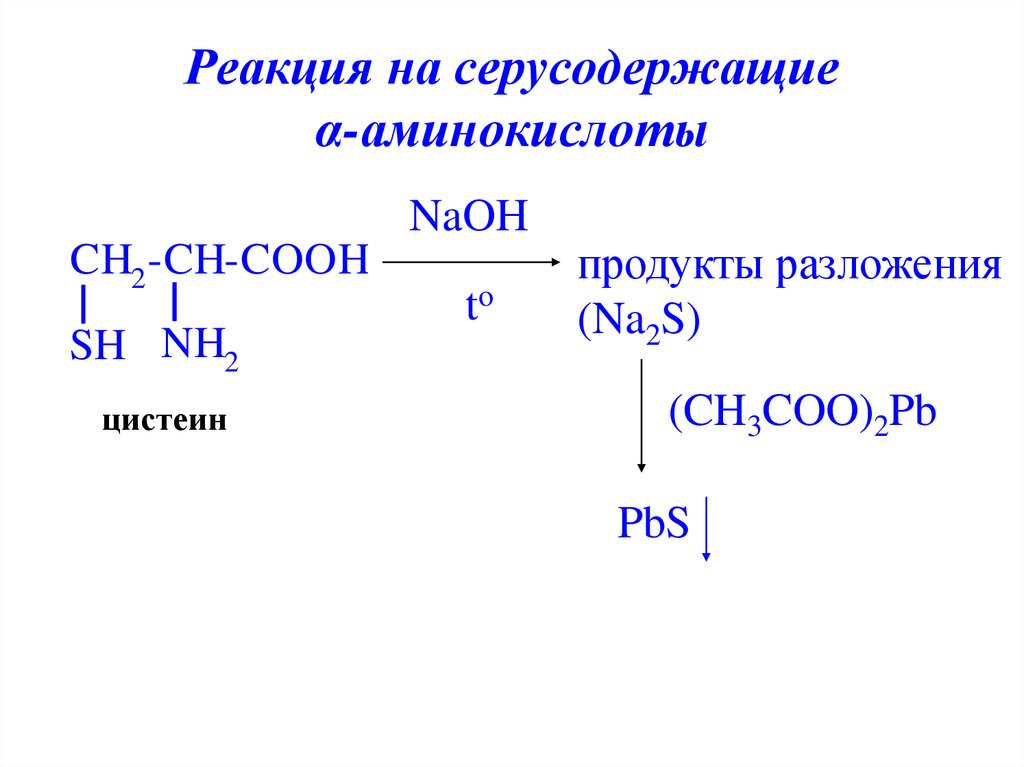
19. Реакция на серусодержащие α-аминокислоты
NaOHCH2 -CH-COOH
SH NH2
цистеин
to
продукты разложения
(Na2S)
(CH3COO)2Pb
PbS
20. Реакции α-аминокислот in vivo
декарбоксилирование
дезаминирование
переаминирование
образование пептидов
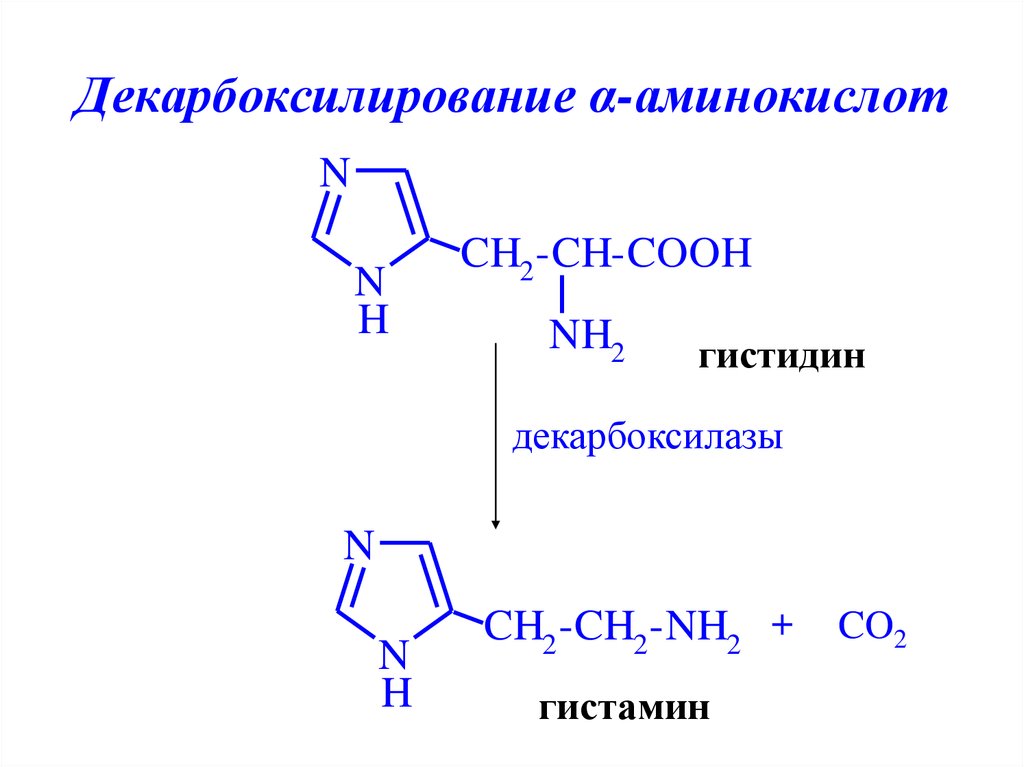
21. Декарбоксилирование α-аминокислот
NN
H
CH2 -CH-COOH
NH2
гистидин
декарбоксилазы
N
N
H
CH2 -CH2 -NH2 +
гистамин
CO2
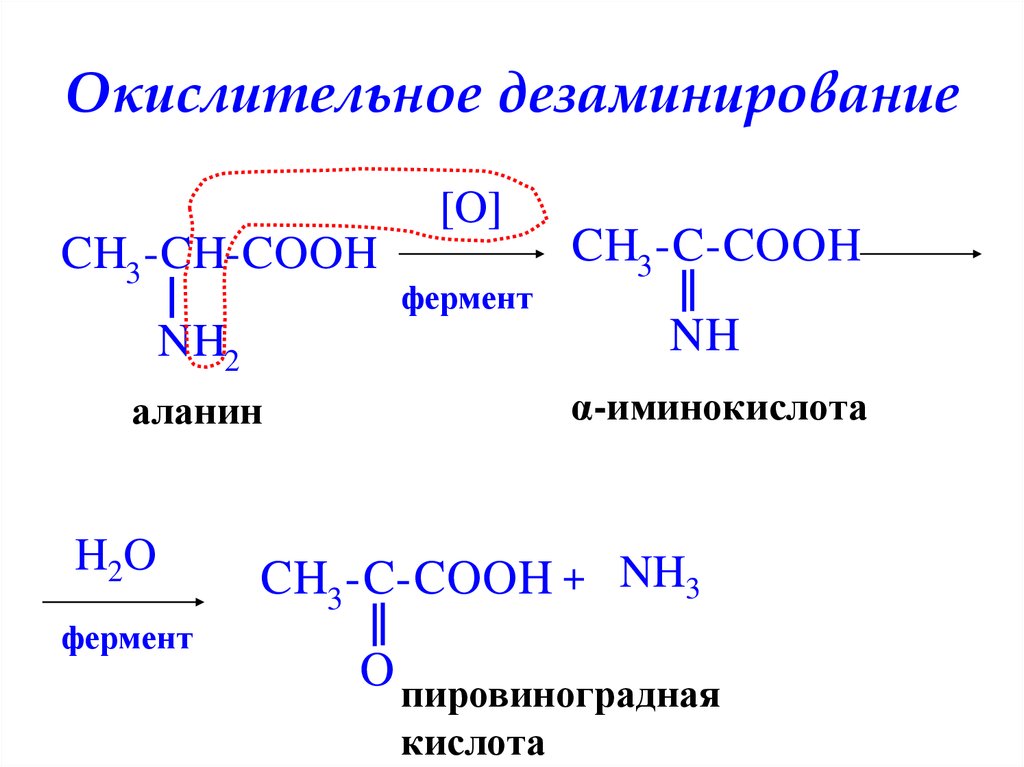
22. Окислительное дезаминирование
[O]CH3 -CH-COOH
фермент
NH
NH2
α-иминокислота
аланин
H2O
фермент
CH3 -C-COOH
CH3 -C-COOH + NH3
O пировиноградная
кислота
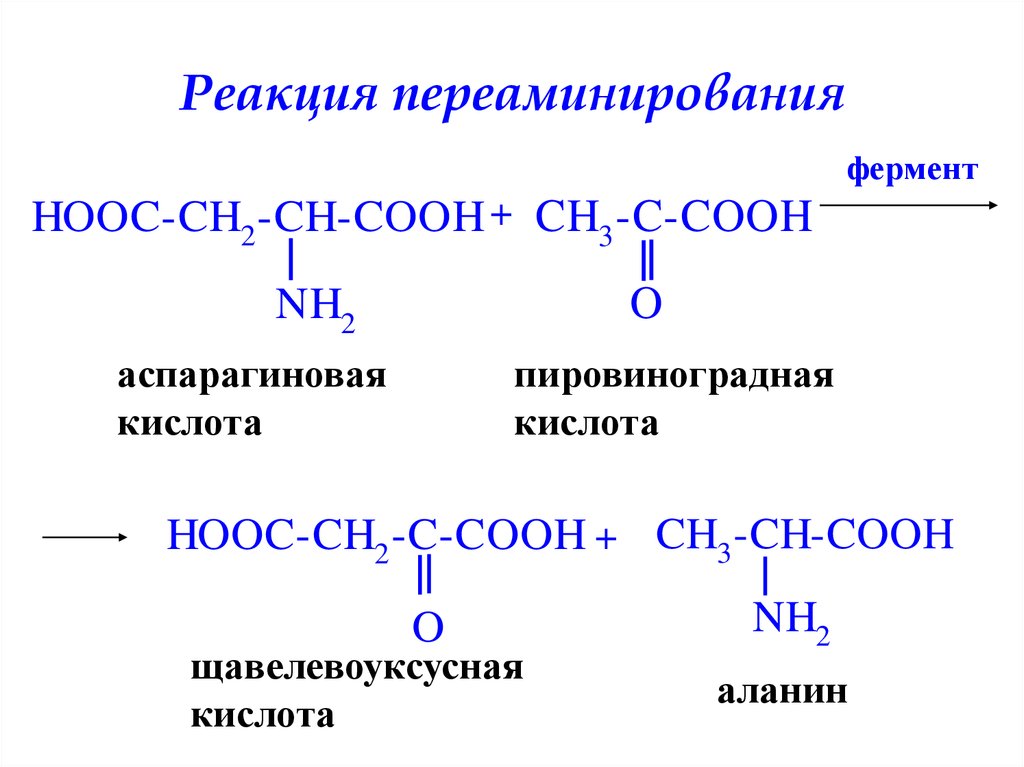
23. Реакция переаминирования
ферментHOOC-CH2 -CH-COOH + CH3 -C-COOH
O
NH2
аспарагиновая
кислота
пировиноградная
кислота
HOOC-CH2 -C-COOH + CH3 -CH-COOH
O
щавелевоуксусная
кислота
NH2
аланин
24. Пептиды и белки
25.
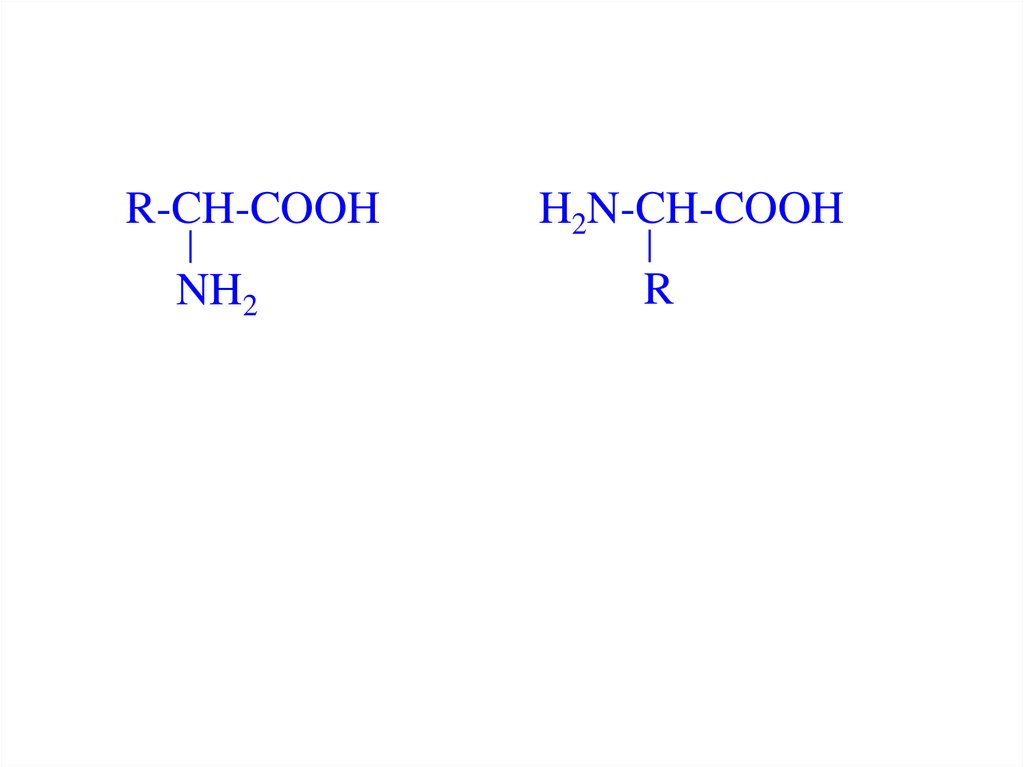
R-CH-COOHNH2
H2N-CH-COOH
R
26.
OH2 N-CH-C
R
O
+ H2 N-CH-C
OH
R'
O
+ H2 N-CH-C
OH
R''
OH
пептидная связь
N-конец
O
O
H2 N-CH-C-NH-CH-C-NH-CH-COOH
R
R"
R'
трипептид
C-конец
27.
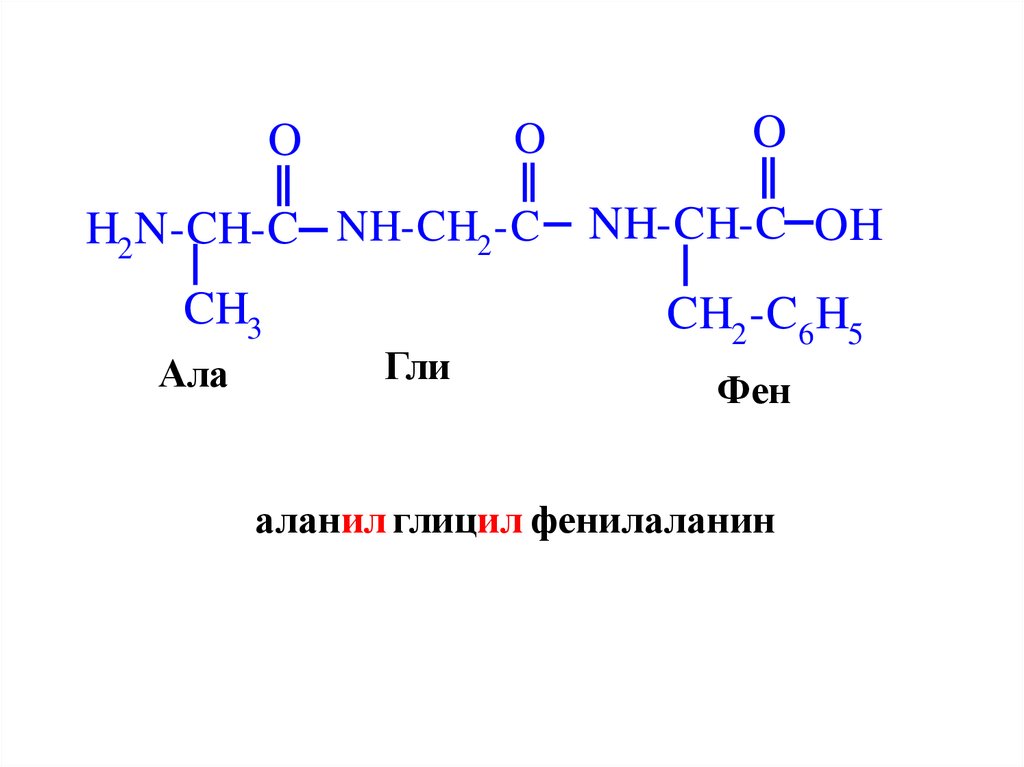
OO
H2 N-CH-C NH-CH2 -C
CH3
Ала
Гли
O
NH-CH-C OH
CH2 -C6 H5
Фен
аланил глицил фенилаланин
28. Электронное строение пептидной связи
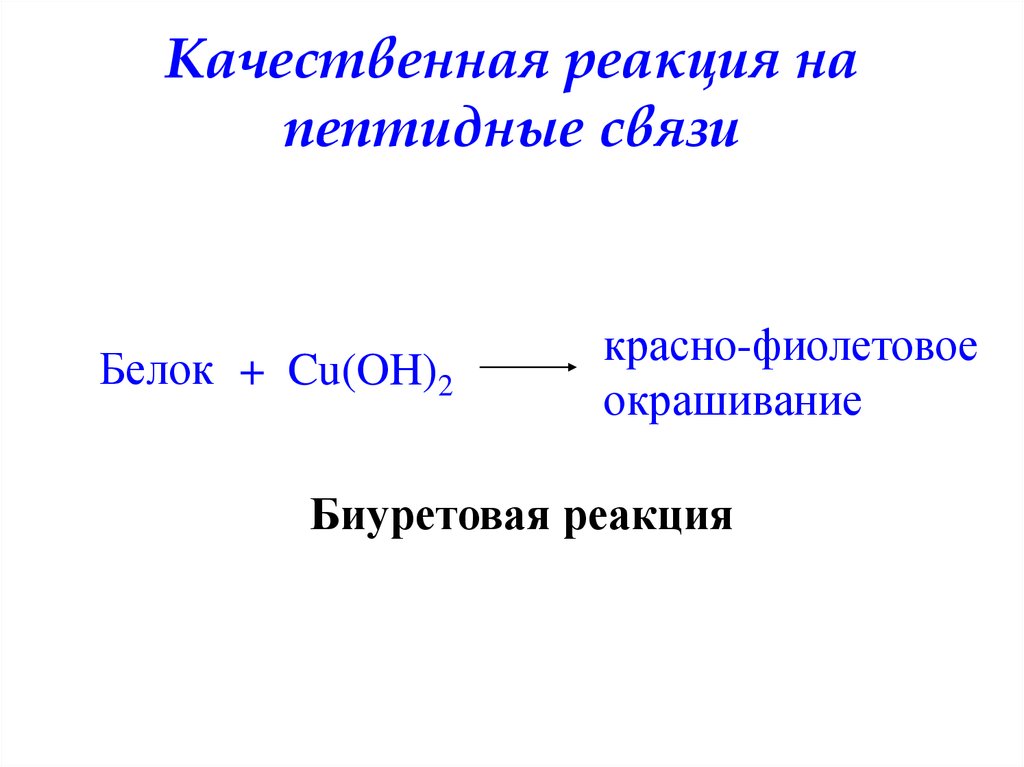
Качественная реакция напептидные связи
Белок + Cu(OH)2
красно-фиолетовое
окрашивание
Биуретовая реакция
29.
Первичная структура белка – это определеннаяаминокислотная последовательность, т.е.
порядок чередования аминокислотных остатков
в молекуле белка.
Первичная структура характеризуется
•аминокислотным составом
•аминокислотной последовательностью
30. Качественная реакция на пептидные связи
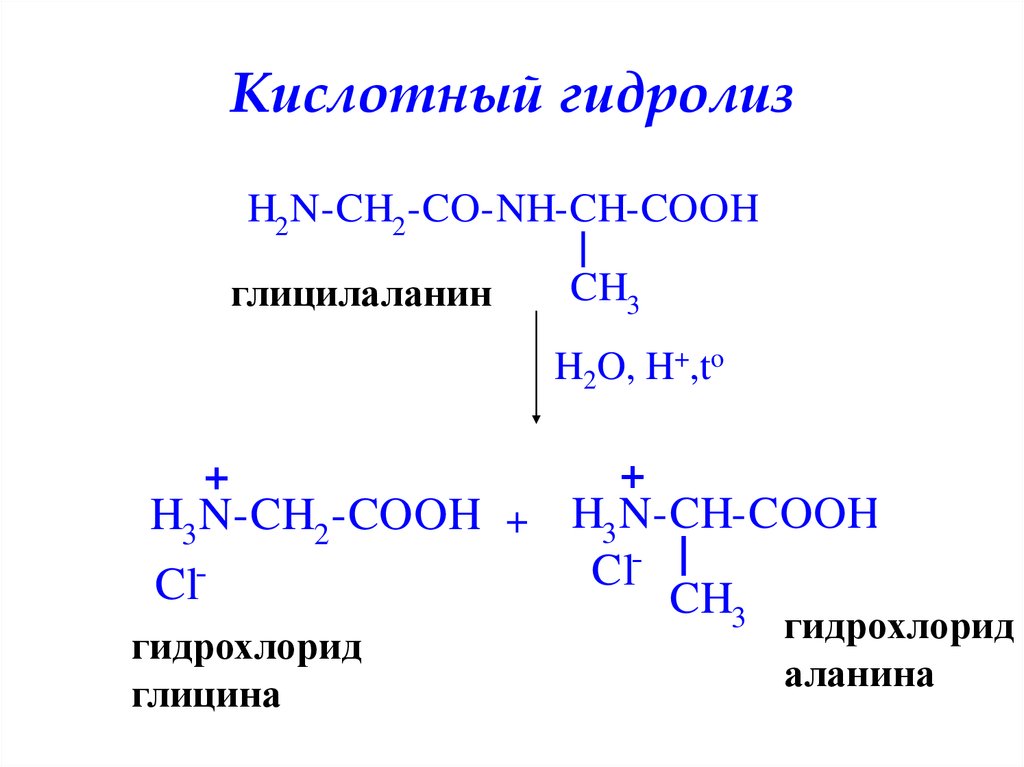
Кислотный гидролизH2 N-CH2 -CO-NH-CH-COOH
глицилаланин
CH3
H2O, H+,to
+
+
H3 N-CH2 -COOH + H3 N-CH-COOH
Cl
Cl
CH
гидрохлорид
глицина
3
гидрохлорид
аланина
31.
Щелочной гидролизH2 N-CH2 -CO-NH-CH-COOH
глицилаланин
CH3
H2O, NaOH,to
H2 N-CH2 -COONa +
натриевая соль
глицина
H2 N-CH-COONa
CH3
натриевая соль
аланина
32. Кислотный гидролиз
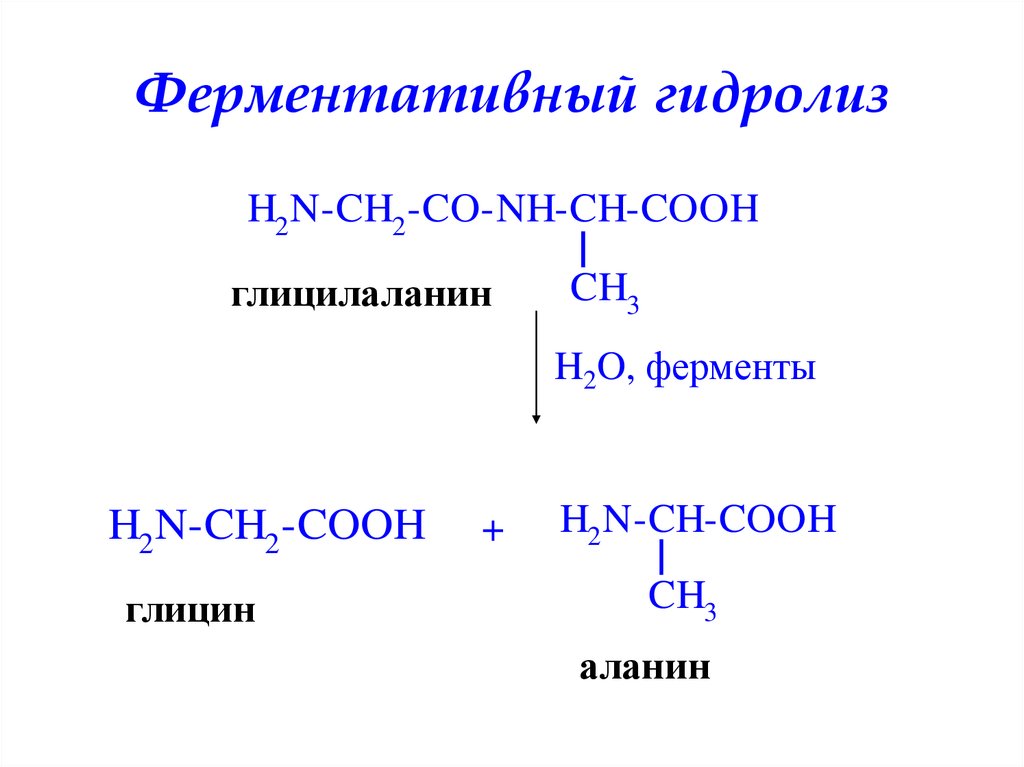
Ферментативный гидролизH2 N-CH2 -CO-NH-CH-COOH
глицилаланин
CH3
H2O, ферменты
H2 N-CH2 -COOH
глицин
+
H2 N-CH-COOH
CH3
аланин
33. Щелочной гидролиз
Вторичная структура белка – определенноепространственное расположение полипептидной
цепи.
• α-спираль
• β-складчатая структура
34. Ферментативный гидролиз
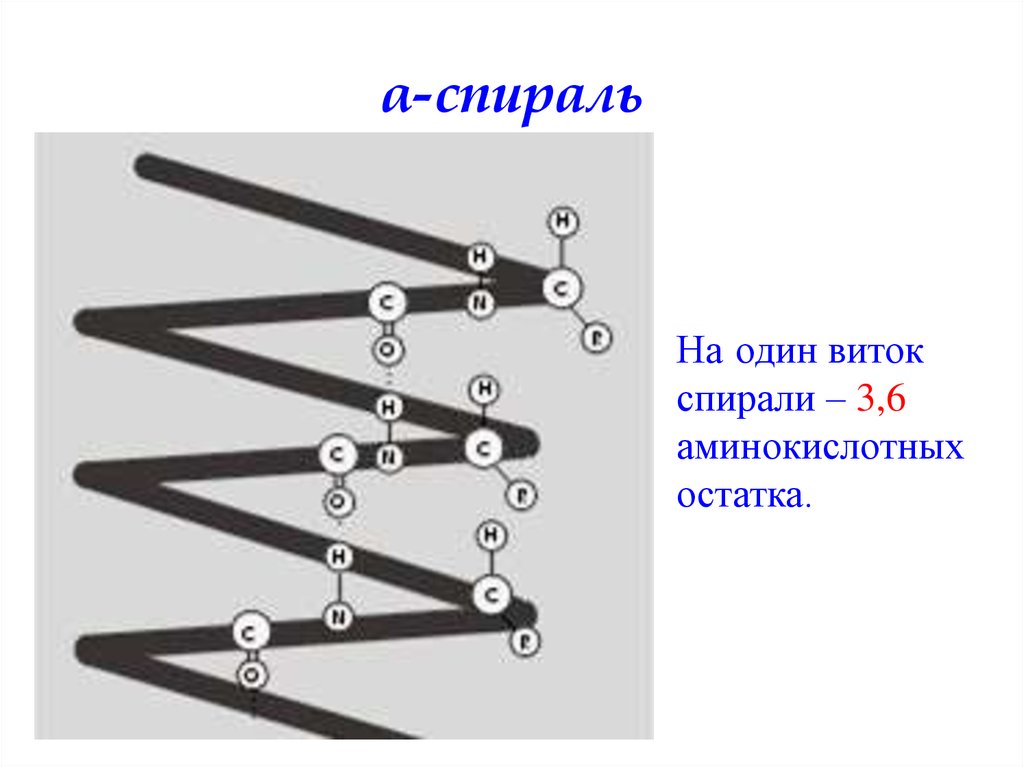
α-спиральНа один виток
спирали – 3,6
аминокислотных
остатка.
35.
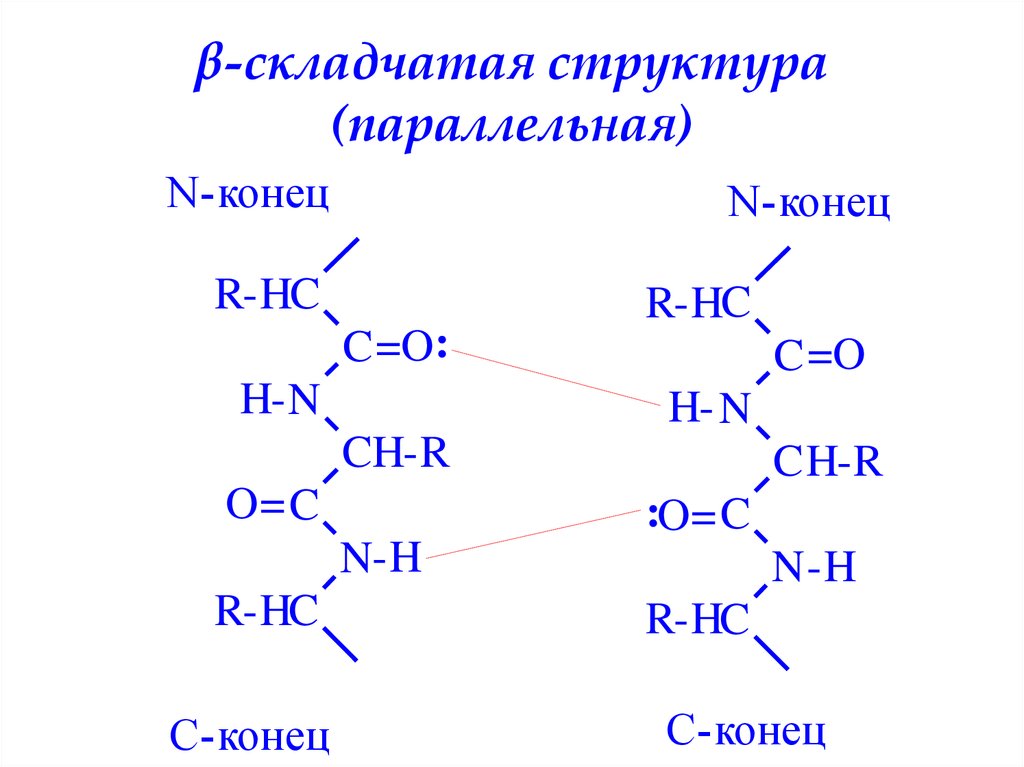
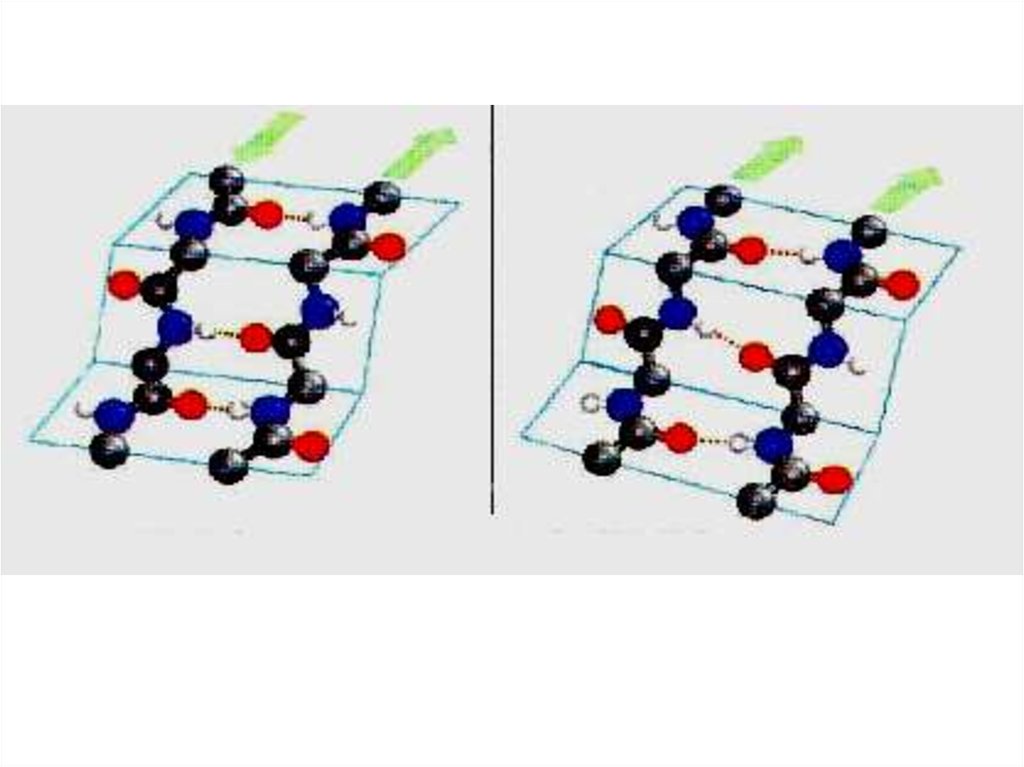
β-складчатая структура(параллельная)
N-конец
N-конец
R-HC
C =O:
H- N
R-HC
C =O
H- N
CH-R
O= C
C H-R
:O= C
N-H
R-HC
C-конец
N -H
R-HC
C-конец
36. α-спираль
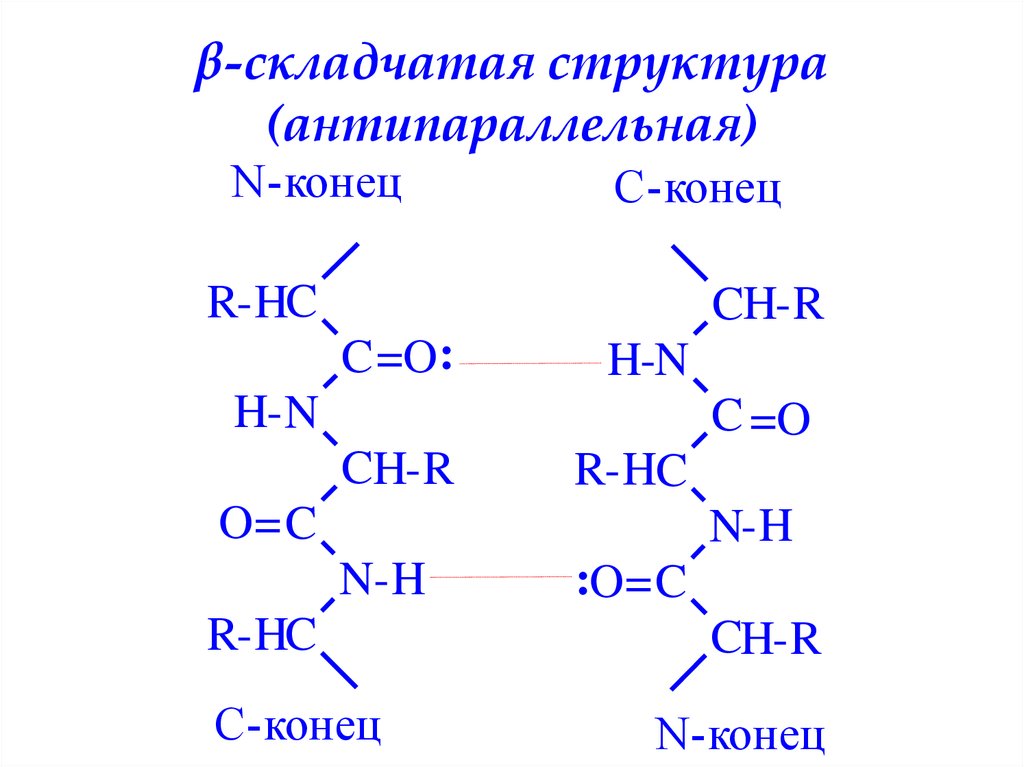
β-складчатая структура(антипараллельная)
N-конец
C-конец
R-HC
CH-R
C =O:
H-N
H- N
C =O
CH-R
R-HC
O= C
N-H
N-H
R-HC
C-конец
:O= C
CH-R
N-конец
37. β-складчатая структура (параллельная)
38. β-складчатая структура (антипараллельная)
Третичная структура белка39.
C =OH- N
O= C
H- N
O= C
CH-CH2 -COOH +
H2 N-(CH2 )4 -H C
Асп
Лиз
CH-CH2 -COO -
N-H
C =O
+
H3 N-(CH2 )4 -HC
N-H
ионная связь
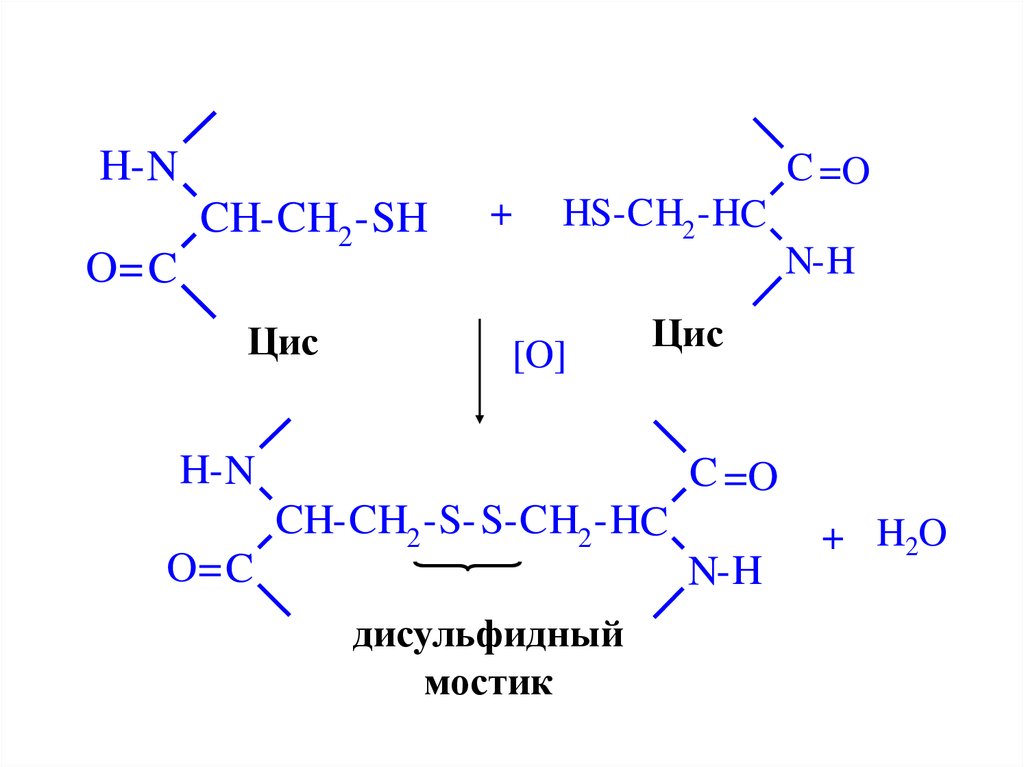
40. Третичная структура белка
H- NO= C
C =O
CH-CH2 -SH
Цис
+
HS-CH2 -HC
N-H
[O]
Цис
H- N
O= C
C =O
CH-CH2 -S- S-CH2 -HC
N-H
дисульфидный
мостик
+ H2O
41.
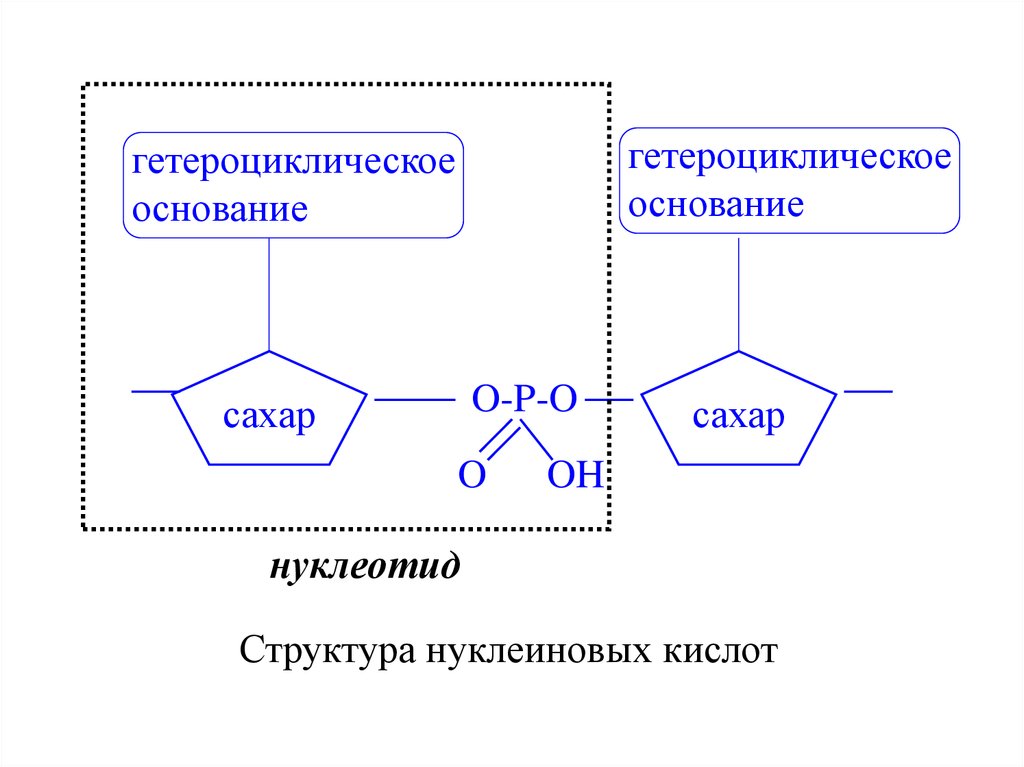
Нуклеиновые кислоты42.
гетероциклическоеоснование
гетероциклическое
основание
O-P-O
сахар
O
сахар
OH
нуклеотид
Структура нуклеиновых кислот
43. Нуклеиновые кислоты
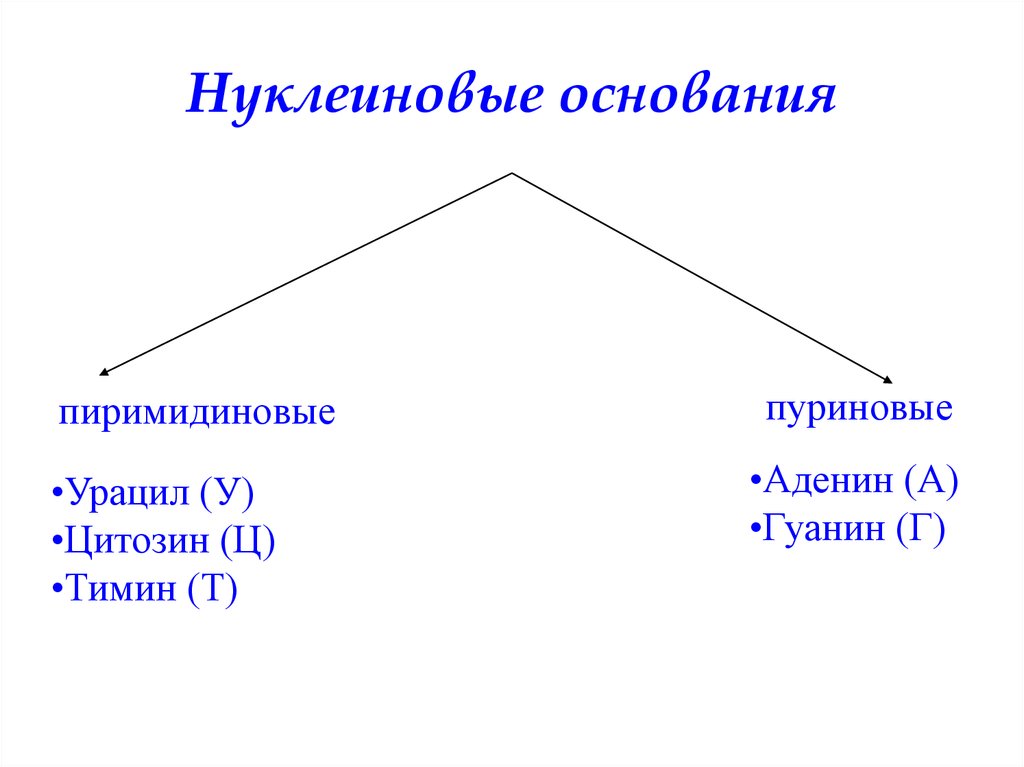
Нуклеиновые основанияпиримидиновые
•Урацил (У)
•Цитозин (Ц)
•Тимин (Т)
пуриновые
•Аденин (А)
•Гуанин (Г)
44.
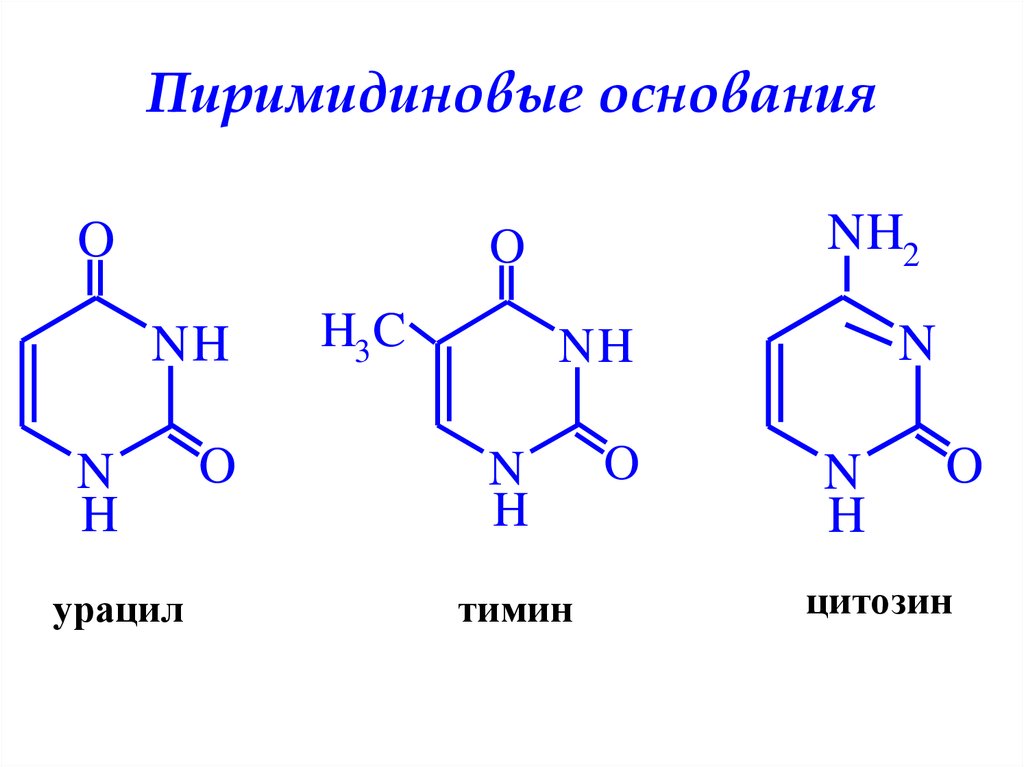
Пиримидиновые основанияO
NH2
O
NH
N
H
урацил
O
H3 C
N
NH
N
H
тимин
O
N
H
O
цитозин
45. Нуклеиновые основания
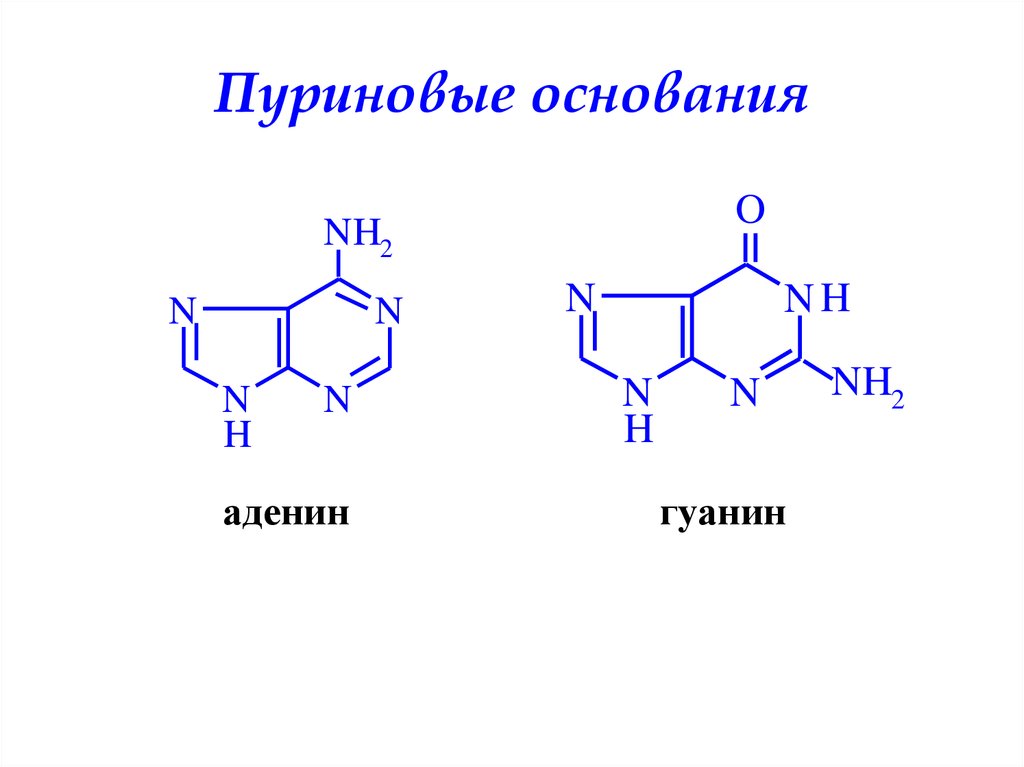
Пуриновые основанияO
NH2
N
N
N
H
N
аденин
N
NH
N
H
N
гуанин
NH2
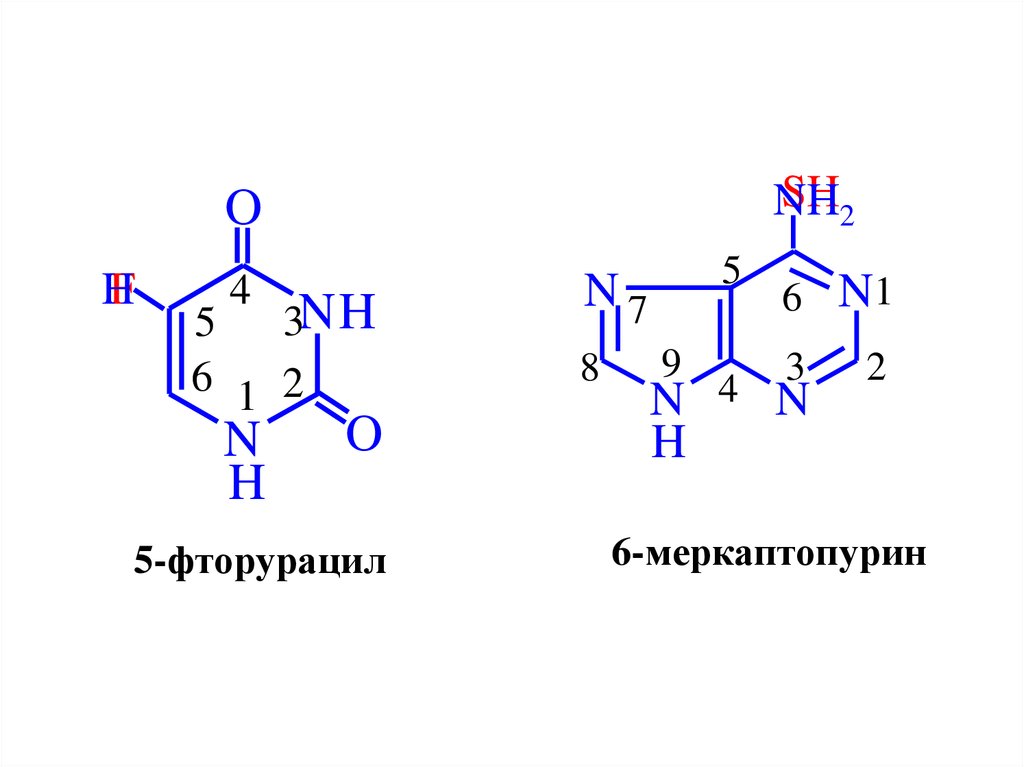
46. Пиримидиновые основания
SH2NH
O
H
F
4
3NH
5
6 1 2
N
H
O
5-фторурацил
5
N7
8
9
6
N1
3
2
N 4 N
H
6-меркаптопурин
47. Пуриновые основания
Нуклеозиды – это N-гликозидырибозы
или
дезоксирибозы
и
нуклеинового основания
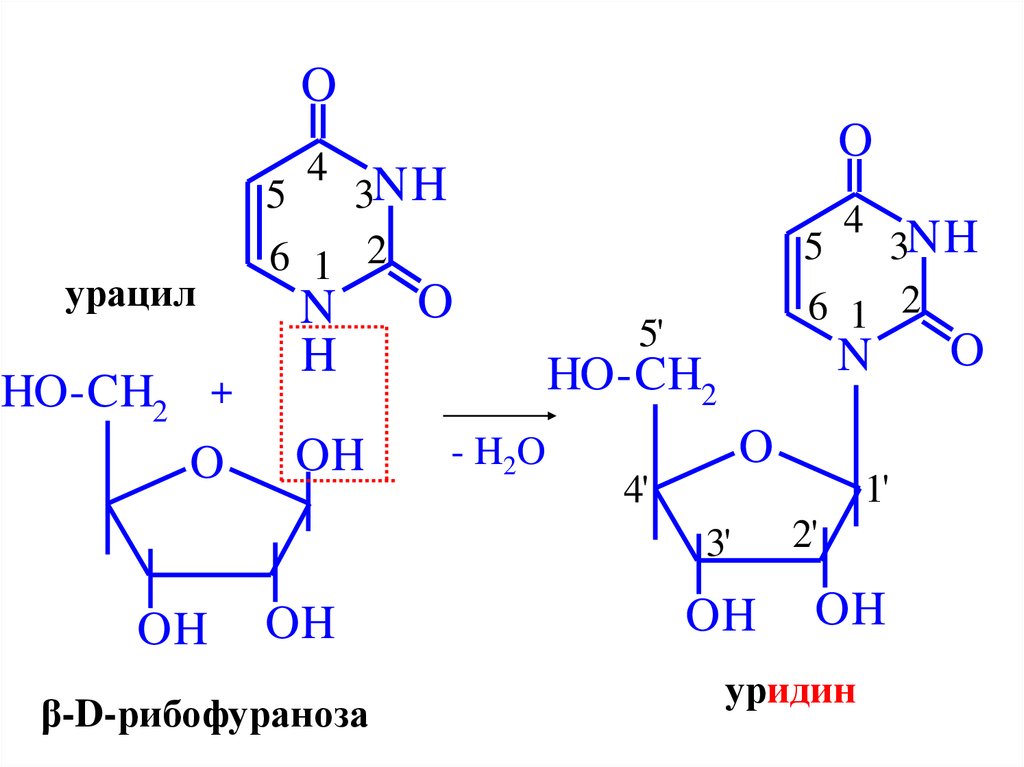
48.
OHO-CH2 +
O
4
3NH
6 1 2
5
урацил
O
N
H
OH
3NH
6 1 2
5
O
5'
N
HO-CH2
- H2O
O
1'
4'
3'
OH
OH
β-D-рибофураноза
4
OH
2'
OH
уридин
O
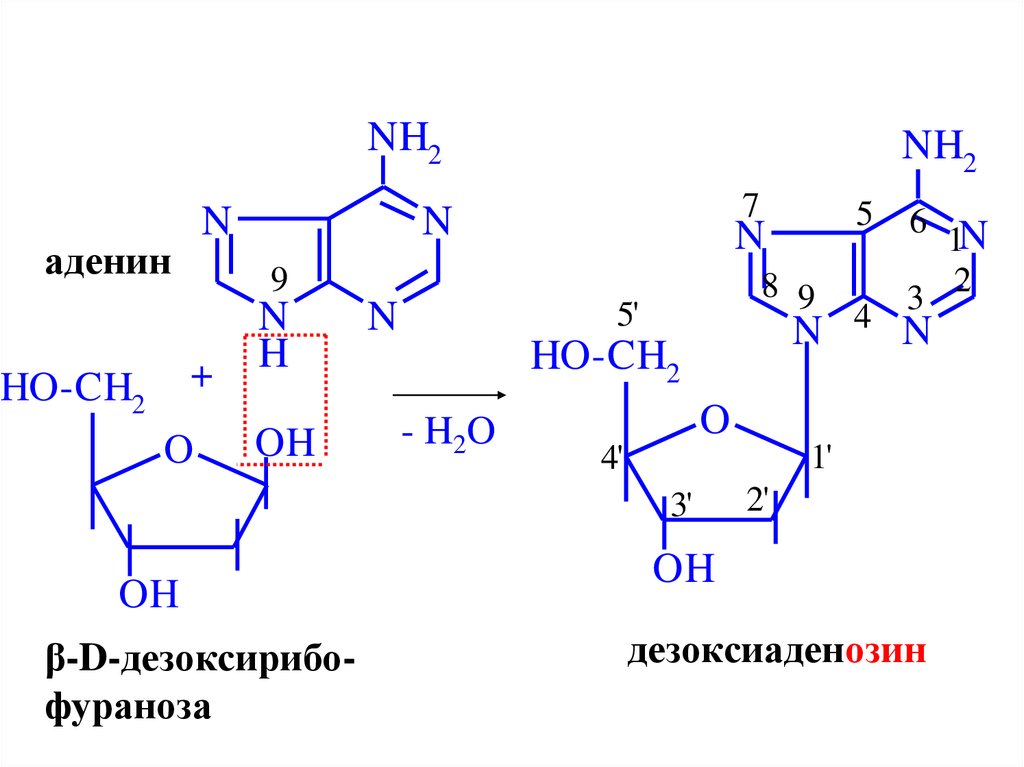
49. Нуклеозиды – это N-гликозиды рибозы или дезоксирибозы и нуклеинового основания
NH2N
аденин
7
N
O
N
H
OH
N
8 9
5'
N
HO-CH2
- H2O
β-D-дезоксирибофураноза
4
6
3
N
O
1'
4'
3'
OH
5
N
9
+
HO-CH2
NH2
2'
OH
дезоксиаденозин
1N
2
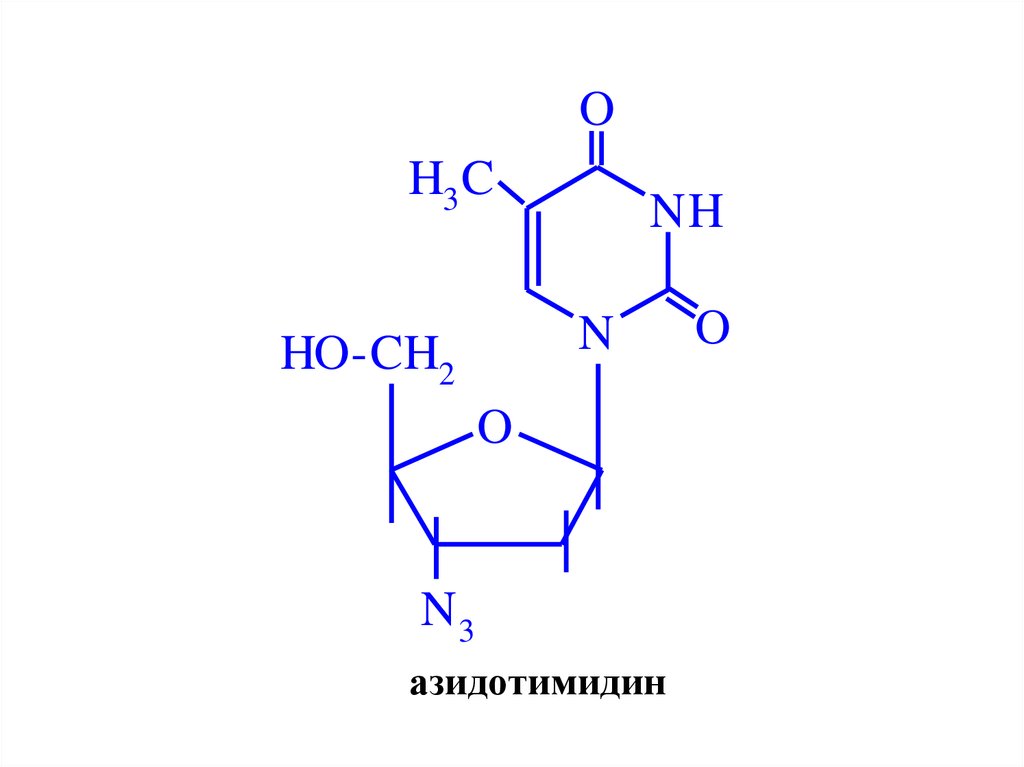
50.
OH3 C
NH
N
HO-CH2
O
N3
азидотимидин
O
51.
ONH
N
N
HO-H2C
O
CH2
CH2
ацикловир
N
NH2
52.
Нуклеотиды – сложные эфирынуклеозидов и фосфорной кислоты
(фосфаты нуклеозидов)
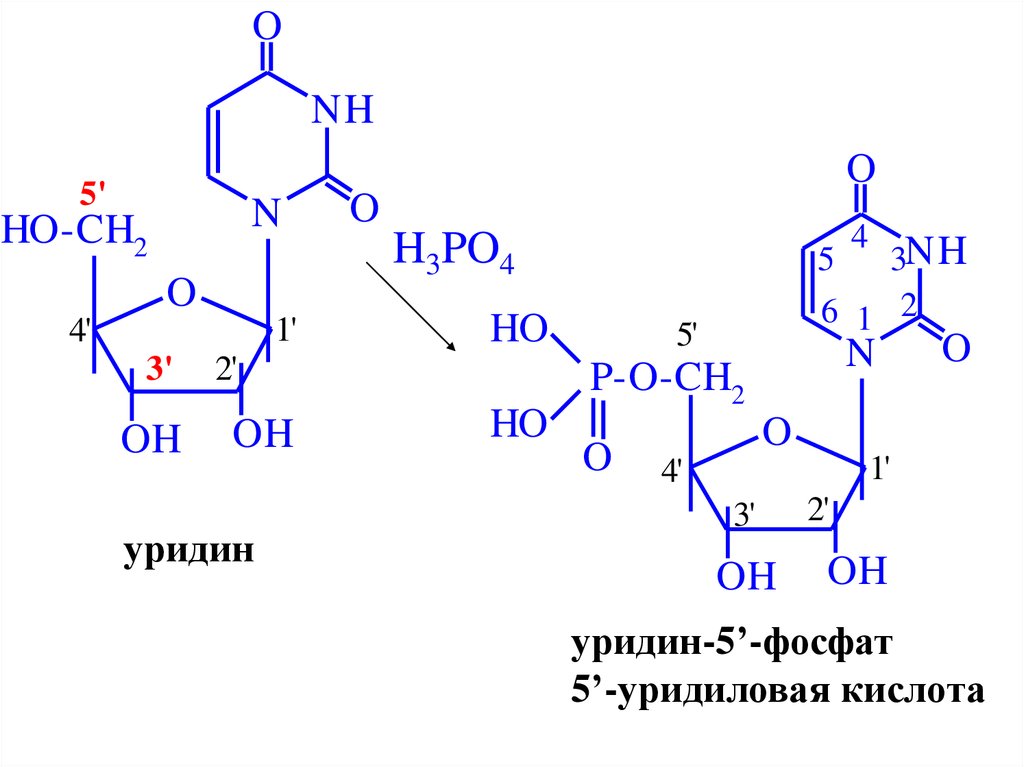
53.
ONH
O
5'
N
HO-CH2
O
1'
4'
3'
OH
O
H3PO4
2'
OH
уридин
HO
3N H
6 1 2
5
HO
5'
N
P-O-CH2
O
4
O
O
1'
4'
3'
OH
2'
OH
уридин-5’-фосфат
5’-уридиловая кислота
54. Нуклеотиды – сложные эфиры нуклеозидов и фосфорной кислоты (фосфаты нуклеозидов)
ON
5'
NH
N
HO-CH2
N
NH2
O
1'
4'
3'
2'
O
O=P
OH
OH
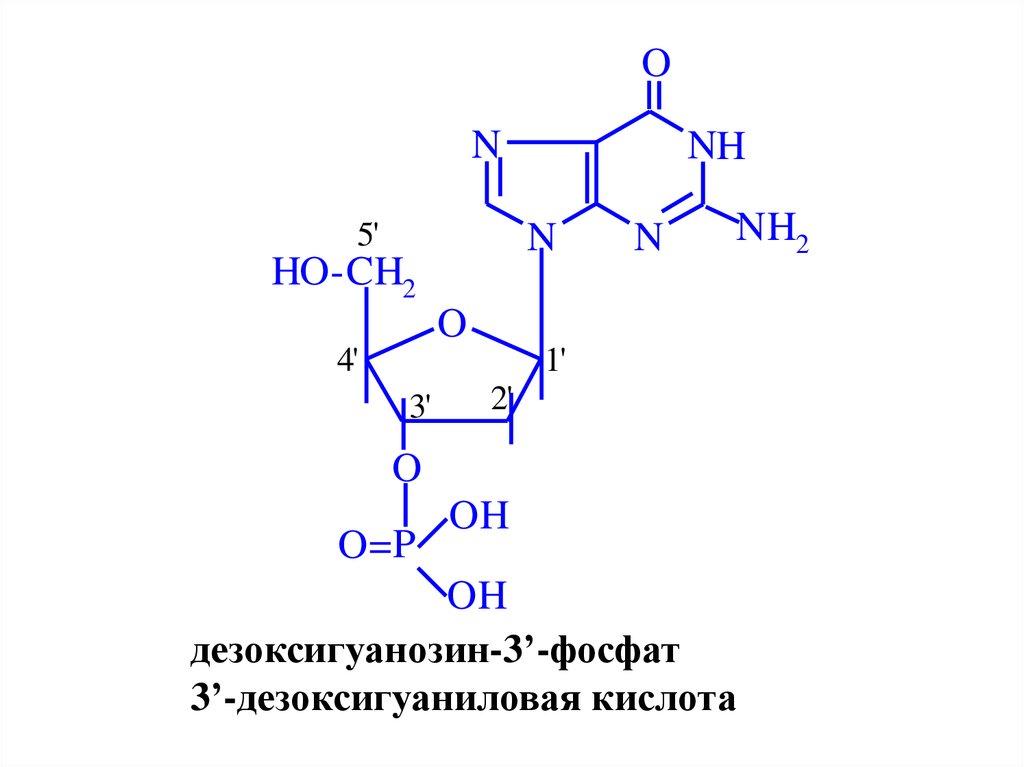
дезоксигуанозин-3’-фосфат
3’-дезоксигуаниловая кислота
55.
NH2N
5'
N
N
O-CH2
N
O
HO
P
O
3'
O
OH
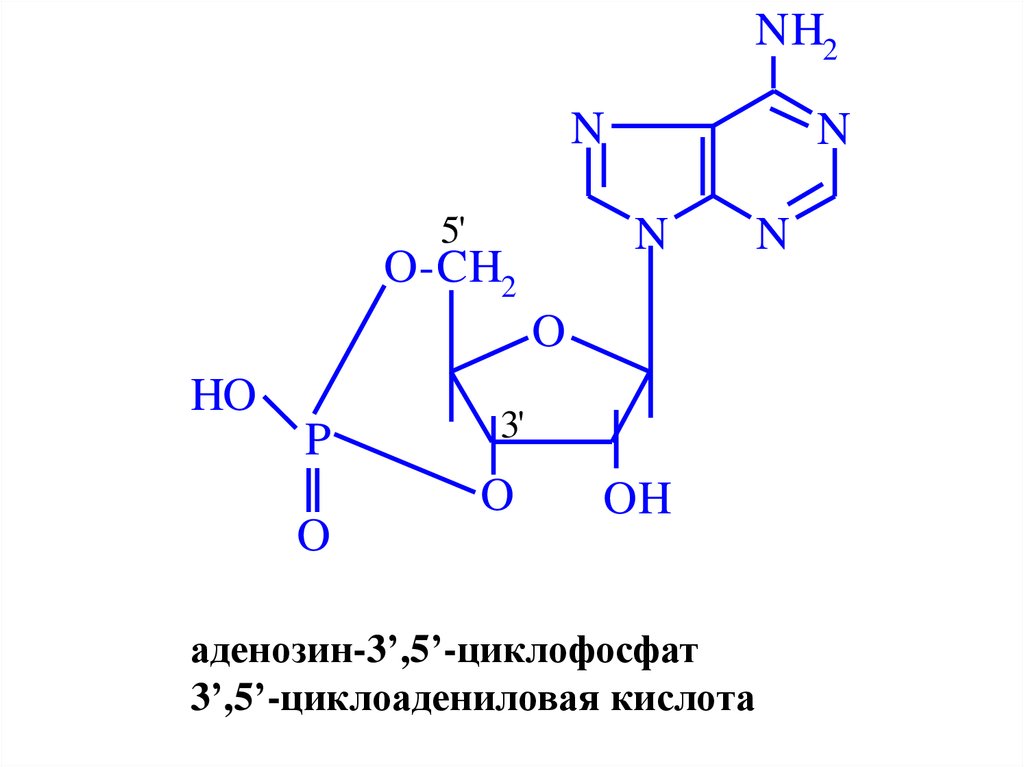
аденозин-3’,5’-циклофосфат
3’,5’-циклоадениловая кислота
56.
NH2 NH2N N
NN
OH OH
OH OH OH
OH
N
NN
N
P-O-CH
HO-PO-P-OHO-P-O-CH
P-O-CH
HO-P-O2
2
2
O
O
O
OO O
O O O
OH OH
OH OHOH
АДФ
АТФ(аденозинмонофосфат)
(аденозиндифосфат
(аденозинтрифосфат
) )
АМФ
NH2
N
N
N
H33PO44
OH
N
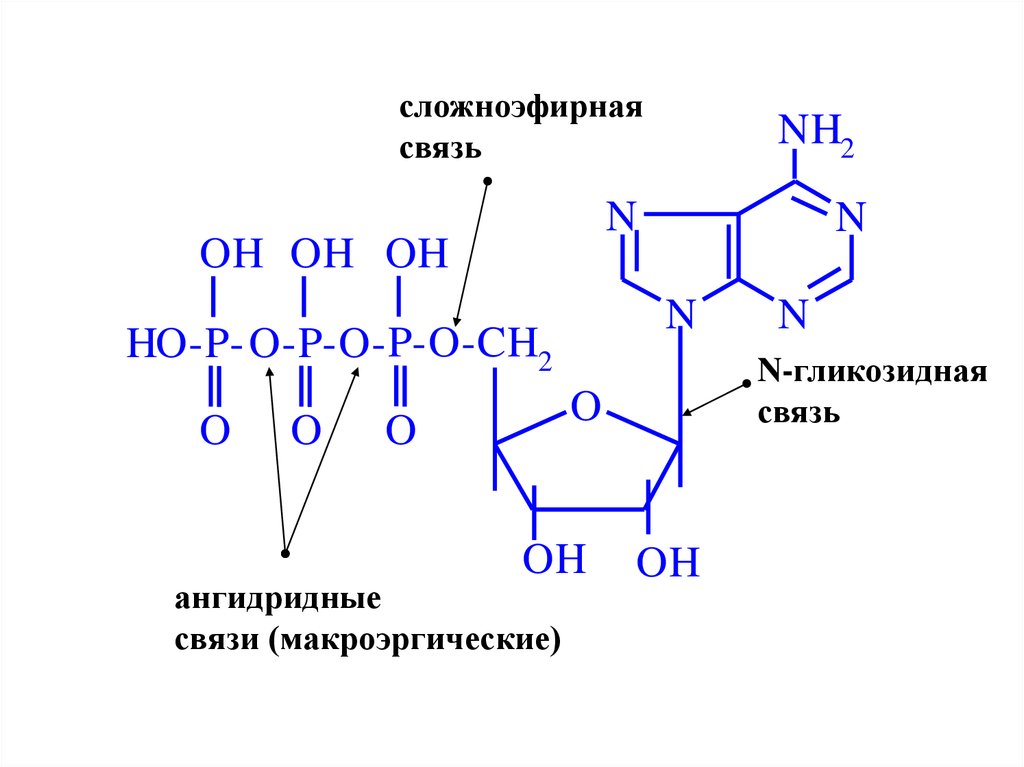
57.
сложноэфирнаясвязь
N
OH OH OH
O
N
N
HO-P- O-P-O- P-O-CH2
O
NH2
N-гликозидная
связь
O
O
OH
ангидридные
связи (макроэргические)
N
OH
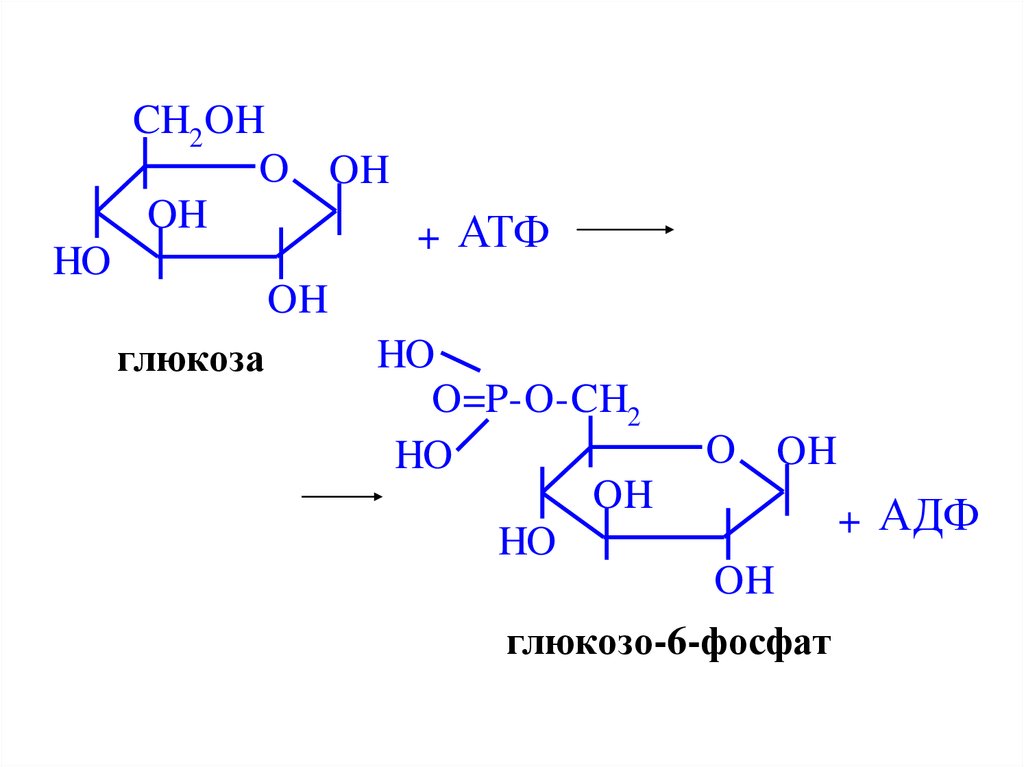
58.
CH2 OHO OH
OH
HO
+ АТФ
OH
глюкоза
HO
O=P-O-CH2
HO
OH
HO
O OH
OH
глюкозо-6-фосфат
+ АДФ
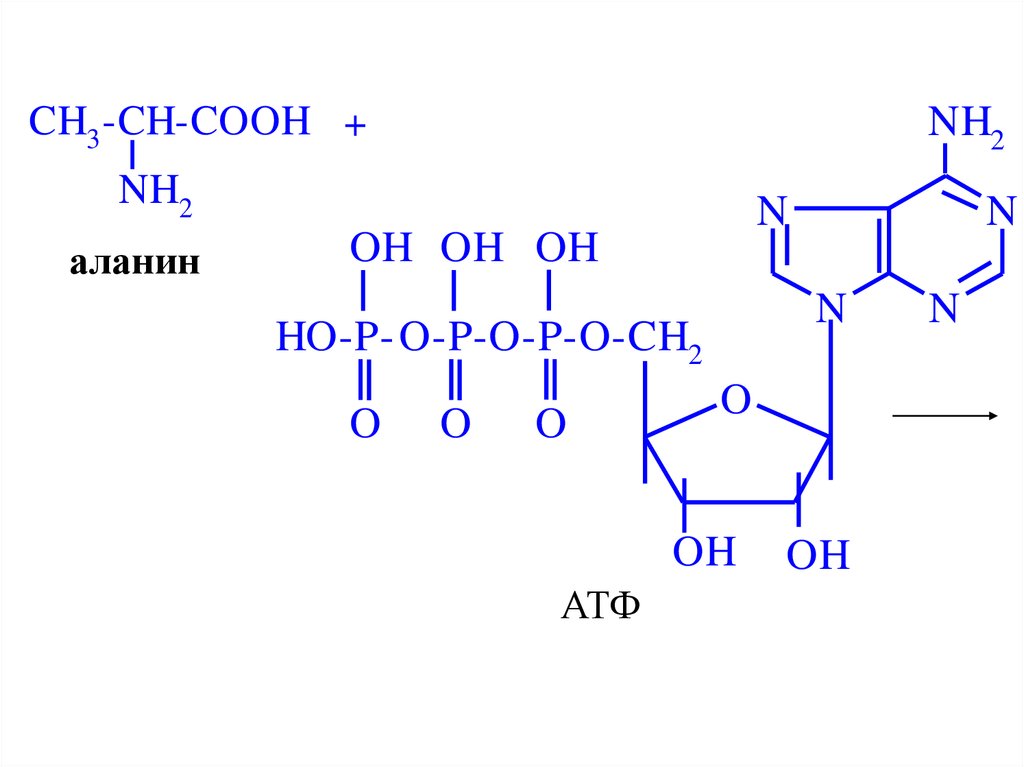
59.
CH3 -CH-COOH +NH2
NH2
аланин
N
OH OH OH
N
HO-P- O-P-O- P-O-CH2
O
O
O
O
OH
АТФ
N
OH
N
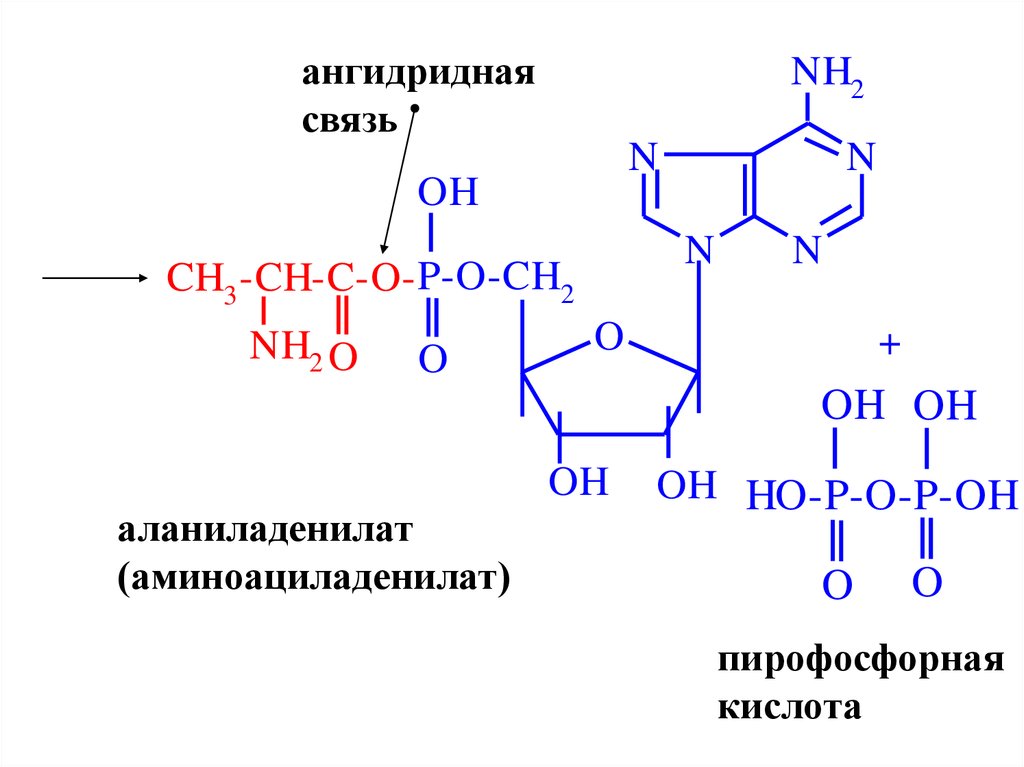
60.
ангидриднаясвязь
NH2
N
OH
N
CH3 -CH-C-O- P-O-CH2
NH2 O
O
N
N
O
+
OH OH
OH
аланиладенилат
(аминоациладенилат)
OH HO-P-O-P-OH
O
O
пирофосфорная
кислота
61.
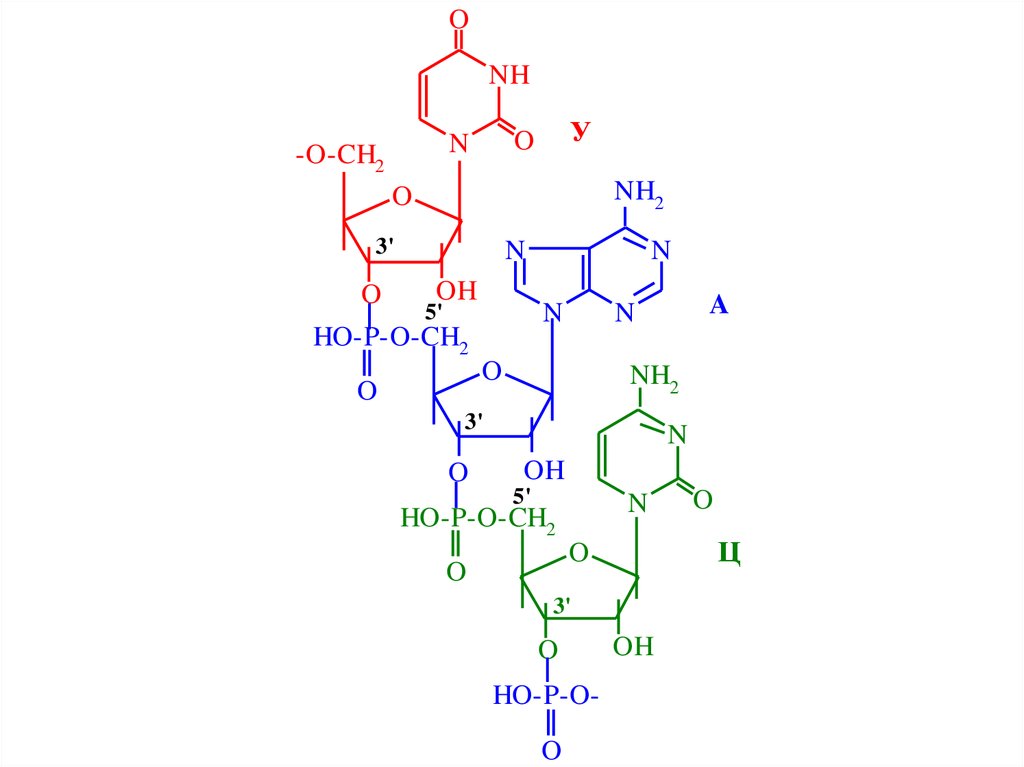
Первичная структура нуклеиновых кислот– нуклеотидная последовательность в
полинуклеотидной цепи
62.
ONH
У
O
N
-O-CH2
NH2
O
3'
O
N
OH
N
N
5'
HO-P-O-CH2
O
O
NH2
3'
O
A
N
N
OH
5'
N
HO-P-O-CH2
Ц
O
O
3'
O
HO-P-OO
O
OH
63. Первичная структура нуклеиновых кислот – нуклеотидная последовательность в полинуклеотидной цепи
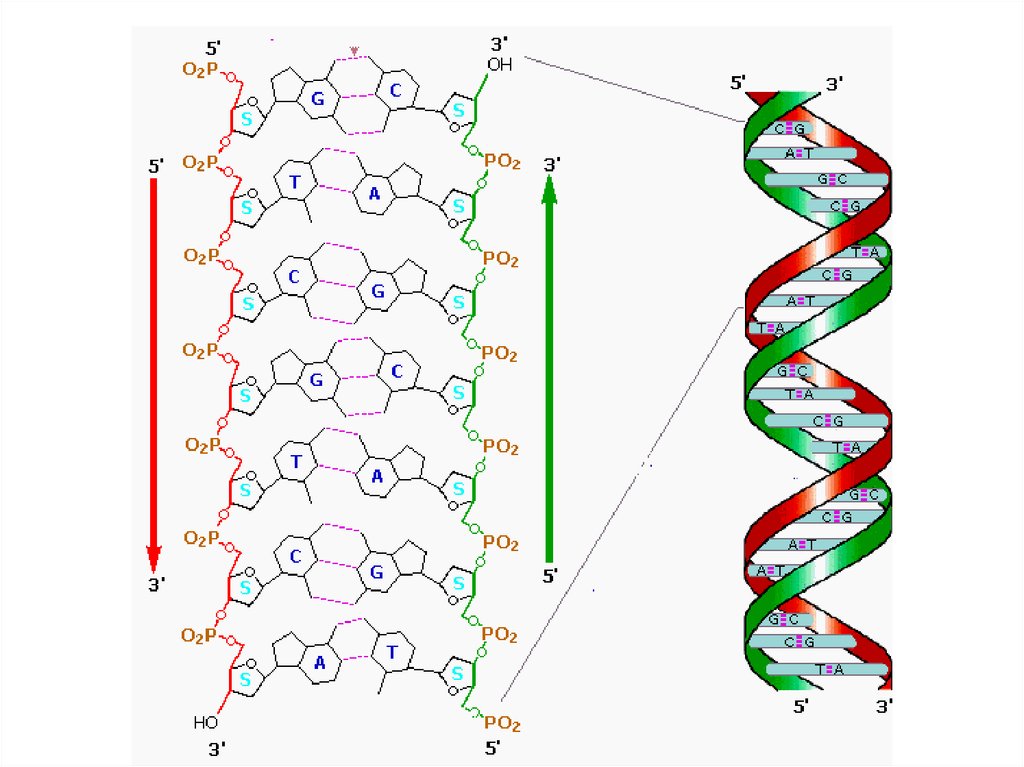
Вторичная структура нуклеиновых кислот –пространственная
организация
полинуклеотидных цепей, т.е. определенное
расположение полинуклеотидной цепи в
пространстве
64.
65. Вторичная структура нуклеиновых кислот – пространственная организация полинуклеотидных цепей, т.е. определенное расположение
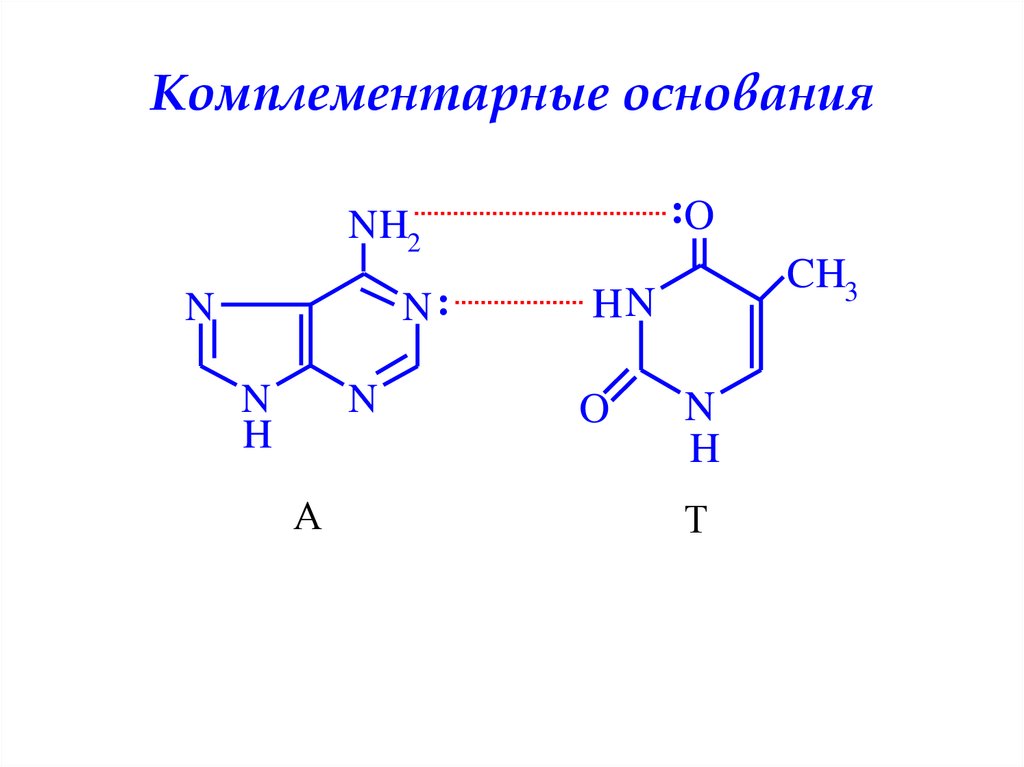
Комплементарные основания:O
NH2
N:
N
N
H
N
А
CH3
HN
O
N
H
Т
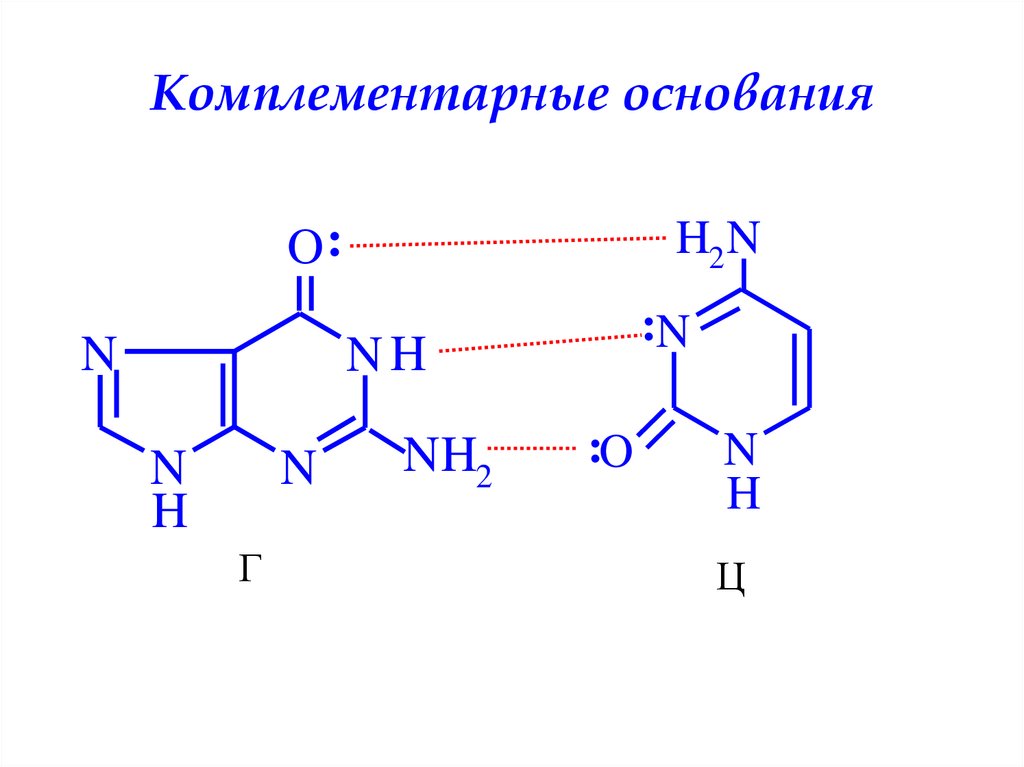
66.
Комплементарные основанияH2 N
O:
N
:N
NH
N
H
N
Г
NH2
:O
N
H
Ц





















 chemistry
chemistry








