Similar presentations:
Анализ кислотно-основного состояния крови
1. АНАЛИЗ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ КРОВИ
Карташов С.Н.ДОКТОР
БИОЛОГИЧЕСКИХ НАУК,
ПРОФЕССОР
2. КИСЛОТНО-ЩЕЛОЧНОЕ РАВНОВЕСИЕ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
КИСЛОТНО-ЩЕЛОЧНОЕ
РАВНОВЕСИЕ
КЩР определенное
соотношение концентрации
протонов водорода Н+ и
гидроксильных анионов (ОН-) в
биологических средах
организма
Когда увеличивается
содержание протонов
водорода, говорят об ацидозе
Когда увеличивается содержание
гидроксильных анионов, говорят
об алкалозе
3. Концентрация Н+ во внеклеточной жидкости составляет одну миллионную от содержания натрия
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
КОНЦЕНТРАЦИЯ Н+ ВО ВНЕКЛЕТОЧНОЙ ЖИДКОСТИ
СОСТАВЛЯЕТ ОДНУ МИЛЛИОННУЮ ОТ СОДЕРЖАНИЯ
НАТРИЯ
1. Врачи, как правило, соглашаются
с важностью понимания
расстройств КЩР, но
сопротивляются пониманию
научной части патологии и
области ее применения
2. рН является наиболее жесткой
физикохимической константой.
Концентрация Н+ во
внеклеточной жидкости
составляет одну миллионную
от содержания натрия и калия,
а регуляция на два порядка
точнее
4. ЗНАЧЕНИЕ ПОСТОЯНСТВА КЩР ДЛЯ ОРГАНИЗМА
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ЗНАЧЕНИЕ ПОСТОЯНСТВА
КЩР ДЛЯ ОРГАНИЗМА
1) рН определяет физикохимические свойства
коллоидных структур
2) рН определяет активность, конформацию белков
3) рН определяет чувствительность клеточных
рецепторов
4) рН определяет проницаемость клеточных мембран
4) рН регулирует сосудистый тонус
5) рН определяет состояние дыхательного центра
6) рН влияет на состояние ЦНС
5. ПОСЛЕДСТВИЯ СДВИГА рН+ В ТУ ИЛИ ИНУЮ СТОРОНУ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
+
ПОСЛЕДСТВИЯ СДВИГА РН В ТУ
ИЛИ ИНУЮ СТОРОНУ
сдвиг рН на одну десятую (0,1) от
нормы – выражается в тяжелой
патологии;
сдвиг рН на две три десятые (0,2-0,3)
– развивается коматозное состояние;
если рН сдвигается на три-четыре
десятые (0,3-0,4) – организм погибает.
ПОЧЕМУ ВОЗМОЖЕН ВЫХОД рН ЗА
ГРАНИЦЫ НОРМЫ?
Из-за недостаточности механизмов
регулирующих (выравнивающих)
соотношение кислот и оснований
6. МЕХАНИЗМЫ ПОДДЕРЖАНИЯ КЩР
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
МЕХАНИЗМЫ ПОДДЕРЖАНИЯ КЩР
Выделяют два основных
механизма, обеспечивающих
уравновешивание кислых
ионов:
1. Химические буферные
системы крови и тканей
2. Физиологические
буферные системы (дыхание
и почечная регуляция)
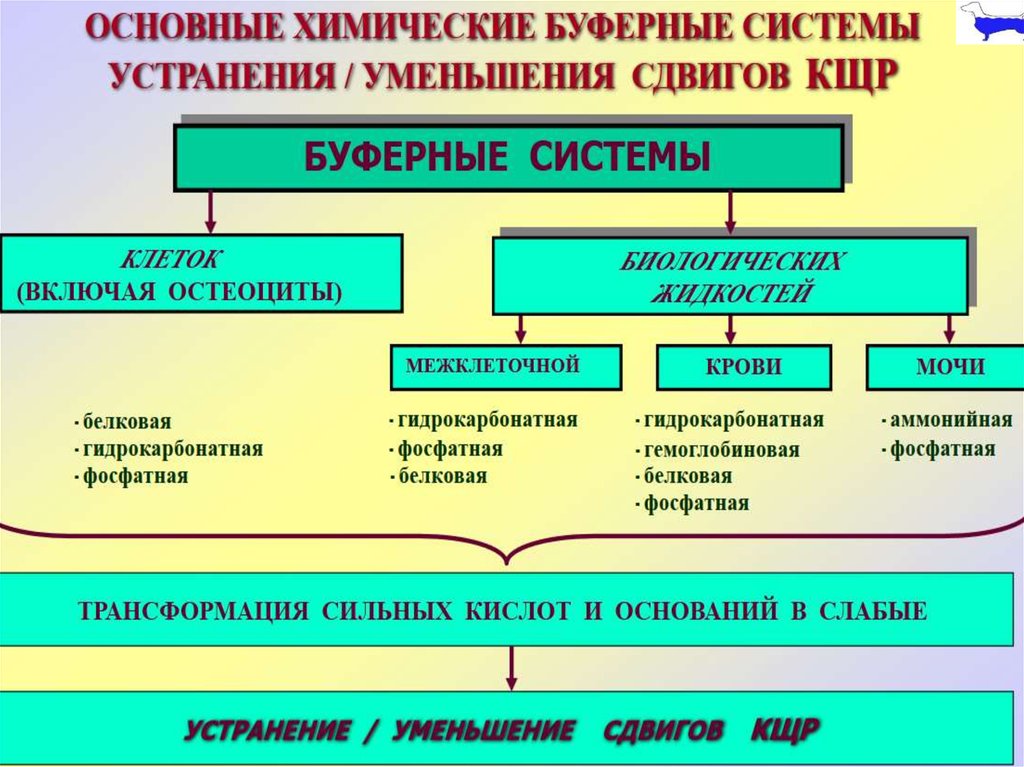
7. Химические буферные системы крови и тканей
ХИМИЧЕСКИЕ БУФЕРНЫЕСИСТЕМЫ КРОВИ И ТКАНЕЙ
8. ГИДРОКОРБОНАТНЫЙ БУФЕР
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ГИДРОКОРБОНАТНЫЙ БУФЕР
=
[H+]=24×(pCO2):[HCO3-]
УРАВНЕНИЕ Гендерсона-Хассельбаха
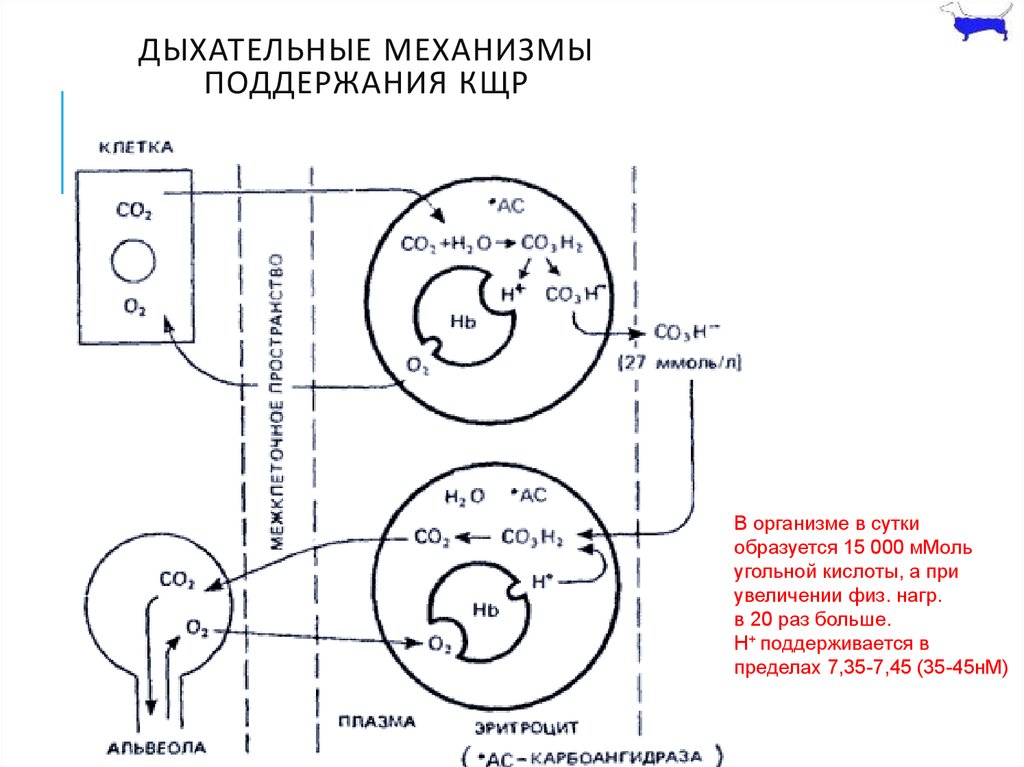
9. ДЫХАТЕЛЬНЫЕ МЕХАНИЗМЫ ПОДДЕРЖАНИЯ КЩР
В организме в суткиобразуется 15 000 мМоль
угольной кислоты, а при
увеличении физ. нагр.
в 20 раз больше.
H+ поддерживается в
пределах 7,35-7,45 (35-45нМ)
10. ПОЧЕЧНЫЕ МЕХАНИЗМЫ ПОДДЕРЖАНИЕ КЩР
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
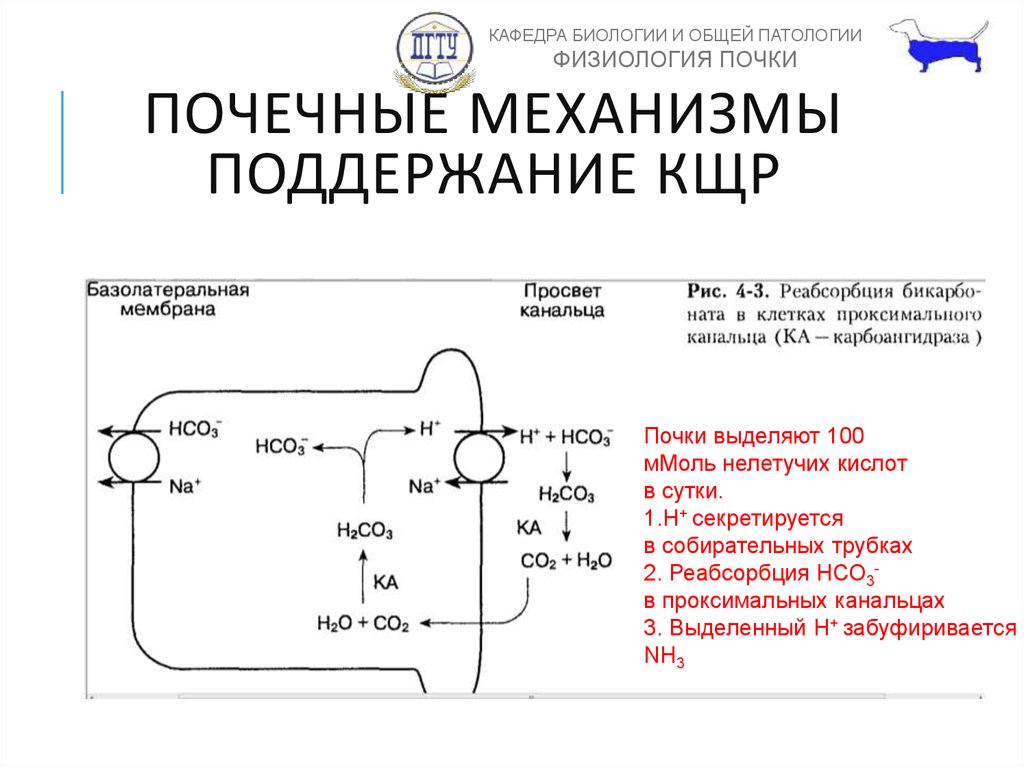
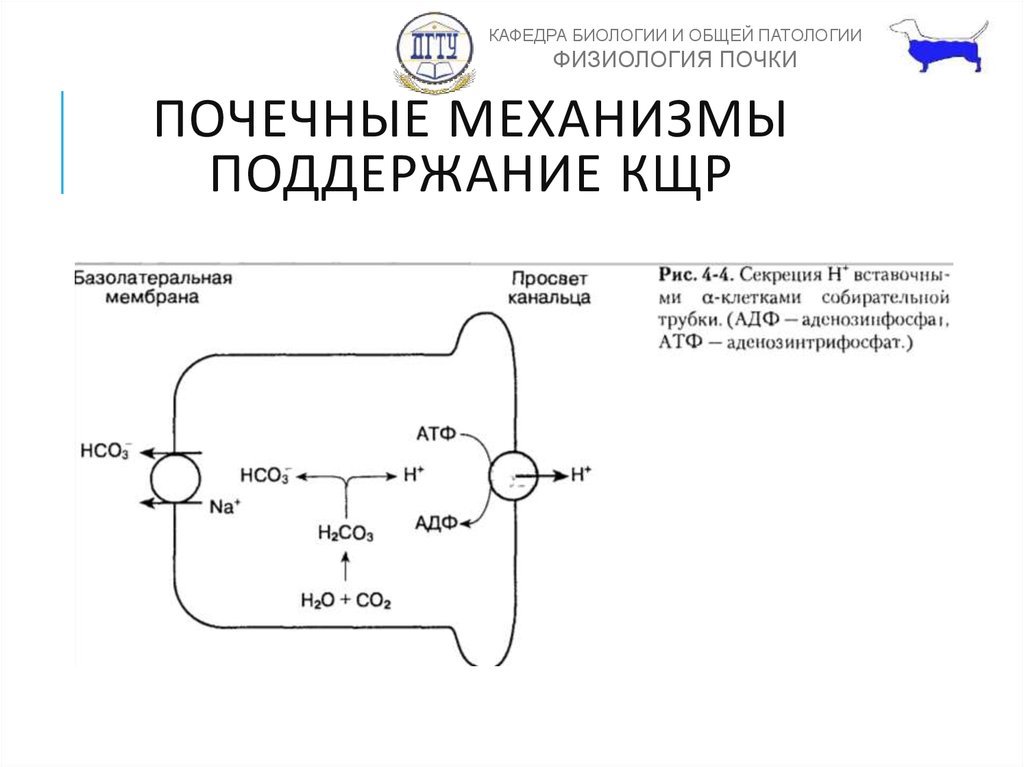
ПОЧЕЧНЫЕ МЕХАНИЗМЫ
ПОДДЕРЖАНИЕ КЩР
Почки выделяют 100
мМоль нелетучих кислот
в сутки.
1.H+ секретируется
в собирательных трубках
2. Реабсорбция HСО3в проксимальных канальцах
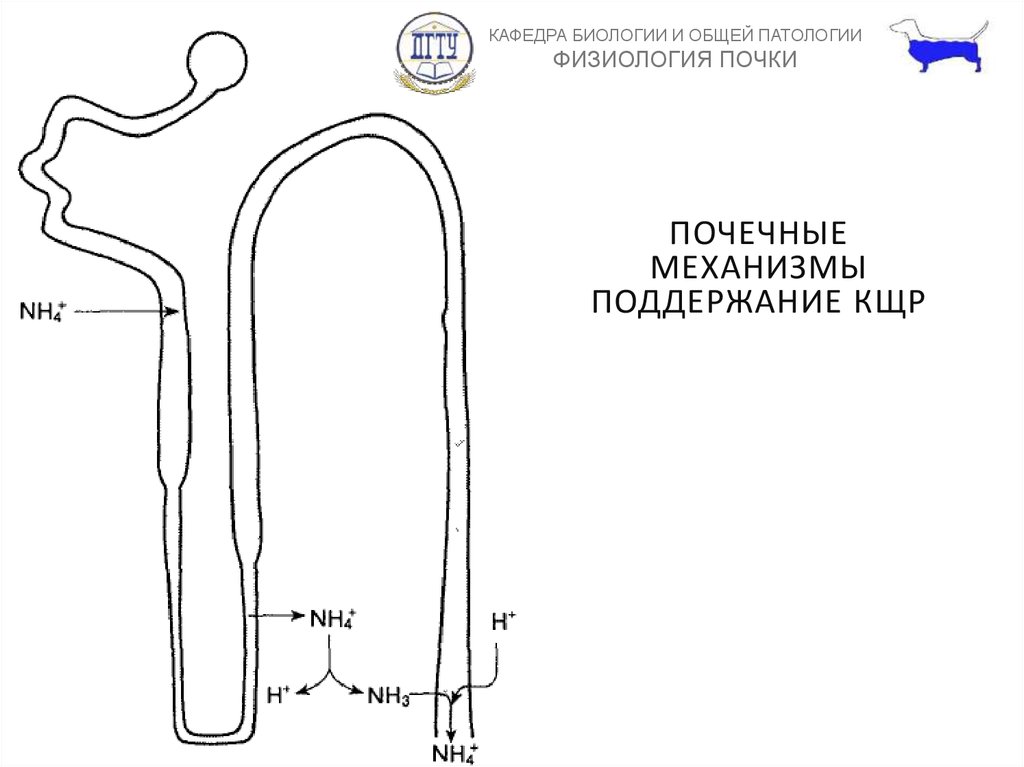
3. Выделенный H+ забуфиривается
NH3
11. ПОЧЕЧНЫЕ МЕХАНИЗМЫ ПОДДЕРЖАНИЕ КЩР
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ПОЧЕЧНЫЕ МЕХАНИЗМЫ
ПОДДЕРЖАНИЕ КЩР
12. ПОЧЕЧНЫЕ МЕХАНИЗМЫ ПОДДЕРЖАНИЕ КЩР
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ПОЧЕЧНЫЕ
МЕХАНИЗМЫ
ПОДДЕРЖАНИЕ КЩР
13.
РАБОТА ФИЗИОЛОГИЧЕСКИХ БУФЕРОВ ОРГАНИЗМА14. КИСЛОТНОСТЬ (PH)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
КИСЛОТНОСТЬ (PH)
pH
7,4±0,04
(норма)
7,36-7,44
4!
Ацидоз (ацидемия)
pH<7,35
Алкалоз (алкалемия)
pH>7,45
15. ФИЗИОЛОГИЯ КОС
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
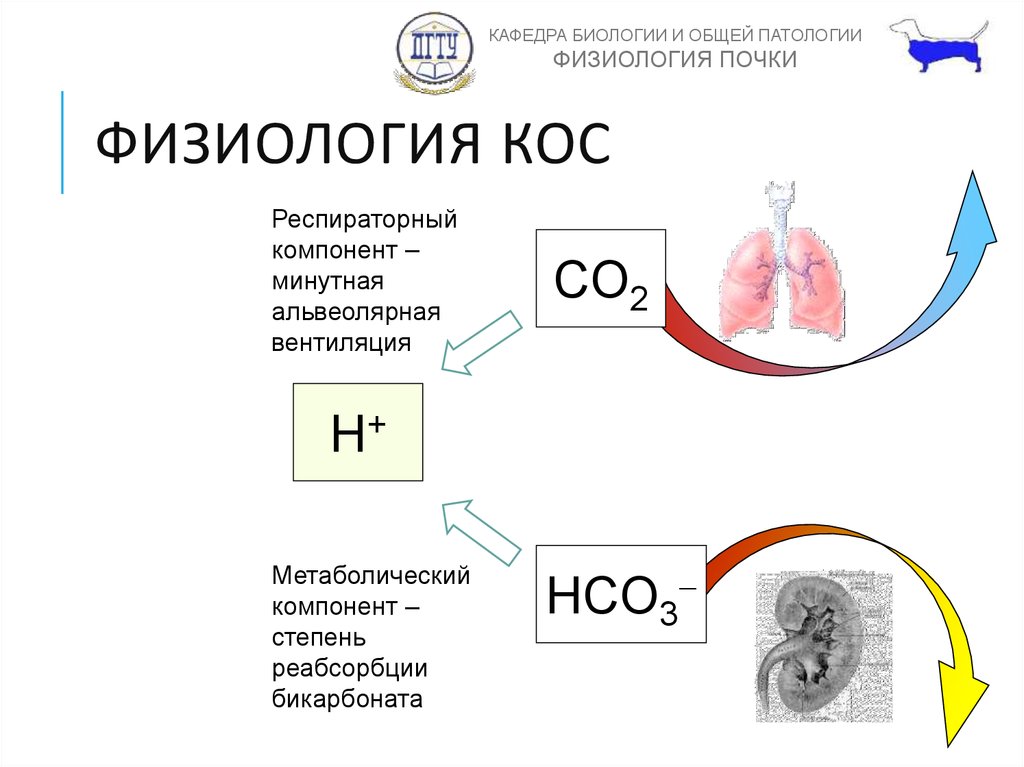
ФИЗИОЛОГИЯ КОС
Респираторный
компонент –
минутная
альвеолярная
вентиляция
CO2
H+
Метаболический
компонент –
степень
реабсорбции
бикарбоната
HCO3
16. ФИЗИОЛОГИЯ КОС
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
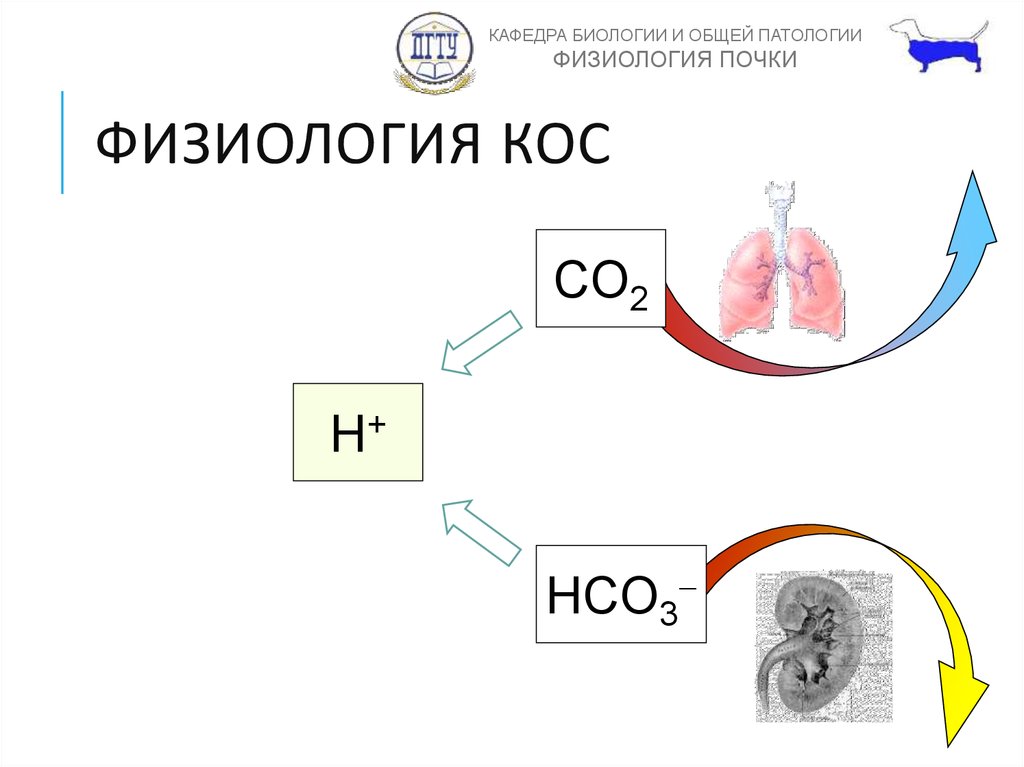
ФИЗИОЛОГИЯ КОС
CO2
H+
HCO3
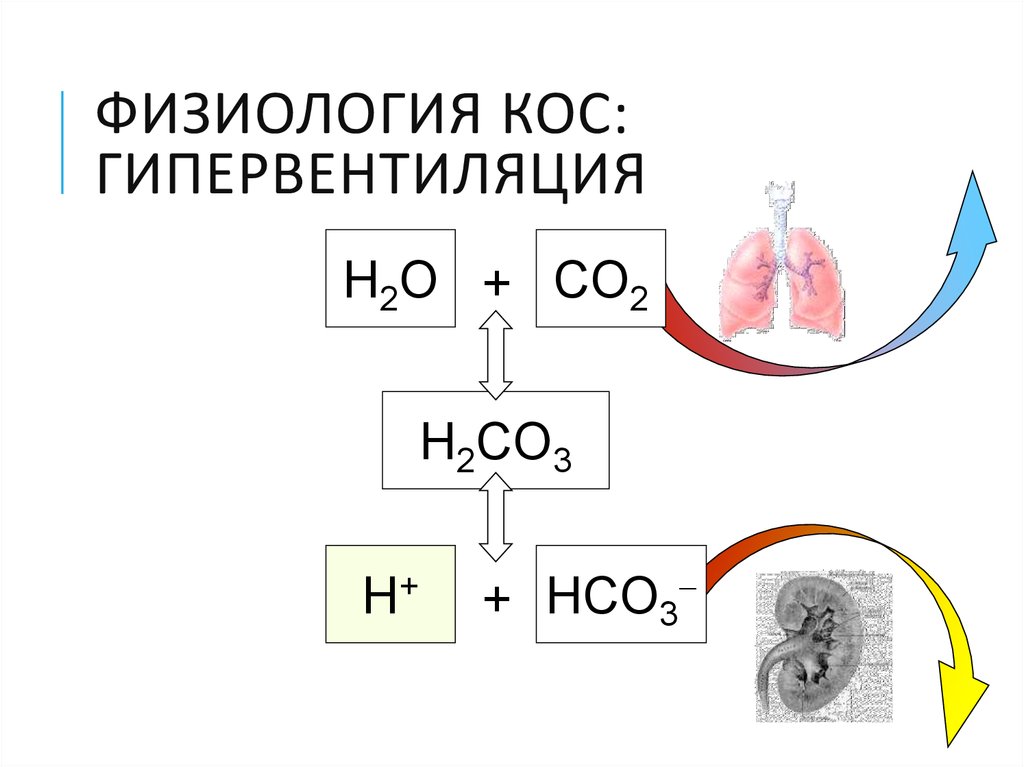
17. ФИЗИОЛОГИЯ КОС: ГИПЕРВЕНТИЛЯЦИЯ
H2O + CO2H2CO3
H+
+ HCO3
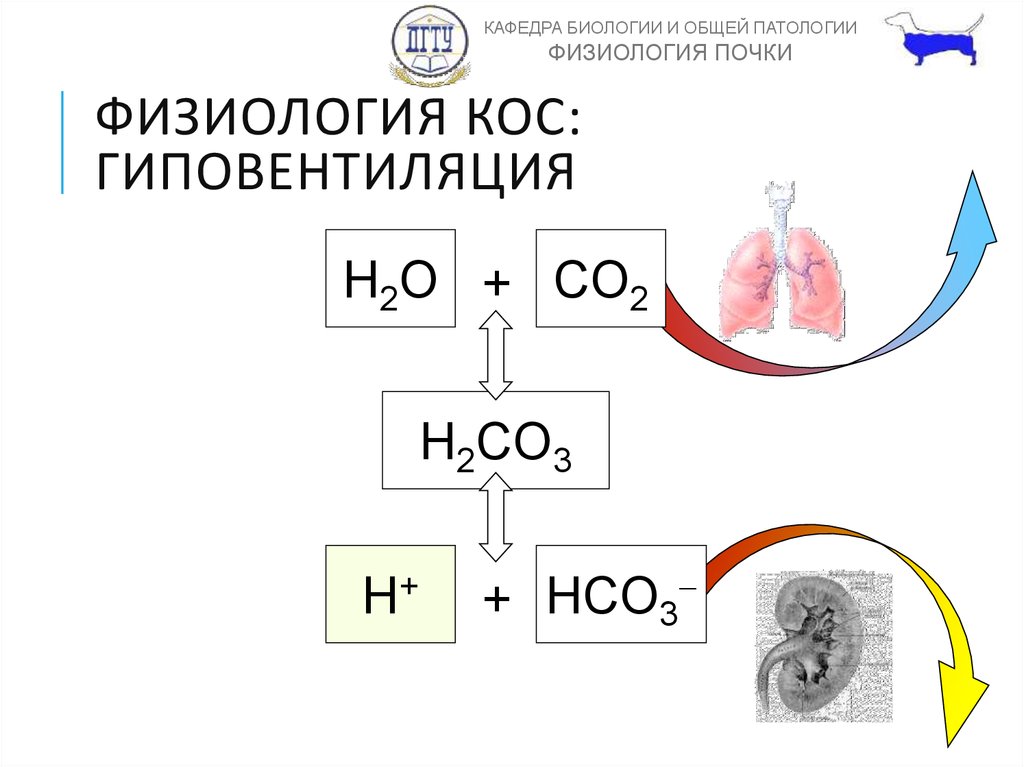
18. ФИЗИОЛОГИЯ КОС: ГИПОВЕНТИЛЯЦИЯ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ФИЗИОЛОГИЯ КОС:
ГИПОВЕНТИЛЯЦИЯ
H2O + CO2
H2CO3
H+
+ HCO3
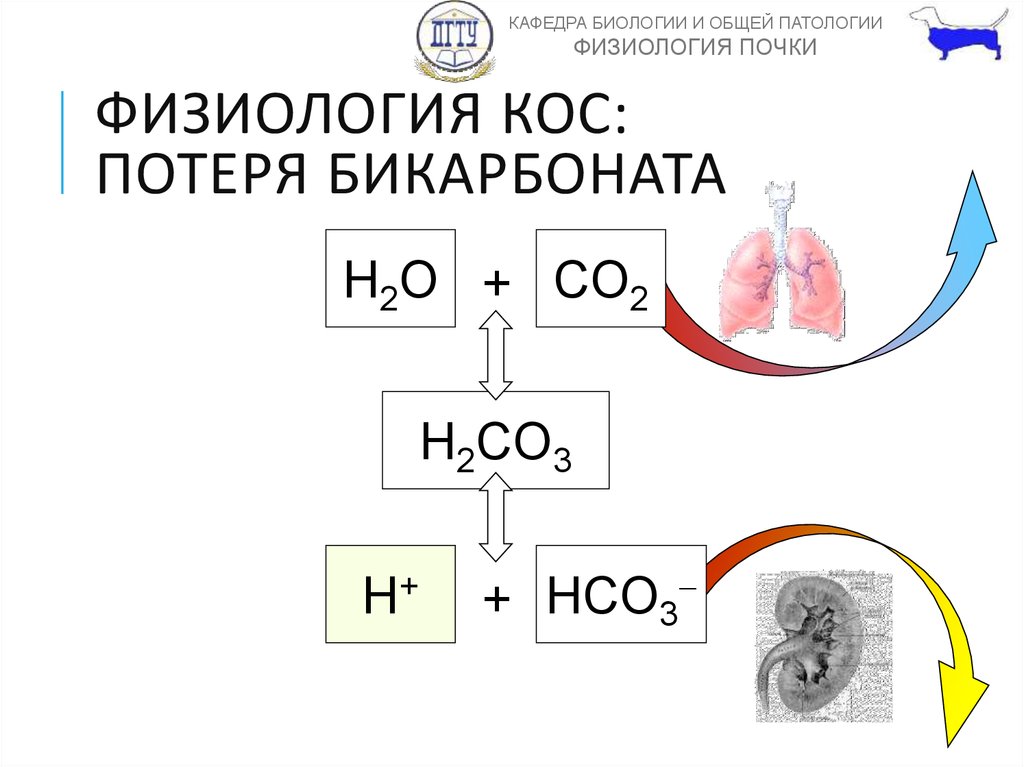
19. ФИЗИОЛОГИЯ КОС: ПОТЕРЯ БИКАРБОНАТА
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ФИЗИОЛОГИЯ КОС:
ПОТЕРЯ БИКАРБОНАТА
H2O + CO2
H2CO3
H+
+ HCO3
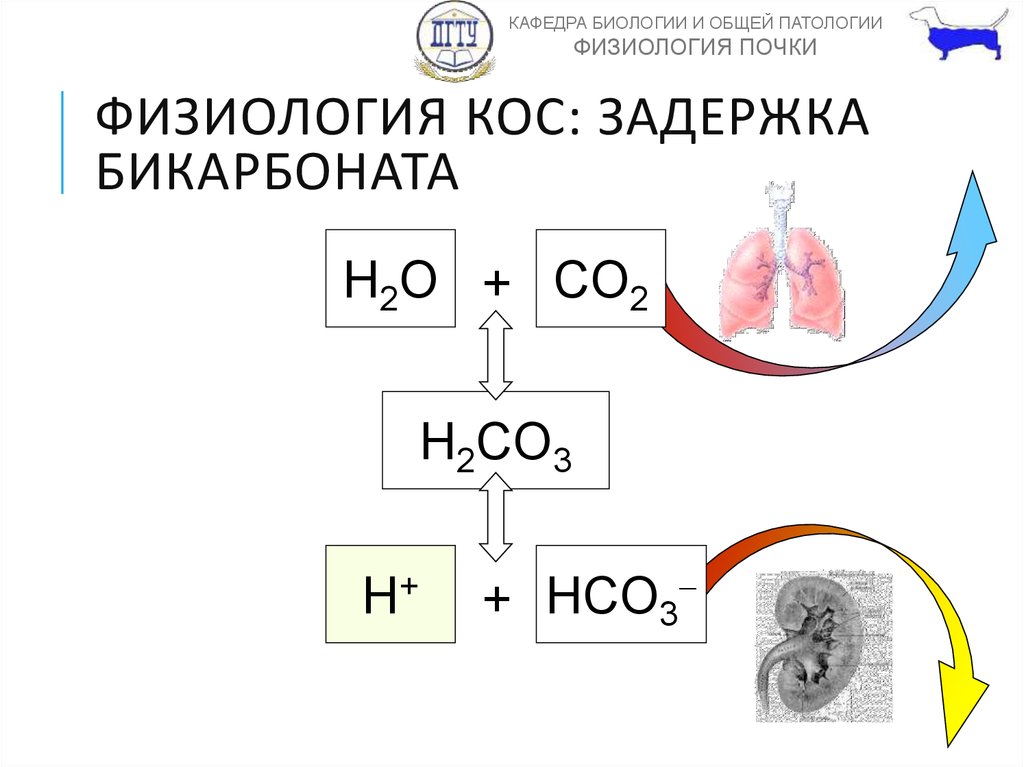
20. ФИЗИОЛОГИЯ КОС: ЗАДЕРЖКА БИКАРБОНАТА
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ФИЗИОЛОГИЯ КОС: ЗАДЕРЖКА
БИКАРБОНАТА
H2O + CO2
H2CO3
H+
+ HCO3
21.
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
Бикарбонат – это сода (щелочная
реакция)
Протоны H+ - это кислота
их источник в том числе и H2CO3
22. НОРМЫ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
НОРМЫ
pH
7,4±0,04
pCO2
40±4 мм рт. ст.
HCO3
24±4 ммоль/л
4!
23. РЕСПИРАТОРНЫЙ КОМПОНЕНТ: ВЕНТИЛЯЦИЯ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
РЕСПИРАТОРНЫЙ КОМПОНЕНТ:
ВЕНТИЛЯЦИЯ
Оценивается по CO2
Прямо пропорциональна минутной альвеолярной
вентиляции (л/мин)
Чем больше вентилиция, тем меньше pCO2
Зависит от:
Респираторного драйва, нервно-мышечной передачи и
дыхательной мускулатуры
Проходимость дыхательных путей
Состояния плевральной полости и каркаса грудной клетки
Вентиляционно-перфузионного отношения
24. МЕТАБОЛИЧЕСКИЙ КОМПОНЕНТ: КОНЦЕНТРАЦИЯ БИКАРБОНАТА
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
МЕТАБОЛИЧЕСКИЙ КОМПОНЕНТ:
КОНЦЕНТРАЦИЯ БИКАРБОНАТА
Оценивается по HCO3- и BE
(щелочной резерв)
Зависит от:
Реабсорбции/задержки бикарбоната почками
Появления кислот, диссоциирующих на анион и
H+, связывающий бикарбонат
Потерь бикарбоната с экссудатами и мочой
25. ФИЗИОЛОГИЯ НАРУШЕНИЯ КОС
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ФИЗИОЛОГИЯ НАРУШЕНИЯ
КОС
Первичное нарушение приводит к
сдвигу pH
Вторичное нарушение является
компенсаторным, направлено в
противоположную сторону
26. ПОНЯТИЕ КОМПЕНСАЦИИ И ДЕКОМПЕНСАЦИИ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ПОНЯТИЕ КОМПЕНСАЦИИ И
ДЕКОМПЕНСАЦИИ
Компенсация – pH в норме,
а pCO2 и HCO3 изменены хронический или медленный процесс, в
ОРИТ встречается реже
Декомпенсация – наличие сдвига pH, в
ОРИТ встречается чаще
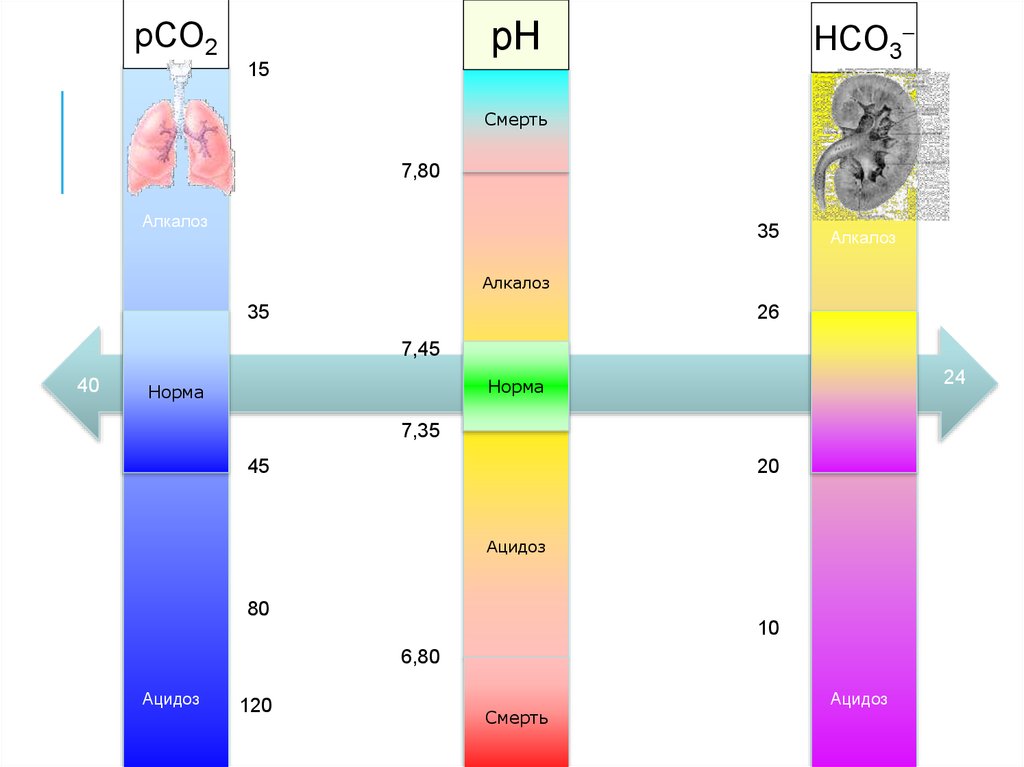
27.
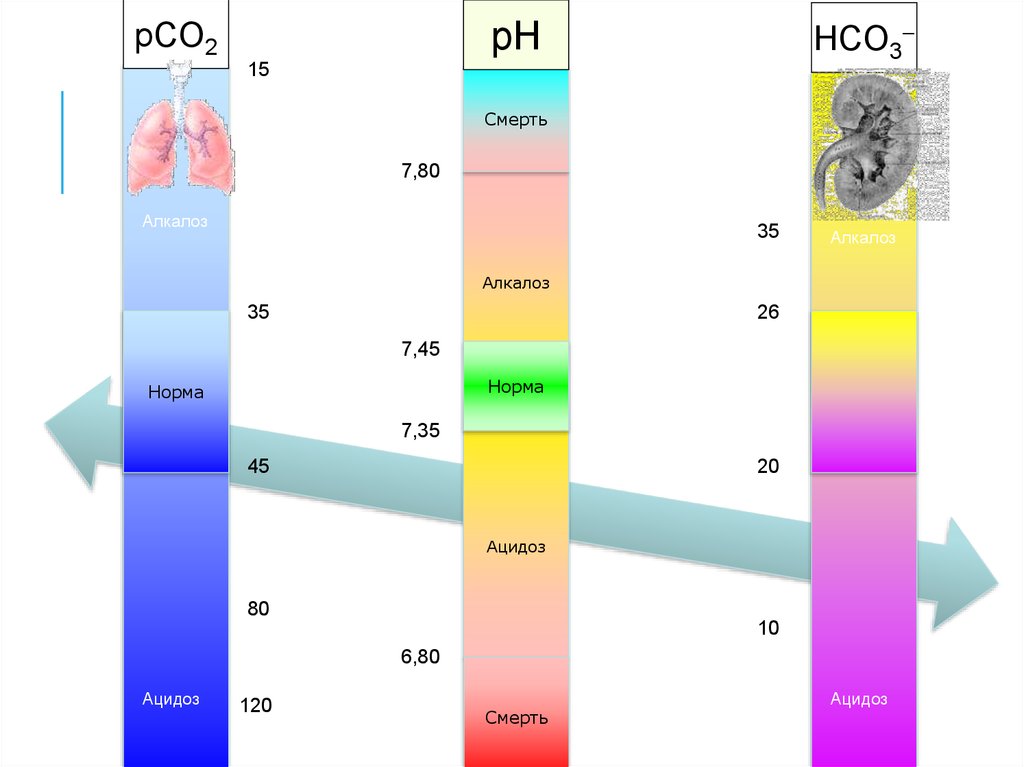
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
40
24
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
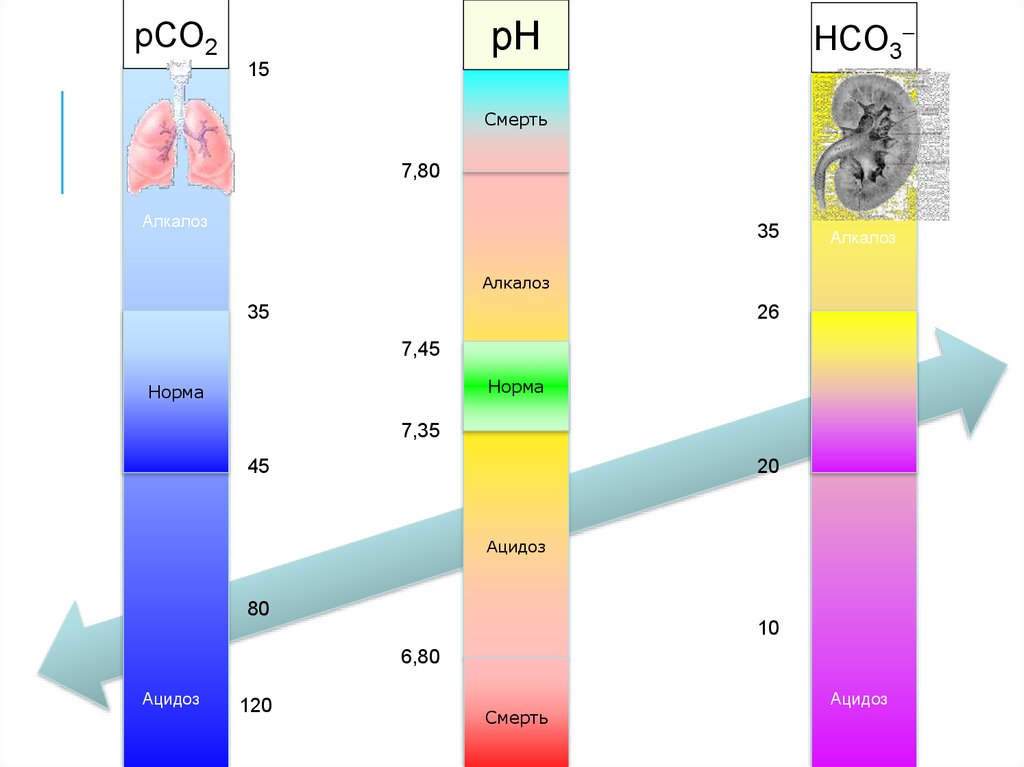
28.
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
40
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
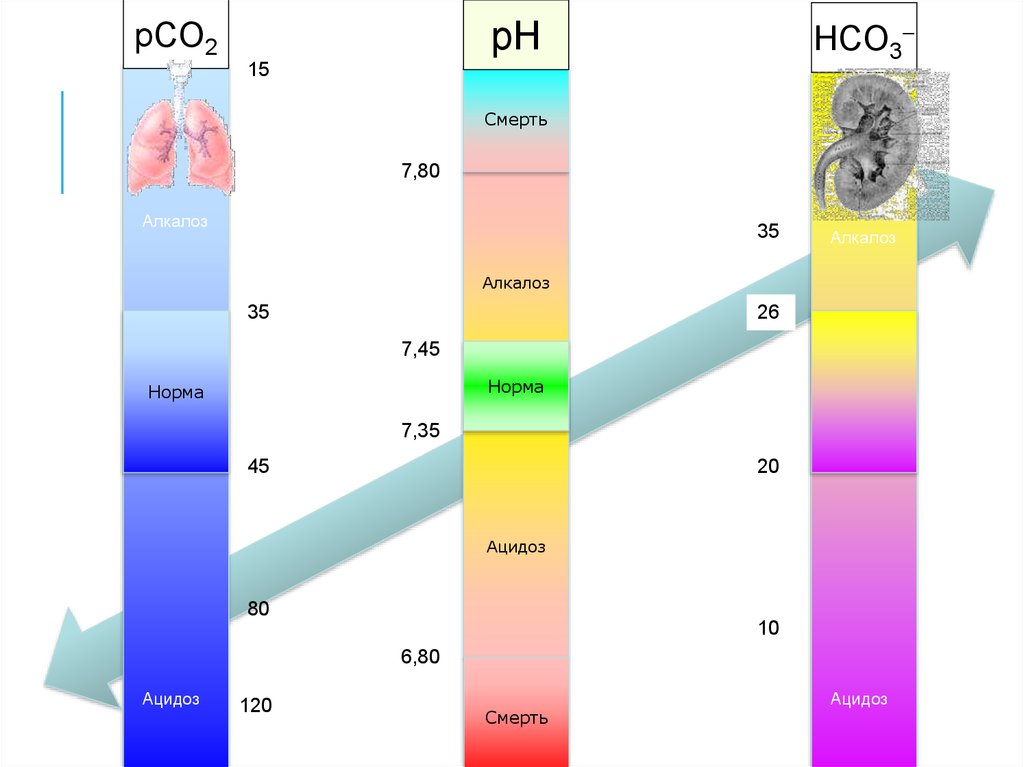
29.
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
40
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
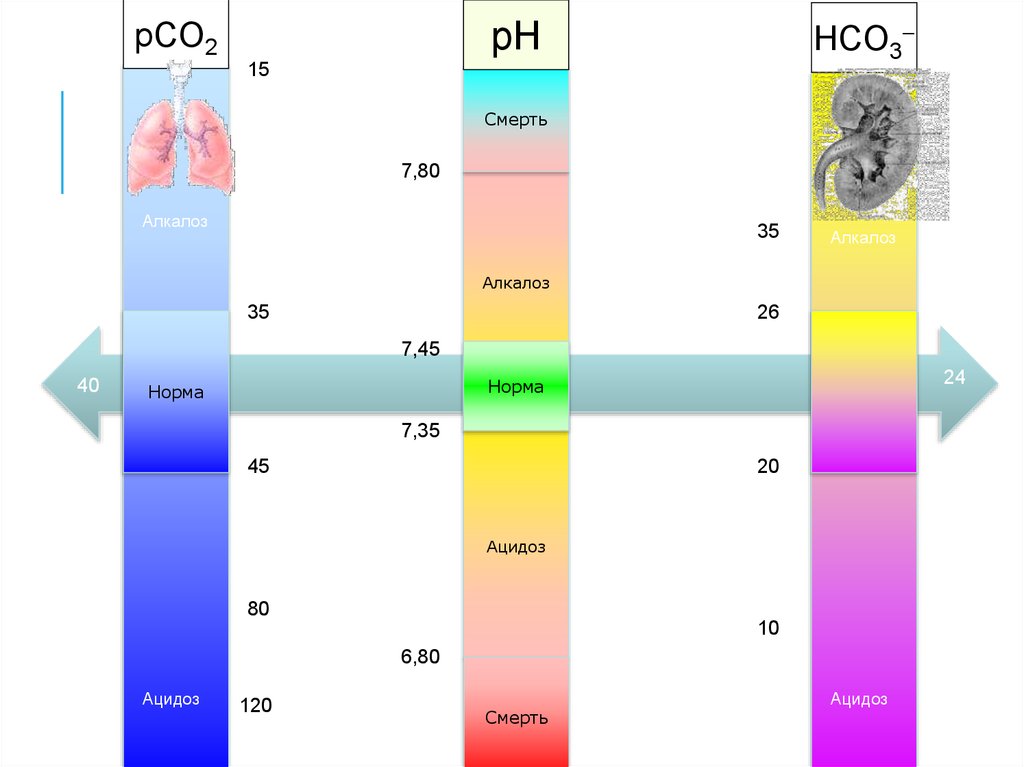
30.
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
40
24
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
31.
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
24
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
32.
HCO3pH
pCO2
15
Смерть
25
7,80
Алкалоз
35
Алкалоз
Алкалоз
35
26
7,45
24
Норма
Норма
7,35
45
20
Ацидоз
80
10
6,80
Ацидоз
120
Смерть
Ацидоз
33. ДЕКОМПЕНСИРОВАННОЕ НАРУШЕНИЕ КОС
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
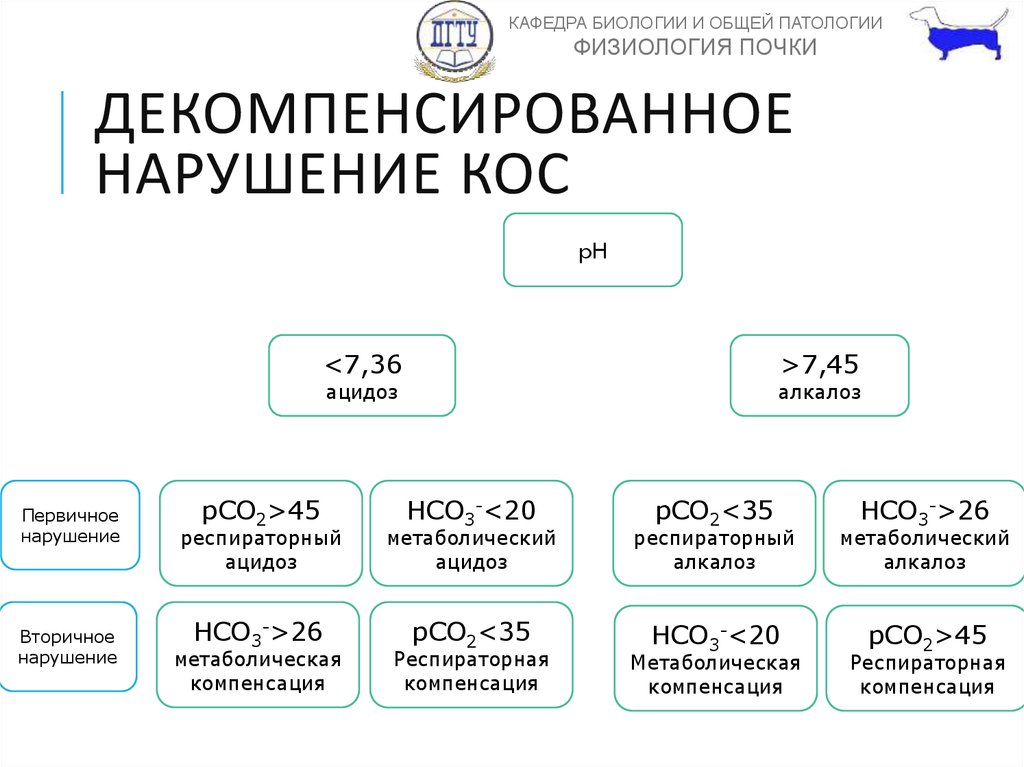
ДЕКОМПЕНСИРОВАННОЕ
НАРУШЕНИЕ КОС
pH
<7,36
>7,45
ацидоз
Первичное
нарушение
Вторичное
нарушение
pCO2>45
алкалоз
HCO3-<20
pCO2<35
HCO3->26
респираторный
ацидоз
метаболический
ацидоз
респираторный
алкалоз
метаболический
алкалоз
HCO3->26
pCO2<35
HCO3-<20
pCO2>45
метаболическая
компенсация
Респираторная
компенсация
Метаболическая
компенсация
Респираторная
компенсация
34. ПЕРВИЧНОЕ НАРУШЕНИЕ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ПЕРВИЧНОЕ НАРУШЕНИЕ
pH
7,30
pO2
130
Что приводит к сдвигу pH?
pCO2 25
HCO3 10
BE
-10
SpO2
100
K
4,1
Na
133
Cl
115
Hb
140
Htc
40%
Респираторный (pCO2)
компонент
или
Метаболический (HCO3 )
компонент?
35. ВТОРИЧНОЕ НАРУШЕНИЕ (КОМПЕНСАЦИЯ)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ВТОРИЧНОЕ НАРУШЕНИЕ
(КОМПЕНСАЦИЯ)
pH
7,30
pO2
130
Что старается вернуть pH в
норму?
pCO2 25
HCO3 10
BE
-10
SpO2
100
K
4,1
Na
133
Cl
115
Hb
140
Htc
40%
Респираторный (pCO2)
компонент
или
Метаболический (HCO3 )
компонент?
36. ЩЕЛОЧНОЙ РЕЗЕРВ (BE)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ЩЕЛОЧНОЙ РЕЗЕРВ (BE)
BE = 0,9287 [HCO3 – 24,4 + 14,83 (pH – 7,4)]
Oтражает метаболический компонент КЩС при
нормальных условиях
(давление 1 атм, paCO2=40)
Количество ммоль кислоты или основания,
которые необходимо добавить к 1 л крови,
чтобы pH вернулось в норму
Норма BE: 0…+2
37. ИНТЕРПРЕТАЦИЯ BE
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ИНТЕРПРЕТАЦИЯ BE
Норма 0±4 (обычно +2)
“-” метаболический ацидоз или
компенсация
“+” метаболический алкалоз или
компенсация
38. АНИОННАЯ РАЗНИЦА (ANION GAP)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
АНИОННАЯ РАЗНИЦА
(ANION GAP)
Разница между неизмеряемыми
анионами и катионами
AG=(Na+ + K+) - (HCO3 +Cl )
Позволяет увидеть появление
дополнительного неизмеряемого
аниона
39. АНИОННАЯ РАЗНИЦА (AG)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
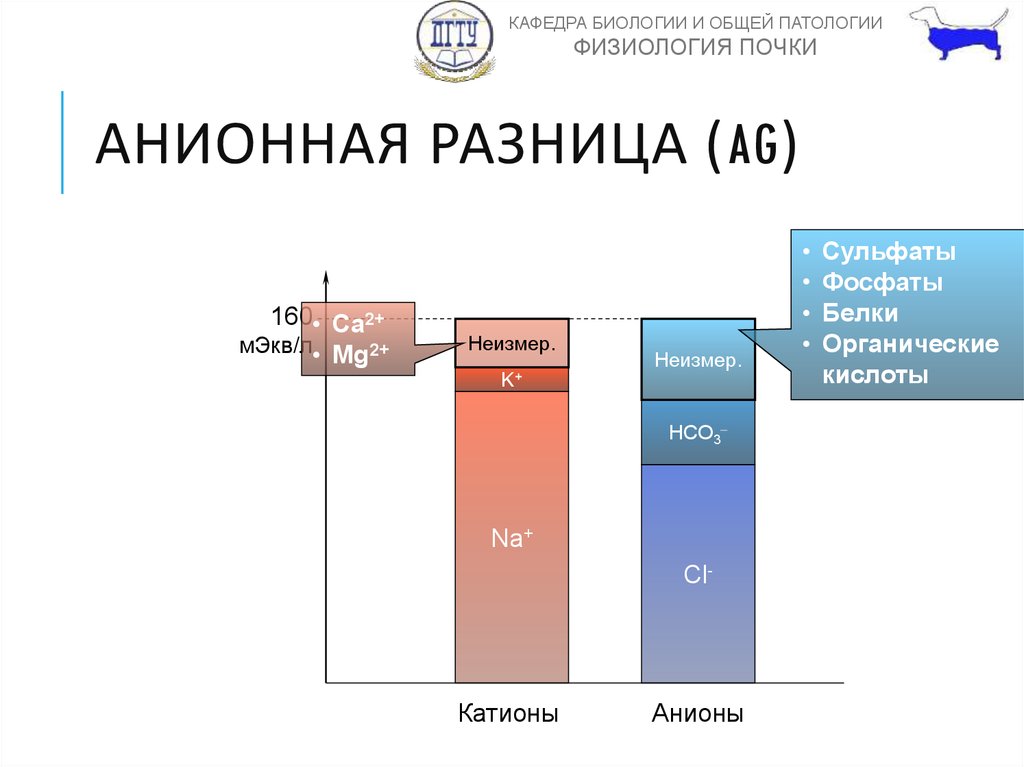
АНИОННАЯ РАЗНИЦА (AG)
160• Ca2+
мЭкв/л• Mg2+
Неизмер.
Неизмер.
K+
HCO3
Na+
Cl-
Катионы
Анионы
Сульфаты
Фосфаты
Белки
Органические
кислоты
40. АНИОННАЯ РАЗНИЦА (AG)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
АНИОННАЯ РАЗНИЦА (AG)
Anion gap
K+
HCO3
Na+
Cl-
Норма
41. ГИПЕРХЛОРЕМИЧЕСКИЙ АЦИДОЗ – ПРИ ПОТЕРЕ HCO3-
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
ГИПЕРХЛОРЕМИЧЕСКИЙ
АЦИДОЗ – ПРИ ПОТЕРЕ HCO3-
K+
HCO3
Na+
Cl-
Гиперхлоремический
HCO3
Cl-
42. НОРМОХЛОРЕМИЧЕСКИЙ АЦИДОЗ – ПРИ ПОЯВЛЕНИИ НЕИЗМЕРЯЕМОГО АНИОНА
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
НОРМОХЛОРЕМИЧЕСКИЙ
АЦИДОЗ – ПРИ ПОЯВЛЕНИИ
НЕИЗМЕРЯЕМОГО АНИОНА
K+
HCO3
Na+
Cl-
Гиперхлоремический
HCO3
Cl-
HCO3
Cl-
Нормохлоремический
43. НОРМА AG
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
НОРМА AG
Человеки 8-12 мЭкв/л
Собаки 12-24 мЭкв/л
Кошки 13-27 мЭкв/л
такая разница потому, что у животных
белки имеют бóльший заряд, чем у человека
44. СНИЖЕНИЕ AG
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
СНИЖЕНИЕ AG
Гипопротеинемия
Снижение общего белка на 10 г/л
снижает AG на 2,5 мЭкв/л
Гипоальбуминемия
Снижение альбумина на 10 г/л
снижает AG на 4,1 мЭкв/л
45. ВИДЫ НАРУШЕНИЙ КОС
46. РЕСПИРАТОРНЫЙ АЦИДОЗ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
РЕСПИРАТОРНЫЙ АЦИДОЗ
pH
7,28
pO2
60
pCO2
78
Неэффективная вентиляция и/или
перфузия легких
HCO3 29
BE
-4
SpO2
90
ЦНС, n. phrenicus,
дыхательные мышцы
K
6,2
Воздухоносные пути
Na
155
Cl
108
Hb
155
Htc
49%
Плевральная полость,
грудная стенка, диафрагма
47. РЕСПИРАТОРНЫЙ АЛКАЛОЗ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
РЕСПИРАТОРНЫЙ АЛКАЛОЗ
pH
7,51
pO2
100
pCO2
20
HCO3 19
BE
+5
SpO2
100
K
3,2
Na
147
Cl
111
Hb
140
Htc
40%
Тахипноэ
Повреждения ЦНС
Возбуждение
Лихорадка, гипертермия
Ятрогенное тахипноэ при ИВЛ
Эклампсия
48. МЕТАБОЛИЧЕСКИЙ АЦИДОЗ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
МЕТАБОЛИЧЕСКИЙ АЦИДОЗ
Потери бикарбоната
(гиперхлоремический)
Введение H+ и связывание бикарбоната
(нормохлоремический)
Дифференцируем по анионной разнице,
уровню хлора и клинической картине
49. АЦИДОЗ С УВЕЛИЧЕНИЕМ AG (НОРМОХЛОРЕМИЧЕСКИЙ)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
АЦИДОЗ С УВЕЛИЧЕНИЕМ AG
(НОРМОХЛОРЕМИЧЕСКИЙ)
pH
7,25
pO2
100
pCO2
33
HCO3 15
BE
-8
SpO2
100
K
6,6
Na
155
Cl
109
Hb
138
Htc
37%
H+ связывает бикарбонат
Увеличиваются неизмеряемые
анионы
Лактат-ацидоз
Шок
Серьезная гипоксемия
Генерализованные судороги
Тяжелый сепсис
50. АЦИДОЗ С УВЕЛИЧЕНИЕМ AG (НОРМОХЛОРЕМИЧЕСКИЙ)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
АЦИДОЗ С УВЕЛИЧЕНИЕМ AG
(НОРМОХЛОРЕМИЧЕСКИЙ)
pH
7,25
pO2
100
pCO2
33
HCO3 15
BE
-8
SpO2
100
Парентеральное питание (избыток
аминокислот)
Уремические токсины
Кетоацидоз
Отравление
K
6,6
Na
155
Cl
109
Hb
138
Htc
37%
Метанол
Этиленгликоль
Паральдегид
Салицилаты
51. АЦИДОЗ БЕЗ УВЕЛИЧЕНИЯ AG (ГИПЕРХЛОРЕМИЧЕСКИЙ)
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
АЦИДОЗ БЕЗ УВЕЛИЧЕНИЯ AG
(ГИПЕРХЛОРЕМИЧЕСКИЙ)
pH
7,30
pO2
85
pCO2
23
HCO3
11
BE
-6
SpO2
100
K
3,5
Na
141
Cl
130
Hb
140
Htc
40%
Потери бикарбоната, компенсируются
повышением ClЧерез ЖКТ
Диарея
Панкреат. или билиарн. фистула
Через почки
Компенсация респ. алкалоза
Канальцевый некроз
Гипоперфузия почек
Ингибиторы карбоангидразы
Ятрогенный
52. МЕТАБОЛИЧЕСКИЙ АЛКАЛОЗ
КАФЕДРА БИОЛОГИИ И ОБЩЕЙ ПАТОЛОГИИФИЗИОЛОГИЯ ПОЧКИ
МЕТАБОЛИЧЕСКИЙ АЛКАЛОЗ
pH
7,65
pO2
100
pCO2
35
HCO3 38
Потеря хлора – «желудочная рвота»,
фуросемид
BE
+9
Гемоконцентрация
SpO2
100
Рвота, полиурия, асцит
K
3,1
Na
153
Гипокалиемия, в т.ч. при
гиперальдостеронизм
Cl
112
Введение щелочных растворов
Hb
181
Htc
65%

































 medicine
medicine biology
biology








