Similar presentations:
Биологически важные ароматические и гетероциклические соединения
1. Биологически важные ароматические и гетероциклические соединения
Лекция № 13Биологически важные
ароматические и
гетероциклические
соединения
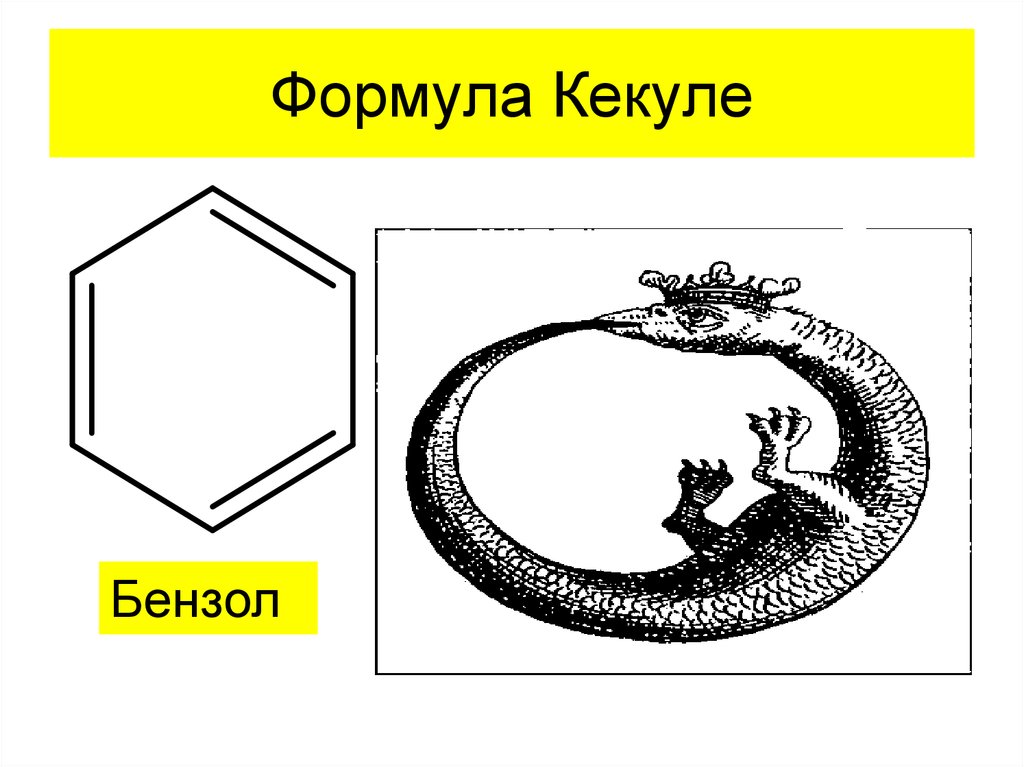
2. Формула Кекуле
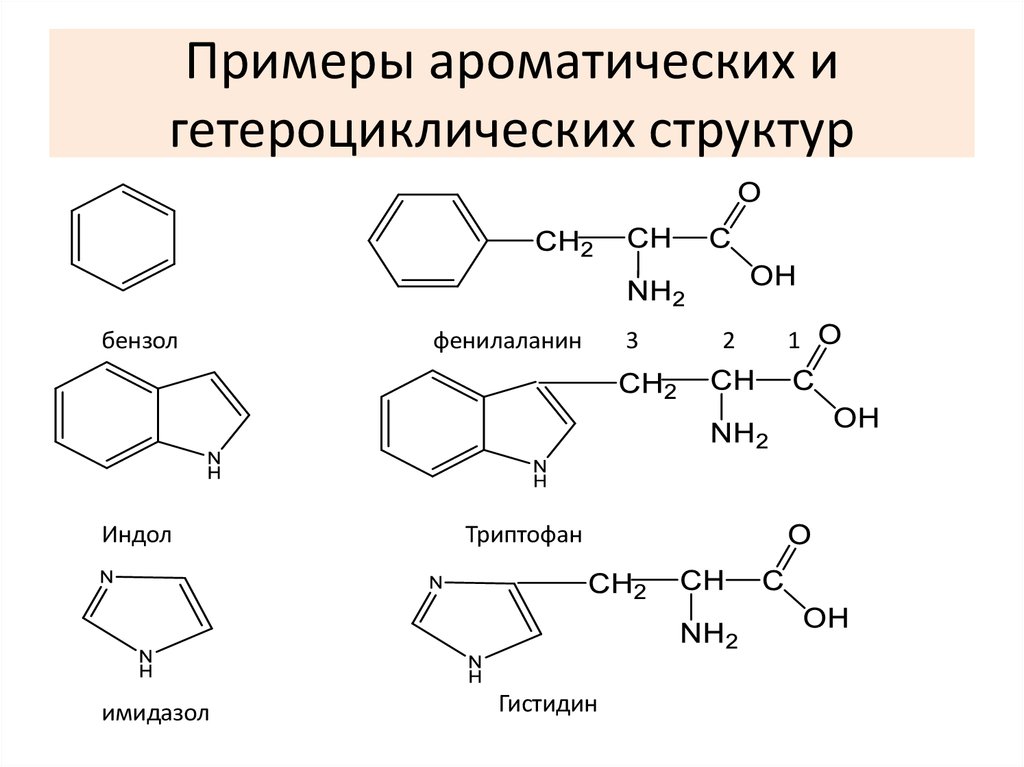
Бензол3. Примеры ароматических и гетероциклических структур
бензолфенилаланин
Индол
Триптофан
имидазол
Гистидин
3
2
1
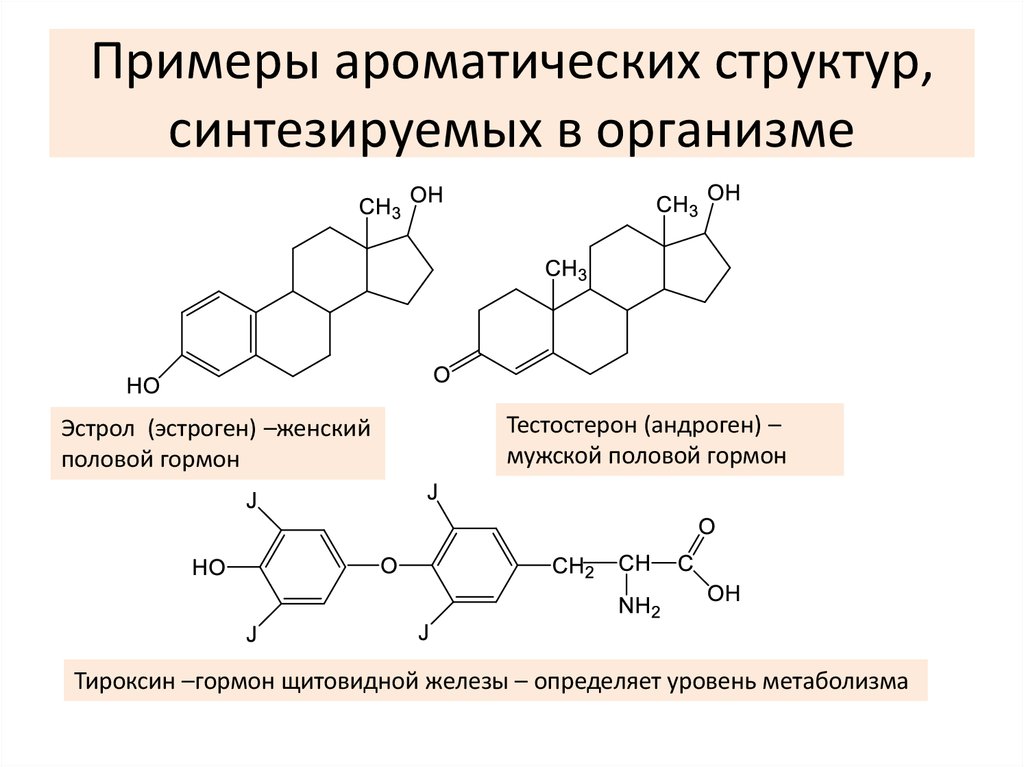
4. Примеры ароматических структур, синтезируемых в организме
Эстрол (эстроген) –женскийполовой гормон
Тестостерон (андроген) –
мужской половой гормон
Тироксин –гормон щитовидной железы – определяет уровень метаболизма
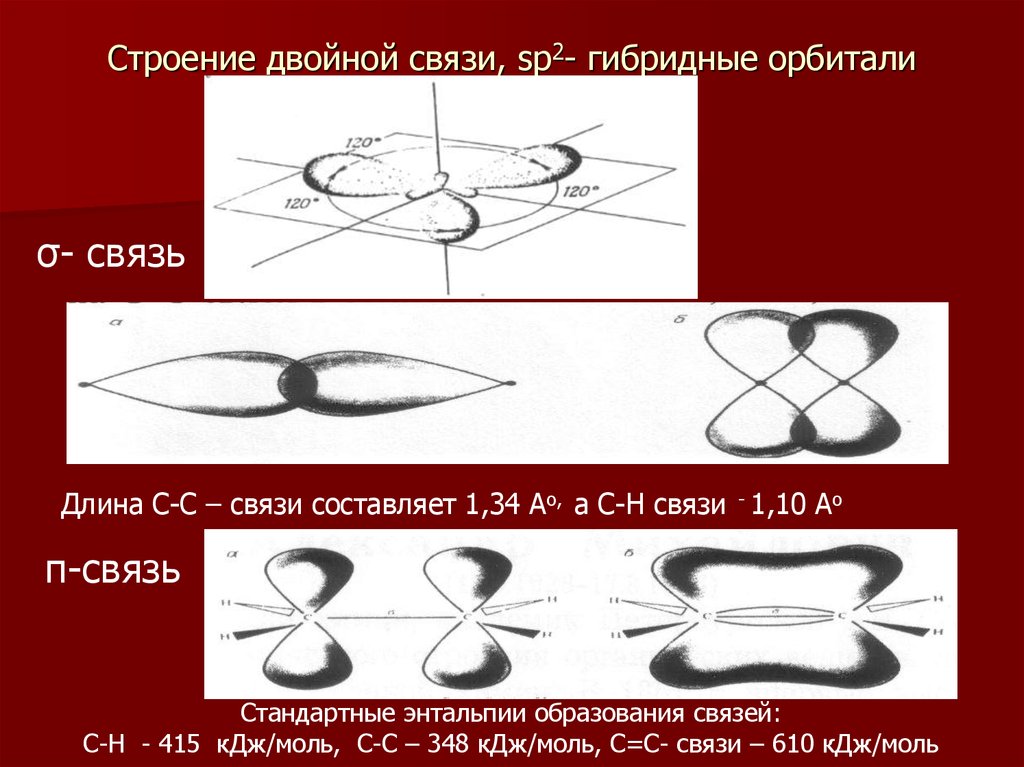
5. Строение двойной связи, sp2- гибридные орбитали
σ- связьДлина С-С – связи составляет 1,34 Ао, а С-Н связи - 1,10 Ао
π-связь
Стандартные энтальпии образования связей:
С-Н - 415 кДж/моль, С-С – 348 кДж/моль, С=С- связи – 610 кДж/моль
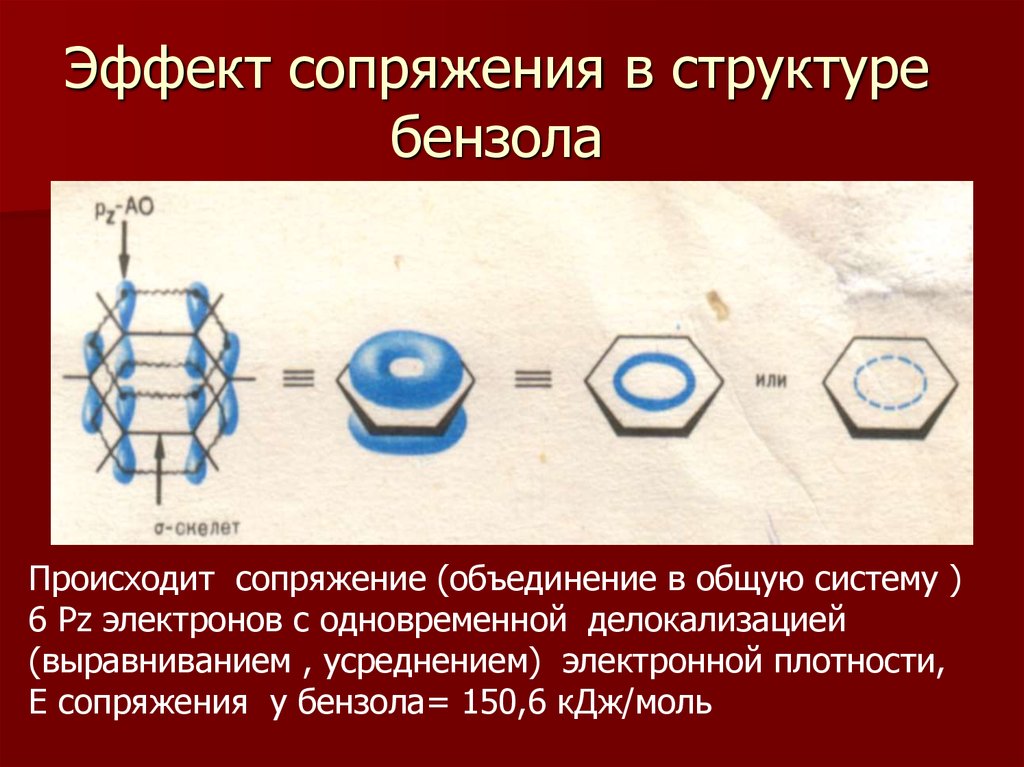
6. Эффект сопряжения в структуре бензола
Происходит сопряжение (объединение в общую систему )6 Pz электронов с одновременной делокализацией
(выравниванием , усреднением) электронной плотности,
Е сопряжения у бензола= 150,6 кДж/моль
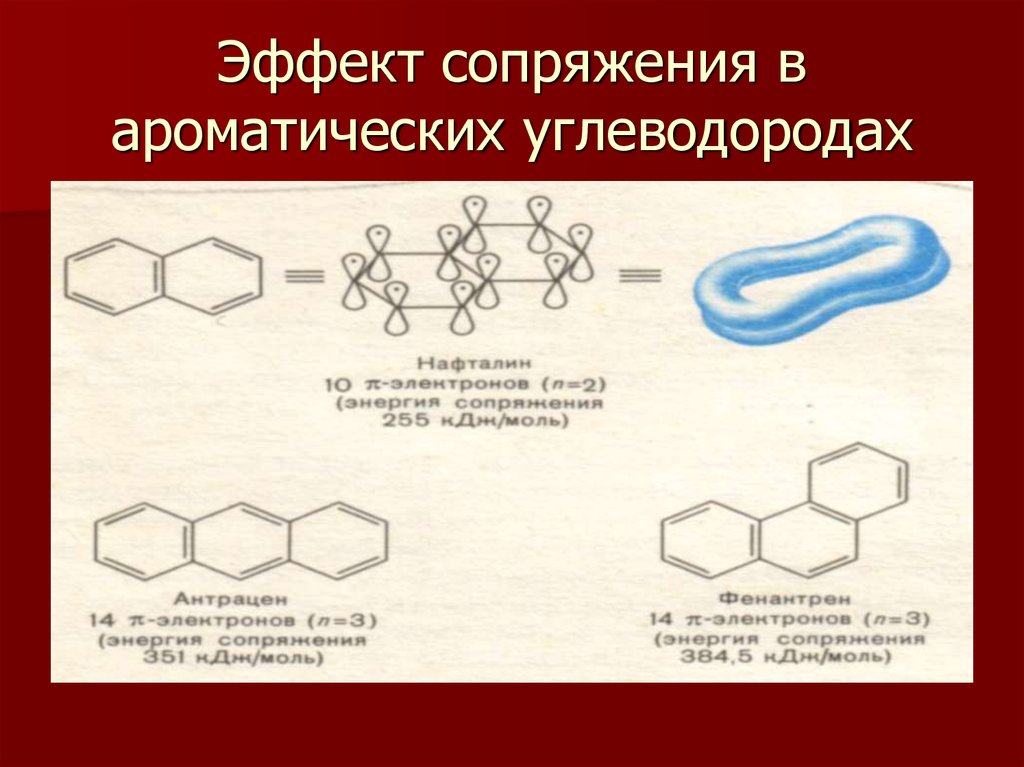
7. Эффект сопряжения в ароматических углеводородах
8. Признаки ароматичности
1. SP2 - гибридизация углеродных
атомов;
2. Плоская структура молекулы;
3. Наличие системы сопряжения и
делокализации Р z -электронов с числом,
равным (4 n + 2) (Правило Хюккеля)
(6, 10, 14-электронов);
4. Склонность к реакциям электрофильного
замещения SE (c положительно заряженными
частицами);
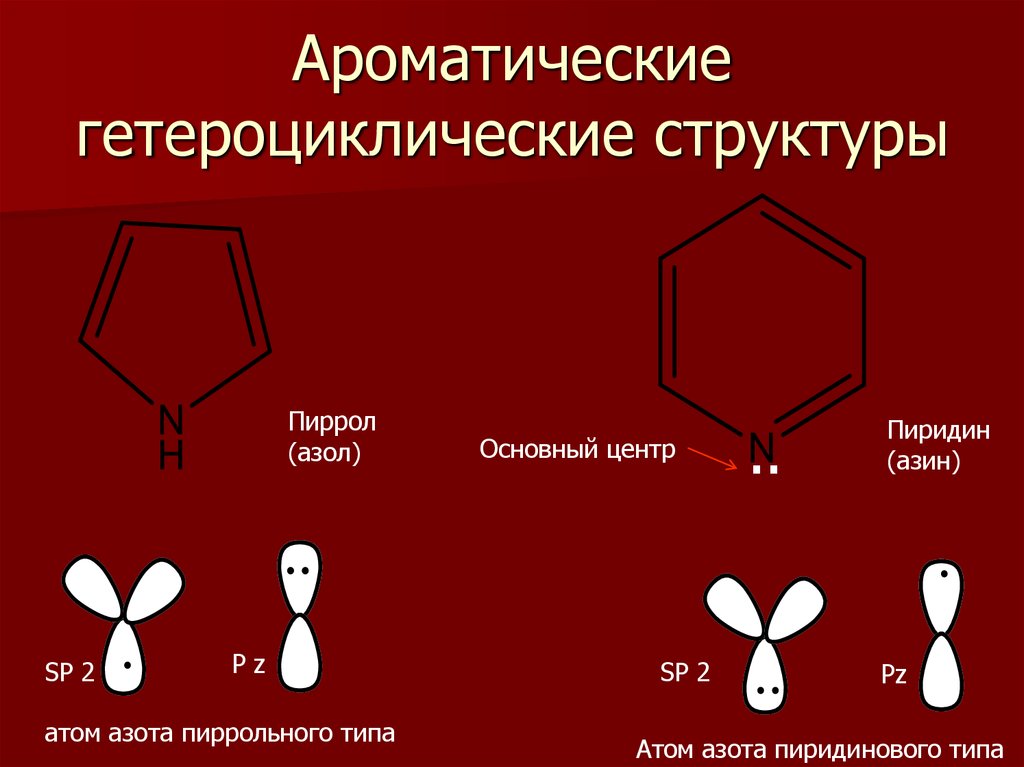
9. Ароматические гетероциклические структуры
Пиррол(азол)
SP 2
Pz
атом азота пиррольного типа
Основный центр
SP 2
..
Пиридин
(азин)
Pz
Атом азота пиридинового типа
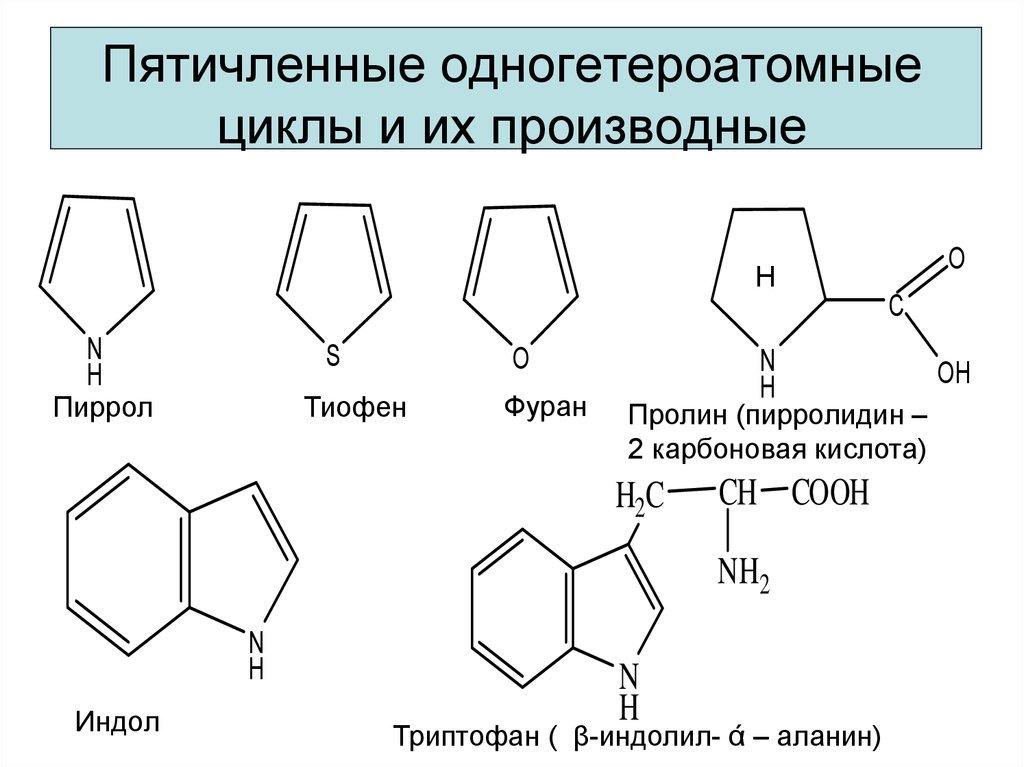
10. Пятичленные одногетероатомные циклы и их производные
OН
C
N
H
S
Пиррол
O
Тиофен
Фуран
N
H
Пролин (пирролидин –
2 карбоновая кислота)
H2C
CH COOH
NH2
N
H
Индол
N
H
Триптофан ( β-индолил- ά – аланин)
OH
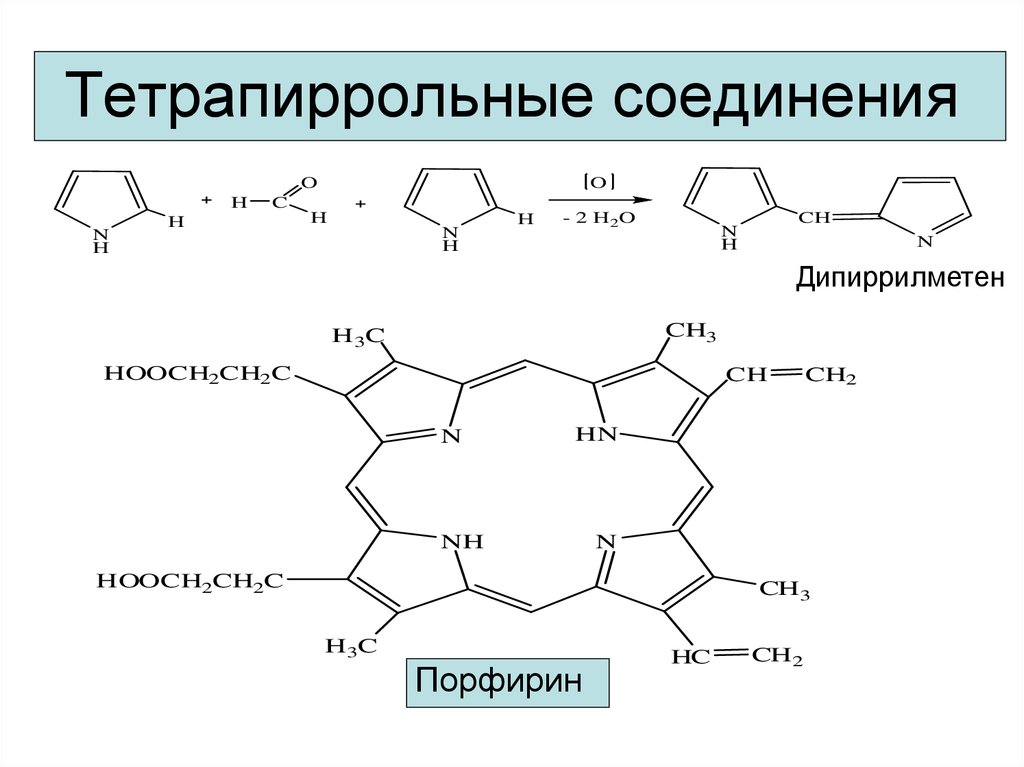
11. Тетрапиррольные соединения
OH
N
H
O
C
H
H
N
H
H
- 2 H 2O
CH
N
H
N
Дипиррилметен
CH3
H 3C
HOOCH2CH2C
CH
N
CH2
HN
NH
N
HOOCH2CH2C
CH 3
H 3C
Порфирин
HC
CH 2
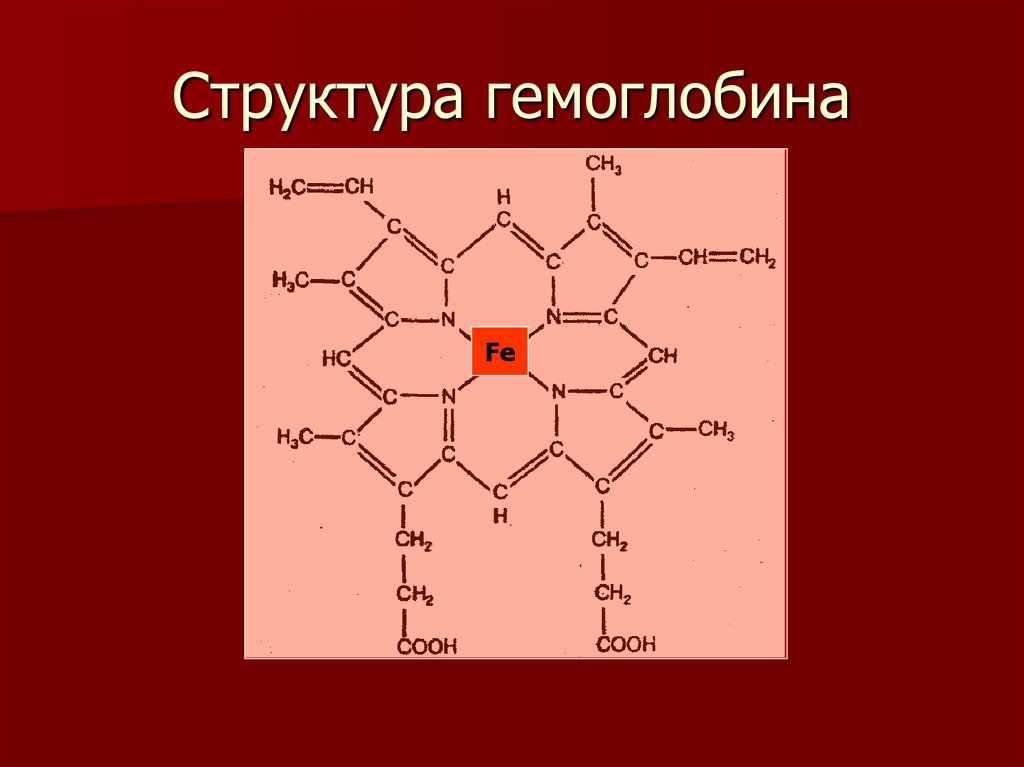
12. Структура гемоглобина
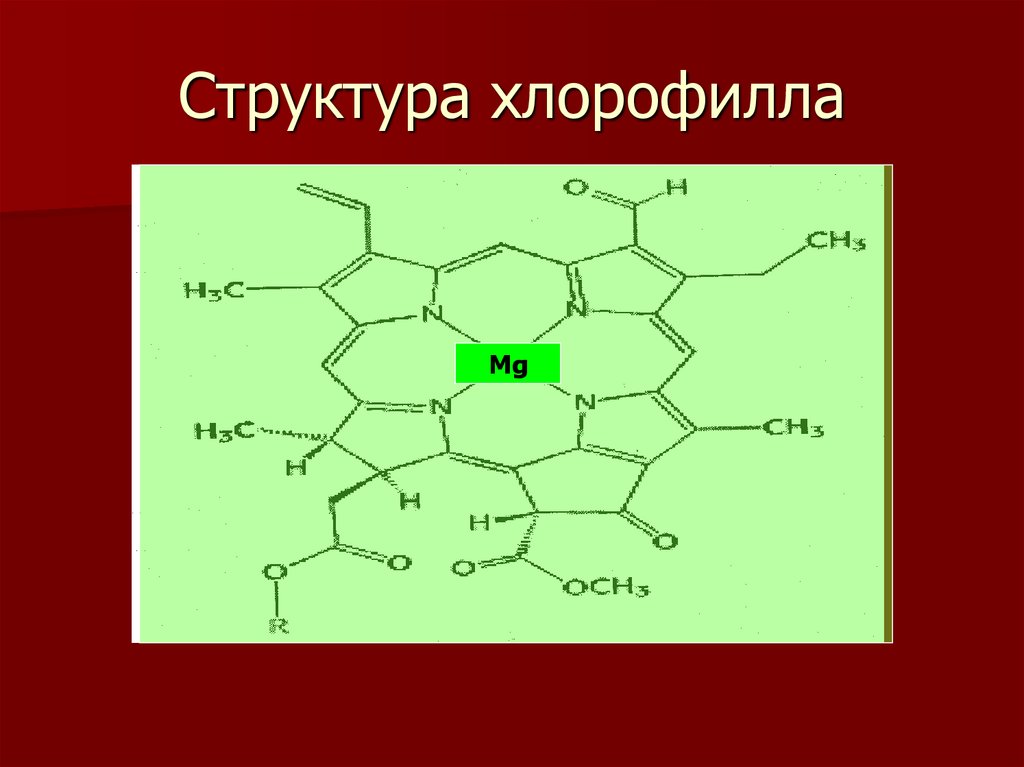
Fe13. Структура хлорофилла
Mg14.
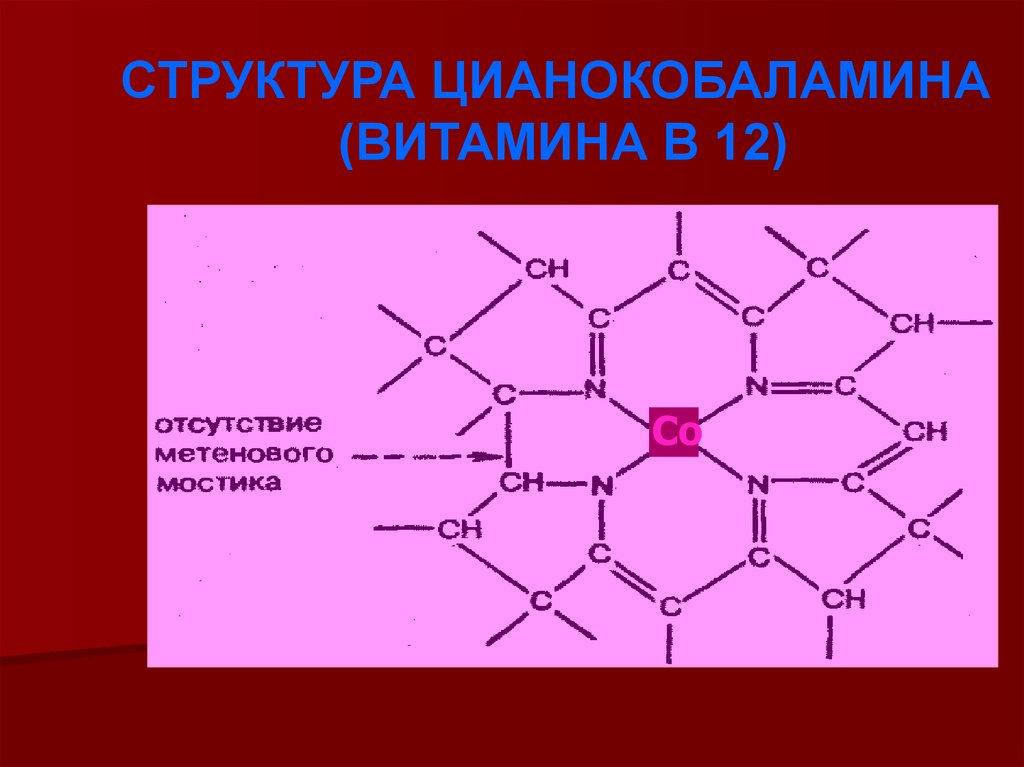
СТРУКТУРА ЦИАНОКОБАЛАМИНА(ВИТАМИНА В 12)
Со
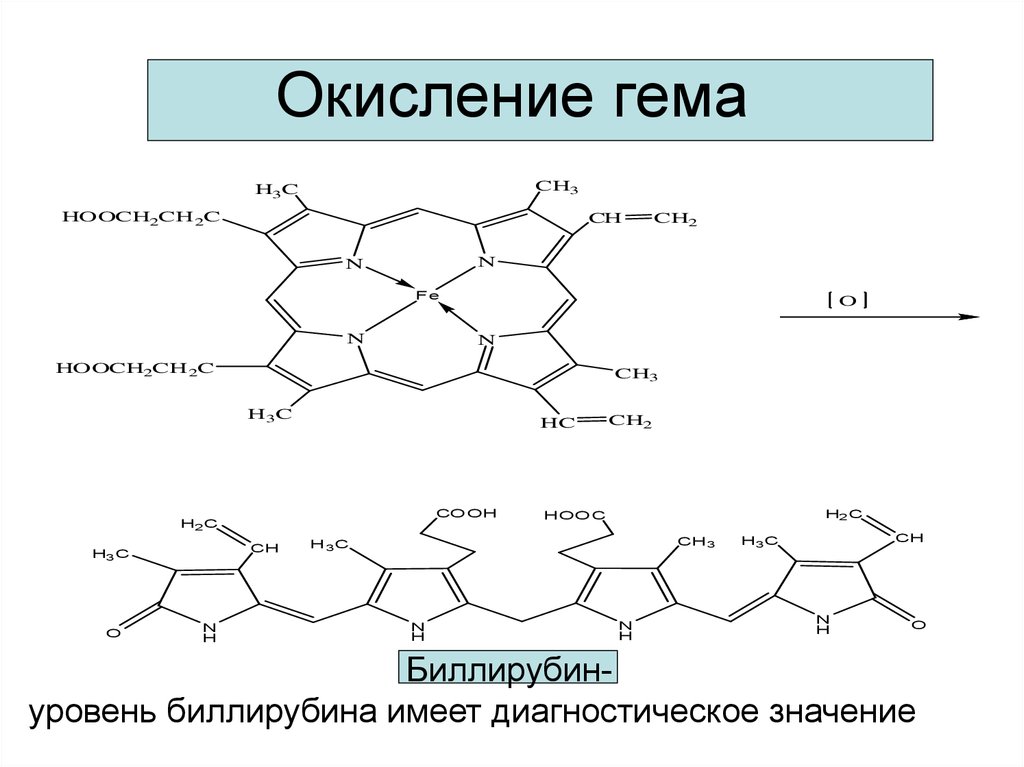
15. Окисление гема
CH3H3C
HOOCH2CH 2C
CH
CH2
N
N
Fe
N
O
N
HOOCH2CH 2C
CH3
H 3C
HC
CO OH
H2 C
CH
H3 C
O
N
H
CH2
H2 C
HOO C
CH 3
H 3C
N
H
N
H
CH
H3 C
N
H
O
Биллирубинуровень биллирубина имеет диагностическое значение
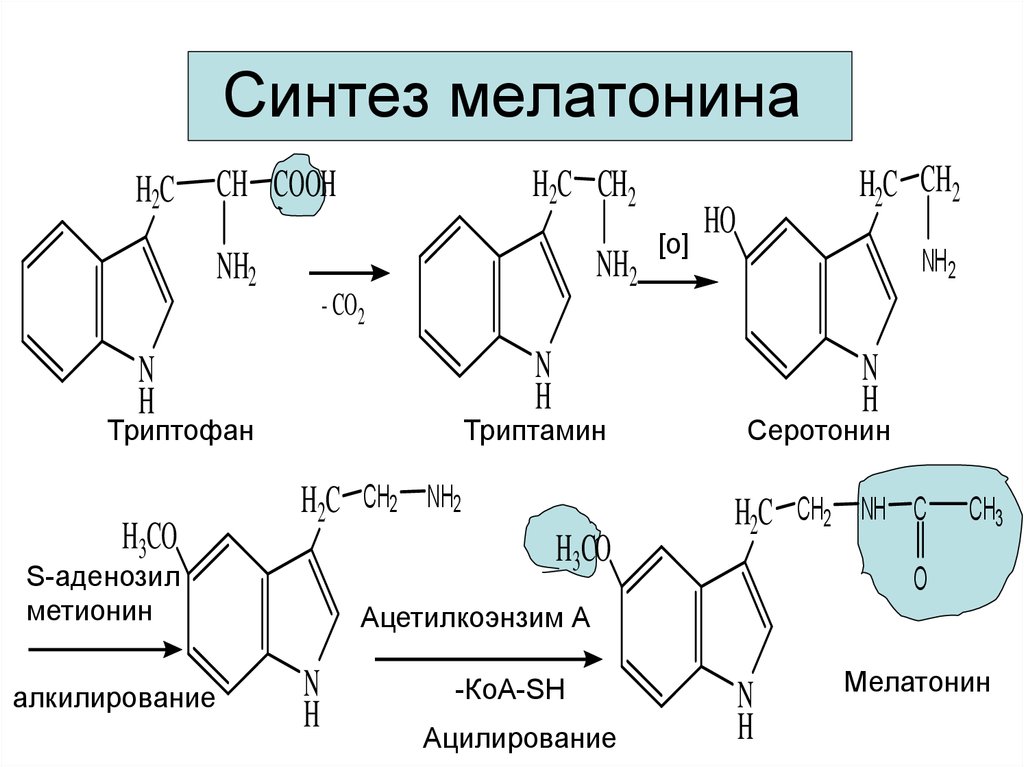
16. Синтез мелатонина
H2CCH COOH
H2C CH2
NH2
NH2
[o]
H2C CH2
HO
NH2
- CO2
N
H
N
H
Триптофан
H3CO
Триптамин
H2C CH2 NH2
H3CO
S-аденозил
метионин
алкилирование
N
H
Серотонин
H2C CH2 NH C
CH3
O
Ацетилкоэнзим А
N
H
-КоА-SH
Ацилирование
N
H
Мелатонин
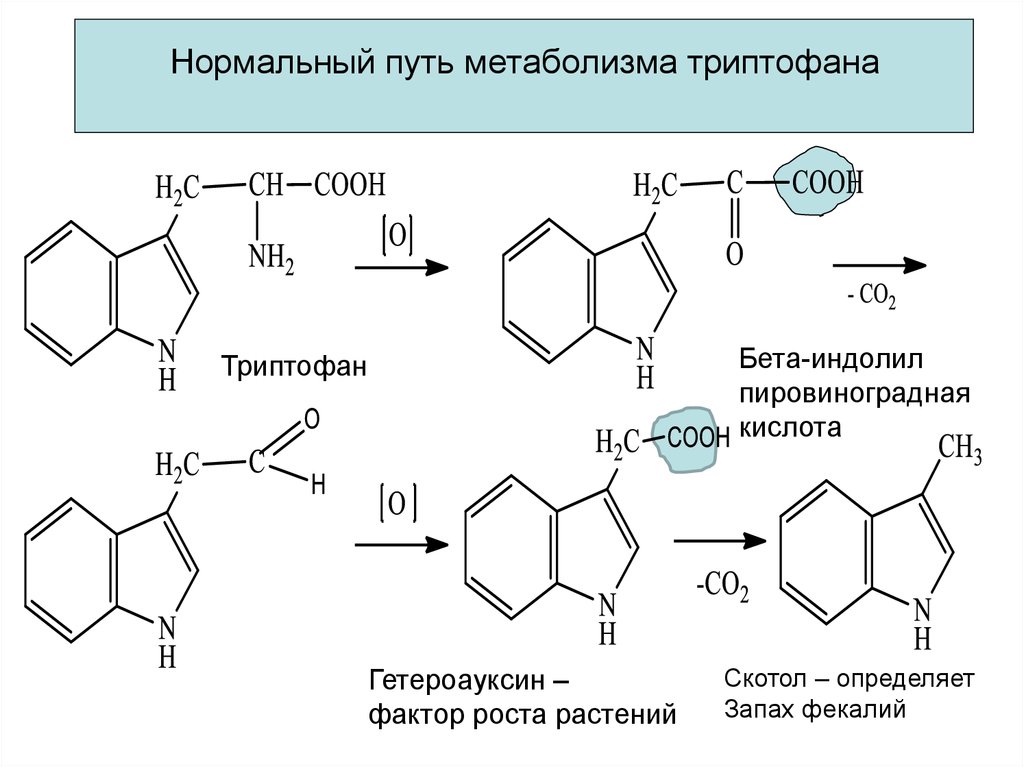
17. Нормальный путь метаболизма триптофана
Бета-индолилпировиноградная
кислота
Триптофан
Гетероауксин –
фактор роста растений
Скотол – определяет
Запах фекалий
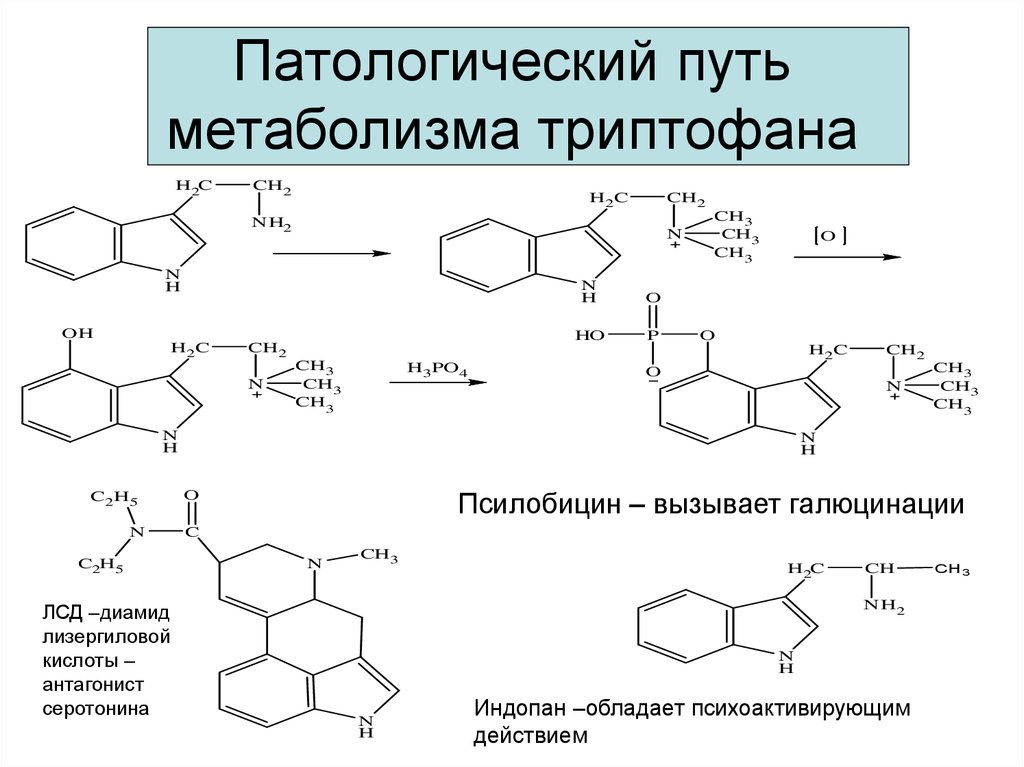
18. Патологический путь метаболизма триптофана
H2CCH2
H 2C
CH2
N H2
N
N
H
OH
H 2C
CH2
N
N
H
O
HO
P
CH3
CH3
CH3
O
O
H2C
CH3
CH3
CH3
H3PO4
O
N
N
H
C2H5
N
C2H5
ЛСД –диамид
лизергиловой
кислоты –
антагонист
серотонина
CH2
CH3
CH3
CH3
N
H
Псилобицин – вызывает галюцинации
O
C
N
CH3
H2C
CH
N H2
N
H
N
H
Индопан –обладает психоактивирующим
действием
CH 3
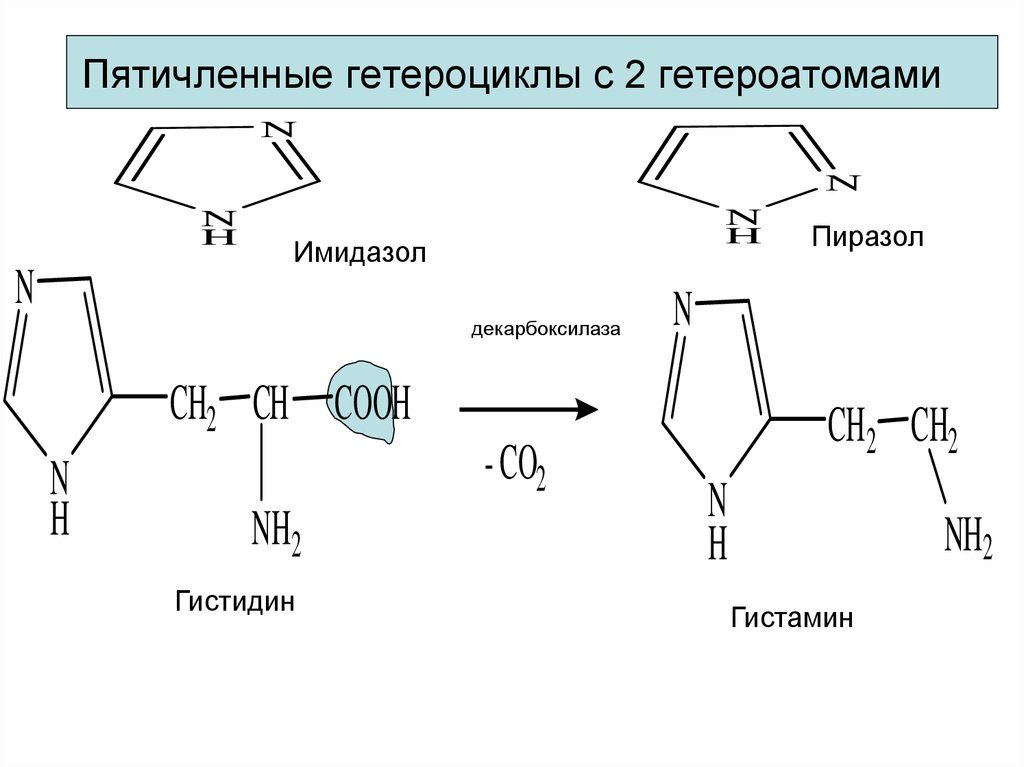
19. Пятичленные гетероциклы с 2 гетероатомами
NN
N
H
N
H
Имидазол
N
декарбоксилаза
N
CH2 CH COOH
N
H
- CO2
NH2
Гистидин
Пиразол
CH2 CH2
N
H
NH2
Гистамин
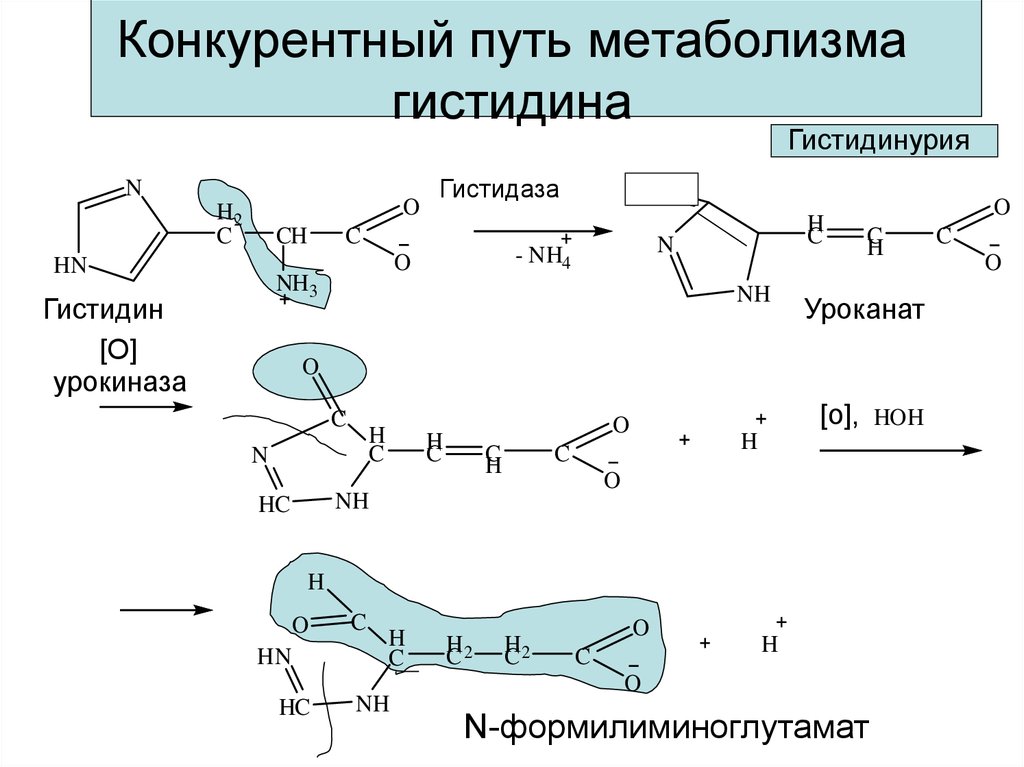
20. Конкурентный путь метаболизма гистидина
ГистидинурияN
O
H2
C
CH
HN
C
O
H
C
N
- NH4
O
NH3
Гистидин
[O]
урокиназа
Гистидаза
NH
O
C
H
Уроканат
O
C
H
C
N
H
C
C
H
H
C
O
NH
HC
[o], HOH
O
H
O
HN
HC
C
H
C
NH
H2
C
H2
C
O
C
H
O
N-формилиминоглутамат
C
O
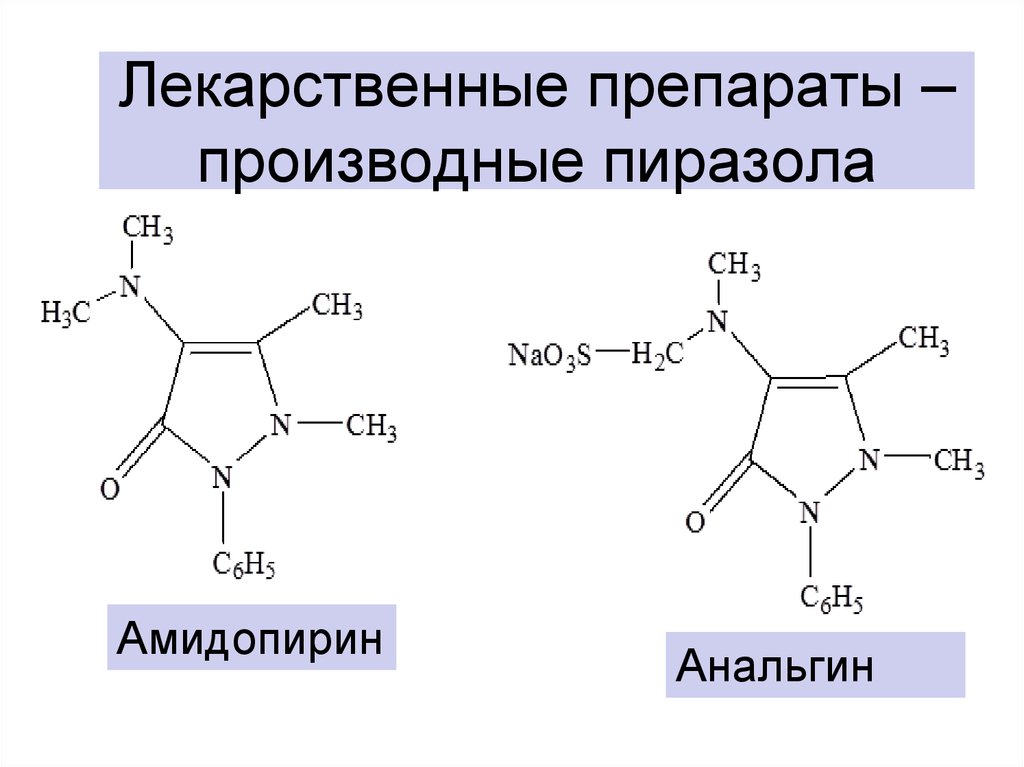
21. Лекарственные препараты – производные пиразола
АмидопиринАнальгин
22. Фуран и его производные
OC
фуран
O
CH
H
C
HC
O
OH
O
CH
- 3 H 2O
CHO
OH
NH 2
фурфурол
R
CH
C
-н2О
H
O
H 2N
HNO3
H
HO
O
Фурфурол
C
O
O2 N
H
тиофен
Синтез фурациллина
HO
H
S
O2 N
N
R
O
семикарбазон
HN
O
C
-Н2О
NH 2
O
CH
O2 N
O
N
NH
фурациллин
C
NH 2
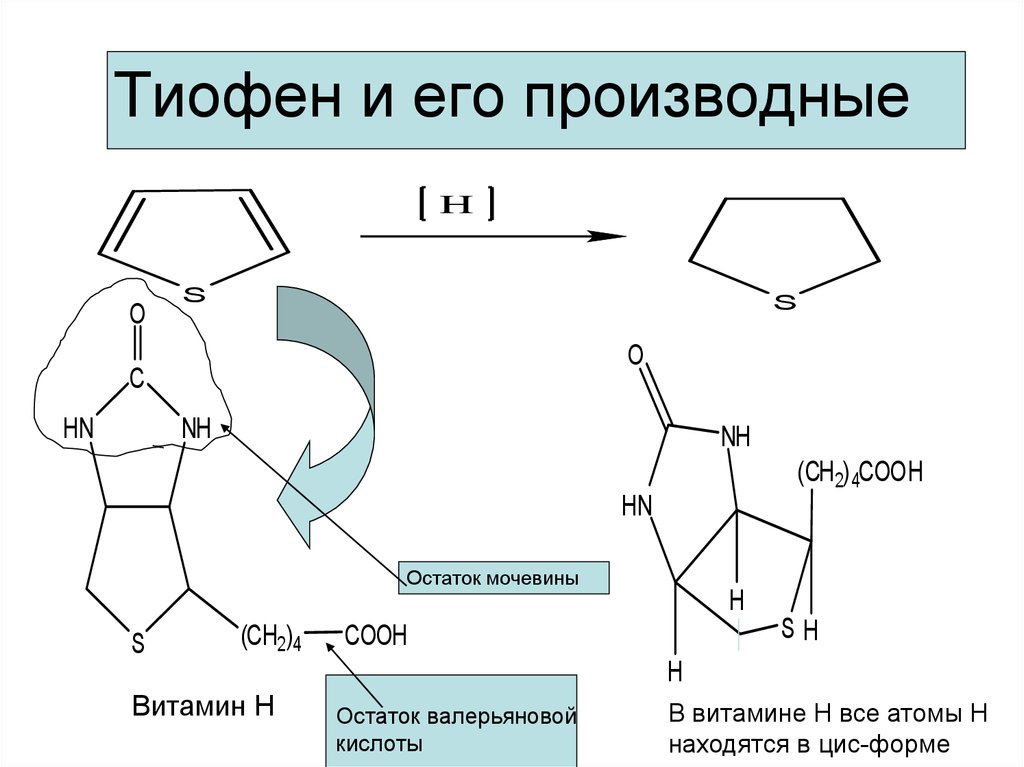
23. Тиофен и его производные
HO
S
S
O
C
HN
NH
NH
(CH 2) 4COOH
HN
Остаток мочевины
H
S
(CH2)4
SH
COOH
H
Витамин Н
Остаток валерьяновой
кислоты
В витамине Н все атомы Н
находятся в цис-форме
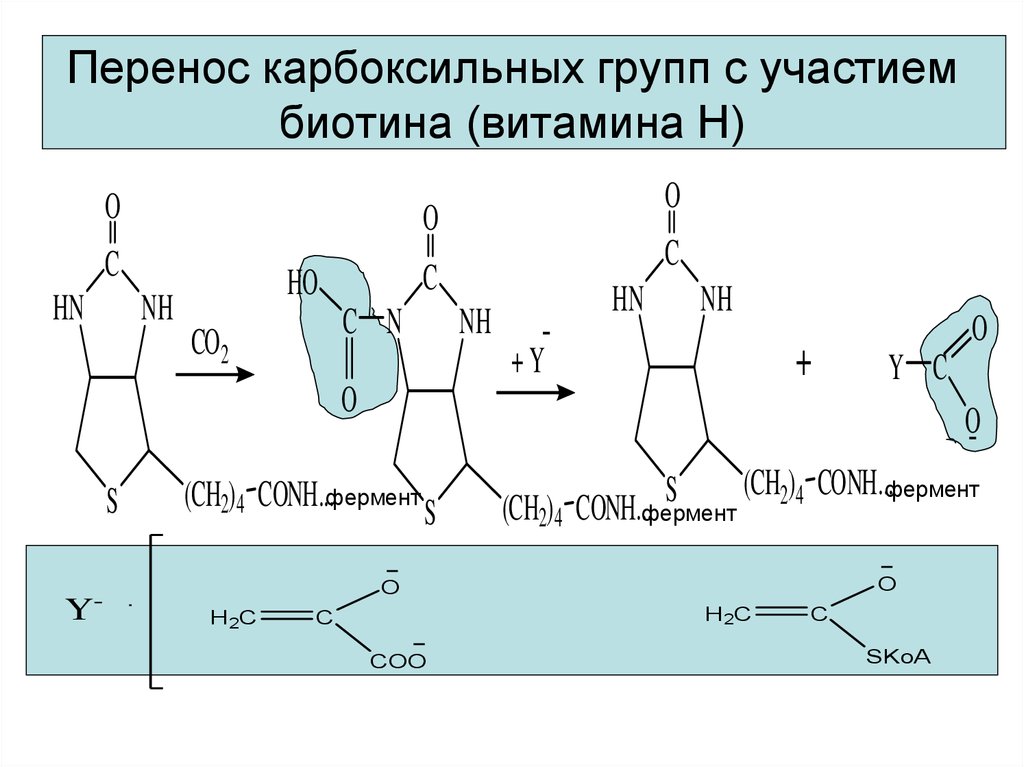
24. Перенос карбоксильных групп с участием биотина (витамина Н)
OO
C
HN
O
C
HO
NH
C N
CO2
C
HN
NH
NH
+
+Y
O
S
Y-
Y C
O
(CH2)4 CONH...фермент
S
S
(CH2)4 CONH...фермент
(CH2)4 CONH...фермент
O
O
H 2C
O
H 2C
C
COO
C
SKoA
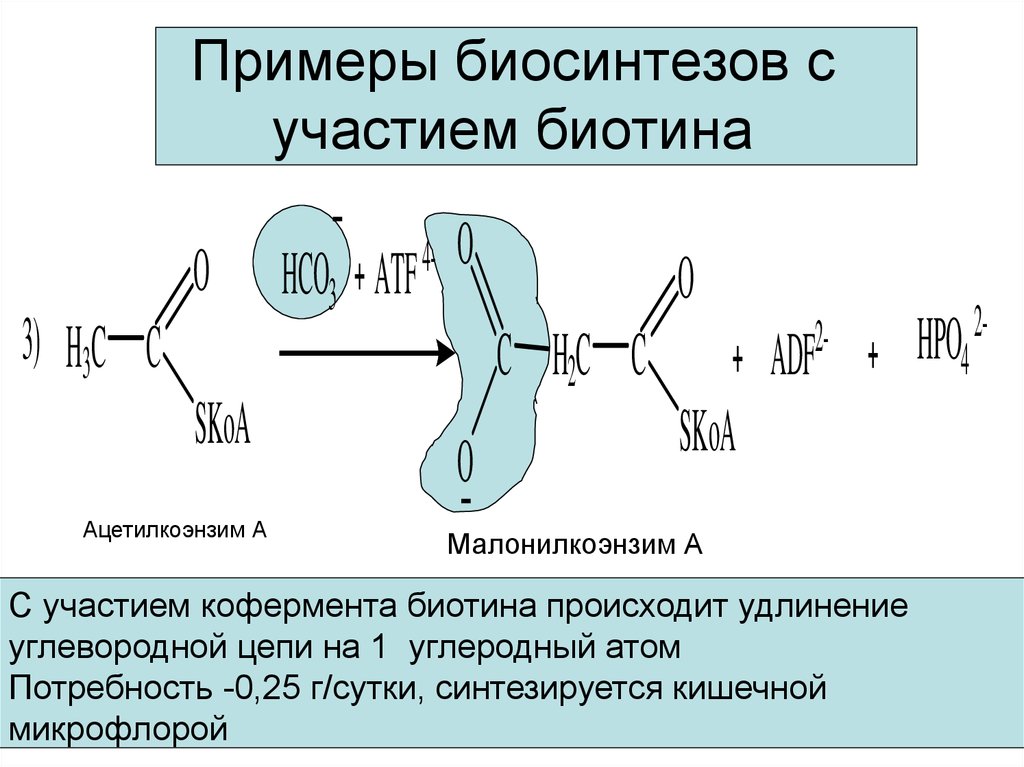
25. Примеры биосинтезов с участием биотина
O3) H3C C
O
HCO3 ATF
4-
O
2ADF
C H2C C
SKoA
Ацетилкоэнзим А
O
SKoA
Малонилкоэнзим А
С участием кофермента биотина происходит удлинение
углевородной цепи на 1 углеродный атом
Потребность -0,25 г/сутки, синтезируется кишечной
микрофлорой
2HPO4
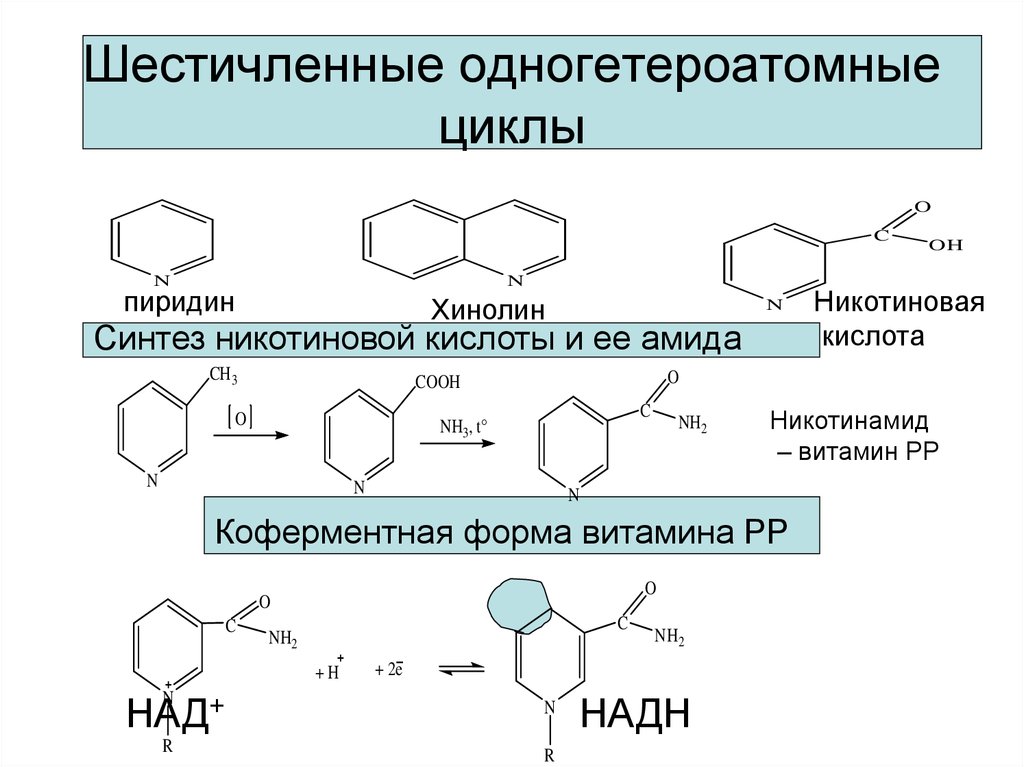
26. Шестичленные одногетероатомные циклы
OC
N
N
пиридин
Хинолин
N
Синтез никотиновой кислоты и ее амида
CH3
C
NH3, t°
N
N
NH2
Никотинамид
– витамин РР
N
Коферментная форма витамина РР
O
O
C
C
NH2
+H
N
НАД+
R
Никотиновая
кислота
O
COOH
O
OH
NH2
+ 2e
N
R
НАДН
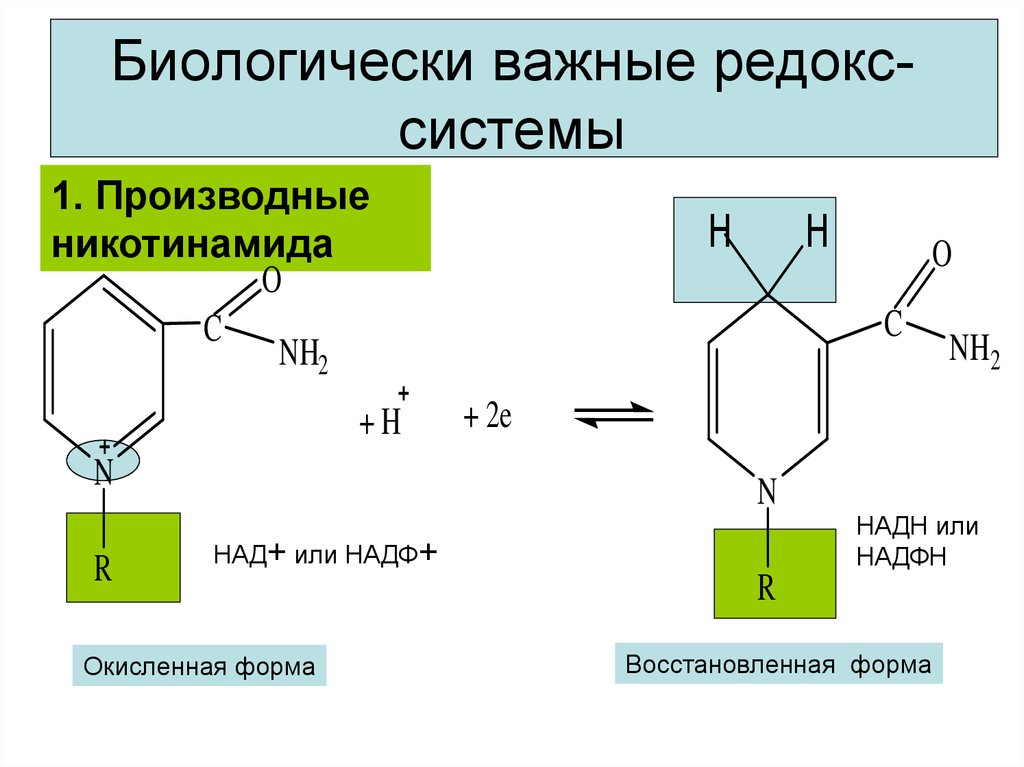
27. Биологически важные редокс-системы
Биологически важные редокссистемы1. Производные
никотинамида
O
C
NH2
+H
N
R
H
H
C
NH2
+ 2e
N
НАД+ или НАДФ+
Окисленная форма
O
НАДН или
НАДФН
R
Восстановленная форма
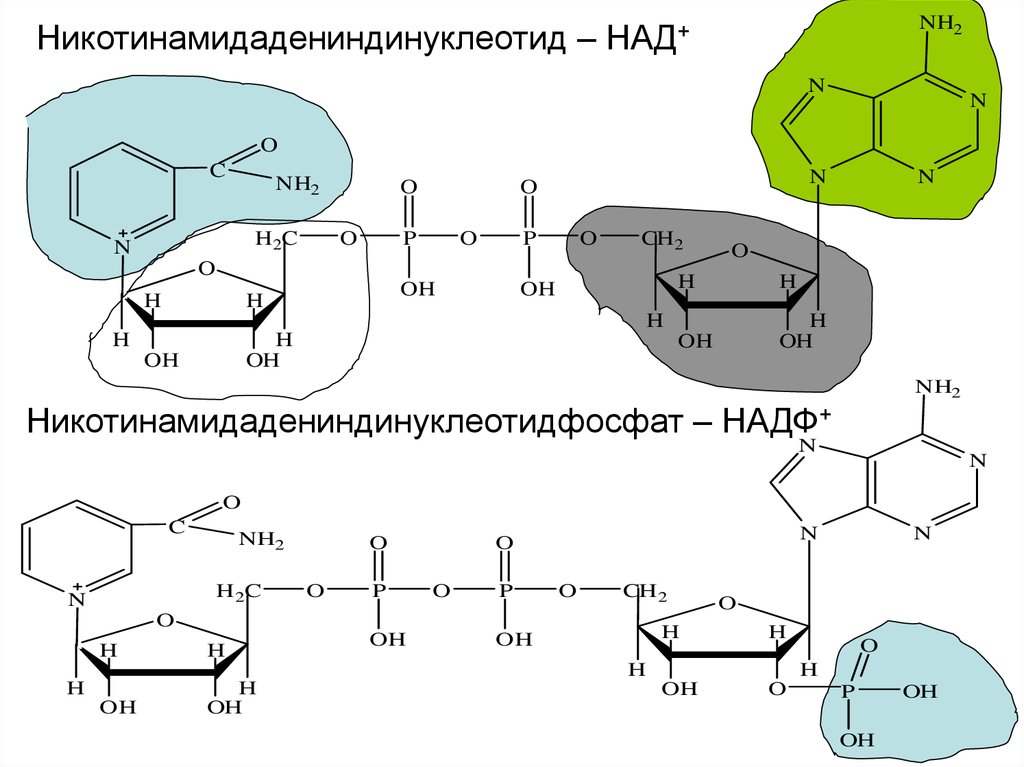
28.
Никотинамидадениндинуклеотид –NH2
НАД+
N
N
O
C
NH2
H 2C
N
O
O
N
O
P
O
P
O
CH 2
O
H
H
OH
H
OH
OH
OH
O
H
H
OH
H
OH
H
H
N
NH2
Никотинамидадениндинуклеотидфосфат – НАДФ+
N
N
O
C
NH2
H 2C
N
O
O
P
N
O
O
P
O
CH 2
O
H
H
OH
H
OH
OH
H
OH
O
H
H
H
N
O
H
OH
O
P
OH
OH
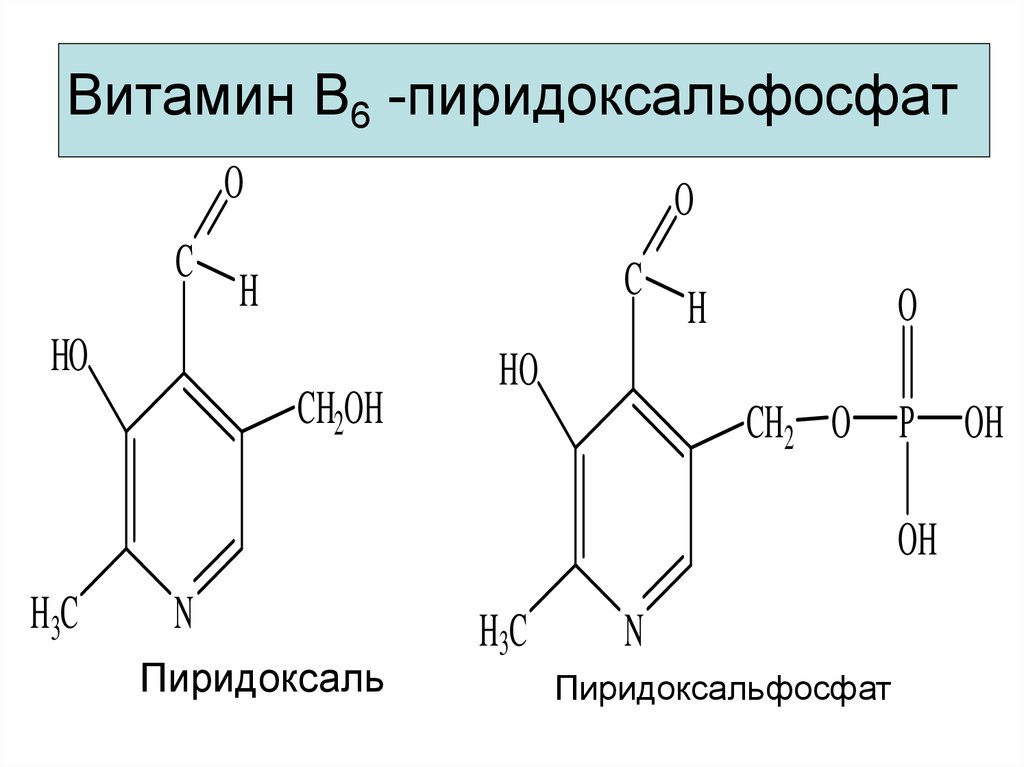
29. Витамин В6 -пиридоксальфосфат
OC
O
C
H
HO
CH2OH
O
H
HO
CH2 O
P
OH
H3C
N
Пиридоксаль
H3C
N
Пиридоксальфосфат
OH
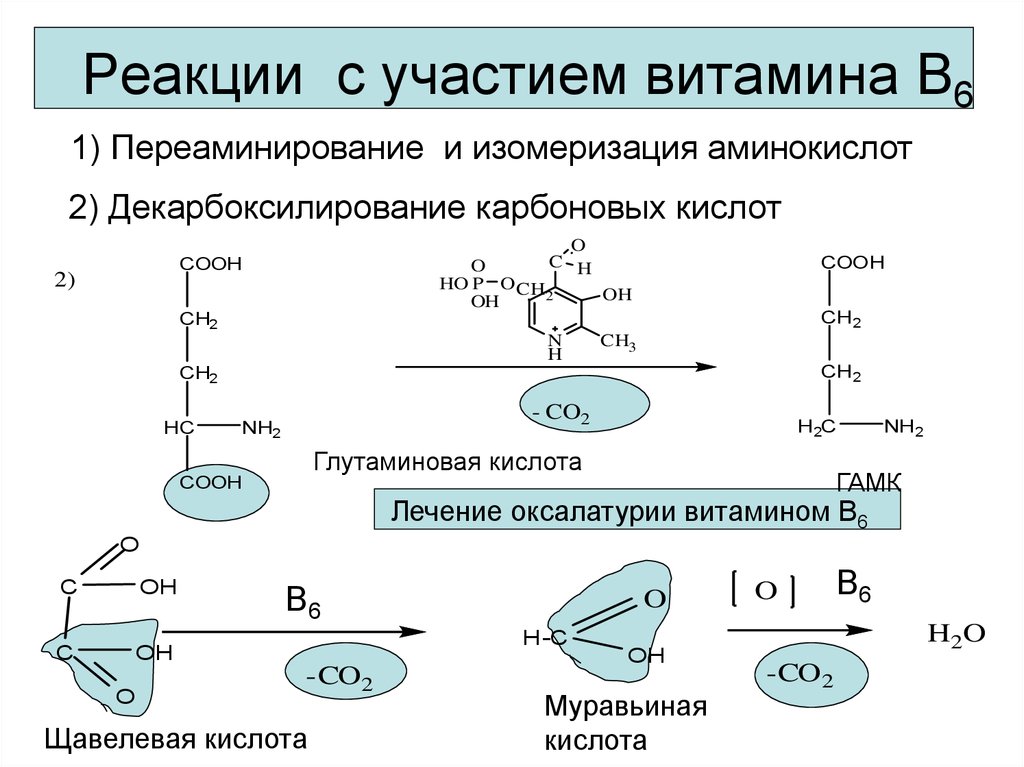
30. Реакции с участием витамина В6
1) Переаминирование и изомеризация аминокислот2) Декарбоксилирование карбоновых кислот
O
C H
O
HO P O CH
2
OH
OH
COOH
2)
COOH
CH 2
CH2
N
H
CH3
CH 2
CH2
HC
- CO2
NH2
H 2C
Глутаминовая кислота
COOH
NH 2
ГАМК
Лечение оксалатурии витамином В6
O
C
OH
C
OH
O
В6
O
H-C
-CO2
Щавелевая кислота
OH
Муравьиная
кислота
O
В6
H 2O
-CO2
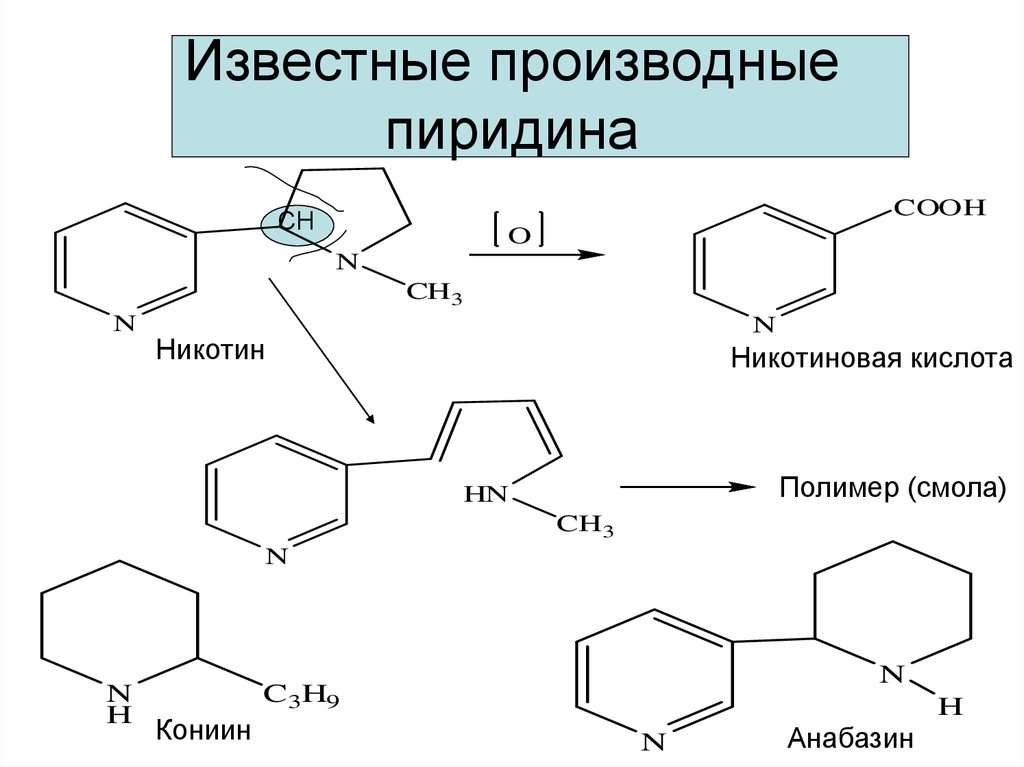
31. Известные производные пиридина
COOHСН
O
N
CH 3
N
N
Никотин
Никотиновая кислота
Полимер (смола)
HN
CH 3
N
N
H
N
C3H9
Кониин
H
N
Анабазин
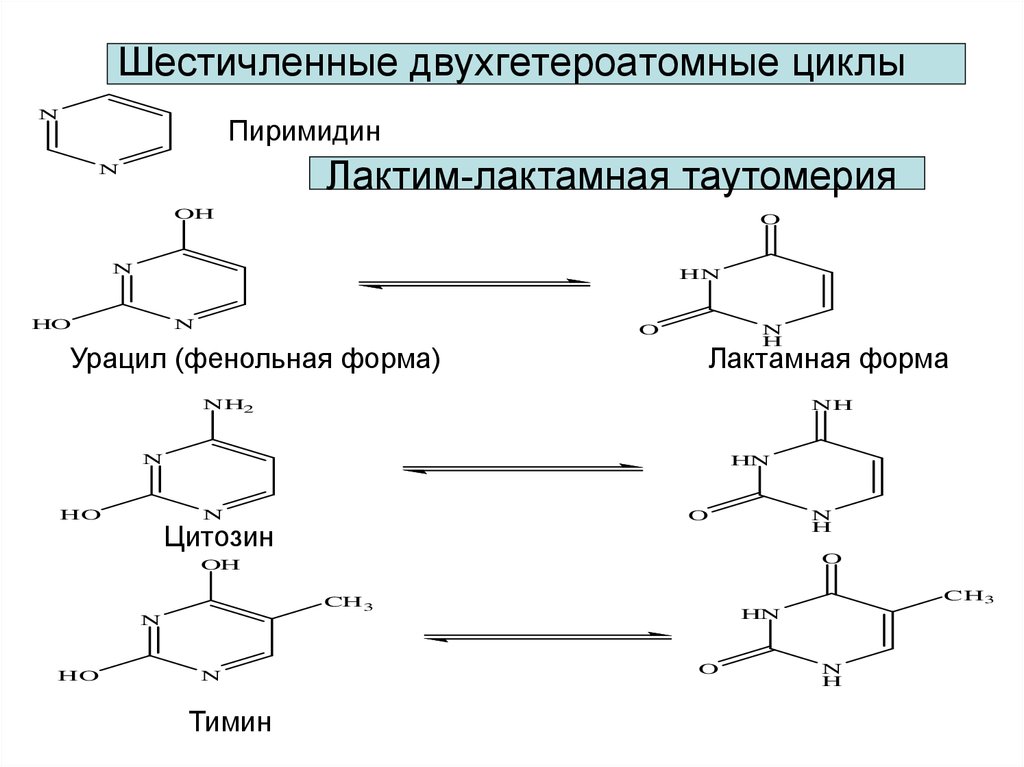
32. Шестичленные двухгетероатомные циклы
NПиримидин
Лактим-лактамная таутомерия
N
OH
O
N
HN
HO
N
O
Урацил (фенольная форма)
N
H
Лактамная форма
NH2
NH
N
HO
HN
N
O
Цитозин
N
H
O
OH
CH 3
CH 3
HN
N
HO
N
Тимин
O
N
H
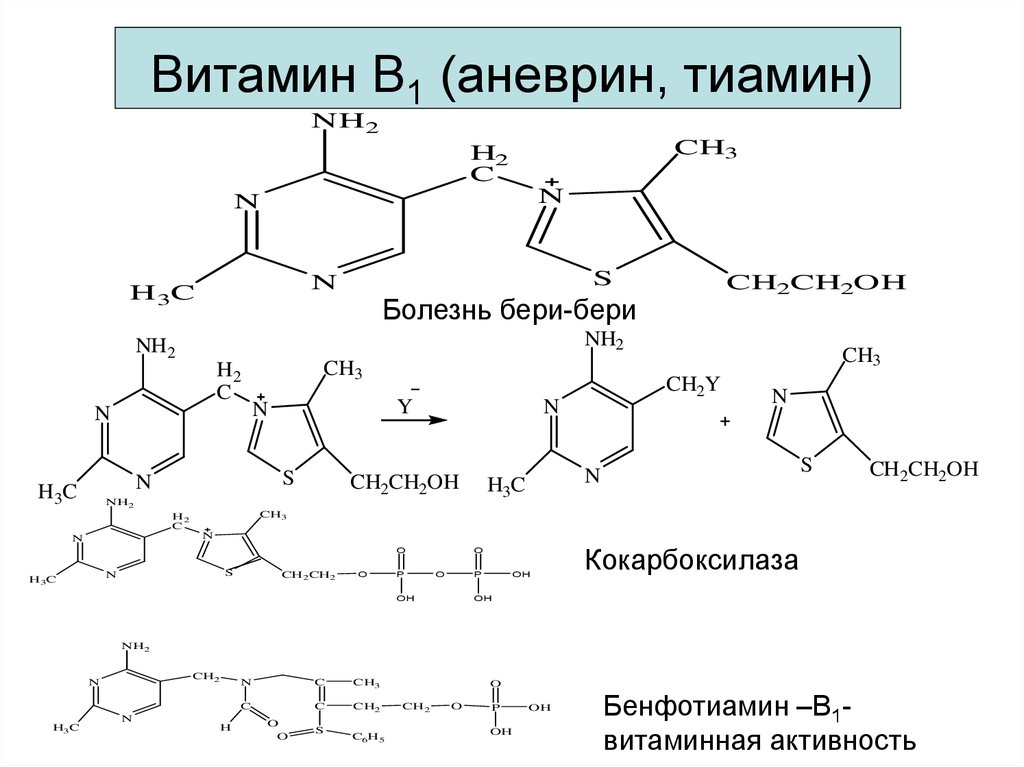
33. Витамин В1 (аневрин, тиамин)
NH 2CH3
H2
C
N
N
CH2CH2OH
Болезнь бери-бери
NH2
NH2
H2
C
N
CH3
Y
N
S
N
H3C
S
N
H 3C
CH2Y
N
CH2CH2OH
N
S
N
H3C
NH2
CH3
CH2CH2OH
CH3
H2
C
N
N
O
S
N
H 3C
CH 2CH 2
O
P
O
O
P
OH
OH
Кокарбоксилаза
OH
NH 2
CH2
N
N
C
N
H3C
H
O
O
C
CH3
C
CH2
S
C6H 5
O
CH 2
O
P
OH
OH
Бенфотиамин –В1витаминная активность
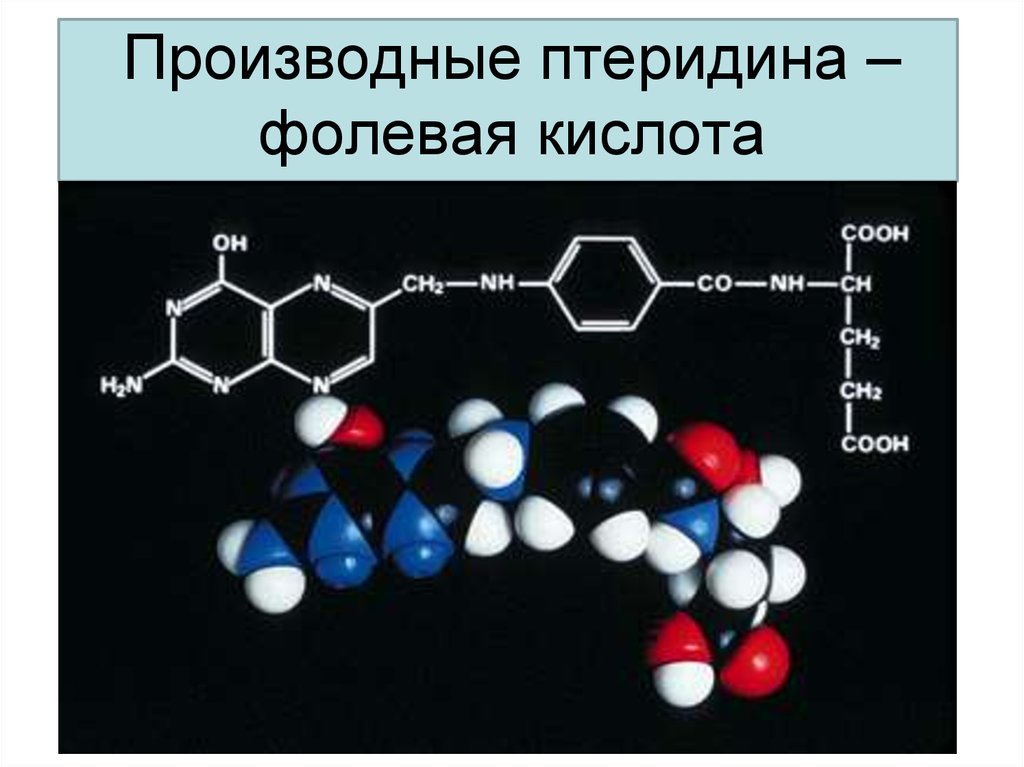
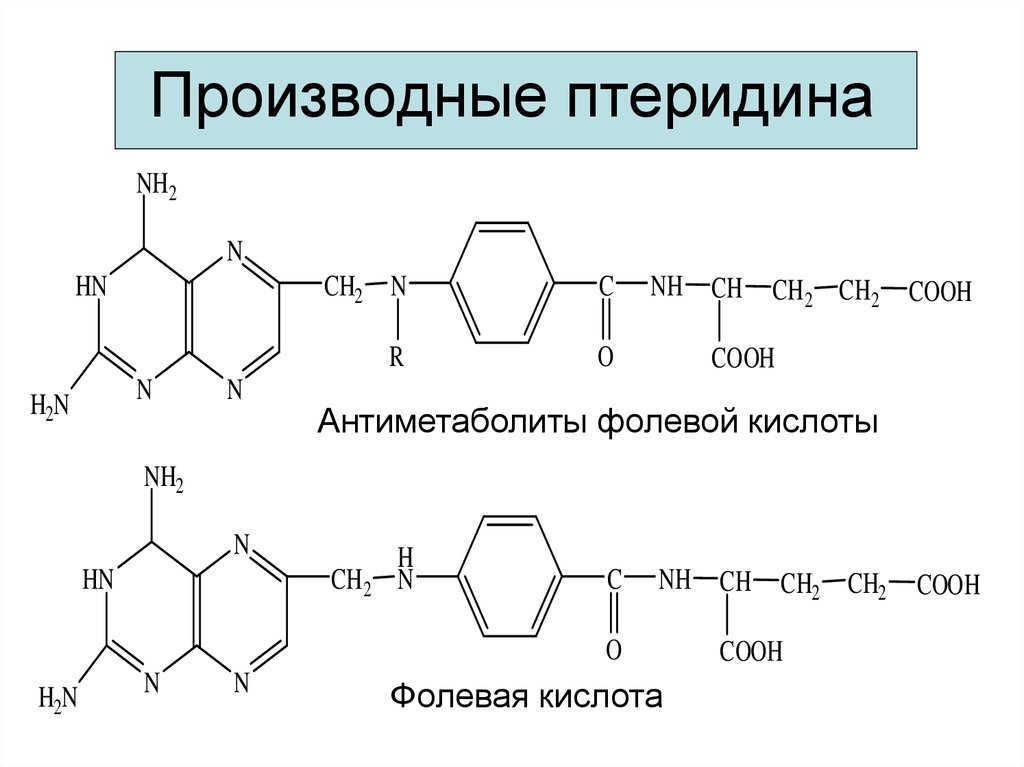
34. Производные птеридина –фолевая кислота
Производные птеридина –фолевая кислота
35. Производные птеридина
NH2N
HN
N
H2N
N
CH2 N
C
R
O
NH CH
CH2 CH2 COOH
COOH
Антиметаболиты фолевой кислоты
NH2
N
CH2
HN
H
N
C
NH CH
O
H2N
N
N
Фолевая кислота
CH2 CH2
COOH
COOH
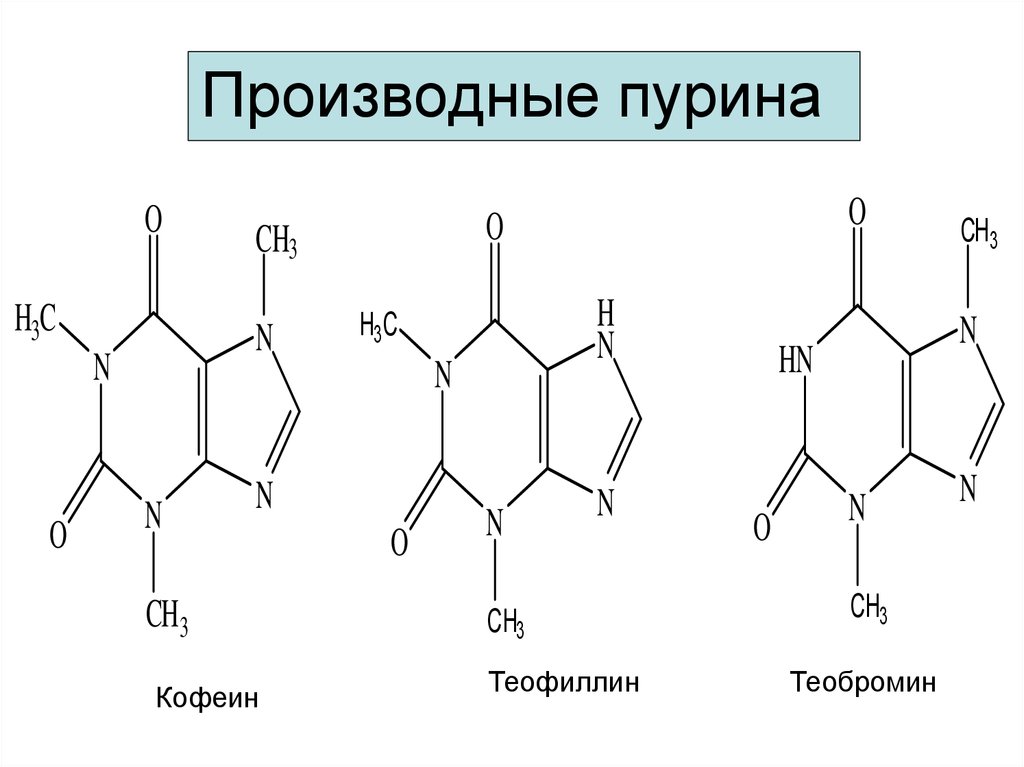
36. Производные пурина
OH3C
N
O
CH3
N
H
N
H3C
N
N
N
CH3
Кофеин
O
O
O
N
N
CH3
Теофиллин
N
HN
O
CH3
N
CH3
Теобромин
N
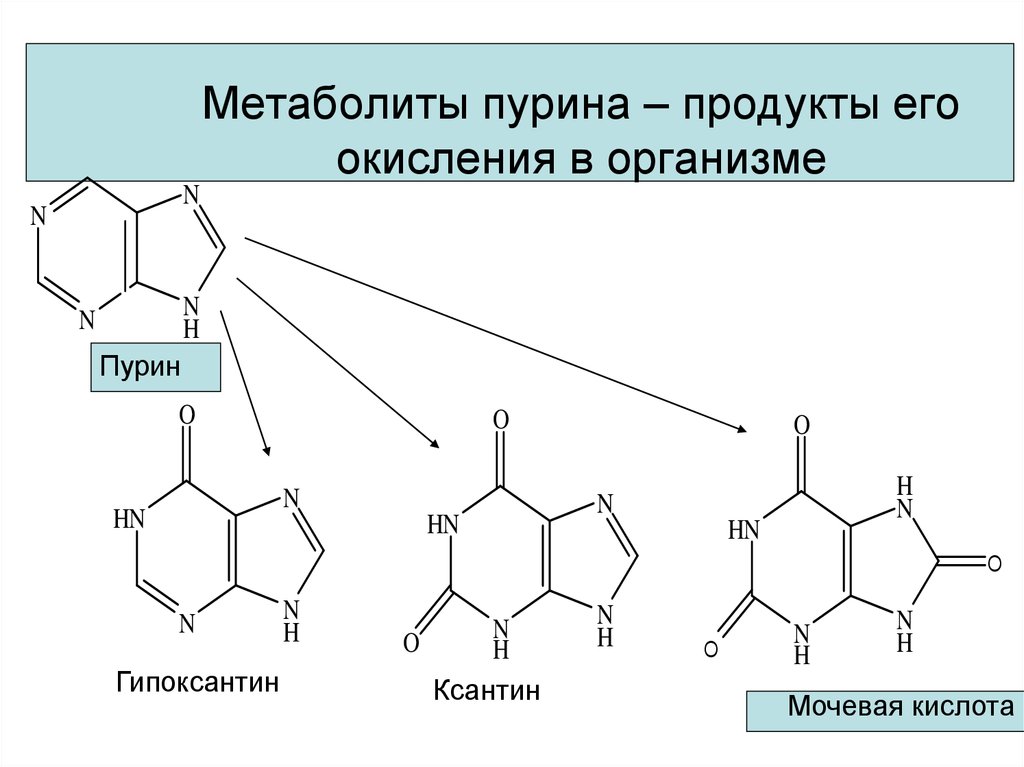
37. Метаболиты пурина – продукты его окисления в организме
NN
N
H
N
Пурин
O
O
N
HN
HN
O
H
N
N
HN
O
N
Гипоксантин
N
H
N
O
H
Ксантин
N
H
O
N
H
N
H
Мочевая кислота
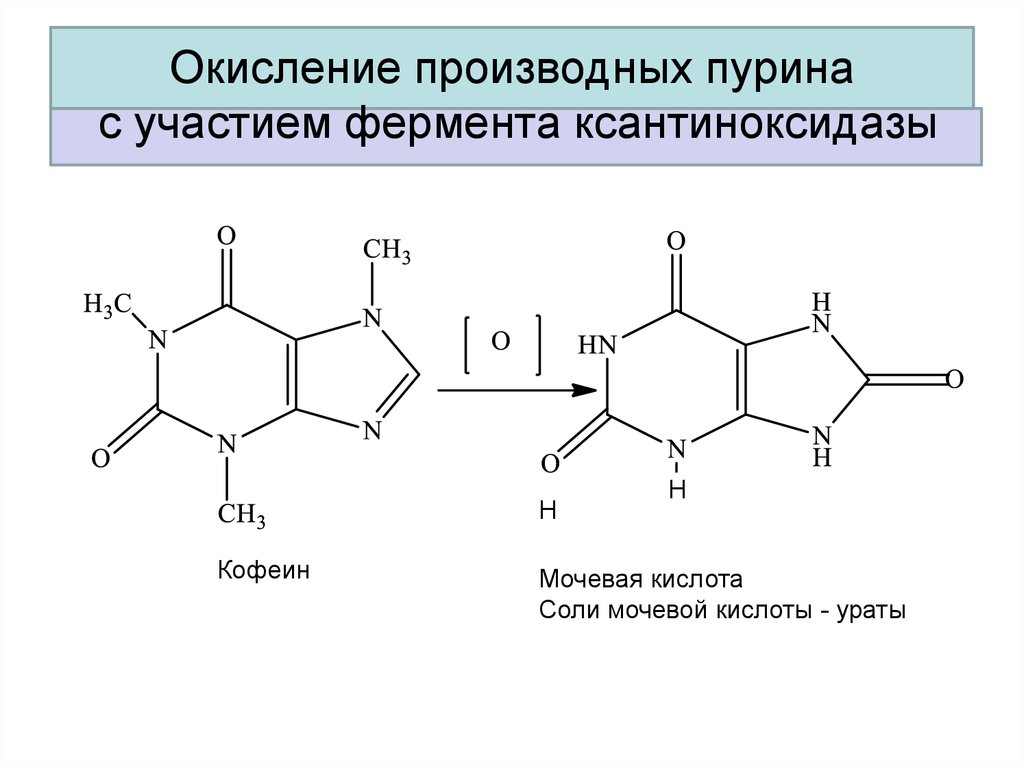
38. Окисление производных пурина с участием фермента ксантиноксидазы
НРРКофеин
Н
Мочевая кислота
Соли мочевой кислоты - ураты



 chemistry
chemistry