Similar presentations:
Растворение. Кристаллогидраты
1. Растворение Кристаллогидраты
2.
• Вода— самоераспространенное
вещество на
поверхности нашей
планеты.
• Водная оболочка
Земли —
гидросфера—
составляет 71%
земной поверхности.
водная оболочка Земли
вода
3.
4. Знаете ли вы…..
• Без воды не может в зеленом листеобразовываться сахар, крахмал, жиры,
кислоты и другие вещества;
• Вода — вечный двигатель живой и
мертвой природы, служит наилучшим
растворителем, обладает наибольшей
теплоемкостью, регулирует температуру
климатических зон и определяет
климатические пояса;
5.
• Растворители: вода, спирты, ацетон и дрРАСТВОРЫ
• .
Твердые
Жидкие
6.
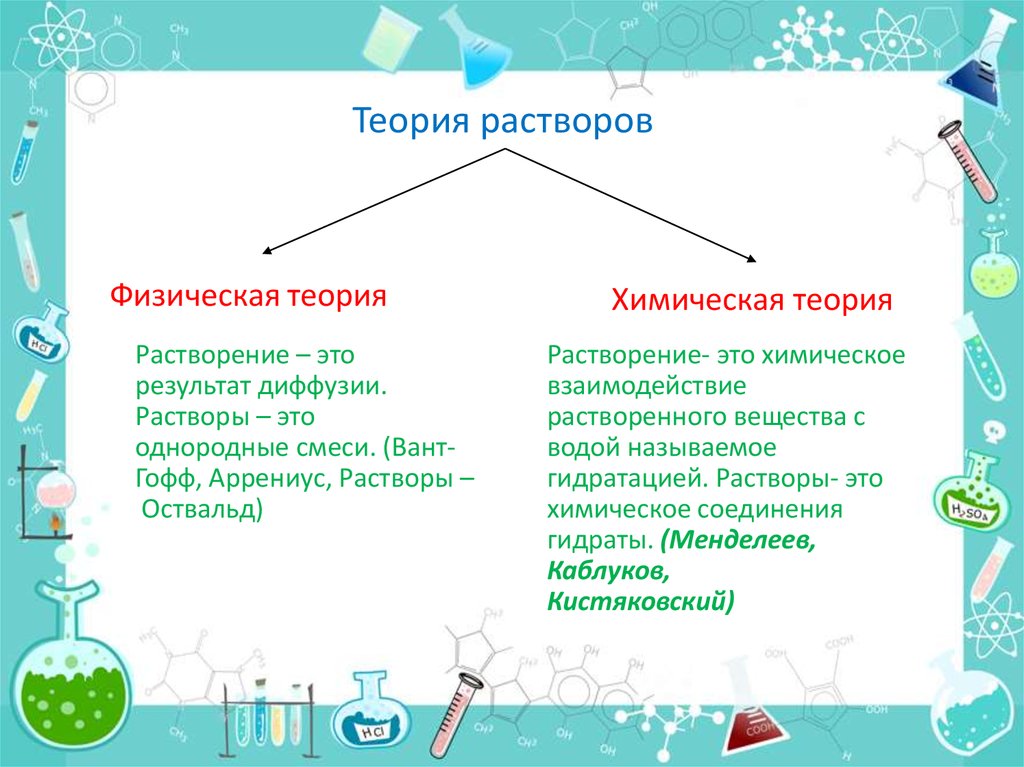
Теория растворовФизическая теория
Растворение – это
результат диффузии.
Растворы – это
однородные смеси. (ВантГофф, Аррениус, Растворы –
Оствальд)
Химическая теория
Растворение- это химическое
взаимодействие
растворенного вещества с
водой называемое
гидратацией. Растворы- это
химическое соединения
гидраты. (Менделеев,
Каблуков,
Кистяковский)
7.
Состав раствораРастворенное
вещество
Растворитель
Продукт их
взаимодействия
( гидраты)
8.
9.
10. Признаки химического взаимодействия при растворении
Тепловые явления, так же, как в случае
химических реакций наблюдаются экзо- и
эндотермические эффекты.
Выделение тепла наблюдается в случае
растворения Н2SO4, NaOH, AgNO3, ZnSO4.
Поглощение тепла наблюдается в случае
растворения NН4NO3, NaNO3, KCl, K2SO4,
KNO2, NH4Cl.
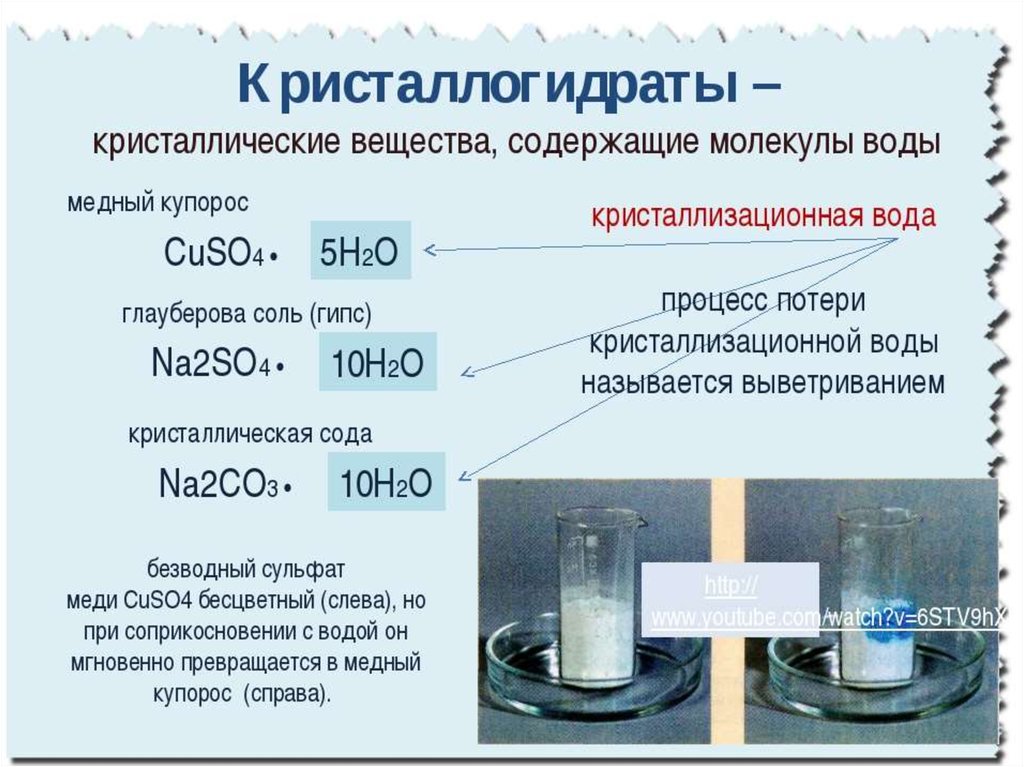
Изменение цвета: CuSO4 – белого цвета, при
растворении в воде – голубого, продукт
взаимодействия сульфата меди с водой так
же синего цвета Cu2SO4·5H2O.
11.
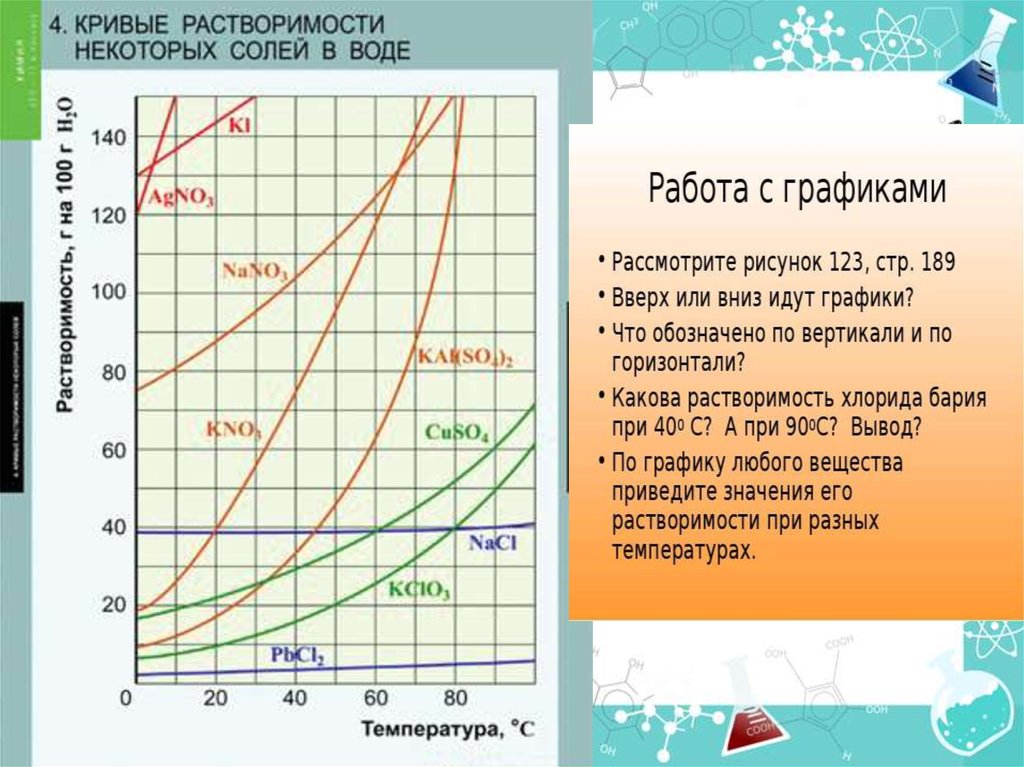
12. Факторы, влияющие на растворимость
• природа растворенноговещества
• температура
• природа растворителя
13.
14.
15.
16. Растворы
Насыщенные - такие растворы, в которых приданной температуре вещество больше не
растворяется.
Ненасыщенные - такие растворы, в которых при
данной температуре находится меньше
растворенного вещества, чем в его насыщенном
растворе.
• Пересыщенные -такие растворы, в которых при
данной температуре находится в растворенном
состоянии больше вещества, чем в его
насыщенном растворе при тех же условиях.
17.
18.
19.
20.
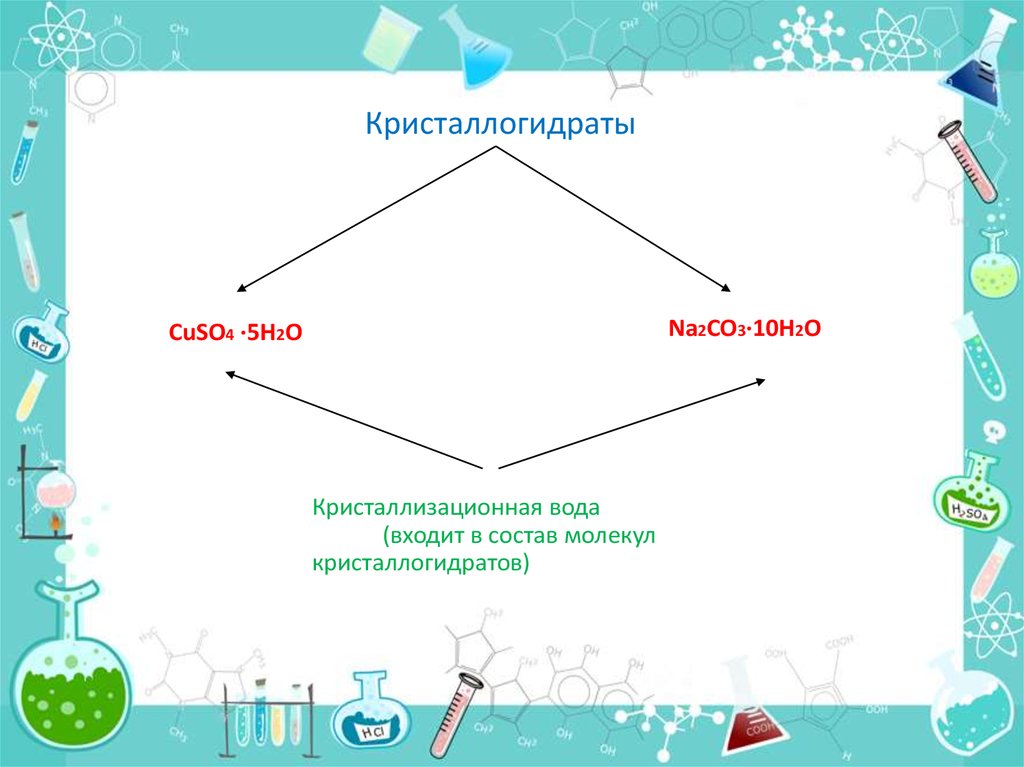
КристаллогидратыNa2CO3·10H2O
CuSO4 ·5H2O
Кристаллизационная вода
(входит в состав молекул
кристаллогидратов)
21. Сульфат меди безводный CuSO4 и кристаллогидрат CuSO4·5H2O (медный купорос)
22.
23. Карбонат натрия безводный Na2CO3 и кристаллогидрат Na2CO3·10Н2О (сода кальцинированная)
24.
25.
I. Задачи на определение формул.1.(Районная олимпиада по химии-2007 год; 9 класс).
Установите формулу кристаллогидрата сульфата железа
(II), если известно, что эта соль содержит 45,32 % воды по
массе.
2.(Кузьменко Н.Е., Еремин В.В. 2500 задач по химии)
Выведите формулу кристаллогидрата сульфата натрия,
если известно, что массовая доля кристаллизационной
воды в нем равна 55,9%.
3.(Подготовительные курсы ЛХФИ -1981 год)
Найти формулу кристаллогидрата хлорида бария зная,
что 36,6 г соли при прокаливании теряют в массе 5,4 г.
4.(Подготовительные курсы ИГМА)
При прокаливании 2,42 г кристаллогидрата нитрата меди
(II) масса вещества уменьшилась на 1,62 г. Установите
формулу кристаллогидрата.
26.
II. Задачи на растворы1. Определите массовую долю сульфата железа (II) в
растворе, полученном при растворении 55,6 г семиводного
кристаллогидрата в 344,4 г воды.
2. Определите количество кристаллогидрата MgС12*6H2О,
которое нужно растворить в 159,4 г воды, чтобы получить
10%-ный раствор хлорида магния.
3. Определите количество воды, в котором надо растворить
27,8 г семиводного сульфата железа (II), чтобы получить
насыщенный при 50 °С раствор сульфата железа (II)
(растворимость соли при этой температуре 48,6 г в 100 г
воды).
4. Какую массу кристаллогидрата сульфата натрия можно
получить при выпаривании 400 мл 12%-ного раствора
плотностью 1,12 г/мл?
























 chemistry
chemistry








