Similar presentations:
Спирты (алканолы)
1. Спирты
2. Спирты
Спирты (алканолы) – это органические вещества,молекулы которых содержат одну или
несколько гидроксильных групп (групп – OH),
соединенных с углеводородным радикалом.
Спирты
Одноатомные
Двухатомные
Трехатомные
3. Виды спиртов
Одноатомные спирты, например:CH3-OH метанол или метиловый спирт,
CH3-CH2-OH этанол или этиловый спирт.
Двухатомные (гликоли), например:
HO-CH2-CH2-OH этандиол-1,2 или этиленгликоль.
Трехатомные спирты, например:
H2C
OH
HC
OH
H2C
OH
Пропантриол-1,2,3 или глицерин.
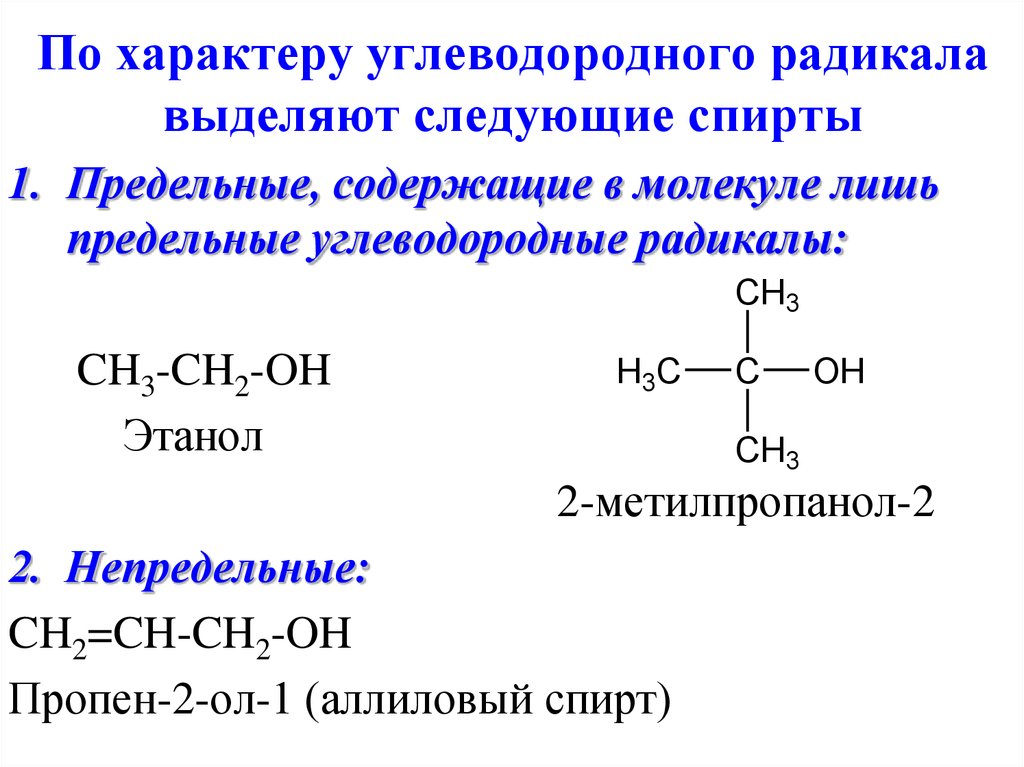
4. По характеру углеводородного радикала выделяют следующие спирты
1. Предельные, содержащие в молекуле лишьпредельные углеводородные радикалы:
CH3
CH3-CH2-OH
Этанол
H3C
C
OH
CH3
2-метилпропанол-2
2. Непредельные:
CH2=CH-CH2-OH
Пропен-2-ол-1 (аллиловый спирт)
5.
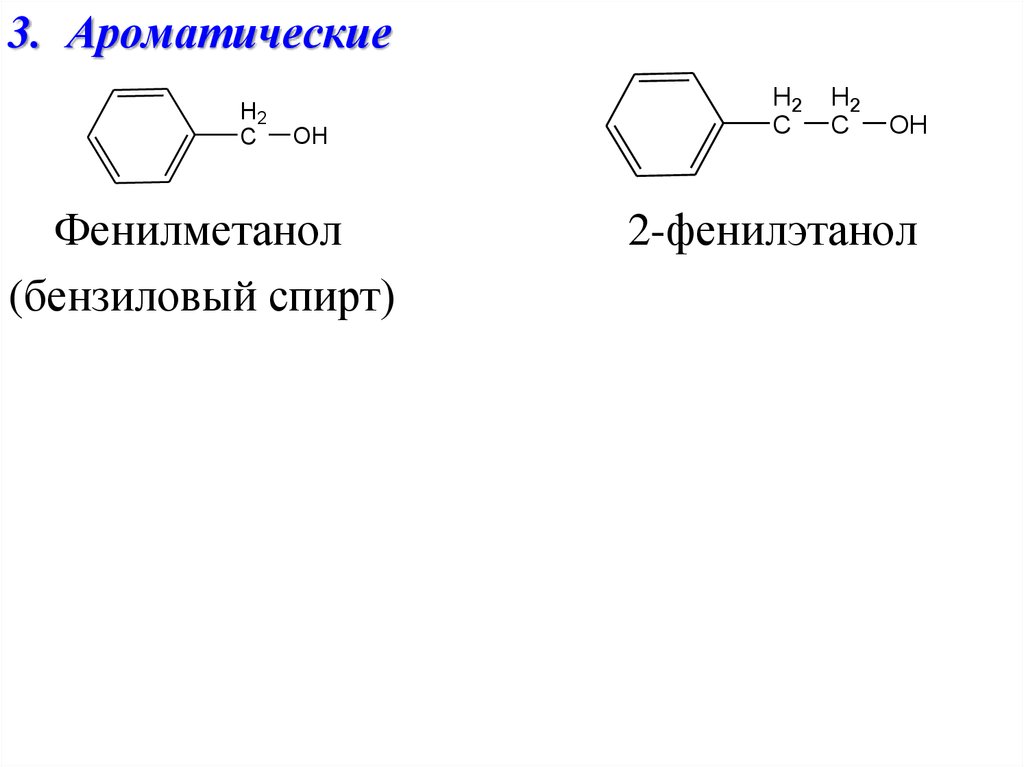
3. АроматическиеH2
C
OH
Фенилметанол
(бензиловый спирт)
H2
C
H2
C
OH
2-фенилэтанол
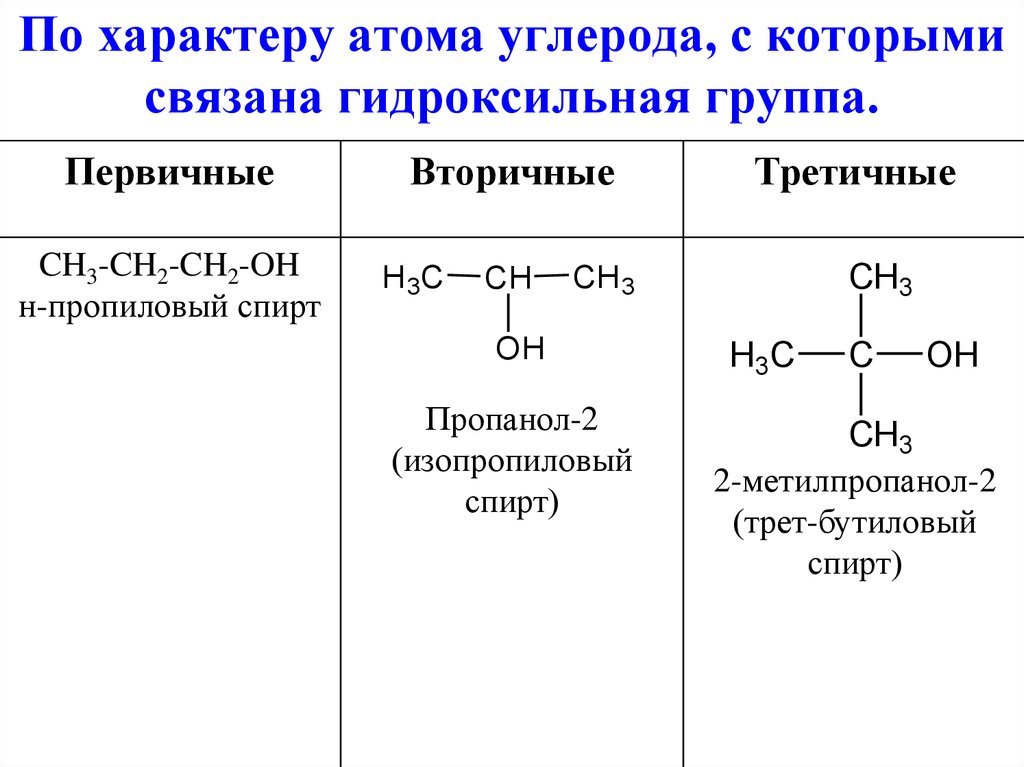
6. По характеру атома углерода, с которыми связана гидроксильная группа.
ПервичныеCH3-CH2-CH2-OH
н-пропиловый спирт
Вторичные
H3C
CH
Третичные
CH3
CH3
OH
Пропанол-2
(изопропиловый
спирт)
H3C
C
OH
CH3
2-метилпропанол-2
(трет-бутиловый
спирт)
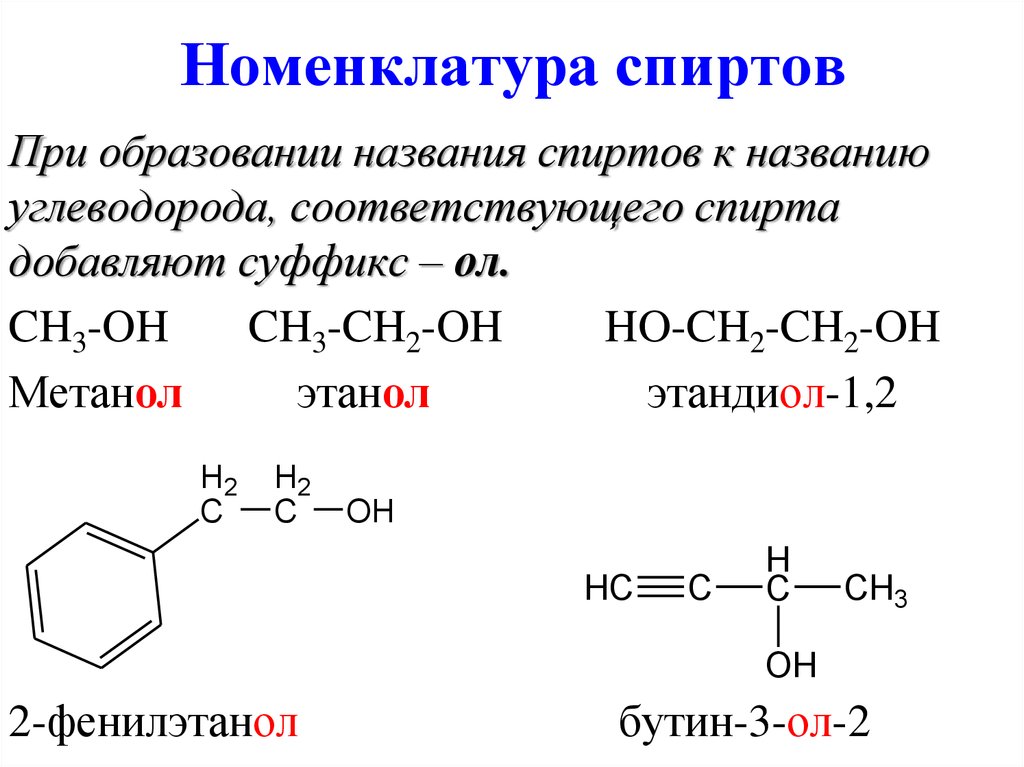
7. Номенклатура спиртов
При образовании названия спиртов к названиюуглеводорода, соответствующего спирта
добавляют суффикс – ол.
CH3-OH
CH3-CH2-OH
HO-CH2-CH2-OH
Метанол
этанол
этандиол-1,2
H2
C
H2
C
OH
HC
C
H
C
CH3
OH
2-фенилэтанол
бутин-3-ол-2
8. Изомерия спиртов
• Изомерия положения OH-группы (начиная с С3):• Углеродного скелета (начиная с С4):
9. Изомерия спиртов
• Межклассовая изомерия с простыми эфирами:10. Способы получения спиртов
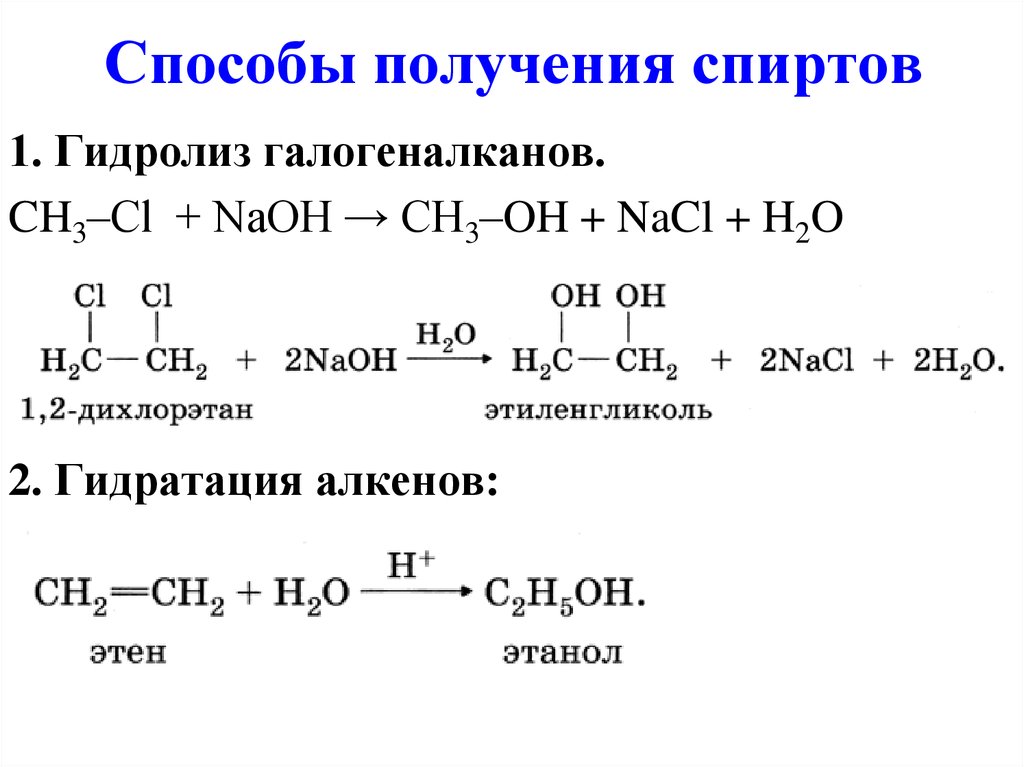
1. Гидролиз галогеналканов.CH3–Cl + NaOH → CH3–OH + NaCl + H2O
2. Гидратация алкенов:
11. Способы получения спиртов
3. Гидрирование альдегидов:4. Окисление алкенов:
12. Способы получения спиртов
5. Специфические способы получения спиртов:6. Брожение глюкозы
13. Химические свойства спиртов
1. Взаимодействие спиртов со щелочными ищелочноземельными металлами:
2Na + 2C2H5OH → 2C2H5ONa + H2
2. Взаимодействие спиртов с
галогеноводородами:
C2H5OH + HBr → C2H5Br + H2O
3. Межмолекулярная дегидратация спиртов:
H2SO4
CH3OH + HOCH3 → CH3 – O – CH3 + H2O
14.
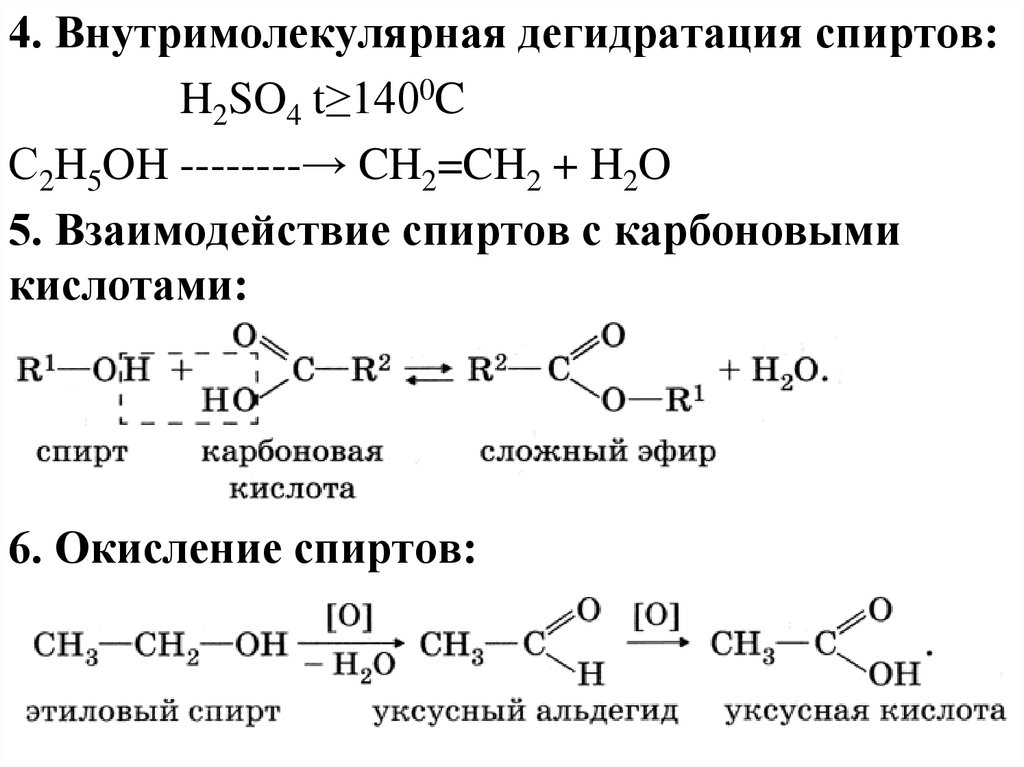
4. Внутримолекулярная дегидратация спиртов:H2SO4 t≥1400C
С2H5OH --------→ CH2=CH2 + H2O
5. Взаимодействие спиртов с карбоновыми
кислотами:
6. Окисление спиртов:
15.
7. Дегидратация спиртов: (R-СH3)8. Специфические свойства многоатомных
спиртов:
Синее окрашивание








 chemistry
chemistry








