Similar presentations:
клас-я и св-ва оксидов(1)
1. Классификация и свойства оксидов
2. Задание на 04.02.2026
ЗАДАНИЕ НА 04.02.20261. Запишите в тетради тему урока.
2. Изучите презентацию по теме урока.
3. Запишите в тетрадь содержание слайдов №14,
№15, №16, №17, №18.
4. Выполните тест по теме слайд №23.
5. Решите задачу – слайд №24.
6. Записи в тетради, выполненный тест и решенную
задачу отправьте на проверку в аис:
8в кл. до 8.50, 8б кл. до 9.50, 8а кл. до 10.50
Дома: п. 23 изучить
3. Классы неорганических соединений
ОксидыКислоты
Основания
Соли
4. оксиды
Бинарные соединения,состоящие из двух
элементов, одним из
которых является
кислород
5. Классификация оксидов
СолеобразующиеНесолеобразующие
Это оксиды, которые
взаимодействуют с
кислотами или со щелочами
с образованием соли и воды:
N2O5, CO2, CaO, Na2O
Это оксиды, которые не
взаимодействуют ни с
кислотами, ни с основаниями и
не образуют солей. Оксиды
образованы атомами
неметаллов:
CO, NO, N2O, SiO2
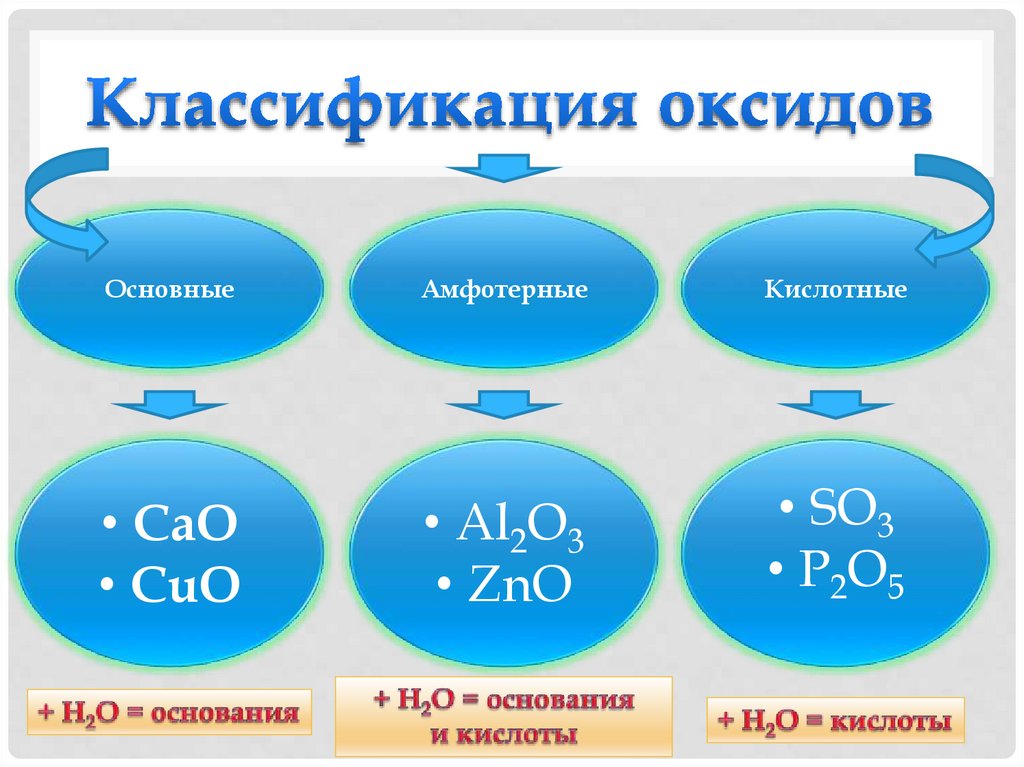
6. Классификация оксидов
ОсновныеАмфотерные
Кислотные
• CaO
• CuO
• Al2O3
• ZnO
• SO3
• P2O5
7. Получение оксидов 1. Взаимодействие простых веществ с кислородом:
С + O2 = CO22Cu + O2 =2CuO
2Ca + O2 =2CaO
8. Получение оксидов 2. Горение сложных веществ:
Получение оксидовCH4 + 2O2 = CO2 +2H2O
Метан
9. Получение оксидов 3. Окисление оксидов:
Получение оксидов4FeO + O2 =2 Fe2O3
2 CO + O2 =2 CO2
10. Получение оксидов 4. Разложение нерастворимых оснований при нагревании:
Получение оксидовMg(OH)2 = MgO + H2O
2Fe(OH)3 = Fe2O3 +3 H2O
11. Получение оксидов 5. Разложение солей:
Получение оксидовCaCO3 = CaO + CO2
CaSO4 = CaO + SO3
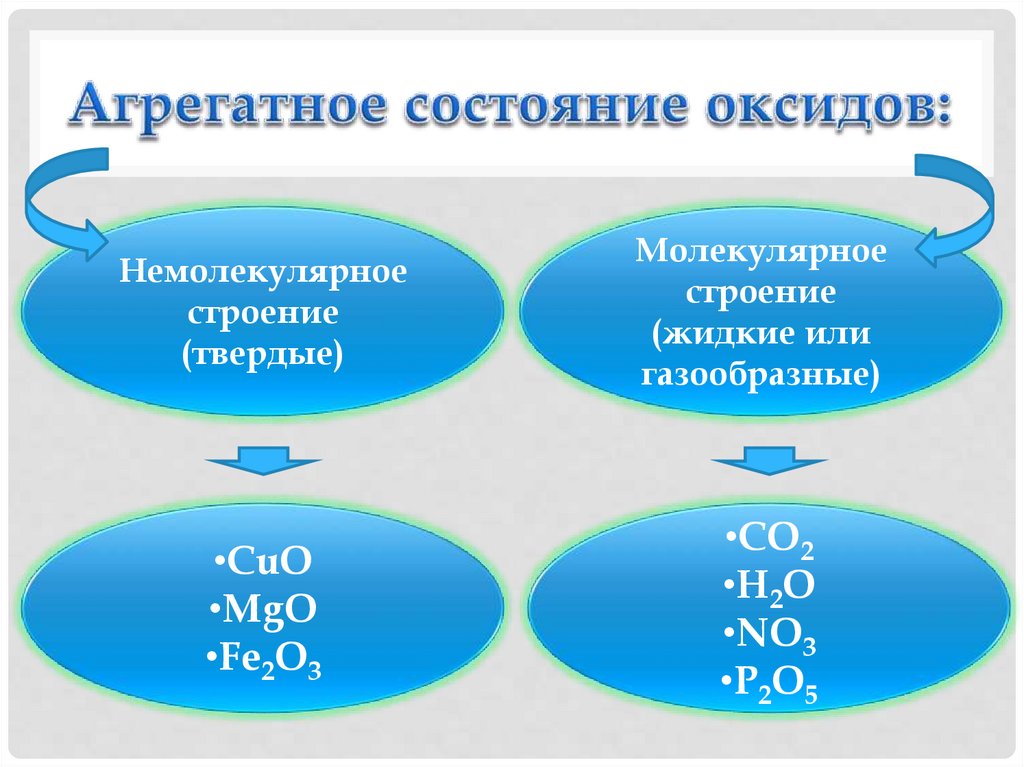
12. Агрегатное состояние оксидов:
Немолекулярноестроение
(твердые)
Молекулярное
строение
(жидкие или
газообразные)
•CuO
•MgO
•Fe2O3
•CO2
•H2O
•NO3
•P2O5
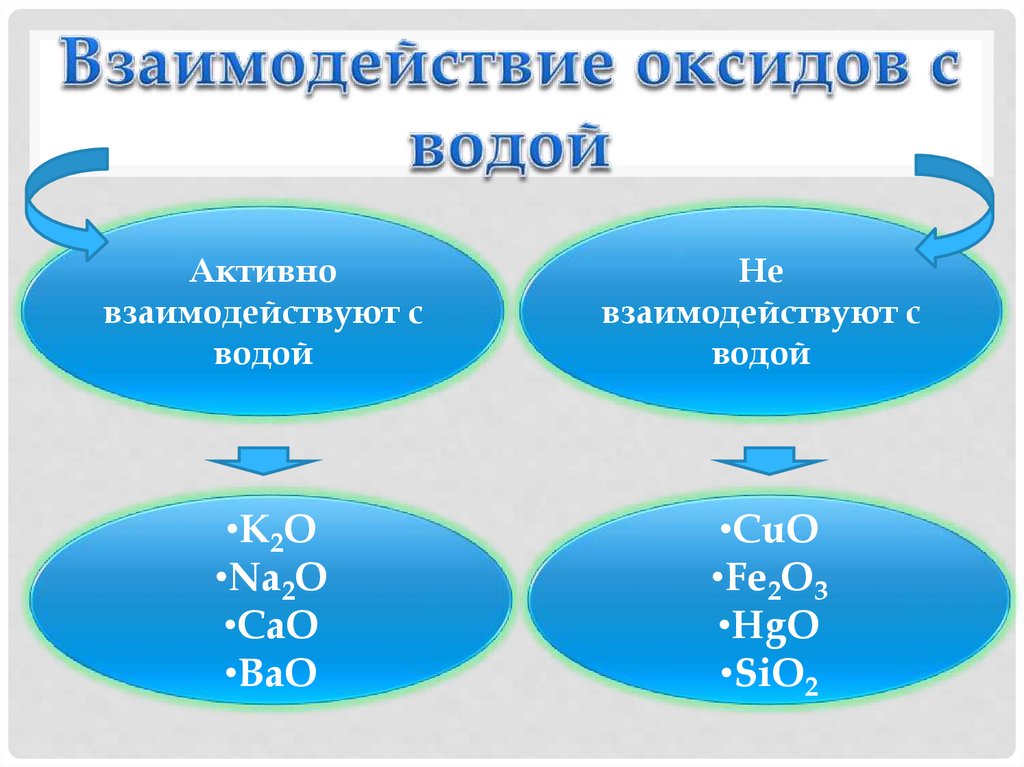
13. Взаимодействие оксидов с водой
Активновзаимодействуют с
водой
Не
взаимодействуют с
водой
•K2O
•Na2O
•CaO
•BaO
•CuO
•Fe2O3
•HgO
•SiO2
14. Химические свойства основных оксидов
Na2O + H2O =2NaOHCaO + H2O = Ca(OH)2
15. Химические свойства основных оксидов
MgO + H2SO4 = MgSO4+ H2OBaO +2HCl = BaCl2 + H2O
16. Химические свойства основных оксидов
CaO + CO2 = CaCO3BaO + SiO2 = BaSiO3
17. Химические свойства кислотных оксидов
SO3 + H2O = H2SO43
2
P2O5 + H2O = H3PO4
18. Химические свойства кислотных оксидов
2 NaOH + SO2 = Na2SO3 + H2OCa(OH)2 + CO2 = CaCO3 + H2O
19. Химические свойства кислотных оксидов
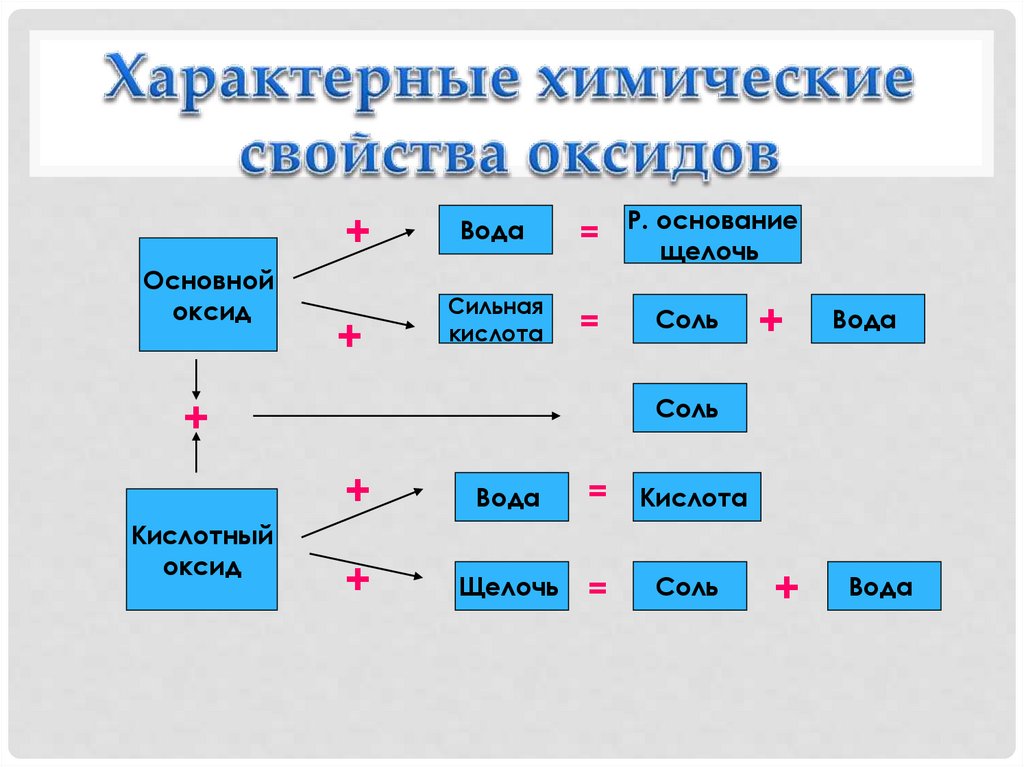
SiO2 + CaO = CaSiO320. Характерные химические свойства оксидов
+Основной
оксид
+
Вода
=
Сильная
кислота
=
+
Кислотный
оксид
Р. основание
щелочь
Соль
+
Вода
+
Вода
Соль
+
Вода
=
Кислота
+
Щелочь
=
Соль
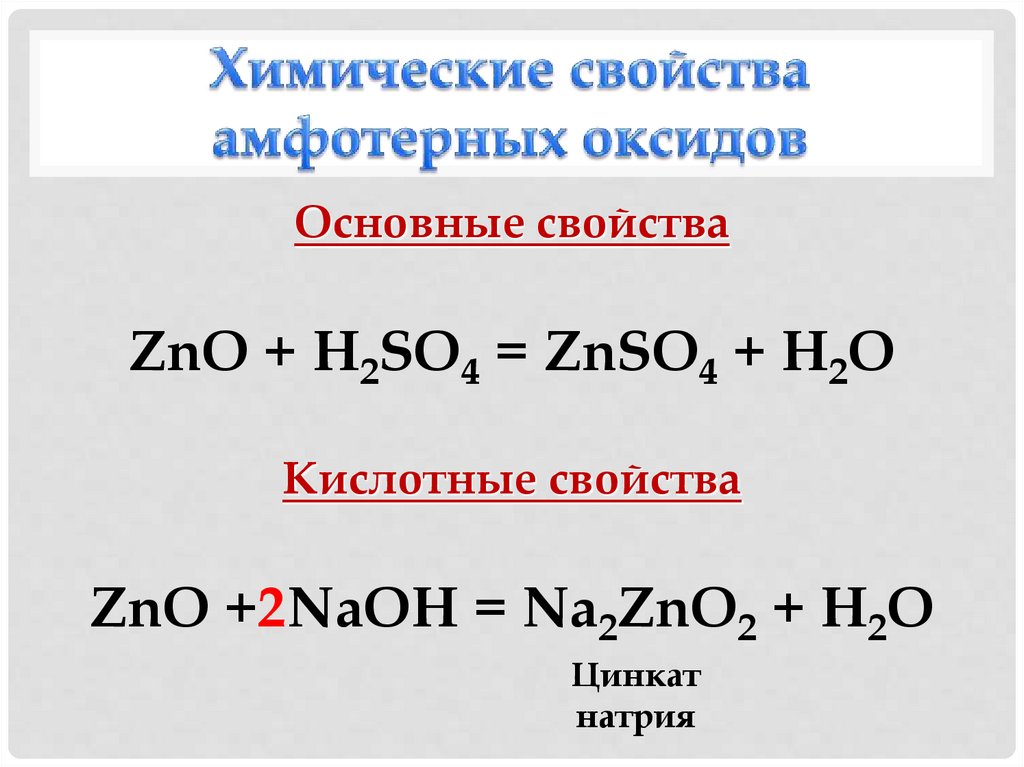
21. Химические свойства амфотерных оксидов
Основные свойстваZnO + H2SO4 = ZnSO4 + H2O
Кислотные свойства
ZnO +2NaOH = Na2ZnO2 + H2O
Цинкат
натрия
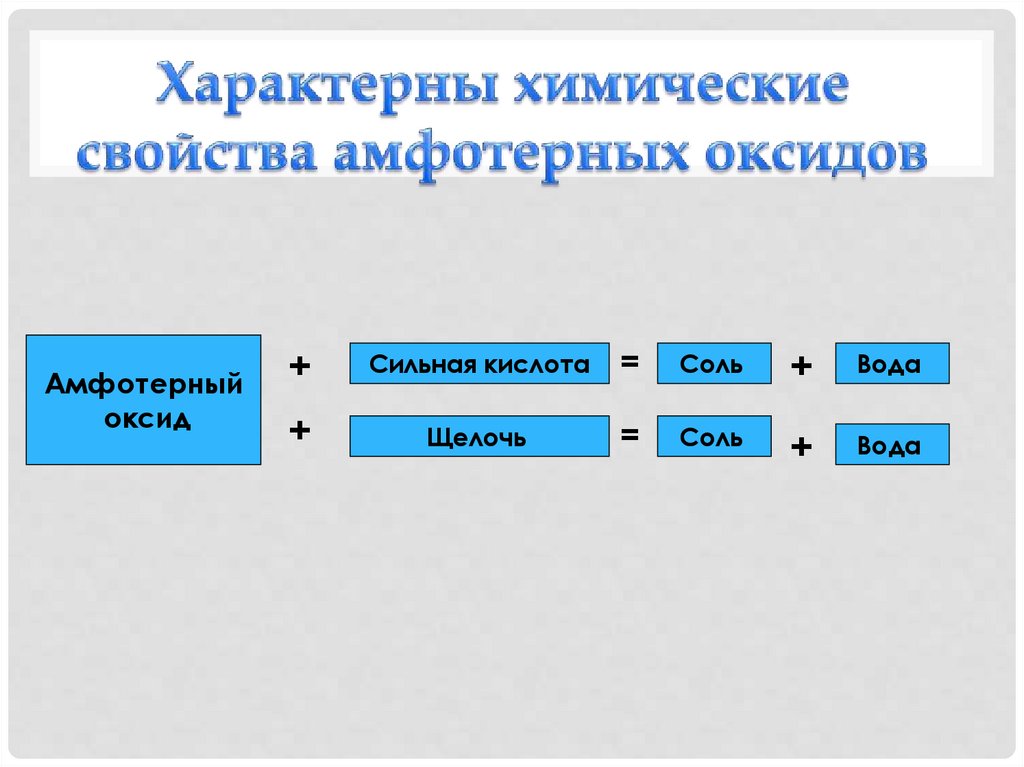
22. Характерны химические свойства амфотерных оксидов
Амфотерныйоксид
+
Сильная кислота
=
Соль
+
Вода
+
Щелочь
=
Соль
+
Вода
23. Тест:
ТЕСТ:1.Укажите формулу оксида: а) HCl; б) NaOH; в) CO2; г) NaCl .
2.Укажите формулу кислотного оксида:
а) MgO; б) BeO; в) Al2O3; г) SO2 .
3.Укажите формулу основного оксида:
а) CO2; б) SO2; в) MgO; г) N2O5.
4.Укажите формулу амфотерного оксида:
а) Al2O3; б) Na2O; в) K2O; г) P2O5.
5.Укажите оксид, который при взаимодействии с водой
образует щелочь:
а) BaO; б) Al2O3; в) CO2; г) MgO.
6.Укажите оксид, который при взаимодействии с водой
образует кислоту:
а) N2O5; б) MgO; в) ZnO; г) CuO.
7.Укажите вещество, с которым реагирует оксид углерода (IV):
а) NaOH; б) HCl; в) H2SO4; г) NaCl
8.Укажите вещество, с которым реагирует оксид магния:
а) H2O; б) HCl; в) NaOH; г) Na2SO4 .
24. Задача.
ЗАДАЧА.Какой объем водорода (н. у.) можно
получить при взаимодействии 13 г
цинка с необходимым количеством
соляной кислоты.

















 chemistry
chemistry








