Similar presentations:
жиры
1. Жиры
2.
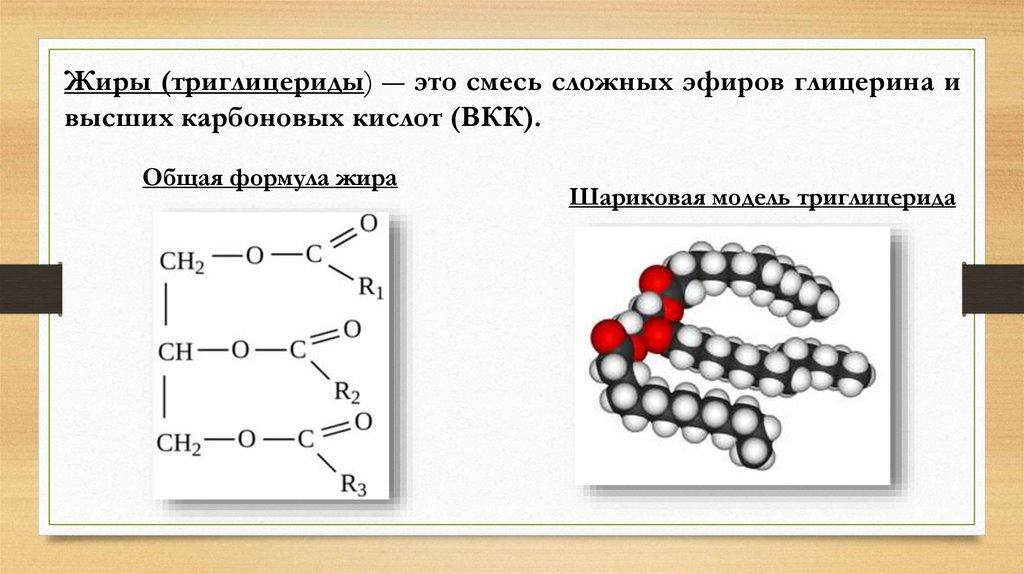
Жиры (триглицериды) ― это смесь сложных эфиров глицерина ивысших карбоновых кислот (ВКК).
Общая формула жира
Шариковая модель триглицерида
3.
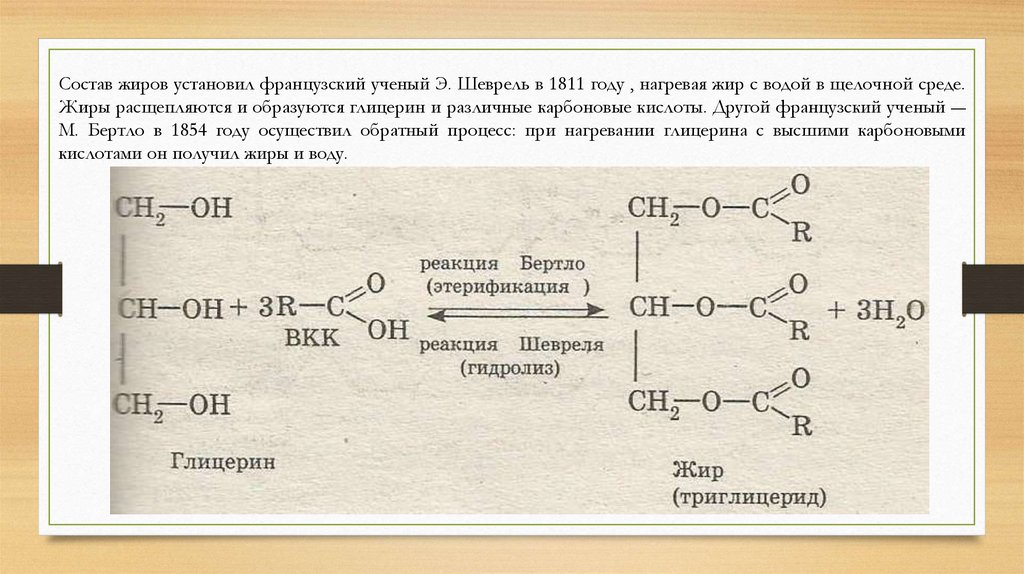
Состав жиров установил французский ученый Э. Шеврель в 1811 году , нагревая жир с водой в щелочной среде.Жиры расщепляются и образуются глицерин и различные карбоновые кислоты. Другой французский ученый ―
М. Бертло в 1854 году осуществил обратный процесс: при нагревании глицерина с высшими карбоновыми
кислотами он получил жиры и воду.
4.
Наиболее важные высшие карбоновые кислоты, входящие всостав жиров
Ненасыщенные
Насыщенные кислоты
кислоты
Масляная кислота
Олеиновая кислота
C3H7COOH
C17H33COOH
1 двойная связь
Пальмитиновая кислота
Линолевая кислота
C15H31COOH
C17H31COOH
2 двойные связи
Стеариновая кислота
Линоленовая кислота
C17H35COOH
C17H29COOH
3 двойные связи
5.
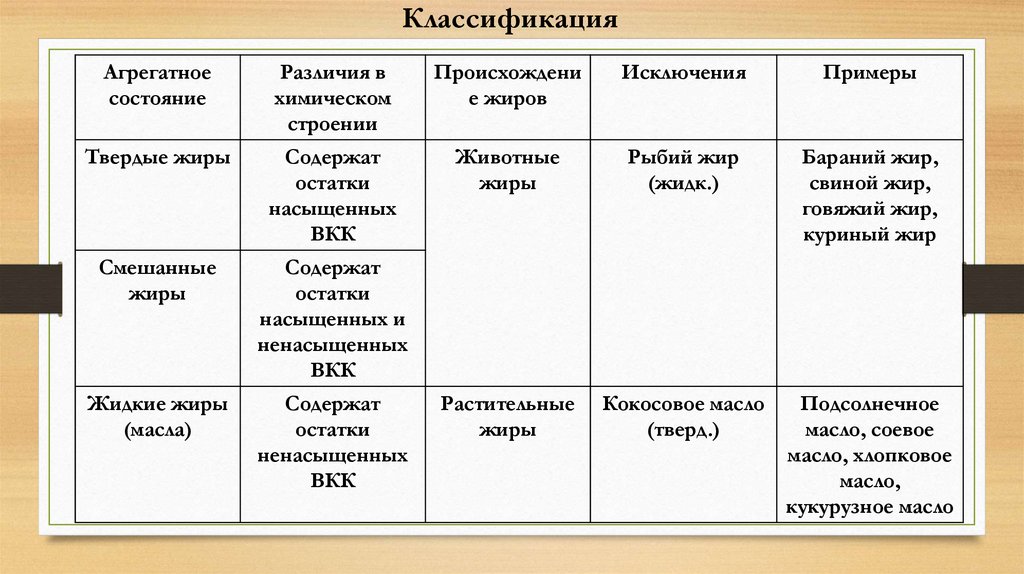
КлассификацияАгрегатное
состояние
Различия в
химическом
строении
Происхождени
е жиров
Исключения
Примеры
Твердые жиры
Содержат
остатки
насыщенных
ВКК
Животные
жиры
Рыбий жир
(жидк.)
Бараний жир,
свиной жир,
говяжий жир,
куриный жир
Смешанные
жиры
Содержат
остатки
насыщенных и
ненасыщенных
ВКК
Жидкие жиры
(масла)
Содержат
остатки
ненасыщенных
ВКК
Растительные
жиры
Кокосовое масло
(тверд.)
Подсолнечное
масло, соевое
масло, хлопковое
масло,
кукурузное масло
6.
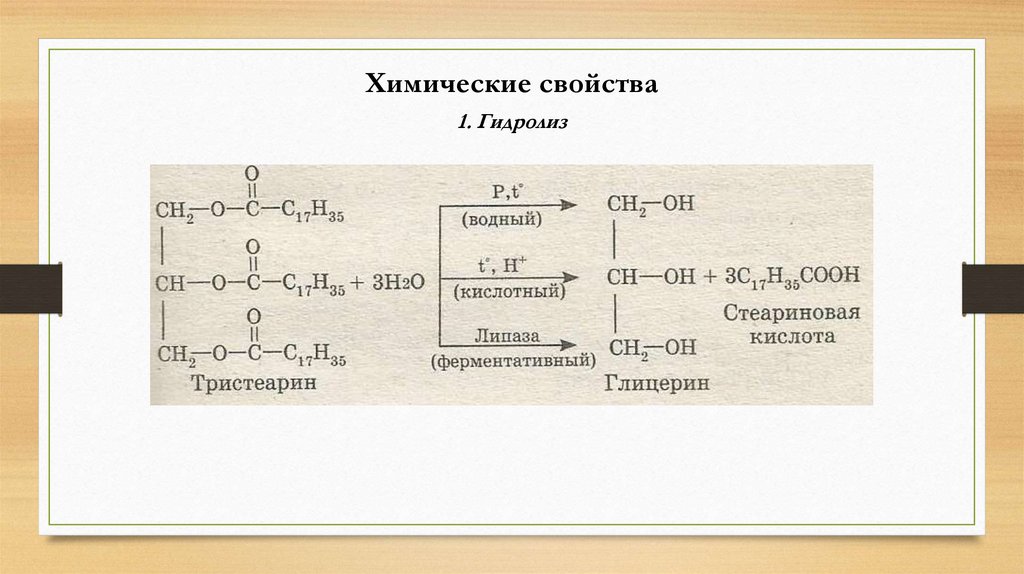
Химические свойства1. Гидролиз
7.
Химические свойства2. Щелочной гидролиз (омыление)
8.
3. Реакции присоединения(для жидких ненасыщенных жиров)
Присоединение водорода (гидрирование). Гидрированный жир используется в производстве маргарина.
9.
Функции жиров в организме1. Энергетическая (при полном расщеплении 1 г жира до CO2 и H2 O освобождается 38,9 кДж энергии).
2. Структурная (жиры ― важный компонент каждой клетки).
3. Защитная (жиры накапливаются в подкожных тканях и тканях, окружающих внутренние органы).
Применение
Пищевая промышленность
Фармацевтика
Жиры
Производство
смазочных материалов
Производство
изделий. Но
мыла
и
косметических
в настоящее время на
производство моющих средств главным образом
идут продукты переработки нефти.
10.
Моющие средства1. Мыло (твердое) ― натриевые слои ВКК.
Высшие карбоновые кислоты получают при крекинге и окислении нефтепродуктов:
2CH3 (CH2 )34 CH3 + 5O2 → 2H2 O + 4CH3 (CH2 )16 COOH
Натриевые соли карбоновых кислот, образованные сильными основаниями и слабыми кислотами, подвергаются
гидролизу:
C17 H35 COO− + Na+ + H+ + OH− ↔ C17 H35 COOH + Na+ + OH−
Натриевые соли (мыло) получают получают при взаимодействии щелочи и соды с высшими карбоновыми
кислотами:
C17 H35 COOH + NaOH → C17 H35 COONa + H2 O
стеарат натрия
Образовавшаяся щелочь эмульгирует, частично разлагает жиры и освобождает прилипшую к ним грязь.
Карбоновые кислоты с водой образуют пену, которая захватывает частицы грязи. Если вода жесткая, она
2+
2+
содержит катионы Ca и Mg , и мыло не пенится, так как образуются нерастворимые соли:
11.
Моющие средства2. Жидкое мыло ― калиевые соли ВКК.
Жидкие мыла получают при взаимодействии гидроксида калия с ВКК:
Пальмитат калия
Стеарат калия
Калиевые соли по сравнению с натриевыми лучше растворимы в воде и поэтому обладают более сильным
моющим действием.
3. Синтетические моющие средства ― натриевые соли сложных эфиров высших спиртов и серной
кислоты (сульфокислот).
Преимущество синтетических моющих средств заключается в том, что их кальциевые соли растворимы в воде.
Поэтому в отличии от обычного мыла они не утрачивают моющее действие и в жесткой воде.






 chemistry
chemistry








