Similar presentations:
b6f30a76cde2483ebfbc322fd64c56d8 (1)
1.
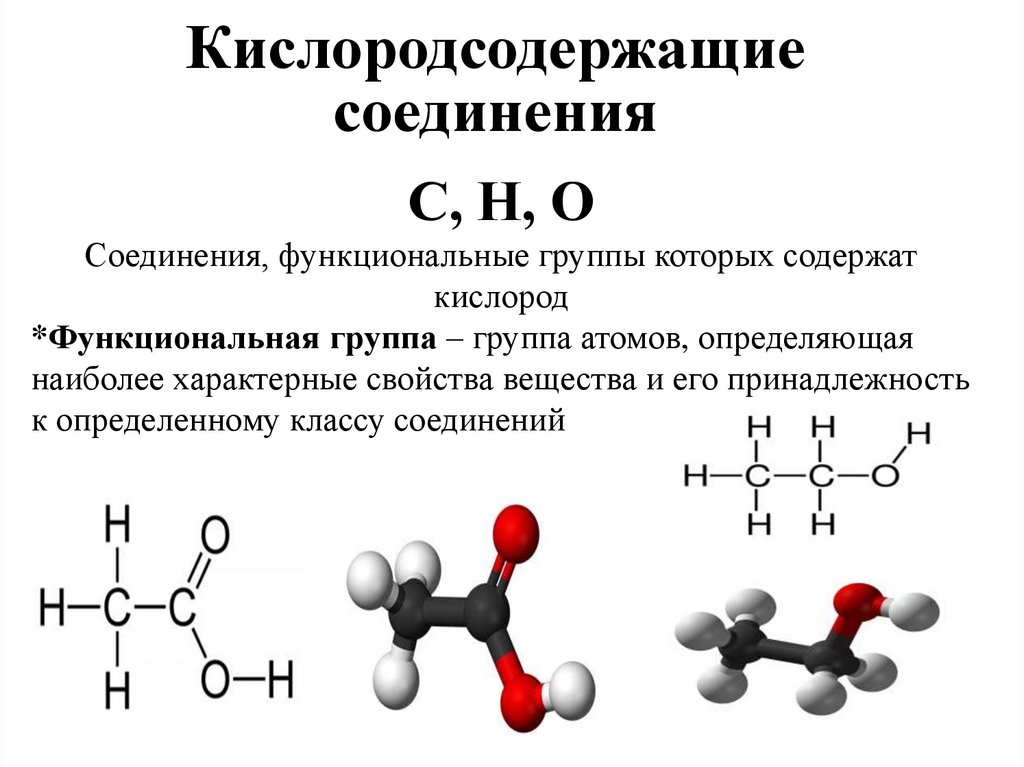
Кислородсодержащиесоединения
С, Н, О
Соединения, функциональные группы которых содержат
кислород
*Функциональная группа – группа атомов, определяющая
наиболее характерные свойства вещества и его принадлежность
к определенному классу соединений
2.
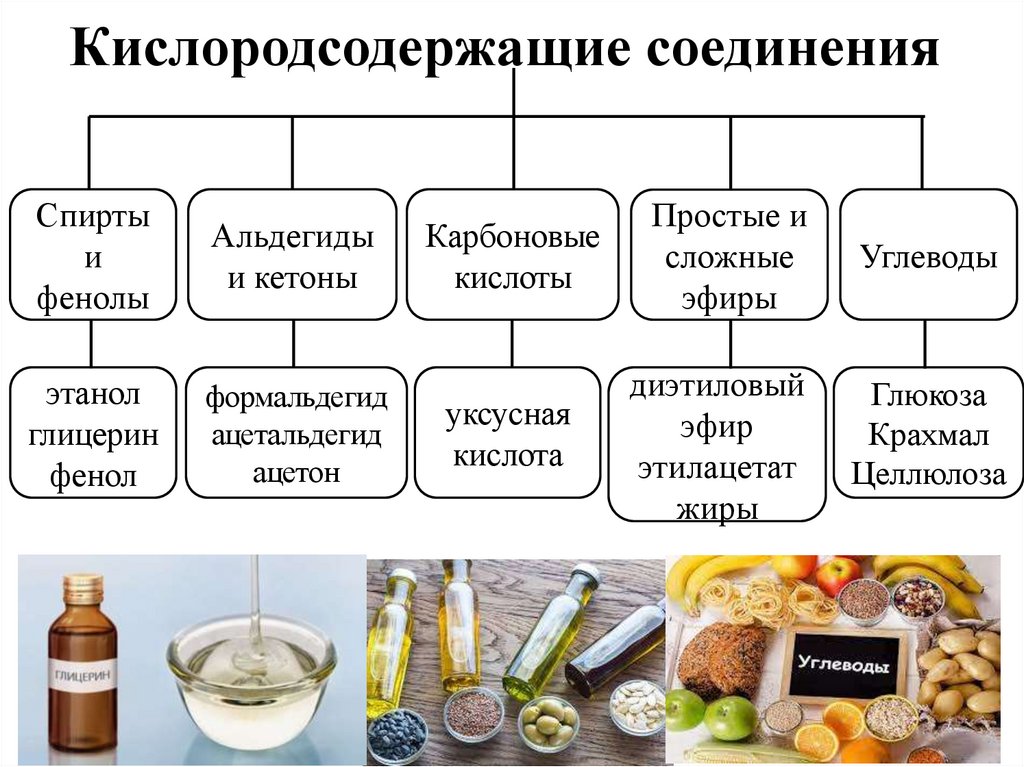
Кислородсодержащие соединенияСпирты
и
фенолы
Альдегиды
и кетоны
этанол
глицерин
фенол
формальдегид
ацетальдегид
ацетон
Карбоновые
кислоты
Простые и
сложные
эфиры
Углеводы
уксусная
кислота
диэтиловый
эфир
этилацетат
жиры
Глюкоза
Крахмал
Целлюлоза
3.
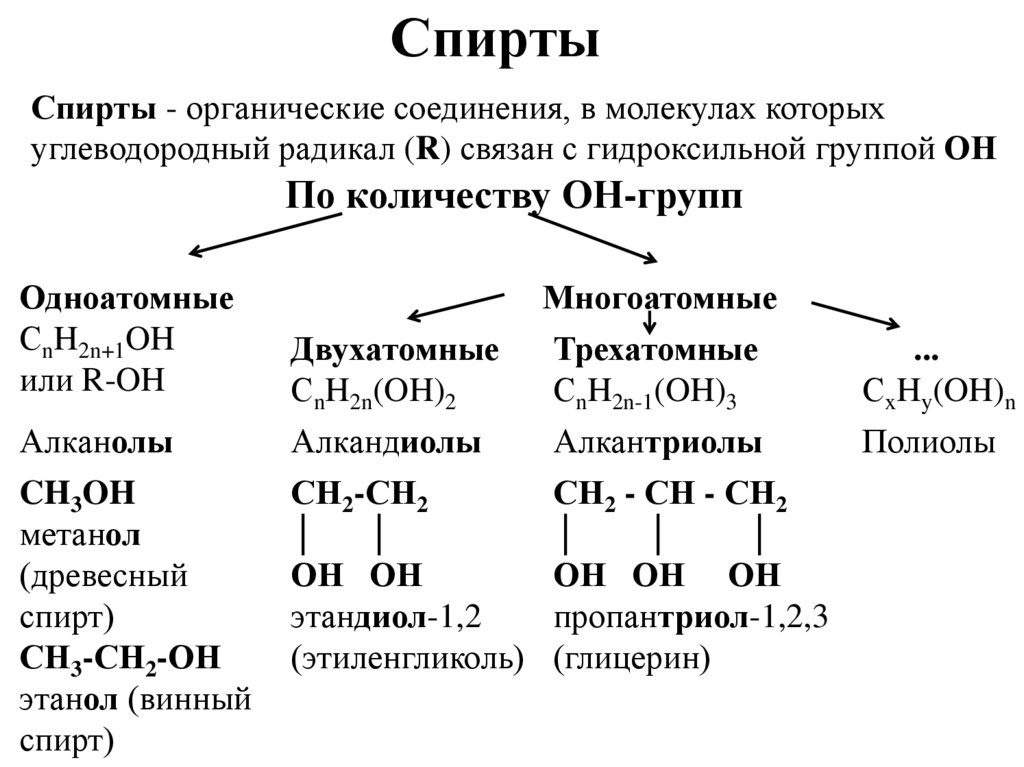
СпиртыСпирты - органические соединения, в молекулах которых
углеводородный радикал (R) связан с гидроксильной группой ОН
По количеству ОН-групп
Одноатомные
СnH2n+1OH
или R-OH
Алканолы
CH3OH
метанол
(древесный
спирт)
СН3-СН2-ОН
этанол (винный
спирт)
Двухатомные
СnH2n(OH)2
Многоатомные
Трехатомные
СnH2n-1(OH)3
Алкандиолы
СН2-СН2
│
│
ОН ОН
этандиол-1,2
(этиленгликоль)
Алкантриолы
Полиолы
СН2 - СН - СН2
│
│
│
ОН ОН ОН
пропантриол-1,2,3
(глицерин)
...
СxHy(OH)n
4.
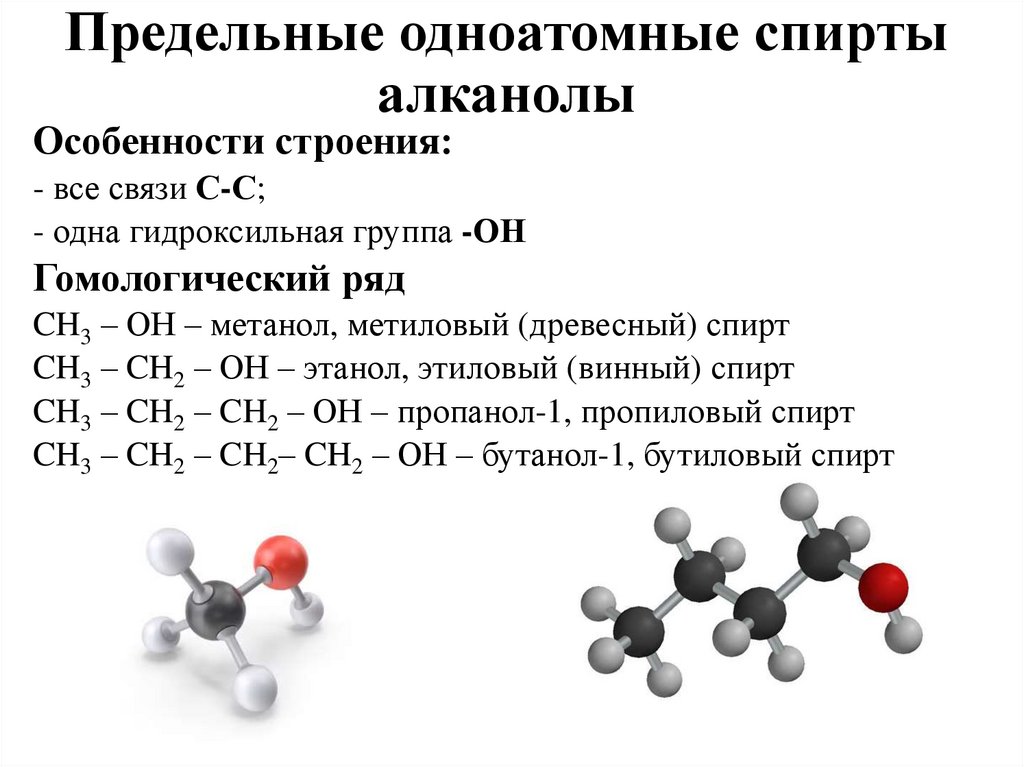
Предельные одноатомные спиртыалканолы
Особенности строения:
- все связи С-С;
- одна гидроксильная группа -ОН
Гомологический ряд
CH3 – ОН – метанол, метиловый (древесный) спирт
CH3 – CH2 – ОН – этанол, этиловый (винный) спирт
CH3 – CH2 – CH2 – ОН – пропанол-1, пропиловый спирт
CH3 – CH2 – CH2– CH2 – ОН – бутанол-1, бутиловый спирт
5.
НоменклатураПредельные одноатомные спирты - алканолы
• суффикс – ол (к названию алкана с
соответствующим числом атомов С)
• положение ОН-группы в углеродной цепи
указывают цифрой
• нумерация с того края, где ближе ОН-группа
Задание: Назовите вещества по международной
номенклатуре ИЮПАК
6.
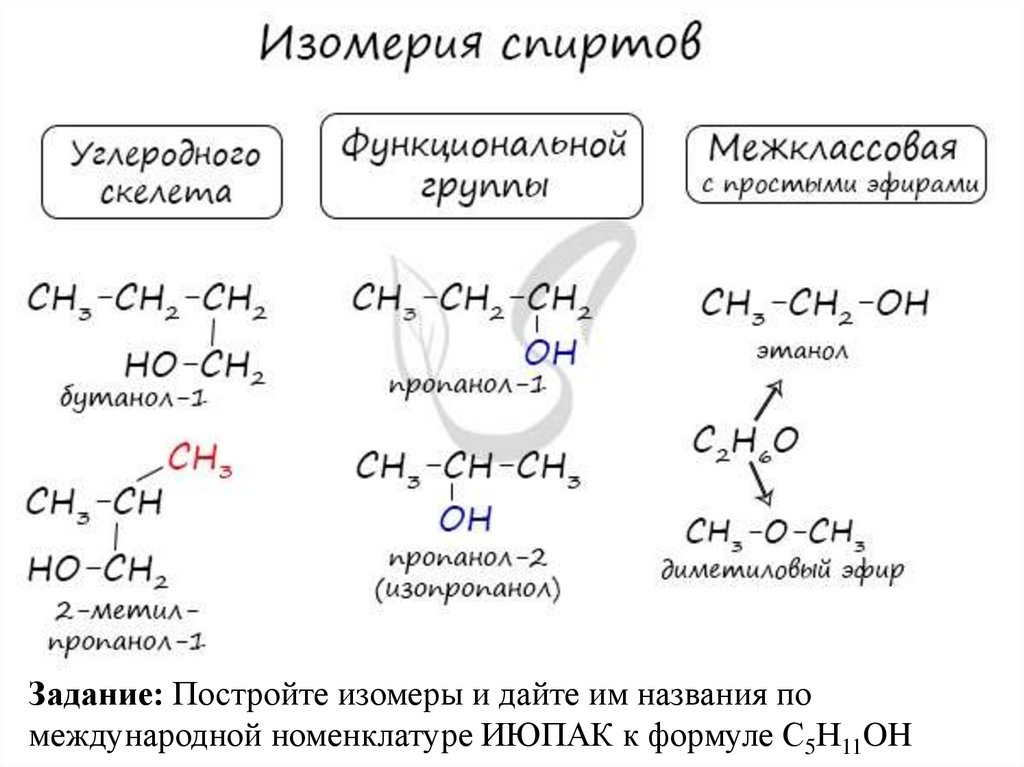
Задание: Постройте изомеры и дайте им названия помеждународной номенклатуре ИЮПАК к формуле С5Н11OH
7.
Получение1 Спиртовое брожение
дрожжи
С6Н12 О6
СН3-СН2-ОН + 2СО2↑
глюкоза
этанол
2 Гидратация алкенов (присоединение молекулы воды)
p, t, H3PO4
СН2 = СН2 + Н2О
СН2 - СН2
│
│
Н ОН
(С2Н5ОН - этанол)
8.
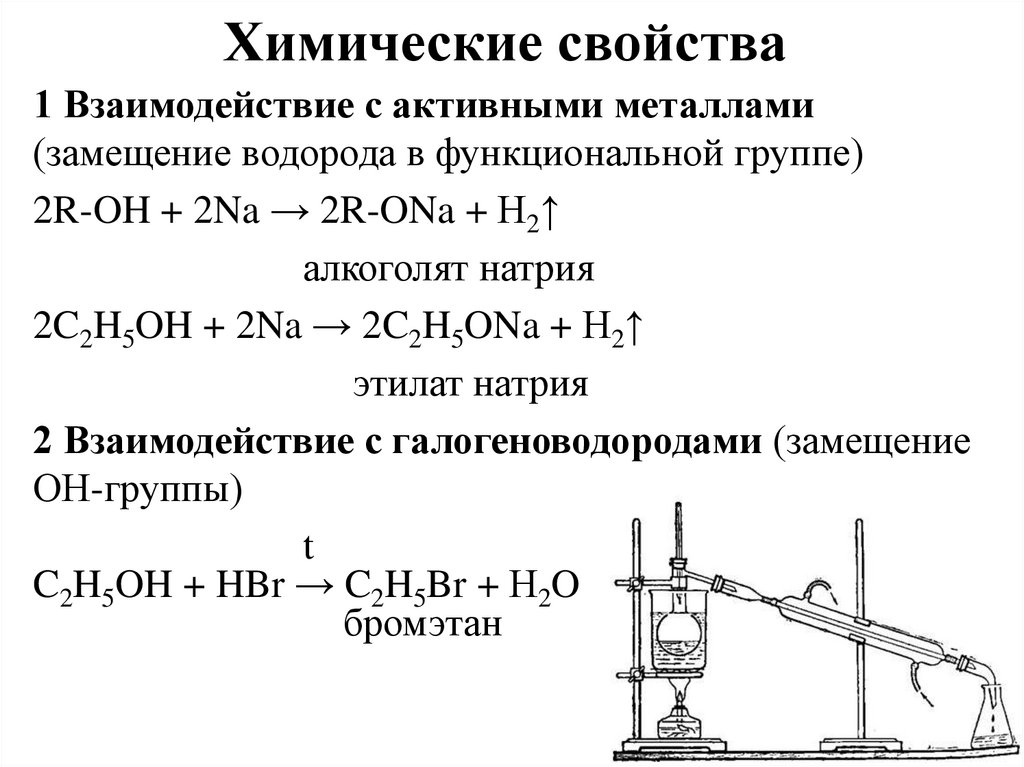
Химические свойства1 Взаимодействие с активными металлами
(замещение водорода в функциональной группе)
2R-OH + 2Na → 2R-ONa + Н2↑
алкоголят натрия
2C2H5OH + 2Na → 2C2H5ONa + Н2↑
этилат натрия
2 Взаимодействие с галогеноводородами (замещение
ОН-группы)
t
C2H5OH + HBr → C2H5Br + Н2O
бромэтан
9.
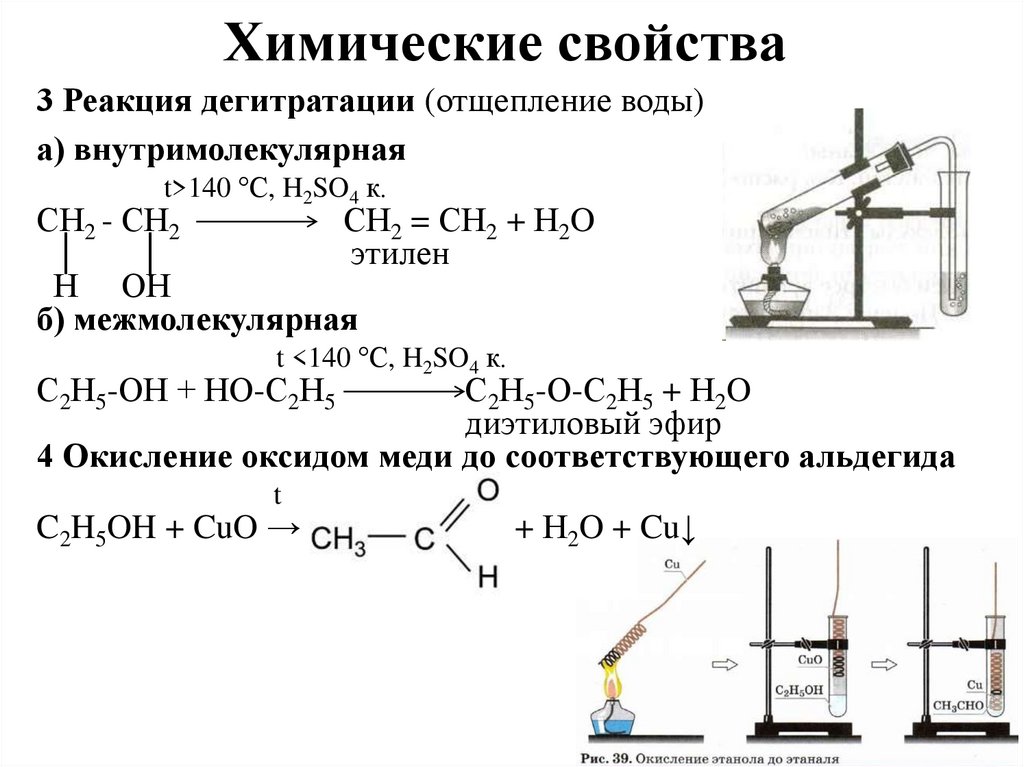
Химические свойства3 Реакция дегитратации (отщепление воды)
а) внутримолекулярная
t>140 °С, H2SO4 к.
СН2 - СН2
СН2 = СН2 + Н2O
│
│
этилен
Н ОН
б) межмолекулярная
t <140 °С, H2SO4 к.
С2Н5-ОН + НО-С2Н5
С2Н5-О-С2Н5 + Н2O
диэтиловый эфир
4 Окисление оксидом меди до соответствующего альдегида
t
C2H5OH + CuO →
+ Н2O + Cu↓
10.
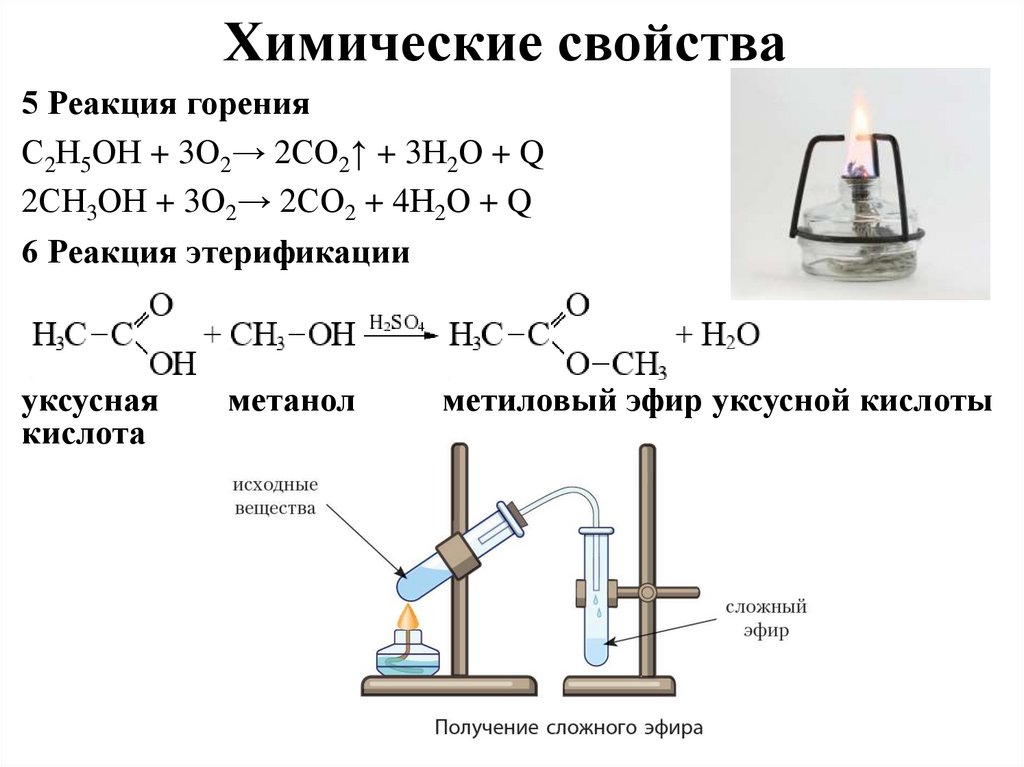
Химические свойства5 Реакция горения
С2Н5ОН + 3О2→ 2СО2↑ + 3Н2О + Q
2СН3ОН + 3О2→ 2СО2 + 4Н2О + Q
6 Реакция этерификации
уксусная
кислота
метанол
метиловый эфир уксусной кислоты
11.
Применение12.
Применение13.
ПрименениеЭТИЛЕНГЛИКОЛЬ
14.
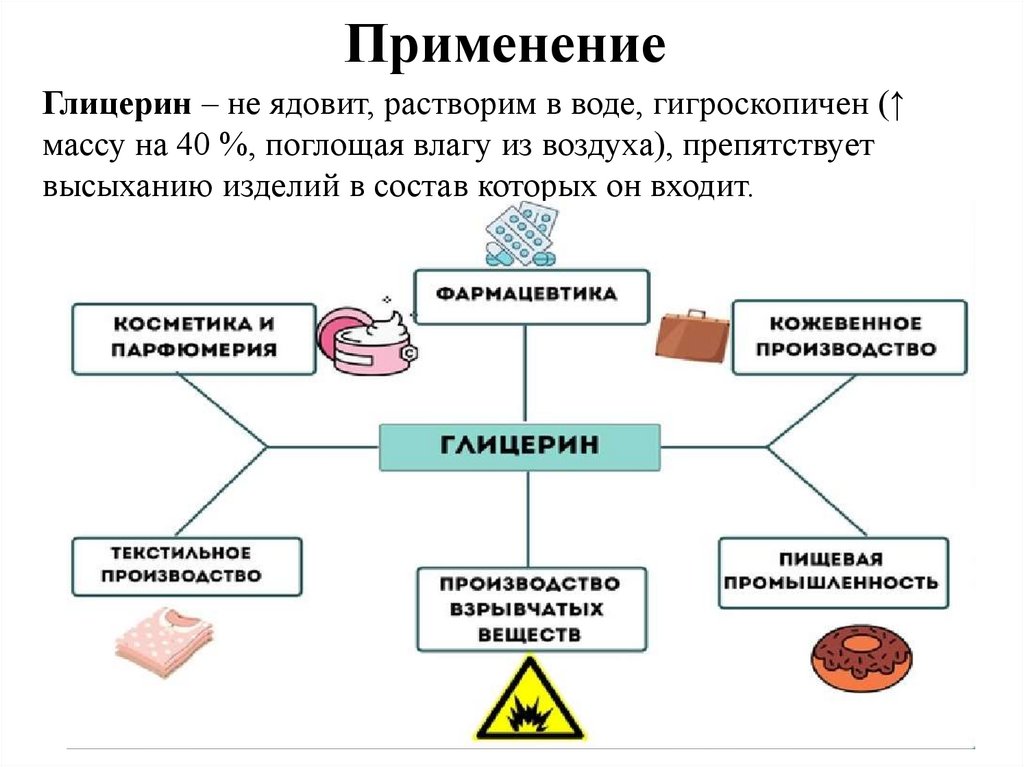
ПрименениеГлицерин – не ядовит, растворим в воде, гигроскопичен (↑
массу на 40 %, поглощая влагу из воздуха), препятствует
высыханию изделий в состав которых он входит.
15.
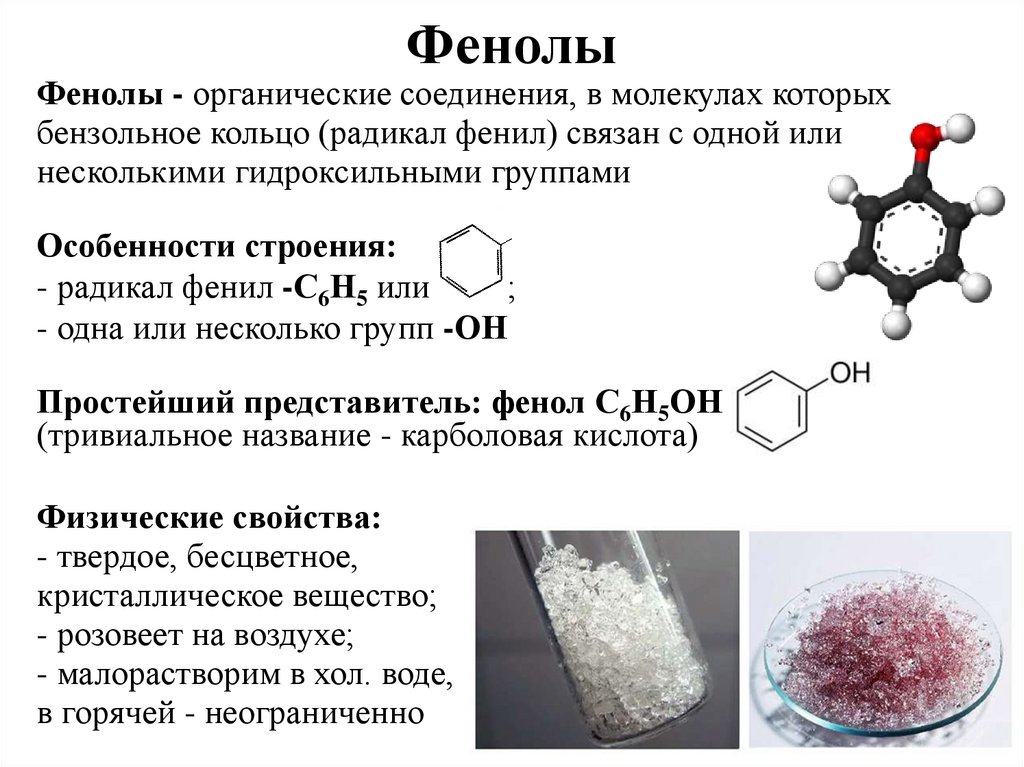
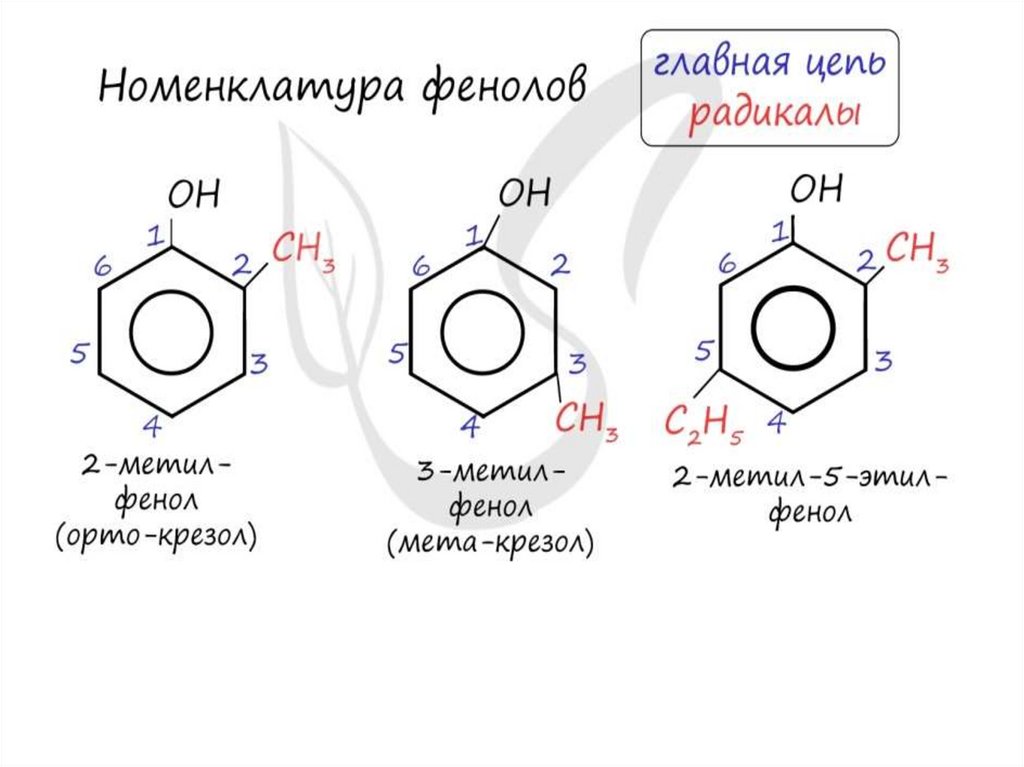
ФенолыФенолы - органические соединения, в молекулах которых
бензольное кольцо (радикал фенил) связан с одной или
несколькими гидроксильными группами
Особенности строения:
- радикал фенил -С6Н5 или
;
- одна или несколько групп -ОН
Простейший представитель: фенол С6Н5ОН
(тривиальное название - карболовая кислота)
Физические свойства:
- твердое, бесцветное,
кристаллическое вещество;
- розовеет на воздухе;
- малорастворим в хол. воде,
в горячей - неограниченно
16.
17.
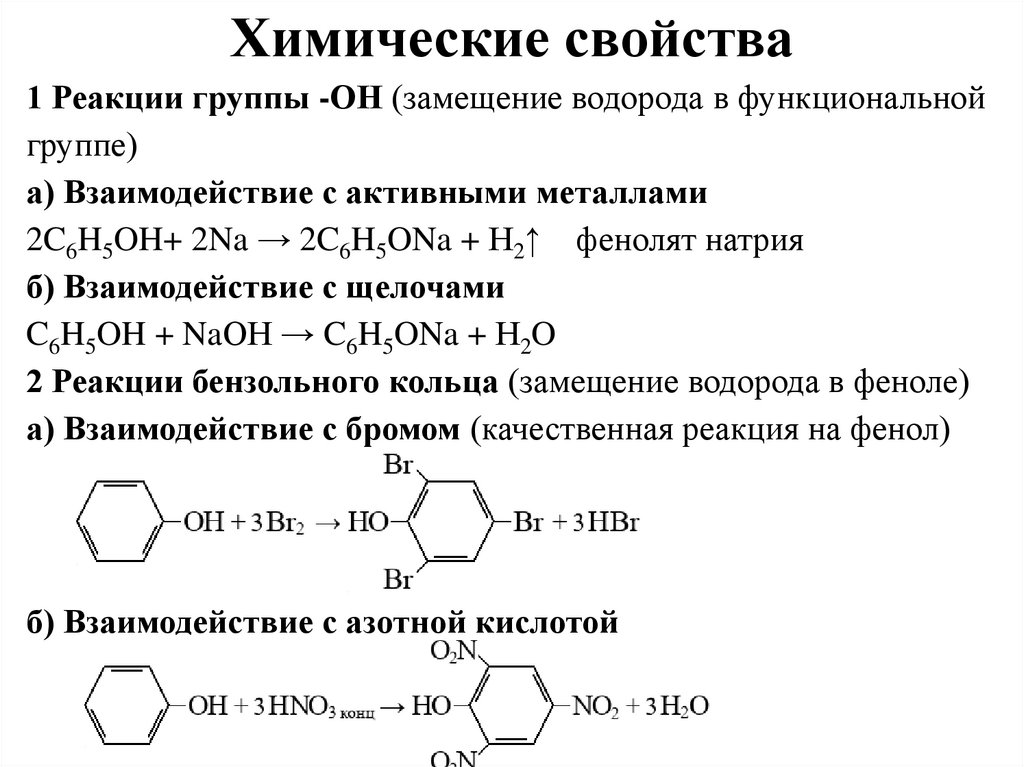
Химические свойства1 Реакции группы -ОН (замещение водорода в функциональной
группе)
а) Взаимодействие с активными металлами
2C6H5OH+ 2Na → 2C6H5ONa + Н2↑ фенолят натрия
б) Взаимодействие с щелочами
C6H5OH + NaОН → C6H5ONa + Н2O
2 Реакции бензольного кольца (замещение водорода в феноле)
а) Взаимодействие с бромом (качественная реакция на фенол)
б) Взаимодействие с азотной кислотой
18.
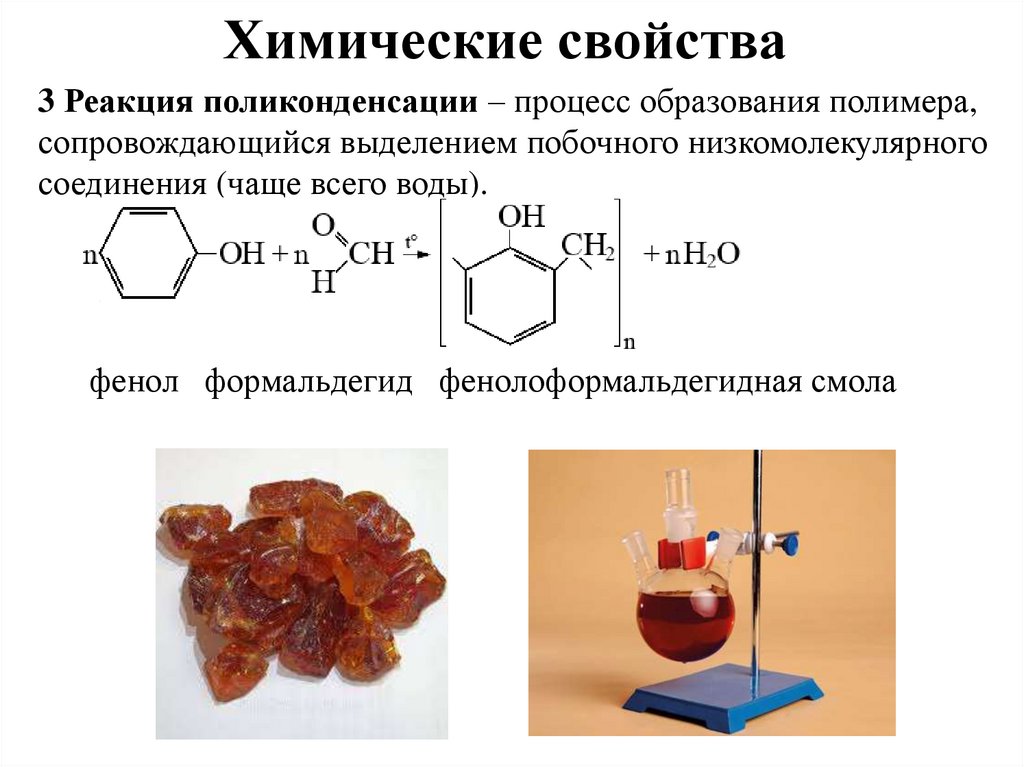
Химические свойства3 Реакция поликонденсации – процесс образования полимера,
сопровождающийся выделением побочного низкомолекулярного
соединения (чаще всего воды).
фенол формальдегид фенолоформальдегидная смола
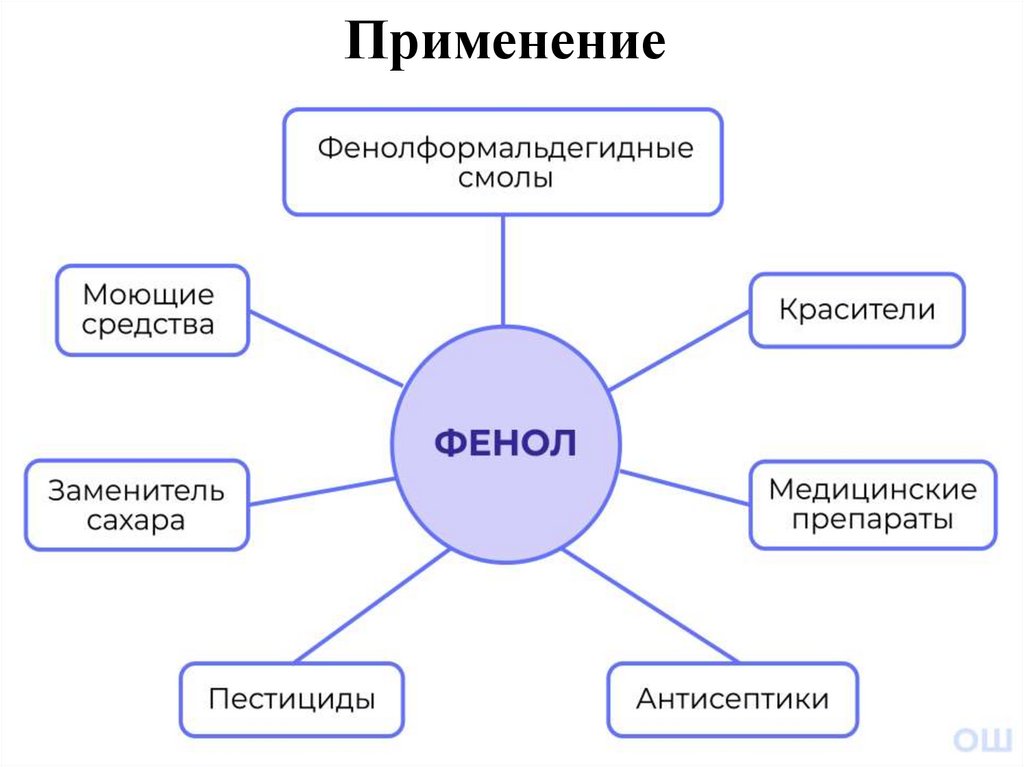
19.
Применение3




 chemistry
chemistry