Similar presentations:
азотная кислота (2)
1.
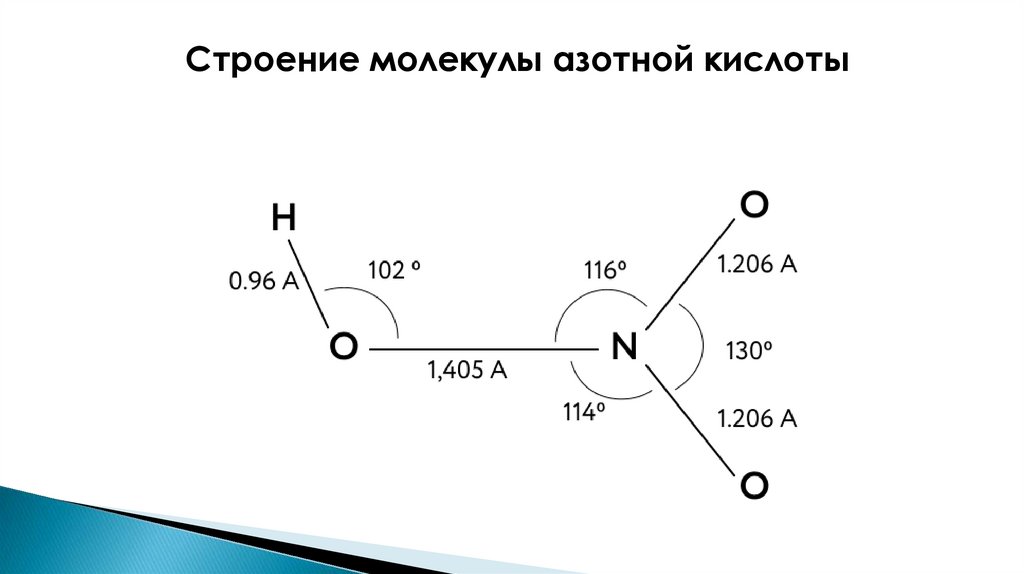
Строение молекулы азотной кислоты2.
Физические свойства азотной кислотыЧистая азотная кислота представляет собой бесцветную жидкость с
резким запахом. Чистую безводную азотную кислоту называют дымящей,
азотную кислоту с концентрацией 68% и выше — концентрированной.
Азотная кислота смешивается с водой в любых соотношениях и в водных
растворах практически полностью диссоциирует на ионы.
HNO3 → H++NO3
Азотная кислота ядовита, при попадании на кожу разрушающе
действует на неё, оставляя жёлтые пятна вследствие взаимодействия с
белками кожи.
На свету азотная кислота частично разлагается с выделением оксида
азота(IV) NO₂ бурого цвета и поэтому приобретает жёлтую окраску:
4HNO3 → 4NO2+2H2O+O2
Азотная кислота проявляет свойства, общие с другими кислотами, и
специфические, которые обусловлены её сильной окислительной
способностью.
3.
Общие свойства кислотАзотная кислота реагирует с основными и амфотерными оксидами и
гидроксидами с образованием нитратов:
CuO+2HNO3 = Cu(NO3)2+H2О
AL(ОH)3+3HNO3 = Al(NO3)3+3H2О
Азотная кислота вступает в реакции обмена с солями других кислот,
если образуется газ или осадок:
CaCO3+2HNO3 = Ca(NO3)2+H2О+CO2↑
4.
Особые свойстваВ отличие от других кислот азотная кислота реагирует с большинством металлов,
кроме благородных.
В реакциях азотной кислоты с металлами никогда не образуется водород.
Окислителем в этих реакциях выступает атом азота кислотного остатка, поэтому
продуктами реакции являются соединения азота в разной степени окисления. Состав
соединений зависит от активности металла и концентрации азотной кислоты. Так, при
взаимодействии концентрированной азотной кислоты с медью образуется бурый
оксид азота(IV): 4НNO3 + Cu = Cu(NO3)2+2NО2 ↑+2H2О
При взаимодействии разбавленной азотной кислоты с медью продукт реакции —
бесцветный оксид азота(II): 8HNО3+3Cu = 3Cu(NO3)2+2NO↑+4H2O
Концентрированная азотная кислота пассивирует железо и алюминий.
На их поверхности под действием концентрированной кислоты образуется прочная плёнка,
которая защищает металл от дальнейшей реакции. Поэтому концентрированную азотную
кислоту можно транспортировать в стальных или алюминиевых цистернах.
Азотная кислота способна окислять и другие неорганические и органические вещества.
Органические вещества могут воспламеняться при соприкосновении с азотной кислотой,
и работа с ней требует аккуратности и осторожности.
5.
6.
ПолучениеВ лаборатории азотную кислоту получают, нагревая
твердый нитрат натрия или калия с концентрированной
серной кислотой:
NaNO3(тв)+H2SO4(конц) =
NaHSO4+HNO3
В промышленности азотную кислоту получают из аммиака.
Процесс состоит из нескольких стадий:
NH3 → NO → NO2 → HNO3
7.
красителейПрименение
пластмасс
Азотная кислота используется в промышленности
для получения:
минеральных удобрений
взрывчатых веществ
лекарств







 chemistry
chemistry








