Similar presentations:
Тема_24_Тепловой_эффект_химической_реакции_понят
1. ХИМИЯ
Тепловой эффект химической реакции, понятие отермохимическом уравнении, экзо- и
эндотермических реакциях.
2.
Химические реакции сопровождаются изменениемзапаса энергии веществ.
Тепловой эффект Q – это количество теплоты, выделяющееся
или поглощающееся в ходе реакции.
Тепловой эффект
положительный
отрицательный
(теплота выделяется)
(теплота поглощается)
Оно указывается в термохимических уравнениях реакций:
H2(г) + F2(г) = 2HF(г) + 537 кДж (+)
3О2(г) = 2О3(г) – 285 кДж (-)
3.
Тепловой эффект реакции зависит от агрегатногосостояния веществ.
Пример: образование газообразной и жидкой
воды происходит с выделением разного
количества теплоты:
2H2(г) + О2(г) = 2H2О(г) + 484 кДж
2H2(г) + О2(г) = 2H2О (ж) + 572 кДж
4.
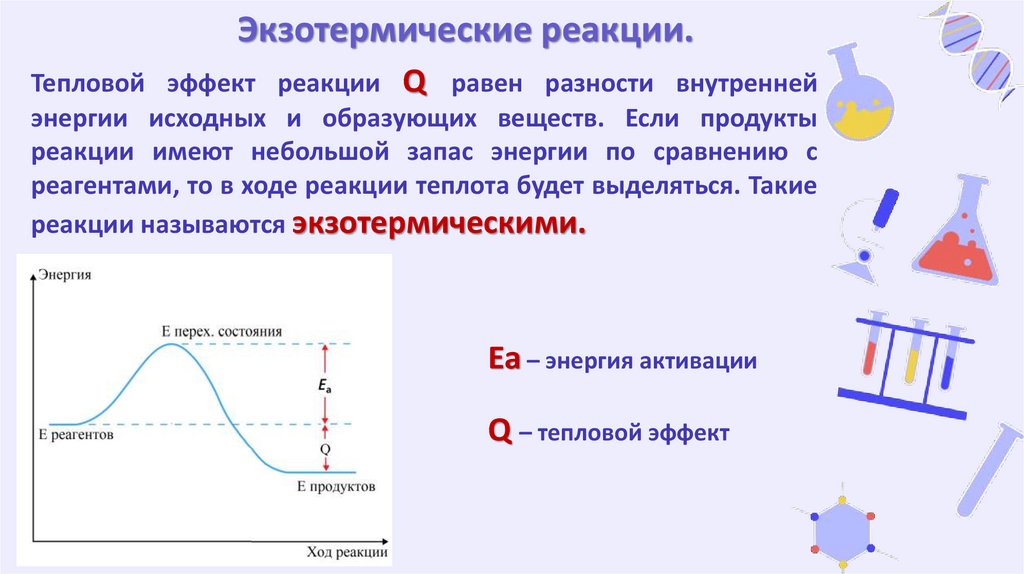
Экзотермические реакции.Тепловой эффект реакции Q равен разности внутренней
энергии исходных и образующих веществ. Если продукты
реакции имеют небольшой запас энергии по сравнению с
реагентами, то в ходе реакции теплота будет выделяться. Такие
реакции называются экзотермическими.
Еа – энергия активации
Q – тепловой эффект
5.
Экзотермическими реакциями являются:-
Реакции горения.
Большинство реакций соединения (кроме взаимодействия
азота с кислородом и некоторых других процессов).
Реакции нейтрализации между щелочами и сильными
кислотами.
Реакции активных металлов и их оксидов с водой, а так же
реакции металлов с кислотами.
Экзотермические реакции:
N2(г) + 3H2(г) = 2NH3(г) + 92 кДж
2SO2(г) + О2(г) = 2SO2(г) + 284 кДж
CaO(тв) + H2O(ж) = Ca(OH)2(тв) + 65 кДж
СH4(г) + 2О2(г) = CO2(г) + 2H2О(г) + 891 кДж
6.
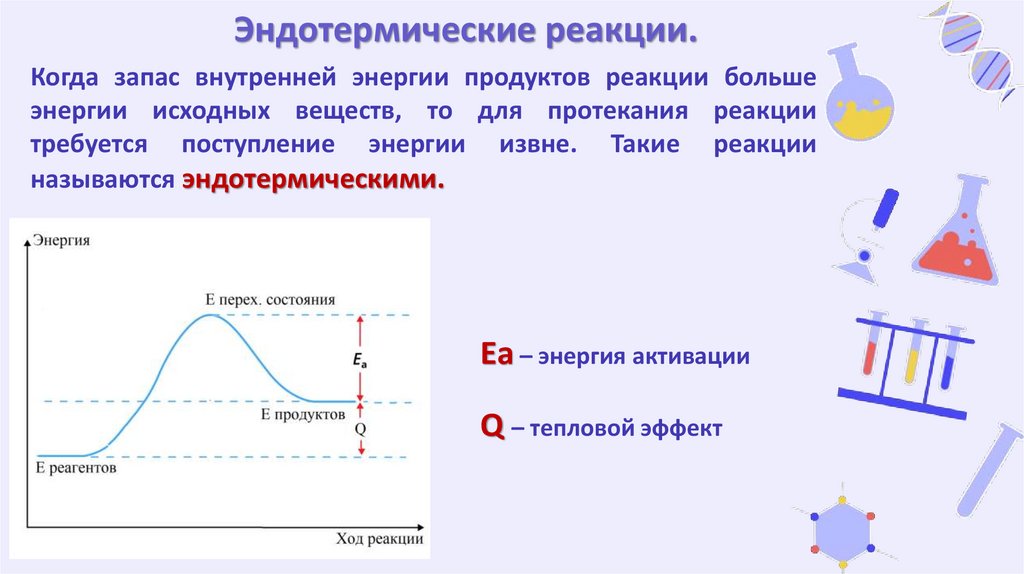
Эндотермические реакции.Когда запас внутренней энергии продуктов реакции больше
энергии исходных веществ, то для протекания реакции
требуется поступление энергии извне. Такие реакции
называются эндотермическими.
Еа – энергия активации
Q – тепловой эффект
7.
Эндотермическими реакциями являются:-
Большинство реакций разложения.
Реакции фотосинтеза.
Примеры эндотермических реакций:
CaCO3(тв) = CaO(тв) + CO2(г) - 157 кДж
2HgO(тв) = 2Hg(тв) + O2(г) - 180 кДж
6CO2(г) + 6H2O(ж) = C6H12O6(тв) + 6O2(г) - 29206 кДж
N2(г) + О2(г) = 2NO(г) - 175 кДж






 chemistry
chemistry








