Similar presentations:
Сердечно-сосудистая система
1.
Сердечно-сосудистая системадоцент кафедры гистологии и
эмбриологии
Ордена Трудового Красного Знамени
Медицинский нститут
им. С.И. Георгиевского
Купша Елена Ивановна
2.
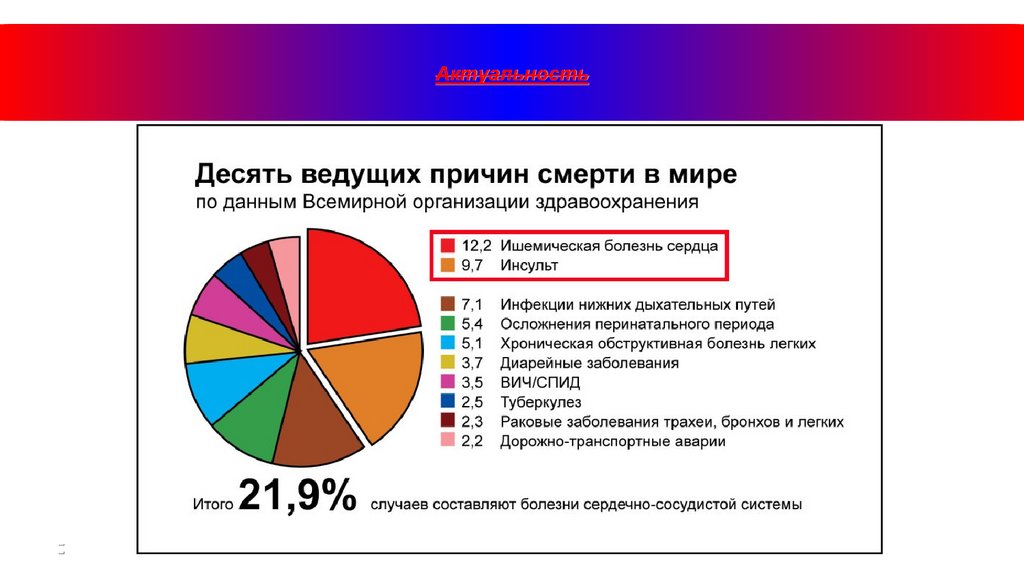
Актуальность3.
РазвитиеПервичный ангиогенез – образование кровяных
островков
в стенке желточного мешка на 3-ей неделе
эмбриогенеза под индуктивным влиянием
входящей в его состав энтодермы.
Дальнейшее развитие отдельных участков сосудистой стенки происходит под влиянием гемодинамических
условий: давления первичной крови, величины его скачков, скорости кровотока, возникающего весового
дисбаланса.
Поэтому различные виды сосудов (аорта, средние и мелкие артерии, капилляры, вены) приобретают те или
Вторичный
ангиогенез
представляет собой рост новых сосудов от уже образованных. Он делится на
иные
особенности
строения.
эмбриональный и постэмбриональный.
постэмбриональный. После того, как в результате первичного ангиогенеза образовался
эндотелий, дальнейшее формирование сосудов идет только за счет вторичного ангиогенеза, то есть путем
отрастания от уже существующих сосудов.
4.
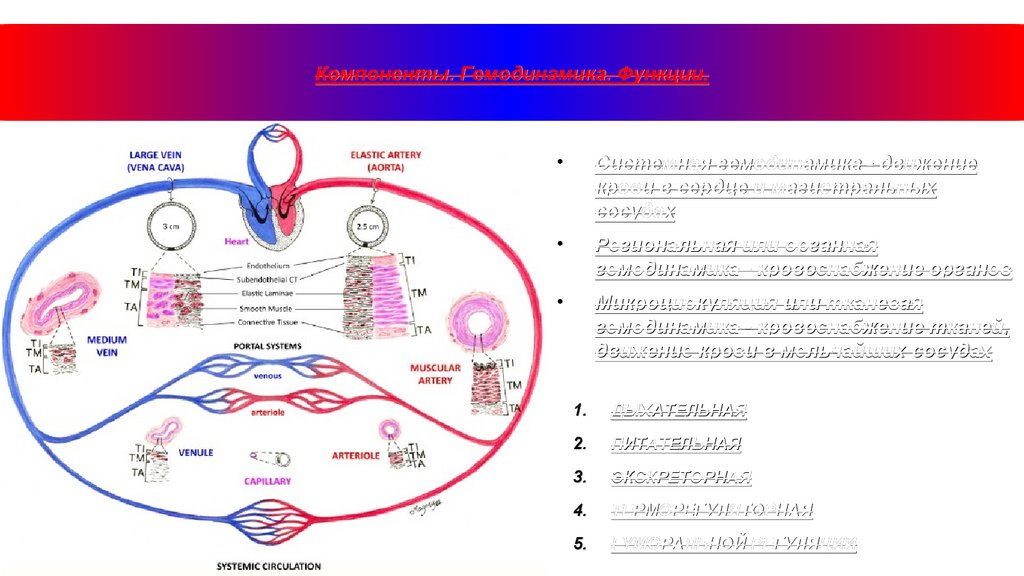
Компоненты. Гемодинамика. Функции.Системная гемодинамика - движение
крови в сердце и магистральных
сосудах
Региональная или органная
гемодинамика - кровоснабжение органов
Микроциркуляция или тканевая
гемодинамика - кровоснабжение тканей,
движение крови в мельчайших сосудах
1.
ДЫХАТЕЛЬНАЯ
2.
ПИТАТЕЛЬНАЯ
3.
ЭКСКРЕТОРНАЯ
4.
ТЕРМОРЕГУЛЯТОРНАЯ
5.
ГУМОРАЛЬНОЙ РЕГУЛЯЦИИ
5.
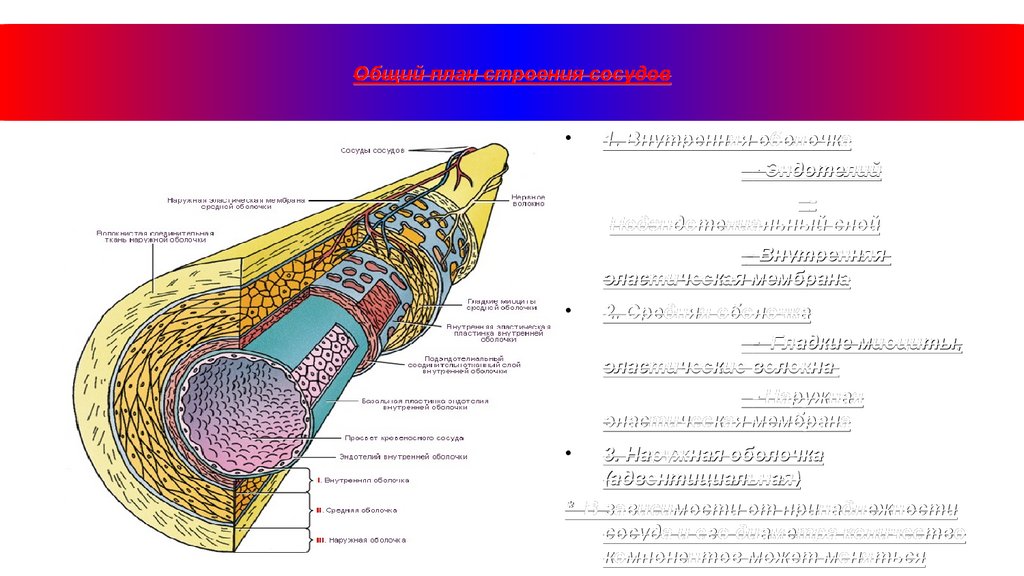
Общий план строения сосудов1. Внутренняя оболочка
- Эндотелий
Подэндотелиальный слой
- Внутренняя
эластическая мембрана
2. Средняя оболочка
- Гладкие миоциты,
эластические волокна
- Наружная
эластическая мембрана
3. Наружная оболочка
(адвентициальная)
* В зависимости от принадлежности
сосуда и его диаметра количество
компонентов может меняться
6.
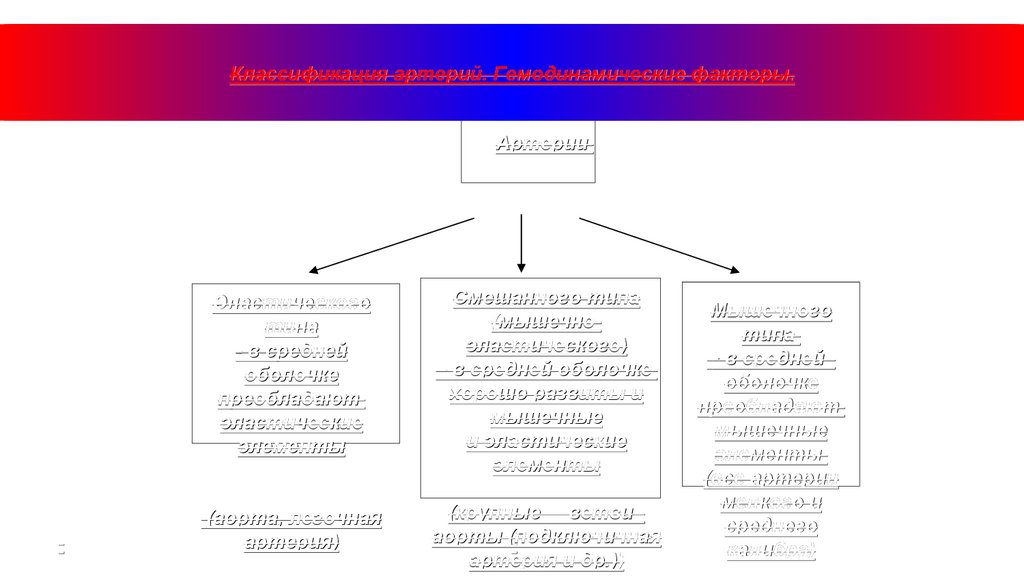
Классификация артерий. Гемодинамические факторы.Артерии
Эластического
типа
- в средней
оболочке
преобладают
эластические
элементы
Смешанного типа
(мышечноэластического)
– в средней оболочке
хорошо развиты и
мышечные
и эластические
элементы
(аорта, легочная
артерия)
(крупные ветви
аорты (подключичная
артерия и др.))
Мышечного
типа
- в средней
оболочке
преобладают
мышечные
элементы
(все артерии
мелкого и
среднего
калибра)
7.
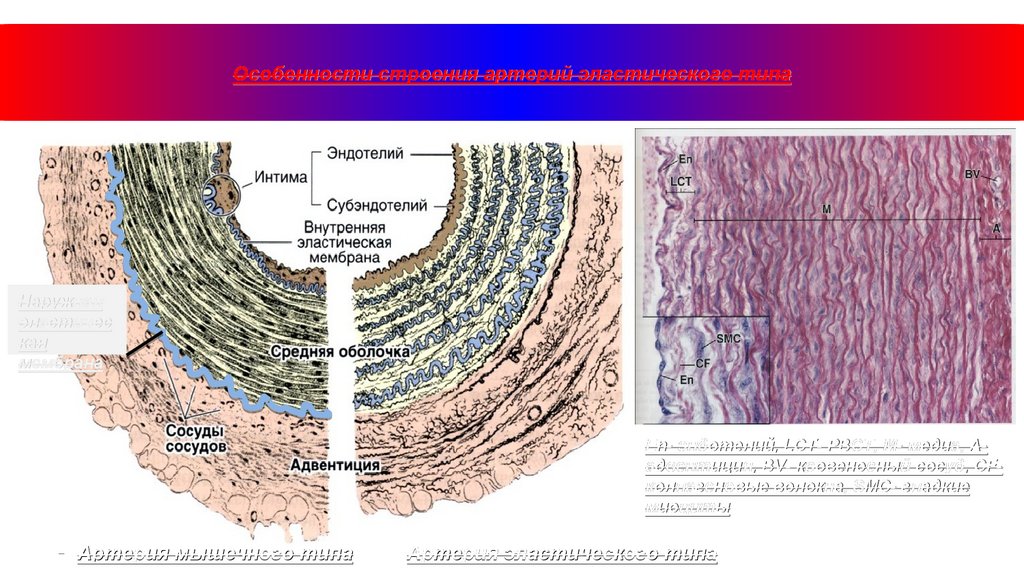
Особенности строения артерий эластического типаНаружная
эластичес
кая
мембрана
En- эндотелий, LCT- РВСТ, М- медиа, Аадвентиция, BV- кровеносный сосуд, CFколлагеновые волокна, SMC- гладкие
миоциты
Артерия мышечного типа
Артерия эластического типа
8.
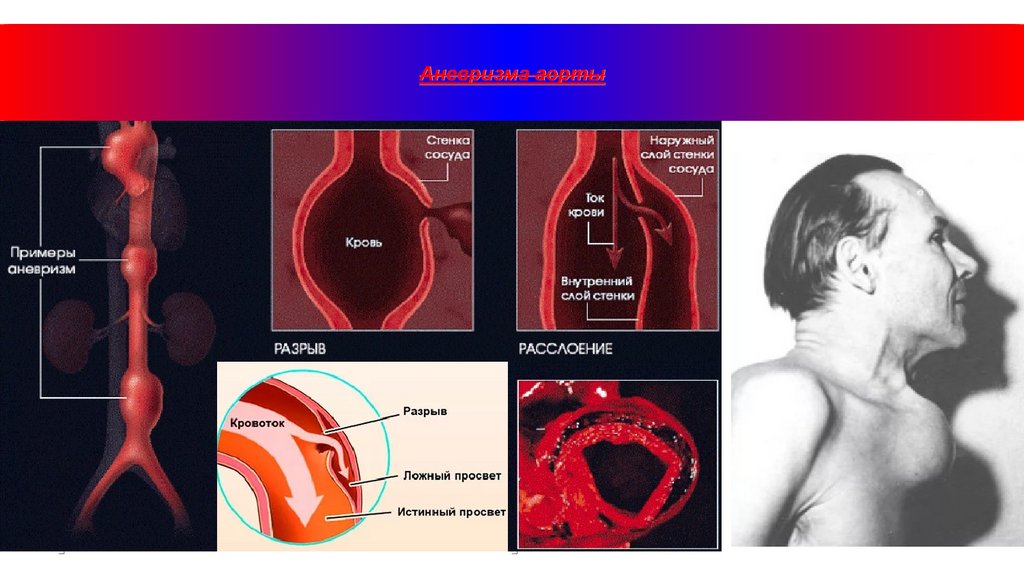
Аневризма аорты9.
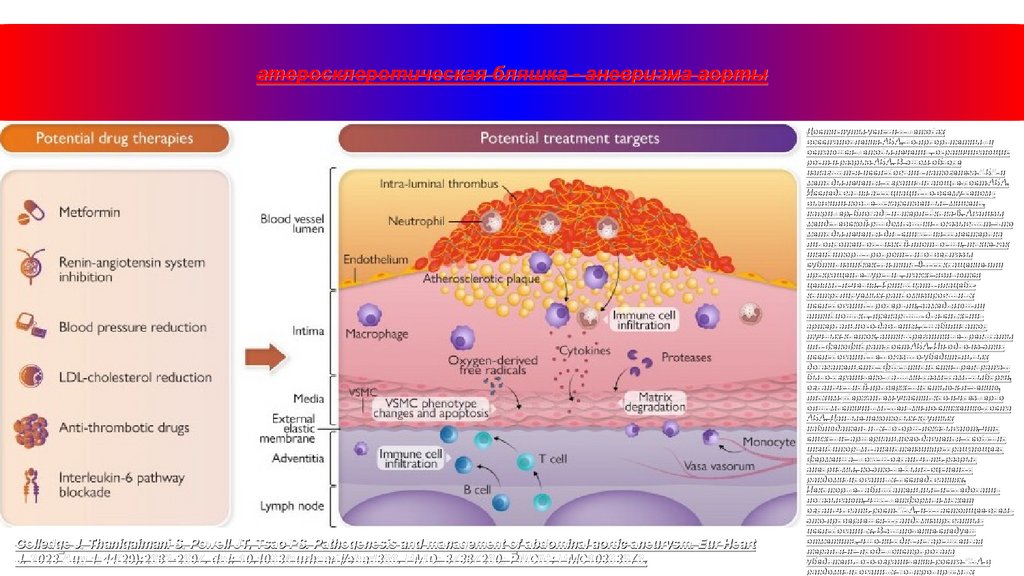
атеросклеротическая бляшка - аневризма аортыGolledge J, Thanigaimani S, Powell JT, Tsao PS. Pathogenesis and management of abdominal aortic aneurysm. Eur Heart
J. 2023 Aug 1;44(29):2682-2697. doi: 10.1093/eurheartj/ehad386. PMID: 37387260; PMCID: PMC10393073.
Достигнуты успехи в методах
восстановления АБА, но приоритетными
остаются методы лечения, ограничивающие
рост и разрыв АБА. В этом обзоре
излагаются исследования патогенеза АБА и
методы лечения, ограничивающие рост АБА.
Исследования ассоциаций по всему геному
выявили новые лекарственные мишени,
например, блокаду интерлейкина-6. Анализы
менделевской рандомизации показывают, что
методы лечения для снижения холестерина
липопротеинов низкой плотности, такие как
ингибиторы пропротеинконвертазы
субтилизин/кексин типа 9 и сокращение или
прекращение курения, также являются
целями лечения. Тринадцать плацебоконтролируемых рандомизированных
исследований проверяли, замедляют ли
антибиотики, препараты для снижения
артериального давления, стабилизатор
тучных клеток, антиагрегантные препараты
или фенофибрат рост АБА. Ни одно из этих
исследований не показало убедительных
доказательств эффективности препарата и
было ограничено малыми размерами выборки,
ограниченной приверженностью к лечению,
плохим удержанием участников и чрезмерно
оптимистичными целями по снижению роста
АБА. Данные некоторых крупных
наблюдательных когорт показывают, что
снижение артериального давления, особенно
ингибиторами ангиотензинпревращающего
фермента, может ограничить разрыв
аневризмы, но это не было оценено в
рандомизированных исследованиях.
Некоторые наблюдательные исследования
показывают, что метформин может
ограничивать рост АБА, и в настоящее время
это проверяется в рандомизированных
исследованиях. В заключение следует
отметить, что ни одна лекарственная
терапия не продемонстрировала
убедительного ограничения роста АБА в
рандомизированных контролируемых
10.
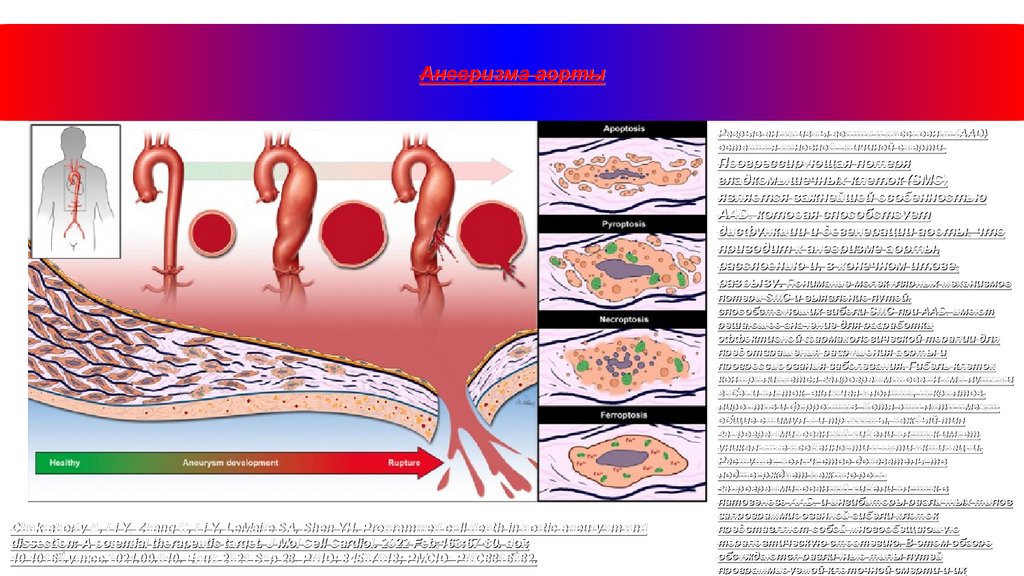
Аневризма аортыРазрыв аневризмы аорты и расслоение (AAD)
остается основной причиной смерти.
Прогрессирующая потеря
гладкомышечных клеток (SMC)
является важнейшей особенностью
AAD, которая способствует
дисфункции и дегенерации аорты, что
приводит к аневризме аорты,
расслоению и, в конечном итоге,
разрыву. Понимание молекулярных механизмов
Chakraborty A, Li Y, Zhang C, Li Y, LeMaire SA, Shen YH. Programmed cell death in aortic aneurysm and
dissection: A potential therapeutic target. J Mol Cell Cardiol. 2022 Feb;163:67-80. doi:
10.1016/j.yjmcc.2021.09.010. Epub 2021 Sep 28. PMID: 34597613; PMCID: PMC8816882.
потери SMC и выявление путей,
способствующих гибели SMC при AAD, имеют
решающее значение для разработки
эффективной фармакологической терапии для
предотвращения разрушения аорты и
прогрессирования заболевания. Гибель клеток
контролируется запрограммированными путями
гибели клеток, включая апоптоз, некроптоз,
пироптоз и ферроптоз. Хотя эти пути имеют
общие стимулы и триггеры, каждый тип
запрограммированной гибели клеток имеет
уникальные особенности и пути активации.
Растущее количество доказательств
подтверждает важную роль
запрограммированной гибели клеток в
патогенезе AAD, и ингибиторы различных типов
запрограммированной гибели клеток
представляют собой многообещающую
терапевтическую стратегию. В этом обзоре
обсуждаются различные типы путей
программируемой клеточной смерти и их
11.
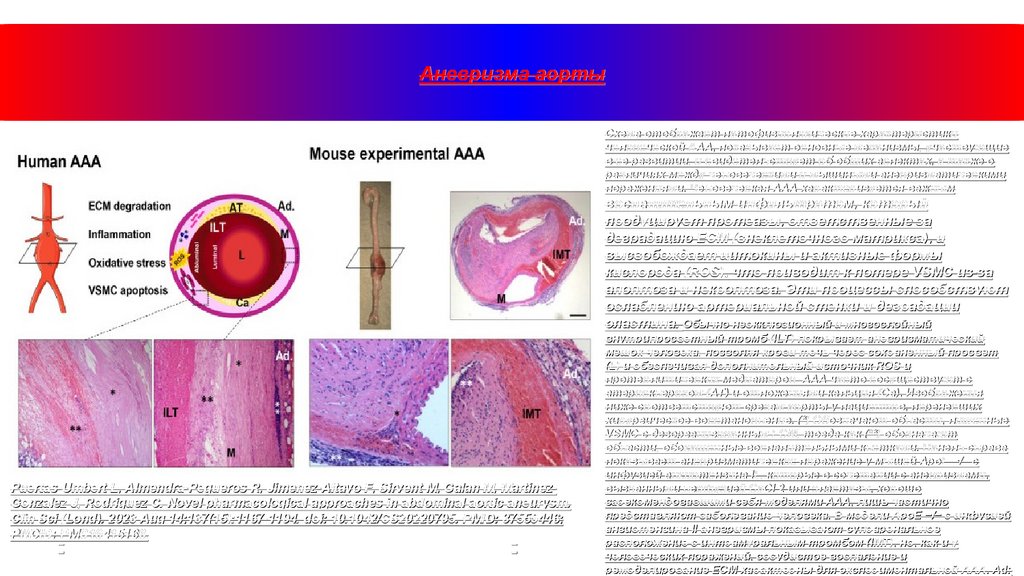
Аневризма аортыСхема отображает патофизиологические характеристики
человеческой ААА, показывает основные механизмы, участвующие
в ее развитии, и свидетельствует об общих аспектах, а также о
различиях между человеческими и мышиными аневризматическими
поражениями. Человеческая ААА характеризуется важным
воспалительным инфильтратом, который
продуцирует протеазы, ответственные за
деградацию ECM (внеклеточного матрикса), и
высвобождает цитокины и активные формы
кислорода (ROS), что приводит к потере VSMC из-за
апоптоза и некроптоза. Эти процессы способствуют
ослаблению артериальной стенки и деградации
эластина. Обычно неокклюзионный и многослойный
Puertas-Umbert L, Almendra-Pegueros R, Jimenez-Altayo F, Sirvent M, Galan M, MartinezGonzalez J, Rodriguez C. Novel pharmacological approaches in abdominal aortic aneurysm.
Clin Sci (Lond). 2023 Aug 14;137(15):1167-1194. doi: 10.1042/CS20220795. PMID: 37559446;
PMCID: PMC10415166.
внутрипросветный тромб (ILT) покрывает аневризматический
мешок человека, позволяя крови течь через сохраненный просвет
(L) и обеспечивая дополнительный источник ROS и
протеолитических медиаторов. AAA часто сосуществуют с
атеросклерозом (AT) и отложениями кальция (Ca). Изображения
ниже соответствуют срезам аорты у пациентов, перенесших
хирургическое восстановление. (*) Обозначают области, лишенные
VSMC с дезорганизованным ECM, тогда как (**) обозначают
области, обогащенные воспалительными клетками. Панель справа
показывает аневризматическое поражение у мышей ApoE −/− с
инфузией ангиотензина II , которые в сочетании с аневризмами,
вызванными перфузией CaCl 2 или эластазы, хорошо
зарекомендовавшими себя моделями AAA, лишь частично
представляют заболевание человека. В модели ApoE −/− с инфузией
ангиотензина II аневризмы показывают супраренальное
расположение с интрамуральным тромбом (IMT), но, как и у
человеческих поражений, сосудистое воспаление и
ремоделирование ECM характерны для экспериментальной AAA. Ad:
12.
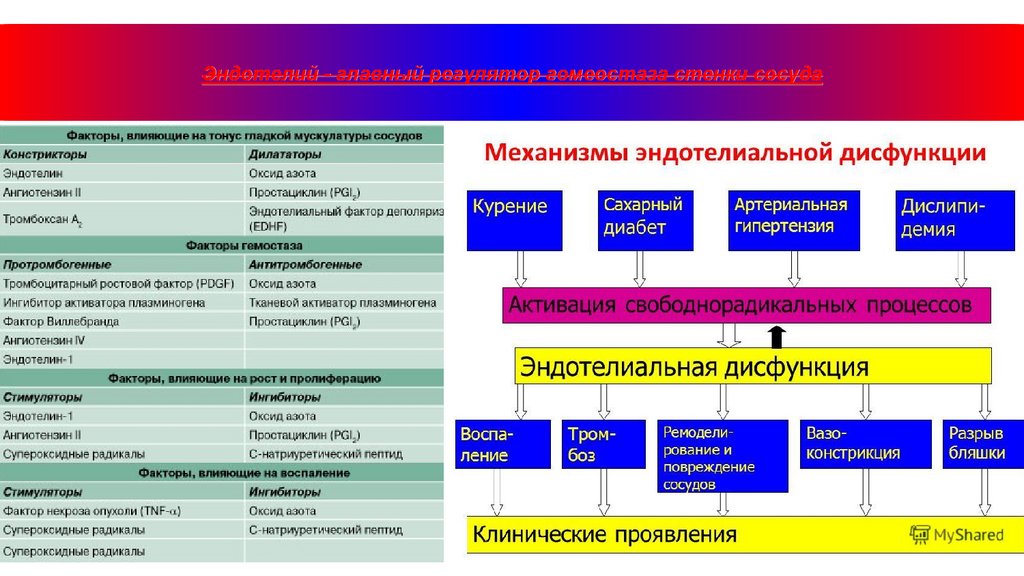
Эндотелий - главный регулятор гомеостаза стенки сосуда13.
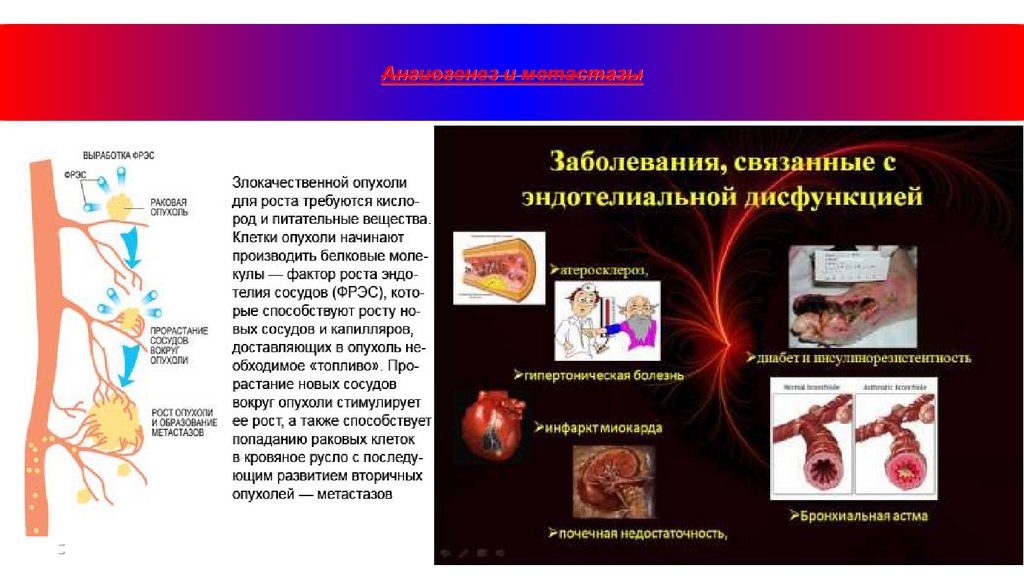
Ангиогенез и метастазы14.
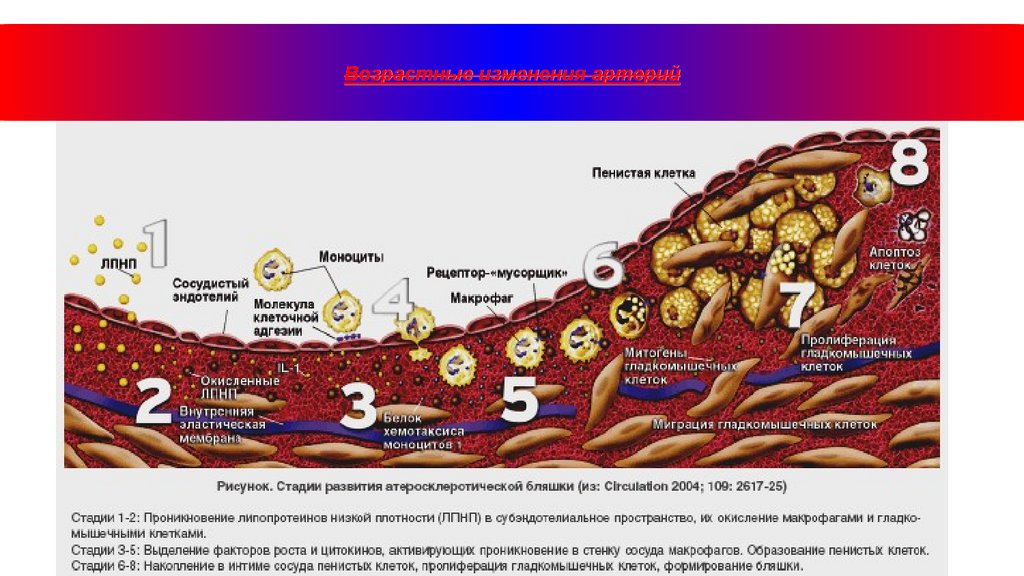
Возрастные изменения артерий15.
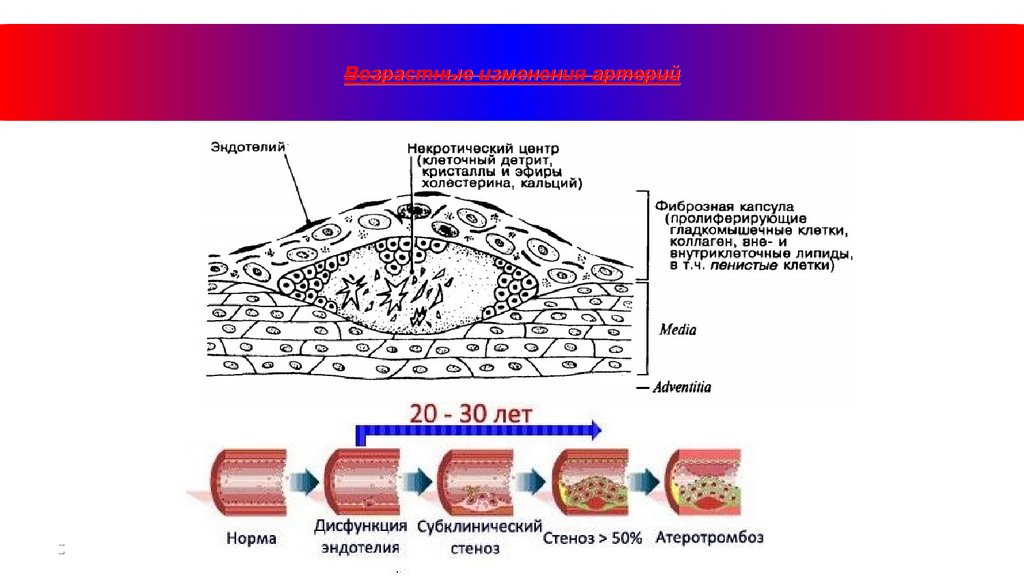
Возрастные изменения артерий16.
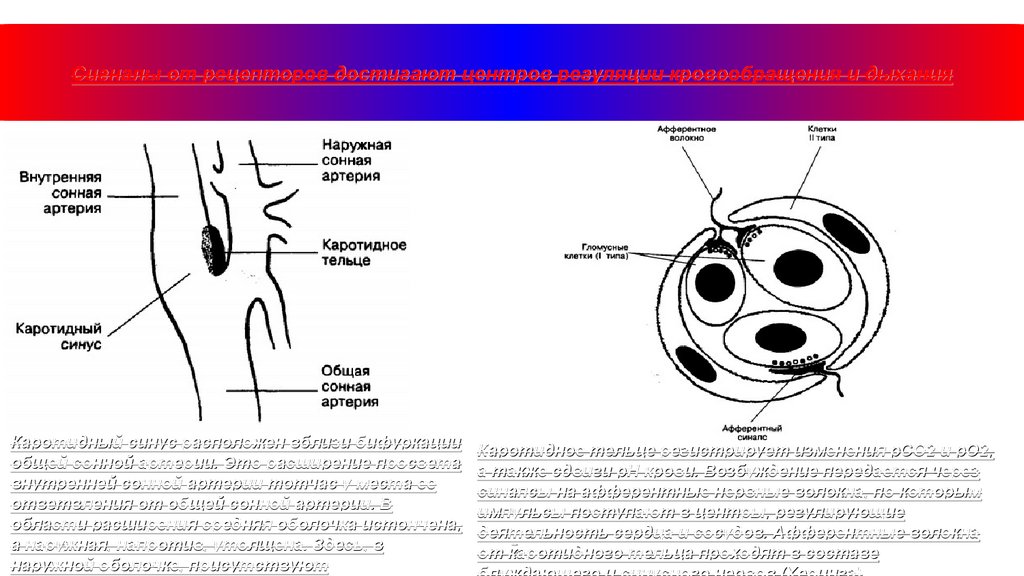
Сигналы от рецепторов достигают центров регуляции кровообращения и дыханияКаротидный синус расположен вблизи бифуркации
общей сонной артерии. Это расширение просвета
внутренней сонной артерии тотчас у места ее
ответвления от общей сонной артерии. В
области расширения средняя оболочка истончена,
а наружная, напротив, утолщена. Здесь, в
наружной оболочке, присутствуют
Каротидное тельце регистрирует изменения рСО2 и рО2,
а также сдвиги рН крови. Возбуждение передается через
синапсы на афферентные нервные волокна, по которым
импульсы поступают в центры, регулирующие
деятельность сердца и сосудов. Афферентные волокна
от каротидного тельца проходят в составе
17.
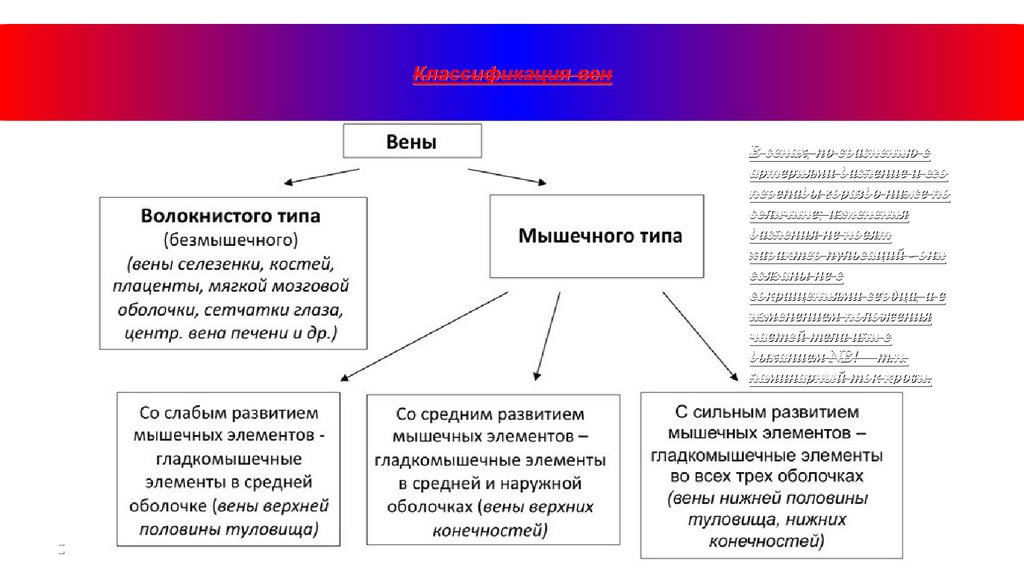
Классификация венВ венах, по сравнению с
артериями давление и его
перепады гораздо ниже по
величине; изменения
давления не носят
характер пульсаций - они
связаны не с
сокращениями сердца, а с
изменением положения
частей тела или с
дыханием NB! – т.н.
ламинарный ток крови.
крови.
18.
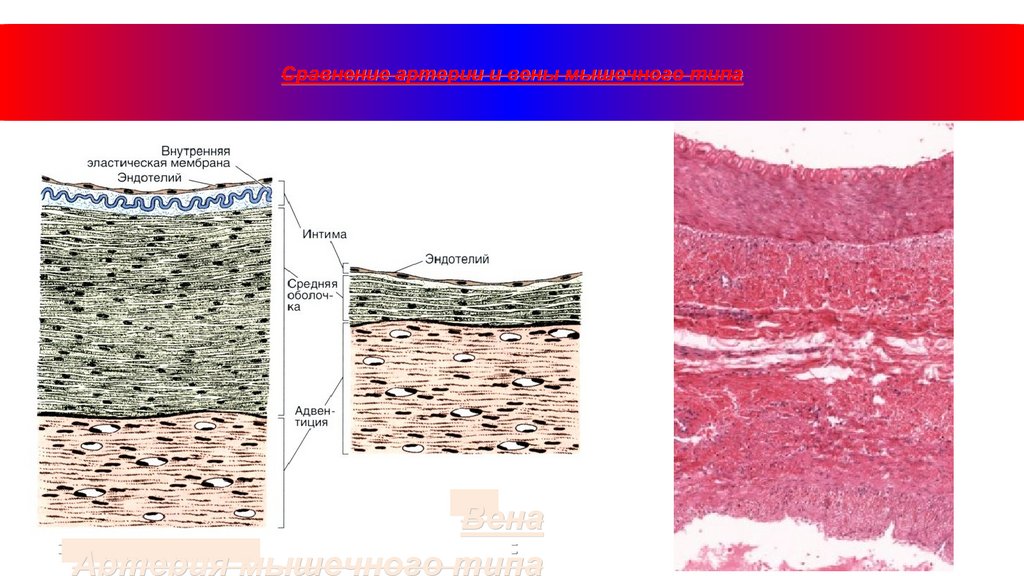
Сравнение артерии и вены мышечного типаВена
Артерия мышечного типа
19.
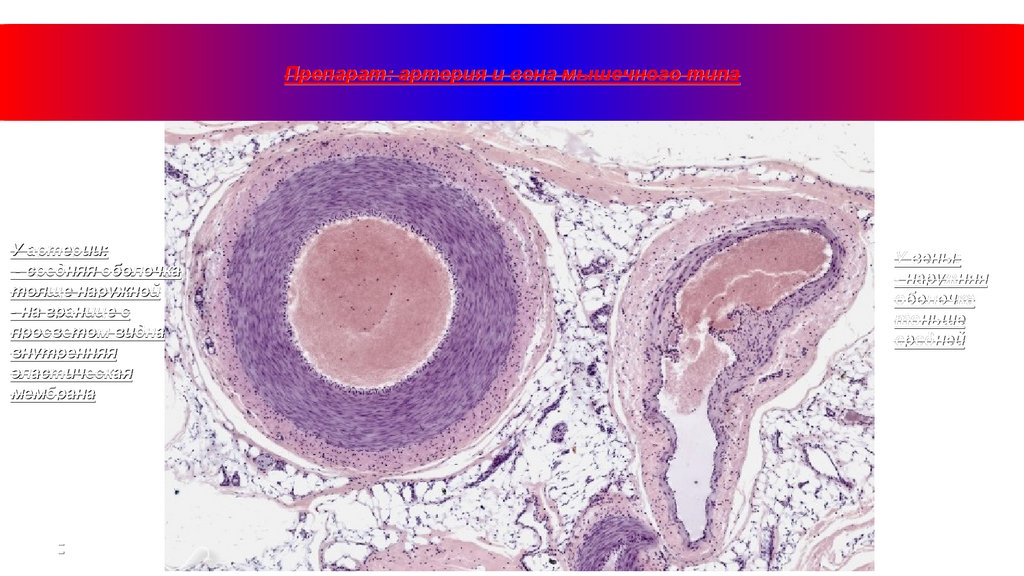
Препарат: артерия и вена мышечного типаУ артерии:
- средняя оболочка
толще наружной
- на границе с
просветом видна
внутренняя
эластическая
мембрана
У вены:
- наружняя
оболочка
тоньше
средней
20.
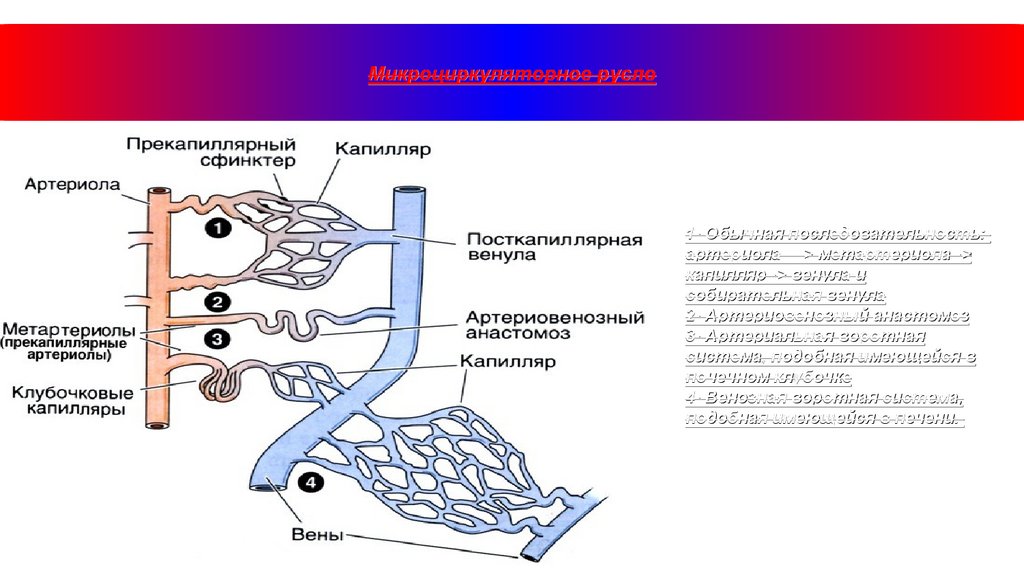
Микроциркуляторное русло1- Обычная последовательность:
артериола —> метартериола ->
капилляр -> венула и
собирательная венула
2- Артериовенозный анастомоз
3- Артериальная воротная
система, подобная имеющейся в
почечном клубочке
4- Венозная воротная система,
подобная имеющейся в печени.
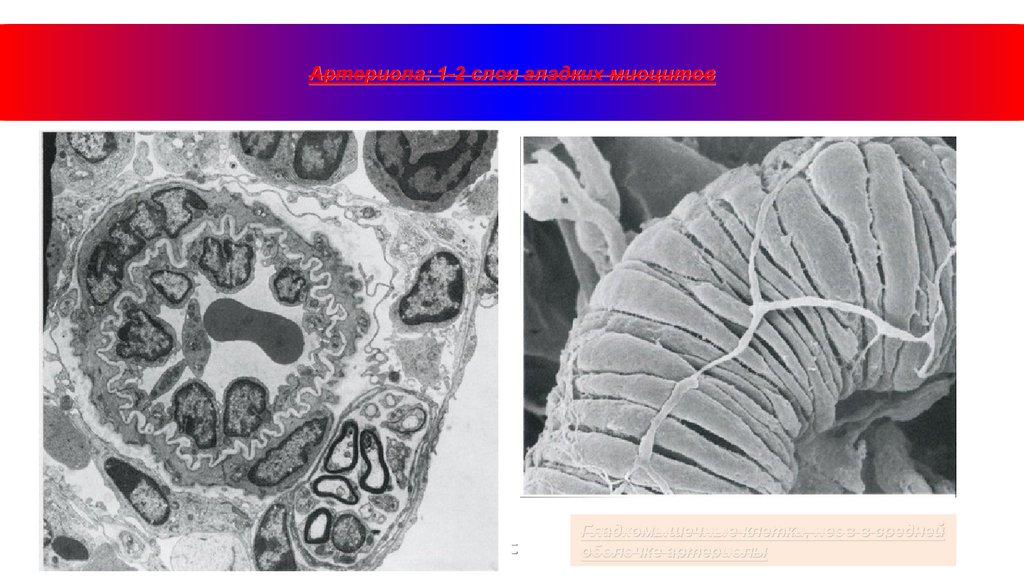
21.
Артериола: 1-2 слоя гладких миоцитовГладкомышечные клетки, нерв в средней
оболочке артериолы
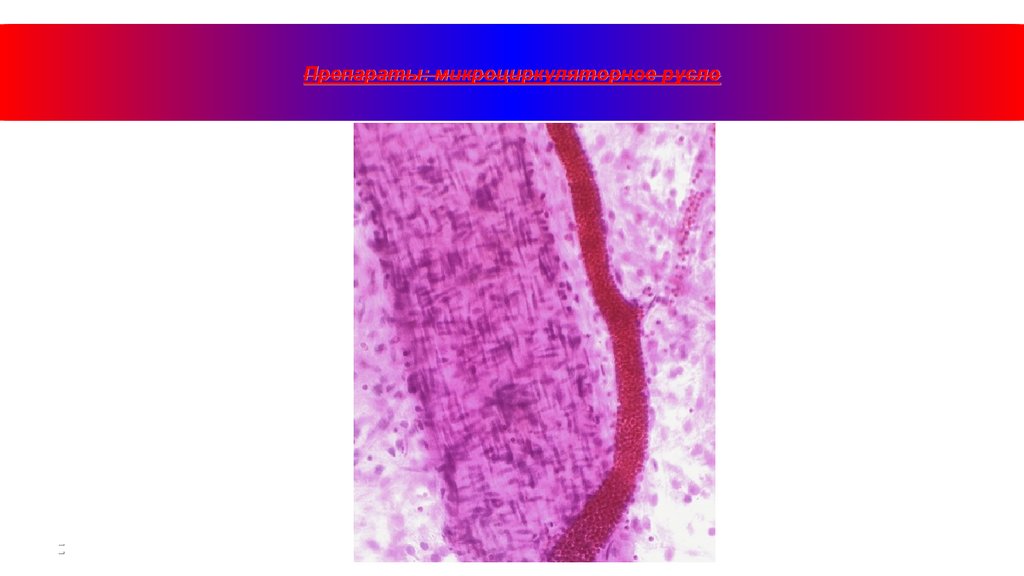
22.
Препараты: микроциркуляторное русло23.
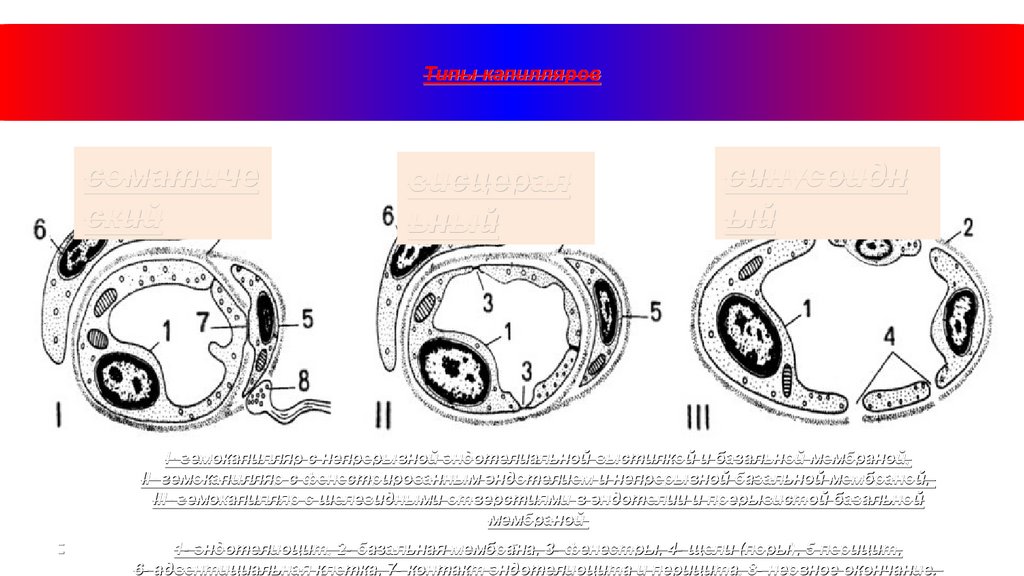
Типы капилляровсоматиче
ский
висцерал
ьный
синусоидн
ый
I- гемокапилляр с непрерывной эндотелиальной выстилкой и базальной мембраной,
II- гемокапилляр с фенестрированным эндотелием и непрерывной базальной мембраной,
III- гемокапилляр с шелевидными отверстиями в эндотелии и прерывистой базальной
мембраной
1- эндотелиоцит, 2- базальная мембрана, 3- фенестры, 4- щели (поры), 5 перицит,
6- адвентициальная клетка, 7- контакт эндотелиоцита и перицита, 8- нервное окончание.
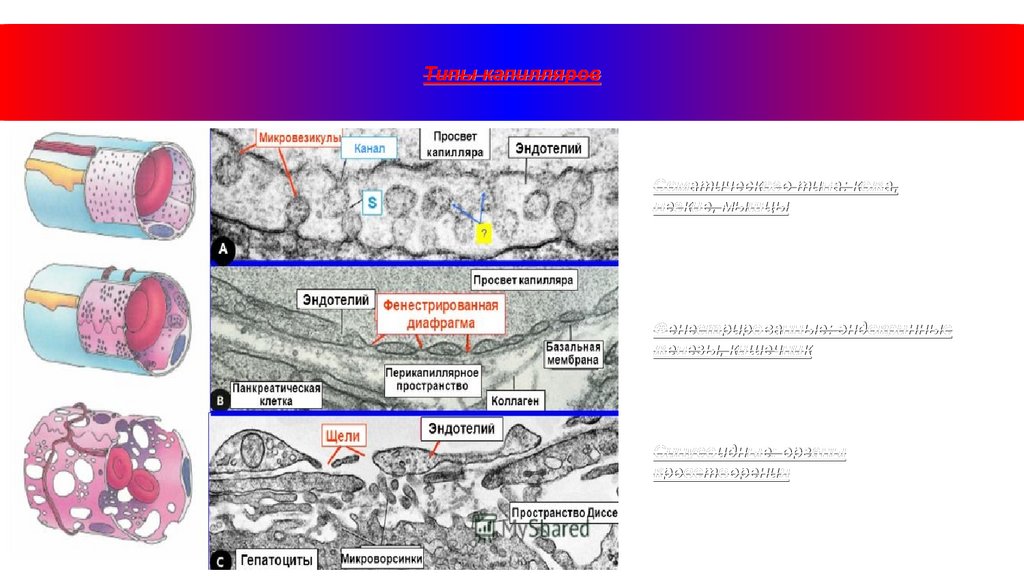
24.
Типы капилляровСоматического типа: кожа,
легкие, мышцы
Фенестрированные: эндокринные
железы, кишечник
Синусоидные: органы
кроветворения
25.
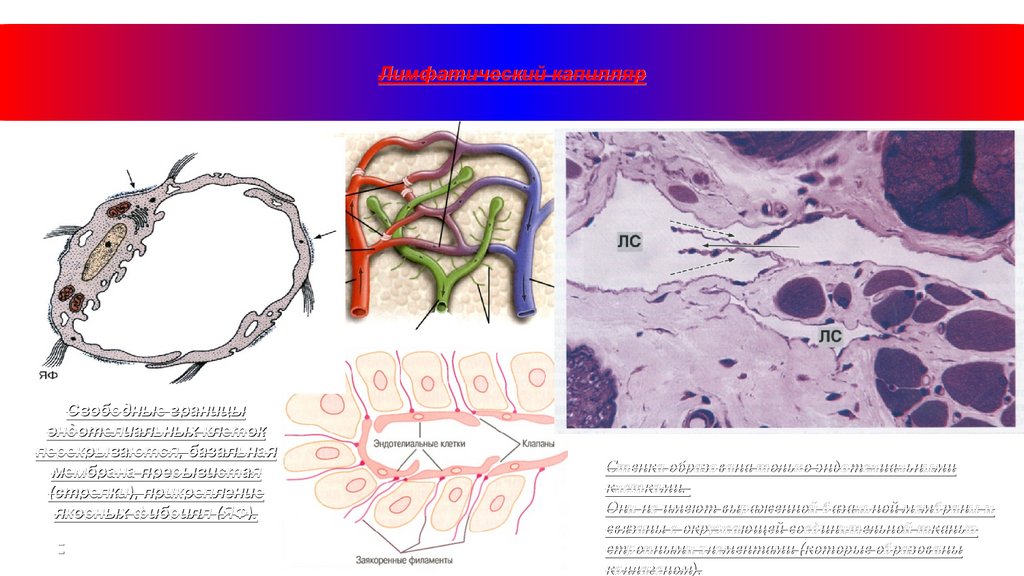
Лимфатический капиллярCвободные границы
эндотелиальных клеток
перекрываются, базальная
мембрана прерывистая
(стрелки), прикрепление
якорных фибрилл (ЯФ).
Стенка образована только эндотелиальными
клетками.
Они не имеют выраженной базальной мембраны и
связаны с окружающей соединительной тканью
стропными элементами (которые образованы
коллагеном).
26.
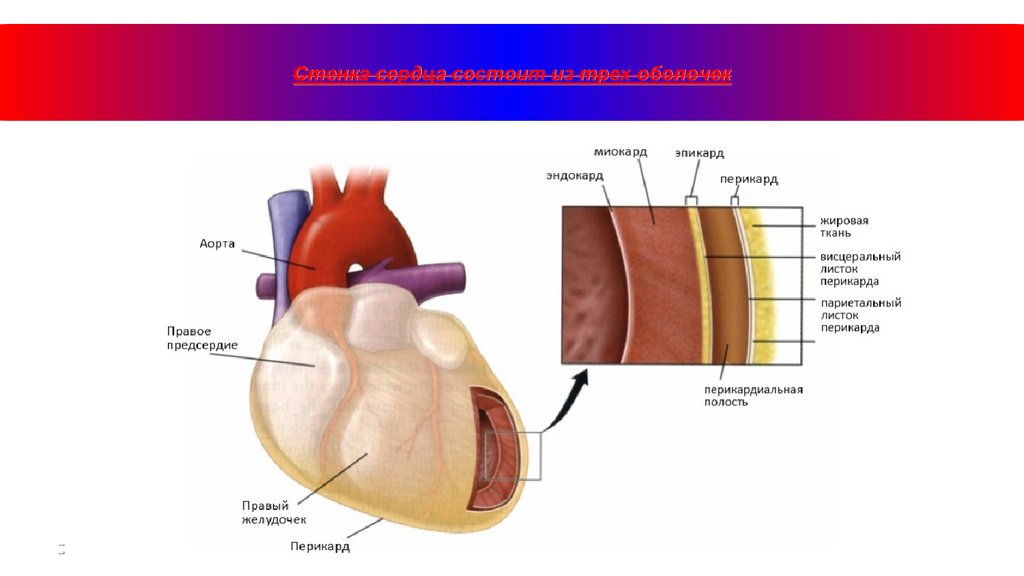
Стенка сердца состоит из трех оболочек27.
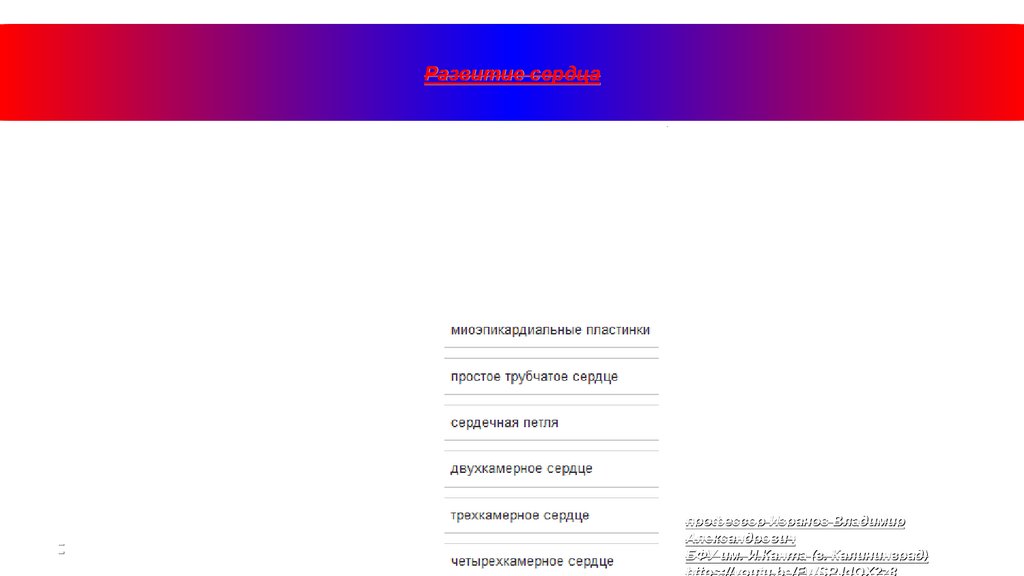
Развитие сердцапрофессор Изранов Владимир
Александрович
БФУ им. И.Канта (г. Калининград)
28.
Развитие сердца, этапы с риском основных 6 аномалий29.
Развитие сердца, этапы с риском аномалий30.
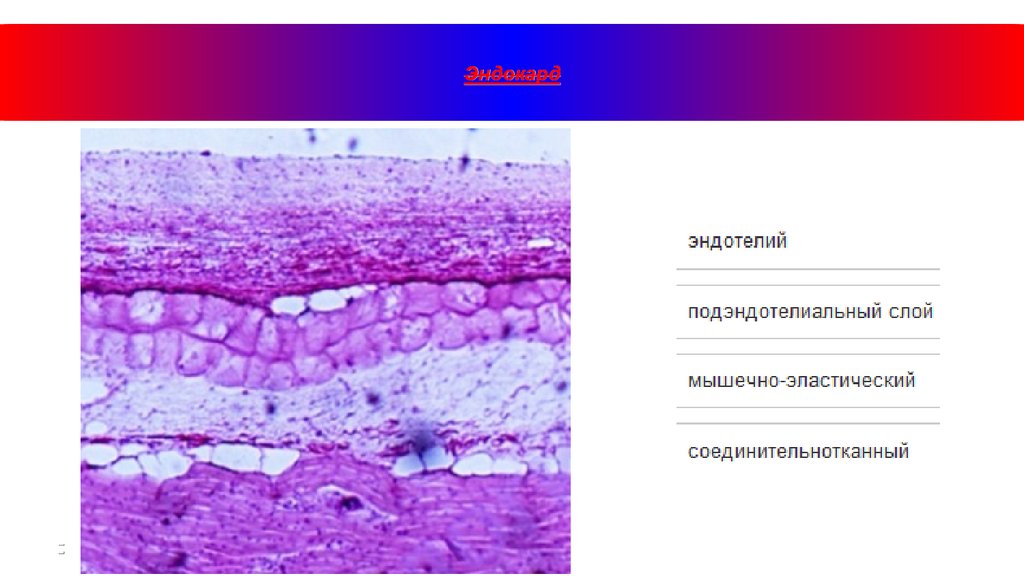
Эндокард31.
Типы кардиомиоцитов32.
Сократительные кардиомиоциты33.
Сократительные кардиомиоциты34.
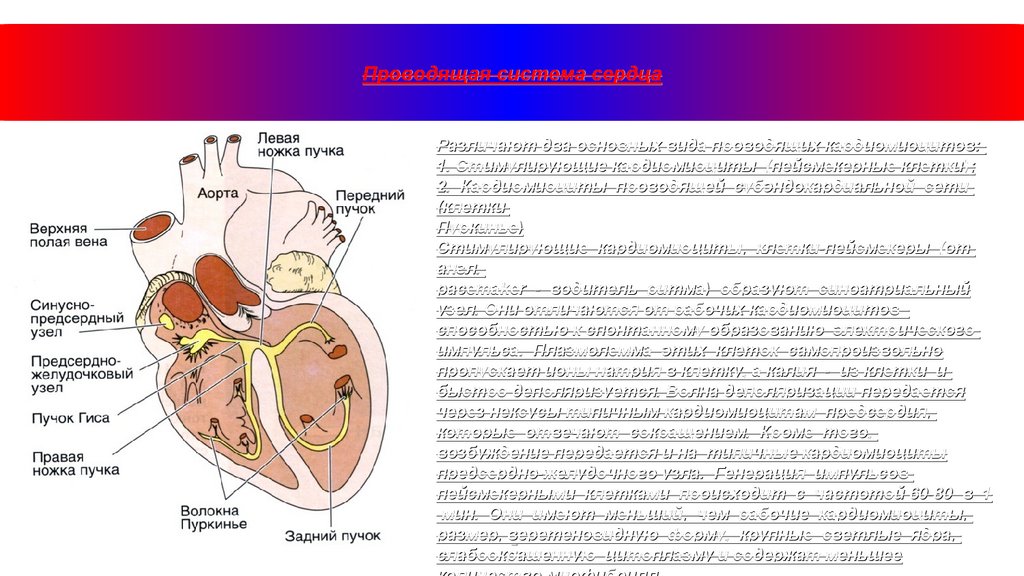
Проводящая система сердцаРазличают два основных вида проводящих кардиомиоцитов:
1. Стимулирующие кардиомиоциты (пейсмекерные клетки);
клетки);
2. Кардиомиоциты проводящей субэндокардиальной сети
(клетки
Пуркинье)
Стимулирующие кардиомиоциты, клетки-пейсмекеры (от
англ.
pacemaker - водитель ритма) образуют синоатриальный
узел. Они отличаются от рабочих кардиомиоцитов
способностью к спонтанному образованию электрического
импульса. Плазмолемма этих клеток самопроизвольно
пропускает ионы натрия в клетку, а калия - из клетки и
быстро деполяризуется. Волна деполяризации передается
через нексусы типичным кардиомиоцитам предсердия,
которые отвечают сокращением. Кроме того,
возбуждение передается и на типичные кардиомиоциты
предсердно-желудочного узла. Генерация импульсов
пейсмекерными клетками происходит с частотой 60-80 в 1
мин. Они имеют меньший, чем рабочие кардиомиоциты,
размер, веретеновидную форму, крупные светлые ядра,
слабоокрашенную цитоплазму и содержат меньшее
35.
Проводящая система сердцаКлетки атриовентрикулярного узла образованы
совокупностью кардиомиоцитов, похожих на
пейсмекерные клетки, но содержат больше
миофибрилл. Друг с другом они связаны как при
помощи простых контактов, так и вставочных
дисков. Функция проводящих сердечных волокон
состоит в передаче возбуждения на рабочие
кардиомиоциты, а также на второй вид атипичных
кардиомиоцитов – кардиомиоциты проводящей
субэндокардиальной сети Пуркинье.
Кардиомиоциты атриовентрикулярного узла также
способны самостоятельно генерировать
электрические импульсы, частота которых, однако,
ниже, чем частота импульсов, генерируемых
пейсмекерными клетками, и составляет 30-40 в мин.
36.
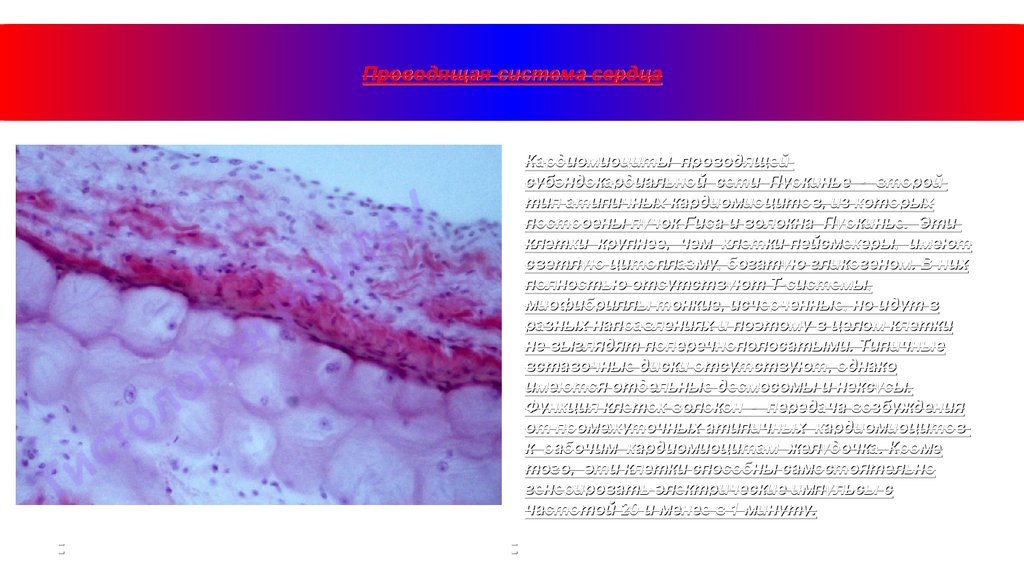
Проводящая система сердцаКардиомиоциты проводящей
субэндокардиальной сети Пуркинье - второй
тип атипичных кардиомиоцитов, из которых
построены пучок Гиса и волокна Пуркинье. Эти
клетки крупнее, чем клетки-пейсмекеры, имеют
светлую цитоплазму, богатую гликогеном. В них
полностью отсутствуют Т-системы,
миофибриллы тонкие, исчерченные, но идут в
разных направлениях и поэтому в целом клетки
не выглядят поперечнополосатыми. Типичные
вставочные диски отсутствуют, однако
имеются отдельные десмосомы и нексусы.
Функция клеток-волокон - передача возбуждения
от промежуточных атипичных кардиомиоцитов
к рабочим кардиомиоцитам желудочка. Кроме
того, эти клетки способны самостоятельно
генерировать электрические импульсы с
частотой 20 и менее в 1 минуту.
37.
Секреторные предсердные кардиомиоцитыЭти отростчатые клетки находятся преимущественно в
правом предсердии и ушках сердца. В клетках содержится
небольшое количество митохондрий, меньше, чем в
рабочих, миофибрилл и саркоплазматической сети, однако
хорошо развиты грЭПС и комплекс Гольджи. В гранулах
содержится натрийуретический фактор (НУФ).
(НУФ). Он
выделяется в кровь тогда, когда в предсердие поступает
большое количество крови, т.е. при угрозе повышения АД.
Выделившись в кровь, этот гормон действует на канальцы
почек, препятствуя обратной реабсорбции натрия в кровь из
первичной мочи.
мочи. При этом в почках вместе с натрием из
организма выделяется вода, что ведет к уменьшению объема
циркулирующей жидкости и падению АД.
АД. Одновременно НУФ
приводит к расширению сосудов,
сосудов, а также к угнетению
секреции гормонов,
гормонов, повышающих артериальное давление:
альдостерона и кортизола надпочечниками, вазопрессина
ядрами переднего гипоталамуса.
гипоталамуса. Кроме того, в гранулах
секреторных кардиомиоцитов находится вещество,
снижающее свертываемость крови.
крови. Следовательно,
секреторные кардиомиоциты выделяют гормоны,
являющиеся внутрисистемными факторами
ауторегуляции, т.к. регулируют АД и вязкость крови,
38.
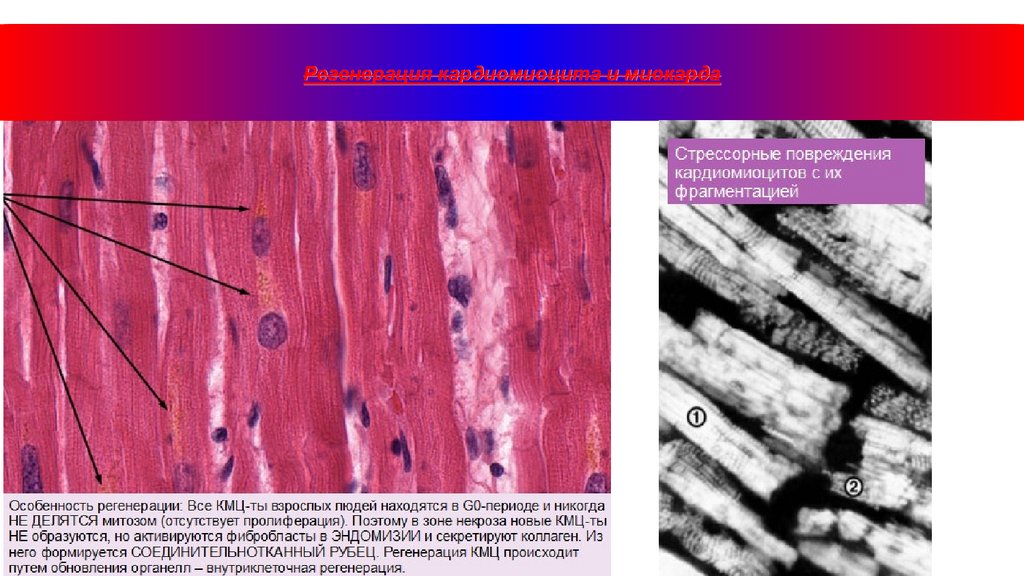
Регенерация кардиомиоцита и миокарда39.
Мышечная ткань40.
Хроническое и острое повреждение миокарда41.
гликолиз - митозИнгибирование СДГ малонатом способствует пролиферации
взрослых кардиомиоцитов, реваскуляризации и регенерации сердца
посредством метаболического перепрограммирования. Эти
результаты поддерживают потенциально важный новый
терапевтический подход к сердечной недостаточности человека.
Введение конкурентного ингибитора SDH, malonate, предотвращает
накопление succinate и последующую метаболизацию, которая
увеличивает уровни ROS (переключение с гликолиза на
окислительное фосфорилирование) во время
ишемического/реперфузионного повреждения.
SDH играет важную роль в метаболизме и активности клеточного
цикла, т.к. это первый митохондриальный белок,
идентифицированный как опухолевой супрессор. Мутации в SDH при
синдромах семейного рака способствуют метаболическому сдвигу в
сторону гликолиза, который управляет клеточным делением.
Bae J, Salamon RJ, Brandt EB, Paltzer WG, Zhang Z, Britt EC, Hacker TA, Fan J, Mahmoud AI. Malonate
Promotes Adult Cardiomyocyte Proliferation and Heart Regeneration. Circulation. 2021 May
18;143(20):1973-1986. doi: 10.1161/CIRCULATIONAHA.120.049952. Epub 2021 Mar 5. PMID: 33666092;
PMCID: PMC8131241.
42.
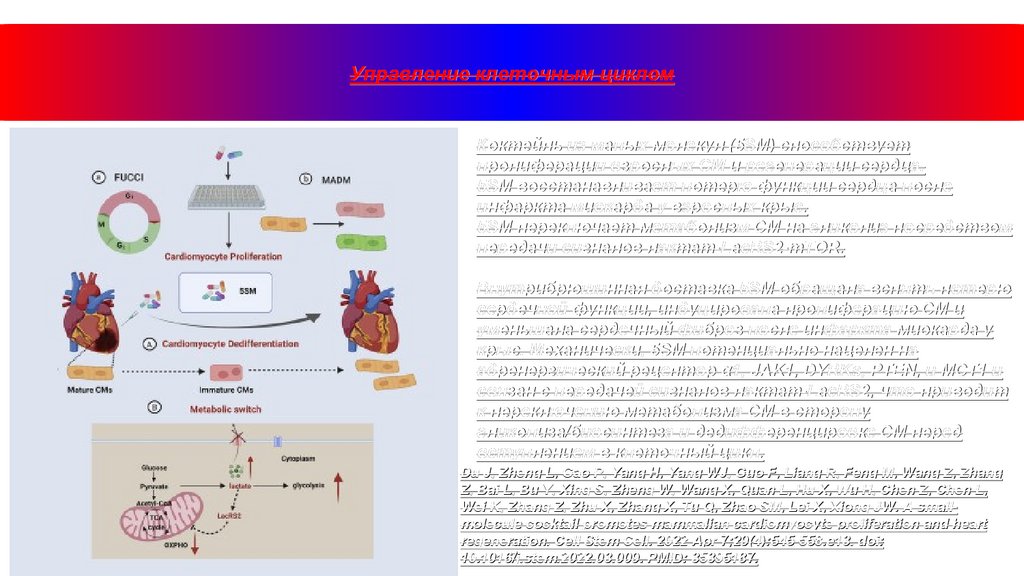
Управление клеточным цикломКоктейль из малых молекул (5SM) способствует
пролиферации взрослых CM и регенерации сердца.
5SM восстанавливает потерю функции сердца после
инфаркта миокарда у взрослых крыс.
5SM переключает метаболизм CM на гликолиз посредством
передачи сигналов лактат-LacRS2-mTOR.
Внутрибрюшинная доставка 5SM обращала вспять потерю
сердечной функции, индуцировала пролиферацию CM и
уменьшала сердечный фиброз после инфаркта миокарда у
крыс. Механически, 5SM потенциально нацелен на
адренергический рецептор α1, JAK1, DYRKs, PTEN, и MCT1 и
связан с передачей сигналов лактат-LacRS2, что приводит
к переключению метаболизма CM в сторону
гликолиза/биосинтеза и дедифференцировке CM перед
вступлением в клеточный цикл.
Du J, Zheng L, Gao P, Yang H, Yang WJ, Guo F, Liang R, Feng M, Wang Z, Zhang
Z, Bai L, Bu Y, Xing S, Zheng W, Wang X, Quan L, Hu X, Wu H, Chen Z, Chen L,
Wei K, Zhang Z, Zhu X, Zhang X, Tu Q, Zhao SM, Lei X, Xiong JW. A smallmolecule cocktail promotes mammalian cardiomyocyte proliferation and heart
regeneration. Cell Stem Cell. 2022 Apr 7;29(4):545-558.e13. doi:
10.1016/j.stem.2022.03.009. PMID: 35395187.
43.
Тесты: Сердце,микроциркуляторное русло
https://onlinetestpad.com/6fkohjtgesb
le
Сосуды.
https://onlinetestpad.com/6fqmxa6grc
s5o
Лекции д.м.н., профессора
Александра Викторовича Иванова
https://vk.com/kursk_histology
Видеокурс д.м.н., профессора
Алексея Владимировича Павлова
https://vk.com/club226972303
д.м.н.,
д.м.н., профессор Изранов
Владимир Александрович
БФУ им. И.Канта (г.
Калининград)лекия по развитию
сердца и аномалиям
https://youtu.be/FWSPJdQX2z8













 medicine
medicine biology
biology