Similar presentations:
Соли, их классификация и свойства
1. Соли, их классификация и свойства
8 класс2.
3.
4.
5.
6.
7.
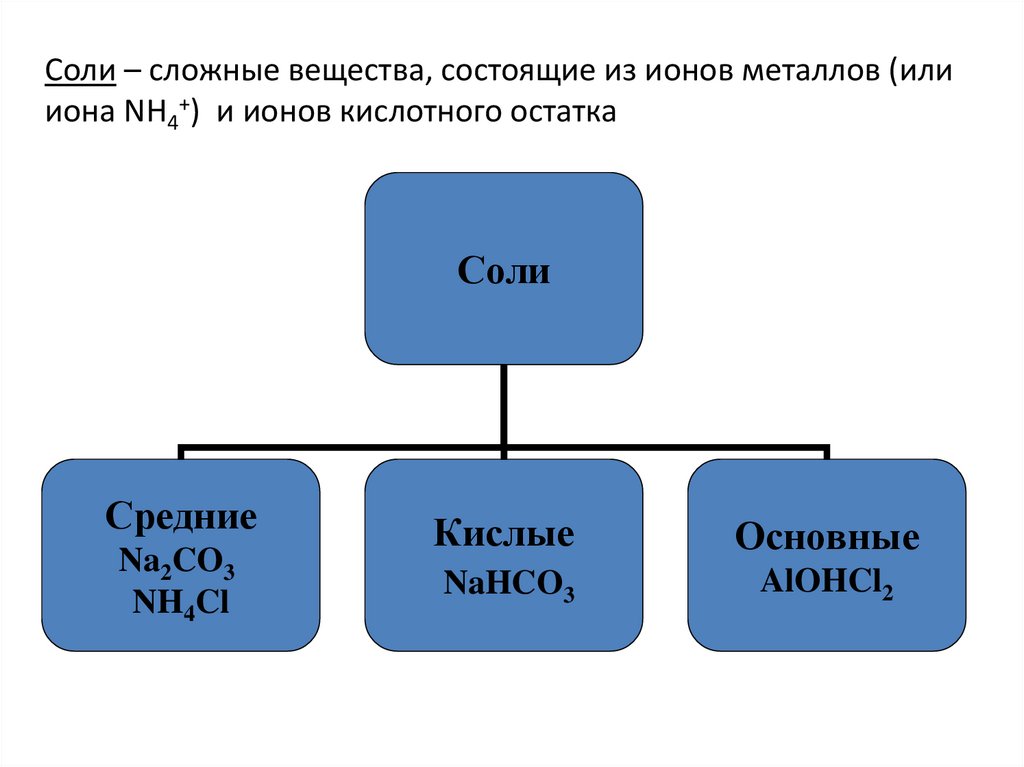
8. Соли – сложные вещества, состоящие из ионов металлов (или иона NH4+) и ионов кислотного остатка
СолиСредние
Na2CO3
NH4Cl
Кислые
Основные
NaHCO3
AlOHCl2
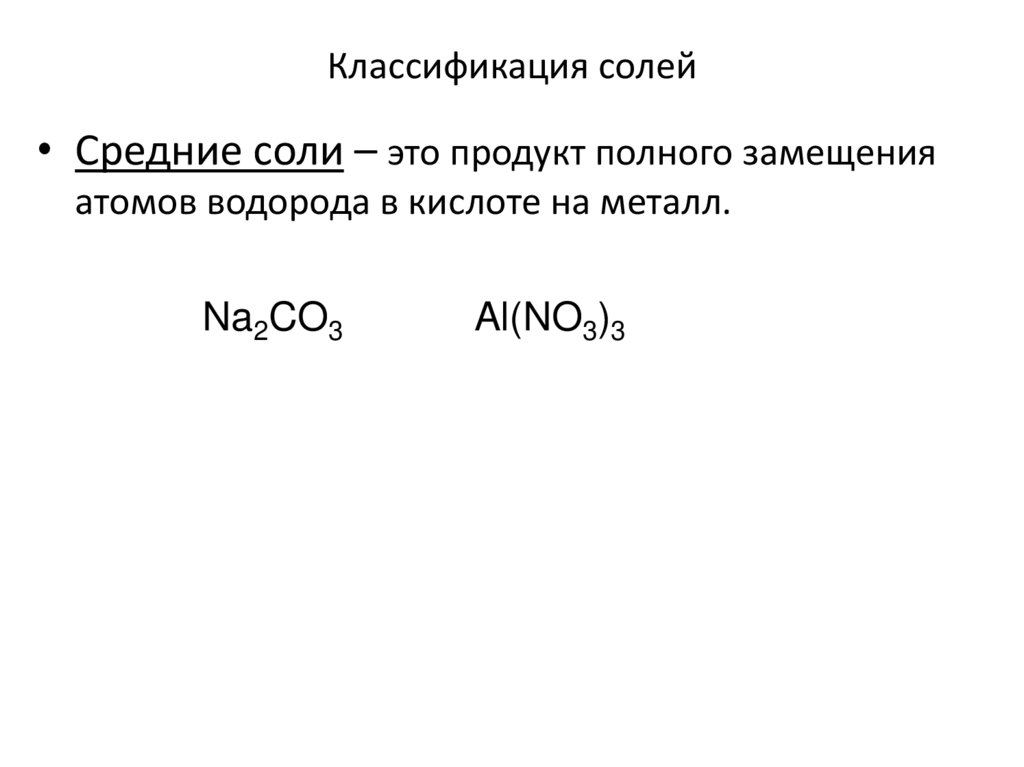
9. Классификация солей
• Средние соли – это продукт полного замещенияатомов водорода в кислоте на металл.
Na2CO3
Al(NO3)3
10. Классификация солей
• Кислые соли – это продукт неполного замещенияатомов водорода в кислоте на металл.
NaHCO3 Ca(HSO4)2
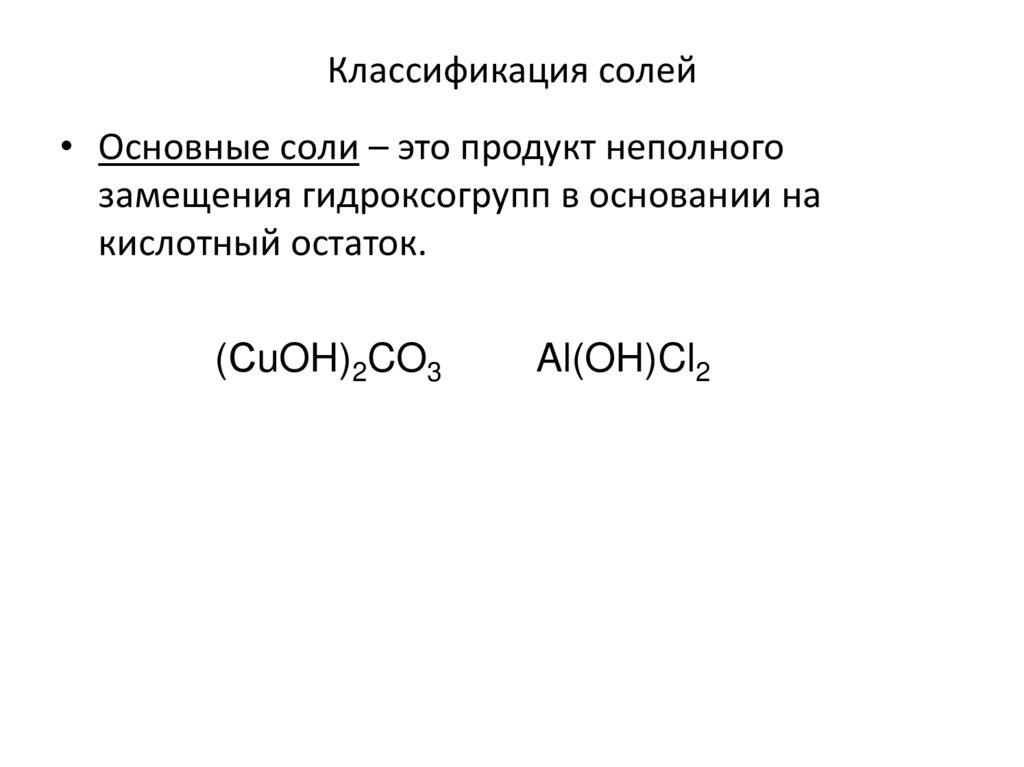
11. Классификация солей
• Основные соли – это продукт неполногозамещения гидроксогрупп в основании на
кислотный остаток.
(СuOH)2CO3
Al(OH)Cl2
12. Установите соответствие
ФОРМУЛА ВЕЩЕСТВАКЛАСС ВЕЩЕСТВА
А) Cu(NO3)2
Б) Ca(OH)2
В) H3PO4
1) оксид
2) кислота
3) соль
4) основание
13. Установите соответствие
ФОРМУЛА ВЕЩЕСТВАКЛАСС ВЕЩЕСТВА
А) Cа(ОН)NO3
Б) Ca(НСO3)2
В) Са3(PO4)2
1) соль средняя
2) соль кислая
3) соль основная
4) основание
5) кислота
14. Химические свойства солей
15.
1) Соль + кислота → новая соль + новая кислота(если один из продуктов газ или осадок)
2) Соль + Щелочь →новая соль + новое основание
(если исходные вещества растворимы, а один из
продуктов нерастворим)
3) Соль1 + соль2 → соль3 + соль4
(если исходные соли растворимы, а один из продуктов
нет)
4) Соль1 + Металл1 → Соль2 + Металл2
(если соли растворимые, а металл 1 активнее металла
соли)
16. Типичные реакции солей
1. H2SO4 + BaCl2 =7. CuCl2 + KOH =
2. CaCO3 + HCl =
8. ZnSO4 + Cu(OH)2 =
3. CaCl2 + HBr =
9. BaCl2 + NaOH =
4. CaCl2 + K2CO3 =
10. CuCl2 + Fe =
5. MgSO4 + KCl =
11. FeSO4 + Zn =
6. MgSO4 + CaCO3 =
12. FeSO4 + Cu =













 chemistry
chemistry








