Similar presentations:
Хроматографические методы
1.
2.
3.
4.
В основе метода хроматографии лежит явлениесорбции
Сорбция – процесс поглощения газов, паров и
растворенного вещества твердыми или жидкими
сорбентами
Виды сорбции
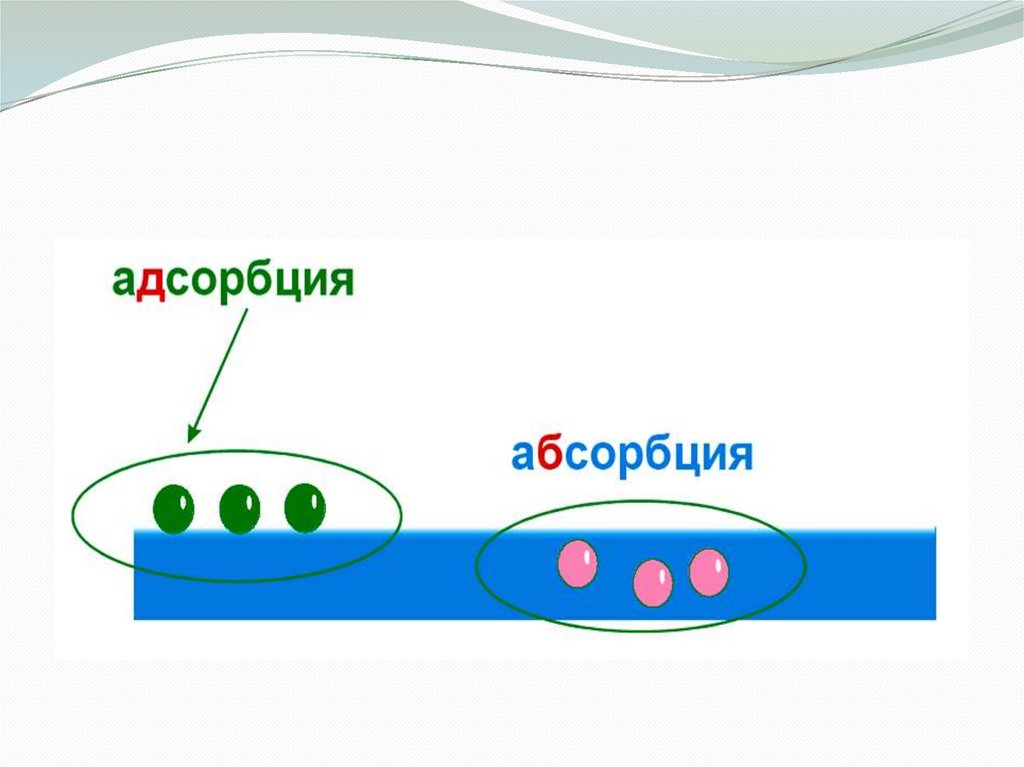
Адсорбция – концентрирование вещества на
поверхности раздела фаз
Абсорбция – распределение веществ между двумя
несмешивающимися фазами (растворитель и
жидкая фаза на твердом носителе)
Капиллярная конденсация – образование жидкой
фазы в порах и капиллярах твердого сорбента при
поглощении паров вещества
Обычно наблюдают смешанный механизм
5.
6.
Сорбцию используют для разделения иконцентрирования веществ
Метод сочетается с любыми методами
определения; например, со спектроскопическими,
если сорбцию вести в твердой фазе
Метод легко автоматизировать
Процесс сорбции можно вести в статических и
динамических условиях
Динамический вариант положен в основу
хроматографических методов разделения
7.
Хроматография – это физико-химический методразделения и определения веществ, основанный на
многократном повторении актов распределения
компонентов между двумя фазами – подвижной и
неподвижной
НФ обычно твердое вещество (сорбент) или пленка
жидкости, нанесенная на твердое вещество
ПФ представляет собой жидкость или газ,
протекающий через неподвижную фазу
8.
Метод хроматографиипредложил русский
ученый-ботаник
М.С.Цвет, который
впервые в 1903 г.
применил явление
адсорбции для анализа
зеленой части
хлорофилловых
пигментов листьев
9.
10.
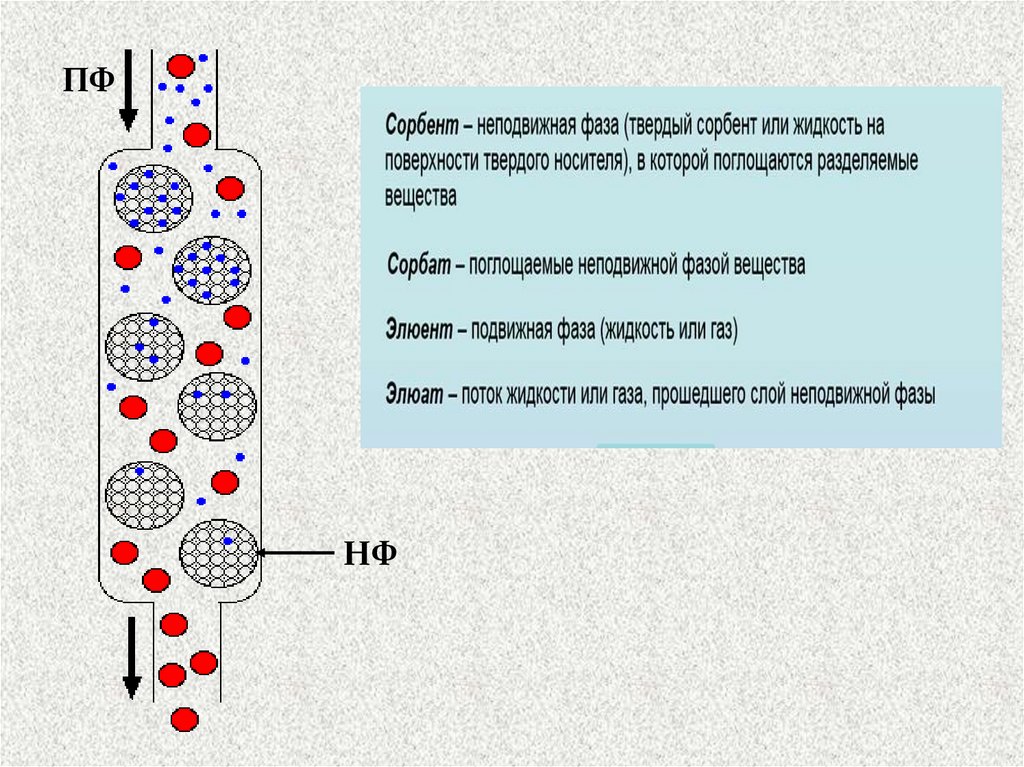
НФ чаще всего помещают в колонку (стекляннуюили металлическую трубку), и компоненты
анализируемой смеси вместе с ПФ перемещаются
вдоль колонки
В процессе хроматографирования устанавливается
динамическое равновесие между ПФ и НФ
Компоненты часть времени находятся в НФ, часть
– в ПФ
11.
ПФНФ
12.
Молекулы разных компонентов разделяемой смесиобладают различной адсорбируемостью или
растворимостью, так что
средняя скорость
передвижения их по колонке различна
Одни компоненты остаются в верхнем слое
сорбента, другие, с меньшей адсорбируемостью,
оказываются в нижней части колонки, некоторые
покидают колонку вместе с подвижной фазой
Так достигается разделение компонентов
13.
Классификация хроматографическихметодов
В основу классификации хроматографических
методов положены следующие признаки:
агрегатное состояние фаз
механизм взаимодействия сорбент – сорбат
способы проведения хроматографического анализа
аппаратурное оформление (техника выполнения)
процесса хроматографирования
цель хроматографирования
14.
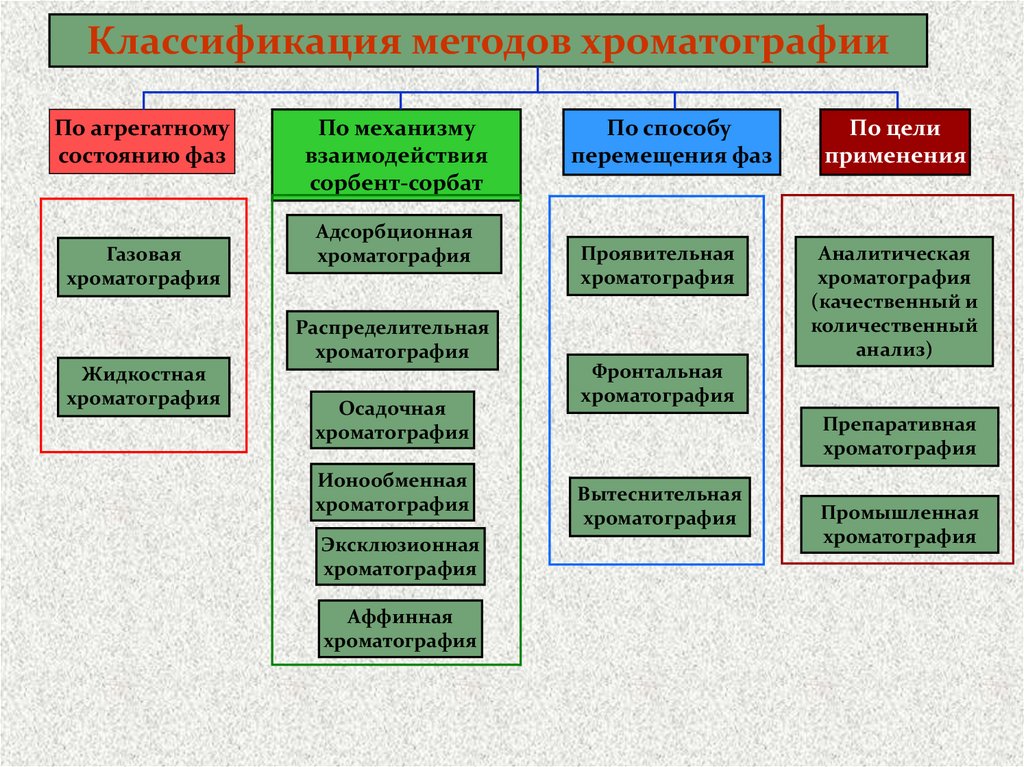
Классификация методов хроматографииПо агрегатному
состоянию фаз
Газовая
хроматография
По механизму
взаимодействия
сорбент-сорбат
Адсорбционная
хроматография
Распределительная
хроматография
Жидкостная
хроматография
Осадочная
хроматография
Ионообменная
хроматография
Эксклюзионная
хроматография
Аффинная
хроматография
По способу
перемещения фаз
По цели
применения
Проявительная
хроматография
Аналитическая
хроматография
(качественный и
количественный
анализ)
Фронтальная
хроматография
Препаративная
хроматография
Вытеснительная
хроматография
Промышленная
хроматография
15.
Классификация хроматографических методовПо агрегатному состоянию фаз хроматографию
разделяют на газовую и жидкостную
ПФ
Метод
НФ
Вариант метода
Газ
ГХ –
газовая
хроматография
Жидкость
ГЖХ –
газожидкостная
хроматография
Твердое
вещество
ГАХ – газоадсорбционная
хроматография
Жидкость
Жидкостно-жидкостная
хроматография
Твердое
вещество
Жидкостно-твердофазная
хроматография
Жидкость
ЖХ –
жидкостная
хроматография
16.
По механизму взаимодействия сорбента и сорбатаможно выделить несколько видов хроматографии:
адсорбционная (НФ – Т) основана на различии в
адсорбируемости веществ твердым сорбентом
распределительная (НФ – Ж) основана на различной
растворимости разделяемых веществ в неподвижной
фазе (ГЖХ) или на различной растворимости веществ
в подвижной и неподвижной фазах (жидкостная
хроматография)
ионообменная
хроматография
–
на
разной
способности веществ к обмену между ионами
разделяемой смеси и подвижными ионами сорбента
осадочная - основана на образовании отличающихся по
растворимости осадков разделяемых веществ с
сорбентом (НФ – Т, пропитана осадителем)
17.
эксклюзионная(гель-хроматография, молекулярноситовой анализ) – основана на различии в размерах и
формах молекул разделяемых веществ
НФ – растворитель – находится в порах сорбента.
Небольшие молекулы попадают в поры и удерживаются
там, большие молекулы не могут проникнуть в поры и
вымываются из колонки ПФ
аффинная
–
основана
на
специфических
взаимодействиях,
характерных
для
некоторых
биологических и биохимических процессов (например,
антитело и антиген, фермент и ингибитор, гормон и
рецептор и др.)
классификация по механизму взаимодействия весьма
условна: ее используют в том случае, если известен
доминирующий механизм; часто процесс разделения
протекает сразу по нескольким механизмам
18.
Эксклюзионная хроматография19.
Классификация хроматографических методовПо технике выполнения выделяют
колоночную хроматографию, когда разделение
проводится в специальных колонках
плоскостную хроматографию, когда разделение
проводится на специальной бумаге (бумажная
хроматография) или в тонком слое сорбента
(тонкослойная хроматография)
В
колоночной
хроматографии
используют
насадочные и капиллярные колонки. Насадочную
колонку заполняют сорбентом (насадкой), а
внутреннюю
стенку
капиллярной
колонки
покрывают пленкой жидкости или пылью
адсорбента
20.
Классификация хроматографических методовВ
зависимости
от
цели
проведения
хроматографического процесса различают
аналитическую хроматографию (качественный и
количественный анализ)
препаративную хроматографию (для получения
веществ в чистом виде, для концентрирования и
выделения микропримесей)
промышленную
(производственную)
хроматографию для автоматического управления
процессом (при этом целевой продукт из колонки
поступает в датчик)
21.
Классификация хроматографических методовКлассификация по способам проведения
анализа подразделяет хроматографию на три
вида:
1) фронтальный
2) проявительный
3) вытеснительный
22.
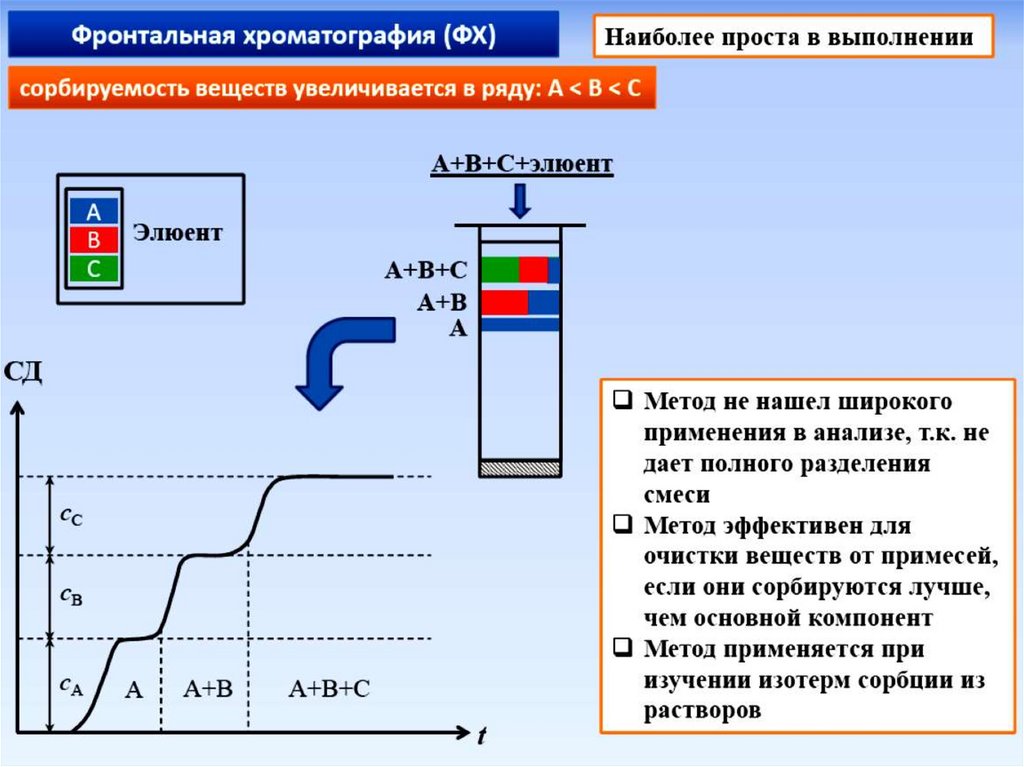
Фронтальный методЧерез хроматографическую колонку с сорбентом
непрерывным потоком пропускают раствор или
газовую смесь исследуемых веществ, сорбируемость
которых увеличивается в ряду А < В < С Соответственно
этому компоненты располагаются в колонке
Однако они разделяются не полностью. В чистом виде
можно выделить лишь часть наименее
сорбирующегося компонента; он движется вдоль слоя
сорбента впереди остальных
За зоной компонента А следует в непосредственном
контакте зона, содержащая смесь компонентов А и В.
Третья зона содержит смесь первого, второго и третьего
компонентов
В некоторый момент времени сорбент насыщается, и
наступает «проскок», т.е. из колонки начинают
выходить компоненты в соответствии с их
сорбируемостью
23.
24.
Если на выходе из колонкификсировать концентрацию
вещества в ПФ, полученная
выходная кривая будет иметь
форму ступенчатой кривой
Для разделения метод
используется мало
Применим для очистки:
умягчение воды
очистка воздуха от ОВ в
противогазах
очистка лекарственных
веществ
концентрирование ценных
примесей в сточных водах
Схема разделения и
выходная кривая
фронтального метода
25.
Вытеснительный методПосле введения порции исследуемой смеси колонку
промывают подвижной фазой, к которой добавлено
вещество
(вытеснитель),
обладающее
большей
сорбируемостью, чем любое из компонентов смеси:
А˂В˂С˂D
По мере продвижения по колонке элюент вытесняет
вещество С, которое в свою очередь вытесняет
вещество В и т.д.
Разделяемые вещества и на колонке, и в элюате
располагаются последовательно друг за другом
Каждый из компонентов выделяется в чистом виде, но
не количественно, так как зоны компонентов не
разделены промежутками чистого сорбента
26.
В аналитических целях методне
используется,
т.к.
невозможно количественно
получить
компоненты
разделяемой смеси
Для препаративных целей
метод не потерял значения,
так как высокоактивные и
доступные
адсорбенты
(например, активированные
угли) позволяют достигнуть
высокой производительности
Еще одно достоинство метода
- зоны не размываются в
отличие от проявительного
анализа
Схема разделения и
выходная кривая
вытеснительного метода
27.
аВытеснительная хроматография (ВХ)28.
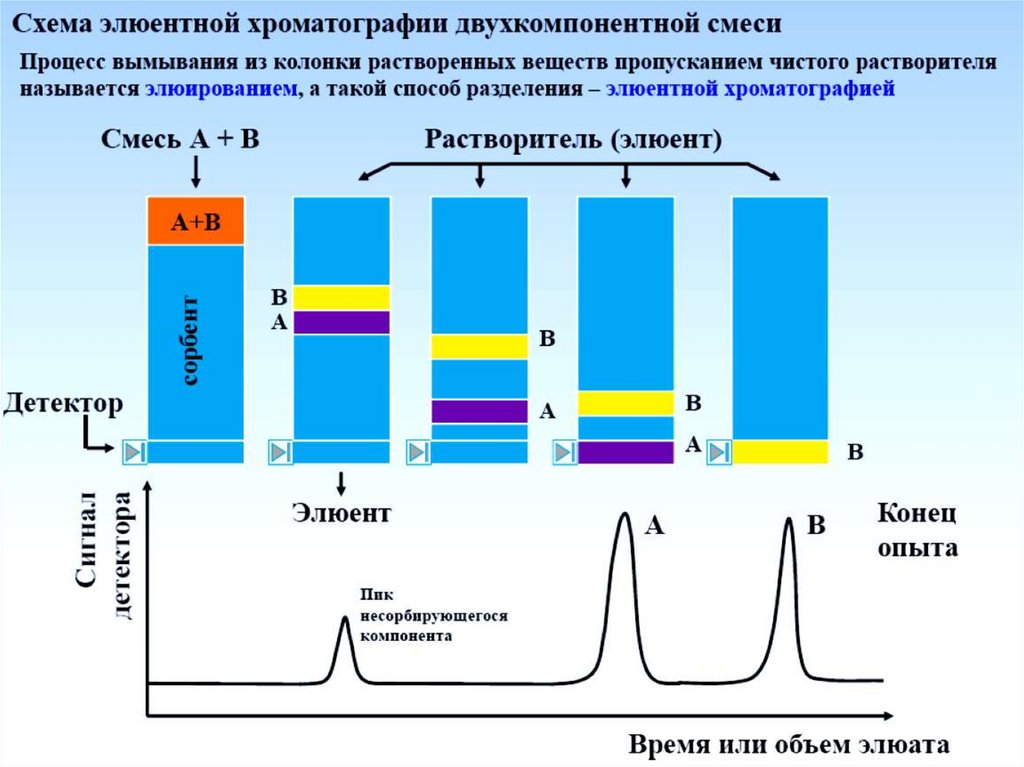
Проявительный (элюентный) методХроматографическую колонку
промывают растворителем или
газом-носителем (элюентом),
обладающим меньшей
сорбируемостью, чем любое из
разделяемых веществ: Е˂ А ˂ В ˂ С
Затем в колонку вводят
исследуемую смесь в виде порции
раствора или газа и продолжают
пропускать элюент
Разделяемые вещества
перемещаются вдоль колонки с
разными скоростями в
соответствии с их сорбируемостью
Выходная кривая в виде ряда
пиков, число которых
соответствует числу разделенных
компонентов
Схема разделения и
выходная кривая
проявительного метода
29.
30.
31.
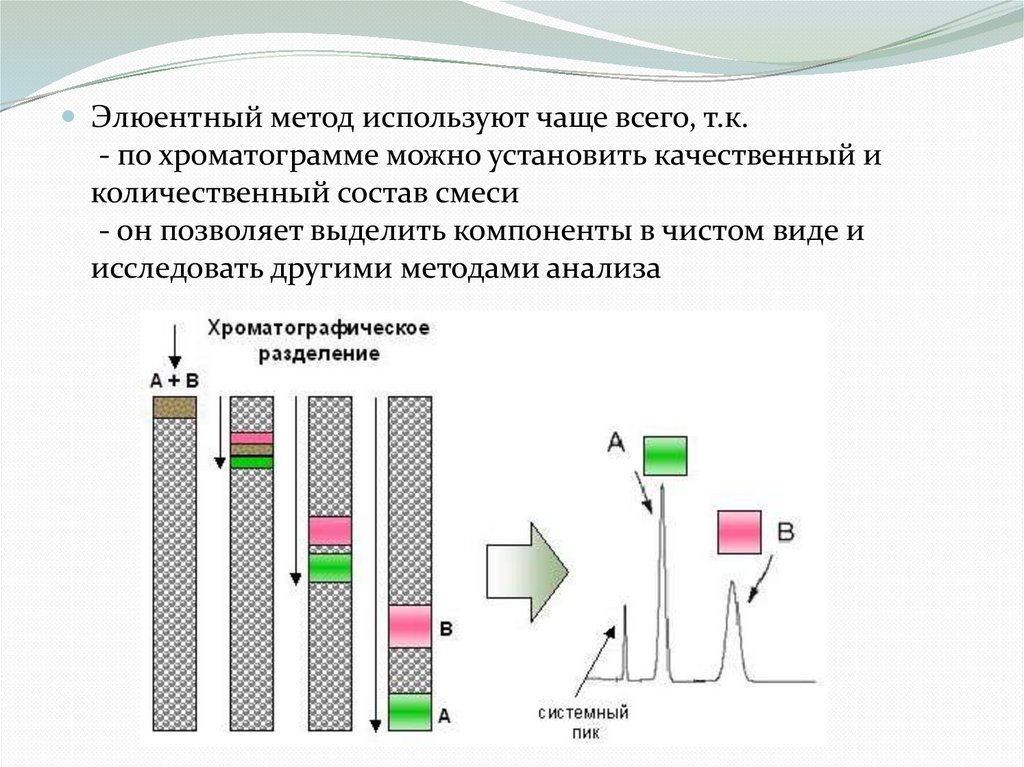
Элюентный метод используют чаще всего, т.к.- по хроматограмме можно установить качественный и
количественный состав смеси
- он позволяет выделить компоненты в чистом виде и
исследовать другими методами анализа
32.
Плоскостная хроматографияЭто - жидкостная хроматография. Различают
бумажную (БХ)
и тонкослойную (ТСХ) - используют чаще
ПФ – жидкость
НФ – твердый сорбент или жидкость на твердом
носителе
Выделяют адсорбционную, распределительную,
обращенно-фазовую
и
ионообменную
плоскостную хроматографию
33.
34.
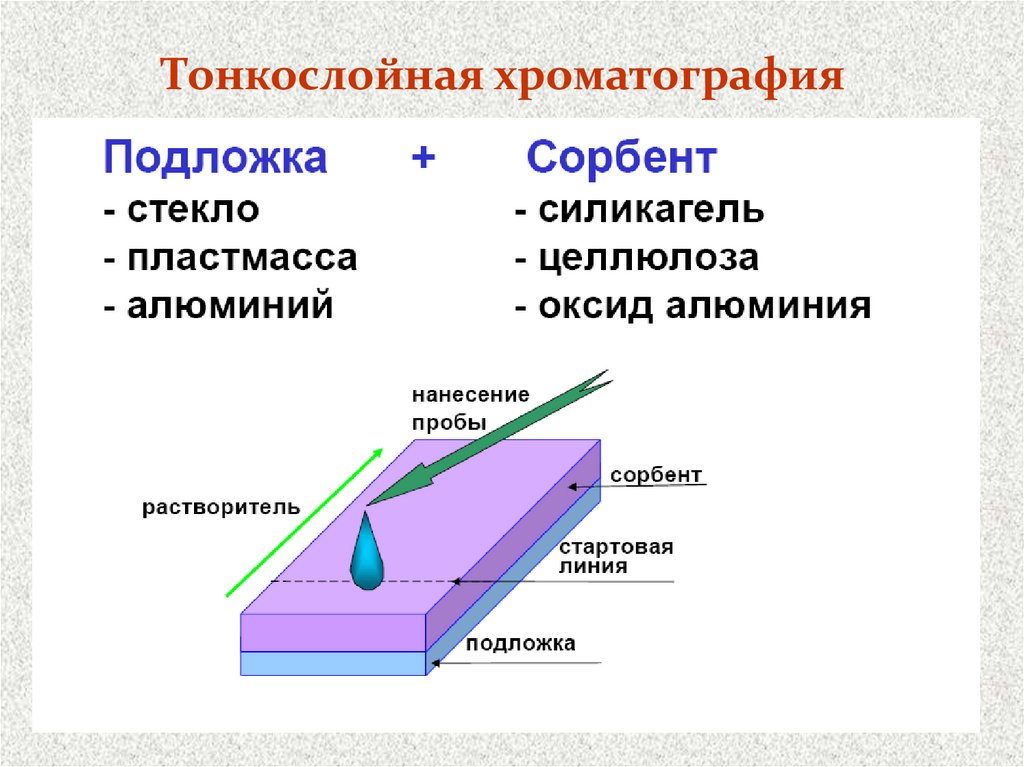
Тонкослойная хроматографияМетод разработан Н. А. Измайловым и М. С.
Шрайбер еще в 1938 г.
НФ тонким слоем 0,1-0,3 мм наносится на
(стеклянную), пластмассовую или металлическую
пластинку
НФ - силикагель, оксид алюминия, порошок
целлюлозы, жидкие иониты и др.
ПФ - растворители или их смеси, органические и
неорганические кислоты
Выбор ПФ зависит от природы сорбента и свойств
анализируемых соединений
35.
Тонкослойная хроматография36.
ВТСХ чаще используют восходящий способ
получения хроматограммы
Раствор образца наносят микропипеткой на
небольшом расстоянии от края пластинки на
стартовую линию, и край пластинки погружают в
растворитель
Под действием капиллярных сил растворитель
поднимается вверх по пластинке и с разной
скоростью переносит за собой компоненты смеси,
что приводит к их пространственному разделению
Чтобы растворитель не испарялся с поверхности
сорбента, пластинку помещают в герметически
закрытую прозрачную камеру
37.
Восходящая тонкослойнаяхроматография
Камера
Начало хроматографирования
Через 10 минут
38.
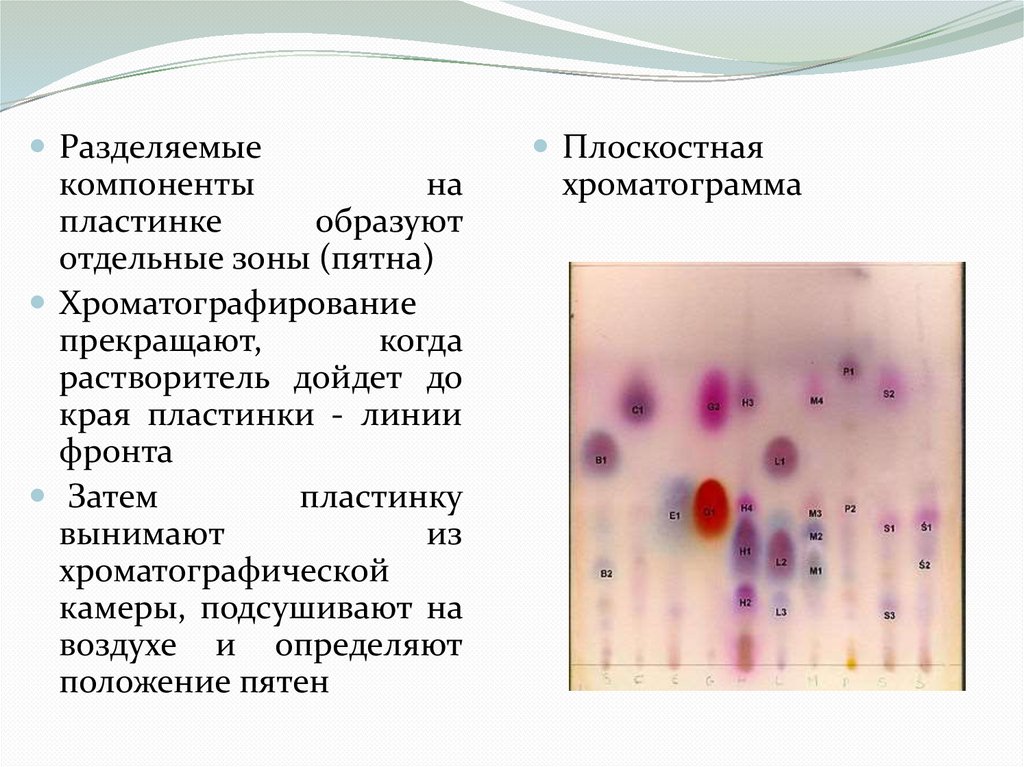
Разделяемыекомпоненты
на
пластинке
образуют
отдельные зоны (пятна)
Хроматографирование
прекращают,
когда
растворитель дойдет до
края пластинки - линии
фронта
Затем
пластинку
вынимают
из
хроматографической
камеры, подсушивают на
воздухе и определяют
положение пятен
Плоскостная
хроматограмма
39.
Внисходящей хроматографии растворитель
передвигается по слою вниз под действием и
капиллярных, и гравитационных сил
В круговой хроматографии каплю анализируемой
смеси вносят в центр пластинки и непрерывно
подают растворитель, который движется в
радиальном направлении от центра
Компоненты смеси образуют на пластинке ряд
концентрических колец
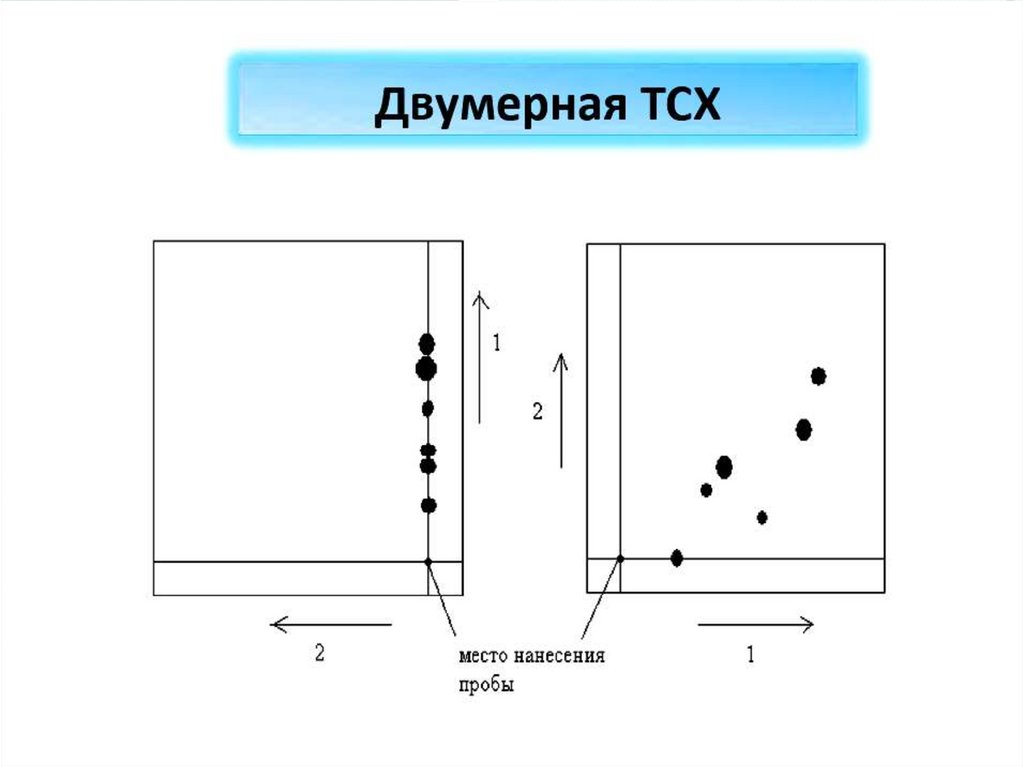
В двумерной хроматографии смесь помещают в
угол пластины, проводят разделение в одном
растворителе, затем поворачивают пластину на 90◦
и продолжают разделение в другом растворителе
40.
41.
42.
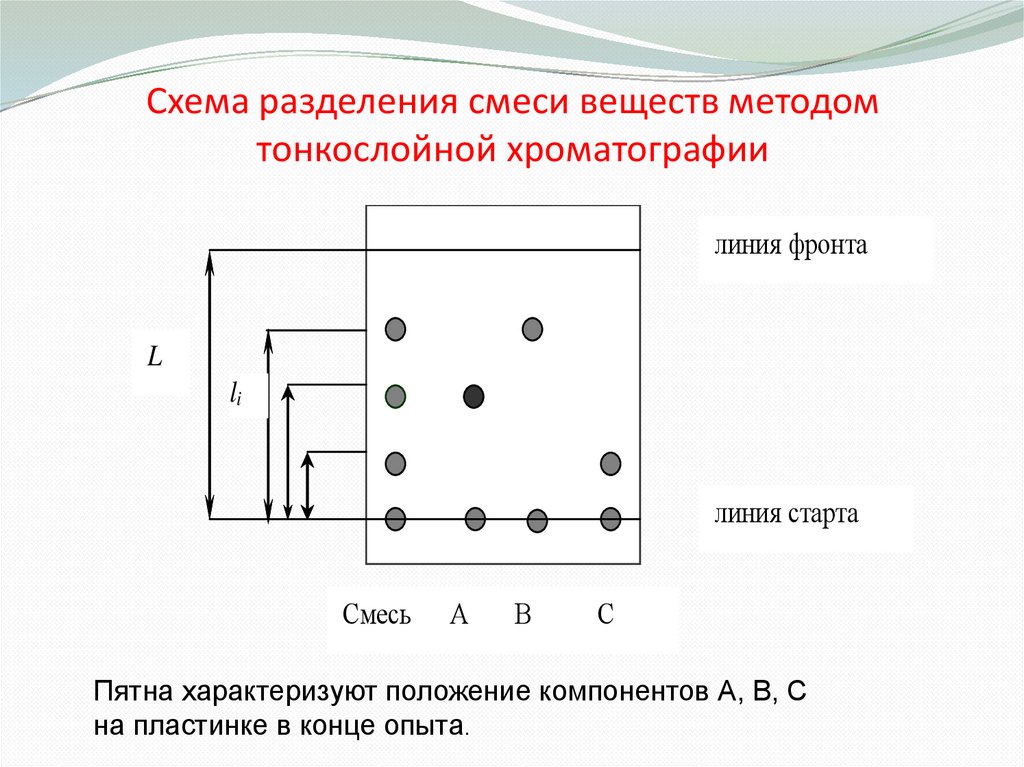
Схема разделения смеси веществ методомтонкослойной хроматографии
линия фронта
L
li
линия старта
Смесь
А
В
С
Пятна характеризуют положение компонентов А, В, С
на пластинке в конце опыта.
43.
44.
45.
Rf–
подвижность
(относительная
скорость
перемещения
компонентов
в
тонком
слое)
характеризует сорбционные свойства системы в ТСХ
Величины Rf рассчитывают из экспериментальных
данных:
l
Rf i
L
li – расстояние от стартовой линии до центра пятна,
L – расстояние, пройденное растворителем от
стартовой линии до границы фронта растворителя
Rf ≤ 1
46.
Rfхарактеризует положение пятна на
хроматограмме
для данного вещества на данном сорбенте в данной
системе растворителей
Rf =const
На величину Rf влияют:
качество и активность сорбента
его влажность
толщина слоя
качество и природа растворителя
техника эксперимента (способ нанесения пробы,
способ детектирования) и другие факторы
47.
На практике частопользуются
относительной
величиной
R f ,отн
R f ,i
R f ,ст
Rf,ст рассчитывают для
стандартного вещества
Условие разделения
веществ с Rf,1 и Rf,2 :
Rf,1 > Rf,2 и Δ Rf ≥ 0,1
48.
Качественный анализ в ТСХ1. Идентификация вещества по характерной окраске
Невидимые хроматограммы проявляют
соответствующими реагентами, как правило,
групповыми
При обработке пластинки, например, парами иода
четко проявляются непредельные соединения
при опрыскивании пластинки тиоцианатом кобальта
амины образуют голубые пятна на розово-белом фоне
Некоторые вещества флуоресцируют под действием
УФ-излучения
49.
ПульверизаторКамера для опрыскивания хроматограмм
реагентом
50.
51.
УФ-облучатель для обнаружения веществ на хроматограммах52.
53.
2. Сравнение величины Rf с табличными данными(если они получены в тех же условиях опыта)
более надежно использовать значения Rf,отн
3. Метод свидетелей (стандартных веществ) самый надежный способ
Стандартное вещество в том же растворителе
наносят на пластинку рядом с анализируемой
пробой и хроматографируют в тех же условиях
Совпадение Rf компонента пробы и одного из
свидетелей дает основание для отождествления
веществ
54.
Количественный анализ в ТСХКоличественный
анализ основан на зависимости
площади пятна от количества компонента
1. Непосредственно на пластинке каким-либо способом
измеряют площадь пятна и по заранее построенному
градуировочному
графику
находят
количество
вещества
2. Методом спектрофотометрии измеряют оптическую
плотность А=f(C) в центре пятна на пластинке
3. Анализируемое вещество удаляют с пластинки
механическим путем или вымывают подходящим
растворителем после вырезания зоны, а затем
анализируют
спектрофотометрическим,
флуориметрическим,
атомно-абсорбционным
методами
55.
Программно-аппаратный комплекс для количественнойоценки хроматограмм по размеру пятен
56.
57.
Применение метода ТСХМетод ТСХ прост по методике выполнения и
аппаратуре, экспрессен и не требует для анализа
больших количеств вещества
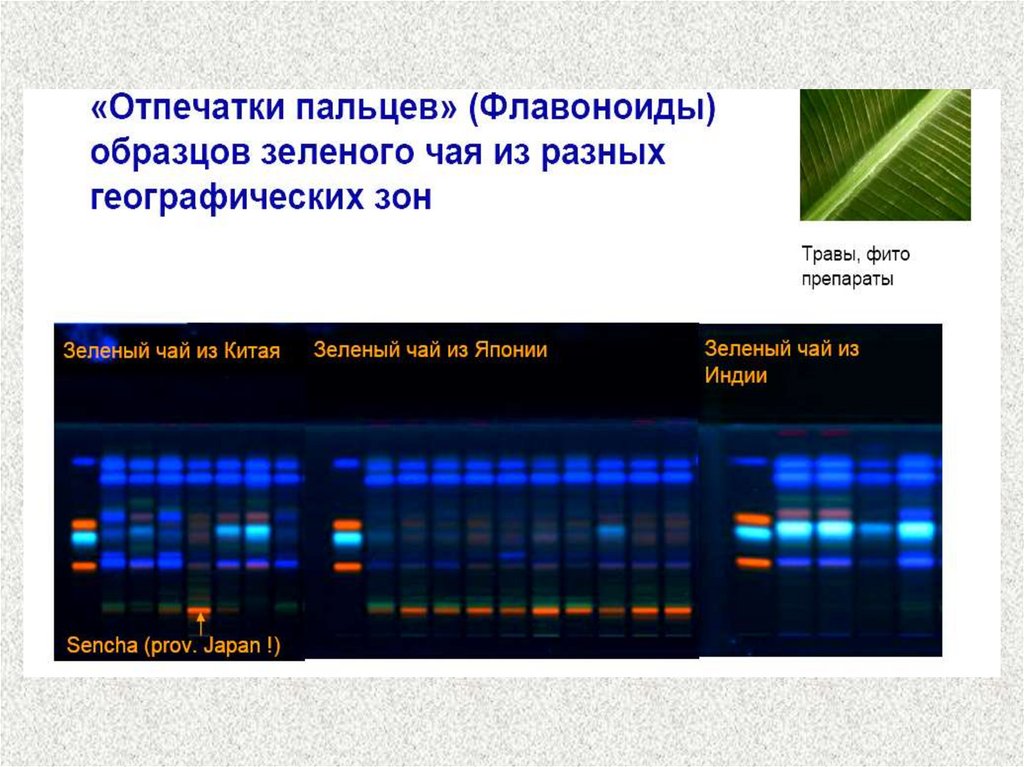
Метод широко используется для идентификации
компонентов
лекарств,
биохимических
препаратов, неорганических веществ
58.
59.
60.
Бумажная хроматографияМетод предложен в 1941 г. Мартином и Синджем
В роли твердого носителя можно использовать
специальную хроматографическую бумагу в виде
листов или полосок
Хроматографическая
бумага
должна
быть
химически чистой, нейтральной, инертной по
отношению к компонентам раствора и подвижной
фазе и быть однородной по плотности; имеют
значение структура молекул целлюлозы в бумаге,
ориентация волокон и другие свойства, влияющие
на скорость движения подвижной фазы
Основные операции в бумажной хроматографии
проводятся примерно так же, как и в тонкослойной
61.
СтеклоЗажим
Валик
Бумага
Проба
Растворитель
Сосуд для
растворителя
Устройство камеры для бумажной хроматографии
62.
Восходящий и нисходящий варианты БХ63.
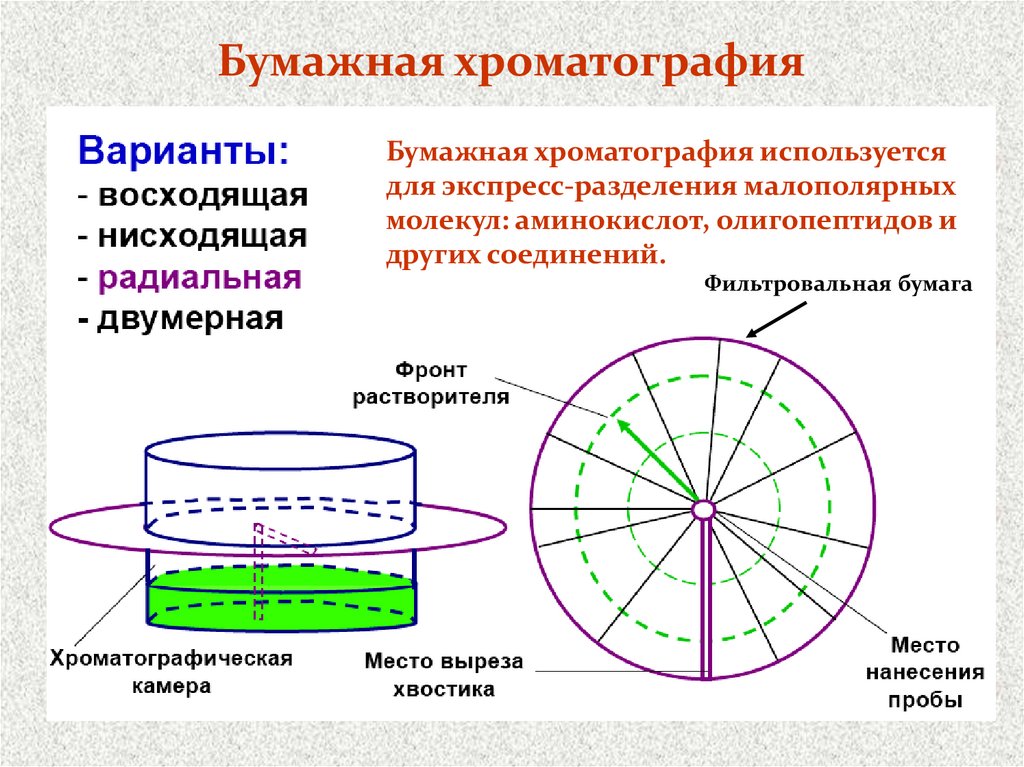
Круговой вариант БХ1 – круглый фильтр
2 – «фитиль», погружаемый в растворитель
А – место нанесения анализируемого раствора
64.
Бумажная хроматографияБумажная хроматография используется
для экспресс-разделения малополярных
молекул: аминокислот, олигопептидов и
других соединений.
Фильтровальная бумага
65.
Приразделениии водорастворимых веществ,
например, неорганических ионов, в качестве ПФ
берут органический растворитель, а в качестве НФ
– воду (бумагу заранее смачивают водой)
При
разделении
компонентов,
хорошо
растворимых в органических растворителях,
гидрофильную
бумагу
превращают
в
гидрофобную,
пропитывая
ее
растворами
органических веществ (парафина, растительного
масла и др.), а в качестве подвижной фазы
используют воду, водный раствор какой-либо
кислоты или щелочи, буферный раствор
66.
Качественный анализ так же, как и в ТСХ, проводятпо специфической окраске отдельных пятен на
хроматограмме, или по численному значению Rf
каждого компонента
Количественные определения в БХ выполняются
по хроматографическим характеристикам (по
площади
пятна
на
хроматограмме
и
интенсивности его окраски) или - после
вымывания - подходящим физико-химическим
методом
Метод используют для разделения не слишком
сложных смесей, в настоящее время используют в
аналитических лабораториях довольно редко
67.
68.
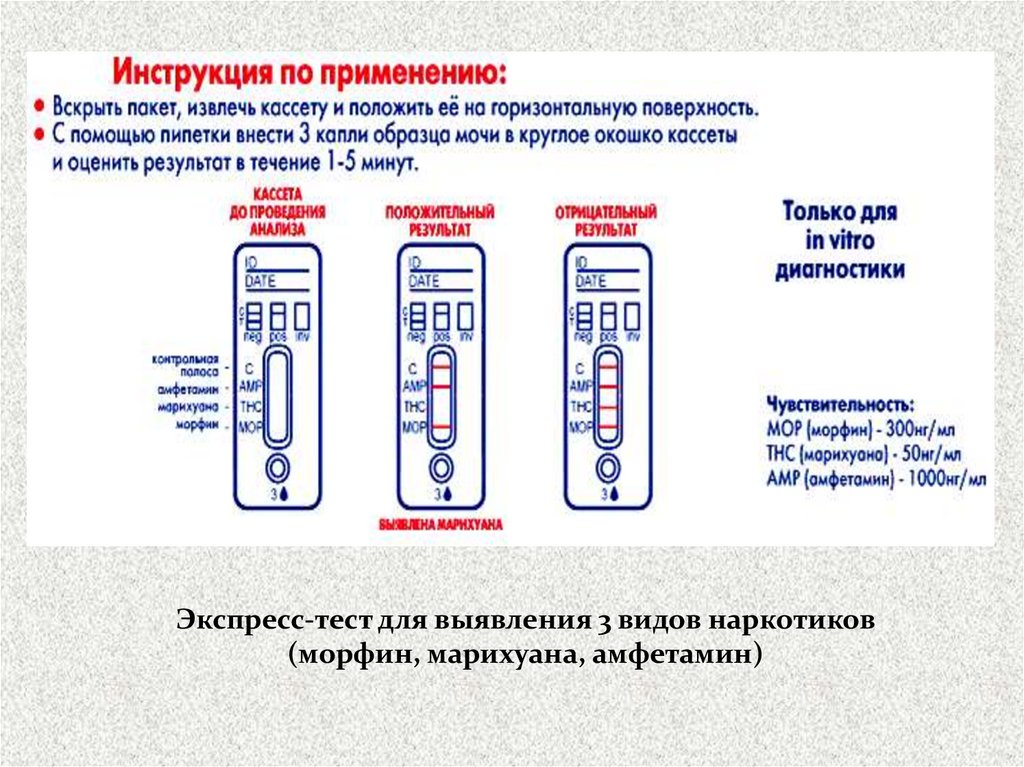
Экспресс-тест для выявления 3 видов наркотиков(морфин, марихуана, амфетамин)

























































 chemistry
chemistry








